2. 中国科学院生态环境研究中心, 中国科学院饮用水科学与技术重点实验室, 北京 100085;
3. 清华大学环境学院水质与水生态研究中心, 北京 100084
2. Key Laboratory of Drinking Water Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China;
3. Center for Water and Ecology, School of Environment, Tsinghua University, Beijing 100084, China
高级氧化技术(AOPs)广泛应用于高毒性、难降解染料废水处理[1~3].Fe(Ⅲ)与Fe(Ⅱ)的氧化-还原循环可活化双氧水(H2 O2), 从而产生具有极强氧化能力的羟基自由基(·OH).上述芬顿(Fenton)反应可将难降解有机物氧化为小分子有机物, 并且以条件温和、处理成本低、操作简单等优势而得到广泛应用[4].传统均相Fenton反应要求pH在2~4之间[5, 6], 产生大量铁泥、铁盐难以回收再利用, 这些因素限制其在很多工程中的应用[7, 8].开发稳定性高、pH适用范围广的非均相类Fenton反应具有很好的应用前景[9, 10], 国内外先后报道了零价铁[11]、金属氧化物[12]和固定化过渡金属材料等类Fenton催化剂[13].另一方面, Fe(Ⅲ)还原为Fe(Ⅱ)是大多数类Fenton反应限速步骤, 且传质效率低和H2 O2利用率低等也是重要限制因素[14].
铁基金属有机骨架化合物(Fe-MOFs)是由铁离子或铁簇与有机配体自组装而成的多孔材料[15].Fe-MOFs具有比表面积高、孔隙率高和活性位点均匀分散等优点, 有助于充分暴露反应位点, 加速传质.此外, MOFs具有良好的组成和结构可调性, 可通过有机配体修饰和金属掺杂等方式加速MOFs中Fe(Ⅲ)→Fe(Ⅱ)速率, 提高非均相催化H2 O2降解污染物效率.MILs(materials of institute lavoisier)系列MOFs是由三价金属离子[Fe(Ⅲ)、Al(Ⅲ)或Cr(Ⅲ)等]与对苯二甲酸或均苯二甲酸配体自组装而成的三维有机骨架材料[16, 17].国内外先后报道了MIL-53(Fe)、MIL-88B-Fe和MIL-100(Fe)等Fe-MOFs[18~20], 作为类Fenton催化剂降解污染物, 但催化性能仍有待提高.与Fe(Ⅲ)→Fe(Ⅱ)相似, Cu(Ⅱ)→Cu(Ⅰ)循环也可活化H2 O2产生·OH.有研究证实, 铜基催化剂可高效活化H2 O2并降解抗生素、雌激素和染料等污染物[21]; 铁和铜等2种金属氧化还原对可发挥协同作用而加速界面电子转移, 进而提高催化性能[22].
铁-铜双金属催化剂开发是类芬顿催化领域研究热点, 在Fe-MOFs中引入Cu有望改善类Fenton催化性能.基于此, 本研究的目的在于:①在具有优异化学稳定性和水稳定性的MIL-101(Fe)中引入Cu(Ⅱ), 采用溶剂热法制备Fe-Cu双金属有机骨架催化剂; ②以亚甲基蓝(MB)为代表, 分析不同溶液pH、H2 O2浓度、催化剂投量和共存阴离子等条件下类芬顿催化性能, 并评估催化剂可重复使用性; ③提出可能涉及的主导反应机制.
1 材料与方法 1.1 实验试剂六水合氯化铁(FeCl3·6H2 O)、三水合硝酸铜[Cu(NO)2·3H2 O]、过氧化氢(H2 O2)、亚甲基蓝(MB)、盐酸(HCl)、氯化钠(NaCl)、氢氧化钠(NaOH)、硝酸钠(NaNO3)、硫酸钠(Na2SO4)、碳酸钠(Na2CO3)和无水乙醇(C2 H6 O)均为分析纯, 叔丁醇(TBA)、对-苯醌(p-BQ)、DMPO(5, 5-dimethyl-1-pyrroline-N-oxide)、对-苯二甲酸(H2BDC)和N, N-二甲基甲酰胺(DMF)均为优级纯.
1.2 材料制备 1.2.1 MIL-101(Fe)的制备采用溶剂热法制备MIL-101(Fe)类芬顿催化剂[23], 具体方法如下:将1.08 g FeCl3·6H2 O和0.66 g H2BDC溶解在80 mL DMF中, 磁力搅拌3 h; 混合溶液转移到100 mL有聚四氟乙烯内衬的高压反应釜中, 在110℃条件下持续加热20 h; 自然冷却至室温, 将所得的砖红色悬浊液分别用DMF、无水乙醇和超纯水在12 000 r·min-1下离心10 min进行清洗, 每种溶剂均清洗3次; 在真空干燥箱中60℃干燥过夜, 得到MIL-101(Fe)催化剂.
1.2.2 MIL-101(Fe, Cu)的制备除在配制FeCl3·6H2 O和H2BDC混合溶液时加入0.19 g Cu(NO)2·3H2 O之外, MIL-101(Fe, Cu)制备方法与MIL-101(Fe)相同.
1.2.3 催化剂表征采用D8型X射线衍射仪(XRD, 德国Bruker公司)表征材料晶体结构; 采用JSM-7600F型场发射扫描电镜(FE-SEM, 日本株式会社)分析材料表面形貌; 通过N2吸附-脱附法分析材料比表面积(SBET)和孔径分布; 采用X射线光电子能谱(XPS, Thermo ESCALAB 250Xi)分析MIL-101(Fe, Cu)表面金属价态变化; 采用500E型电子自旋共振波谱仪(ESR, 德国Bruker公司)分析DMPO捕获后的·OH和超氧自由基(·O2-).
1.3 类Fenton催化降解亚甲基蓝将0.2 g·L-1催化剂投入100 mL 20 mg·L-1 MB溶液, 采用0.1 mol·L-1 HCl或0.1 mol·L-1 NaOH溶液调节pH至7.0;避光以500 r·min-1磁力搅拌30 min达到吸附-解吸平衡; 之后加入50 μL H2 O2继续反应, 水浴控制温度为(25±1)℃.反应一定时间, 用注射器移取2 mL悬浊液, 经0.22 μm滤膜过滤, 滤液中迅速加入过量过氧化氢酶.采用紫外分光光度计(U-3900, 日本HITACHI公司)在波长664 nm处测定吸光度.使用电感耦合等离子体质谱(ICP-MS)检测反应后溶解性总铁和总铜浓度.
2 结果与讨论 2.1 MIL-101(Fe)和MIL-101(Fe, Cu)结构表征图 1(a)为MIL-101(Fe)和MIL-101(Fe, Cu)的XRD谱图.MIL-101(Fe)表现出很高的结晶度, 5个主要衍射峰2θ值分别为8.38°、8.99°、9.85°、10.50°和16.39°, 这些结果与前人研究结果一致[24]. MIL-101(Fe, Cu)的XRD图谱与MIL-101(Fe)相似, 说明引入铜对材料晶型和骨架拓扑结构影响不大.图 1(b)为MIL-101(Fe)和MIL-101(Fe, Cu)在2θ为8.6°~10.0°区间的局部放大XRD谱图.与MIL-101(Fe)相比, MIL-101(Fe, Cu)的2θ值向大角度分别偏移至8.45°、9.09°、9.95°、10.60°和16.47°, 且衍射峰的相对强度也明显降低.这些结果表明, 铜可掺杂到MIL-101(Fe)晶格中形成双金属MIL-101(Fe, Cu)催化剂.

|
图 1 MIL-101(Fe)和MIL-101(Fe, Cu)的X射线衍射谱图 Fig. 1 X-Ray diffraction patterns of MIL-101(Fe) and MIL-101(Fe, Cu) |
图 2为MIL-101(Fe)和MIL-101(Fe, Cu)的SEM图.图 2(a)表明, MIL-101(Fe)具有三维八面体结构且表面光滑, 晶体直径范围为500 nm~1 μm.铜的掺入对材料形貌和晶体粒径影响不大; 相对于MIL-101(Fe), MIL-101(Fe, Cu)表面略显粗糙.

|
(a)MIL-101(Fe); (b)MIL-101(Fe, Cu) 图 2 MIL-101(Fe)和MIL-101(Fe, Cu)的SEM形貌图 Fig. 2 Scanning electron microscopy of MIL-101(Fe) and MIL-101(Fe, Cu) |
XPS表面元素分析结果显示(表 1), MIL-101(Fe)和MIL-101(Fe, Cu)中铁元素比例分别为4.0%和3.2%, 铜元素比例为0和0.2%.MIL-101(Fe)引入铜后铁含量下降, 这说明铜离子可与对苯二甲酸配位, 占据部分铁离子位点.MIL-101(Fe)和MIL-101(Fe, Cu)的SBET分别为414.7 m2·g-1和667.2 m2·g-1, 平均孔径分别为1.7 nm和1.9 nm(表 1).引入铜离子可增大催化剂SBET, 有利于暴露活性位点和加速传质. MIL-101(Fe, Cu)平均孔径略微增加, 这可能是由于Cu2+半径较Fe3+更大所致.
|
|
表 1 MIL-101(Fe)和MIL-101(Fe, Cu)的比表面积、平均孔径和表面元素含量 Table 1 Specific surface area, average pore diameter, and surface elemental contents of MIL-101(Fe) and MIL-101(Fe, Cu) |
2.2 MIL-101(Fe)和MIL-101(Fe, Cu)催化性能
图 3(a)对比MIL-101(Fe, Cu)与MIL-101(Fe)催化H2 O2降解MB性能.其中, MB初始浓度为20 mg·L-1, 催化剂投量为0.2 g·L-1, H2 O2浓度为5 mmol·L-1, 初始pH为5.0.单独H2 O2对MB去除率几乎为0, 表明H2 O2自身的氧化能力可忽略不计.未投加H2 O2时, MIL-101(Fe)和MIL-101(Fe, Cu)反应20 min对MB的吸附去除率为18.2%和25.1%.投加H2 O2后, MIL-101(Fe)和MIL-101(Fe, Cu)体系中MB去除率显著提高至56.9%和100%, 证实引入Cu元素可显著提高MIL-101(Fe)类芬顿催化降解MB性能. MIL-101(Fe, Cu)的SBET更高、孔径更大, 可有效加速传质过程和活性位点暴露.此外, MIL-101(Fe, Cu)结构中Fe和Cu等位点在类芬顿催化过程中可能存在协同作用, 这将在下面进一步讨论.

|
MB浓度:20 mg·L-1, 催化剂投量:0.2 g·L-1, H2 O2投量:5 mmol·L-1, 初始pH=5.0(只有考察的参数发生变化) 图 3 不同反应条件对MIL-101(Fe, Cu)类芬顿催化降解MB的影响 Fig. 3 Fenton-like catalytic degradation of MB by MIL-101(Fe, Cu)/H2 O2 under various conditions |
图 3(b)为初始pH对MIL-101(Fe, Cu)催化降解MB的影响.当初始pH从5.0增加至7.0, 反应20 min后MB去除率由100%降低至95.3%;进一步增大pH到9.0, MB去除率进一步降低至66.1%. pH升高, ·OH氧化电位降低, 且H2 O2在较高pH下发生自分解[23].上述结果显示, MIL-101(Fe, Cu)在pH 5~9广谱范围内均表现出良好的催化降解MB效果, 尤其中性pH下优异性能使得其相对于均相Fenton具有很好的优势.
图 3(c)为H2 O2投量对MIL-101(Fe, Cu)催化降解MB的影响.H2 O2投量为1 mmol·L-1时, 反应20 min后MB去除率为79.2%;增大H2 O2投量到5 mmol·L-1时, MB去除率达到100%, 这主要是由于MIL-101(Fe, Cu)活化产生·OH量增加所致.进一步增大H2 O2投量至10 mmol·L-1, MB去除率降低至73.6%, 这主要是由于过量H2 O2消耗产生的·OH[反应式(1)和反应式(2)][25].

|
(1) |
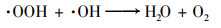
|
(2) |
催化剂投量对MB降解的影响结果表明[图 3(d)], 随着MIL-101(Fe, Cu)投量从0.1 g·L-1增加到0.8 g·L-1, 反应20 min后MB去除率从47.4%增加到100%.催化剂投量增大, 可提供更多活化H2 O2的活性位点, ·OH生成量增大.
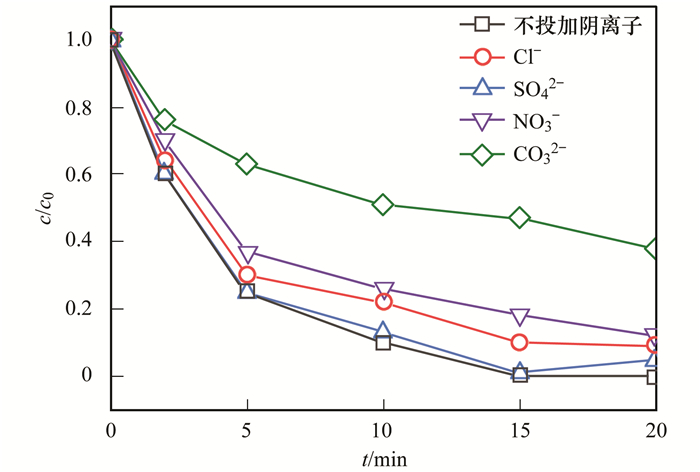
实际废水中存在各种无机阴离子, 可能对类芬顿催化效果产生影响.图 4给出了分别存在浓度为5 mmol·L-1的Cl-、SO42-、NO3-和CO32-等4种阴离子时, MIL-101(Fe, Cu)活化H2 O2降解MB的效果.具体而言, SO42-对MB去除影响不大, Cl-、NO3-和CO32-对MB降解表现出明显抑制, 且抑制作用顺序为CO32->NO3->Cl-.这主要是由于上述阴离子的·OH猝灭作用, 与·OH结合产生氧化能力更弱的ClOH-·、NO3·和CO3-·等自由基所致[式(3)~(5)][26, 27].
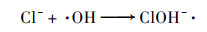
|
(3) |

|
(4) |

|
(5) |
|
MB浓度:20 mg·L-1, 催化剂投量:0.2 g·L-1, H2 O2投量:5 mmol·L-1, 初始pH=5.0 图 4 共存阴离子对MIL-101(Fe, Cu)/H2 O2去除MB的影响 Fig. 4 Effect of coexisting anions on MB degradation using MIL-101(Fe, Cu)/H2 O2 |
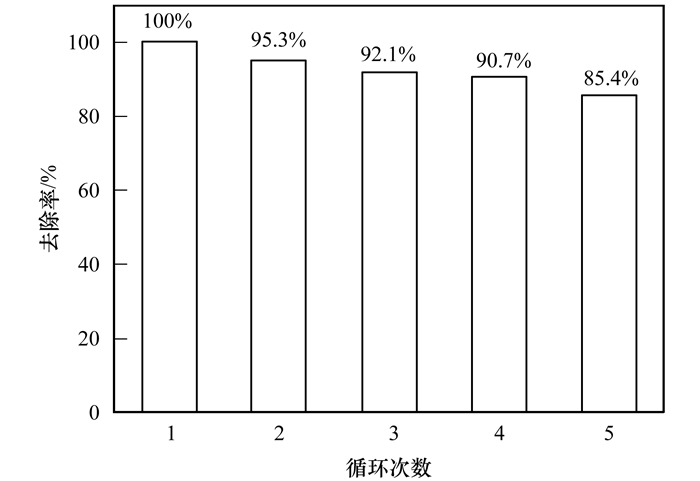
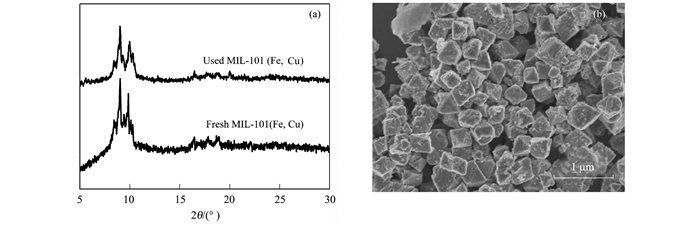
稳定性和可重复利用性是决定催化剂长期应用可行性的重要指标[24], 在相同反应条件下对多次类芬顿催化降解MB性能进行评估.图 5表明, 连续5次循环实验, MIL-101(Fe, Cu)催化H2 O2对MB降解率分别为100%、95.3%、92.1%、90.7%和85.4%, 去除率略微降低, 具有较好的可重复利用性.另外, 测定反应后水中溶解性总铁和总铜浓度, 5次循环的溶解性总铁浓度为1.21、1.33、1.16、1.29和1.03 mg·L-1, 溶解性总铜浓度分别为0.15、0.19、0.13、0.18和0.10 mg·L-1, 均低于我国和欧盟规定的废水排放标准限值(均为 < 2 mg·L-1).进一步采用SEM表征循环使用5次后催化剂形貌(图 6), 未见显著变化, 证实MIL-101(Fe, Cu)具有良好的稳定性.此外, 将反应后悬浊液过滤去除MIL-101 (Fe, Cu), 往含有溶解性铁和铜的滤液体系中投加H2 O2降解MB, 发现MB去除率在10.5%以下, 说明MIL-101(Fe, Cu)/H2 O2体系中非均相类芬顿反应发挥主导作用.
|
MB浓度:20 mg·L-1, 催化剂投量:0.2 g·L-1, H2 O2投量:5 mmol·L-1, 初始pH=5.0 图 5 MIL-101(Fe, Cu)类芬顿催化降解MB的可重复利用性 Fig. 5 Reusability of MIL-101(Fe, Cu) in Fenton-like degradation of MB using MIL-101(Fe, Cu)/H2 O2 |
|
(a)XRD图谱; (b)SEM形貌图 图 6 MIL-101(Fe, Cu)经5次循环实验后的XRD图谱和SEM形貌 Fig. 6 XRD patterns and SEM image of MIL-101(Fe, Cu) after five cycles |
为了进一步揭示MIL-101(Fe, Cu)活化H2 O2的反应机制, 采用ESR分析催化降解MB过程中产生的自由基(图 7).结果表明, 单独H2 O2体系未见自由基信号, 引入MIL-101(Fe)或MIL-101(Fe, Cu)之后出现明显的DMPO-·OH(1:2:2:1)和DMPO-·O2-等2种自由基的加和信号峰, 证实MIL-101(Fe)和MIL-101(Fe, Cu)均可活化H2 O2产生·OH和·O2-等强氧化活性物种.但MIL-101(Fe, Cu)/H2 O2的DMPO-·OH信号强度显著高于MIL-101(Fe)/H2 O2而其DMPO-·O2-信号强度反而略低于MIL-101(Fe)/H2 O2, 这表明MIL-101(Fe, Cu)可活化H2 O2产生更多的·OH而不是·O2-.

|
图 7 MIL-101(Fe)/H2 O2和MIL-101(Fe, Cu)/H2 O2体系中自由基的ESR谱图 Fig. 7 Electron spin-resonance spectroscopy of radicals in the MIL-101(Fe)/H2 O2 and MIL-101(Fe, Cu)/H2 O2 systems |
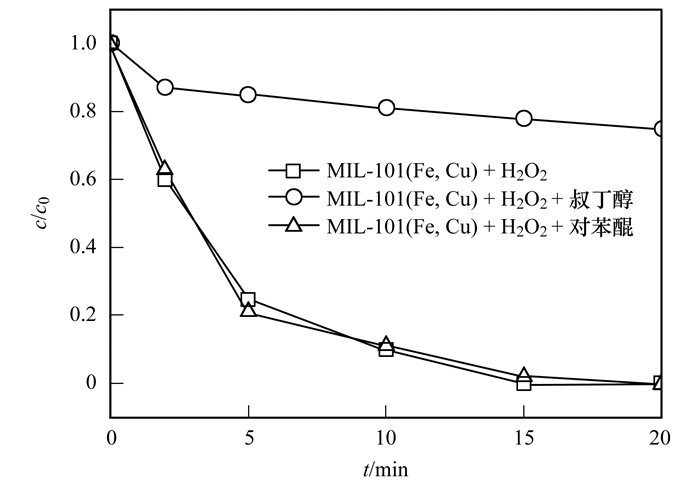
为明确MIL-101(Fe, Cu)/H2 O2降解MB的主要活性物种, 进一步分别以叔丁醇(TBA)和对苯醌(p-BQ)作为·OH和·O2-猝灭剂进行自由基猝灭实验.图 8表明, 反应体系中引入300 mmol·L-1 TBA, 明显抑制MB降解, MB去除率由100%降低至21.3%;投加300 mmol·L-1 p-BQ对MB降解未见明显影响, MB去除率为99.9%.因此, ·OH是MIL-101(Fe, Cu)/H2 O2催化降解污染物的主要活性物种.
|
MB浓度:20 mg·L-1, 催化剂投量:0.2 g·L-1, H2 O2投量:5 mmol·L-1, 初始pH=5.0 图 8 不同自由基猝灭剂对MIL-101(Fe, Cu)类芬顿催化降解MB的影响 Fig. 8 Effects of different free radical quenching agents on Fenton-like degradation of MB using MIL-101(Fe, Cu)/H2 O2 |
为阐明MIL-101(Fe, Cu)活化H2 O2体系下可能的电子转移过程, 采用XPS研究反应前、后MIL-101(Fe, Cu)表面Fe和Cu元素价态变化.图 9(a)显示, MIL-101(Fe, Cu)中键合能在712.4 eV和726.0 eV处两个最强的峰分别对应于Fe 2p3/2和Fe 2p1/2.经分峰拟合分析, 键合能711.8 eV和725.6 eV处3个拟合峰分别归属为Fe(Ⅲ), 且718.2 eV和729.5 eV处两个拟合峰为Fe(Ⅲ)的卫星峰[28].此外, 键合能710.5 eV处拟合峰为Fe(Ⅱ)峰[29], 所占比例为6.2%;反应后Fe(Ⅱ)所占比例下降至1.6%, 表明反应过程中Fe(Ⅱ)可失电子给H2 O2, 进而使H2 O2分解为·OH[图 9(b)].图 9(c)表明, MIL-101(Fe, Cu)中键合能为933.1 eV和934.8 eV处的吸收峰对应于Cu 2p3/2, 键合能953.6 eV和954.6 eV吸收峰则对应于Cu 2p1/2.上述4个拟合峰均归属于Cu(Ⅱ), 且941.3 eV和943.9 eV处两个拟合峰对应于Cu(Ⅱ)的卫星峰, 说明MIL-101(Fe, Cu)中Cu元素主要以二价形式存在[30].反应后, Cu(Ⅱ)的比例由100%降低到94.8%, 且在932.8 eV处出现Cu(Ⅰ)拟合峰[31].上述结果表明, 催化过程中Cu(Ⅱ)可被还原为Cu(Ⅰ), 进而活化H2 O2分子产生·OH.

|
空心圆为实际数据点; 黑色线为实际数据的拟合线 图 9 反应前后MIL-101(Fe, Cu)的Fe 2p和Cu 2p XPS谱图 Fig. 9 XPS spectra of Fe 2p and Cu 2p of MIL-101(Fe, Cu) before and after the Fenton-like reaction |
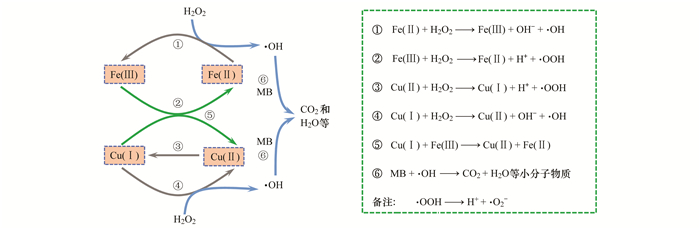
综合上述结果, MIL-101(Fe, Cu)活化H2 O2产生·OH和降解MB主要包括以下6个步骤(图 10):①催化剂表面Fe(Ⅱ)自发将电子转移给吸附在表面的H2 O2分子, 活化产生·OH, 同时自身被氧化为Fe(Ⅲ); ②催化剂表面Fe(Ⅲ)可被H2 O2还原为Fe(Ⅱ), 同时H2 O2被氧化为·O2-.这一过程不仅导致催化反应速率减慢且需要消耗额外的H2 O2用以生成Fe(Ⅱ), 是类芬顿催化反应的限速步骤; ③表面Cu(Ⅱ)位点催化H2 O2产生Cu(Ⅰ)和·O2-; ④产生的Cu(Ⅰ)继续活化H2 O2, Cu(Ⅰ)被氧化为Cu(Ⅱ)的同时产生·OH; ⑤由于Cu(Ⅱ)/Cu(Ⅰ)的氧化还原电位低于Fe(Ⅲ)/Fe(Ⅱ)[32], 在第3步产生的Cu(Ⅰ)可促进Fe(Ⅲ)向Fe(Ⅱ)的循环, 促进Fe(Ⅱ)与H2 O2反应生成·OH.这克服了MIL-101(Fe)/H2 O2降解MB中的限速步骤; ⑥产生的·OH会攻击MB, 将其降解为小分子有机物, 甚至矿化为CO2和H2 O.因此, 与MIL-101(Fe)相比, MIL-101(Fe, Cu)不仅引入了新的活性位点, 且Cu(Ⅱ)/Cu(Ⅰ)可与Fe(Ⅲ)/Fe(Ⅱ)循环协同产生更多的·OH, 以显著提高类芬顿催化效果.
|
图 10 MIL-101(Fe, Cu)类芬顿催化降解MB的主要反应途径 Fig. 10 Main pathways involved in the MB degradation using MIL-101(Fe, Cu) Fenton-like reaction |
采用溶剂热法将Cu(Ⅱ)引入至MIL-101(Fe)中, 成功制备双金属有机骨架MIL-101(Fe, Cu); 相对于MIL-101(Fe), MIL-101(Fe, Cu)表面粗糙度增大, 比表面积和平均孔径均得到提高.MIL-101(Fe, Cu)可作为类芬顿催化剂, 在广谱pH值范围内可活化H2 O2高效降解MB, 相对于传统均相Fenton大幅拓展pH适用范围; SO42-对MB去除影响不大, Cl-、NO3-和CO32-由于与·OH结合产生氧化能力更弱的ClOH-·、NO3·和CO3-·而表现出明显抑制作用.连续5次循环实验证实, MIL-101(Fe, Cu)催化剂使用过程中Fe和Cu溶出量很低, 具有良好的稳定性和可重复使用性.·OH是MIL-101(Fe, Cu)/H2 O2类芬顿降解MB主导活性物种, Cu(Ⅱ)掺杂不仅引入新的活性位点, 且Cu(Ⅱ)/Cu(Ⅰ)可与Fe(Ⅲ)/Fe(Ⅱ)循环协同产生更多的·OH以提高类芬顿催化效果.MIL-101(Fe, Cu)以效果好、pH适用范围广和稳定性好等优势而在类芬顿催化中具有较好的应用前景.
| [1] | Hodges B C, Cates E L, Kim J H. Challenges and prospects of advanced oxidation water treatment processes using catalytic nanomaterials[J]. Nature Nanotechnology, 2018, 13(8): 642-650. DOI:10.1038/s41565-018-0216-x |
| [2] | Nguyen X S, Zhang G K, Yang X F. Mesocrystalline Zn-doped Fe3O4 hollow submicrospheres:formation mechanism and enhanced photo-Fenton catalytic performance[J]. ACS Applied Materials & Interfaces, 2017, 9(10): 8900-8909. |
| [3] | Chen Y, Zhang G, Liu H J, et al. Confining free radicals in close vicinity to contaminants enables ultrafast Fenton-like processes in the interspacing of MoS2 membranes[J]. Angewandte Chemie International Edition, 2019, 58(24): 8134-8138. DOI:10.1002/anie.201903531 |
| [4] | Li X N, Huang X, Xi S B, et al. Single cobalt atoms anchored on porous N-doped graphene with dual reaction sites for efficient Fenton-like catalysis[J]. Journal of the American Chemical Society, 2018, 140(39): 12469-12475. DOI:10.1021/jacs.8b05992 |
| [5] | Du J K, Bao J G, Fu X Y, et al. Mesoporous sulfur-modified iron oxide as an effective Fenton-like catalyst for degradation of bisphenol A[J]. Applied Catalysis B:Environmental, 2016, 184: 132-141. DOI:10.1016/j.apcatb.2015.11.015 |
| [6] | Clarizia L, Russo D, Di Somma I, et al. Homogeneous photo-Fenton processes at near neutral pH:a review[J]. Applied Catalysis B:Environmental, 2017, 209: 358-371. DOI:10.1016/j.apcatb.2017.03.011 |
| [7] | Pignatello J J, Oliveros E, Mackay A. Advanced oxidation processes for organic contaminant destruction based on the Fenton reaction and related chemistry[J]. Critical Reviews in Environmental Science and Technology, 2006, 36(1): 1-84. DOI:10.1080/10643380500326564 |
| [8] | Xing M Y, Xu W J, Dong C C, et al. Metal sulfides as excellent co-catalysts for H2 O2 decomposition in advanced oxidation processes[J]. Chem, 2018, 4(6): 1359-1372. DOI:10.1016/j.chempr.2018.03.002 |
| [9] | Liu Y Y, Jin W, Zhao Y P, et al. Enhanced catalytic degradation of methylene blue by α-Fe2O3/graphene oxide via heterogeneous photo-Fenton reactions[J]. Applied Catalysis B:Environmental, 2017, 206: 642-652. DOI:10.1016/j.apcatb.2017.01.075 |
| [10] | Zhang N Q, Chen J Y, Fang Z Q, et al. Ceria accelerated nanoscale zerovalent iron assisted heterogenous Fenton oxidation of tetracycline[J]. Chemical Engineering Journal, 2019, 369: 588-599. DOI:10.1016/j.cej.2019.03.112 |
| [11] | Martins R C, Lopes D V, Quina M J, et al. Treatment improvement of urban landfill leachates by Fenton-like process using ZVI[J]. Chemical Engineering Journal, 2012, 192: 219-225. DOI:10.1016/j.cej.2012.03.053 |
| [12] | Chen F X, Xie S L, Huang X L, et al. Ionothermal synthesis of Fe3O4 magnetic nanoparticles as efficient heterogeneous Fenton-like catalysts for degradation of organic pollutants with H2 O2[J]. Journal of Hazardous Materials, 2017, 322: 152-162. DOI:10.1016/j.jhazmat.2016.02.073 |
| [13] | Cheng M, Zeng G M, Huang D L, et al. Efficient degradation of sulfamethazine in simulated and real wastewater at slightly basic pH values using Co-SAM-SCS/H2 O2 Fenton-like system[J]. Water Research, 2018, 138: 7-18. DOI:10.1016/j.watres.2018.03.022 |
| [14] | Cheng M, Lai C, Liu Y, et al. Metal-organic frameworks for highly efficient heterogeneous Fenton-like catalysis[J]. Coordination Chemistry Reviews, 2018, 368: 80-92. DOI:10.1016/j.ccr.2018.04.012 |
| [15] | Peng Y, Li Y S, Ban Y J, et al. Metal-organic framework nanosheets as building blocks for molecular sieving membranes[J]. Science, 2014, 346(6215): 1356-1359. DOI:10.1126/science.1254227 |
| [16] |
周珍宇.新型MIL-101(Cr)@PFs和MIL-101(Cr, Mg)的制备及对CO2的吸附性能[D].广州: 华南理工大学, 2016. Zhou Z Y. Preparation of novel MIL-101(Cr)@PFs and bimetallic MIL-101(Cr, Mg) and their CO2 adsorption performances[D]. Guangzhou: South China University of Technology, 2016. |
| [17] |
闫增元, 习海玲, 袁立永. 金属有机框架MIL-53(Fe)可见光催化还原水中U(Ⅵ)[J]. 环境科学, 2019, 40(4): 1819-1825. Yan Z Y, Xi H L, Yuan L Y. Metal organic framework MIL-53(Fe) as a photocatalyst for visible-light catalytic reduction of U(Ⅵ) in aqueous solution[J]. Environmental Science, 2019, 40(4): 1819-1825. |
| [18] | Lv H L, Zhao H Y, Cao T C, et al. Efficient degradation of high concentration azo-dye wastewater by heterogeneous Fenton process with iron-based metal-organic framework[J]. Journal of Molecular Catalysis A:Chemical, 2015, 400: 81-89. DOI:10.1016/j.molcata.2015.02.007 |
| [19] | Gao C, Chen S, Quan X, et al. Enhanced Fenton-like catalysis by iron-based metal organic frameworks for degradation of organic pollutants[J]. Journal of Catalysis, 2017, 356: 125-132. DOI:10.1016/j.jcat.2017.09.015 |
| [20] | Ai L H, Zhang C H, Li L L, et al. Iron terephthalate metal-organic framework:Revealing the effective activation of hydrogen peroxide for the degradation of organic dye under visible light irradiation[J]. Applied Catalysis B:Environmental, 2014, 148-149: 191-200. DOI:10.1016/j.apcatb.2013.10.056 |
| [21] | Lyu L, Yan D B, Yu G F, et al. Efficient destruction of pollutants in water by a dual-reaction-center Fenton-like process over carbon nitride compounds-complexed Cu(Ⅱ)-CuAlO2[J]. Environmental Science & Technology, 2018, 52(7): 4294-4304. |
| [22] | Wang Q, Ma Y, Xing S T. Comparative study of Cu-based bimetallic oxides for Fenton-like degradation of organic pollutants[J]. Chemosphere, 2018, 203: 450-456. DOI:10.1016/j.chemosphere.2018.04.013 |
| [23] | Wang D K, Huang R K, Liu W J, et al. Fe-based MOFs for photocatalytic CO2 reduction:role of coordination unsaturated sites and dual excitation pathways[J]. ACS Catalysis, 2014, 4(12): 4254-4260. DOI:10.1021/cs501169t |
| [24] | Duan M J, Guan Z Y, Ma Y W, et al. A novel catalyst of MIL-101(Fe) doped with Co and Cu as persulfate activator:synthesis, characterization, and catalytic performance[J]. Chemical Papers, 2018, 72(1): 235-250. |
| [25] | Hu X B, Liu B Z, Deng Y H, et al. Adsorption and heterogeneous Fenton degradation of 17α-methyltestosterone on nano Fe3O4/MWCNTs in aqueous solution[J]. Applied Catalysis B:Environmental, 2011, 107(3-4): 274-283. DOI:10.1016/j.apcatb.2011.07.025 |
| [26] | Liang H, Li T R, Zhang J, et al. 3-D hierarchical Ag/ZnO@CF for synergistically removing phenol and Cr(Ⅵ):Heterogeneous vs. homogeneous photocatalysis[J]. Journal of Colloid and Interface Science, 2020, 558: 85-94. DOI:10.1016/j.jcis.2019.09.105 |
| [27] | Zheng H, Bao J G, Huang Y, et al. Efficient degradation of atrazine with porous sulfurized Fe2O3 as catalyst for peroxymonosulfate activation[J]. Applied Catalysis B:Environmental, 2019, 259. DOI:10.1016/j.apcatb.2019.118056 |
| [28] | Tang J T, Wang J L. Iron-copper bimetallic metal-organic frameworks for efficient Fenton-like degradation of sulfamethoxazole under mild conditions[J]. Chemosphere, 2020, 241. DOI:10.1016/j.chemosphere.2019.125002 |
| [29] | Tang J T, Wang J L. Metal organic framework with coordinatively unsaturated sites as efficient Fenton-like catalyst for enhanced degradation of sulfamethazine[J]. Environmental Science & Technology, 2018, 52(9): 5367-5377. |
| [30] | Sun Y, Yang Z X, Tian P F, et al. Oxidative degradation of nitrobenzene by a Fenton-like reaction with Fe-Cu bimetallic catalysts[J]. Applied Catalysis B:Environmental, 2019, 244: 1-10. DOI:10.1016/j.apcatb.2018.11.009 |
| [31] | Tang J T, Wang J L. MOF-derived three-dimensional flower-like FeCu@C composite as an efficient Fenton-like catalyst for sulfamethazine degradation[J]. Chemical Engineering Journal, 2019, 375. DOI:10.1016/j.cej.2019.122007 |
| [32] | Zhang T, Zhu H B, Croué J P. Production of sulfate radical from peroxymonosulfate induced by a magnetically separable CuFe2O4 spinel in water:efficiency, stability, and mechanism[J]. Environmental Science & Technology, 2013, 47(6): 2784-2791. |
 2020, Vol. 41
2020, Vol. 41


