活性污泥法自诞生以来就以其低廉的成本和优良的处理效果而在世界范围内得到了广泛应用[1], 但冬季频发的污泥膨胀却始终制约着其进一步发展, 而在这些污泥膨胀中, 仅由丝状菌优势生长所引起的就能占到90%, 因此, 过往大量关于污泥膨胀的研究报道都围绕着膨胀污泥的优势丝状菌展开[2~5].然而, 尽管已有超过30种不同的丝状菌在污水厂中被发现和研究, 但不同丝状菌的生理特性往往具有差异, 如微丝菌(Microthrix parvicella)的数量受季节影响很大, 冬季多夏季少, 而Type 0092则与之相反; 软发菌(Haliscomenobacter hydrossis)和浮游球衣菌属(Sphaerotilus natans)很少出现在去除营养物质的污水处理厂, M. parvicella却常常出现[6, 7].由于针对丝状菌进行的纯培养成功率低且所获得微生物学信息具有片面性, 加之污水处理厂中的优势丝状菌还会随水质和环境的变化而发生动态的变迁, 都使得当下膨胀污泥微生物学角度的研究难以实现进一步的突破[8, 9].由于活性污泥的本质是由无数微生物组成的混合体, 丝状菌污泥膨胀正是这一微生物混合体受外界因素影响而发生的群落失衡, 故应将相关生物学研究视角转换到系统内不同微生物群落结构的整体研究和对比分析上来, 才能弥补目前本领域研究内容的不足.当下, 随着高通量测序等先进分子生物学技术的发展和应用, 不仅为实现微生物群落的深度测序带来了可能, 也为膨胀领域微生物学研究内容的补充带来了可行性与技术支撑.虽然基于高通量测序的研究已在水处理领域大规模展开, 如针对养殖废水[10]、城市污水[11]、腈纶废水[12]、含油废水[13]及工业废水[14]等诸多水处理系统的菌群结构研究.但针对污泥膨胀领域的研究, 尤其是低温导致的污泥膨胀的相关微生物学多样性的研究仍然十分不足, 而各大污水厂冬季仍面临着污泥膨胀高发的风险和困境.故本实验以低温下发生的丝状菌污泥膨胀为切入点, 采用低温-SBR装置, 成功将反应温度控制在(14±1)℃, 深入研究了低温条件下污泥膨胀过程中微生物菌群整体的多样性变化, 以及特定菌群、特定菌属的相对丰度变化, 通过扩大污泥膨胀微生物学领域的研究视角, 以期为阐明污泥沉降性能变化的微生物学机制和丝状菌污泥膨胀的应对及解决提供更多的生物学支撑.
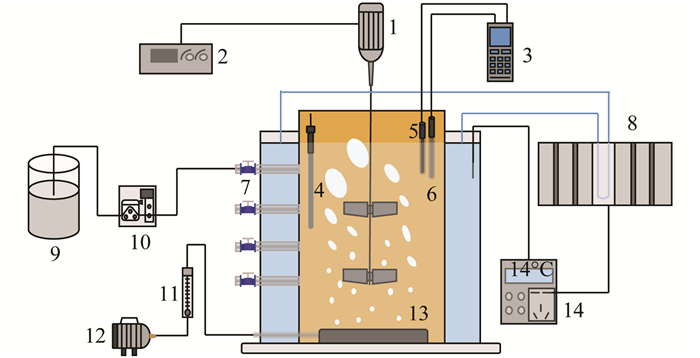
1 材料与方法 1.1 实验装置本实验采用序批式低温-SBR反应器作为主要装置, 反应器容积8 L, 运行期间每日进水4 L排水4 L, 排水比50%(图 1).与之连接的制冷器最低可在30 min内将8 L活性污泥的水温由28℃降至8℃, 配套的温控器的控温范围为-9~99℃, 膨胀期间控制温度在(14±1)℃, 与城市污水厂冬季水温保持一致.反应器下部安装的曝气盘与转子流量计和空气压缩机连接, 为装置内的活性污泥提供溶解氧, 同时配置的WTW3420型溶氧仪装有DO和pH探头, 不仅可用于观察反应器内实际溶解氧水平, 还可实现对系统内pH值的实时监测, 装置上部电动搅拌器的主要功能是保证泥水充分混匀.此外, 还根据实际需求设置了进水口与排水口, 分别于蠕动泵和电动阀相连, 实现系统的自动进排水.
|
1.电动搅拌器; 2.电动机; 3. WTW3420型溶解氧仪; 4.加热棒; 5.pH探头; 6.DO探头; 7.取样口; 8.制冷器; 9.配水水箱; 10.蠕动泵; 11.气体流量计; 12.空气压缩机; 13.曝气盘; 14.温控器 图 1 低温-SBR反应器示意 Fig. 1 Schematic diagram of the low-temperature SBR |
本实验接种污泥取自北京市高碑店污水处理厂二沉池回流污泥, 该污泥脱氮除磷性能良好, 沉降性正常.进水水质采用人工配水, 详细水质数据如表 1和表 2所示.
|
|
表 1 人工配水水质情况 Table 1 Characteristics of artificial wastewater |
|
|
表 2 微量元素配方/mg ·L-1 Table 2 Composition of the trace elements/mg ·L-1 |
1.3 实验运行方案
本实验采取传统硝化反硝化工艺, 分3个阶段共运行80 d, 阶段一为污泥驯化阶段, 该阶段主要目的是使污泥适应本实验所采取的水质及运行方式, 实验时控制溶解氧在2 mg ·L-1, 温度在28℃以上运行30 d, 阶段二为低温下丝状菌污泥膨胀的诱发阶段, 降低温度至(14±1)℃左右运行22 d, 阶段三为恶性膨胀阶段, 该阶段污泥沉降性能恶化严重, 故将运行周期由3次·d-1降至2次·d-1, 并将沉淀时间由40 min延长至280 min后运行28 d.实验期间每周期进水4 L排水4 L, 排水比50%, 具体的运行方式如表 3所示.
|
|
表 3 实验运行方案 Table 3 Operation stages and experimental procedure |
1.4 分析指标和方法
在本实验的分析过程中, 对化学需氧量(COD)、总氮(TN)、污泥浓度(MLSS)和污泥指数(SVI), 系统优势丝状菌以及微生物群落结构等内容进行了检测, 其中COD、TN、MLSS和SVI依据标准方法测得[15, 16].在优势丝状菌的鉴定方面, 在对污泥絮体进行革兰式染色后, 先根据Olympus BX61型显微镜的镜检结果以及Eikelboom丝状菌手册推测优势丝状菌, 再通过荧光原位杂交技术(FISH)进行菌种定性, 所用的FISH分析方法与焦二龙[17]所使用的方法一致, 实验中FISH定性所使用的泥样采集于2019年5月6日, 所使用的详细的寡核苷酸探针信息如表 4所示.分别于2019年3月1日、4月19及5月6日采集了不同运行阶段的污泥泥样进行了高通量测序, 高通量测序的实验过程如下:首先采用Fast DNA Spin Kit for Soil(QBIO gen IncCarlsba, CA, 美国)DNA提取试剂盒并按照其步骤要求完成不同泥样中总DNA的提取, 并将提取后的DNA送至上海美吉生物公司进行PCR扩增、PCR产物定量以及MiSeq文库构建, 最终获得经Illumina MiSeq高通量测序后的微生物群落结构信息.借助美吉云平台iSanger对3个样本中获得的不同序列按最小序列数进行数据抽平后, 进行了α多样性分析和Venn图的绘制, 以高通量测序后在不同分类学水平上获得的微生物相对丰度数据, 借助Excel进行数据分类汇总后, 采用Origin软件进行绘图.
|
|
表 4 FISH分析中采用的寡核普酸探针 Table 4 Oligonucleotide probes used in FISH |
2 结果与讨论 2.1 SBR工艺低温型丝状菌污泥膨胀的发生 2.1.1 低温下丝状菌污泥膨胀过程中的沉降性变化
从北京高碑店污水处理厂二沉池内取泥后, 于0.5 h内快速运回实验室, 并投加到反应器中进行培养, 测得原始泥样的SVI为95.6mL ·g-1, 污泥沉降性能较好.正式实验共3个阶段, 全阶段运行期间的污泥沉降性能及膨胀前后的扫描电镜效果见图 2.
|
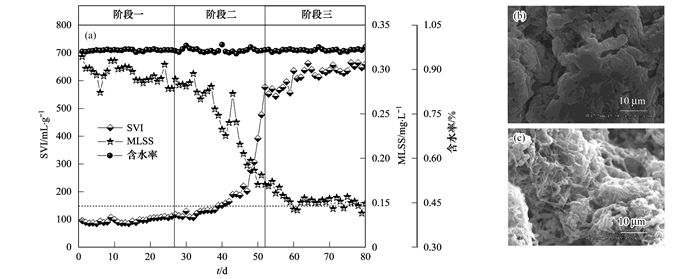
(a)全阶段污泥沉降性能变化; (b)原始泥样电镜图; (c)膨胀泥样电镜图 图 2 运行期间污泥沉降性能变化及扫描电镜 Fig. 2 Variations of SVI during operation and SEM observation |
如图 2所示, 本实验全阶段共运行90 d, 阶段一运行期间SVI值维持在85~100mL ·g-1, 沉降性能良好.阶段二为诱发丝状菌污泥膨胀将温度降至(14±1)℃后, SVI显著提升, 并在阶段二运行至第10 d时升至150 mL ·g-1, 发生污泥膨胀, 至全阶段运行至第52 d时, 污泥沉降性能已恶化至500 mL ·g-1以上.为防止污泥流失进一步加剧, 在不改变其它运行参数的前提下, 延长反应器沉淀时间, 进入阶段三, 运行期间系统污泥沉降性能逐渐稳定在600~700 mL ·g-1左右, 污泥流失现象消失.鉴于扫描电镜能够更加直观地展现污泥絮体表面形态和结构特征, 故对膨胀前后的污泥进行了扫描电镜观察, 可明显看出, 原始泥样的表面较为光滑, 整体形态较好, 而膨胀后的污泥絮体则粗糙多孔, 表面被丝状菌密集覆盖.说明膨胀对絮体形态结构产生了较大影响, 在污泥未发生膨胀时, 丝状菌多处于絮体的内部, 成为菌胶团菌絮凝在一起的骨架, 而当膨胀发生后, 原本位于絮体内部的丝状菌便会扩散生长, 菌丝伸出至絮体表面, 四散生长或包裹住原有的菌胶团菌.
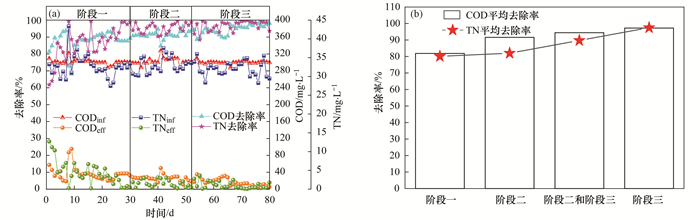
2.1.2 低温下丝状菌污泥膨胀过程中的污染物去除效果如图 3所示, 反应器运行期间全阶段污水处理效果较好, 尽管COD和TN的去除效果在系统运行初期曾出现较小的波动, 但随着反应器的运行波动现象消失, 去除效果转好, 说明污泥驯化较为成功.值得注意的是, 尽管本实验在低温条件下成功诱发了丝状菌污泥膨胀, 但污染物去除效果并未随沉降性能的恶化而变差, 反而越来越好, 造成该结果的原因主要有以下几点.首先, 阶段一运行前期, 污泥尚未完全适应本实验的进水水质, 所以该阶段一些较差的出水水质拉低了膨胀前系统的污染物平均去除率.而在阶段二开始后, 降低的温度虽会影响到部分降解污染物的功能菌的代谢与增殖, 但随之发生的污泥膨胀使得丝状菌从絮体内部伸出, 产生了网捕作用[21], 进而促进了水质的净化, 提升了污染物的去除效果.之后, 随着污泥沉降性能的继续恶化, 丝状菌大量增殖使得网捕作用进一步加大, 水质的净化作用进一步提高.此外, 由于本实验中在低温条件下大量增殖的优势丝状菌为Thiothrix, 其脱氮能力已在相关报道中得到验证[22], 故该菌的大量增殖也是出水水质提升的重要原因.
|
(a)全阶段污染物进出水及去除率; (b)不同阶段内污染物平均去除率 图 3 全阶段运行期间污染物去除效果 Fig. 3 Pollutants removal effect during the continuous operational period |
为克服传统丝状菌不易纯培养的困境, 深度分析不同膨胀状态下活性污泥内微生物菌群结构及多样性变化, 探究污泥微生物与系统沉降性能、出水水质之间的相关关系, 选取膨胀前、轻微膨胀及恶性膨胀3个阶段内的污泥样品进行Illumina MiSeq高通量测序, 多样性分析结果如表 5和图 4所示.
|
|
表 5 不同污泥样品的α多样性分析 Table 5 The α diversity analysis of different sludge samples |
|
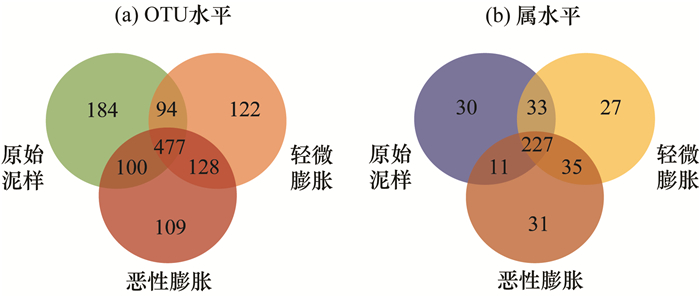
图 4 Veen图 Fig. 4 Venn diagram |
由表 5可知, 从本次测序的3个污泥样品中分别获得了40 671、49 704和43 265条优化序列, 为便于后续不同样本微生物多样性之间的对比分析, 以最少序列样本40671进行数据抽平, 抽平后3个泥样的微生物序列数据总量一致.在97%的相似水平下进行Alpha多样性分析, 并对非重复序列进行操作分类单元(OTU)划分, 在3个不同的污泥样本中分别得到855、821和814个OTUs, 呈降低趋势, 说明随污泥沉降性能的恶化, 系统内微生物种类数减少.此外, Ace与Shannon指数都呈降低趋势, Simpson指数呈升高趋势, 由于Ace指数和Simpson指数主要用来衡量样本的多样性及反映样品中微生物的丰富度, Ace指数越小, Simpson指数越大, 则系统内物种多样性越小, 而Shannon指数除用于评估污泥中的微生物的多样性外, 还可用于评估其均一性, 可见本实验中微生物的均一性也呈下降趋势.故随污泥沉降性能的逐渐恶化, 系统内的物种种类数、多样性、丰富度及均一性均呈降低趋势.利用Venn图分别在OTU水平和属水平进行多样性分析, 发现有498个OTUs和232个菌属同时存在于3种不同沉降性能的污泥中, 这说明尽管运行条件如温度、沉淀时间和污泥沉降性能均发生了较大的改变, 实验中污泥样品内的微生物种群整体仍呈稳定状态.
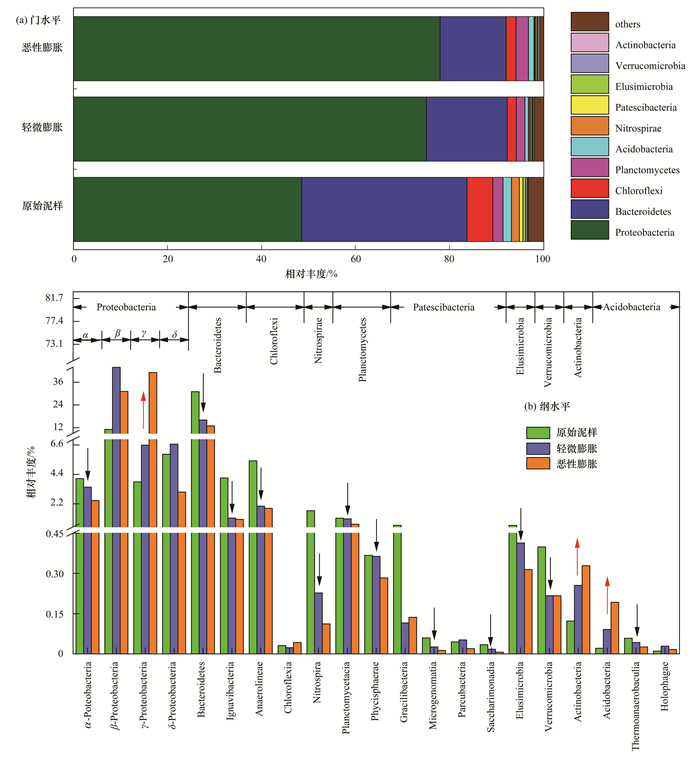
2.2.2 微生物菌群整体多样性变化从图 5中两种不同分类学水平上的测序结果来看, 共有10种门类的微生物在膨胀过程中被发现, 其中占比排在前三位的分别为变形菌门(Proteobacteria)、拟杆菌门(Bacteroidetes)和绿弯菌门(Chloroflexi).作为众多水处理领域微生物研究中的优势门类, Proteobacteria门的相对丰度由原泥中的48.54%上升至恶性膨胀后的77.96%, 扩大了60%.从纲水平的分析结果可知, 在脱氮除磷中发挥重要作用的β-变形菌纲(β-Proteobacteria)是该门类下的优势菌群, 由于其在本实验中的相对丰度随污泥膨胀的发生先升高后降低, 整体呈升高趋势, 故对污染物处理效果影响不大.此外, 同样来自Proteobacteria门下的α-变形菌纲(α-Proteobacteria)、γ-变形菌纲(γ-Proteobacteria)和δ-变形菌纲(δ-Proteobacteria)的相对丰度分别呈现出了递增, 递减和先增后减的变化趋势, 说明同一门类下微生物菌群的相对丰度变化趋势不具有共性.
|
图 5 微生物菌群整体多样性变化 Fig. 5 Overall changes in microbial community diversity |
作为本实验中占比第二大的微生物菌群, Bacteroidetes门的相对丰度随污泥膨胀的发生呈递减趋势, Hill等[23]的研究认为该门类的微生物具有非常强的营养物质代谢能力, 可降解如蛋白质和脂类等复杂的有机物, 该门类下的优势菌纲为拟杆菌纲(Bacteroidetes), 相对丰度同样呈递减趋势.有研究称Chloroflexi门的微生物不仅广泛存在于城市污水厂中[24], 在废水厌氧处理系统及颗粒污泥中也经常出现, 且具有较好的生物除磷作用.该门下的优势菌纲为厌氧绳菌纲(Anaerolineae), 其相对丰度随污泥膨胀的发生而降低, 而赵婷婷等[25]在淀粉废水下的膨胀污泥中也得到了相似结论, 说明该菌对污泥膨胀具有一定的指示作用.作为活性污泥中典型脱氮菌群的硝化螺旋菌门(Nitrospirae)以及该分类下的硝化螺旋菌纲(Nitrospira)随污泥膨胀的发生相对丰度同样不断降低, 与Wang等[26]在实际污水厂中得到的研究结果较为一致.值得注意的是, 常引发活性污泥系统泥水分离问题的放线菌门(Actinobacteria), 在本实验中的相对丰度虽呈递增趋势, 但总样本量中的整体比例却很小, 这说明造成此次污泥膨胀的优势丝状菌并非来自Actinobacteria门.
从微生物菌群的整体多样性分析中可以发现, 不同菌群的丰度变化与其在污水处理中所执行的功能密切相关, 而环境中温度的变化影响并改变了它们在活性污泥中的总体分布, 从而引发了污泥膨胀的发生.如Nitrospira及Anaerolineae纲在本实验以及其它膨胀研究中表现出的相同变化规律, 说明某些菌群与污泥膨胀之间极有可能存在固定的相关关系, 如能准确获得这些微生物的具体名称及生理生态学特性或许将为实现污泥膨胀的防治带来可能.
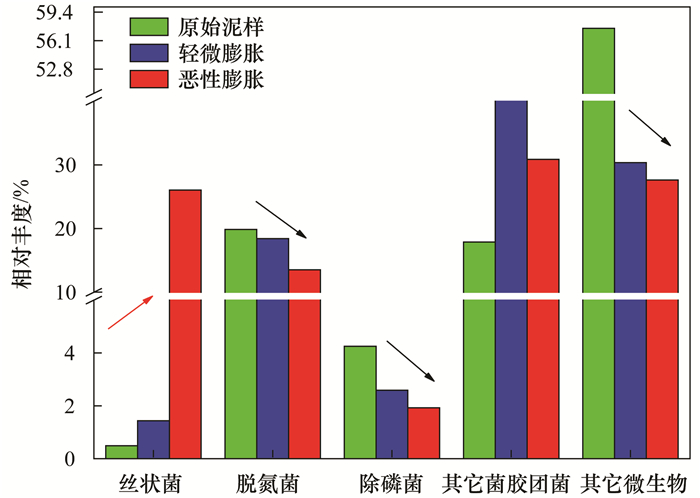
2.3 膨胀污泥各特定菌群与特定菌属的变化特征由于不同菌群在污水处理过程中所执行的功能体现了其独特的生理特性, 而环境的变化会通过影响微生物的生理特性来影响污水的处理效果与污泥的沉降性能, 故将属水平下检测出的, 除名称不明的微生物外的全部菌属进行文献检索后, 按照其在研究报道中所展现出的主要功能进行分类, 以便于对系统内不同微生物菌群多样性变化的分析.如图 6所示, 将系统中所有相对丰度≥0.01%的菌属按照其在污水处理过程中展现的性能进行分类合并后, 共得到5种不同的微生物群体, 分别为在活性污泥中扩散生长并起丝状骨架作用的丝状菌群、起脱氮除磷作用的脱氮菌群和除磷菌群、其它功能不明的菌胶团菌以及没有检测出名称的其它微生物.可以发现, 随污泥沉降性能的恶化, 丝状菌群整体的相对丰度显著递增, 由阶段一的0.48%升至阶段三的26.04%, 扩大了53.25倍, 而脱氮菌和除磷菌两种功能菌群的相对丰度却呈降低趋势, 分别由最初的19.85%和4.25%降低至轻微膨胀时的18.43%和2.59%, 并最终降低至恶性膨胀阶段的13.51%和1.93%, 减少了32%和54.59%.除以上在污水处理过程中发挥主要作用的微生物外, 系统中检测出的其它菌胶团菌的相对丰度无显著变化, 而其它不明微生物的相对丰度虽呈递减趋势, 但由于菌属名称及性质不明, 故后续不做进一步的分析.
|
图 6 各特定菌群的微生物多样性变化 Fig. 6 Changes in microbial diversity of specific community |
如图 7所示, 对膨胀泥样进行的镜检染色显示优势丝状菌呈革兰氏阴性、无分枝、菌丝较粗且内有硫粒积累, 推断为发硫菌属(Thiothrix), 进一步的FISH定性验证了这一推断.此外, 实验中共发现5种丝状菌属, 其中有3种的相对丰度随污泥沉降性能恶化呈递增趋势, 1种呈递减趋势, 另一种无明显规律.优势丝状菌Thiothrix在初始泥样中的占比仅为0.002%左右, 但随恶性膨胀的发生最终提高至25.9%, 成为第一优势丝状菌.Thiothrix来自变形菌门, 生理学的研究表明其具有自养、兼氧特性, 不仅能够以脂肪酸类的低分子化合物为营养源, 还能将NO3-还原为NO2-[27].Haliscomenobacter是本实验中占比第二的丝状菌属, 研究称[28]其丰度一般随水温的升高而下降, 在低温甚至超低温(≤10℃)下丰度会相对较高, 而在本实验中, 其相对丰度却随温度的降低呈递减趋势, 这说明在本实验中有温度以外的因素对Haliscomenobacter的丰度产生了影响.来自Actinobacteria门的Tetrasphaera在本实验中的相对丰度呈递增趋势, 该菌属下的诺卡氏菌(Nostocoida limicola)是造成活性污泥膨胀的常见物种.虽然Tessaracoccus在原始泥样中的相对丰度仅为0.001 5%, 但至阶段末恶性膨胀发生时提升到了0.013%, 扩大了约8倍, 它是一种革兰氏阳性的兼性厌氧菌, 不能运动且不产孢子.尽管都来自Actinobacteria门, 分枝杆菌属(Mycobacterium)却与Tessaracoccus不同, 没有明显变化规律.

|
(a)革兰氏染色图; (b)FISH镜检图; (c)丝状菌的相对丰度变化 图 7 染色镜检与丝状菌的相对丰度变化 Fig. 7 Microscopic staining and changes in relative abundance of filamentous bacteria |
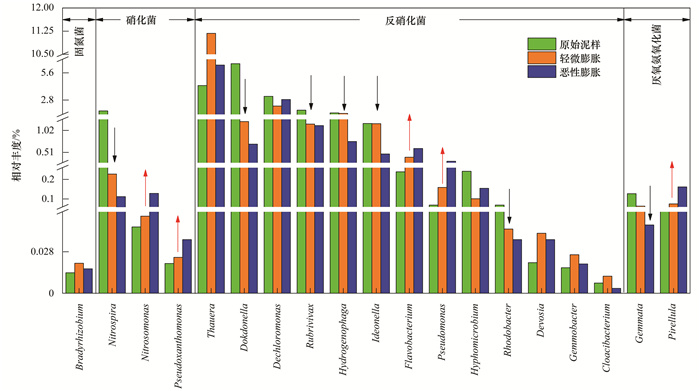
如图 8所示, 在本实验发现的参与生物脱氮的19种菌属中, 有亚硝化单胞菌属(Nitrosomonas)、假黄色单胞菌属(Pseudoxanthomonas)、黄杆菌属(Flavobacterium)、假单胞菌属(Pseudomonas)和小梨形菌属(Pirellula)共5种菌属的相对丰度呈递增趋势, 硝化螺旋菌属(Nitrospira)、Dokdonella、红长命菌属(Rubrivivax)、嗜氢菌属(Hydrogenophaga)、Ideonella、红杆菌属(Rhodobacter)和Gemmata共7种菌属的相对丰度呈递减趋势.为便于分析, 将这些菌属分成了固氮菌、硝化菌、反硝化菌和厌氧氨氧化菌这4个部分, 发现唯一一种来自固氮菌群的菌属Bradyrhizobium在本实验中的相对丰度先升高后降低, 没有显著规律.而来自反硝化菌群的3种菌属中, Nitrospira是唯一一种丰度递减的菌属, 这可能与其既能执行氨氧化功能, 又能执行亚硝酸盐氧化功能的独特性质有关, 作为一种典型的脱氮菌, 在相关研究中相对丰度也随膨胀的发生而逐渐下降[25], 且被认为与丝状菌存在竞争关系.Nitrosomonas是一种影响含氮污染物转化途径的关键菌属[29], 在氨氮转化为羟胺的过程中起主导作用, 郝明辉等[30]曾筛选出1株能进行异养硝化作用, 快速繁殖且可以高效去除氨氮的Pseudoxanthomonas菌, 而本实验中Nitrosomonas和Pseudoxanthomonas菌两者同样递增的相对丰度说明温度及膨胀对其增殖的影响不大.在本实验发现的13种反硝化菌属中, 占比最大的为来自β-Proteobacteria纲的Thauera, 该菌属广泛存在于各种类型的废水处理装置中并能降解大部分主要有机物, 是一种具有多种芳香族污染物降解能力的重要功能菌[31].此外, 本实验还发现了Gemmata和Pirellula两种厌氧氨氧化菌属, 尽管黄方玉等[32]在相关研究中认为, 由于厌氧氨氧化菌对温度更敏感, 所以低温条件会引起反应器脱氮性能的下降, 但在本实验中的低温条件下系统仍体现了较好的总氮的去除效果, 且Pirellula的相对丰度随温度下降呈上升趋势.
|
图 8 脱氮菌的相对丰度变化 Fig. 8 Changes in relative abundance of denitrifying bacteria |
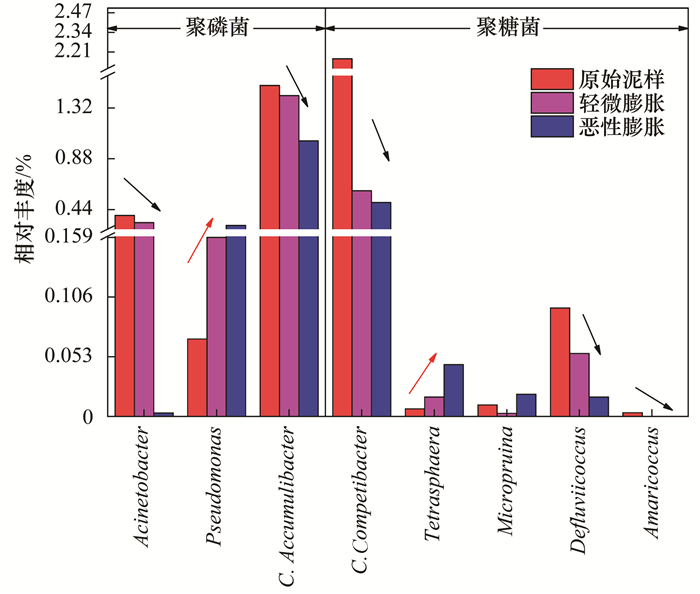
如图 9所示, 将本实验中发现的8种参与除磷的菌属分为聚磷菌和聚糖菌两大类, 可看出Candidatus_ Accumulibacter是聚磷菌中占比最大的菌属, 其相对丰度随污泥沉降性能的恶化而逐渐降低, 这与高晨晨等[33]和Wang等[34]的研究结果较为一致, 说明该菌在膨胀污泥中存在较为普遍的丰度降低现象.同样作为聚磷菌的不动杆菌属(Acinetobacter)与其变化趋势相同, 该菌属在自然界中分布较为广泛且可以在很宽的温度范围内生长[35], 故其在原泥中0.39%到恶性膨胀中0.003 3%相对丰度的大幅降低表明有温度以外的因素对它的生长产生了影响.假单胞菌属(Pseudomonas)是本实验所发现的聚磷菌中唯一一种相对丰度递增的菌属, 由于其包含多种反硝化聚磷菌, 因而既可被归类于反硝化菌也可被归类于除磷菌.在发现的5种聚糖菌属中, 有3种的相对丰度随污泥沉降性能的恶化而递减, 分别为Candidatus_Competibacter、Defluviicoccus和Amaricoccus, 其中C.Competibacter和Defluviicoccus的占比最大, 且在洪颖[36]与Henriet等[37]的研究中均被认为是有利于污泥沉降的微生物菌属, 而两者随污泥膨胀呈现出的丰度降低也印证了这种说法.由于聚糖菌中的Amaricoccus在原泥中的占比微弱(0.003 4%), 在后续的轻微膨胀及恶性膨胀污泥中均消失不见, 故对污泥性质的影响较小.作为EBPR系统中最丰富的除磷菌之一, Tetrasphaera菌属的分类下还含有以N.limicola为代表的丝状菌, 因而可以参与到污泥膨胀中并表现出逐渐递增的丰度变化.此外, 唯一一种相对丰度没有发生变化的菌属是Micropruina.
|
图 9 除磷菌的相对丰度变化 Fig. 9 Changes in relative abundance of phosphate-removing bacteria |
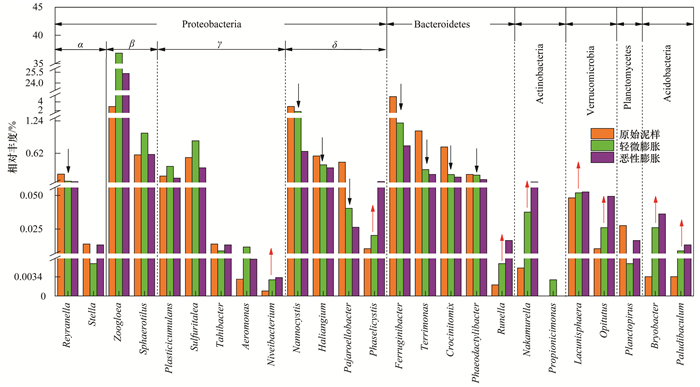
如图 10, 为便于分析, 对属水平上发现的其它菌胶团菌中相对丰度占比在前25的菌属进行绘图, 发现共有8种菌属(32%)的相对丰度呈递增趋势, 8种菌属(32%)的相对丰度呈递减趋势, 仅6种菌属(24%)在活性污泥中的相对丰度超过1%, 所有菌属大多来自Proteobacteria门(52%)和Bacteroidetes门(20%).在25种菌属中, 占比最大的为来自β-Proteobacteria纲的动胶菌属(Zoogloea), 作为一种典型的好氧菌胶团菌, Zoogloea不仅能够有效降低污水的生物需氧量(BOD)和化学需氧量(COD), 在脱氮除磷过程中也发挥着重要作用, 从而在许多污水处理工艺中都占有优势地位.虽然在本实验中Zoogloea的相对丰度先增高后降低, 但其在恶性膨胀时的相对丰度25.32%仍远高于原泥中的2.92%, 说明该菌在低温及膨胀条件下仍能较好地增殖.在8种相对丰度递增的菌属中, 占比最大的为来自δ-Proteobacteria纲的Phaselicystis, 该菌在其它报道中较为少见, 仅刘欣等[38]曾在土壤有关的研究中将其划分为类诺卡式菌, 这说明其相对丰度的增高可能与其本身与丝状菌的相似性有关.而在8种相对丰度递减的菌属中, 占比最大的为来自Bacteroidetes门的Ferruginibacter, 一种以颗粒态有机物作为电子供体进行降解的絮凝细菌, 且能够参与细胞合成和EPS的分泌[39].刘小博等[40]的研究认为该菌属可对菌胶团菌的生长起到积极促进的作用.由于检测出的其它菌胶团菌数量较多, 且仍有大量菌属在活性污泥中的相对丰度不足1%, 所以对于这些系统占比较低的微生物在水处理以及污泥膨胀中的影响及意义仍有待考证.
|
图 10 其它菌胶团菌的相对丰度变化 Fig. 10 Changes in relative abundance of other zoogloea bacteria |
(1) 采用传统硝化反硝化工艺并将运行温度降至(14±1)℃后可成功诱发丝状菌污泥膨胀, SVI最高可升至663.99 mL ·g-1, 虽然全阶段运行期间污泥沉降性能恶化严重, 但并未影响到污水处理效果, COD去除率可维持在90%左右, TN去除率可维持在86%左右.
(2) 污泥膨胀的发生会导致系统内微生物的多样性减小、均一性降低, 常见门类中Proteobacteria门相对丰度的升高以及Bacteroidetes门、Nitrospirae门和Patescibacteria门丰度的降低.虽然污泥膨胀对微生物菌群结构产生较大影响, 但不同泥样中始终存在的477个OTUs和227个菌属说明反应器内主要微生物的分布仍呈相对稳定状态.
(3) 在特定菌群的分析中, 发现低温下污泥膨胀的发生会引起丝状菌群丰度的升高以及脱氮菌群、除磷菌群丰度的下降.在特定菌属的分析中, 共发现5种丝状菌属, 其中以Thiothrix为代表的3种菌属的丰度递增, 仅Haliscomenobacter的丰度递减; 共发现19种脱氮菌属, 其中以Nitrosomonas为代表的5种菌属的丰度递增, 以Nitrospira为代表的7种菌属的丰度递减; 共发现8种除磷菌属, 其中Pseudomonas和Tetrasphaera的丰度递增, 以C.Competibacter为代表的5种菌属丰度递减.
(4) 以Zoogloea为代表的25种其它菌胶团菌大多来自Proteobacteria门(52%)和Bacteroidetes门(20%), 其中又以Niveibacterium为代表的8种菌属丰度递增, 以Reyranella为代表的8种菌属的丰度递减.
| [1] | Wang P, Yu Z S, Zhao J H, et al. Seasonal changes in bacterial communities cause foaming in a wastewater treatment plant[J]. Microbial Ecology, 2016, 71(3): 660-671. DOI:10.1007/s00248-015-0700-x |
| [2] | Wang B B, Zhang L, Peng D C, et al. Extended filaments of bulking sludge sink in the floc layer with particulate substrate[J]. Chemosphere, 2013, 93(11): 2725-2731. DOI:10.1016/j.chemosphere.2013.08.099 |
| [3] | Vuilleumier S, Nadalig T, Ul Haque M F, et al. Complete genome sequence of the chloromethane-degrading Hyphomicrobium sp. Strain MC1[J]. Journal of Bacteriology, 2011, 193(18): 5035-5036. DOI:10.1128/JB.05627-11 |
| [4] |
高春娣, 安冉, 韩徽, 等. Type 0092丝状菌污泥微膨胀在短程硝化中的实现[J]. 环境科学, 2019, 40(8): 3722-3729. Gao C D, An R, Han H, et al. Realization of limited filamentous bulking with Type 0092 filamentous bacteria as the dominant filamentous bacteria in shortcut nitrification[J]. Environmental Science, 2019, 40(8): 3722-3729. |
| [5] |
高春娣, 孙大阳, 安冉, 等. 间歇曝气下短程硝化耦合污泥微膨胀稳定性[J]. 环境科学, 2018, 39(7): 3271-3278. Gao C D, Sun D Y, An R, et al. Stability of nitritation combined with limited filamentous bulking under intermittent aeration[J]. Environmental Science, 2018, 39(7): 3271-3278. |
| [6] | Nielsen P H, Kragelund C, Seviour R J, et al. Identity and ecophysiology of filamentous bacteria in activated sludge[J]. FEMS Microbiology Reviews, 2009, 33(6): 969-998. DOI:10.1111/j.1574-6976.2009.00186.x |
| [7] | Rossetti S, Tomei M C, Nielsen P H, et al. "Microthrix parvicella", a filamentous bacterium causing bulking and foaming in activated sludge systems:a review of current knowledge[J]. FEMS Microbiology Reviews, 2005, 29(1): 49-64. DOI:10.1016/j.femsre.2004.09.005 |
| [8] |
高春娣, 赵楠, 安冉, 等. FNA对短程硝化污泥菌群结构的影响[J]. 中国环境科学, 2019, 39(5): 1977-1984. Gao C D, Zhao N, An R, et al. Effect of FNA on microorganism community structures of partial nitrification sludge[J]. China Environmental Science, 2019, 39(5): 1977-1984. DOI:10.3969/j.issn.1000-6923.2019.05.022 |
| [9] | Yuan L, Zhi W, Liu Y S, et al. Lead toxicity to the performance, viability, and community composition of activated sludge microorganisms[J]. Environmental Science & Technology, 2015, 49(2): 824-830. |
| [10] |
黄薇, 刘兰英, 吴妙鸿, 等. 养殖废水处理系统中微生物菌群结构及动态变化[J]. 中国环境科学, 2019, 39(2): 839-848. Huang W, Liu L Y, Wu M H, et al. Microbial community structure and dynamics in swine wastewater treatment system[J]. China Environmental Science, 2019, 39(2): 839-848. DOI:10.3969/j.issn.1000-6923.2019.02.049 |
| [11] | Ji B, Zhang X C, Zhang S F, et al. Insights into the bacterial species and communities of a full-scale anaerobic/anoxic/oxic wastewater treatment plant by using third-generation sequencing[J]. Journal of Bioscience and Bioengineering, 2019, 128(6): 744-750. DOI:10.1016/j.jbiosc.2019.06.007 |
| [12] |
谢慧娜, 王亚娥, 李杰, 等. 不同价态铁处理腈纶废水过程中菌群结构分析[J]. 中国环境科学, 2018, 38(9): 3406-3412. Xie H N, Wang Y E, Li J, et al. Analysis of microbial community structure in acrylic fiber wastewater treated by different valence forms of iron[J]. China Environmental Science, 2018, 38(9): 3406-3412. DOI:10.3969/j.issn.1000-6923.2018.09.026 |
| [13] | Nakasaki K, Koyama M, Maekawa T, et al. Changes in the microbial community during the acclimation process of anaerobic digestion for treatment of synthetic lipid-rich wastewater[J]. Journal of Biotechnology, 2019, 306: 32-37. DOI:10.1016/j.jbiotec.2019.09.003 |
| [14] | Bengtsson-Palme J, Milakovic M, Švecová H, et al. Industrial wastewater treatment plant enriches antibiotic resistance genes and alters the structure of microbial communities[J]. Water Research, 2019, 162: 437-445. DOI:10.1016/j.watres.2019.06.073 |
| [15] | 国家环境保护总局. 水和废水监测分析方法[M]. ((第四版)). 北京: 中国环境科学出版社, 2002. |
| [16] | GB 18918-2002, 城镇污水处理厂污染物排放标准[S]. |
| [17] | 焦二龙.污水生物脱氮过程丝状菌污泥膨胀与控制研究[D].北京: 北京工业大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10005-1013047126.htm |
| [18] | Amann R I, Binder B J, Olson R J, et al. Combination of 16s rRNA-targeted oligonucleotide probes with flow cytometry for analyzing mixed microbial populations[J]. Applied and Environmental Microbiology, 1990, 56(6): 1919-1925. DOI:10.1128/AEM.56.6.1919-1925.1990 |
| [19] | Daims H, Brühl A, Amann R, et al. The domain-specific probe EUB338 is insufficient for the detection of all Bacteria:development and evaluation of a more comprehensive probe set[J]. Systematic and Applied Microbiology, 1999, 22(3): 434-444. DOI:10.1016/S0723-2020(99)80053-8 |
| [20] | Wagner M, Amann R, Kämpfer P, et al. Identification and in situ detection of Gram-negative filamentous bacteria in activated sludge[J]. Systematic and Applied Microbiology, 1994, 17(3): 405-417. DOI:10.1016/S0723-2020(11)80058-5 |
| [21] | 彭永臻, 郭建华. 活性污泥膨胀机理、成因及控制[M]. 北京: 科学出版社, 2012. |
| [22] | Trubitsyn I V, Belousova E V, Tutukina M N, et al. Expansion of ability of denitrification within the filamentous colorless sulfur bacteria of the genus Thiothrix[J]. FEMS Microbiology Letters, 2014, 358(1): 72-80. DOI:10.1111/1574-6968.12548 |
| [23] | Hill V R, Kahler A M, Jothikumar N, et al. Multistate evaluation of an ultrafiltration-based procedure for simultaneous recovery of enteric microbes in 100-liter tap water samples[J]. Applied and Environmental Microbiology, 2007, 73(13): 4218-4225. DOI:10.1128/AEM.02713-06 |
| [24] | Larsen P, Nielsen J L, Otzen D, et al. Amyloid-like adhesins produced by floc-forming and filamentous bacteria in activated sludge[J]. Applied and Environmental Microbiology, 2008, 74(5): 1517-1526. DOI:10.1128/AEM.02274-07 |
| [25] |
赵婷婷, 乔凯, 王蕾, 等. 淀粉废水处理系统中活性污泥的微生物群落结构及多样性分析[J]. 环境科学, 2020, 41(1): 321-329. Zhao T T, Qiao K, Wang L, et al. Measurements of bacterial community and biodiversity from activated sludge for a wastewater treatment containing starch[J]. Environmental Science, 2020, 41(1): 321-329. |
| [26] | Wang P, Yu Z S, Qi R, et al. Detailed comparison of bacterial communities during seasonal sludge bulking in a municipal wastewater treatment plant[J]. Water Research, 2016, 105: 157-166. DOI:10.1016/j.watres.2016.08.050 |
| [27] | Aruga S, Kamagata Y, Kohno T, et al. Characterization of filamentous Eikelboom type 021N bacteria and description of Thiothrix disciformis sp. Nov. and Thiothrix flexilis sp. nov[J]. International Journal of Systematic and Evolutionary Microbiology, 2002, 52(4): 1309-1316. |
| [28] | Ma Z, Wen X H, Zhao F, et al. Effect of temperature variation on membrane fouling and microbial community structure in membrane bioreactor[J]. Bioresource Technology, 2013, 133: 462-468. DOI:10.1016/j.biortech.2013.01.023 |
| [29] | Yu T, He P J, Lü F, et al. Mediating N2O emissions from municipal solid waste landfills:impacts of landfill operating conditions on community structure of ammonia-oxidizing bacteria in cover soils[J]. Ecological Engineering, 2009, 35(5): 882-889. DOI:10.1016/j.ecoleng.2008.12.025 |
| [30] |
郝明辉, 于鲁冀, 李廷梅, 等. 一株异养硝化菌的筛选及生长特性研究[J]. 生物技术通报, 2016, 32(4): 168-174. Hao M H, Yu L Y, Li T M, et al. Screening and growth characteristics of a heterotrophic nitrification bacterium[J]. Biotechnology Bulletin, 2016, 32(4): 168-174. |
| [31] |
郑林雪, 李军, 胡家玮, 等. 同步硝化反硝化系统中反硝化细菌多样性研究[J]. 中国环境科学, 2015, 35(1): 116-121. Zheng L X, Li J, Hu J W, et al. Analysis of denitrifying bacteria community composition in simultaneous nitrification and denitrification systems[J]. China Environmental Science, 2015, 35(1): 116-121. |
| [32] |
黄方玉, 邓良伟, 杨红男, 等. 温度对自养型同步脱氮工艺处理猪场废水厌氧消化液性能及微生物群落的影响[J]. 环境科学, 2019, 40(5): 2357-2367. Huang F Y, Deng L W, Yang H N, et al. Effect of different temperatures on the performance of autotrophic nitrogen removal and microbial community from swine wastewater[J]. Environmental Science, 2019, 40(5): 2357-2367. |
| [33] |
高晨晨, 游佳, 陈轶, 等. 丝状菌污泥膨胀对脱氮除磷功能菌群的影响[J]. 环境科学, 2018, 39(6): 2794-2801. Gao C C, You J, Zheng Y, et al. Effect of denitrification and phosphorus removal microorganisms in activated sludge bulking caused by filamentous bacteria[J]. Environmental Science, 2018, 39(6): 2794-2801. |
| [34] | Wang J, Qi R, Liu M M, et al. The potential role of 'Candidatus Microthrix parvicella' in phosphorus removal during sludge bulking in two full-scale enhanced biological phosphorus removal plants[J]. Water Science & Technology, 2014, 70(2): 367-375. |
| [35] | Saunders A M, Oehmen A, Blackall L L, et al. The effect of GAOs (glycogen accumulating organisms) on anaerobic carbon requirements in full-scale Australian EBPR (enhanced biological phosphorus removal) plants[J]. Water Science and Technology, 2003, 47(11): 37-43. DOI:10.2166/wst.2003.0584 |
| [36] |
洪颖, 姚俊芹, 马斌, 等. 基于高通量测序的SBR反应器丝状膨胀污泥菌群分析[J]. 环境科学, 2018, 39(7): 3279-3285. Hong Y, Yao J Q, Ma B, et al. Filamentous sludge microbial community of a SBR reactor based on high-throughput sequencing[J]. Environmental Science, 2018, 39(7): 3279-3285. |
| [37] | Henriet O, Meunier C, Henry P, et al. Filamentous bulking caused by Thiothrix species is efficiently controlled in full-scale wastewater treatment plants by implementing a sludge densification strategy[J]. Scientific Reports, 2017, 7(1): 1430. DOI:10.1038/s41598-017-01481-1 |
| [38] |
刘欣, 李志英, 刘瑞瑞, 等. 大豆不同生育期根际土壤细菌群落结构的变化[J]. 广西植物, 2018, 38(10): 1363-1370. Liu X, Li Z Y, Liu R R, et al. Changes of bacterial flora structure in rhizosphere soil of soybean at different growth stages[J]. Guihaia, 2018, 38(10): 1363-1370. DOI:10.11931/guihaia.gxzw201712023 |
| [39] | An W X, Guo F, Song Y L, et al. Comparative genomics analyses on EPS biosynthesis genes required for floc formation of Zoogloea resiniphila and other activated sludge bacteria[J]. Water Research, 2016, 102: 494-504. DOI:10.1016/j.watres.2016.06.058 |
| [40] |
刘小博, 袁林江, 陈希, 等. 有机物特性对AAO系统污泥沉降性能的影响[J]. 环境科学, 2019, 40(7): 3186-3194. Liu X B, Yuan L J, Chen X, et al. Effect of organic characteristics on sludge settleability in an AAO System[J]. Environmental Science, 2019, 40(7): 3186-3194. |
 2020, Vol. 41
2020, Vol. 41

