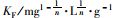2. 江苏省石油化工安全与环保工程研究中心, 常州 213164;
3. 贵州大学农学院, 贵阳 550025
2. Jiangsu Petrochemical Safety and Environmental Engineering Research Center, Changzhou 213164, China;
3. College of Agriculture, Guizhou University, Guiyang 550025, China
重金属污染是当前重要的环境问题之一.含镉(Cd)废水作为危害最严重的重金属废水之一, 可通过采矿、冶金、染料和电镀等工业活动排放的废水进入水体环境, 并进一步通过食物链的传递和富集最终转移到人体, 导致心脑血管疾病、肾衰竭和癌症等, 严重影响人类的健康[1].因此如何有效处理含镉废水, 已经成为国内外研究的热点.
目前对废水中重金属的处理方法主要有沉淀法、吸附法、离子交换法和膜分离法等[2], 其中吸附法因其方法简单、经济高效和绿色环保而备受关注[3].在吸附法中, 吸附剂是决定重金属污染水体是否能成功修复的重要环节, 因此, 通过吸附法处理含有重金属的废水时, 应开发高效、经济和安全的吸附剂[4].
生物炭是由生物质原料在缺氧下经高温热解产生的高度芳香化的富碳物质, 其呈碱性, 比表面积大, 表面含有丰富的官能团和大量的负电荷等, 能有效吸附污染物[5, 6].同时, 其原料来源广、成本低而备受关注.但不同原料、不同热解温度和时间下制备的生物炭的性质和结构存在很大的不同, 吸附重金属的能力存在明显的差异.有研究表明, 作物秸秆生物炭对重金属的吸附能力较畜禽粪便和木材生物炭好[1].
小麦是我国主要的粮食作物之一, 秸秆产量大, 可用于制备生物炭, 但大量的小麦秸秆被焚烧或堆置, 不仅造成资源浪费而且导致环境污染.因此利用小麦秸秆制备生物炭不仅实现农业废弃物资源化利用和减少其所引起的环境问题, 而且因其具有良好的吸附性能可用于对重金属污染水体的治理和修复. Wang等[6]的研究表明, 350℃和550℃两种炭化温度制备的小麦秸秆生物炭, 比表面积分别为0.97 m2·g-1和0.75 m2·g-1, 对Cd2+的去除率均低于3%.刘莹莹等[7]的研究表明, 小麦秸秆生物炭对Cd2+最大理论吸附量仅为5.95 mg·g-1. Sun等[8]的研究表明, 200℃下炭化得到的小麦秸秆生物炭, 其比表面积为7.98 m2·g-1, 孔容为0.000 128 cm3·g-1, 对溶液中Cd2+的吸附量为12.5 mg·g-1.由此可知, 直接热解制备的生物炭比表面积较小, 对溶液中Cd2+的吸附量也较小, 去除Cd2+效果不够理想, 因此如何提高其吸附性能成为近年来的研究热点.
大量研究表明, 酸、碱、氧化剂、负磁、纳米和无机材料等可改变生物炭的结构和性质, 从而提高其对重金属的吸附能力[8~15]. Sizmur等[8]的研究表明, 碱处理可增加生物炭的孔隙率和比表面积, 产生大量的含氧官能团, 从而提高对重金属的吸附性能. Sun等[9]的研究表明, 用KOH改性小麦秸秆生物炭, 其比表面积从7.98 m2·g-1增加到了241.63 m2·g-1, 同时芳香族和含氧官能团(如羧基)明显增加, 其对Cd2+的吸附量增加了1~2倍. Bashir等[10]的研究表明, 用NaOH改性稻秆生物炭, 增加了COO—、CH2和—OH等官能团, 导致其对Cd2+的吸附量明显增加.
尽管生物炭经碱改性后, 其吸附Cd2+的能力有较大的提高, 但生物炭本身作为一种吸附材料如何有效地从水体分离出来, 避免对水体造成二次污染, 逐渐受到人们关注. Thines等[11]的研究表明, 负磁改性可解决非磁性生物炭固液分离难的问题, 表现出良好的回收再生应用潜力.赵华轩等[12]的研究表明, Fe2 (SO4)3和FeSO4改性后的芦苇秆生物炭的比饱和磁化强度为6.71 emu·g-1, 表现出较强的磁性.朱司航等[13]的研究表明, Fe(NO3)3改性后的小麦秸秆生物炭具有超顺磁性, 其磁化强度为6.96 emu·g-1, 能进行分离和回收. Tan等[14]的研究表明, Fe2(SO4)3和FeSO4混合溶液改性后的稻秆生物炭具有良好的磁性, 能稳定地分散在水溶液中, 并可用永磁体将其从水溶液分离出来.杜文琪等[15]的研究表明, FeCl3和FeCl2混合溶液改性后的谷壳生物炭对Cd2+的吸附量为8.6 mg·g-1, 经3次“吸附-再生-再吸附”, 对Cd2+的吸附量仍达到7.1 mg·g-1, 显示出良好的吸附稳定性.但Sizmur等[8]的研究表明金属盐或金属氧化物改性生物炭, 会堵塞孔隙, 导致比表面积减小. Tan等[14]的研究表明, 氧化铁堵塞了稻杆生物炭的孔隙, 使其比表面积从5.398 m2·g-1降低到3.49 m2·g-1. Li等[16]的研究也表明, FeCl3改性油菜秸秆生物炭后, 其比表面积从19.13 m2·g-1减小到6.82 m2·g-1.由此可见, 单一的改性方法存在较多问题, 如改性效果不佳、二次污染和对重金属固着能力不强等.利用多种方法对生物炭进行复合改性的研究鲜见报道.
鉴于此, 本研究利用小麦秸秆制备原始生物炭, 并对其进行碱与磁复合改性, 通过对其进行表征、吸附动力学及影响因子分析, 探究复合改性生物炭对Cd2+的吸附性能和机制, 以期重金属污染治理及小麦秸秆的资源化利用提供理论依据.
1 材料与方法 1.1 实验试剂Ca(NO3)2、KOH、FeCl3·6H2O、HNO3、HCl、NaOH和CdCl2·2.5H2O均为分析纯, 购于国药集团化学试剂有限公司.
1.2 生物炭的制备 1.2.1 原始生物炭的制备小麦秸秆来源于江苏宿迁.小麦秸秆洗净、烘干后粉碎过20目筛, 置于管式炉中, 通入N2, 升温速率为10℃·min-1, 450℃下热解2 h, 自然冷却至室温后取出, 去离子水洗至中性, 80℃下烘干至恒重, 即制得小麦秸秆生物炭[17], 记为BC.
1.2.2 碱和磁复合改性生物炭的制备将BC浸渍在一定量2 mol·L-1 KOH溶液中, 固液比1:10(g:mL), 100℃下加热搅拌2 h, 自然冷却后过滤, 去离子水洗涤至pH不变, 80℃烘干, 即制得碱改性小麦秸秆生物炭[18], 记为KC.将干燥后的KC浸渍在一定量1 mol·L-1 FeCl3溶液中, 铁与生物炭质量比1:2, 用1 mol·L-1 NaOH调节pH至11, 混合静置4 h, 超声波处理30 min, 80℃搅拌2 h后80℃烘干, 去离子水洗涤至pH不变[19], 即制得碱和磁复合改性小麦秸秆生物炭, 记为FKC.
1.3 生物炭的结构表征采用带能谱的扫描电镜(D/MAX2500, 日本)观察BC和FKC的表面形貌特征, 采用吸附仪(TriStar3020, 美国)测定其比表面积和介孔结构分析, 采用傅立叶红外光谱仪(Nicolet IS5, 美国)测定其表面官能团, 采用X射线粉末衍射仪(Smartlab9, 日本)测定其晶体结构, 采用振动磁强计(Lake Shore7404, 美国)测定其磁化强度.
1.4 吸附实验 1.4.1 等温吸附设置Cd初始质量浓度梯度为0、10、20、30、40、50、70、90、110、130、150、200、250和300 mg·L-1, 以0.01 mol·L-1的Ca(NO3)2溶液作为背景电解质.分别准确称取0.05 g BC、KC和FKC于50 mL聚乙烯离心管, 加入25 mL不同浓度Cd2+溶液, 200 r·min-1下恒温(25℃±0.5℃)振荡24 h后, 过0.45 μm滤膜即为待测液.
1.4.2 吸附动力学分别准确称取0.05 g BC和FKC于50 mL聚乙烯离心管, 加入25 mL 50 mg·L-1的Cd2+溶液, 以0.01 mol·L-1的Ca(NO3)2溶液作为背景电解质, 200 r·min-1下恒温(25℃±0.5℃)振荡(THZ型, 上海精宏实验设备有限公司), 分别在5、10、20 min及0.5、1、2、4、8、12、24和36 h取出一组离心管, 过0.45 μm滤膜即为待测液.
1.4.3 吸附热力学实验分别准确称取0.05 g BC和FKC于50 mL聚乙烯离心管, 加入25 mL 50 mg·L-1的Cd2+溶液, 温度设置为25、30和35℃, 200 r·min-1下恒温振荡24 h后, 过0.45 μm滤膜即为待测液.
1.4.4 溶液初始pH值对吸附的影响分别准确称取0.05 g BC和FKC于50 mL聚乙烯离心管, 加入25 mL 50 mg·L-1的Cd2+溶液, 用1 mol·L-1 HNO3或NaOH调节pH为2、3、4、5、6、7和8, 200 r·min-1下恒温(25℃±0.5℃)振荡24 h后, 过0.45 μm滤膜即为待测液.
1.4.5 投加量对吸附的影响分别准确称取一定量的BC和FKC于50 mL聚乙烯离心管, 设投加量为1、2、10和20 g·L-1, 加入25 mL 50 mg·L-1的Cd2+溶液, 200 r·min-1下恒温(25℃±0.5℃)振荡24 h后, 过0.45 μm滤膜即为待测液.
1.4.6 吸附-解吸将等温吸附中吸附饱和后的BC和FKC分别加入到25 mL 1 mol·L-1的NaOH溶液中, 200 r·min-1下恒温(25℃±0.5℃)振荡解吸24 h, 用去离子水洗至pH不变, 烘干至恒重, 进行下一次吸附, 上述“吸附-解吸-再吸附”过程共循环3次, 每次吸附结束后过0.45 μm滤膜即为待测液.
以上每组实验均重复3次, 用原子吸收分光光度计(AA7000, 日本)测定待测液中Cd2+浓度.
1.5 数据处理通过平衡时生物炭对Cd2+的吸附量Qe和Cd2+去除率来判断其吸附能力, 按公式(1)和(2)计算:
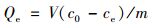
|
(1) |
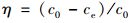
|
(2) |
式中, Qe是平衡吸附量, mg·g-1; c0是初始Cd2+浓度, mg·L-1; ce是平衡时Cd2+浓度, mg·L-1; m是生物炭质量, g; V是Cd2+溶液体积, mL; η是去除率, %.
通过准一级动力学方程[式(3)]、准二级动力学方程[式(4)]和颗粒内扩散方程[式(5)]分析生物炭对Cd2+的吸附动力学:
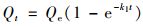
|
(3) |
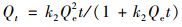
|
(4) |
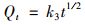
|
(5) |
式中, Qt为t时吸附量, mg·g-1; Qe为平衡时吸附量, mg·g-1; k1(h-1)、k2[g·(mg·h)-1]和k3[mg·(g·h1/2)-1]为动力学方程的速率常数.
通过Langmuir方程[式(6)]和Freundlich方程[式(7)]分析生物炭对Cd2+的吸附等温线:
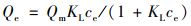
|
(6) |
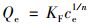
|
(7) |
通过分离因子与初始浓度的关系曲线判断吸附能力大小, 按公式(8)计算:
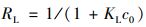
|
(8) |
式中, ce为吸附平衡时Cd2+浓度, mg·L-1; Qe为吸附平衡时Cd2+吸附量, mg·g-1; KL为Langmuir模型参数, L·mg-1; Qm为理论最大吸附量, mg·g-1; KF为Freundlich模型参数, 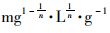
通过吉布斯自由能变化(ΔGθ)[式(9)]、熵变(ΔSθ)和焓变(ΔHθ)[式(10)]分析生物炭对Cd2+的吸附热力学:
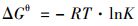
|
(9) |
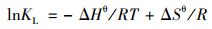
|
(10) |
式中, R为气体常数, 8.314 J·(mol·K)-1; T是热力学温度, K; K是吸附量和平衡浓度的线性方程的截距, L·mol-1.
2 结果与讨论 2.1 FKC与KC的性能比较由图 1(a)可知, 随着初始Cd2+浓度增大, BC、KC和FKC对Cd2+的吸附量逐渐增大.在初始Cd2+浓度为300 mg·L-1的条件下, FKC的吸附量为23.05 mg·g-1, 是BC的1.66倍, 是KC的1.27倍.可见经碱和磁复合改性后其对Cd2+吸附性能较单一碱改性进一步提高.此外, 由图 1(b)可知, 与KC相比, FKC可以被外部磁场所吸引, 说明磁改性有利于进行分离与回收.综合比较, FKC不仅Cd2+吸附能力强而且有回收利用能力, 所以本文主要分析FKC性质及其对Cd2+的吸附特性.

|
图 1 FKC和KC的性能比较 Fig. 1 Comparison of performance of KFC and KC |
对BC和FKC进行SEM-EDS分析可知(图 2), BC结构紧致, 表面附着杂质且几乎看不见孔隙.碱和磁复合改性处理后, 生物炭结构形貌发生显著变化, 结构疏松, 孔隙结构明显增多, 呈蜂窝型, 有利于Cd2+扩散进入生物炭内部而被吸附; 表面杂质减少, 可能是碱对灰分物质的腐蚀作用, 导致其比表面积增大, 使更丰富和活跃的吸附位点暴露出来[20].一些白色颗粒物质负载于FKC表面, 可能是FeOx[15].

|
图 2 BC和FKC的扫描电镜图 Fig. 2 SEM of BC and FKC |
由表 1可知, 与BC相比, FKC中C和O含量有所提高, 质量分数分别提高了13.38%和5.46%, 而H含量降低了67.28%. FKC的O/C较BC下降了7.32%, 说明碱和磁复合改性能降低生物炭的极性, 有利于保持其在溶液中稳定的形态[21]. FKC的H/C比值较BC下降了75.00%, 表明FKC具有更强的芳香性[22]. FKC的Na、K、Ca和Si所占质量分数均降低, 较BC分别降低了44.00%、15.38%、60.00%和93.61%, 说明碱和磁复合改性后灰分降低. FKC的Fe含量增加, 表明碱和磁复合改性后, Fe成功负载于BC上, 这与图 1的结果相一致.
|
|
表 1 EDS分析元素组成 Table 1 EDS analysis of element composition |
2.2.2 比表面积和孔径
大量研究表明生物炭吸附能力与其比表面积密切相关.从表 2可知, FKC的比表面积是BC的20.11倍, 说明碱和磁复合改性使BC的结构变化很大, 比表面积显著增加.
|
|
表 2 BC和FKC的微观结构性质 Table 2 Microstructural properties of BC and FKC |
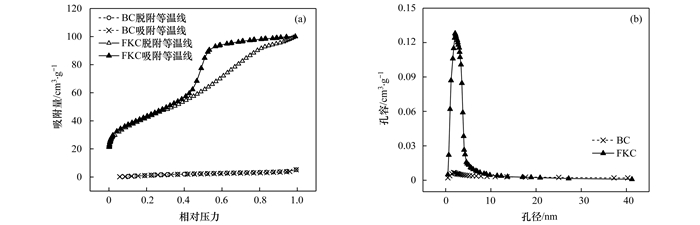
如图 3(a)所示, BC和FKC对N2的吸附曲线均符合IUPAC中第Ⅳ类相, 说明二者均为中孔毛细凝聚型吸附材料.BC为H3滞后环, 而FKC为H2滞后环, 说明BC的孔隙是由片状粒子堆积形成的, 而FKC的孔隙是由多孔吸附质或均匀粒子堆积造成的.
|
图 3 BC和FKC的N2吸附脱附曲线和孔径分布曲线 Fig. 3 N2 adsorption and desorption curves and pore size distribution curves of BC and FKC |
BC和FKC的孔容随孔径的变化如图 3(b)所示, BC的孔峰变化不明显, 说明BC的孔容很小, BC的总孔容为0.006 7 cm3·g-1, 表面孔径分布在2~5 nm范围内稍多, 平均孔径为3.14 nm.改性后, FKC孔径分布特征发生改变, 在2~10 nm区间集聚, 平均孔径为7.12 nm.而FKC在2~5 nm范围内出现明显的孔峰, 其总孔容为0.13 cm3·g-1.由表 2可知, FKC总孔容较BC增大了19.40倍, 平均孔径增大了2.27倍, 说明碱和磁复合改性具有扩孔作用, 从而扩大了生物炭的比表面积并且增加了中孔数量.
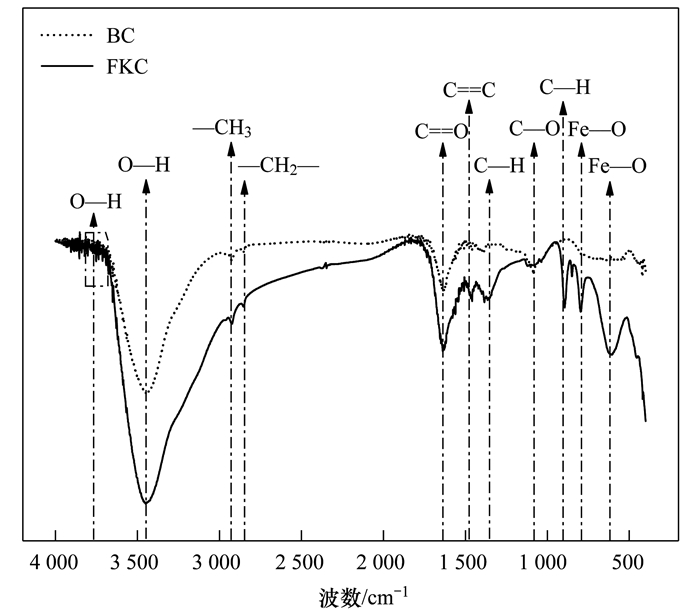
2.2.3 表面官能团种类为了分析碱和磁复合改性对官能团的影响, 对FKC和BC进行了FT-IR分析.由图 4可知, 3 750~3 300 cm-1范围内, BC和FKC均有明显宽阔而强烈的吸收峰, 为羧基、羟基和羰基上自由或缔合O—H的伸缩振动, 有利于发生离子交换吸附[23]; 3 750~3 600 cm-1范围内, FKC吸收峰数量明显多于BC, 且在3 450 cm-1附近, FKC含氧官能团吸收峰峰强增加, 波峰变宽, 说明碱和磁复合改性后含氧官能团大量增加, 提高了阳离子交换容量, 从而提高对Cd2+的吸附能力. 1 700~1 600 cm-1之间为C=O的伸缩振动, 表明BC和FKC表面含有羧基、酯基或醛基等官能团, FKC的吸收峰较BC更强更尖锐, 表明碱和磁复合改性后C=O增多, 易与Cd2+发生络合作用[24]. 1 500~1 400 cm-1范围内, FKC有一个小而尖锐的吸收峰, 为芳环的C=C伸缩振动峰, 表明FKC具有较高的芳香性和稳定性[25]. 1 380 cm-1和900 cm-1左右, FKC出现芳香C—H间的变形振动形成的吸收峰, 说明FKC芳香化程度高[20], 这与H/C比的结果相一致.有研究发现芳香结构可作为电子供体与溶液中Cd2+产生阳离子-π的配键作用, 有利于吸附Cd2+[4]. 1 200 cm-1左右为醚类(如香/烷基醚键、苯酚和内酯)的C—O伸缩振动峰, FKC峰强较BC略微减小, 说明极性含氧官能团少量减少, 使FKC表面极性减小, 提高了其在水溶液中的稳定性[26], 这与改性后O/C比值略微减少, 极性减小的结果相一致. FKC在796 cm-1和600 cm-1左右出现了新的Fe—O特征峰, 表明Fe3O4成功负载于FKC上[27].有研究表明Cd2+与Fe氧化物有较高的亲和力, Fe氧化物的存在增强了络合吸附作用[28].
|
图 4 BC和FKC的红外图谱 Fig. 4 FT-IR spectra of BC and FKC |
由图 5可知, BC和FKC的衍射图谱峰变化大致相同, 与Bashir等[10]的研究结果相一致, 在扫描角度(2θ)约23°时出现一个小山丘状的肩峰, 此类为有序碳层结构的特征峰, 表明BC和FKC均有经典的芳香化碳结构[29], FKC衍射峰较BC变得更低、更宽, 表明其纤维素结晶度降低, 说明FKC中有机碳可能是无定形碳, 无定形碳的存在会增加比表面积, 从而提高对重金属的吸附能力[30].在35.5°时FKC中产生宽而尖锐的特征衍射峰, 表明FKC中存在Fe3O4的晶体结构[31], 该结果与FT-IR表征结果一致.

|
图 5 BC和FKC的X射线衍射图谱 Fig. 5 XRD patterns of BC and FKC |
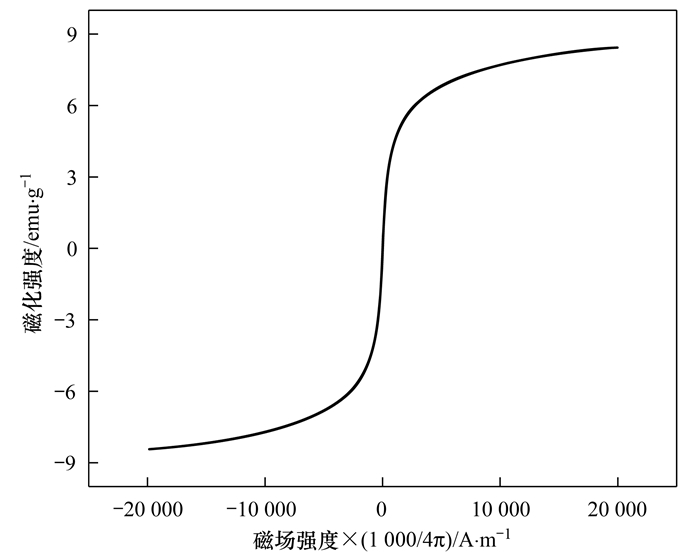
利用VSM分析FKC的磁学性能, 如图 6所示, FKC的饱和磁化强度(Ms)为8.43 emu·g-1, 磁滞回线过原点且以原点成中心对称, 剩余磁感应强度(Br)和矫顽力(Hs)为0, 说明FKC具有超顺磁性, 可进行回收利用.
|
图 6 FKC的磁滞回线 Fig. 6 Magnetization curves of FKC |
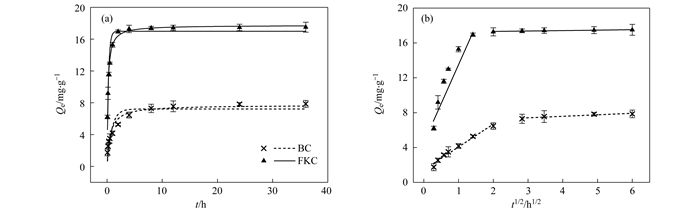
由图 7(a)可知, BC和FKC对溶液中Cd2+的吸附随时间推进均呈先快后慢的变化趋势, 均可分为快反应和慢反应两个阶段. 0~4 h内为BC的快反应阶段, 在第4 h时, BC对Cd2+吸附量为6.46 mg·g-1, 达到其最终吸附量的82.24%, 4 h后为慢反应阶段, 吸附速率减小, 吸附逐渐趋于平衡.对于FKC, 0~2 h为其快反应阶段, 在第2 h时, FKC对Cd2+吸附量为16.94 mg·g-1, 达到其最终吸附量的96.83%, 2 h后为慢反应阶段.可见, FKC吸附速率和吸附量均高于BC.
|
图 7 BC和FKC对Cd2+吸附的动力学方程拟合 Fig. 7 Kinetic equation fitting for Cd2+ adsorption by BC and FKC |
通过对FKC和BC的动力学数据进行拟合以深入分析二者对Cd2+吸附过程.由表 3可知, 准一级动力学方程和准二级动力学方程均能较好地拟合FKC和BC对Cd2+吸附过程, 但准二级动力学方程的R2更高, 且拟合出的吸附量Qe(BC为7.71 mg·g-1, FKC为17.74 mg·g-1)与实验数据(BC为7.86 mg·g-1, FKC为17.50 mg·g-1)相差更小, 因此可用准二级动力学方程描述BC和FKC对Cd2+的吸附过程, 表明该过程受化学吸附控制, Cd2+与FKC、BC间共享或交换电子是主要影响因素[32], 这与Sun等[9]的研究结果相一致. FKC的准二级动力学方程k2大于BC, 进一步说明碱和磁复合改性提高了吸附速率.
|
|
表 3 BC和FKC对Cd2+的吸附动力学拟合参数 Table 3 Kinetic fitting parameters for Cd2+ adsorption by BC and FKC |
通过颗粒内扩散方程可分析BC和FKC对Cd2+吸附过程中的控速步骤和吸附机制, 拟合结果见图 7(b). BC和FKC对Cd2+吸附过程均分两个阶段, 第一阶段为快反应阶段, 斜率大, 吸附量增加快, 这与图 7(a)的结果相一致, 主要是Cd2+通过液膜扩散到BC和FKC表面. BC和FKC的kd1值均大于kd2的值, c1值均小于c2值(表 3), 其中FKC的kd1和c1值均大于BC, 表明Cd2+在溶液-生物炭两相最初的浓度差引起的传质驱动力和充足的吸附位点是BC和FKC吸附Cd2+的初期速率较大的重要原因, 这与表征结果相一致.随着吸附时间的延长, 第二阶段为慢反应阶段, 吸附速率减小, 即吸附平衡阶段, 这是由于BC和FKC表面的吸附位点基本饱和, Cd2+浓度差减小, 颗粒内扩散作用减弱, 吸附趋于饱和[33].
BC和FKC颗粒内扩散方程拟合直线的延长线均不过原点, 说明吸附速率除受颗粒内扩散影响外, 还受离子交换和沉淀等影响[34], 这与表 3中准二级动力学方程能更好地描述Cd2+在BC和FKC上的吸附动力学这一结论相一致.
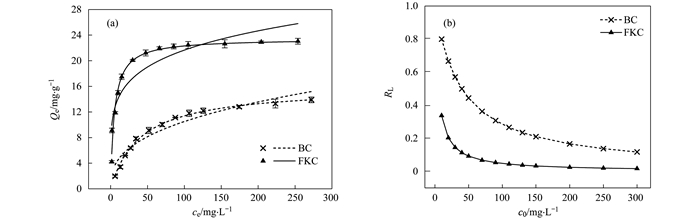
2.4 FKC和BC对Cd2+的等温吸附由图 8(a)可知, 随着溶液中Cd2+平衡浓度的增大, FKC和BC对Cd2+的吸附量逐渐增大. Cd2+浓度在0~50 mg·L-1时, BC和FKC对Cd2+的吸附量均迅速增大, 由0分别迅速增加到7.84 mg·g-1和17.49 mg·g-1, 随着Cd2+浓度的增加, BC和FKC对Cd2+的吸附量增加较小, 趋于平衡, 在110~300 mg·L-1 Cd2+时, BC和FKC对Cd2+吸附量分别仅从11.13 mg·L-1和21.93 mg·L-1增加到13.90 mg·L-1和23.05 mg·L-1.
|
图 8 BC和FKC对Cd2+的吸附等温线以及分离因子与初始浓度关系曲线 Fig. 8 Adsorption isotherms of Cd2+ by BC and FKC and the relationship between the separation factor and initial concentration |
由表 4可知, Langmuir方程和Freundlich方程均能较好地拟合BC和FKC的吸附数据, 两个模型相比, Langmuir模型的R2更高, 特别是FKC, 说明Langmuir模型能更好地描述吸附过程, 表明BC和FKC对Cd2+的吸附均为单分子层吸附. Langmuir模型参数KL表示吸附剂与吸附质之间的亲和力, 数值越大, 吸附亲和力越大, 越有利于吸附[31]. FKC的KL值大于BC的KL值(表 4), 说明FKC对Cd2+有更大的吸附亲和力. BC和FKC的理论最大平衡吸附量Qm分别为15.94 mg·g-1和23.44 mg·g-1, FKC比BC高47.05%, 说明碱和磁复合改性后吸附量得到提高, 但吸附量提高的幅度低于比表面积增加的幅度(表 2), 进一步说明该吸附主要是由化学吸附控制[9, 21, 35].
|
|
表 4 BC和FKC对Cd2+的吸附等温线拟合参数 Table 4 Isotherm fitting parameters for Cd2+ adsorption of BC and FKC |
Langmuir方程可以定义成为一个无量纲的分离因子RL.由图 8(b)可知, BC的RL值在0.117 3~0.799 6之间, FKC的RL值在0.016 7~0.337 3之间, 二者的RL均为0 < RL < 1, 表明BC和FKC均具有有效的吸附能力[26], 同时FKC的RL值均低于BC, 说明FKC对Cd2有更强的亲和力[21], 与等温吸附特征[图 8(a)]相一致.另外, 由图 8(b)可知, 均随初始浓度的增加BC和FKC的RL值均逐渐降低, 说明较高的初始浓度有利于吸附.
Freunflich模型参数1/n和KF可以反映Cd2+浓度对吸附量影响的大小.由表 4可知, 与BC相比, FKC的1/n值减小, KF值增大, 表明小麦秸秆生物炭经过碱磁复合改性后对Cd2+有更高的分配系数, 即吸附性能提高. BC和FKC的1/n均 < 1表明该吸附行为是一种非线性等温吸附, 说明BC和FKC吸附Cd2+存在多种机制[29].
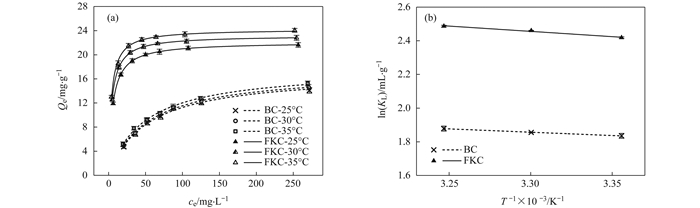
2.5 温度对FKC和BC吸附Cd2+的影响在25、30和35℃下, BC和FKC对Cd2+的Langmuir吸附等温线如图 9(a)所示, BC和FKC对Cd2+的吸附量随温度的上升而增大, 表明二者对Cd2+的吸附均是一个吸热过程.
|
图 9 BC和FKC在不同温度下的Langmuir方程曲线图以及lnKL和1/T的线性关系 Fig. 9 Langmuir equation graph of BC and FKC at different temperatures and linear relationships between lnKL and 1/T |
吉布斯自由能变化(ΔGθ)的绝对值可反映吸附过程的推动力, 由表 5可以看出, BC和FKC的ΔGθ均为负值, 表明其对Cd2+的吸附均是自发的过程, 且随着温度的提高, ΔGθ的绝对值均增加, 说明提高温度能增强吸附的推动力.在同一温度下, 与BC相比, FKC的ΔGθ的绝对值增加, 说明碱磁复合改性能提高Cd2+吸附推动力.熵变(ΔSθ)描述吸附过程中分子在固液界面排列的混乱程度. FKC的ΔSθ值高于BC(表 5), 说明FKC固液界面的自由度增大, 体系无序性增加[24].焓变(ΔHθ)的绝对值大小反映Cd2+与生物炭之间的作用力.从表 5可知, BC和FKC的ΔHθ均为正值, 说明二者对Cd2+的吸附过程均为吸热反应, 表明提高温度有利于吸附, 这与图 9(a)中的结果一致.与BC相比, FKC的ΔHθ绝对值变大, 说明碱和磁复合改性提高了吸附作用力.
|
|
表 5 BC和FKC对Cd2+吸附的热力学参数 Table 5 Thermodynamic parameters of adsorption of Cd2+ by BC and FKC |
BC和FKC的ΔGθ值均处于-20~0 kJ·mol-1之间, 且其ΔHθ的绝对值也均处于0~30 kJ·mol-1间, 说明其吸附过程以物理吸附为主[23]. BC和FKC的ΔHθ值分别为3.26 kJ·mol-1和5.27 kJ·mol-1, 说明FKC对Cd2+的吸附过程中不仅有氢键力和偶极间作用力, 而且同时存在范德华力和疏水键力[36].
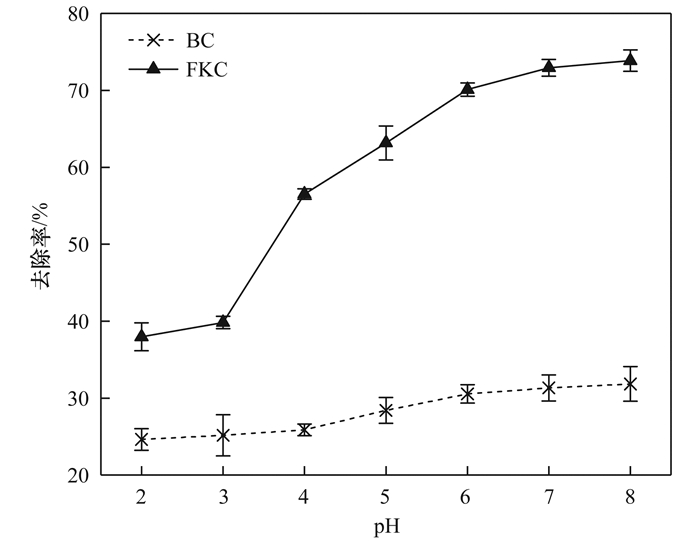
2.6 溶液pH值对FKC和BC吸附Cd2+的影响pH会影响重金属形态, 也会改变生物炭的表面电荷密度[24]. pH过低不利于吸附的进行, 而pH值过高会导致Cd2+沉淀[25], 因此本实验研究了在2~8范围内pH对BC和FKC吸附Cd2+的影响.从图 10中可知, BC和FKC对Cd2+的去除率均随着pH值升高而增大, 说明较高pH能增强生物炭的吸附能力.在溶液初始pH为2~3范围内, 去除率缓慢上升, pH达到3~6范围内, 去除率急剧增加, BC和FKC的去除率分别从25.16%和39.83%增加到30.55%和70.10%, 在pH6~8范围内, 去除率增速减缓趋于稳定.在低pH条件下去除率低, 可能是由于一方面溶液中H+浓度高, 溶液中大量存在的H+与Cd2+存在竞争, 导致生物炭没有足够的吸附点位来吸附Cd2+; 另一方面, 由于pH溶液 < pHpzc(BC和FKC的pHpzc分别为5.6和7.2), 酸性含氧官能团带正电, 与Cd2+有排斥作用[26].随着pH的升高, 去除率增大, 这是由于溶液中H+浓度降低, H+与Cd2+的竞争减弱, Cd2+易与表面带负电荷的结合位点相结合[25].
|
图 10 溶液初始pH对BC和FKC吸附Cd2+的影响 Fig. 10 Effect of initial pH of solution on adsorption of Cd2+ by BC and FKC |
在任一pH值条件下, FKC对Cd2+的去除率均高于BC(图 10), FKC对Cd2+的最大去除率比BC高出42.01%, 说明碱磁复合改性能提高生物炭对pH值的适应性[21].
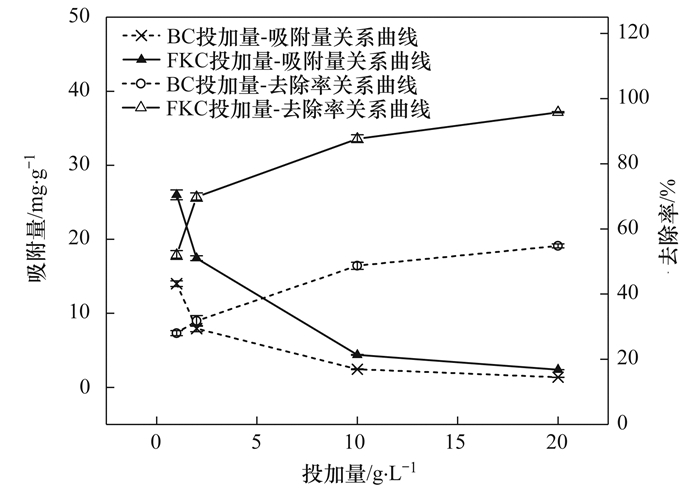
2.7 FKC和BC投加量对Cd2+吸附的影响投加量是影响吸附进程的重要因素.由图 11可知, 随投加量的增加, BC和FKC对Cd2+的去除率均逐渐增大, 当投加量从1 g·L-1提高到20 g·L-1, BC和FKC的去除率分别从28.0%和52.0%增加到54.8%和95.8%, 这是因为吸附位点数量和比表面积与投加量正相关[37].但是单位吸附量反而减少, 分别从14.00 mg·g-1和26.00 mg·g-1降低到1.37 mg·g-1和2.40 mg·g-1.这可能是由于大量的吸附位点争夺有限的Cd2+, 导致吸附量的减小[38]; 此外, 投加量过多会产生团聚现象, 吸附位点重叠, Cd2+扩散受阻[38].
|
图 11 投加量对BC和FKC吸附Cd2+的影响 Fig. 11 Effect of dosage on adsorption of Cd2+ by BC and FKC |
与BC相比, 在投加量较低时, FKC去除率和吸附量均明显大于BC(图 11), 说明碱和磁复合改性后以较低的用量可取得较好的吸附效果.总体来看, 10 g·L-1的投加量较好.
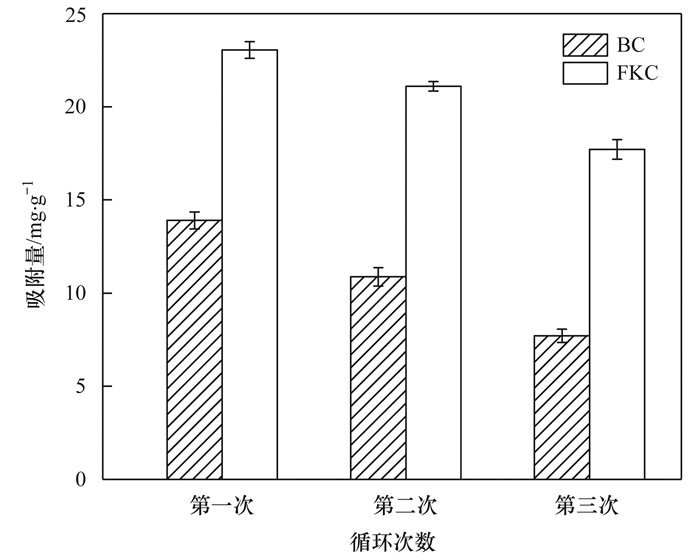
2.8 FKC和BC吸附-解吸解吸再生能力是体现生物炭性能的重要指标.由图 12可知, 3次“吸附-解吸-再吸附”后BC和FKC对Cd2+的吸附量分别从13.90 mg·g-1和23.05 mg·g-1降到7.71 mg·g-1和17.71 mg·g-1, 说明在解吸过程中其吸附位点不可完全逆转[13], FKC对Cd2+的吸附量均明显高于BC, 且经3次循环后FKC对Cd2+的吸附量仍较高, 表明碱磁复合改性能提高小麦秸杆生物炭对Cd2+的固着能力, 可重复利用[15, 39].
|
图 12 循环次数对BC和FKC吸附Cd2+的影响 Fig. 12 Regeneration cycles of BC and FKC for Cd2+ removal |
(1) FKC孔隙发达, 中孔数量增多, 比表面积增大, 芳香性提高, 极性减小, 有利于对水溶液中Cd2+的吸附和稳定. FKC表面具有大量O—H、C=O等含氧官能团和铁的氧化物, 有利于与Cd2+发生离子反应和络合作用.此外, FKC具有磁性, 能够回收利用.
(2) FKC对Cd2+的吸附更符合准二级动力学和Langmuir等温吸附模型, 表明该过程主要受化学吸附所控制, FKC的理论最大平衡吸附量为23.44 mg·g-1, 是BC的1.47倍. FKC对Cd2+的吸附是自发的吸热过程, 其吸附过程中不仅存在氢键力和偶极间作用力, 而且存在范德华力和疏水键力.热力学结果表明碱和磁复合改性有助于提高生物炭吸附Cd2+的推动力.
(3) 较高pH能提高FKC对Cd2+的吸附能力, 且KFC对pH值有较强的适应性. FKC的投加量以10 g·L-1较好, 对Cd2+的去除率可达到87.70%.经过3次“吸附-解吸-吸附”循环后, FKC对Cd2+的吸附量仍达到17.71 mg·g-1, 说明FKC可重复利用.
| [1] |
马锋锋, 赵保卫, 刁静茹. 小麦秸秆生物炭对水中Cd2+的吸附特性研究[J]. 中国环境科学, 2017, 37(2): 551-559. Ma F F, Zhao B W, Diao J R. Adsorptive characteristics of cadmium onto biochar produced from pyrolysis of wheat straw in aqueous solution[J]. China Environmental Science, 2017, 37(2): 551-559. |
| [2] | Atar N, Olgun A, Wang S B. Adsorption of cadmium(Ⅱ) and zinc(Ⅱ) on boron enrichment process waste in aqueous solutions:batch and fixed-bed system studies[J]. Chemical Engineering Journal, 2012, 192(2): 1-7. DOI:10.1016/j.cej.2012.03.067 |
| [3] | Zeng G M, Liu Y Y, Tang L, et al. Enhancement of Cd(Ⅱ) adsorption by polyacrylic acid modified magnetic mesoporous carbon[J]. Chemical Engineering Journal, 2015, 259: 153-160. DOI:10.1016/j.cej.2014.07.115 |
| [4] | Chen T, Zhou Z Y, Han R, et al. Adsorption of cadmium by biochar derived from municipal sewage sludge:Impact factors and adsorption mechanism[J]. Chemosphere, 2015, 134: 286-293. DOI:10.1016/j.chemosphere.2015.04.052 |
| [5] | Ahmad M, Rajapaksha A U, Lim J E, et al. Biochar as a sorbent for contaminant management in soil and water:a review[J]. Chemosphere, 2014, 99: 19-33. DOI:10.1016/j.chemosphere.2013.10.071 |
| [6] | Wang Y, Liu R H. Comparison of characteristics of twenty-one types of biochar and their ability to remove multi-heavy metals and methylene blue in solution[J]. Fuel Processing Technology, 2017, 160: 55-63. DOI:10.1016/j.fuproc.2017.02.019 |
| [7] |
刘莹莹, 秦海芝, 李恋卿, 等. 不同作物原料热裂解生物质炭对溶液中Cd2+和Pb2+的吸附特性[J]. 生态环境学报, 2012, 21(1): 146-152. Liu Y Y, Qin H Z, Li L Q, et al. Adsorption of Cd2+ and Pb2+ in aqueous solution by biochars produced from the pyrolysis of different crop feedstock[J]. Ecology and Environmental Sciences, 2012, 21(1): 146-152. DOI:10.3969/j.issn.1674-5906.2012.01.026 |
| [8] | Sizmur T, Fresno T, Akgül G, et al. Biochar modification to enhance sorption of inorganics from water[J]. Bioresource Technology, 2017, 246: 34-37. DOI:10.1016/j.biortech.2017.07.082 |
| [9] | Sun K J, Tang J C, Gong Y Y, et al. Characterization of potassium hydroxide (KOH) modified hydrochars from different feedstocks for enhanced removal of heavy metals from water[J]. Environmental Science and Pollution Research, 2015, 22(21): 16640-16651. DOI:10.1007/s11356-015-4849-0 |
| [10] | Bashir S, Zhu J, Fu Q L, et al. Comparing the adsorption mechanism of Cd by rice straw pristine and KOH-modified biochar[J]. Environmental Science and Pollution Research, 2018, 25(12): 11875-11883. DOI:10.1007/s11356-018-1292-z |
| [11] | Thines K R, Abdullah E C, Mubarak N M, et al. Synthesis of magnetic biochar from agricultural waste biomass to enhancing route for waste water and polymer application:a review[J]. Renewable and Sustainable Energy Reviews, 2017, 67: 257-276. DOI:10.1016/j.rser.2016.09.057 |
| [12] |
赵华轩, 郎印海. 磁性生物炭对水中CIP和OFL的吸附行为和机制[J]. 环境科学, 2018, 39(8): 3729-3735. Zhao H X, Lang Y H. Behaviors and mechanisms of CIP and OFL adsorption by magnetic biochar[J]. Environmental Science, 2018, 39(8): 3729-3735. |
| [13] |
朱司航, 赵晶晶, 尹英杰, 等. 针铁矿改性生物炭对砷吸附性能[J]. 环境科学, 2019, 40(6): 2773-2782. Zhu S H, Zhao J J, Yin Y J, et al. Application of goethite modified biochar for arsenic removal from aqueous solution[J]. Environmental Science, 2019, 40(6): 2773-2782. |
| [14] | Tan Z X, Wang Y H, Kasiulien De·A, et al. Cadmium removal potential by rice straw-derived magnetic biochar[J]. Clean Technologies and Environmental Policy, 2017, 19(3): 761-774. DOI:10.1007/s10098-016-1264-2 |
| [15] |
杜文琪, 曹玮, 周航, 等. 磁性生物炭对重金属污染废水处理条件优化及机理[J]. 环境科学学报, 2018, 38(2): 492-500. Du W Q, Cao W, Zhou H, et al. Optimization and the mechanismin treatment of heavy metals wastewater with magnetic biochar[J]. Acta Scientiae Circumstantiae, 2018, 38(2): 492-500. |
| [16] | Li B, Yang L, Wang C Q, et al. Adsorption of Cd(Ⅱ) from aqueous solutions by rape straw biochar derived from different modification processes[J]. Chemosphere, 2017, 175: 332-340. DOI:10.1016/j.chemosphere.2017.02.061 |
| [17] | Mohanty P, Nanda S, Pant K K, et al. Evaluation of the physiochemical development of biochars obtained from pyrolysis of wheat straw, timothy grass and pinewood:effects of heating rate[J]. Journal of Analytical and Applied Pyrolysis, 2013, 104: 485-493. DOI:10.1016/j.jaap.2013.05.022 |
| [18] | Li Y C, Shao J A, Wang X H, et al. Characterization of modified biochars derived from bamboo pyrolysis and their utilization for target component (furfural) adsorption[J]. Energy & Fuels, 2014, 28(8): 5119-5127. |
| [19] | Wu Y, Zhang P Y, Zhang H B, et al. Possibility of sludge conditioning and dewatering with rice husk biochar modified by ferric chloride[J]. Bioresource Technology, 2016, 205: 258-263. DOI:10.1016/j.biortech.2016.01.020 |
| [20] | Lin L N, Qiu W W, Wang D, et al. Arsenic removal in aqueous solution by a novel Fe-Mn modified biochar composite:characterization and mechanism[J]. Ecotoxicology and Environmental Safety, 2017, 144: 514-521. DOI:10.1016/j.ecoenv.2017.06.063 |
| [21] |
平巍, 吴彦, 杨春霞, 等. 香蕉皮改性材料对废水中二价Cd离子的吸附特性与机理[J]. 农业工程学报, 2019, 35(8): 269-279. Ping W, Wu Y, Yang C X, et al. Properties and mechanism of Cd(Ⅱ) adsorption from waste water by modified banana peel[J]. Transactions of the Chinese Society of Agricultural Engineering, 2019, 35(8): 269-279. |
| [22] | Singh B, Singh B P, Cowie A L. Characterisation and evaluation of biochars for their application as a soil amendment[J]. Australian Journal of Soil Research, 2010, 48(7): 516-525. DOI:10.1071/SR10058 |
| [23] | Zhang S Q, Yang X, Liu L, et al. Adsorption behavior of selective recognition functionalized biochar to Cd(Ⅱ) in wastewater[J]. Materials, 2018, 11(2): 299. DOI:10.3390/ma11020299 |
| [24] | Wu Q, Chen J, Clark M, et al. Adsorption of copper to different biogenic oyster shell structures[J]. Applied Surface Science, 2014, 311: 264-272. DOI:10.1016/j.apsusc.2014.05.054 |
| [25] | Nassar N N. Rapid removal and recovery of Pb(Ⅱ) from wastewater by magnetic nanoadsorbents[J]. Journal of Hazardous Materials, 2010, 184(1-3): 538-546. DOI:10.1016/j.jhazmat.2010.08.069 |
| [26] | Awwad A M, Salem N M. Kinetics and thermodynamics of Cd(Ⅱ) biosorption onto loquat (Eriobotrya japonica) leaves[J]. Journal of Saudi Chemical Society, 2014, 18(5): 486-493. DOI:10.1016/j.jscs.2011.10.007 |
| [27] | Bakshi S, Banik C, Rathke S J, et al. Arsenic sorption on zero-valent iron-biochar complexes[J]. Water Research, 2018, 137: 153-163. DOI:10.1016/j.watres.2018.03.021 |
| [28] | Noraini M N, Abdullah E C, Othman R, et al. Single-route synthesis of magnetic biochar from sugarcane bagasse by microwave-assisted pyrolysis[J]. Materials Letters, 2016, 184: 315-319. DOI:10.1016/j.matlet.2016.08.064 |
| [29] | Li N, Yang S G, Chen J, et al. Electro-adsorption of tetracycline from aqueous solution by carbonized pomelo peel and composite with aniline[J]. Applied Surface Science, 2016, 386: 460-466. DOI:10.1016/j.apsusc.2016.05.173 |
| [30] | Keiluweit M, Nico P S, Johnson M G, et al. Dynamic molecular structure of plant biomass-derived black carbon (biochar)[J]. Environmental Science & Technology, 2010, 44(4): 1247-1253. |
| [31] | Trakal L, Veselská V, Šafa Dřík I, et al. Lead and cadmium sorption mechanisms on magnetically modified biochars[J]. Bioresource Technology, 2016, 203: 318-324. DOI:10.1016/j.biortech.2015.12.056 |
| [32] | Ali R M, Hamad H A, Hussein M M, et al. Potential of using green adsorbent of heavy metal removal from aqueous solutions:adsorption kinetics, isotherm, thermodynamic, mechanism and economic analysis[J]. Ecological Engineering, 2016, 91: 317-332. DOI:10.1016/j.ecoleng.2016.03.015 |
| [33] | Belayachi A, Bestani B, Bendraoua A, et al. The influence of surface functionalization of activated carbon on dyes and metal ion removal from aqueous media[J]. Desalination and Water Treatment, 2016, 57(37): 17557-17569. DOI:10.1080/19443994.2015.1086701 |
| [34] | Kołodyńska D, Wnętrzak R, Leahy J J, et al. Kinetic and adsorptive characterization of biochar in metal ions removal[J]. Chemical Engineering Journal, 2012, 197: 295-305. DOI:10.1016/j.cej.2012.05.025 |
| [35] | Peng H B, Gao P, Chu G, et al. Enhanced adsorption of Cu(Ⅱ) and Cd(Ⅱ) by phosphoric acid-modified biochars[J]. Environmental Pollution, 2017, 229: 846-853. DOI:10.1016/j.envpol.2017.07.004 |
| [36] | Von Oepen B, Kördel W, Klein W. Sorption of nonpolar and polar compounds to soils:processes, measurements and experience with the applicability of the modified OECD-Guideline[J]. Chemosphere, 1991, 22: 285-304. DOI:10.1016/0045-6535(91)90318-8 |
| [37] | Nair V, Panigrahy A, Vinu R. Development of novel chitosan-lignin composites for adsorption of dyes and metal ions from wastewater[J]. Chemical Engineering Journal, 2014, 254: 491-502. DOI:10.1016/j.cej.2014.05.045 |
| [38] | Rahmani A, Mousavi H Z, Fazli M. Effect of nanostructure alumina on adsorption of heavy metals[J]. Desalination, 2010, 253(1-3): 94-100. DOI:10.1016/j.desal.2009.11.027 |
| [39] |
胡学玉, 陈窈君, 张沙沙, 等. 磁性玉米秸秆生物炭对水体中Cd的去除作用及回收利用[J]. 农业工程学报, 2018, 34(19): 208-218. Hu X Y, Chen Y J, Zhang S S, et al. Cd removal from aqueous solution using magnetic biochar derived from maize straw and its recycle[J]. Transactions of the Chinese Society of Agricultural Engineering, 2018, 34(19): 208-218. DOI:10.11975/j.issn.1002-6819.2018.19.027 |
 2020, Vol. 41
2020, Vol. 41