2. 西安建筑科技大学西北水资源与环境生态教育部重点实验室, 西安 710055;
3. 西安水务集团黑河金盆水库管理公司, 西安 710401
2. Key Laboratory of Northwest Water Resource, Environment and Ecology, Ministry of Education, Xi'an University of Architecture and Technology, Xi'an 710055, China;
3. Xi'an Water Group Heihe Jinpen Reservoir Management Company, Xi'an 710401, China
随着地下水资源逐渐匮乏及其过度开采带来的地质安全、地下水质量恶化等问题不断加剧, 湖泊和水库逐渐成为城市的主要供水水源[1].然而, 大多数水库水深较大, 水体分层现象明显, 表层水体溶解氧向下传质强烈受阻[2].对于富营养化程度较高的湖库, 底部水体呈季节性厌氧, 继而引发严重的周期性沉积物内源污染[3].大量研究证明, 微生物在厌氧条件下可利用沉积物中高价态的金属作为电子受体对有机物进行厌氧分解[4], 导致铁、锰等还原性污染物大量向上覆水体释放[5~7], 严重污染水库水质.因此, 如何控制分层型湖库底部水体周期性厌氧是在源头削减污染负荷、有效抑制或消除内源污染的关键[1].
近年来, 人工充氧技术在解决水源水库水体周期性厌氧、底部水体还原性污染物积聚、沉积物溶解态金属污染物释放等问题上得到了广泛应用[8].Gantzer等[9]在Carvins Cove水库利用同温层曝气技术去除还原性锰的研究表明:通过增加底部水体溶解氧浓度, 可有效促进微生物对还原态锰的生物氧化过程, 锰污染物以颗粒形式沉降在表层沉积物, 不断在沉积物-水界面积聚.Munger等[10]在Falling Creek水库利用同温层曝气技术去除水体铁锰的研究则表明, 由于铁锰离子氧化还原电位不同, 充氧过程对水体溶解态铁污染物控制效果较好, 而对于溶解态锰污染的控制效果较差.周子振等[11]利用扬水曝气技术改善黑河金盆水库水质, 结果表明通过人工强制混合充氧过程可有效削减水体还原性铁锰浓度, 其中对溶解态铁的削减率达78.6%.丛海兵等[12]的研究认为, 利用底部充氧、人工强制混合等技术维持分层水体底部溶解氧高于2 mg·L-1以上时, 可有效抑制底泥中污染物的释放.上述研究均表明人工充氧技术可有效去除水体还原性污染物, 然而对于充氧过程中污染物在沉积物-水界面的动态循环过程以及不同充氧强度对沉积物内源污染抑制效果的研究却鲜见报道.
本文以西安金盆水库为研究对象, 对比分析扬水曝气系统运行过程中不同溶解氧水平下沉积物间隙水及上覆水中铁锰浓度的分布规律, 并利用Fick第一定律计算金盆水库内源铁锰扩散通量, 通过探究在不同溶解氧水平下沉积物-水界面铁锰循环过程, 以期为金盆水库铁锰污染防治提供参考依据.
1 材料与方法 1.1 研究区域概况黑河金盆水库位于陕西省西安市周至县境内(34°02′~34°03′N, 108°11′~108°12′E), 是西安市最主要的饮用水源地[13].金盆水库于2002年建成供水, 总库容2.0亿m3, 平均水深70~100 m.金盆水库在夏季(7~8月)会形成稳定的热分层, 分层期库底溶解氧浓度迅速降低, 沉积物释放大量还原态铁锰进入上覆水体[14].
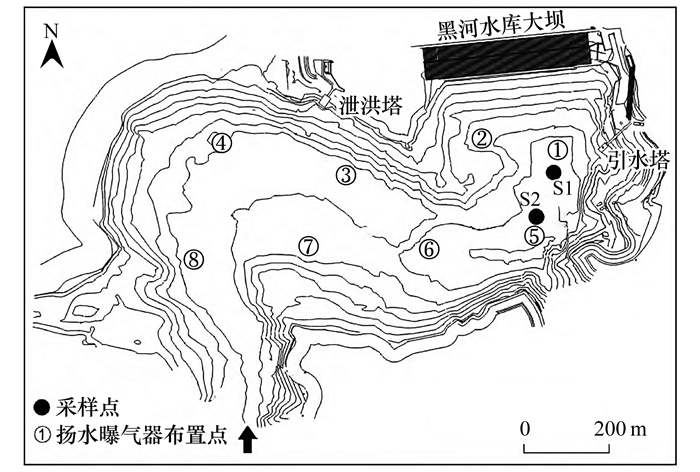
为解决金盆水库分层期底部溶解氧耗竭和铁锰释放的问题, 本研究采用扬水曝气技术对底部水体直接充氧, 同时促进上下层水体混合及溶解氧传递[15].金盆水库在主库区共设置8台扬水曝气器, 设计间距为250~300 m[16], 分布如图 1所示.
|
图 1 金盆水库主库区采样点及扬水曝气布置点示意 Fig. 1 Schematic diagram of sampling points and WLAs arrangement points in the main reservoir area of Jinpen Reservoir |
2018年扬水曝气系统自8月21日开启, 至11月4日关闭. 1号曝气器在此期间连续运行, 而5号曝气器作为参考在系统运行期间短暂关闭, 具体时间为:9月28日关闭, 10月8日重新开启.
1.2 采样点选取与采样频率选取主库区1号曝气器和5号曝气器附近分别设置S1和S2采样点(图 1).其中S1位于引水塔前, 可较好地代表水库供水水质, S2为主库区最深处, 底部水体充氧及人工强制混合效率较S1处略低.数据采集周期为2018年9月25日至12月10日, 采样频率为每周一次.
1.3 样品采集与处理(1) 上覆水的获取 利用柱状采泥器采集沉积物与上覆水样品, 采集过程中沉积物-水界面未受扰动.采集完成后现场进行上覆水样品的获取, 利用连接有洗净橡胶软管的注射器分别吸取沉积物以上20、10和1 cm的上覆水各10 mL, 立即使用0.45 μm针头式过滤器过滤至硝酸预酸化的10 mL离心管中.
(2) 间隙水的获取 将对应柱状沉积物样品密封后, 保持竖直状态尽快运回实验室, 按1 cm的间隔分割(沉积物表层按0.5 cm的间隔单独分割), 使用离心机在6 000 r·min-1下离心8 min获取对应间隙水, 经0.45 μm玻璃纤维滤膜过滤后加优级纯硝酸酸化至pH<2.
上覆水与间隙水样品保存于4℃冰箱中, 迅速完成溶解态铁锰的测定.
1.4 分析方法水温、溶解氧等常规理化指标采用美国HACH Hydro-Lab DS5型水质分析仪进行原位测定.上覆水及间隙水样品中溶解态铁锰浓度按火焰原子吸收分光光度法(GB 11911-89)进行测定.在本研究中, 将20、10和1 cm处的沉积物上覆水体铁锰浓度的平均值作为底部水体铁锰浓度.
1.5 扩散通量计算方法利用Fick第一定律计算沉积物-水界面(SWI)处的铁锰扩散通量[17], 公式为:
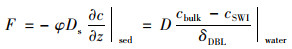
|
(1) |
式中, F为物质通过沉积物-水界面的扩散通量[mg·(m2·d)-1]; φ为沉积物孔隙度(%); Ds和D分别为沉积物和上覆水体中物质的实际扩散系数(cm2·s-1); ∂c/∂z为表层沉积物内(紧靠沉积物-水界面)的物质浓度梯度[mg·(L·m)-1]; cbulk为上覆水中物质浓度(mg·L-1); cSWI为沉积物-水界面处的物质浓度(mg·L-1); δDBL为扩散边界层(DBL)的厚度(m).
扩散通量既可以从水体一侧计算, 也可以从沉积物一侧计算, 若将沉积物水界面看作极薄的一层, 则两侧的计算结果应该是相等的[18].公式(1)中第二项为沉积物侧的计算公式, 第三项为水体一侧的计算公式.扩散边界层为沉积物上极薄的一层水膜, 容易受到水流扰动及地形粗糙度等因素的影响, 且其厚度δDBL一般小于1 mm[19].由于本研究使用的上覆水取样方法无法获得此分辨率的铁锰样品, 故通过沉积物一侧进行铁锰扩散通量的计算.其中φ采用各次取样中, 表层沉积物样品的平均孔隙度为0.89; z由间隙水浓度剖面中∂c/∂z斜率拐点确定; Ds通常根据理想流体中溶质的扩散系数D0与孔隙度φ来推导, 公式为[20]:

|
(2) |
D0会受水温影响, 可应用Stokes-Einstein方程进行修正[21]:
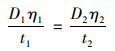
|
(3) |
式中, D1为参考温度t1(℃)与水黏性η1下的扩散系数, D2为实测水温t2与对应水黏性η2下的扩散系数.根据金盆水库9月末至12月初底部平均水温为11.55℃, 选用与其温度接近的18℃作为t1, 对应t1下理想流体中Fe2+和Mn2+的扩散系数D1参考文献[22]的结果.实测水温的对应水黏性可通过以下公式估算:
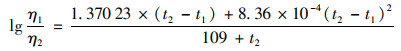
|
(4) |
将计算的实际水黏性系数代入公式(3), 从而对D0进行修正.
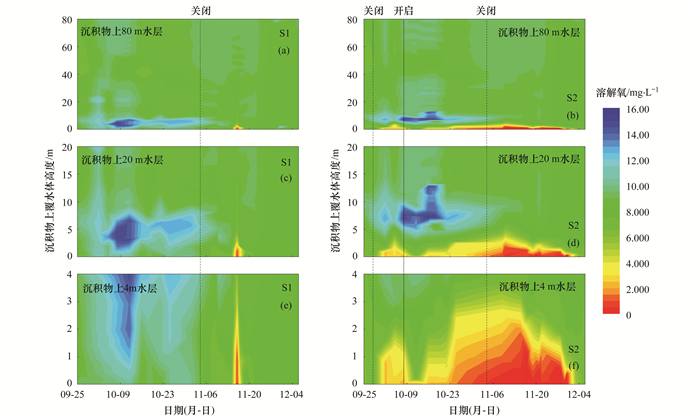
2 结果与讨论 2.1 金盆水库S1和S2水体理化性质的变化特征 2.1.1 水体溶解氧垂向分布特征图 2为金盆水库水体9月末至12月初S1和S2处溶解氧的变化特征.S1扬水曝气系统运行期间(9月25日至11月4日)全层溶解氧浓度较高, 变化范围为6.77~15.1 mg·L-1, 均值为9.06 mg·L-1[图 2(a)], 沉积物以上5 m水层受深层曝气作用影响出现明显富氧区[图 2(c)]; 11月4日系统运行结束后, S1处溶解氧浓度全层逐渐下降[图 2(a)], 其中底部水体溶解氧浓度下降较快, 11月16日降至0.26 mg·L-1[图 2(e)].S2全层水体溶解氧浓度垂向上呈“上高下低”分布[图 2(b)], 在5号曝气器短暂关闭期间(9月28日至10月8日), 水体溶解氧浓度自沉积物-水界面迅速下降, 最低降至2.29 mg·L-1, 10月8日5号曝气器开启后, 沉积物2 m以上水层溶解氧浓度较高, 底部0~2 m水层内溶解氧浓度依然较低, 平均值为3.13 mg·L-1[图 2(f)], 在11月4日系统运行结束后, S2底部于11月9日进入厌氧状态, 并持续至11月30日, 厌氧层厚度最高达1.97 m, 11月30日之后底部水体溶解氧浓度呈迅速增加趋势, 12月3日升至5.36 mg·L-1[图 2(f)].
|
图 2 金盆水库S1和S2水体溶解氧的垂向分布特征 Fig. 2 Vertical distribution characteristics of dissolved oxygen at the S1 and S2 sites of Jinpen Reservoir |
由于扬水曝气系统的充氧作用, S1在系统运行期全层水体维持好氧状态, 系统运行结束后, 受水体及沉积物耗氧的影响, S1底部在11月16日短暂进入缺氧状态. 10月初5号曝气器短暂关闭, 沉积物耗氧使得S2底部水体溶解氧浓度降低, 且由于S2地势较低, 地形因素影响了5号曝气器对S2区域底部水体的混合充氧效率[23], 故系统重新开启后底部溶解氧的补充也未达理想效果, 以致于在系统关闭后, S2迅速进入厌氧状态.
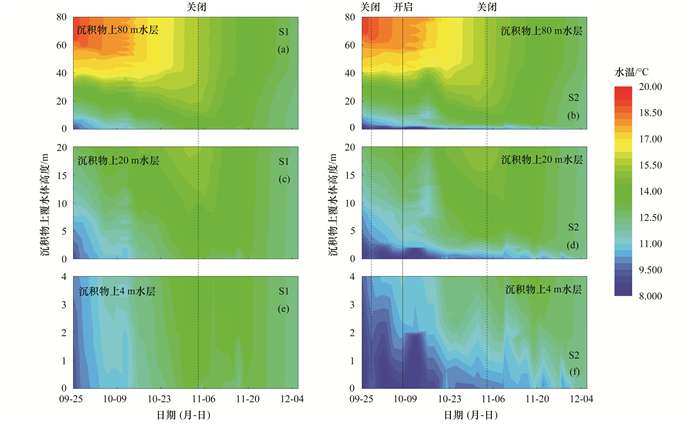
2.1.2 水温的垂向分布特征由于S2处较深, 人工强制混合效率较低, S1和S2底部水体垂向混合程度存在差异.如图 3所示, S1在扬水曝气垂向混合作用的影响下, 温跃层逐渐下移, 上部变温层水温逐渐降低, 底部同温层水温逐渐升高, 垂向混合程度逐渐提高, 9月25日水体垂向温差为10.11℃, 11月4日系统运行结束时水体垂向仍存在2.68℃温差[图 3(a)], 由于温差依然存在, 系统运行结束后水体混合并不完全, 11月19日温差降低至1℃以内, 说明S1在此时达到了较为完全的混合状态[图 3(a)].S2在系统短暂关闭期间(9月28日至10月8日)水体维持稳定的分层[图 3(b)], 10月8日系统运行后, 在人工强制混合作用的影响下水体持续混合[图 3(b)], 但S2地势较低, 水体混合程度较差[图 3(f)], 系统运行结束时水体上下温差为4.81℃[图 3(b)], 其中沉积物界面以上4 m水层内温差便达2.89℃[图 3(f)], 混合层并未下潜至沉积物界面, 直至12月3日才达到完全混合.
|
图 3 金盆水库S1和S2水温的垂向分布特征 Fig. 3 Vertical distribution characteristics of water temperature at the S1 and S2 sites of Jinpen Reservoir |
S1和S2水体不同的混合状态对底部溶解氧浓度变化有重要影响.对S1来说, 系统运行结束后, 水体垂向混合过程进行更快, 在底部溶解氧耗尽前便进入完全混合状态, 上层水体溶解氧的补充使底部迅速恢复好氧状态.对S2来说, 在扬水曝气系统关闭时, 水体混合层并未下潜至沉积物界面, 直到混合层整体温度下降至与沉积物上覆水温度一致时, 水体才完成完全混合, 底部水体溶解氧才能得到补充, 这使得S2底部在12月3日才恢复好氧状态.
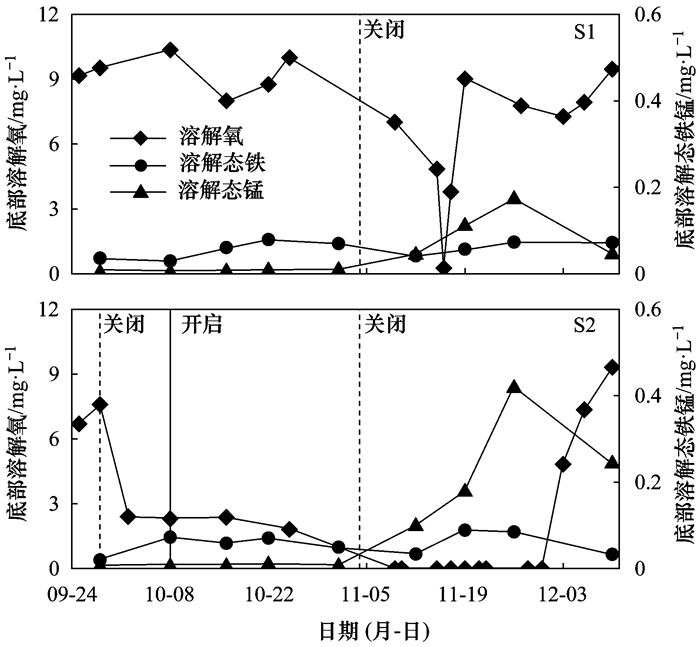
2.2 金盆水库S1和S2铁锰的变化特征 2.2.1 S1和S2底部铁锰的变化特征图 4为扬水曝气系统关闭前后, S1和S2底部铁锰及溶解氧浓度随时间的变化.从中可知, S1在系统运行期底部水体溶解氧浓度较高, 溶解态铁、锰维持较低水平, 平均值分别为0.05 mg·L-1和0.01 mg·L-1; 系统关闭后, S1底部溶解氧浓度以0.964 mg·(L·d)-1的速率下降至0.26 mg·L-1, 待11月17日水体完全混合后, 底部溶解氧浓度又迅速回升.水体溶解态锰浓度变化受溶解氧浓度影响逐渐增加, 在11月26日出现峰值, 达0.17 mg·L-1, 而水体溶解态铁浓度较为稳定, 说明沉积物中还原态锰更难被氧化, 当水体溶解氧浓度降低时迅速由沉积物释放进入上覆水体, 这与Bryant等[17]利用同温层曝气技术抑制沉积物中锰释放的研究结果一致.
|
图 4 S1和S2底部溶解氧及铁锰浓度的时间变化 Fig. 4 Variations of dissolved oxygen, iron, and manganese with time in the bottom water at the S1 and S2 sites |
S2在5号曝气器短暂关闭期间(9月28日至10月8日)底部溶解氧迅速由7.59 mg·L-1降低至2.41 mg·L-1, 10月8日5号曝气器重新运行后, 由于该处水体混合充氧效率较低, 底部水体溶解氧浓度维持在2.30 mg·L-1左右, 并于11月4日系统运行结束后迅速进入厌氧状态, 该状态一直持续至11月30日, 系统运行结束后底部溶解态铁、锰分别以平均0.008 mg·(L·d)-1和0.023 mg·(L·d)-1的速度升高, 溶解态铁、锰分别于11月19日和11月26日达到峰值, 峰值浓度分别为0.09 mg·L-1和0.42 mg·L-1.受沉积物上覆水体好氧/厌氧边界层的影响, 上部好氧水体中溶解态锰被氧化为颗粒态向表层沉积物沉积, 进入还原环境的沉积物中重新被还原为溶解态锰, 表现为溶解态锰不断在表层沉积物及上覆水体中积聚(图 5).

|
图 5 S1和S2沉积物间隙水-上覆水中溶解态铁锰浓度的垂向分布特征 Fig. 5 Vertical distribution characteristics of dissolved iron and manganese in pore-water-overlying water at the S1 and S2 sites |
S1和S2沉积物间隙水-上覆水中铁锰浓度的垂向分布如图 5所示.S1沉积物间隙水中溶解态铁锰浓度峰值均出现在10~15 cm处, 浓度在10.86~16.43 mg·L-1之间, 峰值处溶解态铁浓度略高于溶解态锰[图 5(a)、5(c)和5(e)].S2沉积物间隙水中溶解态铁锰峰值区域分别出现在12~16 cm和5~9 cm, 峰值区域浓度变化范围分别为10.29~23.30 mg·L-1和10.18~14.81 mg·L-1[图 5(f)~5(j)].该结果与康亭等[24]对阿哈湖间隙水铁锰浓度分布的测定结果类似.由于铁锰氧化还原电位存在差异, 锰(Ⅳ)通常优先于铁(Ⅲ)被还原[25], 在有机物降解过程中锰氧化物作为电子受体优先被还原溶解, 而10 cm以下铁氧化物逐渐参与有机质的降解反应, 成为优势电子受体.该现象在S1沉积物间隙水中溶解态铁锰浓度分布的测定结果中也有一定体现, 但规律性不明显.
S1表层沉积物间隙水中溶解态锰在11月19日出现升高现象, 表层0.5 cm处溶解态锰浓度为4.65 mg·L-1[图 5(c)], 上覆水中也随之出现升高现象, 11月26日沉积物以上1 cm处溶解态锰浓度升至0.26 mg·L-1[图 5(d)].S2底部水体在11月9日进入厌氧状态后, 表层沉积物间隙水和上覆水中溶解态锰浓度均随时间不断升高[图 5(g)~5(i)], 浓度最高分别为9.24 mg·L-1和0.65 mg·L-1, 11月30日后底部溶解氧浓度升高(图 4), 表层沉积物间隙水和上覆水中溶解态锰浓度随之降低[图 5(j)].表层沉积物间隙水及上覆水中溶解态锰的升高均发生在底部溶解氧迅速降低或进入厌氧状态时, 这说明还原态锰难以被氧化, 同时沉积于表层沉积物的颗粒态锰重新还原释放, 溶解态锰不断在表层沉积物中积聚[图 5(c)、5(h)和5(i)]. 12月10日沉积物-水界面处已恢复好氧状态, 但溶解态锰依然存在该特点[图 5(j)], 这可能是由于厌氧期间界面处溶解态锰积聚较多所致.
S1和S2表层沉积物间隙水中溶解态铁浓度均较低, 变化范围分别为0.18~1.19 mg·L-1和0.13~0.82 mg·L-1, 平均值分别为0.68 mg·L-1和0.55 mg·L-1(图 5).S1表层沉积物间隙水中溶解态铁的释放受到了沉积物-水界面处高浓度溶解氧的抑制.而S2在进入厌氧状态后, 表层沉积物间隙水中溶解态铁浓度并没有显著地升高趋势, 一方面, 铁锰氧化还原电位的差异导致的峰位差异(图 5)是需要考虑的因素, 铁氧化物在表层沉积物中不是优势电子受体, 故较难还原溶解; 另一方面, 还原态铁会受到上层沉积物中其他氧化剂(锰氧化物、硝酸盐等)的抑制, 有研究表明锰氧化物可以氧化溶解态铁[26], 罗莎莎等[27]认为该反应是洱海间隙水铁锰垂向分布中峰位出现差异的重要因素.这说明沉积物中溶解态铁的释放, 不仅受到溶解氧的抑制, 也受到了锰氧化物等其他氧化剂的抑制.
2.3 S1和S2沉积物-水界面处铁锰的扩散通量本研究利用沉积物一侧间隙水中溶解态铁锰浓度分布情况计算溶解态铁锰通过沉积物界面处的扩散通量[17, 28], 扩散通量为正表示溶解态铁锰自沉积物向界面处扩散, 为负表示自界面处向沉积物内部扩散.在以往研究中, 由于沉积物间隙水中溶解态铁锰浓度远高于上覆水, 因此通常认为溶解态铁锰的扩散都是由沉积物向界面处扩散[29].然而, 最近的研究认为, 人工充氧设施不断将水体中还原态的铁锰氧化, 铁锰氧化物颗粒不断沉降至还原性的沉积物中, 再次溶解并短时期内不断在沉积物-水界面处积聚[17, 28].在上述条件下, 溶解态铁锰表现为由沉积物界面处向两侧扩散(图 5), 则沉积物一侧扩散通量可能为负值.
由表 1可知, S1和S2沉积物水界面处溶解态铁多表现为自沉积物向界面处扩散, 但强度较低, 扩散通量的变化范围为-0.84~1.05 mg·(m2·d)-1.S1沉积物水界面处溶解态锰除11月19日外均为正值, 扩散通量变化范围为-1.96~4.07 mg·(m2·d)-1; S2沉积物水界面处溶解态锰在11月19日后均为负值, 扩散通量变化范围为-1.35~4.39 mg·(m2·d)-1.
|
|
表 1 金盆水库S1和S2沉积物-水界面处铁锰的扩散通量/mg·(m2·d)-1 Table 1 Diffusion flux of iron and manganese at the sediment-water interface at the S1 and S2 sites of Jinpen Reservoir/mg·(m2·d)-1 |
S2底部水体在进入厌氧状态后, 沉积物中的溶解态锰不断向上覆水体释放(图 4), 而沉积物-水界面处溶解态锰在短时期内出现积聚现象(图 5), 呈现出向界面两侧扩散的特点, 使扩散通量出现负值(表 1).这一方面可能是由于扬水曝气系统关闭导致底部边界层扰动削弱, 间隙水中溶解态锰迅速向上释放, 同时上部好氧水层的颗粒态锰不断向下沉积, 导致S2处沉积物-水界面及上覆水溶解态锰浓度迅速升高; 另一方面, 由柱状采泥器获取的厘米级间隙水浓度剖面分辨率不足, 为分析沉积物-水界面处的瞬时扩散通量带来了一定难度.Bryant等[17]讨论了不同分辨率的间隙水锰获取方法(厘米级与毫米级)对扩散通量计算的影响, 认为毫米级的测定方法能更准确地获取沉积物-水界面处锰的浓度梯度变化, 从而得到更为精准的扩散通量.
对于本研究来说, 11月4日扬水曝气系统运行结束后, S1和S2溶解态锰的扩散通量均出现降低趋势.此结果与Li等[28]对扬水曝气技术影响沉积物-水界面处铁锰扩散通量的研究结果一致, 也与Bryant等[17]的研究结果一致.系统运行结束后, S1和S2底部水体溶解氧浓度迅速降低(图 4), 沉积物-水界面处溶解态锰浓度升高(图 5), 从而导致∂c/∂z以及扩散通量的降低[28].S1和S2溶解态铁的扩散通量均较低, 且整体规律性不明显.这一方面与铁锰氧化还原性质的差异有关, 沉积物中的氧化态铁较难还原释放, 一方面与间隙水剖面的测定误差有关.
2.4 厌氧层内铁锰的生物地球化学循环作用由Fick第一定律估算的扩散通量只能体现铁锰离子的一维物理扩散过程, 并没有考虑其他过程的影响.由径流携带或由库区内部产生的颗粒态锰沉降进入厌氧层后会向溶解态锰转化, 该过程亦会导致厌氧层中溶解态锰的积聚[30].并且, 随着水体垂向混合的进行, 厌氧层的体积缩小, 也会导致厌氧层中溶解态锰浓度进一步提高.
为验证上述过程对厌氧层中溶解态锰积聚的影响, 采用如下公式计算厌氧层内溶解态锰浓度(mg·L-1):
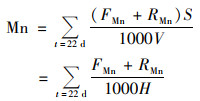
|
(5) |
式中, FMn为溶解态锰扩散通量[mg·(m2·d)-1]; RMn为颗粒态锰平均沉降通量[mg·(m2·d)-1], 采用该时期好氧区域S1沉降颗粒收集器数据计算而来, 为15.31 mg·(m2·d)-1; S为底部厌氧区域面积(m2); V为厌氧区域体积(m3); H为厌氧层高度(m).为了简化模型, 假设底部厌氧区域为以S2为中心的圆形, 那么由于V=S·H, 最终公式中包含FMn、RMn与H这3项.S2底部水体的厌氧状态持续至11月30日(图 4), 故本计算终止于11月30日.最终结果如图 6所示.
|
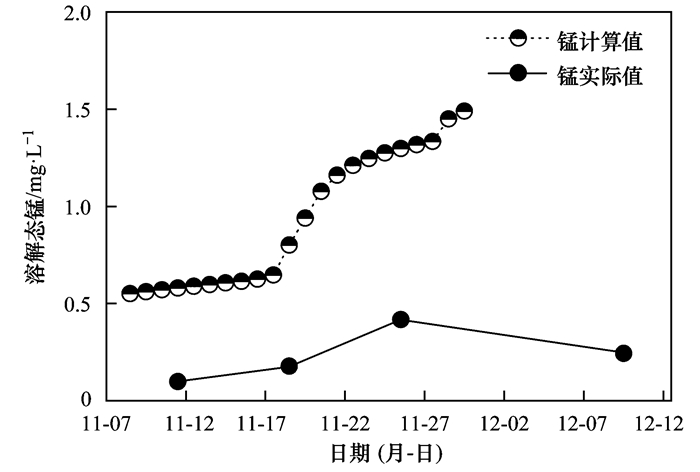
图 6 利用质量平衡计算验证生物地球化学循环过程对厌氧层中溶解态锰浓度的影响 Fig. 6 Mass balance calculation to verify the effect of the biogeochemical cycle on manganese concentration in the anaerobic layer |
锰的计算值显著高于实测值, 这是由于本计算假设沉淀进入厌氧层的颗粒态锰全部会转化为溶解态锰, 从而导致计算值偏高.计算值与实测值的变化趋势是相似的, 一定程度上体现了沉降通量、扩散通量与厌氧层高度三项因素对厌氧层内溶解态锰积聚的影响.实际水体中, 铁锰在厌氧层中的循环过程涉及因素较多, 由于本计算较为简单, 仅考虑了三项因素, 故此计算只做辅助参考使用.关于厌氧层内铁锰的生物地球化学循环作用有待于进一步的研究.
在本研究中, 地形因素及扬水曝气装置的安装高度影响了扬水曝气系统的混合充氧效果, 从而导致S2混合效率较低, 沉积物释放大量溶解态锰污染底部水体.为削弱地形因素的影响, 可通过尽量贴近水库底部安装曝气器、提高曝气器的气体流量等方式来增强人工强制混合充氧系统对底部水体的混合充氧效果, 从而较为合理地指导扬水曝气系统运行.
3 结论(1) 水库地形地貌在一定程度上会影响扬水曝气系统的混合充氧效率, 导致金盆水库底部不同区域溶解氧浓度出现差异.在2018年11月4日系统运行结束后, S1底部溶解氧于11月16日下降至最低值0.26 mg·L-1, 之后迅速回升; S5底部水体进入厌氧状态, 该状态从11月9日持续至11月30日.
(2) S1和S2底部水体溶解氧的不同变化使底部溶解态锰产生了不同的释放强度.系统运行结束后, S1底部溶解态锰浓度最高达0.17 mg·L-1, S2底部溶解态锰释放更加剧烈, 浓度最高达0.42 mg·L-1.
(3) 受铁锰不同氧化还原特性的影响, 金盆水库沉积物间隙水中溶解态锰更容易向上覆水体中释放.S2进入厌氧状态后, 沉积物-水界面处溶解态锰浓度不断升高, 呈现出在表层沉积物中积聚的特征.沉积物中溶解态铁的释放既受到溶解氧的抑制, 也受到锰氧化物等其他氧化剂的抑制.
(4) 扬水曝气系统运行结束后, S1和S2底部水体溶解氧浓度降低且沉积物-水界面处溶解态锰浓度升高, 最终导致溶解态锰的扩散通量不断降低.厌氧层中溶解态锰的积聚过程不仅与扩散通量有关, 还受沉降通量、厌氧层厚度等因素的影响.关于铁锰在厌氧层内的生物地球化学循环作用有待进一步研究.
| [1] | 黄廷林. 水源水库水质污染原位控制与改善是饮用水水质安全保障的首要前提[J]. 给水排水, 2017, 43(1): 1-3, 69. DOI:10.3969/j.issn.1002-8471.2017.01.001 |
| [2] |
黄廷林, 章武首, 柴蓓蓓. 大水深水库内源污染特征及控制技术[J]. 环境污染与防治, 2010, 32(3): 1-4. Huang T L, Zhang W S, Chai B B. Study on the characteristics and control of endogenous pollution in source water reservoir with great depth[J]. Environmental Pollution and Control, 2010, 32(3): 1-4. DOI:10.3969/j.issn.1001-3865.2010.03.001 |
| [3] | Zhang Y L, Wu Z X, Liu M L, et al. Dissolved oxygen stratification and response to thermal structure and long-term climate change in a large and deep subtropical reservoir (Lake Qiandaohu, China)[J]. Water Research, 2015, 75: 249-258. DOI:10.1016/j.watres.2015.02.052 |
| [4] | Schwefel R, Steinsberger T, Bouffard D, et al. Using small-scale measurements to estimate hypolimnetic oxygen depletion in a deep lake[J]. Limnology and Oceanography, 2018, 63(S1): S54-S67. DOI:10.1002/lno.10723 |
| [5] |
邱晓鹏, 黄廷林, 曾明正. 溶解氧对湖库热分层和富营养化的响应——以枣庄周村水库为例[J]. 中国环境科学, 2016, 36(5): 1547-1553. Qiu X P, Huang T L, Zeng M Z. Responses of dissolved oxygen on thermal stratification and eutrophication in lakes and reservoirs-An example in Zhoucun Reservoir in Zaozhuang City[J]. China Environmental Science, 2016, 36(5): 1547-1553. DOI:10.3969/j.issn.1000-6923.2016.05.040 |
| [6] |
杨思远, 赵剑, 余华章, 等. 南亚热带地区水库夏季铁、锰垂直分布特征[J]. 环境科学, 2017, 38(11): 4546-4552. Yang S Y, Zhao J, Yu H Z, et al. Vertical distribution characteristics of Fe and Mn in subtropical reservoirs during summer[J]. Environmental Science, 2017, 38(11): 4546-4552. |
| [7] |
刘树元, 郑晨, 袁琪, 等. 台州长潭水库铁锰质量浓度变化特征及其成因分析[J]. 环境科学, 2014, 35(10): 3702-3708. Liu S Y, Zheng C, Yuan Q, et al. Analysis on the variation characteristics of iron and manganese concentration and its genesis in Changtan Reservoir in Taizhou, Zhejiang Province[J]. Environmental Science, 2014, 35(10): 3702-3708. |
| [8] |
黄廷林, 柴蓓蓓. 水源水库水质污染与富营养化控制技术研究进展[J]. 地球科学进展, 2009, 24(6): 588-596. Huang T L, Chai B B. Advances in the study of controlling mechanics and technology for source water reservoir quality[J]. Advances in Earth Science, 2009, 24(6): 588-596. DOI:10.3321/j.issn:1001-8166.2009.06.003 |
| [9] | Gantzer P A, Bryant L D, Little J C. Controlling soluble iron and manganese in a water-supply reservoir using hypolimnetic oxygenation[J]. Water Research, 2009, 43(5): 1285-1294. DOI:10.1016/j.watres.2008.12.019 |
| [10] | Munger Z W, Carey C C, Gerling A B, et al. Effectiveness of hypolimnetic oxygenation for preventing accumulation of Fe and Mn in a drinking water reservoir[J]. Water Research, 2016, 106: 1-14. DOI:10.1016/j.watres.2016.09.038 |
| [11] |
周子振, 黄廷林, 李扬, 等. 扬水曝气器对水源水库水质改善及沉积物控制[J]. 中国环境科学, 2017, 37(1): 210-217. Zhou Z Z, Huang T L, Li Y, et al. Improvement of water quality and sediment control by WLAs in a source water reservoir[J]. China Environmental Science, 2017, 37(1): 210-217. |
| [12] |
丛海兵, 黄廷林, 赵建伟, 等. 扬水曝气技术在水源水质改善中的应用[J]. 环境污染与防治, 2006, 28(3): 215-218. Cong H B, Huang T L, Zhao J W, et al. Application of the technology of lifting water and aeration for improving water quality[J]. Environmental Pollution and Control, 2006, 28(3): 215-218. DOI:10.3969/j.issn.1001-3865.2006.03.016 |
| [13] |
王亚平, 黄廷林, 周子振, 等. 金盆水库表层沉积物中营养盐分布特征与污染评价[J]. 环境化学, 2017, 36(3): 659-665. Wang Y P, Huang T L, Zhou Z Z, et al. Distribution and pollution evaluation of nutrients in surface sediments of Jinpen Reservoir[J]. Environmental Chemistry, 2017, 36(3): 659-665. |
| [14] |
马越, 郭庆林, 黄廷林, 等. 西安黑河金盆水库季节性热分层的水质响应特征[J]. 水利学报, 2013, 44(4): 406-415. Ma Y, Guo Q L, Huang T L, et al. Response characteristics of water quality to the seasonal thermal stratification in Jin-pen reservoir along the Heihe river, Xi'an city in China[J]. Journal of Hydraulic Engineering, 2013, 44(4): 406-415. DOI:10.3969/j.issn.0559-9350.2013.04.006 |
| [15] |
巨拓, 黄廷林, 马卫星, 等. 稳定分层水库水质的季节性变化特征及扬水曝气水质改善[J]. 湖泊科学, 2015, 27(5): 819-828. Ju T, Huang T L, Ma W X, et al. Characteristics of seasonal variation and water-lifting aerator improvement of water quality in a steady stratified reservoir[J]. Journal of Lake Sciences, 2015, 27(5): 819-828. |
| [16] |
黄廷林, 谭欣林, 李扬, 等. 金盆水库热分层特性及扬水曝气系统运行效果研究[J]. 西安建筑科技大学学报(自然科学版), 2018, 50(2): 270-276, 284. Huang T L, Tan X L, Li Y, et al. Study of the thermal regime characteristics and effect of water-lifting aerators operation on the Jinpen reservoir[J]. Journal of Xi'an University of Architecture & Technology (Natural Science Edition), 2018, 50(2): 270-276, 284. |
| [17] | Bryant L D, Hsu-Kim H, Gantzer P A, et al. Solving the problem at the source:Controlling Mn release at the sediment-water interface via hypolimnetic oxygenation[J]. Water Research, 2011, 45(19): 6381-6392. DOI:10.1016/j.watres.2011.09.030 |
| [18] |
汪嘉宁, 赵亮, 魏皓. 潮滩动力过程影响下扩散边界层和沉积物-水界面扩散通量的变化[J]. 科学通报, 2012, 57(8): 656-665. Wang J N, Zhao L, Wei H. Variable diffusion boundary layer and diffusion flux at sedimentwater interface in response to dynamic forcing over an intertidal mudflat[J]. Chinese Science Bulletin, 2012, 57(13): 1568-1577. |
| [19] |
雷沛, 张洪, 王超, 等. 沉积物-水界面污染物迁移扩散的研究进展[J]. 湖泊科学, 2018, 30(6): 1489-1508. Lei P, Zhang H, Wang C, et al. Migration and diffusion for pollutants across the sediment-water interface in lakes:a review[J]. Journal of Lake Science, 2018, 30(6): 1489-1508. |
| [20] |
丁帅, 王圣瑞, 张蕊, 等. 滇池水生植物分布对沉积物间隙水磷浓度的影响[J]. 环境科学, 2016, 37(10): 3828-3834. Ding S, Wang S R, Zhang R, et al. Concentration of phosphorus in sediments interstitial water as affected by distribution of aquatic plants in Dianchi Lake[J]. Environmental Science, 2016, 37(10): 3828-3834. |
| [21] |
望雪, 程豹, 杨正健, 等. 澜沧江流域沉积物间隙水-上覆水营养盐特征与交换通量分析[J]. 环境科学, 2018, 39(5): 2126-2134. Wang X, Cheng B, Yang Z J, et al. Differences in diffusive fluxes of nutrients from sediment between the natural river areas and reservoirs in the Lancang River Basin[J]. Environmental Science, 2018, 39(5): 2126-2134. |
| [22] | Li Y H, Gregory S. Diffusion of ions in sea water and in deep-sea sediments[J]. Geochimica et Cosmochimica Acta, 1974, 38(5): 703-714. DOI:10.1016/0016-7037(74)90145-8 |
| [23] |
马卫星.暴雨径流潜流对峡谷分层型水源水库水质影响与水质原位改善[D].西安: 西安建筑科技大学, 2015. 83-86. Ma W X. The effects of rainstorm flow undercurrent on water quality and the in-situ water quality improvement of a canyon-shaped, stratified, source water reservoir[D]. Xi'an: Xi'an University of Architecture and Technology, 2015. 83-86. |
| [24] |
康亭, 宋柳霆, 郑晓笛, 等. 阿哈湖和红枫湖沉积物铁锰循环及重金属垂向分布特征[J]. 生态学杂志, 2018, 37(3): 751-762. Kang T, Song L T, Zheng X D, et al. Iron and manganese cycling and vertical distribution of heavy metals in sediments of Aha Lake and Hongfeng Lake[J]. Chinese Journal of Ecology, 2018, 37(3): 751-762. |
| [25] | Dent S R, Beutel M W, Gantzer P, et al. Response of methylmercury, total mercury, iron and manganese to oxygenation of an anoxic hypolimnion in North Twin Lake, Washington[J]. Lake and Reservoir Management, 2014, 30(2): 119-130. DOI:10.1080/10402381.2014.898350 |
| [26] | Hongve D. Cycling of iron, manganese, and phosphate in a meromictic lake[J]. Limnology and Oceanography, 1997, 42(4): 635-647. DOI:10.4319/lo.1997.42.4.0635 |
| [27] |
罗莎莎, 万国江, 黄荣贵. 云南洱海沉积物——水界面铁、锰的分布和迁移特征[J]. 重庆环境科学, 2000, 22(6): 19-21. Luo S S, Wan G J, Huang R G. Characteristics of distribution and removal of Fe and Mn at the sediment-water interface of Erhai Lake, Yunnan Province[J]. Chongqing Environmental Science, 2000, 22(6): 19-21. DOI:10.3969/j.issn.1674-2842.2000.06.008 |
| [28] | Li N, Huang T L, Mao X J, et al. Controlling reduced iron and manganese in a drinking water reservoir by hypolimnetic aeration and artificial destratification[J]. Science of the Total Environment, 2019, 685: 497-507. DOI:10.1016/j.scitotenv.2019.05.445 |
| [29] |
汪福顺, 刘丛强, 灌瑾, 等. 贵州阿哈水库沉积物中重金属二次污染的趋势分析[J]. 长江流域资源与环境, 2009, 18(4): 379-383. Wang F S, Liu C Q, Guan J, et al. Trend analysis of the recycling of heavy metals in sediments of Aha Lake, Guizhou province[J]. Resources and Environment in the Yangtze Basin, 2009, 18(4): 379-383. DOI:10.3969/j.issn.1004-8227.2009.04.014 |
| [30] | Balistrieri L S, Murray J W, Paul B. The cycling of iron and manganese in the water column of Lake Sammamish, Washington[J]. Limnology and Oceanography, 1992, 37(3): 510-528. DOI:10.4319/lo.1992.37.3.0510 |
 2020, Vol. 41
2020, Vol. 41


