2. 中国科学院大学, 北京 100049;
3. 福建农林大学生命科学学院, 福州 350002
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. College of Life Sciences, Fujian Agriculture and Forestry University, Fuzhou 350002, China
近年来, 人类活动(工业废水和生活污水的排放, 农药和化肥的大量使用, 人畜粪便的排放, 污染物填埋, 化石燃料的外泄等)向水体中排入大量的氮(N)[1].有研究表明, 全球越来越多的水体受到不同程度N污染, 欧洲黑海和地中海等地区由于N污染程度较高导致水质严重恶化[2]; 在亚洲, 以太湖为例水体中总氮浓度在1981~1995年间由0.90 mg·L-1增加至3.06 mg·L-1[3].张菊等[4]的研究指出, 上海河流水体中N负荷已远超过富营养化的N浓度界限.氮素的生物地球化学循环已成为生态环境研究关注的焦点[5].水体中的氮主要包括无机氮和有机氮, 其中无机氮主要以硝酸盐和铵盐的形式存在[6].高浓度的硝酸盐不仅威胁着人类的身体健康, 也会加重水体的富营养化.随着工业化程度的提高以及城市化进程不断加快, 河流和湖泊的富营养化逐渐成为我国地表水水质恶化和水体功能受损最严重的问题[7].当水体中铵盐浓度过高时, 不仅会影响水质, 还会抑制部分水生生物的生长[8].硝酸盐污染治理难度大, 现有的修复技术很难有效控制硝酸盐的面源污染[9], 而相对于硝酸盐, 铵盐在水中的运移速率很慢, 一旦水体受到铵的污染很难用现有的技术和方法加以去除[10].因此, 污染源精准解析逐渐成为控制和管理水体氮素污染的前提.
在识别污染源的各种方法中, 通常利用稳定同位素分析法区分水体中的不同污染源[11].水中硝酸盐污染源来源复杂多样, 随着氮、氧同位素技术的不断发展, 通过硝酸盐氮稳定同位素的分析有助于确定硝酸盐污染来源[12].但是仅仅依靠硝酸盐氮和硝酸盐氧的特征值只能定性地了解污染源, 无法定量地得出各污染源的贡献率, 因此为了估算各污染源对水体硝酸盐污染的贡献率, Phillips[13]提出了贡献率计算模型, 并在此基础上开发了IsoSource软件.孟志龙等[14]运用IsoSource计算等方法判断出汾河下游流域硝酸盐污染来源, 该方法基于稳定同位素质量守恒定律, 利用多元线性混合模型, 求解确定性系统[9].目前, 大多数氮源研究主要是利用水体中硝酸盐氮氧的同位素技术, 由于水中氮的浓度和形态会随着时间的变化而变化, 如果能将氮的初始形态(通常是铵态氮)的同位素组成结合硝酸盐同位素, 可以提高氮素源解析结果的可靠性[15].
自20世纪70年代末以来, 珠江三角洲地区农业活动频繁, 城市化和工业化快速发展, 水体中硝酸盐和铵盐浓度增加[16].大湾区的氮污染逐渐成为环境工作者研究的热点问题, 为了实现可持续的水资源管理和水质保护, 识别污染源和了解污染源影响当地水体营养盐浓度的过程非常重要.木沥河流域位于广东省惠州市惠城区, 是淡水河的一级支流, 水质长期处于劣Ⅴ类水体, 虽经过多年常规治理仍然面临氮素超标的问题.本研究通过对该流域进行铵盐氮稳定同位素的定性分析, 硝酸盐氮、氧定性及定量分析, 结合多元线性混合模型判断木沥河水体中氮素的分布和来源.通过对该流域污染源的解析, 以期达到精确控制流域污染物排放的效果, 从而进一步改善木沥河流域水质状况.
1 材料与方法 1.1 流域概况木沥河流域为亚热带海洋性季风气候, 年平均气温22℃, 年降雨量2 200 mm, 降水主要集中在7和8月.
木沥河流域发源于三栋镇大坑山, 自西向东穿镇而过, 于三栋官桥村紫溪汇入淡水河, 河道全长约16.3 km.该流域由大坑山支流, 鸡笼坑支流和木沥河三部分组成, 两条支流于泰安桥处汇聚成木沥河, 大坑山支流自源头支流起到上塘桥处为上游, 鸡笼坑支流自源头起至村落入口处为上游, 除大坑山支流源头地表裸露较为严重, 两条支流的上游其他区域植被覆盖率高, 农用地占地面积较大, 无明显人口聚居地.两条支流中下游主要以村落和居民聚居地为主.木沥河中上游从泰安桥起至崩山桥主要经厂房和工业园区, 下游从养殖区至淡水河水闸处, 该片区域已远离工业活动区和人口聚居区.
1.2 样品采集本研究于2019年6月底对惠州木沥河流域进行了考察, 整条流域共设置14个监测断面(图 1).每个监测断面设置3个平行组, 每组采集2 L水样, 于野外现场测定水体的pH值(pH)和溶解氧(DO).水样采集后于4℃冷藏带回实验室, 过0.45 μm滤膜后置于4℃冰箱冷藏用于后期水质分析.
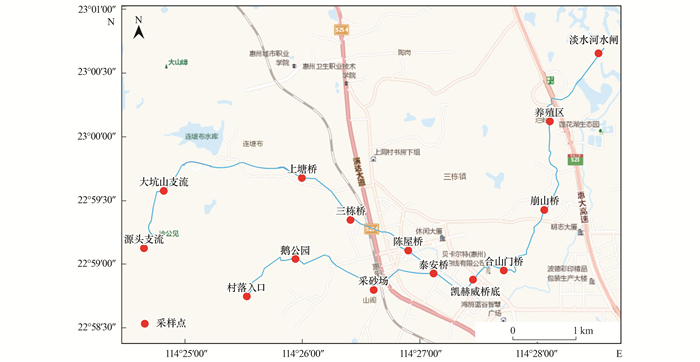
|
图 1 木沥河流域采样点示意 Fig. 1 Schematic diagram of sampling points in the Muli River basin |
水样用COD快速测定仪(5B-5C)测试水样中化学需氧量(COD), 用流动注射分析仪(LACHAT QC8500)分析水样中的总氮(TN)、总磷(TP)、铵态氮(NH4+-N)和硝态氮(NO3--N).
1.4 硝酸盐氮氧同位素测试方法化学处理流程:取40.0 mL水样置于60.0 mL顶空瓶中, 加入0.8 mL CdCl2溶液(20 g·L-1), 然后加入0.8 mL NH4Cl溶液(250 g·L-1), 最后加入3×10 cm 4N(或者3N)洁净锌片(酒精擦拭干净), 在摇床上以220 r·min-1转速振荡15 min(充分反应).取出锌片, 密闭顶空瓶, 完成NO2-还原步骤.向经NO2-还原后的顶空瓶中加入2.0 mL的NaN3溶液(2 mol·L-1)和CH3COOH(20%)的1:1混合液, 剧烈振荡使样品和试剂混匀.之后以220 r·min-1转速振荡30 min(充分反应), 最后加入1.2 mL的NaOH溶液(6 mol·L-1)作为终止剂(溶液显碱性, 不利于叠氮化反应), 结束叠氮化反应.上机测试流程:经上述化学流程反应将硝酸盐转化为N2O气体, 用Gas-Bench-稳定同位素质谱仪联机(Gas-Bench-Mat 253, Thermo公司)测试N2O气体的氮氧同位素值.
δ15Nair值以空气中的氮气作为参考标准, δ15Nair值按公式(1)[17]计算:
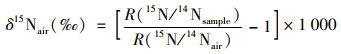
|
(1) |
式中, δ15Nair为样品中稳定同位素比值相对参考物质空气的稳定氮同位素比值的千分差; R(δ15Nair/δ15Nsample)为样品中氮同位素丰度的比值, R(15Nair/15Nsample)为空气中氮气的氮同位素丰度比值.δ15N的分析精度为±0.3‰.
δ18OSMOW作为参考标准, δ18OSMOW值按公式(2)[17]计算:
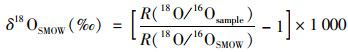
|
(2) |
式中, δ18OSMOW为样品中的氧稳定同位素比值相对参考物质标准平均海洋水的稳定氧同位素比值的千分差; R(18O/16OSMOW)为样品中氧同位素丰度比值; R(18O/16Osample)为标准平均海水中的氧同位素比值; δ18O分析精度为±0.3‰.
所得数据质量:硝酸盐中氮同位素(δ15N)STD < 0.3, 氧同位素(δ18O)STD < 0.3.
1.5 铵盐氮同位素测试方法化学处理流程:取30.0 mL于60.0 mL顶空瓶中, 加入3.0 mL次溴酸钠氧化剂溶液, 混匀, 室温放置45 min.加入0.6 mL亚砷酸钠溶液, 去除过量的BrO-, 通过醋酸溶液(20%)调节pH至6~8.向经铵盐还原后的顶空瓶中加入1.5 mL的NaN3溶液(2 mol·L-1)和CH3COOH(20%)的1:1混合液, 剧烈振荡使样品和试剂混匀.之后以220 r·min-1转速振荡30 min, 最后加入1 mL的NaOH溶液(10 mol·L-1)作为终止剂(溶液显碱性, 不利于叠氮化反应), 结束叠氮化反应.
经上述化学流程反应将硝酸盐转化为N2O气体, 用Gas-Bench-稳定同位素质谱仪联机(Gas-Bench- MAT 253, Thermo公司)测试N2O气体的氮氧同位素值.
δ15Nair值以空气中氮气作为参考标准, δ15Nair值按公式(3)[17]计算:
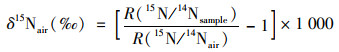
|
(3) |
式中, δ15Nair为样品的氮稳定同位素比值相对参考物质空气的稳定氮同位素比值的千分差; R(15N/14Nsample)为样品中氮同位素丰度比值; R(15N/14Nair)为空气中氮气的氮同位素丰度比值; δ15N值的分析精度为±0.3‰.
数据质量:铵盐中氮同位素(δ15N)STD < 0.3.
1.6 多元线性混合模型多元线性混合模型的原理是通过水体与特定硝酸盐来源(假定设为3种来源)中的氮、氧同位素值构建质量守恒模型[18], 见公式(4):

|
(4) |
式中, fA、fB和fC为不同硝酸盐来源所占比例, δA、δB和δC为不同来源氮同位素的数值, λA、λB和λC为不同来源氧同位素的数值.δM和λM为某点水样中氮和氧同位素的值.
本研究采用多元线性混合模型计算4类污染源[大气沉降(AP-Atmospheric deposition)、土壤氮(SN-Soil nitrogen)、化肥(CF-Chemical Fertilizer)和污水及粪肥(M & S-Manure and sewage)]对木沥河流域14个断面水体中NO3-的贡献率.
2 结果与讨论 2.1 流域的水化学特征木沥河整条流域总体偏弱碱性, pH值变化范围不大(6.89~7.78).从表 1可以看出该流域COD变化范围为:4.91~37.90 mg·L-1之间, 虽然两条支流汇合后水体COD值明显升高, 但是浓度基本在Ⅴ类水标准范围内.整条流域TP的浓度在0.02~0.52 mg·L-1之间变化, 根据文献[19], 大坑山支流和鸡笼坑支流均处于地表水环境质量Ⅰ和Ⅱ类标准, 合流处由于含P污染物大量流入, 导致水体TP浓度显著增加, 部分断面甚至超过Ⅴ类水标准限值.
|
|
表 1 水体营养盐浓度/mg·L-1 Table 1 Water nutrient concentration/mg·L-1 |
木沥河流域TN浓度变化范围为0.55~5.36 mg·L-1, 大坑山支流除陈屋桥断面(2.02 mg·L-1)略微高于地表水环境质量Ⅴ类标准, 余下各断面均低于该类水标准.鸡笼坑支流水质状况较好, 浓度均低于地表水环境质量Ⅲ类标准的浓度范围(1.0 mg·L-1).两条支流汇合后水体TN浓度范围为2.13~5.36 mg·L-1, 均大于地表水环境质量Ⅴ类标准.木沥河流域NH4+-N的浓度在0.40~4.74 mg·L-1之间, 其中大坑山支流NH4+-N的浓度范围为0.40~1.13 mg·L-1, 除源头支流断面NH4+-N浓度较高, 其余均低于地表水环境质量Ⅲ类标准; 鸡笼坑支流NH4+-N浓度范围为0.05~0.08 mg·L-1, 均低于地表水环境质量Ⅰ类标准; 木沥河NH4+-N浓度范围为1.55~4.74 mg·L-1, 除淡水河水闸处低于地表水环境质量Ⅴ类标准, 其余均大于该类标准.木沥河流域NO3--N浓度在0.23~1.25 mg·L-1, 远低于集中式生活饮用水地表水源地补充项目标准限值.
木沥河流域TN、NH4+-N和NO3--N浓度变化规律与COD和TP类似, 均表现出合流后浓度高于两条支流浓度, 该趋势可能是因为人类活动导致含氮污水不断排入, 使得水体中TN、NH4+-N和NO3--N浓度偏高[20].值得注意的是, 大坑山支流源头处(源头支流和大坑山支流)无明显人口居住地, 然而该区域NH4+-N浓度高于该支流位于人口聚居区的中下游处.此外, 木沥河下游处两个监测断面(养殖区和淡水河水闸)均远离人口聚居区, 并且养殖区断面附近区域前期养殖业(鸭类和鱼类)较为发达, 现已停止养殖, 但该断面处TN、NH4+-N和NO3--N浓度明显高于淡水河水闸处.通过水化学特征, 本研究只能初步了解木沥河流域氮素污染程度, 无法有效识别该片流域氮素污染来源, 为识别木沥河流域水质未能达标的原因, 本研究引入了铵盐氮同位素技术和硝酸盐氮、氧同位素技术对该片流域氮素污染源进行了精准解析.
2.2 铵盐同位素解析在天然条件下, 硝态氮是淡水流域中溶解态氮的主要存在形式[21], 然而由表 1的数据可知:木沥河流域合流处水体氮素主要来自于铵盐.类似研究表明, 利用铵盐氮稳定同位素可以帮助识别和量化水体中氮素的来源[15, 20], Lee等[22]通过对汉江流域铵盐氮同位素的有效分析得出该流域NH4+污染主要来自于人类生活污水的排放, Ryu等[15]利用铵盐氮同位素揭示了不同时期化肥, 土壤及人畜粪便对韩国清米河氮素污染情况.因此, 通过测定铵盐氮稳定同位素对水体中NH4+进行污染源解析是可行的.当水体pH值大于9.30时, NH4+易转化为NH3[14].在本研究中, 该流域pH值变化范围为6.89~7.78, 因此在对水体铵盐污染源的解析过程中, 不需要考虑氨挥发带来的影响.
本研究表明大坑山支流铵盐氮同位素值在2.3‰~13.8‰, 其中最大值落在三栋桥断面(13.8‰), 最小值落在源头支流断面(2.3‰).鸡笼坑支流铵盐氮同位素值分别为村落入口断面3.8 ‰, 鹅公围断面4.4‰, 采砂场断面6.0‰.两条支流汇合后木沥河铵盐氮同位素值范围为4.2‰~11.4‰, 其中最大值在养殖区(11.4‰), 凯赫威桥底的值在该合流内最低(4.2‰).Freyer等[23]的研究发现, 由动物排泄物释放的氨的δ15N值范围为-12.0‰~-4.0‰, 而来自于肥料的氨的δ15N值为-5.0‰~0.0‰.Heaton等[24]的观测结果表明, 大气中颗粒物中铵态氮的δ15N值范围为0.0‰~15.0‰.本研究中铵盐氮同位素值在2.3‰~13.8‰之间(图 2), 就流域整体而言铵盐氮稳定同位素值主要落在大气颗粒物范围内.
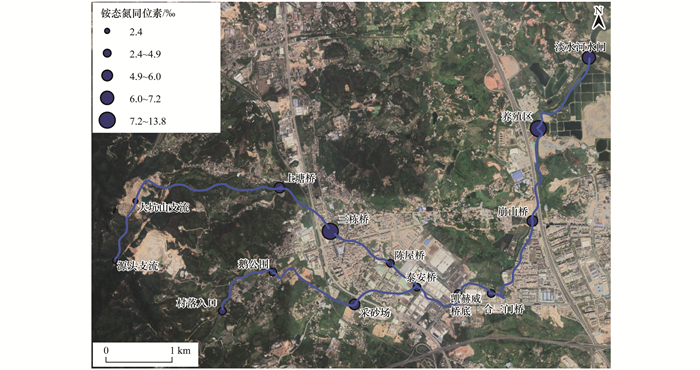
|
图 2 木沥河流域铵态氮同位素值(δ15N-NH4+)时空分布特征 Fig. 2 Spatiotemporal distribution of ammonium nitrogen isotopic values(δ15N-NH4+) in the Muli River basin |
由表 1数据可知除NH4+-N外NO3--N亦是该片流域溶解态氮的主要存在形式, 因此仅仅通过铵盐源解析不足以说明木沥河流域氮素污染来源.为了对木沥河流域氮素污染做出更全面和更精准地解析, 本研究引入了硝酸盐氮、氧同位素示踪技术.
氮元素在自然界迁移转化过程中, 伴随的一系列物理、化学和生物反应使得氮氧同位素发生分馏, 其中微生物的反硝化作用会导致水体中硝酸盐氮同位素值随着硝酸盐浓度的增高呈指数增加, 对硝酸盐氮氧同位素技术精准溯源具有较大的影响.因此, 识别是否存在反硝化作用是用同位素方法识别硝酸盐来源的一个重要前提[25].木沥河溶解氧浓度范围为2.67~7.98 mg·L-1, 研究表明当水体溶解氧浓度大于2.00 mg·L-1时不利于微生物反硝化作用发生[26].并且在本研究中, 木沥河流域的硝酸盐浓度与硝酸盐氮同位素浓度和硝酸盐氧同位素浓度不存在负相关关系, 由此推断该流域没有明显的反硝化作用发生[27].
由图 3和4可知, 木沥河流域硝酸盐氮、氧同位素值具有较大的空间差异性:整体而言木沥河硝酸盐氮、氧同位素值要大于大坑山支流和鸡笼坑支流, 6个断面2种同位素值较为接近; 大坑山支流硝酸盐氮同位素值上塘桥断面最高, 而硝酸盐氧同位素值大坑山支流断面则远大于该支流其余各断面; 鸡笼坑支流3个断面硝酸盐氮、氧同位素值差异不大.结合多元线性混合模型定性分析的结果可知(图 5), 在本研究中大坑山支流硝酸盐氮同位素值的范围是(-3.8‰~2.7‰), 平均值为-0.7‰; 氧同位素值的范围是(-6.6‰~6.3‰), 平均值为0.8‰.鸡笼坑支流硝酸盐氮同位素值的范围是(1.9‰~2.5‰), 平均值为2.2‰; 氧同位素的值范围是(5.5‰~7.6‰), 平均值为6.7‰.木沥河硝酸盐氮同位素值的范围是(2.7‰~4.6‰), 平均值为3.6‰; 氧同位素的值范围是(4.0‰~9.3‰), 平均值为7.0‰.大多数陆地物质的硝酸盐氮同位素特征值在-20.0‰~30.0‰之间, 硝酸盐氧同位素特征值在-5.0‰~75.0‰, 其中人工合成化肥δ15N大多在0.0‰±3.0‰左右, δ18O在22‰±3‰左右; 土壤含氮有机物经过微生物硝化作用δ15N值在-3.0‰~10.0‰变化[28], δ18O值在-5.0‰~7.0‰变化[29].大气氮沉降的δ15N值受到大气中复杂的化学反应及各种人类活动(化石燃料的燃烧)的影响, 其范围是-13.0‰~13.0‰[30], δ18O范围是20.0‰~70.0‰[31].由于同位素特征的相似性, 将污水和粪便作为一个来源, 其δ15N的值10.0‰~25.0‰[29], δ18O的平均值在14.5‰±1.8‰左右[32].依据硝酸盐氮氧同位素来源可知[33], 就流域整体而言氮氧同位素主要落在化肥(铵肥, 硝态氮肥)、污水及粪肥和土壤氮范围内(图 5).
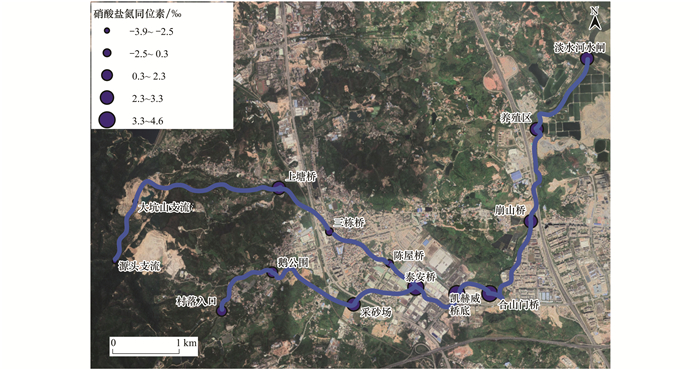
|
图 3 木沥河流域硝酸盐氮同位素值(δ15N-NO3-)时空分布特征 Fig. 3 Spatiotemporal distribution of nitrate nitrogen isotopic values(δ15N-NO3-) in the Muli River basin |

|
图 4 木沥河流域硝酸盐氧同位素值(δ18O-NO3-)时空分布特征 Fig. 4 Spatiotemporal distribution of nitrate nitrogen isotopic values(δ18O-NO3-) in the Muli River basin |
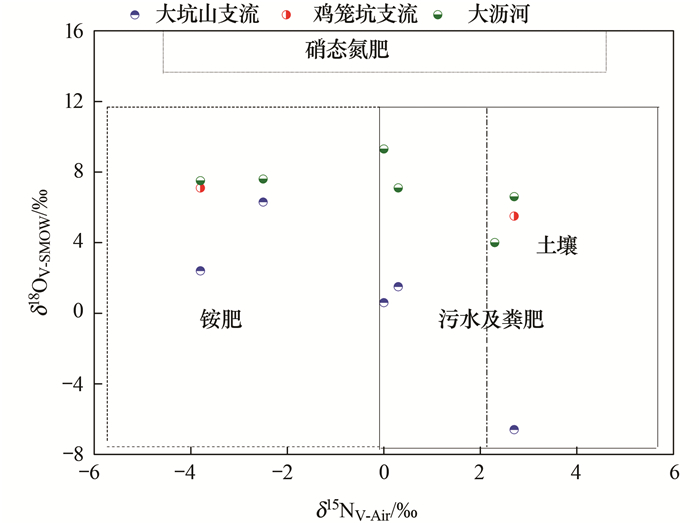
|
图 5 木沥河流域硝酸盐氮同位素值(δ15N-NO3-)和硝酸盐氧同位素值(δ18O-NO3-) Fig. 5 Nitrate nitrogen isotope values (δ15N-NO3-) and nitrate oxygen isotope values (δ18O-NO3-) in the Muli River basin |
通过污染源氮、氧稳定同位素范围比较法来判定硝酸盐来源只能得到定性的结果, 不能量化各个污染源对水体氮污染的贡献率.为此, 在本研究中, 采用多元线性混合模型计算4类污染源[大气沉降(AP)、土壤氮(SN)、化肥(CF)和污水及粪肥(M & S)]对木沥河流域14个断面NO3-的贡献率.根据混合模型输出的结果, 木沥河流域3条支流(图 6)以及各支流不同断面(图 7)4类污染源贡献率有较大的差别.由图 6可知, 大坑山支流硝酸盐污染主要来源于大气沉降, 平均值为61%左右.鸡笼坑支流和木沥河污水及粪肥对硝酸盐污染贡献率最高, 平均值分别为43%和39%左右.
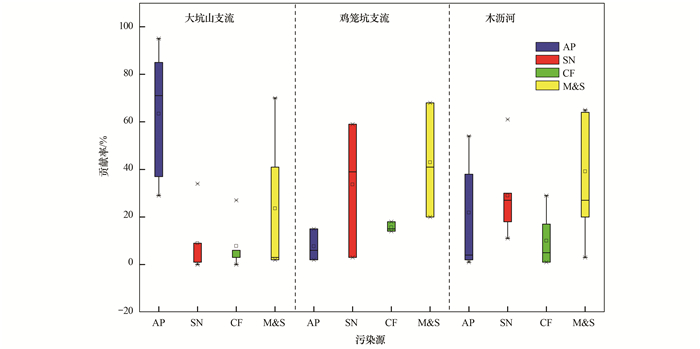
|
AP表示大气沉降(atmospheric deposition); SN表示土壤氮(soil nitrogen); CF表示化肥(chemical fertilizer); M & S表示污水及粪肥(manure and sewage), 下同 图 6 木沥河流域硝酸盐来源的贡献率分布 Fig. 6 Distribution of nitrate source contribution rates in the Muli River basin |
|
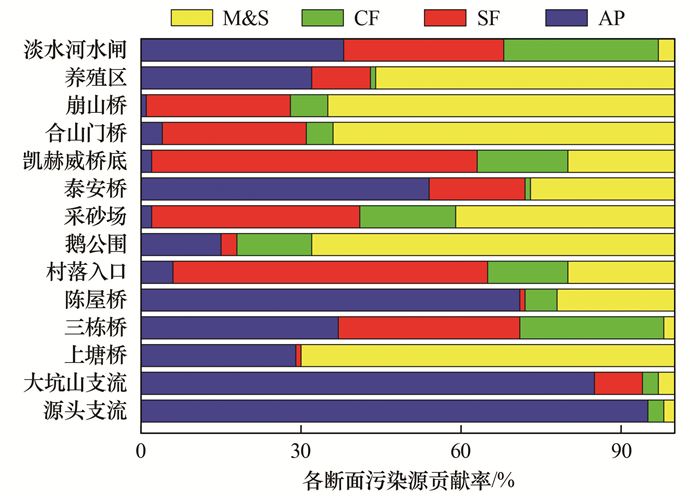
图 7 木沥河流域各段面硝酸盐来源的贡献率 Fig. 7 Contribution rates of nitrate sources in different sections of the Muli River basin |
就流域整体而言, 大气沉降对硝酸盐污染贡献率在1%~95%之间, 土壤有机氮贡献率在0%~59%之间, 化肥贡献率在0%~29%之间, 污水及粪肥对硝酸盐污染贡献率在2%~70%之间.
结合土地利用方式发现, 大坑山支流上游(从源头支流至大坑山支流)、鸡笼坑支流上游(从村落入口至鹅公围)以及木沥河下游(从养殖区至淡水河水闸)均无明显人口聚居地, 但是水体硝酸盐的来源有显著差异.其中大坑山支流上游大气沉降值占主要硝酸盐污染源的85%~95%(图 7), 这可能由于该区域降雨量较大, 地表裸露使得雨水氮的贡献比例较高.鸡笼坑支流上游处土壤有机氮贡献比例高达59%(图 7), 该区域主要土地利用方式为农田使用地.张妍等[34]的研究表明, 过高的氮素投入和低的作物吸收率将导致农田土壤氮大量累积, 土壤中累积的硝态氮会随着降雨形成的地表径流汇入流域中从而使得土壤有机氮成为硝酸盐污染的主要来源.木沥河下游处两个监测断面(养殖区和淡水河水闸)各污染源来源贡献率存在明显的差别, 养殖区断面污水及粪肥的贡献率占56%(图 7), 而淡水河水闸断面污水及粪肥的贡献率仅占3%(图 7).早期养殖区处禽类和鱼类养殖较为密集, 养殖废水直接排入水体, 虽然调查期间各种养殖已被清理, 但是水体残留的排泄物可能仍然超过了环境可消纳量, 使得水体中营养盐浓度长期处于较高水平, 从而导致污水及粪肥对该断面水体硝酸盐污染贡献率大, 不过具体情况如何还需要进一步地研究来证实.
大坑山支流下游(陈屋桥)、鸡笼坑支流中下游(从鹅公围至采砂场)以及木沥河上游(从泰安桥至崩山桥)污水及粪肥的贡献率在22%~68%之间(图 7), 峰值出现在鹅公围(68%), 其次是崩山桥(65%), 合山门桥(64%).已有研究表明当研究区域处于人口聚居区, 且缺乏完善的排污设施会导致生活污水及人畜粪便中携带的营养盐进入到水体中, 从而使得污水及粪肥对该片区域硝酸盐贡献率处于较高水平[35].然而, 现场调查结果表明这一区域虽然人口密度较大, 但是已经完成生活污水截流工程, 木沥河沿岸几乎没有发现有明显的排污口.采样期间惠州正处于雨季, 流域硝酸盐较高的污水及粪肥贡献率可能要归咎于污水井溢流.此外, 大坑山支流下游、鸡笼坑支流中下游以及木沥河上游均为硬质化河岸, 几乎没有水质净化功能, 大量城区暴雨径流使得人类生活污水和人畜粪便以面源污染的形式直接进入水体, 进而导致污水及粪肥对该片区域硝酸盐污染贡献率高.
为保护和改善木沥河流域水质, 控制水体中N素浓度不断增高, 结合污染源示踪结果提出以下建议:①大坑山支流上游处应通过人为调控提高该片区域植被覆盖率, 减少因降雨形成的地表径流中携带的雨水氮直接进入到水体中; ②鸡笼坑支流上游处应注意防控水土流失, 减少土壤有机氮直接进入自然水体中; ③养殖区断面需对流域中底泥进行彻底清除, 从而避免前期残留污染物导致水质持续恶化; ④大坑山支流下游、鸡笼坑支流下游以及木沥河上游应加强对污水井管理和生态驳岸带建设, 减少人类生活污水和畜禽粪便直接进入流域中, 造成水体污染.
3 结论(1) 木沥河流域氮污染严重, 合流后水体氮素浓度显著高于大坑山支流和鸡笼坑支流.值得注意的是, 大坑山支流和养殖区两个断面分布位于木沥河上游和下游, 均远离人口聚集地, 仍然存在严重的NH4+-N污染.
(2) 通过对木沥河流域铵盐氮同位素以及硝酸盐氮、氧同位素定性分析可知, 该流域氮污染主要来自于大气颗粒物、生活污水、动物及人排泄物和肥料这4类.
(3) 多元线性混合模型分析的结果表明, 木沥河流域水体硝酸盐来源具有空间差异性, 且与土地利用方式有一定的相关性.大坑山支流上游植被覆盖率低, 该断面硝酸盐污染的主要来源为大气沉降; 鸡笼坑支流上游土地利用类型以农田为主, 土壤有机氮为该片区域硝酸盐污染的主要来源; 大坑山支流下游、鸡笼坑支流下游和木沥河中上游流经木栋镇, 人类生活污水和人畜粪便是水体硝酸盐污染的主要来源.此外, 养殖区断面沉积物中残留的禽畜排泄物为水体硝酸盐污染的主要来源.
(4) 本研究通过对比土地利用方式, 结合硝酸盐稳定同位素分析以及多元线性混合模型对木沥河流域硝酸盐污染源做出了精准解析, 为高效控制该流域氮污染提供了可靠的建议及意见.
| [1] | Curt M D, Aguado P, Sánchez G, et al. Nitrogen isotope ratios of synthetic and organic sources of nitrate water contamination in Spain[J]. Water, Air, and Soil Pollution, 2004, 151(1-4): 135-142. |
| [2] | Rhue R D, Appel C, Kabengi N. Measuring surface chemical properties of soil using flow calorimetry[J]. Soil Science, 2002, 167(12): 782-790. |
| [3] |
高超, 朱建国, 窦贻俭. 农业非点源污染对太湖水质的影响:发展态势与研究重点[J]. 长江流域资源与环境, 2002, 11(3): 260-263. Gao C, Zhu J G, Dou Y J. Contribution of agricultural non-point source pollution to water quality deterioration in Tai Lake watershed:recent trends and research priorities[J]. Resources and Environment in the Yangtze Basin, 2002, 11(3): 260-263. |
| [4] |
张菊, 陈振楼, 刘杰. 上海河流氮负荷的年际变化及其水体富营养化的原因探讨[J]. 环境污染与防治, 2005, 27(1): 29-33. Zhang J, Chen Z L, Liu J. Annual changes of nitrogen loading and the pilot study on the causes of the eutrophication of rivers in Shanghai city[J]. Environmental Pollution and Control, 2005, 27(1): 29-33. |
| [5] | Tobari Y, Koba K, Fukushima K, et al. Contribution of atmospheric nitrate to stream-water nitrate in Japanese coniferous forests revealed by the oxygen isotope ratio of nitrate[J]. Rapid Communications in Mass Spectrometry, 2010, 24(9): 1281-1286. |
| [6] | Bu H M, Meng W, Zhang Y. Nitrogen pollution and source identification in the Haicheng River basin in Northeast China[J]. Science of the Total Environment, 2011, 409(18): 3394-3402. |
| [7] | Zhou Y, Khu S T, Xi B D, et al. Status and challenges of water pollution problems in China:learning from the European experience[J]. Environmental Earth Sciences, 2014, 72(4): 1243-1254. |
| [8] | Reddy-Lopata K, Auerswald L, Cook P. Ammonia toxicity and its effect on the growth of the South African abalone Haliotis midae Linnaeus[J]. Aquaculture, 2006, 261(2): 678-687. |
| [9] |
曹胜伟, 费宇红, 田夏, 等. 硝酸盐污染氮氧同位素溯源及贡献率分析——以南阳地区为例[J]. 水文地质工程地质, 2019, 46(2): 82-91. Cao S W, Fei Y H, Tian X, et al. Using isotopes of nitrogen and oxygen to trace groundwater nitrate contamination and contribution analysis:exemplified by the Nanyang District[J]. Hydrogeology and Engineering Geology, 2019, 46(2): 82-91. |
| [10] |
宁卓, 张翠云, 张胜. 地下水铵污染及其氮同位素研究[J]. 南水北调与水利科技, 2011, 9(3): 129-132. Ning Z, Zhang C Y, Zhang S. Study of groundwater contamination of ammonium and its nitrogen isotope[J]. South-to-North Water Diversion and Water Science & Technology, 2011, 9(3): 129-132. |
| [11] | Yuan Z W, Wang L, Lan T, et al. Water quality assessment and source identification of water pollution in the Banchengzi reservoir, Beijing, China[J]. Desalination and Water Treatment, 2016, 57(60): 29240-29253. |
| [12] | Guo Z F, Yan C Z, Wang Z S, et al. Quantitative identification of nitrate sources in a coastal peri-urban watershed using hydrogeochemical indicators and dual isotopes together with the statistical approaches[J]. Chemosphere, 2020, 243: 125364. |
| [13] | Phillips D L, Gregg J W. Source partitioning using stable isotopes:coping with too many sources[J]. Oecologia, 2003, 136(2): 261-269. |
| [14] |
孟志龙, 杨永刚, 秦作栋, 等. 汾河下游流域水体硝酸盐污染过程同位素示踪[J]. 中国环境科学, 2017, 37(3): 1066-1072. Meng Z L, Yang Y G, Qin Z D, et al. Isotopic tracing for nitrate pollution process of water body in the lower reaches of Fenhe River[J]. China Environmental Science, 2017, 37(3): 1066-1072. |
| [15] | Ryu H D, Kim M S, Chung E G, et al. Assessment and identification of nitrogen pollution sources in the Cheongmi River with intensive livestock farming areas, Korea[J]. Environmental Science and Pollution Research, 2018, 25(14): 13499-13510. |
| [16] | Huang X P, Huang L M, Yue W Z. The characteristics of nutrients and eutrophication in the Pearl River estuary, South China[J]. Marine Pollution Bulletin, 2003, 47(1-6): 30-36. |
| [17] | McLaughlin K, Nezlin N P, Howard M D A, et al. Rapid nitrification of wastewater ammonium near coastal ocean outfalls, Southern California, USA[J]. Estuarine, Coastal and Shelf Science, 2017, 186: 263-275. |
| [18] | Yue F J, Li S L, Liu C Q, et al. Using dual isotopes to evaluate sources and transformation of nitrogen in the Liao River, Northeast China[J]. Applied Geochemistry, 2013, 36: 1-9. |
| [19] | GB 3838-2002, 地表水环境质量标准[S]. |
| [20] |
吴文欢, 何小娟, 吴海露, 等. 运用氮、氧双同位素技术研究永安江硝酸盐来源[J]. 生态与农村环境学报, 2016, 32(5): 802-807. Wu W H, He X J, Wu H L, et al. Identification of sources of nitrate in the Yongan River with isotopic Technology[J]. Journal of Ecology and Rural Environment, 2016, 32(5): 802-807. |
| [21] |
袁洁.汉江流域上游氮污染的时空变化格局及其来源解析[D].武汉: 中国科学院武汉植物园, 2017. 25. Yuan J. Spatial and temporal variations and source identification of nitrogen pollution in the upper Han River[D]. Wuhan: The Wuhan Botanical Garden of the Chinese Academy of Sciences, 2017. 25. |
| [22] | Lee J, Park T, Kim M S, et al. Stable isotope on the evaluation of water quality in the presence of WWTPs in rivers[J]. Environmental Science and Pollution Research, 2016, 23(18): 18175-18182. |
| [23] | Freyer H D. Seasonal trends of NH4+ and NO3- nitrogen isotope composition in rain collected at Julich, Germany[J]. Tellus, 1978, 30(1): 83-92. DOI:10.1111/j.2153-3490.1978.tb00820.x |
| [24] | Heaton T H E. Isotopic studies of nitrogen pollution in the hydrosphere and atmosphere:a review[J]. Chemical Geology:Isotope Geoscience Section, 1986, 59: 87-102. |
| [25] |
贺国平, 刘培斌, 慕星, 等. 永定河冲洪积扇地下水中硝酸盐来源的同位素识别[J]. 水利学报, 2016, 47(4): 582-588. He G P, Liu P B, Mu X, et al. Identification of nitrate sources in groundwater in the Yongding River alluvial fan with isotope technology[J]. Journal of Hydraulic Engineering, 2016, 47(4): 582-588. |
| [26] | Kendall C, Elliott E M, Wankel S D. Tracing anthropogenic inputs of nitrogen to ecosystems[A]. In: Michener R, Lajtha K, (Eds.). Stable Isotopes in Ecology and Environmental Science[M]. 2nd ed. New Jersey: Blackwell Publishing, 2007. 375-449. |
| [27] |
邢萌, 刘卫国. 浐河、灞河硝酸盐端元贡献比例——基于硝酸盐氮、氧同位素研究[J]. 地球环境学报, 2016, 7(1): 27-36. Xing M, Liu W G. Nitrate source proportional contributions in the Chanhe and Bahe Rivers-Using its isotopic ratios in combination with a Bayesian isotope mixing mode[J]. Journal of Earth Environment, 2016, 7(1): 27-36. |
| [28] | Ye F, Ni Z X, Xie L H, et al. Isotopic evidence for the turnover of biological reactive nitrogen in the Pearl River Estuary, south China[J]. Journal of Geophysical Research, 2015, 120(4): 661-672. |
| [29] | Xue D M, Botte J, De Baets B, et al. Present limitations and future prospects of stable isotope methods for nitrate source identification in surface- and groundwater[J]. Water Research, 2009, 43(5): 1159-1170. |
| [30] | Kendall C, McDonnell J J. Isotope tracers in catchment hydrology[M]. Amsterdam: Elsevier, 1998: 519-576. |
| [31] |
庞凤梅, 吴文良, 孟凡乔, 等. 利用氮、氧稳定同位素识别地下水硝酸盐污染源研究进展[J]. 农业环境与发展, 2011, 28(4): 64-69. Pang F M, Wu W L, Meng F Q, et al. Identification of nitrate source in groundwater using dual isotope (δ15N and δ18O) methods[J]. Agro-Environment and Development, 2011, 28(4): 64-69. |
| [32] | Xing M, Liu W G. Using dual isotopes to identify sources and transformations of nitrogen in water catchments with different land uses, Loess Plateau of China[J]. Environmental Science and Pollution Research, 2016, 23(1): 388-401. |
| [33] |
刘贯群, 周书玉, 黄修东, 等. 多种方法识别青岛大沽河平原区地下水硝酸盐污染来源[J]. 环境科学学报, 2017, 37(1): 347-356. Liu G Q, Zhou S Y, Huang X D, et al. Multiple methods to recognize sources of underground water nitrate contamination in plain area of Dagu River, Qingdao, China[J]. Acta Scientiae Circumstantiae, 2017, 37(1): 347-356. |
| [34] |
张妍, 张秋英, 李发东, 等. 基于稳定同位素和贝叶斯模型的引黄灌区地下水硝酸盐污染源解析[J]. 中国生态农业学报(中英文), 2019, 27(3): 484-493. Zhang Y, Zhang Q Y, Li F D, et al. Source identification of nitrate contamination of groundwater in Yellow River Irrigation Districts using stable isotopes and Bayesian model[J]. Chinese Journal of Eco-Agriculture, 2019, 27(3): 484-493. |
| [35] |
闫亚男, 张列宇, 席北斗, 等. 改良化粪池/地下土壤渗滤系统处理农村生活污水[J]. 中国给水排水, 2011, 27(10): 69-72. Yan Y N, Zhang L Y, Xi B D, et al. Treatment of rural domestic sewage by modified septic tanks/subsurface soil infiltration system[J]. China Water & Wastewater, 2011, 27(10): 69-72. |
 2020, Vol. 41
2020, Vol. 41


