Impact of Hydraulic Retention Time on Performance of Partial Nitrification Granular Sludge in Continuous Stirred-Tank Reactor
稳定的亚硝化技术是短程脱氮工艺的关键[1, 2].将短程硝化与污泥颗粒化技术结合, 培养具有亚硝化性能的颗粒污泥(PNG)是实现高效、稳定亚硝酸盐累积的可行方法[3], 并可作为全自养型脱氮工艺的重要步骤.PNG上富集有大量慢速生长的自养硝化微生物, 因而具有较异养AGS更好的密实度和沉降性能.阴方芳等将SBR中培养成熟的亚硝化颗粒污泥接种到连续流完全混合式反应器(CSTR)中, 可以在无机条件下实现极高的氨氮去除效能, 氨氮去除率稳定在80%左右, 亚硝积累率稳定在84%左右[4].
对于CSTR而言, 水力停留时间(HRT)影响污泥截留性能和颗粒结构, 成为反应器效能调控重要的运行参数[5, 6].在传统活性污泥法中, HRT直接决定了微生物与污染物的接触反应时间, 过短的HRT易导致出水水质下降和污泥流失率增大[7].好氧颗粒污泥(AGS)由于具有良好的沉降性能, 能够在更短的HRT条件下实现稳定运行, 较短的HRT为AGS提供充足的水力选择压, 有助于促进胞外聚合物(EPS)分泌, 改善颗粒形态结构[8~10].
目前, 关于CSTR中HRT对好氧颗粒污泥的影响多是结合基质负荷变化进行的[11~13], 将HRT作为单一因素考察对PNG性能和功能微生物影响鲜见报道.本研究在保持进水氨氮负荷不变的前提下, 较系统地考察HRT对CSRT中颗粒形态结构、氮转化性能、微生物活性和群落结构的影响.
1 材料与方法
1.1 实验装置及运行条件
本实验所用装置为合建式连续流CSTR反应器, 如图 1所示, 由有机玻璃制成, 分曝气区和沉淀区两部分, 有效容积分别为1.7 L和0.6 L.曝气区底部装有曝气装置, 控制曝气量为0.6 L·min-1(表面上升流速0.156 cm·s-1), 为污泥系统提供溶解氧和剪切力.反应器置于恒温水浴箱中, 温度控制在28℃左右.
1.2 接种污泥及实验用水
接种污泥取自本实验室SBR中成熟的亚硝化颗粒污泥, 亚硝酸盐累积率在80% ~85%.初始MLSS和SVI分别约为4.8 g·L-1和35 mL·g-1.
本研究所用模拟污水组成如下:125~500 mg·L-1NH4Cl(以N计), 18 mg·L-1 K2HPO4, 49 mg·L-1 MgSO4, 60 mg·L-1 CaCl2, 1.5 mg·L-1 FeCl3·6H2 O, 1 mL·L-1的微量元素, 微量元素配方见文献[14].通过向进水中投加NaHCO3, 维持反应器中pH在7.8~8.0.控制反应器进水氨氮负荷稳定在3.0 kg·(m3·d)-1, 运行工况分为3个阶段, 反应器具体运行参数如表 1所示.
表 1
(Table 1)
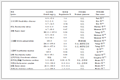
表 1 反应器运行工况和参数
Table 1 Operating conditions and parameters in CSTR
水力停留时间
/h |
运行时间
/d |
进水氨氮
/mg·L-1 |
氮容积负荷
/kg·(m3·d)-1 |
| 4 |
1~30 |
500 |
3 |
| 2 |
31~60 |
250 |
3 |
| 1 |
61~90 |
125 |
3
|
|
表 1 反应器运行工况和参数
Table 1 Operating conditions and parameters in CSTR
|
1.3 分析测试方法
NH4+-N、NO2--N、NO3--N、TN和MLSS/MLVSS等水质指标分别按文献[15]中规定的纳氏试剂比色法、N-(1-萘基)-乙二胺光度法、紫外分光光度法、过硫酸钾氧化法、重量法等进行测定.pH由PB-10型pH计(Sartorius公司)测定, 温度和DO采用H1946N型溶解氧测定仪(WTW公司)进行测定.
采用甲醛-NaOH法进行颗粒污泥EPS的提取, 并使用苯酚-硫酸法、改进的Lowry法分别测定蛋白质(PN)和聚多糖(PS)组分的含量.颗粒污泥沉降速率采用清水静沉法测定.
采用筛分法测算颗粒污泥的粒径分布.定期从反应器中取出部分污泥样品, 经0.9% NaCl溶液反复清洗后, 依次通过孔径为2.5、1.6、1.25、0.8和0.3 mm的分样筛, 称量各筛网截留的污泥质量.根据样品总质量, 计算各粒径区间所占比例和颗粒平均粒径.
1.4 功能菌动力学活性
当反应器出水水质达到稳定状态, 通过批次实验测定颗粒污泥的基质比降解速率和产物比累积速率, 以表征不同功能菌的动力学活性.具体方法为:取湿重为2 g的颗粒污泥, 经0.9% NaCl溶液反复清洗后, 置于250 mL烧杯中, 注入200 mL基质溶液, 曝气反应2 h.控制初始NH4+-N浓度为150 mg·L-1, 其他组分与反应器进水相同, pH=8.0, 水温为28℃, DO浓度在2~4 mg·L-1.期间, 定期取样测定水质指标, 并计算以下比速率值.
NH4+-N比降解速率,mg·(g·h)-1:

|
(1) |
NO2--N比累积速率, mg·(g·h)-1:
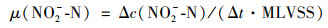
|
(2) |
NO3--N比累积速率, mg·(g·h)-1:

|
(3) |
式中, Δc(NH4+-N)、Δc(NO2--N)和Δc(NO3--N)分别指反应时间Δt内, 上清液中NH4+-N、NO2--N和NO3--N的浓度变化, mg·L-1;MLVSS为挥发性悬浮固体浓度, g·L-1;Δt为各参数值呈线性变化的时间段, h.
1.5 微生物高通量测序分析
在HRT稳定运行条件下反应器中多点采样混合后作为污泥样品, 采用FastPrep DNA提取试剂盒抽提基因组DNA.用16S rRNA基因引物338F(ACTCCTACGGGAGGCAGCAG)和806R(GGACTA CHVGGGTWTCTAAT)对细菌16S rRNA基因进行PCR扩增.使用AxyPrepDNA凝胶回收试剂盒(AXYGEN公司)切胶回收PCR产物, 由上海美吉生物医药科技有限公司完成对PCR扩增产物的高通量测序.
2 结果与讨论
2.1 颗粒污泥的理化特征变化
随着HRT的逐渐缩短, 亚硝化颗粒污泥粒径分布变化如图 2所示.当HRT=4 h时, 粒径1.6~2.5 mm和>2.5 mm的大颗粒分别占到了约40%和35%, 污泥平均粒径为1.8 mm.缩短反应器HRT会使得大颗粒污泥逐渐减少, 粒径在0.3~0.8 mm的颗粒快速增多.当HRT=1 h时, 粒径在0.3~0.8 mm的颗粒占据主导地位, 约占50%, 粒径>1.6 mm和 < 0.3 mm的颗粒分别占到36%和5%以下, 污泥平均粒径稳定在1.3 mm.该结果表明, 缩短HRT, 增大水力冲刷强度, 提升了选择压, 可显著改变CSTR中颗粒污泥的粒径分布, 并使颗粒形态更加均匀和密实.
从图 3可知, 缩短HRT, 反应器出水SS总体呈下降趋势.反应器中污泥浓度从5.2 g·L-1持续增加, 运行至第90 d, MLSS高达15g·L-1左右, 比启动初期提高了近2倍.HRT从4 h减小到1 h, 进水氨氮容积负荷始终维持在3.0kg·(m3·d)-1不变, 污泥MLSS增幅加大, 进一步证实了颗粒污泥可显著提升反应器污泥的生物截留能力, 由于污泥密实度高、沉降速率快, 缩短水力停留时间, 并未出现污泥流失.有研究表明, 随着HRT减小, 容积负荷逐渐增加使得微生物具有较高的生长速率, MLSS显著增加[16, 17].Beun等[18]提出较短的HRT有利于颗粒污泥的形成, SBR反应器HRT为8 h运行10周, 颗粒污泥的MLSS从1.2 g·L-1增加到1.3 g·L-1, 缩短HRT到6.75 h运行8周, 颗粒污泥的MLSS从1.3 g·L-1增加到2.7 g·L-1.Liu等[6]维持进水氨氮容积负荷在8.0kg·(m3·d)-1, 考察HRT单一因素对污泥颗粒化过程的影响, 运行14 d, HRT为4 h的反应器, MLSS从2 g·L-1增加到3.6 g·L-1, 较短的HRT有利于污泥增殖.Rosman等[12]和Pan等[13]均证实了较短的HRT条件下形成的颗粒污泥结构密实, 形状规则, 具有较好的沉降性能.本研究自养亚硝化颗粒污泥中AOB、NOB属于慢速生长微生物, 较短的HRT, 提高了水力选择压, 有利于微生物增殖, 且使污泥颗粒粒径分布更加均匀.
EPS对颗粒污泥的形成和稳定性具有显著影响[19, 20], 微生物细胞产生EPS, 形成交联的网络, 并进一步加强颗粒的完整性使得颗粒结构更加密实.本研究发现(图 4), 缩短HRT, EPS总量逐渐升高, 蛋白质和多糖都有所提高, 蛋白质的增幅略高于多糖, 符合成熟亚硝化颗粒污泥典型的EPS分布特征[21].EPS中的蛋白质比多糖具有更丰富的静电键与金属架桥, 有利于污泥结构的稳定.胞外蛋白质富含各类降解酶, 包埋于EPS中的微生物可降解特定污染物[22].较短的HRT, 提高颗粒污泥水力剪切力, 促使微生物分泌更多的胞外聚合物(EPS), 有利于提升微生物活性和颗粒物稳定性.这一现象可进一步解释在低HRT条件下, 反应器具有良好微生物截留性能, 较高的污泥增殖速率的原因.
2.2 HRT对氮转化效能的影响
HRT不断缩短过程中, 亚硝化颗粒污泥反应器的整体运行状况如图 5所示.随着HRT降低, 氨氮去除率呈阶梯式增长最终稳定在99%左右.其中HRT为2 h时, 氨氮去除率出现较为明显的波动, 出水亚硝酸盐浓度略有波动.HRT对微生物群落结构和反应器性能会产生影响[23].缩短HRT, 促进污泥增殖, 使颗粒污泥粒径分布更加均匀.对于连续流反应器, HRT是重要参数, 过高的HRT会导致反应器处理效率降低, 而缩短HRT, 易加剧污泥流失.本研究在HRT为1 h的条件下, 系统仍具有较高的脱氮性能, 这与颗粒污泥良好的沉降性能密不可分.
有研究发现, 随着HRT降低, 反应器的硝化性能下降[23], 而本研究整个运行过程中亚硝酸盐累积率始终保持在85%以上(图 5), 随着HRT不断下降, 氨氮去除率逐步增长, 出水硝态氮浓度逐渐降低至10 mg·L-1左右.本研究控制氮容积负荷不变, 进水氨氮浓度随着HRT缩短而下降(表 1), 污泥氮负荷进一步下降.系统中微生物处于低负荷运行, 污泥活性增强, 氮去除效率提高.通过逐渐缩短HRT的方式, 降低污泥沉降时间, 将沉降性能较差的絮状污泥逐渐从反应器内淘洗出去, 污泥龄(SRT)缩短, 起到淘洗NOB的作用[4].本研究缩短HRT成为有效抑制NOB、维持颗粒污泥稳定亚硝化性能的有效因素.笔者认为可能存在以下3个原因:①研究所用接种污泥具有良好的亚硝化效果, 保证了反应器中较高的AOB和较低的NOB数量;②在自适应条件下, 缩短HRT增加了水力选择压, 颗粒污泥粒径分布集中于0.3~0.8 mm, 有利于优化基质和DO的传质条件, 提高AOB的活性, 抑制NOB;③由于颗粒污泥中不同功能微生物呈层状分布, AOB通常分布在颗粒的外层, 有利于获得更好的基质和生长条件, 相对于NOB, 更易在颗粒化污泥中成为优势种群[24, 25].
2.3 HRT对功能微生物动力学活性的影响
HRT对CSTR中亚硝化颗粒污泥的粒径分布产生了较大影响, HRT为1 h, 反应器中污泥粒径集中于0.3 mm~0.8 mm.颗粒污泥粒径的差异, 将直接影响反应器性能.
本研究对不同HRT稳定运行条件下, 粒径小于0.8 mm和大于0.8 mm的两大类污泥中功能微生物AOB和NOB的活性进行分析, 氨氮比降解速率μ(NH4+-N)、亚硝酸盐比生成速率μ(NO2--N)和硝酸盐比生成速率μ(NO3--N)测定结果见表 2.
表 2
(Table 2)

表 2 不同HRT条件下CSTR中大小颗粒污泥功能微生物活性对比
Table 2 Comparison of sludge activity at various HRT in CSTR
污泥粒径
/mm |
功能微生物活性
/mg·(g·h)-1 |
HRT/h |
| 4 |
2 |
1 |
|
| μ(NH4+-N) |
13.3 |
16.3 |
22.0 |
| >0.8 |
μ(NO2--N) |
12.9 |
16.0 |
20.9 |
|
| μ(NO3--N) |
0.7 |
1.0 |
1.9 |
|
| μ(NH4+-N) |
35.2 |
31.6 |
24.7 |
| < 0.8 |
μ(NO2--N) |
30.6 |
30.1 |
23.2 |
|
| μ(NO3--N) |
3.6 |
3.4 |
1.9
|
|
表 2 不同HRT条件下CSTR中大小颗粒污泥功能微生物活性对比
Table 2 Comparison of sludge activity at various HRT in CSTR
|
结果发现, 粒径 < 0.8 mm的颗粒污泥, 氨氮比降解速率和亚硝酸盐比生成速率、硝酸盐比生成速率均高于粒径>0.8 mm的颗粒污泥, 说明粒径较小颗粒污泥中AOB和NOB均具有更高的活性.因此, 在HRT缩短过程中, 0.3~0.8 mm的颗粒比例逐渐提升, 反应器亚硝化性能也得以提升.不同粒径污泥中功能微生物的活性受HRT的影响完全不同.粒径>0.8 mm的颗粒污泥, 缩短HRT, AOB和NOB功能微生物的活性都逐渐提升;与之相反, 粒径 < 0.8 mm的颗粒污泥, 缩短HRT, AOB和NOB功能微生物的活性都有所下降.在本研究中, 两种效果叠加, 缩短HRT, NOB在竞争基质和DO时处于劣势, 硝酸盐比生成速率总体下降, 证实了较低的HRT对NOB有较好的抑制作用, 这一结果与运行数据HRT缩短, 硝酸盐生成量减少的情况吻合.
粒径相对较小颗粒污泥, 既具有颗粒污泥沉降性能好、生物富集度高的优势, 又具有相对较大的比表面积, 有利于富集在颗粒污泥表面的优势微生物生长代谢.在实际工程运用中, 可根据主导颗粒污泥粒径分布调控合理的HRT, 提高系统效能.
2.4 高通量测序结果分析
图 6为CSTR系统在HRT为4 h和1 h稳定运行条件下, 污泥测序在门水平下微生物群落多样性分析结果, 主要包括变形菌门(Proteobacteria)、拟杆菌门(Bacteroidetes)、绿菌门(Chlorobi)、绿弯菌门(Chloroflexi)、浮霉菌门(Planctomycets).涉及到脱氮功能微生物的变形菌门占绝对优势, 超80%.HRT从4 h缩短至1 h, 变形菌门比例略有升高.系统中出现厌氧氨氧化菌所在的浮霉菌门, HRT缩短后, 这类微生物的比例略有下降.
为了进一步阐明HRT对CSRT污泥微生物种群变化影响, 对属水平样品功能微生物和优势微生物菌群进行分析.如图 7所示, 亚硝化单胞菌属(Nitrosomomas)在CSTR污泥微生物群落中占绝对优势.亚硝化单胞菌属(Nitrosomomas)是典型的AOB[26], 在本系统污泥中富集度高达56%以上.短程硝化技术实现的关键在于亚硝酸盐的积累[27], 也就是通过富集污泥中的AOB, 并控制AOB和NOB的数量与活性平衡, 在硝化过程中实现亚硝酸盐的稳定积累.高通量微生物测序结果表明, 优势微生物Nitrosomomos的高度富集度, 也进一步解释系统具有良好的氨氧化性能和亚硝酸盐积累率.缩短HRT, Nitrosomomos丰度提高3%左右, 与系统脱氮性能提升结果吻合.尽管维持容积负荷不变, HRT从4 h到1 h, AOB绝对优势不变, 微生物门类一致, 但微生物种类和丰度发生变化, 有利于颗粒污泥中微生物的自平衡, 提升污泥自适应性能.
3 结论
(1) HRT从4 h缩短至1 h, CSTR中颗粒污泥粒径分布发生显著变化.随着HRT缩短, 粒径 < 0.3 mm和粒径>1.6 mm颗粒的质量分数分别由17%和75%逐渐下降至5%和36%, HRT为1 h时, 粒径为0.3~0.8 mm颗粒占比约达50%.
(2) 缩短HRT, CSRT中亚硝化颗粒污泥性能稳定, 亚硝酸盐累积率稳定在85%以上, HRT缩短至1 h, 氨氮的去除率提高到99%.整个运行过程中, 颗粒结构更加密实, 无颗粒解体现象, MLSS由5.2g·L-1上升至15g·L-1.
(3) 粒径 < 0.8 mm的颗粒, 氨氮比降解速率和亚硝酸盐比生成速率、硝酸盐比生成速率均高于粒径>0.8 mm的颗粒污泥.缩短HRT有利于大颗粒功能微生物活性提升, 在较长的HRT条件下, 粒径 < 0.8 mm的颗粒污泥活性更高.
(4) 系统中变形菌门(Proteobacteria)占绝对优势, 亚硝化单胞菌属(Nitrosomomas)为代表的AOB在系统污泥中富集度高达56%以上, 缩短HRT有利于AOB的富集.
 2020, Vol. 41
2020, Vol. 41