2. 福建省农村污水处理与用水安全工程研究中心, 厦门理工学院水资源环境研究所, 厦门 361005
2. Fujian Engineering and Research Center of Rural Sewage Treatment and Water Safety, Water Resources and Environmental Institute, Xiamen University of Technology, Xiamen 361005, China
人工甜味剂(artificial sweeteners), 又名低热量甜味剂或非营养性甜味剂, 常作为添加剂用于食品、饮料、饲料、药品及个人护理品, 因其高甜度低热量的特点, 深受糖尿病、龋齿、肥胖患者及减肥人群的欢迎[1, 2].全球允许使用的人工甜味剂常见的有安赛蜜(acesulfame, ACE)、三氯蔗糖(sucralose, SUC)、糖精(saccharin, SAC)、甜蜜素(cyclamate, CYC)、阿斯巴甜(aspartame, ASP)和纽甜(neotame, NEO)等.ACE与SUC因其突出的稳定性与持久性, 常作为示踪剂揭示地下水等是否受到人为因素的污染[3, 4].
据报道2012年全球大约消耗人工甜味剂11.7万t[5], 中国也逐渐成为亚太地区人工甜味剂的主要消费国与生产国[2].大部分的人工甜味剂在生物体内几乎不被代谢吸收, 会以母体形式随排泄物大量进入污水系统[6], 部分稳定性极高的甜味剂甚至穿透污水处理系统进入环境水体甚至饮用水中[7, 8].欧洲、北美洲和亚洲的近20个国家的调查研究表明人工甜味剂普遍存在于污水及地表水中, 最高浓度可达几百μg·L-1[4, 9~12];污水处理工艺对SAC、CYC、ASP和NEO有较好的处理效果, 但对SUC和ACE去除效果不佳[13, 14].地表水中的人工甜味剂主要来源于生活污水、工业废水及面源污染.人工甜味剂排入受纳水体后, 稀释和扩散等作用使其浓度略低于污水处理系统[12, 15], 欧洲国家的河流中检出SUC, 浓度高达1 μg·L-1[16].人工甜味剂可经由下渗等过程进入地下水中, 天津市某地下水中检出了ACE、SAC、CYC与SUC, 浓度范围在6.10~80ng·L-1, SAC和ACE的浓度较高, SUC最低[12].加拿大地下水中检出浓度相对国内高, ACE和SUC的最高浓度超过20 μg·L-1[3].饮用水处理系统中人工甜味剂的相关研究不多, Scheurer等[17]的研究发现德国6个水厂均可检测到ACE, 浓度高达2μg·L-1.Buerge等[4]在瑞士某水厂的调查发现水源中ACE浓度在1.1~2.6 μg·L-1之间, 臭氧处理后, 末端管中ACE的浓度降至0.02~0.07μg·L-1.本课题组于浙江省某市饮用水处理及管网自来水中检出微量SUC, 浓度范围为0.11~0.75 μg·L-1[18], 发现水处理工艺对人工甜味剂控制能力有限, 饮用水水质可能受到人工甜味剂的影响.
毒理学研究表明人工甜味剂在控制剂量下使用风险很低[19], 但近期有研究证实甜味剂的长期摄入可能对动物产生不良后果.ACE会降低脑补血糖并极大影响小鼠的短期记忆与认知功能[20].SUC可能会改变小鼠和人类肠道内菌群, 造成葡萄糖不耐受, 增加糖尿病的发病风险[21], 中等剂量的SAC可能诱导小鼠睡眠障碍[22], 过量的ASP摄入可能参与某些精神障碍的发病机制(DSM-IV-TR 2000)以及影响学习和情绪功能[23].饮用水是人们摄入人工甜味剂途径之一, 人工甜味剂在水环境尤其是水源及饮水环境中的分布及含量调查对于掌握污染基础信息, 评价其健康风险等具有科学意义.
本文通过优化固相萃取-高效液相色谱法(solid phase extraction-high performance liquid chromatography, SPE-HPLC), 以浙江省的污水处理、饮用水处理及供水系统为目标, 在国内首次针对不同水环境展开了中人工甜味剂调查, 获取污染状况基础数据, 并评价常规及深度水处理工艺对水源中微量人工甜味剂的控制能力, 以期为后续污染控制的工艺选择等深入研究提供数据支撑.
1 材料与方法 1.1 样品采集与保存于2017年8月~2018年11月在浙江省境H1市和H2市的污水、饮用水处理及供水系统中选点取样.H1市QT、JX、NX和XF这4座自来水厂分别以QT江和DT为水源.H2市的TH、CX两座自来水厂分别以T湖XT溪与LHT水库为水源.BL污水厂位于H2市.供水管网样品采自QT路和DSZ路每隔800 m建筑内水龙头, 为QT水厂供出.在水源、水厂各处理工艺段以及不同管网点采集的水样保存于4℃棕色玻璃瓶中, 并于48 h内处理分析, 预处理前经0.45 μm的滤膜过滤.
1.2 试剂与材料4种人工甜味剂标准品ACE(98%)、SAC(>99%)、ASP(98%)与NEO(>99%)购于阿拉丁生化科技股份有限公司(中国);HPLC级甲醇、乙腈购自CNW(德国);所需溶液均由超纯水配制.
试验用预处理及分析仪器包括SHIMADZU LC20A高效液相色谱(含四元泵, 自动进样器, 紫外检测器, 柱温箱)配InertsilODS-3液相色谱柱(4.6×150 mm, 5 μm, SHIMADZU, 日本);N-EVAP-111型氮吹仪(美国ORGANOMATION公司);BS124S型电子精密分析天平(赛多利斯科学仪器有限公司);UPHW1-90T型纯水机/超纯水制造系统(北京优普时代科技有限公司);Visipre TM SPE 12孔型固相萃取装置(美国SUPECLO公司);Poly-SeryC18柱、SeryPWAX柱、Poly-SeryHLB柱(60 mg/3 mL, 德国CNW科技公司产品).
1.3 样品前处理采用固相萃取对水样进行富集与提纯, 其中C18小柱作为除杂柱与HLB或PWAX小柱串联.用6 mL甲醇活化萃取柱, 6 mL纯水平衡(PWAX柱用pH为4, 浓度为25 mmol·L-1的醋酸铵溶液平衡), 1 L水样过柱, 流速为3 mL·min-1, 真空抽干2 min, 用6 mL甲醇溶液缓慢淋洗小柱(每次3 mL, 真空抽干2 min).收集洗脱液, 氮气吹干, 用1 mL纯水定容, 并用HPLC分析.
1.4 样品分析方法采用液相色谱对4种人工甜味剂进行定量分析, 流动相A为20 mmol·L-1的硫酸铵溶液, 流动相B为乙腈.检测波长为200 nm, 色谱柱采用Inertsil ODS-3柱(4.6×150 mm, 5 μm, 岛津, 日本), 柱温40℃, 流速1 mL·min-1, 进样量80 μL.梯度洗脱程序为0~2 min, 95%A, 5%B; 2~30 min, 50%A, 50%B; 30~40 min, 95%A, 5%B.
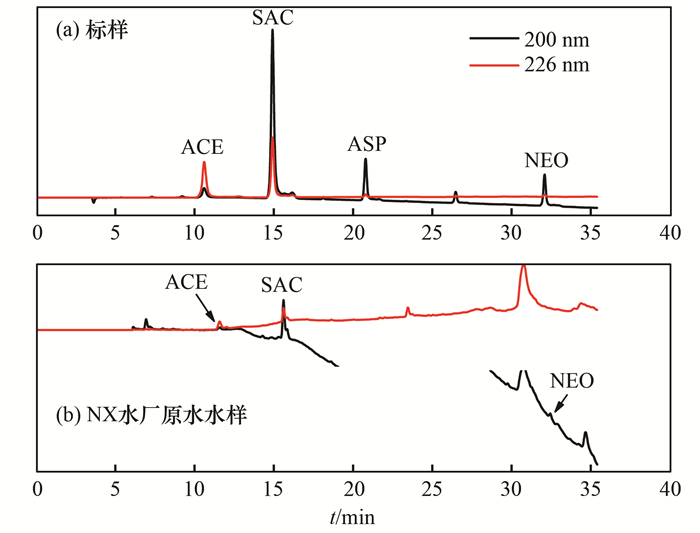
2 结果与讨论 2.1 SPE-HPLC测定人工甜味剂的优化利用SPE-HPLC法对4种人工甜味剂进行测定, 选择在200 nm和226 nm进行定量分析, 并进行比较, 液相色谱图如图 1所示.
|
图 1 4种人工甜味剂的双波长色谱图 Fig. 1 Dual-wavelength chromatograms of four artificial sweeteners |
由图 1可见, 4种人工甜味剂在反相柱中实现良好分离, ACE于226 nm波长处的响应高于200 nm, 其余3种甜味剂在200 nm处的响应明显优于226 nm, 两个波长下的响应值差异也作为在复杂水样中定性甜味剂峰的辅助手段.用外标法分别对其进行定量, 线性范围为0.5~100 mg·L-1, 线性相关系数均高于0.999 7, 除ASP外其余3种人工甜味剂方法的相对标准偏差均小于6%.方法检测限为3倍信噪比, 定量限为10倍信噪比, ACE、SAC、ASP和NEO的检测限为57、120、170和47μg·L-1, 定量限分别为190、400、567和157μg·L-1.
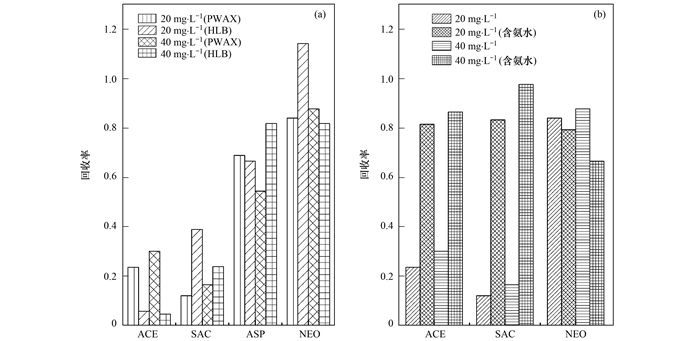
2.2 方法优化与有效性4种人工甜味剂SPE预处理方法的有效性由目标物加标回收率进行评价.甜味剂加标浓度为20 mg·L-1和40 mg·L-1, 分别采用HLB与PWAX两种吸附柱经过柱吸附、洗脱、吹干和定容, 测定浓度, 计算回收率, 结果如图 2(a)所示.
|
(a)HLB与PWAX两种填料对比; (b)PWAX柱改良洗脱对3种ACE、SAC与NEO种甜味剂回收率优化 图 2 人工甜味剂固相萃取纯水加标回收率 Fig. 2 Solid phase extraction recoveries of artificial sweeteners spiked in pure water |
4种人工甜味剂中, 两种填料对ASP和NEO的回收率较为理想, ASP为70.0%左右, NEO的回收率在80.0%以上.ACE和SAC的回收率都低于40.0%, 与Arbeláez[11]和Gan[24]的研究结果相符, 可能是由于填料对ACE和SAC的强吸附性或不合适的洗脱剂影响了回收率.HLB对ACE的回收效果不理想, 为提高ACE的回收率, 对PWAX柱的固相萃取方法进行优化.优化方法为甲醇中加入2.0%的氨水作为洗脱液, 对PWAX小柱进行洗脱, ACE、SAC和NEO回收率的对比结果如图 2(b).优化后20 mg·L-1与40 mg·L-1浓度下ACE与SAC回收率提高, 均超过80.0%.
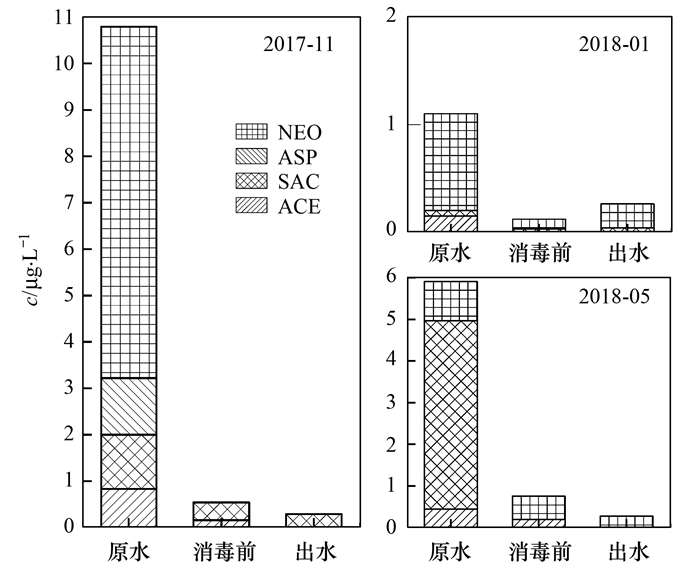
2.3 人工甜味剂在污水处理系统中的分布H2市BL污水厂为小型生活污水处理系统, 采用序批式活性污泥法(SBR)处理工艺.采集水厂原水、生物处理出水及消毒后出水进行分析, 污水处理系统中甜味剂浓度变化如图 3.
|
图 3 4种人工甜味剂在BL污水厂中的浓度分布 Fig. 3 Concentration distribution of four artificial sweeteners in BL wastewater treatment plant |
原水中ACE、SAC和NEO的检出率为100.0%, ASP仅在2017年11月污水原水中检出, 浓度为1.22μg·L-1, 且低于其它人工甜味剂, 因其易被生物降解, 在pH值高于5时发生环化反应[25~27].调查期间, ACE的最高浓度为0.85μg·L-1, 最小浓度为0.15μg·L-1(低于定量限), SAC的检出范围为ND~4.52μg·L-1, NEO的检出范围为ND~7.57μg·L-1.
污水处理系统中人工甜味剂均有不同程度的减少, ASP在工艺阶段基本被去除, NEO的去除率超过70.0%, 与研究报道类似[28].ACE在生物处理工艺段去除率为54.9%~80.2%, 与污水处理工艺对ACE的去除效果报道(去除率10%~40%)相比略高[12], ACE在污水系统中的减量受微生物活性影响较大, 因而波动较大[5].此外, ACE可光解, 可被氯氧化, 因此污水出水中ACE普遍低于检测限[29, 30].污水处理系统对SAC的控制效果也十分明显, 去除率最高可达100.0%, 冬季低于春夏, 可能冬季温度较低, 生物活性低导致.
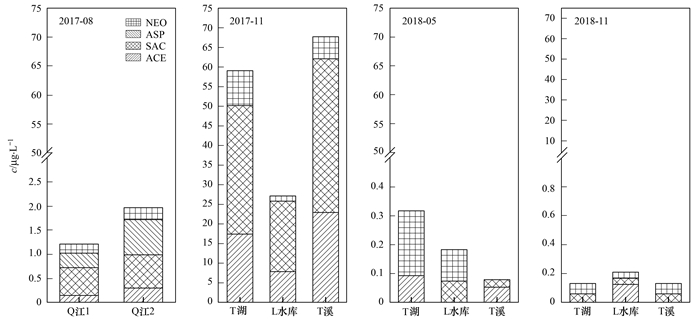
2.4 人工甜味剂在饮用水处理及供水系统中的分布 2.4.1 水源环境中的人工甜味剂水源环境中ACE、SAC与NEO的检出率较高, 其中SAC浓度较高, ASP由于其不稳定性, 易分解, 检出率较低, 4种人工甜味剂在水源中的分布情况如图 4所示.
|
图 4 4种人工甜味剂在水源水中的分布 Fig. 4 Distribution of four artificial sweeteners in source waters |
Q江水系为H1市的主要饮用水水源, 2017年8月ACE、SAC、ASP和NEO的检出浓度分别为0.15~0.30、0.58~0.69、0.30~0.73和0.19~0.25μg·L-1, SAC浓度最高, NEO浓度最低.
T湖、L水库和T溪水源水中4种甜味剂均有检出.T湖及T溪内浓度较高, L水库污染相对较轻.SAC的检出率较高, 2017年11月3种原水水源的检出浓度范围为17.94~39.17 μg·L-1, 且该月水样所有检出甜味剂的浓度均超过1 μg·L-1, 其原因尚不知, 可能为点源、面源污染的大量排入. 2018年5月与11月中ACE的检出范围为ND~0.13 μg·L-1, SAC为LOD~0.07 μg·L-1, NEO为ND~0.22 μg·L-1, 未检测出ASP.
2.4.2 饮用水处理工艺中人工甜味剂的变化CX水厂以T溪与L水库的混合水为原水, 处理工艺采用常规混凝、沉淀、过滤和消毒工艺, 不同工艺段4种人工甜味剂含量如表 1所示.
|
|
表 1 CX水厂各工艺段4种人工甜味剂的含量1)/μg·L-1 Table 1 Occurrence of four artificial sweeteners in each process sections of CX waterwork/μg·L-1 |
由表 1可见, 经过常规水处理工艺后, ACE、SAC和NEO浓度均有不同程度降低.与Scheurer等[1]的报道类似, SAC在混凝沉淀与过滤阶段大幅减少, ACE也有一定程度的减少, 可能与混凝携带、滤料表面的微生物等有关.消毒阶段部分人工甜味剂可被氧化去除, 浓度降低同时能生成一定量消毒副产物[30, 31].
TH水厂以T湖为原水, 处理工艺为预臭氧、絮凝、沉淀、砂滤、后臭氧、活性炭滤池和氯消毒, 2017年12月和2018年5月、11月不同工艺段内4种人工甜味剂的浓度变化如图 5所示.
|
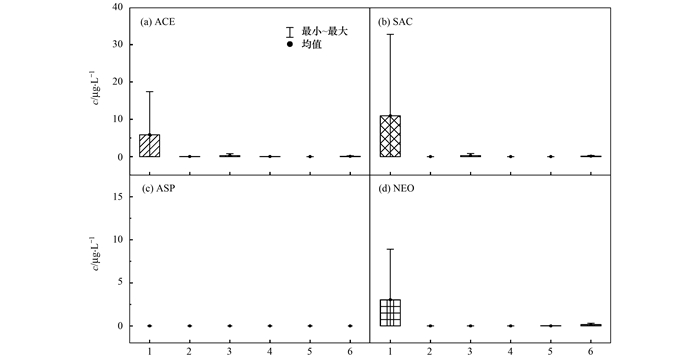
1.原水; 2.预臭氧出水; 3.砂滤池出水; 4.后臭氧出水; 5.活性炭滤池出水; 6.出水 图 5 4种人工甜味剂在TH水厂深度处理工艺中的变化 Fig. 5 Variation of four artificial sweeteners in the advanced treatment process of TH water plants |
饮用水处理系统中, ACE、SAC和NEO的检出率为38.9%、27.8%和33.3%, ASP极易分解, 浓度低于检测限.预臭氧工艺去除了水中大部分人工甜味剂, 对ACE、SAC和NEO的去除率为67.7%~100.0%, 深度处理工艺对ACE、SAC和NEO的去除率为73.7%~100.0%.Soh等[32]的研究证明, ACE在5 min之内可被高浓度(100倍浓度)臭氧完全降解, ACE、SAC与NEO均具有不饱和碳碳键, 可被臭氧分子氧化.絮凝、沉淀和砂滤在一定程度上去除了水体中部分杂质, 使得目标甜味剂更容易被富集, 所以能在滤池出水中检测到人工甜味剂的存在.经过氯消毒, 水厂出水中的人工甜味剂含量极低, 可被余氯氧化.Li等[30]的研究发现ACE氯消毒后会产生几种受管制的消毒副产物, 对饮用水安全产生一定的威胁.
2.4.3 人工甜味剂在供水系统中的分布供水管网采样点中4种人工甜味剂均未检出, 可见饮用水暂未受到4种目标甜味剂污染.
3 结论(1) 优化SPE-HPLC法可实现水环境中微量人工甜味剂的准确测定, 4种甜味剂安赛蜜、糖精、阿斯巴甜和纽甜回收率可满足分析需求, 检测限为57、120、170和47 μg·L-1, 定量限分别为190、400、567和157 μg·L-1.
(2) 生活污水处理系统、地表水源及饮用水处理系统中4种目标甜味剂均有检出, 污水中的检出率及浓度普遍高于地表水.污水及饮用水处理系统可实现ACE、SAC、ASP和NEO等人工甜味剂的减量化, 供水管网中未检出目标人工甜味剂.
(3) 饮用水处理系统中可能存在甜味剂的转化, 尽管供水管网中未检出, 但其可能衍生臭氧降解产物、消毒副产物及其影响等需深入探讨.
| [1] | Scheurer M, Brauch H J, Lange F T. Analysis and occurrence of seven artificial sweeteners in German waste water and surface water and in soil aquifer treatment (SAT)[J]. Analytical and Bioanalytical Chemistry, 2009, 394(6): 1585-1594. DOI:10.1007/s00216-009-2881-y |
| [2] | Sylvetsky A C, Jin Y C, Clark E J, et al. Consumption of low-calorie sweeteners among children and adults in the United States[J]. Journal of the Academy of Nutrition and Dietetics, 2017, 117(3): 441-448. DOI:10.1016/j.jand.2016.11.004 |
| [3] | Van Stempvoort D R, Roy J W, Brown S J, et al. Artificial sweeteners as potential tracers in groundwater in urban environments[J]. Journal of Hydrology, 2011, 401(1-2): 126-133. DOI:10.1016/j.jhydrol.2011.02.013 |
| [4] | Buerge I J, Buser H R, Kahle M, et al. Ubiquitous occurrence of the artificial sweetener acesulfame in the aquatic environment:an ideal chemical marker of domestic wastewater in groundwater[J]. Environmental Science & Technology, 2009, 43(12): 4381-4385. |
| [5] | Castronovo S, Wick A, Scheurer M, et al. Biodegradation of the artificial sweetener acesulfame in biological wastewater treatment and sandfilters[J]. Water Research, 2017, 110: 342-353. DOI:10.1016/j.watres.2016.11.041 |
| [6] |
冯碧婷, 干志伟, 胡宏伟, 等. 人工甜味剂环境行为研究进展[J]. 环境化学, 2013, 32(7): 1158-1167. Feng B T, Gan Z W, Hu H W, et al. Research progress on the environmental behavior of artificial sweeteners[J]. Environmental Chemistry, 2013, 32(7): 1158-1167. |
| [7] | Xu Y, Lin Z Y, Wang Y, et al. The UV/peroxymonosulfate process for the mineralization of artificial sweetener sucralose[J]. Chemical Engineering Journal, 2017, 317: 561-569. DOI:10.1016/j.cej.2017.02.058 |
| [8] | Toth J E, Rickman K A, Venter A R, et al. Reaction kinetics and efficiencies for the hydroxyl and sulfate radical based oxidation of artificial sweeteners in water[J]. The Journal of Physical Chemistry A, 2012, 116(40): 9819-9824. DOI:10.1021/jp3047246 |
| [9] | Ordoñez E Y, Quintana J B, Rodil R, et al. Determination of artificial sweeteners in sewage sludge samples using pressurised liquid extraction and liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A, 2013, 1320: 10-16. DOI:10.1016/j.chroma.2013.10.049 |
| [10] | Spoelstra J, Schiff S L, Brown S J. Artificial sweeteners in a large Canadian river reflect human consumption in the watershed[J]. PLoS One, 2013, 8(12): e82706. DOI:10.1371/journal.pone.0082706 |
| [11] | Arbeláez P, Borrull F, Pocurull E, et al. Determination of high-intensity sweeteners in river water and wastewater by solid-phase extraction and liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A, 2015, 1393: 106-114. DOI:10.1016/j.chroma.2015.03.035 |
| [12] | Gan ZW, Sun HW, Feng BT, et al. Occurrence of seven artificial sweeteners in the aquatic environment and precipitation of Tianjin, China[J]. Water Research, 2013, 47(14): 4928-4937. DOI:10.1016/j.watres.2013.05.038 |
| [13] | Tran N H, Nguyen V T, Urase T, et al. Role of nitrification in the biodegradation of selected artificial sweetening agents in biological wastewater treatment process[J]. Bioresource Technology, 2014, 161: 40-46. DOI:10.1016/j.biortech.2014.02.116 |
| [14] | Tran N H, Gan J, Nguyen V T, et al. Sorption and biodegradation of artificial sweeteners in activated sludge processes[J]. Bioresource Technology, 2015, 197: 329-338. DOI:10.1016/j.biortech.2015.08.083 |
| [15] | Sang Z Y, Jiang Y N, Tsoi Y K, et al. Evaluating the environmental impact of artificial sweeteners:A study of their distributions, photodegradation and toxicities[J]. Water Research, 2014, 52: 260-274. DOI:10.1016/j.watres.2013.11.002 |
| [16] | Loos R, Gawlik B M, Boettcher K, et al. Sucralose screening in European surface waters using a solid-phase extraction-liquid chromatography-triple quadrupole mass spectrometry method[J]. Journal of Chromatography A, 2009, 1216(7): 1126-1131. DOI:10.1016/j.chroma.2008.12.048 |
| [17] | Scheurer M, Storck F R, Brauch H J, et al. Performance of conventional multi-barrier drinking water treatment plants for the removal of four artificial sweeteners[J]. Water Research, 2010, 44(12): 3573-3584. DOI:10.1016/j.watres.2010.04.005 |
| [18] |
朱世翠, 陆思嘉, 宋亚丽, 等. 典型饮水系统中人工甜味剂三氯蔗糖的调查[J]. 浙江大学学报(工学版), 2019, 53(11): 2197-2205. Zhu S C, Lu S J, Song Y L, et al. Investigation of artificial sweetener sucralose in typical drinking water systems[J]. Journal of Zhejiang University (Engineering Science), 2019, 53(11): 2197-2205. |
| [19] | Chattopadhyay S, Raychaudhuri U, Chakraborty R. Artificial sweeteners-a review[J]. Journal of Food Science and Technology, 2014, 51(4): 611-621. DOI:10.1007/s13197-011-0571-1 |
| [20] | Ibi D, Suzuki F, Hiramatsu M. Effect of AceK (acesulfame potassium) on brain function under dietary restriction in mice[J]. Physiology & Behavior, 2018, 188: 291-297. |
| [21] | Suez J, Korem T, Zeevi D, et al. Artificial sweeteners induce glucose intolerance by altering the gut microbiota[J]. Nature, 2014, 514(7521): 181-186. DOI:10.1038/nature13793 |
| [22] | Oishi K, Higo-Yamamoto S, Yasumoto Y. Moderately high doses of the artificial sweetener saccharin potentially induce sleep disorders in mice[J]. Nutrition, 2016, 32(10): 1159-1161. DOI:10.1016/j.nut.2016.03.013 |
| [23] | Humphries P, Pretorius E, Naudé H. Direct and indirect cellular effects of aspartame on the brain[J]. European Journal of Clinical Nutrition, 2008, 62(4): 451-462. DOI:10.1038/sj.ejcn.1602866 |
| [24] | Gan Z W, Sun H W, Wang R N, et al. A novel solid-phase extraction for the concentration of sweeteners in water and analysis by ion-pair liquid chromatography-triple quadrupole mass spectrometry[J]. Journal of Chromatography A, 2013, 1274: 87-96. DOI:10.1016/j.chroma.2012.11.081 |
| [25] | Berset J D, Ochsenbein N. Stability considerations of aspartame in the direct analysis of artificial sweeteners in water samples using high-performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS)[J]. Chemosphere, 2012, 88(5): 563-569. DOI:10.1016/j.chemosphere.2012.03.030 |
| [26] | Tran N H, Hu JY, Ong S L. Simultaneous determination of PPCPs, EDCs, and artificial sweeteners in environmental water samples using a single-step SPE coupled with HPLC-MS/MS and isotope dilution[J]. Talanta, 2013, 113: 82-92. DOI:10.1016/j.talanta.2013.03.072 |
| [27] | Baena-Nogueras R M, Traverso-Soto J M, Biel-Maeso M, et al. Sources and trends of artificial sweeteners in coastal waters in the bay of Cadiz (NE Atlantic)[J]. Marine Pollution Bulletin, 2018, 135: 607-616. DOI:10.1016/j.marpolbul.2018.07.069 |
| [28] | Subedi B, Kannan K. Fate of artificial sweeteners in wastewater treatment plants in New York State, U.S.A[J]. Environmental Science & Technology, 2014, 48(23): 13668-13674. |
| [29] |
干志伟.人工甜味剂在环境中的分布、迁移转化及光降解机理研究[D].天津: 南开大学, 2014. Gan Z W. Distribution, fate, and photolysis mechanism of artificial sweeteners in environment[D]. Tianjing: Nankai University, 2014. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2755792 |
| [30] | Li A J, Wu P R, Law J C F, et al. Transformation of acesulfame in chlorination:kinetics study, identification of byproducts, and toxicity assessment[J]. Water Research, 2017, 117: 157-166. DOI:10.1016/j.watres.2017.03.053 |
| [31] | Prescott M, Krasner S W, Guo Y C. Estimation of NDMA precursor loading in source water via artificial sweetener monitoring[J]. Journal-American Water Works Association, 2017, 109(6): E243-E251. |
| [32] | Soh L, Connors K A, Brooks B W, et al. Fate of sucralose through environmental and water treatment processes and impact on plant indicator species[J]. Environmental Science & Technology, 2011, 45(4): 1363-1369. |
 2020, Vol. 41
2020, Vol. 41


