缓流水体的富营养化已成为当前全世界所面临的一个严重水环境问题[1, 2].磷是一种会引起缓流水体富营养化的关键营养元素[1, 2].因此, 控制水中磷的浓度水平对于缓流水体的富营养化控制至关重要.水体中磷的来源分外源和内源.当外源磷输入得到有效控制时, 底泥内源磷释放的控制就成为了水体中磷浓度水平削减的关键[2, 3].鉴于此, 人们已经开发了许多水体内源磷释放控制技术, 包括底泥疏浚[4]、铝盐钝化[5]、硝酸钙注射[6]、曝气供氧[7]、惰性覆盖[8]和活性覆盖[9~22]等.其中, 活性覆盖技术, 即将钝磷能力卓越的固体吸附剂材料投加到底泥-水界面上方形成一层覆盖层以达到拦截水体内源磷释放的目的, 近年来已引起了国内外学者的广泛关注, 极具应用前景[9~22].
应用活性覆盖技术控制水体内源磷释放的一个关键问题是要寻找到安全、高效且经济的活性覆盖材料.为此, 近年来许多吸附剂材料已经被开发出来作为活性覆盖材料用于水体内源磷释放的控制, 具体包括:方解石[9~12]、沸石[13]、膨润土[14]、镧改性黏土[15]、镧改性沸石[16]、铝改性沸石[17]、锆改性沸石[18~20]、热改性凹凸棒土[21]和铁铝污泥[22]等.方解石的化学成分主要为碳酸钙(CaCO3), 是晶型属三方晶系的碳酸盐矿物, 不仅来源广泛、价格低廉、对环境友好, 而且对水中的磷酸盐具有良好的钝化能力, 将其作为活性覆盖材料预计应用前景较为广阔[9~12].但是, 方解石活性覆盖系统控制水体内源磷释放的效率仍然有待进一步提高[11, 12].铁氧化物同样是一种来源广泛、环境友好的材料, 并且其对水中的磷酸盐具有卓越的吸附能力[23].如果采用铁氧化物对方解石进行改性, 所获得的铁改性方解石预计对水中磷酸盐的去除能力会强于未改性的方解石, 可能比原始方解石更适合作为一种底泥活性覆盖材料用于水体内源磷释放的控制.然而, 目前国内外关于铁改性方解石覆盖控制底泥内源磷释放的研究尚鲜见报道.
本文的主要研究目的就是要确定铁改性方解石活性覆盖控制水体内源磷释放的效率.为达到这一目的, 本文首先制备了一种铁改性方解石, 并采用X射线衍射(XRD)仪和X射线荧光光谱(XRF)仪对其进行表征, 然后通过批量实验考察了其对水中磷酸盐的去除性能, 再通过底泥培养实验对比分析了原始和铁改性方解石覆盖对上覆水中溶解性活性磷(SRP)和底泥磷形态的影响, 最后采用磷形态连续提取分析法和生物可利用性磷分析法评估了原始和铁改性方解石覆盖层中磷的稳定性, 以期为应用铁改性方解石作为活性覆盖材料控制水体内源磷释放提供科学依据.
1 材料与方法 1.1 实验材料本实验所用的底泥取自上海市浦东新区的一条景观河道, 所采集的底泥经自然风干、破碎和过100目筛后备用.实验中所用的方解石购自于浙江省长兴县的工厂, 实验所用的FeCl3·6H2O、KH2PO4、Na2S2O4、NaHCO3、HCl、NH4Cl、NaOH、H2SO4、抗坏血酸和钼酸铵等化学试剂均购自中国国药集团化学试剂有限公司, 均为分析纯.本实验中的用水均为去离子水.采用KH2PO4和去离子水配制磷酸盐储备液, 再通过稀释的方式获得磷酸盐使用液.磷酸盐使用液的浓度均以元素磷计.
1.2 材料制备和表征铁改性方解石的制备过程为:称取20 g过200目筛的方解石粉末放入500 mL锥形瓶中, 并向该锥形瓶中加入5 g FeCl3·6H2O, 再向该锥形瓶中加入100 mL去离子水并摇匀; 接着, 将该锥形瓶置于磁力搅拌器上, 用1 mol·L-1氢氧化钠溶液以稳定速度滴入到锥形瓶中, 调节悬浮液的pH值至10, 然后继续连续搅拌反应1 h; 随后采用离心分离的方式获得固体材料, 再采用去离子水清洗材料5遍, 以去除固体材料表面残留的溶解性阴阳离子; 将所得到的固体材料放入105℃烘箱中烘干, 烘干后将材料研磨收集即得到铁改性方解石粉末, 并用自封袋密封备用.
采用照相机拍摄得到原始和铁改性方解石的实物照片.采用XRD仪(型号为UltimaⅣ, 生产厂商为日本株式会社理学, Cu靶, Kα射线源, λ=0.154 06 nm)对原始和铁改性方解石的晶体结构进行分析.采用波长色散型XRF仪(型号为XRF-1800, 生产厂商为日本岛津公司)对原始和铁改性方解石中的各化学元素含量进行测定.
1.3 磷酸盐去除的批量实验首先对比考察原始和铁改性方解石对水中磷酸盐的去除性能, 步骤为:分别将25 mg的方解石和铁改性方解石加入到25 mL的磷酸盐溶液(初始磷浓度为10 mg·L-1, pH值为7)中, 再置于水浴振荡器(150 r·min-1, 25℃)中反应24 h, 反应结束后通过离心分离获得上清液, 并采用钼锑抗比色法测定磷浓度.
进一步考察材料投加量对铁改性方解石去除水中磷酸盐的影响, 步骤为:分别称取质量为10、15、20、25、30、40、50、60、80和100 mg的铁改性方解石置于50 mL锥形瓶中, 并向该锥形瓶中加入25 mL的磷溶液(pH值为7、浓度为5 mg·L-1), 再将该锥形瓶放入水浴振荡器中以反应温度为25℃和转数为150 r·min-1的条件振荡24 h; 反应后, 通过离心获取上清液, 并采用钼锑抗比色法测定上清液中磷酸盐浓度.
随后进一步考察初始磷浓度对铁改性方解石去除水中磷酸盐的影响, 步骤为:分别将25 mg铁改性方解石加入到一系列的50 mL锥形瓶中, 再分别加入25 mL不同初始浓度的磷溶液(1、2、4、6、8和10 mg·L-1), 再置于水浴振荡器(温度设为25℃, 转数为150 r·min-1)中恒温振荡24 h, 反应结束后取样进行离心分离, 再采用钼锑抗比色法测定上清液中磷酸盐浓度.
原始或铁改性方解石对水中磷酸盐的去除率(η, %)和单位去除量(Q, mg·g-1)分别采用以下公式进行计算:

|
(1) |
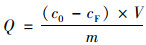
|
(2) |
式中, c0和cF分别为反应前和后水中磷酸盐的浓度(mg·L-1); V为磷酸盐溶液的体积(L); m为材料的投加量(g).
1.4 再生性能评估采用NaOH溶液对负载磷酸盐的铁改性方解石进行再生.首先将50 mg铁改性方解石置于离心管中, 再加入25 mL的磷酸盐溶液(初始磷浓度为10 mg·L-1和pH值为7), 再置于水浴振荡器(25℃和150 r·min-1)中反应24 h, 反应结束后离心分离, 采用钼锑抗比色法测定上清液中残留的磷浓度, 然后再采用去离子水将离心管中的固体材料清洗3遍.去除实验结束后马上开始再生实验, 将25 mL NaOH溶液(1 mol·L-1)加入到离心管中, 再振荡(25℃和150 r·min-1)反应24 h, 反应结束后离心分离, 再采用钼锑抗比色法测定上清液中的磷浓度.采用以下公式计算NaOH溶液对负载磷酸盐后铁改性方解石中磷的解吸率(DE, %):

|
(3) |
式中, cDE为解吸液中磷的浓度(mg·L-1); V为解吸液的体积(L); Q为铁改性方解石对水中磷酸盐的单位去除量(mg·g-1); m为铁改性方解石投加量(g).
1.5 底泥培养实验分别称取50 g干底泥置于3个250 mL广口棕色试剂瓶中, 并对这3个棕色试剂瓶中底泥分别进行以下处理:①底泥不进行任何处理(对照组); ②将10 g方解石均匀覆盖到底泥上方(方解石覆盖组); ③将10 g铁改性方解石材料均匀覆盖到底泥上方(铁改性方解石覆盖组).根据计算, 覆盖层的厚度约为3 mm.配制含10 mmol·L-1 NaCl、1 mmol·L-1 NaHCO3和1 mmol·L-1 CaCl2的pH值为7.5的溶液作为模拟上覆水, 并采用亚硫酸钠氧化法去除模拟上覆水中的溶解氧(DO), 使DO浓度低于0.5 mg·L-1.采用注射器将配制好的模拟上覆水缓慢加入到棕色试剂瓶中, 直至上覆水位到达棕色试剂瓶的瓶口, 然后塞上橡胶塞, 并用白凡士林涂抹封口, 营造缺氧环境.每间隔一段时间采用便携式溶氧仪测定上覆水中DO浓度, 采用便携式pH计测定上覆水的pH值, 与此同时采用注射器吸取15 mL的上覆水样, 再采用0.45 μm的滤膜对所采集水样进行过滤, 然后再采用钼锑抗比色法测定滤液中SRP的浓度.采集水样后, 用注射器吸取15 mL的人工配水缓慢加入到棕色试剂瓶中, 以补充减少的水量.培养163 d后, 取出试剂瓶中的覆盖材料(方解石和铁改性方解石)与底泥.取出的湿底泥和覆盖材料经自然风干、研磨后收集备用.覆盖层对上覆水中SRP的削减率(RE, %)通过以下公式进行计算:

|
(4) |
式中, cD为对照组上覆水中SRP的浓度(mg·L-1); cF为覆盖组上覆水中SRP的浓度(mg·L-1).
1.6 底泥和覆盖材料磷形态分级提取采用五步连续化学提取法对底泥和覆盖材料中的磷形态进行分析, 本次实验将磷形态分为以下5种形态, 即弱吸附态磷(Labile-P)、氧化还原敏感态磷(BD-P)、金属氧化结合态磷(NaOH-rP)、钙结合态磷(HCl-P)以及残渣态磷(Res-P).提取步骤为:称取0.4 g的干底泥或覆盖材料置于离心管中, 依次采用1 mol·L-1 NH4Cl溶液(25℃, 提取2 h)、0.11 mol·L-1 NaHCO3/Na2S2O4溶液(40℃, 提取1 h)、1 mol·L-1 NaOH溶液(25℃, 提取16 h)、0.5 mol·L-1 HCl溶液(25℃, 提取16 h)和1 mol·L-1 NaOH溶液(85℃, 提取1 h)进行提取, 提取液的体积均为25 mL, 每步提取液中磷浓度均采用钼锑抗比色法进行测定, 设置3个平行组[18, 19].上述5种形态磷之和称为总可提取磷(Tot-P).
1.7 覆盖材料中生物可利用性磷提取通过分析覆盖材料(方解石和铁改性方解石)中水溶性磷(WSP)、易解吸磷(RDP)、藻类可利用磷(AAP)和NaHCO3可提取磷(Olsen-P)含量, 评估覆盖材料中磷的生物可利用性.测定覆盖材料中WSP含量的具体步骤为:将0.2 g覆盖材料和20 mL去离子水放入离心管中振荡(25℃和200 r·min-1)反应2 h, 再离心分离后测定上清液中磷的浓度[18].测定覆盖材料中RDP含量的具体程序为:分别称取0.2 g覆盖材料置于离心管中, 并加入20 mL 0.01 mol·L-1 CaCl2溶液, 再振荡(25℃和200 r·min-1)反应1 h, 再离心分离后测定上清液中磷的浓度[18].测定覆盖材料中AAP含量的具体步骤为:首先称取0.2 g覆盖材料放入离心管中, 再将20 mL 0.1 mol·L-1 NaOH溶液加入到离心管中, 然后再将该离心管放入到水浴振荡器(25℃和200 r·min-1)中反应4 h, 离心分离后测定溶液中磷的浓度[3].测定覆盖材料中Olsen-P含量的具体程序为:称取0.2 g覆盖材料放入到离心管中, 再向该离心管中加入20 mL 0.5 mol·L-1 NaHCO3溶液, 再将该离心管放入到水浴振荡器(200 r·min-1, 25℃)中振荡反应0.5 h, 反应结束后通过离心分离的方式获取上清液, 再采用钼锑抗比色法对上清液中的磷浓度进行测定[3].
2 结果与讨论 2.1 铁改性方解石表征图 1为原始和铁改性方解石的实物.从中可见, 原始方解石为白色的粉末状颗粒, 而铁改性方解石则为红棕色的粉末状颗粒.这说明采用本研究的制备方法已经成功地制备得到了铁改性方解石.图 2为原始和铁改性方解石的XRD图谱.从中可见, 原始方解石的主要X射线衍射峰与方解石的标准图谱(JCPDS 01-086-2334)[24]一致.这说明本研究所用方解石的主要矿物成分为方解石晶体.另外, 铁改性方解石的主要X射线衍射峰也与方解石的标准图谱[24]一致.这说明铁改性不会改变方解石的晶体结构.也就是说, 铁改性方解石中仍存在方解石晶体.从表 1可见, 原始方解石主要含Ca和O这2种元素, 铁的含量非常低.这是因为原始方解石的主要矿物成分为方解石的缘故.铁改性方解石同样含大量的Ca和O这2种元素.这进一步证实了铁改性方解石中仍存在大量的方解石.另外, 铁改性方解石中含2.48%的铁, 其铁的含量明显高于原始方解石.这说明经铁改性后, 铁已经被成功负载到了方解石的表面上.确定铁改性方解石在水体中的沉降性能, 对于其实际应用至关重要.为此, 本研究将铁改性方解石直接抛洒到盛放自来水的250 mL量筒的水面上, 以考察其沉降行为, 结果发现10 min后其基本上完全沉降到量筒的底部.这说明, 本研究所制备得到的铁改性方解石具有良好的沉降性能.

|
(a)原始方解石; (b)铁改性方解石 图 1 原始和铁改性方解石的实物 Fig. 1 Photos of raw and iron-modified calcites |

|
图 2 原始和铁改性方解石的XRD图谱 Fig. 2 XRD patterns of raw and iron-modified calcites |
|
|
表 1 原始和铁改性方解石中化学元素的质量分数 /% Table 1 Chemical compositions of raw and iron-modified calcites /% |
2.2 铁改性方解石对水中磷酸盐的去除性能和负载磷酸盐后铁改性方解石的再生性能
为验证铁的改性效果, 本文对比分析了原始和铁改性方解石对水中磷酸盐的去除能力, 结果发现, 在磷浓度为10 mg·L-1、材料与溶液体积之比为1 g·L-1、pH 7、温度为25℃和反应时间为24 h的条件下, 原始和铁改性方解石对水中磷酸盐的去除率分别为4.85%和29.9%, 它们对水中磷酸盐的单位去除量分别为0.485 mg·g-1和2.99 mg·g-1.这说明, 原始方解石对水中磷酸盐具有一定的去除能力, 而铁改性方解石对水中磷酸盐的去除能力则明显强于原始方解石.也就是说, 采用铁对方解石进行改性显著提高了材料对水中磷酸盐的去除能力.文献[25~30]也已经观察到了方解石对水中的磷酸盐具有一定的去除能力, 并且发现方解石除磷的机制既与水中磷酸盐浓度大小密切相关, 也与反应时间密切相关.当水中磷酸盐浓度低时, 方解石会通过快速地吸附反应去除水中的磷酸盐, 表面吸附会占据主导地位; 当水中磷酸盐浓度高时, 初期阶段少量的磷酸盐会通过表面吸附作用而被去除, 此时吸附占据主导地位, 随后大量的磷会通过钙磷沉淀机制而被去除, 此时沉淀作用会占据主导地位[25, 26, 29].李振炫等[29]的研究发现, 当水中磷酸盐初始浓度为0.5 mg·L-1时, 前10 h即完成了大部分磷的去除, 吸附机制占主导地位; 当水中磷酸盐初始浓度为2.5 mg·L-1时, 前10 h仅去除了总磷的20%左右, 前期主要依靠吸附机制去除水中的磷, 而后期主要依靠钙磷沉淀机制去除水中的磷.因此, 笔者推测, 在磷浓度为10 mg·L-1和反应时间为24 h的条件下, 方解石除磷的机制既包括表面吸附作用, 也包括钙磷沉淀作用.与方解石相比, 铁改性方解石对水中磷酸盐的去除能力更强.这说明, 在初始磷浓度为10 mg·L-1和反应时间为24 h时, 铁改性方解石除磷的机制既包括铁氧化物的表面吸附作用, 也包括方解石的表面吸附作用和钙磷沉淀作用.先前研究发现, 铁的水合氧化物吸附去除水中磷酸盐的一个重要机制是磷酸盐先与水合铁氧化物表面的羟基发生配位体交换, 然后再生成内层配合物[31~33].因此, 笔者推测配位体交换和内层配合物形成在铁改性方解石去除水中磷酸盐过程中会起到重要的作用.
通常情况下, 吸附剂材料的投加量是影响水中磷酸盐去除的重要因素之一[34].图 3为材料投加量对铁改性方解石去除水中磷酸盐的影响.从中可见, 当材料投加量由0.4 g·L-1增加到4 g·L-1时, 水中的磷浓度则由4.30 mg·L-1逐渐下降到0.428 mg·L-1, 而铁改性方解石对水中磷酸盐的去除率则由16.2%逐渐增加到91.7%.这说明, 铁改性方解石投加量越大, 越有利于水中磷酸盐的去除.当投加足够量的铁改性方解石时, 水中的磷酸盐可以被降低到很低的水平.当铁改性方解石的投加量越大时, 所提供的材料表面活性吸附位点数量就越多, 越有利于水中磷酸盐被吸附去除, 从而导致水中磷酸盐浓度越低[34].

|
图 3 材料投加量对铁改性方解石去除水中磷酸盐的影响 Fig. 3 Effect of sorbent dosage on phosphate removal from aqueous solution by iron-modified calcite |
图 4为初始磷浓度对铁改性方解石去除水中磷酸盐的影响.从中可见, 当初始磷浓度由1 mg·L-1增加到8 mg·L-1时, 铁改性方解石对水中磷酸盐的去除率逐渐由91.7%下降到29.4%, 此后磷浓度再增加到10 mg·L-1时去除率则基本保持不变, 而铁改性方解石对水中磷酸盐的单位去除量则由0.917 mg·g-1逐渐增加到3.09 mg·g-1.这是因为:初始磷浓度的增加, 有利于克服固相和液相之间磷的传质阻力, 进而有利于水中的磷向铁改性方解石表面输送, 从而导致铁改性方解石的磷单位去除量随着初始浓度的增加而增加[34].根据图 4的实验数据, 可以进一步得到水中残留磷酸盐质量浓度与铁改性方解石单位磷去除量之间的关系, 结果见图 5, 并进一步采用Langmuir、Freundlich和Dubinin-Radushkevitch(D-R)等温吸附模型[35]对这种关系进行分析, 拟合结果见表 2.从中可见, 当反应时间为24 h和磷初始浓度为1~10 mg·L-1时, 与Langmuir模型相比, Freundlich和D-R模型对实验数据的拟合效果更好.计算得到的1/n值为0.297, 小于1[35].这说明铁改性方解石对水中磷酸盐的吸附属于优惠吸附.计算得到的平均吸附自由能为14.6 kJ·mol-1, 明显大于8 kJ·mol-1.这说明铁改性方解石对水中磷酸盐的吸附以化学吸附为主, 因为通常情况下如果E小于8 kJ·mol-1, 那么反应属于物理吸附, 否则属于化学吸附[36].根据图 5还可知, 铁改性方解石对水中磷酸盐的最大单位去除量可以达到3.09 mg·g-1, 高于许多先前文献报道的铁基吸附剂的最大磷单位吸附量(表 3).这说明铁改性方解石具有较高的磷吸附容量.因此, 从去除容量的角度来看, 铁改性方解石是一种有希望用于控制底泥中磷释放的活性覆盖材料.

|
图 4 初始磷浓度对铁改性方解石去除水中磷酸盐的影响 Fig. 4 Impact of initial phosphorus concentration on phosphate removal from aqueous solution by iron-modified calcite |

|
图 5 铁改性方解石单位磷去除量与水中残留磷酸盐质量浓度之间的关系 Fig. 5 Relationship between the amount of phosphate removed by iron-modified calcite and the residual phosphate concentration of the solution after phosphate removal |
|
|
表 2 Langmuir、Freundlich和Dubinin-Radushkevitch(D-R)等温吸附模型的拟合结果1) Table 2 Fitting results of Langmuir, Freundlich, and Dubinin-Radushkevitch (D-R) for phosphate sorption onto iron-modified calcite |
|
|
表 3 已有报道的铁基吸附剂的最大磷单位吸附量 Table 3 Maximum phosphate sorption capacities for iron-based adsorbent materials reported in previous literature |
评价负载磷酸盐后铁改性方解石的再生性能, 不仅有助于深入了解其除磷机制, 而且有助于评估其重复利用率或使用周期.为此, 本研究考察了NaOH溶液对负载磷酸盐后铁改性方解石中磷的解吸特性, 结果发现1 mol·L-1的NaOH溶液对负载磷酸盐后铁改性方解石中磷的解吸率仅为18.0%.Shahid等研究发现, 采用0.2 mol·L-1的NaOH溶液可以使75%被吸附到四氧化三铁表面上的磷酸盐解吸下来[31].Ajmal等[23]的研究发现, 采用1 mol·L-1的NaOH溶液可以使75%、85%和82%被水铁矿、针铁矿和四氧化三铁所吸附的磷酸盐解吸下来.由此可见, NaOH溶液对负载磷酸盐后铁氧化物的再生性能较好.SØ等[25]的研究发现方解石对水中磷酸盐的表面吸附过程是一个可逆的过程, 通过降低水中磷酸盐的浓度容易使被方解石表面所吸附的磷解吸下来.众所周知, 高的pH值有利于钙磷沉淀的生成[45].NaOH溶液对负载磷酸盐后铁改性方解石中磷的解吸效果(本研究)低于单纯的铁氧化物[23, 31], 这说明铁改性方解石对水中磷酸盐的去除机制不仅包括铁氧化物的表面吸附作用, 也包括钙磷沉淀作用.这也说明采用NaOH溶液并不能使负载磷酸盐后铁改性方解石得到很好地再生.因此, 今后进一步探索新的再生方法仍然是非常必要的.
2.3 铁改性方解石覆盖对上覆水磷浓度的影响对照组、方解石覆盖组和铁改性方解石覆盖组上覆水的DO浓度、pH值和SRP浓度的变化见图 6.从图 6(a)可见, 各底泥培养装置中上覆水的DO浓度均小于0.50 mg·L-1, 这说明各装置中底泥在其培养期间均处于缺氧状态.从图 6(b)可见, 随着底泥培养时间的增加, 各培养装置上覆水pH值均先逐渐下降, 此后在小范围内波动.这可能归咎于这么一个事实:底泥中有机物的降解会释放出CO2, 从而降低了上覆水中的pH值[46].在底泥培养期间, 对照组、方解石覆盖组和铁改性方解石覆盖组上覆水的pH值分别位于7.15~7.97、7.23~7.94和7.40~7.97之间.这说明, 各底泥培养装置上覆水的pH值在培养期间均处于中性略微偏碱的范围.除第3 d外, 方解石覆盖组和铁改性方解石覆盖组上覆水的pH值在其他时间均略微高于对照组.这说明方解石覆盖和铁改性方解石覆盖虽然可以增加上覆水的pH值, 但上升的幅度是有限的.

|
图 6 对照组、方解石覆盖组和铁改性方解石覆盖组上覆水的DO浓度、pH值和SRP浓度的变化 Fig. 6 Changes in DO, pH, and SRP of overlying water in control, calcite capping, and iron-modified calcite capping columns |
从图 6(c)可见, 当培养时间为3~69 d时, 对照组上覆水中SRP浓度位于0.143~0.293 mg·L-1, 但是当培养时间由69增加到160 d时, SRP浓度从总体上看会逐渐上升, 至第160 d时达到最大值1.98 mg·L-1, 此后出现一定程度的下降, 到163 d时SRP浓度下降到1.60 mg·L-1.这说明, 在缺氧条件下, 本研究所用底泥会向上覆水体中释放出大量的磷.通常情况下, 底泥中铁/铝结合磷和钙结合磷是底泥中2种主要的磷形式[47].在高的pH值条件下, 底泥中与铁/铝结合的磷容易释放; 在低的pH值条件下, 底泥中与钙结合的磷容易释放; 而在中性范围内这两种形态的磷都不容易释放[47].本研究中, 对照组上覆水pH值位于7.15~7.97, 处于中性略微偏碱的范围, 并且随着培养时间的增加呈现下降的趋势, 与SRP浓度随培养时间的增加呈现增加的趋势相反.这意味着, 对照组底泥中磷的大量释放主要不是由pH值的变化所引起的.铁磷同步释放是缺氧条件下底泥磷释放的一个重要机制[48].在好氧条件下, 底泥中磷会被三价铁氧化物/氢氧化物所吸附, 导致铁磷很难被释放出来; 在缺氧条件下, 三价铁离子会被微生物转化为二价铁离子, 导致三价铁氧化物/氢氧化物溶解并释放出来, 同时导致与铁结合的磷也被释放出来[48].
从图 6(c)还可看出, 当培养时间为3~69 d时, 方解石覆盖组上覆水中SRP浓度处于较低的水平, 位于0.010~0.054 mg·L-1, 明显低于对照组.经计算, 当培养时间为3~69 d时, 方解石覆盖对上覆水中SRP的削减率高达79.5%~96.2%(图 7).这说明方解石覆盖可以有效控制培养初期阶段底泥中磷向上覆水体中的释放.但是, 当培养时间从69增加到160 d时, 上覆水中SRP浓度从总体上看呈现上升的趋势, 至160 d达到最大值1.41 mg·L-1, 此后出现一定程度的下降, 到163 d时SRP浓度下降至1.15 mg·L-1.与对照组相比, 当培养时间为79~163 d时方解石覆盖组上覆水SRP浓度仍然要低.这说明在底泥培养的后期阶段, 方解石覆盖仍然可以有效阻止水体内源磷向上覆水体中释放.但是, 需要指出的是, 当培养时间从79增加到163 d时, 方解石覆盖对上覆水中SRP的削减率从总体上看却呈现下降的趋势, 至163 d时方解石的削减率仅为28.0%(图 7).这说明方解石覆盖在高效控制底泥磷释放一段时间后会出现效率下降的情况.先前的研究也观察到了方解石覆盖系统的这一现象[9, 12].Berg等[9]发现当底泥培养时间为70 d时, 应用1 cm厚的方解石覆盖层可导致内源磷释放通量削减80%.Lin等[12]发现当底泥培养时间为72 d时, 覆盖12.7 kg·m-2方解石对内源磷向上覆水体释放的控制效率为57%.这些先前报道的方解石覆盖效率虽然高于本研究底泥培养结束时的效率(28.0%), 但是仍然要远远低于本研究底泥培养初期的最高效率(96.2%).由此可见, 采用方解石作为覆盖材料, 当运行一段时间后, 很难使上覆水磷浓度控制到很低的水平.

|
图 7 方解石覆盖和铁改性方解石覆盖对上覆水中SRP的削减效果 Fig. 7 Reduction rates of SRP in overlying water by capping with calcite and iron-modified calcite |
与方解石覆盖组不同的是, 铁改性方解石覆盖组上覆水中SRP浓度在整个底泥培养期间(3~169 d)均处于较低的水平, 位于0.003~0.041 mg·L-1之间, 明显低于对照组[图 6(c)].铁改性方解石覆盖对上覆水中SRP的削减率在整个底泥培养期间一直保持很高的水平, 位于95.5%~99.7%(图 7).这说明铁改性方解石覆盖可以有效地控制底泥中磷向上覆水体中的释放, 使得上覆水的磷浓度被控制到很低的水平.在底泥培养时间为85~163 d时, 铁改性方解石覆盖对上覆水中SRP的削减率明显高于方解石覆盖, 并且随着培养时间的增加, 这种差距呈现扩大的趋势(图 7).这说明, 铁改性方解石覆盖控制底泥中磷向上覆水体中释放的效率明显高于方解石覆盖.这主要归功于这样一个事实:铁改性方解石对水中磷酸盐的去除能力明显强于未改性方解石.因此, 从控制效率的角度看, 铁改性方解石比原始方解石更适合作为活性覆盖材料用于水体内源磷释放的控制.
先前的研究发现[15], 镧改性膨润土(PhoslockⓇ)覆盖也可以有效地控制底泥中磷向上覆水的释放, PhoslockⓇ覆盖会导致上覆水中SRP浓度保持很低的水平, 当PhoslockⓇ应用后第10 d时, 上覆水中SRP浓度仅为0.005 mg·L-1, 当PhoslockⓇ应用后第110 d时, 上覆水中SRP的削减率仍然超过98%.由此可见, PhoslockⓇ覆盖控制底泥磷释放的效率明显高于方解石覆盖, 而与铁改性方解石覆盖类似.但是, 应用PhoslockⓇ是否会对水体生态系统产生负面影响仍然需要进一步的研究[49, 50], 而由于铁氧化物和方解石是环境友好的物质[10], 所以铁改性方解石预计对水体生态系统的负面影响是很小的.因此, 综合考虑活性覆盖材料的控磷效率和负面影响, 笔者认为铁改性方解石比PhoslockⓇ更适合作为一种活性覆盖材料用于水体内源磷释放的控制.
无论是方解石覆盖, 还是铁改性方解石覆盖, 它们对上覆水pH值的影响都是有限的.因此, 方解石和铁改性方解石覆盖之所以能有效控制水体内源磷的释放, 并不是由pH改变所引起的.方解石和铁改性方解石对水中的磷酸盐具有亲和力(详见2.2节).所以, 方解石和铁改性方解石覆盖之所以能有效控制水体内源磷的释放, 主要归功于它们对水中磷酸盐的去除能力.通常情况下, 底泥中磷会先释放进入间隙水中, 继而通过上覆水和间隙水之间的浓度梯度扩散作用释放进入上覆水中[51].将方解石或铁改性方解石覆盖到底泥-水界面上方后, 覆盖层中的方解石预计会通过表面吸附作用和钙磷沉淀作用去除间隙水中的SRP, 而覆盖层中的铁改性方解石预计会通过方解石和铁氧化物的表面吸附作用以及钙磷沉淀作用去除间隙水中的SRP, 进而会降低间隙水中SRP穿越泥水界面进入上覆水中的速率, 从而降低了上覆水中SRP的浓度, 达到内源磷释放控制的目的.
2.4 铁改性方解石覆盖对底泥磷形态的影响底泥中不同形态磷通常具有不同的磷释放潜力[52].因此, 了解方解石和铁改性方解石覆盖对底泥中各形态磷含量的影响, 对于确定其控制底泥磷释放的效果是至关重要的.为此, 本文考察了原始和铁改性方解石覆盖对底泥中Labile-P、BD-P、NaOH-rP、HCl-P和Res-P的影响, 结果见图 8.从中可见, 对照组底泥中各形态磷含量从大到小的排序依次为:HCl-P(463 mg·kg-1)>Res-P(426 mg·kg-1)>BD-P(143 mg·kg-1)>NaOH-rP(65.3 mg·kg-1)>Labile-P(3.81 mg·kg-1).与对照组底泥相比, 方解石覆盖组底泥中BD-P、NaOH-rP和HCl-P含量分别下降了20.2%、11.8%和3.56%, 而Res-P含量则增加了15.8%.这说明方解石覆盖会促使底泥中少量的BD-P、NaOH-rP和HCl-P向Res-P转变.从图 8还可见, 与对照组底泥相比, 铁改性方解石覆盖组底泥中BD-P和NaOH-rP分别下降了8.90%和2.52%, HCl-P含量基本保持不变, 而Res-P含量则增加了22.5%.这说明铁改性方解石覆盖会促进底泥中少量的BD-P和NaOH-rP向Res-P转变.底泥中Labile-P和BD-P释放的可能性很大, 它们属于潜在可移动性磷[52].底泥中NaOH-rP和HCl-P相对稳定, 它们释放的可能性属于中等, 而底泥中Res-P则非常稳定, 其释放的可能性非常低[52].因此, 原始和铁改性方解石覆盖作用下底泥中少量的释放可能性高和中等的磷向稳定程度非常高的磷转变, 这是有利于底泥中磷释放控制的.

|
图 8 原始和铁改性方解石覆盖对底泥磷形态的影响 Fig. 8 Influence of raw and iron-modified calcite capping on phosphorus speciation of sediments |
从底泥中释放出来的磷被原始和铁改性方解石覆盖层所固定后, 如果会重新释放出来的话, 那么其很难长期有效地控制底泥中磷的释放.因此, 评估被覆盖材料所钝化磷的稳定性, 对于确定其控制底泥磷释放的效果是至关重要的.为此, 本文进一步分析了原始和铁改性方解石覆盖层中各形态磷和总可提取态磷含量, 结果见图 9.从中可见, 方解石覆盖层中各形态磷含量从大到小的排序依次为:Res-P(313 mg·kg-1)>HCl-P(193 mg·kg-1)>BD-P(119 mg·kg-1)>Labile-P(23.6 mg·kg-1)>NaOH-rP(16.5 mg·kg-1).铁改性方解石覆盖层中不同形态磷含量从大到小的排序依次为:Res-P(505 mg·kg-1)>HCl-P(271 mg·kg-1)>BD-P(79.9 mg·kg-1)>NaOH-rP(47.8 mg·kg-1)>Labile-P(3.66 mg·kg-1).原始和铁改性方解石覆盖层中总可提取态磷含量分别为665 mg·kg-1和907 mg·kg-1.这意味着从底泥中释放出来的磷会被钝化到原始和铁改性方解石覆盖层中, 且与原始方解石相比, 铁改性方解石覆盖层钝化了更多的从底泥中释放出来的磷.这进一步证实了原始和铁改性方解石覆盖层均可以有效控制底泥中磷的释放, 且铁改性方解石控制底泥中磷释放的效果更好.

|
图 9 方解石和铁改性方解石覆盖层中各形态磷和总可提取态磷含量 Fig. 9 Contents of various phosphorus species and total extractable phosphorus in calcite and iron-modified calcite capping layers |
进一步计算得到原始和铁改性方解石覆盖层中不同形态磷占总可提取态磷的比例, 结果见图 10.从中可见, 方解石覆盖层中占比较大的3种形态磷为Res-P(47.0%)、HCl-P(29.0%)和BD-P(18.0%), 另外含少量的Labile-P(3.55%)和NaOH-rP(2.48%).铁改性方解石覆盖层中占比较大的两种形态磷为Res-P(55.7%)和HCl-P(29.8%), 另外还含少量的BD-P(8.81%)、NaOH-rP(5.27%)和Labile-P(0.404%).原始和铁改性方解石覆盖层中释放可能性大的磷占总可提取态磷的比例分别仅为21.5%和9.22%, 而释放可能性低和中等的磷占比则分别高达78.5%和90.8%.这说明被方解石和铁改性方解石覆盖层所固定的磷中大多数属于比较稳定和非常稳定的磷, 难以被重新释放出来.另外, 铁改性方解石覆盖层中释放可能性低和中等的磷占比高于原始方解石, 而前者中释放可能性高的磷占比则低于后者.因此, 从钝磷产物的形态分布角度来看, 原始和铁改性方解石均适合作为活性覆盖材料用于水体内源磷释放的控制, 且与原始方解石相比, 铁改性方解石更适合作为一种底泥活性覆盖材料用于水体内源磷释放的控制.Meis等[52]的研究发现, 被固定到PhoslockⓇ上的磷的形态分布为:HCl-P (60.7%)、NaOH-rP(16.9%)、BD-P(14.4%)、Labile-P(6.6%)、Res-P(1.2%)和有机磷(0.2%), 大部分磷(79%)以较稳定和非常稳定的形式存在(NaOH-rP、HCl-P和Res-P), 很难被重新释放出来, 仅少部分磷(21%)以潜在可移动态磷形式(Labile-P、BD-P和有机磷)存在, 容易被重新释放出来.PhoslockⓇ中较稳定和非常稳定磷的占比(79%)虽然与方解石(78.5%)是相类似的, 但是却明显低于铁改性方解石(90.8%).因此, 从钝磷产物稳定性的角度看, 铁改性方解石比PhoslockⓇ更适合作为一种活性覆盖材料用于控制水体内源磷的释放.

|
图 10 原始和铁改性方解石覆盖层中各形态磷占总可提取态磷的比例 Fig. 10 Percentages of various phosphorus species as a proportion of total extractable phosphorus in calcite and iron-modified calcite capping layers |
生物可利用性磷(BAP)是指直接可被藻类利用的磷再加上那些通过自然过程能够转化为藻类可直接吸收态的磷[53].底泥中BAP含量在一定程度上可用于反映底泥中磷的稳定性[3].为评估被原始和铁改性方解石覆盖层所钝化磷的稳定性, 本文进一步考察了原始和铁改性方解石覆盖层中各生物可利用性磷的含量, 结果见图 11.从中可见, 方解石覆盖层中WSP、RDP、AAP和Olsen-P含量分别为5.17、1.09、20.1和50.6 mg·kg-1, 占总可提取态磷的比例分别为0.778%、0.164%、3.03%和7.61%.铁改性方解石覆盖层中WSP、RDP、AAP和Olsen-P含量分别为3.68、0.747、21.6和37.7 mg·kg-1, 占总可提取态磷的比例分别为0.406%、0.082 4%、2.38%和4.16%.由此可见, 方解石和铁改性方解石覆盖层中生物可利用性磷含量都仅占总可提取态磷的很小一部分, 固定到原始和铁改性方解石覆盖层中的磷的生物可利用性很低, 大部分磷很难被藻类利用而重新释放出来.另外, 铁改性方解石覆盖层中WSP、RDP和Olsen-P含量以及它们占总可提取态磷的比例均低于方解石.这说明与方解石相比, 固定到铁改性方解石覆盖层中的磷更难被藻类利用而释放出来.由以上分析可见, 从钝磷产物的生物可利用性角度看, 方解石和铁改性方解石均适合作为活性覆盖材料用于控制底泥内源磷的释放, 且铁改性方解石更佳.

|
图 11 方解石和铁改性方解石覆盖层中各生物可利用性磷含量 Fig. 11 Contents of various bioavailable phosphorus in calcite and iron-modified calcite capping layers |
(1) 铁改性方解石对水中磷酸盐去除能力明显强于未改性方解石; 增加铁改性方解石的投加量, 有利于水中磷酸盐的去除; 增加初始磷浓度, 铁改性方解石对水中磷酸盐的去除量随之增加, 最大的单位去除量可以达到3.09 mg·g-1.
(2) 铁改性方解石覆盖可以有效地控制底泥中磷向上覆水体的释放, 使得上覆水中SRP浓度处于非常低的水平(0.003~0.041 mg·L-1), 且与原始方解石覆盖相比, 铁改性方解石覆盖控制底泥中磷进入上覆水体中的效果更佳.
(3) 铁改性方解石覆盖作用下底泥中少部分BD-P和NaOH-rP会向Res-P转变, 这对于利用铁改性方解石作为覆盖材料控制底泥磷释放而言是有利的.
(4) 固定到铁改性方解石覆盖层中的磷大部分以相对稳定的磷形态(NaOH-rP和HCl-P)以及非常稳定的磷形态(Res-P)存在, 并且生物可利用性磷占总可提取态磷的比例低, 它们重新释放出来的风险低, 并且与方解石覆盖层相比, 铁改性方解石覆盖层中容易释放磷含量和生物可利用性磷含量更低, 所钝化的磷发生重新释放的风险更低.
(5) 铁改性方解石是一种有望用于控制水体内源磷释放的底泥活性覆盖材料.
| [1] | Le Moal M, Gascuel-Odoux C, Ménesguen A, et al. Eutrophication:a new wine in an old bottle?[J]. Science of the Total Environment, 2019, 651: 1-11. DOI:10.1016/j.scitotenv.2018.09.139 |
| [2] | Tu L Y, Jarosch K A, Schneider T, et al. Phosphorus fractions in sediments and their relevance for historical lake eutrophication in the Ponte Tresa basin (Lake Lugano, Switzerland) since 1959[J]. Science of the Total Environment, 2019, 685: 806-817. DOI:10.1016/j.scitotenv.2019.06.243 |
| [3] | Wang C H, He R, Wu Y, et al. Bioavailable phosphorus (P) reduction is less than mobile P immobilization in lake sediment for eutrophication control by inactivating agents[J]. Water Research, 2017, 109: 196-206. DOI:10.1016/j.watres.2016.11.045 |
| [4] | Oldenborg K A, Steinman A D. Impact of sediment dredging on sediment phosphorus flux in a restored riparian wetland[J]. Science of the Total Environment, 2019, 650: 1969-1979. DOI:10.1016/j.scitotenv.2018.09.298 |
| [5] | Huser B J, Egemose S, Harper H, et al. Longevity and effectiveness of aluminum addition to reduce sediment phosphorus release and restore lake water quality[J]. Water Research, 2016, 97: 122-132. DOI:10.1016/j.watres.2015.06.051 |
| [6] | Foy R H. Suppression of phosphorus release from lake sediments by the addition of nitrate[J]. Water Research, 1986, 20(11): 1345-1351. DOI:10.1016/0043-1354(86)90132-6 |
| [7] | Chen J J, Lu S Y, Zhao Y K, et al. Effects of overlying water aeration on phosphorus fractions and alkaline phosphatase activity in surface sediment[J]. Journal of Environmental Sciences, 2011, 23(2): 206-211. DOI:10.1016/S1001-0742(10)60394-4 |
| [8] | Xu D, Ding S M, Sun Q, et al. Evaluation of in situ capping with clean soils to control phosphate release from sediments[J]. Science of the Total Environment, 2012, 438: 334-341. DOI:10.1016/j.scitotenv.2012.08.053 |
| [9] | Berg U, Neumann T, Donnert D, et al. Sediment capping in eutrophic lakes-efficiency of undisturbed calcite barriers to immobilize phosphorus[J]. Applied Geochemistry, 2004, 19(11): 1759-1771. DOI:10.1016/j.apgeochem.2004.05.004 |
| [10] | Yu X F, Grace M R, Sun G Z, et al. Application of ferrihydrite and calcite as composite sediment capping materials in a eutrophic lake[J]. Journal of Soils and Sediments, 2018, 18(3): 1185-1193. DOI:10.1007/s11368-017-1872-4 |
| [11] |
林建伟, 朱志良, 赵建夫, 等. 方解石活性覆盖系统抑制底泥磷释放的影响因素研究[J]. 环境科学, 2008, 29(1): 121-126. Lin J W, Zhu Z L, Zhao J F, et al. Influencing factors of calcite active barrier system to control phosphorus release from sediments[J]. Environmental Science, 2008, 29(1): 121-126. |
| [12] | Lin J W, Zhan Y H, Zhu Z L. Evaluation of sediment capping with active barrier systems (ABS) using calcite/zeolite mixtures to simultaneously manage phosphorus and ammonium release[J]. Science of the Total Environment, 2011, 409(3): 638-646. DOI:10.1016/j.scitotenv.2010.10.031 |
| [13] |
林建伟, 朱志良, 赵建夫. 天然沸石覆盖层控制底泥氮磷释放的影响因素[J]. 环境科学, 2006, 27(5): 880-884. Lin J W, Zhu Z L, Zhao J F. Influencing factor of natural zeolite barrier for controlling nitrogen and phosphorus release from sediments[J]. Environmental Science, 2006, 27(5): 880-884. |
| [14] | Gu B W, Hong S H, Lee C G, et al. The feasibility of using bentonite, illite, and zeolite as capping materials to stabilize nutrients and interrupt their release from contaminated lake sediments[J]. Chemosphere, 2019, 219: 217-226. DOI:10.1016/j.chemosphere.2018.12.021 |
| [15] | Wang Y, Ding S M, Wang D, et al. Static layer:a key to immobilization of phosphorus in sediments amended with lanthanum modified bentonite (Phoslock®)[J]. Chemical Engineering Journal, 2017, 325: 49-58. DOI:10.1016/j.cej.2017.05.039 |
| [16] |
李佳, 林建伟, 詹艳慧. 镧改性沸石活性覆盖控制重污染河道底泥溶解性磷酸盐和铵释放研究[J]. 环境科学, 2013, 34(11): 4266-4274. Li J, Lin J W, Zhan Y H. Evaluation of in situ capping with lanthanum-modified zeolite to control phosphate and ammonium release from sediments in heavily polluted river[J]. Environmental Science, 2013, 34(11): 4266-4274. |
| [17] | Gibbs M, Özkundakci D. Effects of a modified zeolite on P and N processes and fluxes across the lake sediment-water interface using core incubations[J]. Hydrobiologia, 2011, 661(1): 21-35. DOI:10.1007/s10750-009-0071-8 |
| [18] | Lin J W, He S Q, Zhang H H, et al. Effect of zirconium-modified zeolite addition on phosphorus mobilization in sediments[J]. Science of the Total Environment, 2019, 646: 144-157. DOI:10.1016/j.scitotenv.2018.07.281 |
| [19] |
杨孟娟, 林建伟, 詹艳慧, 等. 锆改性沸石活性覆盖控制重污染河道底泥氮磷释放研究[J]. 农业环境科学学报, 2013, 32(12): 2460-2470. Yang M J, Lin J W, Zhan Y H, et al. Releases of ammonium and phosphorus from river sediments capped with zirconium-modified zeolite[J]. Journal of Agro-Environment Science, 2013, 32(12): 2460-2470. |
| [20] | Yang M J, Lin J W, Zhan Y H, et al. Adsorption of phosphate from water on lake sediments amended with zirconium-modified zeolites in batch mode[J]. Ecological Engineering, 2014, 71: 223-233. DOI:10.1016/j.ecoleng.2014.07.035 |
| [21] | Yin H B, Kong M. Reduction of sediment internal P-loading from eutrophic lakes using thermally modified calcium-rich attapulgite-based thin-layer cap[J]. Journal of Environmental Management, 2015, 151: 178-185. |
| [22] | Wang C H, Gao S J, Pei Y S, et al. Use of drinking water treatment residuals to control the internal phosphorus loading from lake sediments:laboratory scale investigation[J]. Chemical Engineering Journal, 2013, 225: 93-99. DOI:10.1016/j.cej.2013.03.074 |
| [23] | Ajmal Z, Muhmood A, Usman M, et al. Phosphate removal from aqueous solution using iron oxides:adsorption, desorption and regeneration characteristics[J]. Journal of Colloid and Interface Science, 2018, 528: 145-155. DOI:10.1016/j.jcis.2018.05.084 |
| [24] |
林建伟, 李佳, 詹艳慧. 磷酸盐改性方解石去除水中磷酸盐研究[J]. 生态环境学报, 2013, 22(9): 1594-1601. Lin J W, Li J, Zhan Y H. Removal of phosphate from aqueous solution by phosphate-modified calcite[J]. Ecology and Environmental Sciences, 2013, 22(9): 1594-1601. |
| [25] | Sø H U, Postma D, Jakobsen R, et al. Sorption of phosphate onto calcite; results from batch experiments and surface complexation modeling[J]. Geochimica et Cosmochimica Acta, 2011, 75(10): 2911-2923. DOI:10.1016/j.gca.2011.02.031 |
| [26] | Li Z X, Sun X W, Huang L D, et al. Phosphate adsorption and precipitation on calcite under calco-carbonic equilibrium condition[J]. Chemosphere, 2017, 183: 419-428. DOI:10.1016/j.chemosphere.2017.05.139 |
| [27] | Liu Y, Sheng X, Dong Y H, et al. Removal of high-concentration phosphate by calcite:effect of sulfate and pH[J]. Desalination, 2012, 289: 66-71. DOI:10.1016/j.desal.2012.01.011 |
| [28] | Karageorgiou K, Paschalis M, Anastassakis G N. Removal of phosphate species from solution by adsorption onto calcite used as natural adsorbent[J]. Journal of Hazardous Materials, 2007, 139(3): 447-452. DOI:10.1016/j.jhazmat.2006.02.038 |
| [29] |
李振炫, 刁家勇, 黄利东, 等. 开放系统下方解石对磷的去除[J]. 环境科学, 2015, 36(12): 4523-4530. Li Z X, Diao J Y, Huang L D, et al. Removal of phosphate by calcite in open-system[J]. Environmental Science, 2015, 36(12): 4523-4530. |
| [30] |
林建伟, 朱志良, 赵建夫, 等. 方解石去除水中磷酸盐的影响因素研究[J]. 中国给水排水, 2006, 22(15): 67-70. Lin J W, Zhu Z L, Zhao J F, et al. Influencing factors of efficiency of phosphate removal by calcite[J]. China Water & Wastewater, 2006, 22(15): 67-70. |
| [31] | Shahid M K, Kim Y, Choi Y G. Magnetite synthesis using iron oxide waste and its application for phosphate adsorption with column and batch reactors[J]. Chemical Engineering Research and Design, 2019, 148: 169-179. DOI:10.1016/j.cherd.2019.06.001 |
| [32] | Gypser S, Hirsch F, Schleicher A M, et al. Impact of crystalline and amorphous iron- and aluminum hydroxides on mechanisms of phosphate adsorption and desorption[J]. Journal of Environmental Sciences, 2018, 70: 175-189. DOI:10.1016/j.jes.2017.12.001 |
| [33] | Zhang H L, Elskens M, Chen G X, et al. Phosphate adsorption on hydrous ferric oxide (HFO) at different salinities and pHs[J]. Chemosphere, 2019, 225: 352-359. DOI:10.1016/j.chemosphere.2019.03.068 |
| [34] | Qiao H H, Mei L P, Chen G J, et al. Adsorption of nitrate and phosphate from aqueous solution using amine cross-linked tea wastes[J]. Applied Surface Science, 2019, 483: 114-122. DOI:10.1016/j.apsusc.2019.03.147 |
| [35] | Tran H N, You S J, Hosseini-Bandegharaei A, et al. Mistakes and inconsistencies regarding adsorption of contaminants from aqueous solutions:a critical review[J]. Water Research, 2017, 120: 88-116. DOI:10.1016/j.watres.2017.04.014 |
| [36] | D'Arcy M, Weiss D, Bluck M, et al. Adsorption kinetics, capacity and mechanism of arsenate and phosphate on a bifunctional TiO2-Fe2O3 bi-composite[J]. Journal of Colloid and Interface Science, 2011, 364(1): 205-212. DOI:10.1016/j.jcis.2011.08.023 |
| [37] | Liu T Z, Wang H, Zhang Z, et al. Application of synthetic iron-oxide coated zeolite for the pollution control of river sediments[J]. Chemosphere, 2017, 180: 160-168. DOI:10.1016/j.chemosphere.2017.04.023 |
| [38] | Boujelben N, Bouzid J, Elouear Z, et al. Phosphorus removal from aqueous solution using iron coated natural and engineered sorbents[J]. Journal of Hazardous Materials, 2008, 151(1): 103-110. DOI:10.1016/j.jhazmat.2007.05.057 |
| [39] | Yaghi N, Hartikainen H. Enhancement of phosphorus sorption onto light expanded clay aggregates by means of aluminum and iron oxide coatings[J]. Chemosphere, 2013, 93(9): 1879-1886. DOI:10.1016/j.chemosphere.2013.06.059 |
| [40] | Wang Z F, Shi M, Li J H, et al. Sorption of dissolved inorganic and organic phosphorus compounds onto iron-doped ceramic sand[J]. Ecological Engineering, 2013, 58: 286-295. DOI:10.1016/j.ecoleng.2013.07.052 |
| [41] |
唐登勇, 黄越, 胥瑞晨, 等. 改性芦苇生物炭对水中低浓度磷的吸附特征[J]. 环境科学, 2016, 37(6): 2195-2201. Tang D Y, Huang Y, Xu R C, et al. Adsorption behavior of low concentration phosphorus from water onto modified reed biochar[J]. Environmental Science, 2016, 37(6): 2195-2201. |
| [42] |
陆燕勤, 朱丽, 何昭菊, 等. 沸石负载氧化铁吸附剂吸附除磷研究[J]. 环境工程, 2015, 33(4): 48-52. Lu Y Q, Zhu L, He Z J, et al. Phosphorus adsorption from wastewater by iron-oxide-coated-zeolite[J]. Environmental Engineering, 2015, 33(4): 48-52. |
| [43] | 梁美娜, 王敦球, 朱义年, 等. 甘蔗渣活性炭/纳米氧化铁对磷的吸附作用[J]. 环境化学, 2012, 31(8): 1279-1280. |
| [44] | Braun J C A, Borba C E, Godinho M, et al. Phosphorus adsorption in Fe-loaded activated carbon:two-site monolayer equilibrium model and phenomenological kinetic description[J]. Chemical Engineering Journal, 2019, 361: 751-763. DOI:10.1016/j.cej.2018.12.073 |
| [45] | Song Y H, Hahn H H, Hoffmann E. Effects of solution conditions on the precipitation of phosphate for recovery:a thermodynamic evaluation[J]. Chemosphere, 2002, 48(10): 1029-1034. DOI:10.1016/S0045-6535(02)00183-2 |
| [46] | Gao L, Zhang L H, Hou J Z, et al. Decomposition of macroalgal blooms influences phosphorus release from the sediments and implications for coastal restoration in Swan Lake, Shandong, China[J]. Ecological Engineering, 2013, 60: 19-28. DOI:10.1016/j.ecoleng.2013.07.055 |
| [47] | Wang C H, Bai L L, Pei Y S. Assessing the stability of phosphorus in lake sediments amended with water treatment residuals[J]. Journal of Environmental Management, 2013, 122: 31-36. DOI:10.1016/j.jenvman.2013.03.007 |
| [48] | Chen M S, Ding S M, Liu L, et al. Kinetics of phosphorus release from sediments and its relationship with iron speciation influenced by the mussel (Corbicula fluminea) bioturbation[J]. Science of the Total Environment, 2016, 542: 833-840. DOI:10.1016/j.scitotenv.2015.10.155 |
| [49] | Copetti D, Finsterle K, Marziali L, et al. Eutrophication management in surface waters using lanthanum modified bentonite:a review[J]. Water Research, 2016, 97: 162-174. DOI:10.1016/j.watres.2015.11.056 |
| [50] | Reitzel K, Balslev K A, Jensen H S. The influence of lake water alkalinity and humic substances on particle dispersion and lanthanum desorption from a lanthanum modified bentonite[J]. Water Research, 2017, 125: 191-200. DOI:10.1016/j.watres.2017.08.044 |
| [51] | Yu J H, Ding S M, Zhong J C, et al. Evaluation of simulated dredging to control internal phosphorus release from sediments:focused on phosphorus transfer and resupply across the sediment-water interface[J]. Science of the Total Environment, 2017, 592: 662-673. DOI:10.1016/j.scitotenv.2017.02.219 |
| [52] | Meis S, Spears B M, Maberly S C, et al. Sediment amendment with Phoslock® in Clatto Reservoir (Dundee, UK):investigating changes in sediment elemental composition and phosphorus fractionation[J]. Journal of Environmental Management, 2012, 93(1): 185-193. DOI:10.1016/j.jenvman.2011.09.015 |
| [53] |
黄清辉, 王子健. 淡水环境磷的生物有效性评估方法的发展动态[J]. 安全与环境学报, 2006, 6(3): 132-136. Huang Q H, Wang Z J. Review on the development trend of the methods assessing phosphorus bioavailability in freshwater environment[J]. Journal of Safety and Environment, 2006, 6(3): 132-136. |
 2020, Vol. 41
2020, Vol. 41



