2. 西安建筑科技大学西北水资源与环境生态教育部重点实验室, 西安 710055;
3. 中国恩菲工程技术有限公司成都分公司, 成都 610000
2. Key Laboratory of Northwest Water Resource, Environment and Ecology, Ministry of Education, Xi'an University of Architecture and Technology, Xi'an 710055, China;
3. China ENFI Engineering Co., Ltd., Chengdu Branch, Chengdu 610000, China
传统生物脱氮是指利用微生物的同化或异化作用, 在适当条件下将有机氮转化为无机氮, 最后转化为气态氮或微生物细胞内源氮而去除的过程, 是城市污水脱氮处理的重要方法.然而, 此技术存在基建面积和运行成本大、水力停留时间长、硝化效果和系统抗冲击能力差以及造成N2O等温室气体大量排放等问题[1].
高效、低成本生物脱氮新工艺的探索和研究, 是近年废水生物脱氮领域的热点.异养硝化细菌的发现, 为生物脱氮提供了新的思路.异养硝化菌相对于自养硝化菌而言, 具有生长速率快、细胞产量高、所需溶解氧浓度低、耐酸性强等优点, 在特定环境下具有良好的脱氮效果[2-4].然而, 由于异养硝化微生物自身的多样性, 使其异养硝化机制的研究变得困难, 而相关研究的匮乏使得目前对异养硝化细菌本身特性及脱氮能力水平仍不明确.目前, 对于异养硝化细菌的研究多集中于氮素的去除效率以及最佳条件的探究, 对脱氮产物的生成特性及机制等方面的研究尚不完整.部分研究认为异养硝化过程均存在N2O的累积[5], 而另一些研究发现异养硝化细菌脱氮过程较传统脱氮过程更为彻底, 反应产物主要以N2为主, 而非N2O[6, 7], 异养硝化过程脱氮产物认识的巨大差异将直接限制异养硝化细菌脱氮机制的探究和实际工程的应用.因此, 加强异养硝化细菌脱氮产物生成特性的研究, 不仅有助于控逸异养硝化脱氮过程中温室气体N2O的排放, 而且对丰富异养硝化脱氮理论具有重要的意义.
本文对高效异养硝化细菌Pseudomonas aeruginosa YL的生理生化特征、异养硝化-好氧反硝化过程和N2O产生特性进行研究, 从氮素转化、反硝化功能基因扩增、气态氮生成及其环境影响因子等角度进行分析, 探究异养硝化细菌P. aeruginosa YL的异养硝化-好氧反硝化能力和脱氮产物的生成机制.
1 材料与方法 1.1 菌株来源异养硝化菌株Pseudomonas aeruginosa YL(GenBank ID: # KJ765709)筛选于实验室活性污泥系统, 纯化后于25%的甘油中冷冻保存[8].
1.2 培养基亚硝酸盐培养基(g ·L-1):琥珀酸钠5.62, NaNO2 0.49, 微量元素溶液2 mL, pH=7.0.
硝酸盐培养基(g ·L-1):琥珀酸钠5.62, KNO3 0.72, 微量元素溶液2 mL, pH=7.0.
异养硝化培养基(g ·L-1):琥珀酸钠5.62, (NH4)2SO4 0.47, 维氏盐溶液50 mL, pH=7.0.
微量元素溶液(g ·L-1):CuSO4 ·5H2O 1.57, CoCl2 ·6H2O 1.60, ZnSO4 ·7H2O 2.2, FeSO4 5.0, MnCl2 ·4H2O 5.06, CaCl2 5.5, Na2EDTA 50.0.
维氏盐溶液(g ·L-1):MgSO4 ·7H2O 2.5, NaCl 2.5, MnSO4 ·4H2O 0.05, FeSO4 ·7H2O 0.05, K2HPO4 ·3H2O 5.0.
1.3 菌株形态及生理生化分析取冷冻保存的YL菌液于异养硝化培养基中活化, 利用接种环蘸取少量菌液在异养硝化固体培养基中均匀划线, 30℃下恒温培养2 d后观察菌落特征;将活化后菌株YL进行革兰氏染色, 菌株个体形态特征通过显微镜以及扫描电镜进行观测;菌株生理生化特性依据文献[9]进行分析.
1.4 反硝化功能酶基因PCR扩增采用细菌DNA提取试剂盒(沃特森, 上海)提取菌株YL基因组DNA.并将提取的DNA进行PCR扩增.使用的PCR引物序列见表 1, 反应体系为25 μL, 其中包括正反引物各1 μL, dNTP 2 μL, Ex Taq酶0.2 μL, 10×Buffer 2.5 μL, DNA模板2 μL, ddH2O 16.3 μL.反应条件如表 2所示, PCR扩增产物检测采用1%琼脂糖凝胶电泳, 经核酸染料染色后, 通过凝胶成像系统拍照(G:Box EF, Syngene, USA).
|
|
表 1 PCR引物 Table 1 PCR primers |
|
|
表 2 PCR反应条件 Table 2 PCR reaction conditions |
1.5 异养硝化和好氧反硝化过程及脱氮产物生成特性
分别使用初始浓度均为100 mg ·L-1的氨氮、亚硝酸盐氮和硝酸盐氮作为单一氮源, 以琥珀酸钠为碳源, 在接种量为1%、C/N为10、r为160 r ·min-1、温度为30℃条件下于装有100 mL培养基的250 mL锥形瓶中振荡培养, 锥形瓶采用橡胶塞密封, 试验前通过玻璃管向瓶中鼓入充足纯氧, 采用无菌封口膜密封后放入摇床培养48 h, 定时测定氮浓度、D600和气态氮变化.
1.6 不同反应条件对菌株YL脱氮产物N2O生成的影响改变单一影响因子, 固定其余条件不变, 分别研究碳源、C/N、pH、温度、氨氮和亚硝酸盐氮初始浓度对脱氮产物生成的影响.固定基准条件为氨氮浓度100 mg ·L-1、亚硝酸盐氮浓度0 mg ·L-1、温度30℃、pH 7.0、C/N 10以及转速160 r ·min-1.影响因子如下:碳源包括葡萄糖、乙酸钠、蔗糖、柠檬酸钠和琥珀酸钠;C/N为2、5、10和15;pH分别为5、6、7、8、9、10和11;温度为10、20、30和37℃;初始氨氮浓度取50、200、500和1 000 mg ·L-1;亚硝酸盐氮浓度分别取100和200 mg ·L-1.菌株YL以1%接种量接种至经高压灭菌装有100 mL不同培养基的250 mL锥形瓶中, 试验前通过玻璃管向橡胶塞密封的锥形瓶中鼓入纯氧, 采用无菌封口膜密封后摇床培养48 h, 期间测定N2O生成量.
1.7 分析方法采用吸光度法测定菌体生长吸光度(D600);分别采用纳氏试剂光度法、N-(1-萘基)-乙二胺光度法、酚二磺酸光度法以及过硫酸钾氧化-紫外分光光度法测定NH4+-N、NO2--N、NO3--N和TN浓度[10];采用气相色谱法测定N2O、N2、O2[11]. N2O释放因子为N2O-N占去除NH4+-N的比例.
2 结果与讨论 2.1 菌株形态和生理生化特征菌株YL的菌体呈杆状, 无芽孢, 无鞭毛, 革兰氏阴性, 大小为0.5 μm×(1.0~1.5) μm.菌落为蓝绿色, 不透明、不规则、表面扁平湿润, 直径约2~3 mm.生理生化检测结果如表 3所示, YL能够利用柠檬酸盐, 不能进行淀粉水解, 接触酶、氧化酶、硝酸盐还原试验阳性, V.P测定、吲哚、甲基红呈阴性.
|
|
表 3 菌株YL的生理生化特征1) Table 3 Chemical and physical characteristics of strain YL |
2.2 菌株YL异养硝化-好氧反硝化脱氮特性分析 2.2.1 异养硝化特性
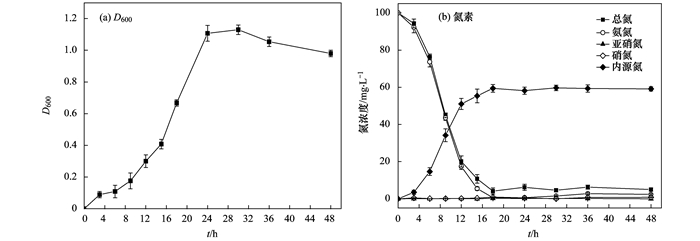
菌株YL在异养硝化过程中的生长情况如图 1(a)所示.菌株在前6 h生长缓慢, D600较低, 菌株YL处于适应期.对数生长期生长速度加快, 约24 h时趋于稳定, 生长期间最大比生长速率达到0.28 h-1, D600最大值为1.13.培养30 h之后, 菌株YL进入内源呼吸期, 在此阶段细菌细胞大量裂解使得D600值有所降低.
|
图 1 以氨氮为唯一氮源时的D600和氮素变化情况 Fig. 1 Changes in D600 and nitrogen compounds when ammonium was used as sole nitrogen source |
图 1(b)为菌株YL在异养硝化过程中的氨氮去除以及中间产物生成情况, NH4+-N在24 h内几乎完全去除, 最大去除率为99.37%, 最大氨氮去除速率为7.05 mg ·(L ·h)-1, 显著高于Pseudomonas alcaligenes AS-1[12]、Pseudomonas sp. ADN-42[13]等其它异养硝化细菌.反应后期NH4+-N浓度逐渐增加, 此时菌群进入内源呼吸期, 将之前用于细胞合成的氮素又再次分解为NH4+-N.菌株YL异养硝化过程中仅有少量的硝化中间产物NO2--N和NO3--N生成, 约59.15 mg氮素转化为内源氮, 占去除TN的62.25%.反应48 h后, TN和NH4+-N最终去除率分别为95.02%和97.63%.
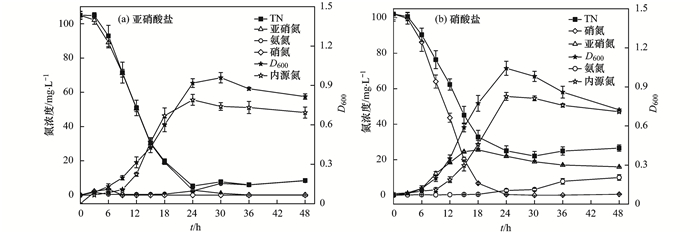
2.2.2 好氧反硝化特性当亚硝酸盐和硝酸盐作为单一氮源时, 菌株YL氮素降解过程和中间产物变化情况如图 2所示.菌株YL分别可以利用亚硝酸盐和硝酸盐作为氮源进行生长代谢, 但相较于以氨氮为氮源时, 其生长适应期更长, D600在24~30 h取得最大值0.96和1.04.以亚硝酸盐为唯一氮源时, 在12~15 h时, 菌株YL出现最大比生长速率0.17 h-1和NO2--N最大降解速率6.85 mg ·(L ·h)-1, NO2--N和TN的最终去除率分别为99.95%和91.95%, 显著高于Acinetobacter sp. HA2[14]等细菌.去除的TN中约48.15 mg转化为内源氮, 占去除TN的49.88%.反应24 h后, 由于菌体进入内源呼吸期, 死亡的菌体所释放的有机氮被转化为NH4+-N从而导致其浓度逐渐升高.当以硝酸盐作为唯一氮源时, 菌株YL最大比生长速率和NO3--N最大降解速率出现在12~15h, 分别为0.19 h-1和7.30 mg ·(L ·h)-1, NO3--N和TN最终去除率分别为99.44%和73.95%, 其中62.34%的TN(47.02mg)转化为内源氮.反应过程出现明显的NO2--N累积, 此现象与Acinetobacter junii YB[15]和Aeromonas sp. HN-02[16]一致, 在18 h时达到最大累积量25.55 mg ·L-1.反应末期TN以NH4+-N和NO2--N形式存在, 主要是反硝化不完全以及菌体进入内源呼吸期释放NH4+-N所致.
|
图 2 以亚硝酸盐和硝酸盐为唯一氮源时菌株YL的好氧反硝化性能 Fig. 2 Capabilities of aerobic denitrification by strain YL when nitrite and nitrate were used as sole N-sources |
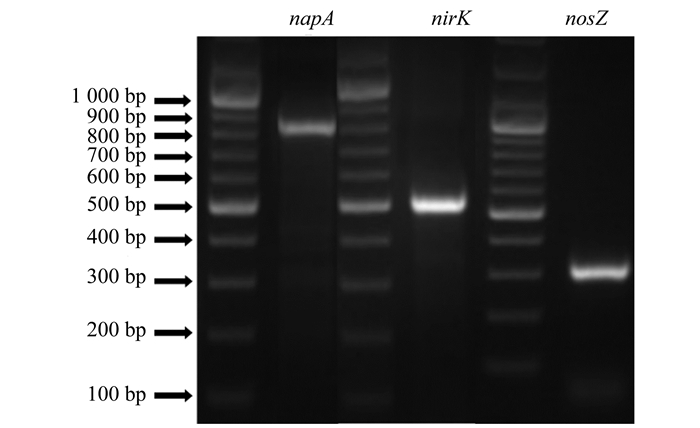
硝酸盐还原酶(Nar)参与好氧反硝化中硝酸盐还原为亚硝酸盐的过程, 在好氧反硝化的过程中优先表达周质Nar[17].由图 3可知, 利用引物NAP1/NAP2对菌株YL进行Nar基因扩增, 于870 bp左右处观察到清晰的目标条带, 对应周质Nar的大亚基napA基因.亚硝酸盐还原酶(Nir)可以将亚硝酸盐还原转化为氮氧化物, 利用引物nirK1F/nirK5R和nirS1F/nirS6R对菌株YL进行DNA扩增, 仅在514bp左右一处发现了清晰的特异性条带, 推测是菌株细胞内基因nirK成功表达, 而nirS未能表达.此结果与一种细菌中只有一类Nir存在相一致[18].氧化亚氮还原酶(Nos)可以将氧化亚氮还原为氮气, 利用引物nosLb/nosRb对菌株YL的DNA进行扩增, 结果表明试验菌株的特异性条带出现在300 bp左右, 与Pseudomonas stutzeri[19]、Halomonas campisalis[20]和Pseudomonas migulae AN-1[21]等细菌相同, 证明nosZ在菌株YL中可成功表达.本研究中napA、nirK和nosZ基因的成功表达可以证明菌株YL存在Nir、Nar和Nos, 具有完整的反硝化酶系及好氧反硝化的能力.
|
图 3 菌株YL的napA、nirK和nosZ基因PCR扩增 Fig. 3 PCR amplification of napA, nirK, and nosZ genes in strain YL |
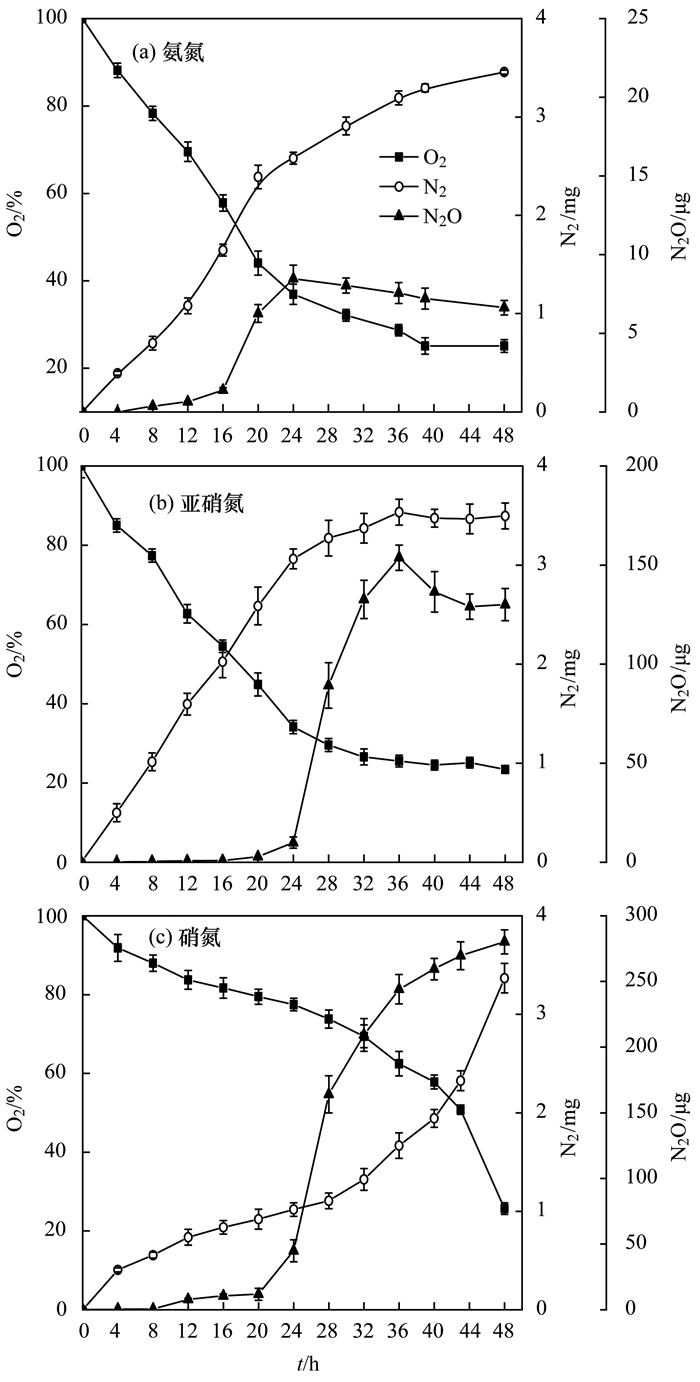
菌株YL以NH4+-N为氮源时的脱氮产物生成情况如图 4(a)所示, 经过48 h反应, 气相中O2含量由初始的100%最终降为25.11%, 共消耗74.89%的O2, 说明摇瓶中的O2足以保证系统处于好氧状态.菌株YL在反应初期即生成N2, 反应3~4 h后N2生成量为0.39 mg, 表明菌株在接入培养基初期便开始进行异养硝化-好氧反硝化作用.在反应9~12 h左右NH4+-N基本降解完全, 但却有大量N2生成, 推测原因可能是菌体生长过程中大量NH4+-N转移至体内并在胞内酶体系作用下完成硝化与反硝化作用, 反应完成后一部分氮素才以N2形式排放.反应末期, 菌株YL氮气生成量共3.46 mg, 约占去除TN的36.41%, 而N2O生成量很低, 其产生量在DO下降到50%后快速增加, 最终为6.63 μg.此外, 一般认为逸出的N2O难以再溶于液相, 从图中可以看出, 菌株YL的N2O生成量达到最大后, 气相中N2O含量出现降低现象, 推测是摇瓶为封闭系统, 逸出到气相中的N2O分压逐渐增大, 随着反应进行液相中溶解N2O逐渐消耗完全, 逸出的N2O仍可以再缓慢溶于液相中.
|
图 4 菌株YL以氨氮、亚硝氮和硝氮为唯一氮源时气态氮变化情况 Fig. 4 Changes in gaseous constituents by strain YL when ammonia, nitrite and nitrate were used as the sole N-sources |
如图 4(b)所示, 以NO2--N为唯一氮源时, 反应48 h菌株YL消耗76.57%的O2, 反应结束气相中残留23.43%的O2, 保证了系统的好氧状态.反应4 h氮气生成量为0.51 mg, 相较于以NH4+-N为唯一氮源时菌株脱氮相对更快, 表明菌株YL的反硝化酶系更容易适应高浓度NO2--N条件.反应48 h后, 最终N2生成量为3.49 mg, 占去除TN的36.15%.此外, 试验菌株在利用NO2--N时的N2O生成量相较于NH4+-N明显增大, 反应38 h达到最大生成量153.74 μg, 而后逐渐降低.从气相组分变化情况来看, N2O大量生成发生在O2迅速降低后, 因此除了高浓度NO2--N对Nos抑制外, 低DO也是导致N2O大量增加的原因之一.
2.3.3 以硝酸盐氮为唯一氮源时脱氮产物生成情况以NO3--N为唯一氮源时, 图 4(c)显示反应48 h菌株YL消耗74.29%的O2, 反应结束气相中残留25.71%的O2.菌株YL在反应前期N2生成速率缓慢, 反应24 h生成量仅为1.02 mg, 24 h后N2生成速率明显加快并在48 h达到最大.从N2生成速率上看, 相较于NO2--N和NH4+-N, 以NO3--N为氮源时N2生成明显滞后, 菌株YL反硝化活性可能受到游离亚硝酸的抑制, 这与NO3--N反硝化过程较高的NO2--N累积相一致.此外, 菌株YL以NO3--N为氮源时N2O生成量在3种氮源中最大, 反应24 h后N2O释放急剧增加, 在46 h达到最大值293.98 μg, 此现象与NO2--N为氮源时类似, 均是随O2显著降低后快速升高.
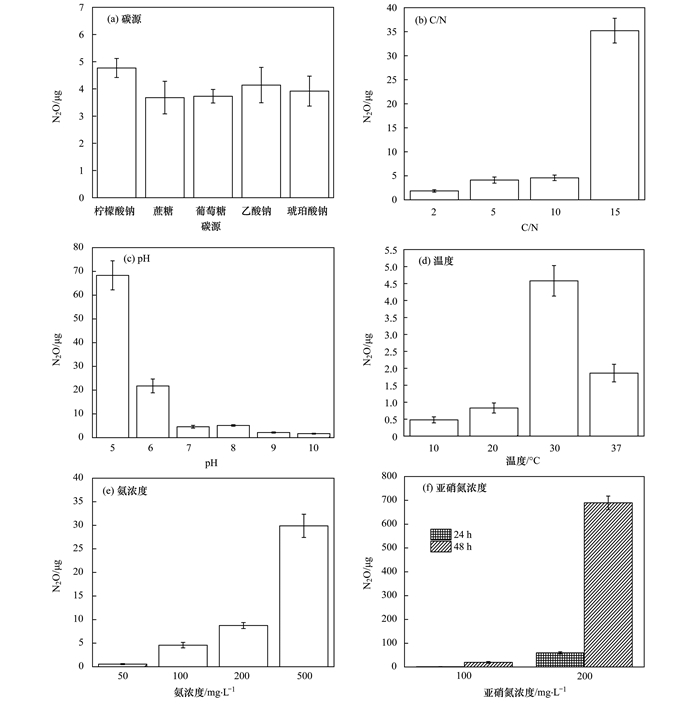
2.3.4 环境因子对N2O生成的影响(1)碳源 如图 5(a)所示, 在柠檬酸钠、蔗糖、葡萄糖、乙酸钠和琥珀酸钠这5种碳源条件下, 菌株YL的N2O生成量大致相同, 分别为4.77、3.68、3.73、4.14和3.92 μg, 其中利用柠檬酸钠等有机酸时生成量略大.前期研究表明碳源的化学结构以及分子质量会对菌株YL异养硝化性能造成影响, 小分子有机酸为碳源条件时的异养硝化效果显著优于大分子糖类为碳源时的情况[8].通过计算, 糖类培养基中N2O释放因子(1.21‰~1.93‰)相对其它几种有机酸碳源(0.42‰~0.53‰)更大, 原因可能是可利用碳源不足时, N2O还原酶相比其它反硝化酶的得电子能力相对较弱[22].因此, 在以有机酸为碳源时, 菌株YL不仅能更好地进行异养硝化作用, 且N2O释放量低.
|
图 5 环境因子对菌株YL异养硝化-好氧反硝化过程N2O产生的影响 Fig. 5 Effects of environmental factors on N2O production during heterotrophic nitrification-aerobic denitrification of strain YL |
(2) C/N 如图 5(b)所示, 在低C/N条件(C/N=2和5), N2O生成量较低, 菌株YL的N2O生成量随C/N比升高而增大.当C/N比从2增到15时, N2O生成量从1.85 μg大幅增加至35.20 μg, 说明高C/N比会促进N2O的生成.而C/N为2和5时的N2O释放因子分别为0.51‰和0.64‰, 均高于C/N=10时的情况(0.49‰), 可能是由于低C/N比条件反硝化不完全和中间产物积累等原因.此外, 当C/N=15, 菌株YL的N2O生成量和释放因子(3.90‰)均大幅增加, 这一结果与C/N高于10会导致脱氮过程中N2O释放增加的结论一致[23].
(3) pH 菌株YL在不同pH(5~10)条件下的N2O生成情况如图 5(c)所示, 反应24 h后N2O生成量分别为68.35、21.78、4.58、5.13、2.16和1.68 μg, 对应的N2O释放因子分别为7.74‰、2.38‰、0.49‰、0.52‰、0.22‰和0.21‰.菌株YL的N2O生成量随pH降低而逐渐增加, 这与Kesik等[24]研究结论较为一致, 菌株Alcaligenes faecalis sp.的N2O生成随pH降低而逐渐减少, 但当pH降低至≤4时却急剧增加, 主要原因在于酸性条件下化学反硝化作用(如亚硝酸盐的化学降解等)大大加强.因此, 酸性条件下N2O的大量生成可能主要归因于生物反硝化抑制作用和化学反硝化作用[8, 24].
(4) 温度 不同温度条件菌株YL的N2O生成量如图 5(d)所示, 低温条件N2O释放量少, 20℃时, N2O生成量及其释放因子仅为0.83 μg和0.09‰, 这可能是反硝化速率慢导致N2O生成量下降或低温条件下N2O溶解度提高所致.随着温度升高到30℃, YL的N2O生成量达到最大4.58 μg, 对应的N2O释放因子为0.49‰.当温度进一步提高到37℃时, 分离菌株的N2O生成量有所下降, 为1.86 μg, N2O释放因子(0.19‰)也随之下降.温度对菌株YL的N2O生成及释放的影响可能是由于不同温度下酶活性和代谢途经改变、酶系间对于电子供体的竞争以及酶促减缓等原因[25~27].
(5) 氨氮浓度 NH4+-N浓度被认为是导致N2O大量生成的主要因素之一.如图 5(e)所示, 菌株YL在48 h的N2O生成量随NH4+-N起始浓度的升高而增加, 50~500 mg ·L-1条件下分别为0.55、4.58、8.73和29.89 μg.此外, 氨氮浓度为50 mg ·L-1条件下N2O释放因子接近于0.10‰, 100 mg ·L-1时增加至0.49‰, 随着NH4+-N浓度升高至200和500 mg ·L-1, YL的N2O释放因子提高到0.50‰和1.28‰.高NH4+-N条件较多的N2O释放主要是由于碱性环境和NO2--N积累[15, 28], 但仍显著低于短程硝化系统(400 mg ·L-1下的N2O释放量为6.4 mg)[29]和自养硝化系统(500 mg ·L-1下的N2O释放量为33.8 mg)[30].因此, 相比于常规脱氮系统, 菌株YL不仅能抵抗高氨氮浓度的冲击[8], 而且能够有效控制污水处理过程中N2O等温室气体的排放.
(6) 亚硝酸盐氮 如图 5(f)所示, NO2--N浓度对试验菌株N2O的产生影响显著, 当NO2--N浓度由100 mg ·L-1提高到200 mg ·L-1, 反应24 h菌株YL的N2O生成量由1.49 μg增长至59.80 μg, 释放因子从0.15‰增加到5.98‰;48 h的N2O生成量由19.51 μg显著提高到689.42 μg, 释放因子从3.14‰增长至37.19‰.急剧增长的N2O释放量可能是由于高浓度NO2--N易对反硝化酶系中的氧化亚氮还原酶产生毒害作用, 导致N2O无法还原而大量积累[31].
3 结论(1) 菌株YL具有高效的异养硝化和好氧反硝化能力, 24 h培养期100 mg ·L-1的NH4+-N、NO2--N和NO3--N能够完全去除, 且异养硝化过程几乎无中间产物生成.同时, 反硝化功能基因napA、nirK和nosZ基因PCR的成功表达, 从分子水平进一步证实菌株YL具有异养硝化和好氧反硝化特性.
(2) 菌株YL的脱氮产物主要为N2, 仅有微量的N2O生成.以NH4+-N、NO2--N和NO3--N分别为唯一氮源时, 菌株YL的N2生成量分别为3.46、3.49和3.36 mg, N2O生成量分别为6.63、153.74和293.98 μg, 气态氮产物约占去除TN的30% ~40%.
(3) 在好氧条件下, 控逸氧化亚氮释放的最佳工艺条件是:琥珀酸钠为碳源, C/N为10, pH为10, 温度为20℃.此外, 高C/N、低pH、高温、氨氮和亚硝酸盐氮积累等条件会促进N2O的生成, 但大部分条件对N2O生成量影响较小, 且最高生成量显著低于短程硝化系统和自养硝化系统, 表明试验菌株具有良好的控逸N2O释放的能力.
| [1] | Hospido A, Moreira M T, Fernández-Couto M, et al. Environmental performance of a municipal wastewater treatment plant[J]. The International Journal of Life Cycle Assessment, 2004, 9: 261-271. DOI:10.1007/BF02978602 |
| [2] | Joo H S, Hirai M, Shoda M. Piggery wastewater treatment using Alcaligenes faecalis strain No. 4 with heterotrophic nitrification and aerobic denitrification[J]. Water Research, 2006, 40(16): 3029-3036. DOI:10.1016/j.watres.2006.06.021 |
| [3] | Yao S, Ni J R, Chen Q, et al. Enrichment and characterization of a bacteria consortium capable of heterotrophic nitrification and aerobic denitrification at low temperature[J]. Bioresource Technology, 2013, 127: 151-157. DOI:10.1016/j.biortech.2012.09.098 |
| [4] | Guo L Y, Chen Q K, Fang F, et al. Application potential of a newly isolated indigenous aerobic denitrifier for nitrate and ammonium removal of eutrophic lake water[J]. Bioresource Technology, 2013, 142: 45-51. DOI:10.1016/j.biortech.2013.05.021 |
| [5] | Zhang Q L, Liu Y, Ai G M, et al. The characteristics of a novel heterotrophic nitrification-aerobic denitrification bacterium, Bacillus methylotrophicus strain L7[J]. Bioresource Technology, 2012, 108: 35-44. DOI:10.1016/j.biortech.2011.12.139 |
| [6] | Zheng M S, He D, Ma T, et al. Reducing NO and N2O emission during aerobic denitrification by newly isolated Pseudomonas stutzeri PCN-1[J]. Bioresource Technology, 2014, 162: 80-88. DOI:10.1016/j.biortech.2014.03.125 |
| [7] |
陈杰, 汪霞, 赵彬, 等. A. faecalis strain NR的包埋固定及其氨氮降解性能[J]. 环境工程学报, 2015, 10(6): 3303-3311. Chen J, Wang X, Zhao B, et al. Embedding immobilization of A. faecalis strain NR and its capability of ammonium removal[J]. Chinese Journal of Environmental Engineering, 2015, 10(6): 3303-3311. |
| [8] | Yang L, Ren Y X, Zhao S Q, et al. Isolation and characterization of three heterotrophic nitrifying-aerobic denitrifying bacteria from a sequencing batch reactor[J]. Annals of Microbiology, 2016, 66(2): 737-747. DOI:10.1007/s13213-015-1161-7 |
| [9] | 东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京: 科学出版社, 2001. |
| [10] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002: 254-279. |
| [11] | Lv Y T, Ju K, Sun T, et al. Effect of the dissolved oxygen concentration on the N2O emission from an autotrophic partial nitritation reactor treating high-ammonium wastewater[J]. International Biodeterioration & Biodegradation, 2016, 114: 209-215. |
| [12] | Su J J, Yeh K S, Tseng P W. A strain of Pseudomonas sp. isolated from piggery wastewater treatment systems with heterotrophic nitrification capability in Taiwan[J]. Current Microbiology, 2006, 53(1): 77-81. DOI:10.1007/s00284-006-0021-x |
| [13] | Jin R F, Liu T Q, Liu G F, et al. Simultaneous heterotrophic nitrification and aerobic denitrification by the marine origin bacterium Pseudomonas sp. ADN-42[J]. Applied Biochemistry and Biotechnology, 2015, 175(4): 2000-2011. DOI:10.1007/s12010-014-1406-0 |
| [14] | Yao S, Ni J R, Ma T, et al. Heterotrophic nitrification and aerobic denitrification at low temperature by a newly isolated bacterium, Acinetobacter sp. HA2[J]. Bioresource Technology, 2013, 139: 80-86. DOI:10.1016/j.biortech.2013.03.189 |
| [15] | Ren Y X, Yang L, Liang X. The characteristics of a novel heterotrophic nitrifying and aerobic denitrifying bacterium, Acinetobacter junii YB[J]. Bioresource Technology, 2014, 171: 1-9. DOI:10.1016/j.biortech.2014.08.058 |
| [16] |
陈茂霞, 王欢, 周后珍, 等. 异养硝化-好氧反硝化菌HN-02的筛选及其特性[J]. 应用与环境生物学报, 2013, 19(4): 688-693. Chen M X, Wang H, Zhou H Z, et al. Screening and characteristics of heterotrophic nitrification-aerobic denitrification strain HN-02[J]. Chinese Journal of Applied & Environmental Biology, 2013, 19(4): 688-693. |
| [17] | Yang L, Ren Y X, Liang X, et al. Nitrogen removal characteristics of a heterotrophic nitrifier Acinetobacter junii YB and its potential application for the treatment of high-strength nitrogenous wastewater[J]. Bioresource Technology, 2015, 193: 227-233. DOI:10.1016/j.biortech.2015.05.075 |
| [18] | Huang F, Pan L Q, Lv N, et al. Characterization of novel Bacillus strain N31 from mariculture water capable of halophilic heterotrophic nitrification-aerobic denitrification[J]. Journal of Bioscience and Bioengineering, 2017, 124(5): 564-571. DOI:10.1016/j.jbiosc.2017.06.008 |
| [19] | Ji B, Wang H Y, Yang K. Tolerance of an aerobic denitrifier (Pseudomonas stutzeri) to high O2concentrations[J]. Biotechnology Letters, 2014, 36(4): 719-722. DOI:10.1007/s10529-013-1417-x |
| [20] | Guo Y, Zhou X M, Li Y G, et al. Heterotrophic nitrification and aerobic denitrification by a novel Halomonas campisalis[J]. Biotechnology Letters, 2013, 35(12): 2045-2049. DOI:10.1007/s10529-013-1294-3 |
| [21] | Qu D, Wang C, Wang Y, et al. Heterotrophic nitrification and aerobic denitrification by a novel groundwater origin cold-adapted bacterium at low temperatures[J]. RSC Advances, 2015, 5: 5149-5157. DOI:10.1039/C4RA13141J |
| [22] | Zhang X W, Wang X Q, Zhang J, et al. Reduction of nitrous oxide emissions from partial nitrification process by using innovative carbon source (mannitol)[J]. Bioresource Technology, 2016, 218: 789-795. DOI:10.1016/j.biortech.2016.07.043 |
| [23] | Otte S, Schalk J, Kuenen J G, et al. Hydroxylamine oxidation and subsequent nitrous oxide production by the heterotrophic ammonia oxidizer Alcaligenes faecalis[J]. Applied Microbiology and Biotechnology, 1999, 51(2): 255-261. DOI:10.1007/s002530051390 |
| [24] | Kesik M, Blagodatsky S, Papen H, et al. Effect of pH, temperature and substrate on N2O, NO and CO2 production by Alcaligenes faecalis p.[J]. Journal of Applied Microbiology, 2006, 101(3): 655-667. DOI:10.1111/j.1365-2672.2006.02927.x |
| [25] | Li H, Pan M L, Zhou S F, et al. Characterization of nitrous oxide emissions from a thermophilic denitrifying bacterium Chelatococcus daeguensis TAD1 in an aerated sequencing batch reactor[J]. Biochemical Engineering Journal, 2016, 112: 233-240. DOI:10.1016/j.bej.2016.04.033 |
| [26] | Adouani N, Limousy L, Lendormi T, et al. N2O and NO emissions during wastewater denitrification step:influence of temperature on the biological process[J]. Comptes Rendus Chimie, 2015, 18(1): 15-22. DOI:10.1016/j.crci.2014.11.005 |
| [27] | Wang X J, Yang X R, Zhang Z J, et al. Long-term effect of temperature on N2O emission from the denitrifying activated sludge[J]. Journal of Bioscience and Bioengineering, 2014, 117(3): 298-304. DOI:10.1016/j.jbiosc.2013.08.009 |
| [28] | Zhao B, An Q, He Y L, et al. N2O and N2 production during heterotrophic nitrification by Alcaligenes faecalis strain NR[J]. Bioresource Technology, 2012, 116: 379-385. DOI:10.1016/j.biortech.2012.03.113 |
| [29] |
吴娟, 张建, 贾文林, 等. 人工湿地污水处理系统中氧化亚氮的释放规律研究[J]. 环境科学, 2009, 30(11): 3146-3151. Wu J, Zhang J, Jia W L, et al. Nitrous oxide fluxes of constructed wetlands to treat sewage wastewater[J]. Environmental Science, 2009, 30(11): 3146-3151. DOI:10.3321/j.issn:0250-3301.2009.11.005 |
| [30] | Kong Q. Impact of ammonium and salinity concentrations on nitrous oxide emission in partial nitrification system[J]. KSCE Journal of Civil Engineering, 2015, 19(4): 873-879. DOI:10.1007/s12205-014-0035-z |
| [31] | Alinsafi A, Adouani N, Béline F, et al. Nitrite effect on nitrous oxide emission from denitrifying activated sludge[J]. Process Biochemistry, 2008, 43(6): 683-689. DOI:10.1016/j.procbio.2008.02.008 |
 2020, Vol. 41
2020, Vol. 41


