2. 合肥工业大学纳米矿物与污染控制安徽普通高校重点实验室, 合肥 230009
2. Key Laboratory of Nano minerals and Pollution Control of Anhui Higher Education Institutes, Hefei University of Technology, Hefei 230009, China
随着城市污水厂建设规模和数量的日益增加, 污水厂尾水排放量越来越大, 由尾水排放带来的生态环境问题引起人们的关注[1].由于污水脱氮除磷工艺技术的局限性, 使得尾水中氮、磷负荷依旧较高, 从而影响河流水质和水生态系统健康.此外, 城市污水厂尾水往往具有微生物可利用性碳源含量偏低的特点[2], 使得河流生源物质循环过程变得更为复杂.磷是水体富营养化的主要限制性因子, 沉积物充当磷“源”或“汇”的何种角色, 往往受到磷平衡浓度(EPC0)与上覆水可溶性磷酸盐浓度相对大小的控制.一般地, EPC0值越高, 沉积物向水体释放磷的风险相对越大[3, 4], 反之则越小.截至目前, 针对河流底质磷平衡浓度的研究已有很多[5, 6], 特别是沉积物性质和环境因素对EPC0值的影响颇受关注[7, 8], 而对污水厂尾水排入可能带来的沉积物EPC0变化及磷释放风险影响还关注不足.Stutter等[9]的研究表明, 污水厂尾水使河道悬浮沉积物EPC0值增大, 但由此导致的河流水环境水生态退化则可以通过调控内源磷释放加以缓解.当前, 我国城市地区河流受污水厂尾水影响情况极为普遍, 从水污染防治和水生态保护角度来看, 有必要针对该情形下河流沉积物磷形态及磷释放风险调控开展专门研究.
巢湖是水体富营养化颇为严重的湖泊[10], 目前全湖水体富营养化存在逐年加重的趋势, 特别是南淝河和十五里河等入湖河口水域水华现象更为突出.据报道, 合肥城区南淝河入流补给水中90%来自污水处理厂尾水, 致使该河道整个干流都表现出较为明显的富营养化特征.李如忠等[11~13]对合肥城区污染严重的多条溪流沟渠, 开展了沉积物磷的生物非生物吸收贡献分析, 测算了沉积物的EPC0值, 但对污水厂尾水可能带来的河道沉积物磷形态及释放风险变化未给予必要的关注.本文拟以南淝河流域板桥河支流为研究对象, 就污水厂尾水汇入对沉积物磷形态和磷平衡浓度影响开展定量化分析, 解析外源碳添加对磷平衡浓度和释放风险的影响, 以期为污水厂尾水受纳河道水环境管理和水污染控制提供依据.
1 研究区概况板桥河是巢湖西半湖入湖河流南淝河的一条重要支流, 起源于合肥市长丰县境内, 横穿合肥北部城区, 全长26.30 km, 流域面积133.78 km2.该河水面平均宽约20m, 河道上口平均宽度50m, 由于河床比降较小, 整条河流水体流动较为缓慢.本研究所在河段位于城市边缘, 河道两侧为环保透水砖砌成的垂直河岸, 河滩上种植香樟、柳树等景观林木.
板桥河中上游地处城郊结合部, 下游为城市建成区.蔡田铺污水厂毗邻板桥河右侧大堤, 地处庐阳区故黄路与九顶山路交口北侧.污水厂一、二期工程设计处理规模均为5万m3 ·d-1, 分别采用氧化沟、A2/O处理工艺, 并分别于2008年和2017年投入运行.三期工程采用A2/O处理工艺, 设计处理规模为20万m3 ·d-1, 目前正处于扩建中.尾水由岸边排入河道, 由于污水厂出水的水泵提升动能转化, 在排放口附近尾水与河水掺混剧烈.采样期间的板桥河及污水厂尾水的水质统计结果见表 1.尾水排放口上、下游及尾水出流的氧化还原电位ORP值差异较为明显, 这与污水处理过程中大量曝气, 导致尾水出流的溶解氧浓度偏高、氧化性增强有关.
|
|
表 1 河流及污水厂尾水主要理化性质 Table 1 Physical and chemical properties of stream water and sewage treatment plant effluent |
2 材料与方法 2.1 采样点布设
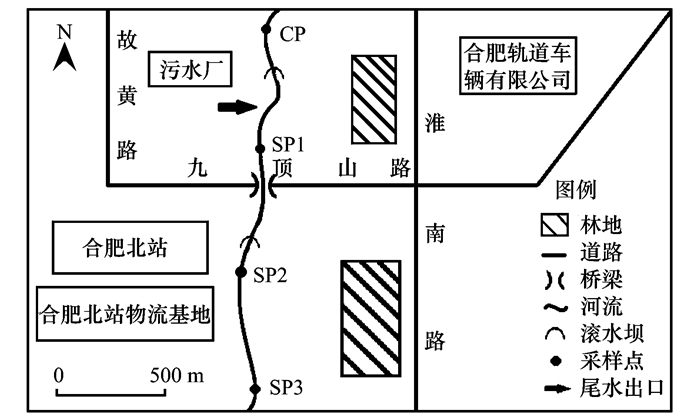
本研究在蔡田铺污水厂尾水排放口的上、下方河道, 沿水流行进方向依次布设了4个采样点位, 即CP、SP1、SP2和SP3.该河段长约2.5 km, 水面宽度25 m左右.其中, 采样点CP位于尾水排放口上游500 m处并作为对照点, 在其下方与尾水排放口之间有一座滚水坝, 水坝上、下水位落差约1 m;SP1、SP2和SP3分别位于排放口下游220、1 000和2 000 m处, 其中SP1处于河流弧形转弯处, 且在SP1和SP2之间也有一座滚水坝, 但该坝的水位落差很小, 仅有20 cm左右.在城市建成区, 板桥河沿河两侧的排污暗渠明显增多, 有些暗渠目前仍处于间歇性的违规排污状态.为尽可能排除这类排污行为的干扰, 将SP1、SP2和SP3设定在排放口下游2 000 m内暗渠或暗管较少的河段内.采样点分布大体情况, 见图 1.
|
图 1 采样点分布示意 Fig. 1 Sketch-map of distribution of sampling sites |
2018年10月~2019年4月, 按照每两个月采样一次的频率采集沉积物和上覆水样.在每个采样点0.5 m2范围内, 采集3份表层(0~5 cm)底质沉积物, 并将其充分混合以代表该点位样品.将采集的新鲜底质泥样放在实验室阴凉通风处自然风干, 剔除枯枝碎叶, 经研磨过100目尼龙筛后装入密封袋备用.现场测定上覆水EC、TDS、ORP和pH指标, 其它水质指标(表 1)均在实验室完成分析测试.
2.3 实验方案设计针对沉积物EPC0, 设计4种实验方案(表 2), 其中方案1为常见实验方法.有关实验方法的具体操作过程描述参见文献[13].考虑到污水脱氮除磷工艺需要消耗大量的碳, 从而影响到尾水中碳含量, 为此这里将方案3、4中外源碳含量提高到250 mg ·L-1.
|
|
表 2 EPC0实验条件 Table 2 EPC0 experimental conditions |
2.4 沉积物磷形态测定
采用SMT法测定沉积物总磷(TP)、无机磷(IP)、铁铝结合态磷(Fe/Al-P)和碎屑磷(Ca-P);采用提取剂为MgCl2的连续提取法, 测定沉积物易交换态磷(Ex-P).
3 结果与分析 3.1 沉积物磷形态特征4个采样点沉积物各形态磷含量, 见表 3.显然, 除2018年10月数据异常外, 其它各次采样中排污口下方各采样点沉积物TP含量均高于排放口上方对照点CP, 高低排序为SP1>SP2>SP3>CP, 即排污口下方沉积物TP呈现递减趋势.虽然2018年10月各采样点沉积物IP、Fe/Al-P含量大体相近, 但在其它时段, 则基本都表现为排放口下方更高一些, Ex-P含量也表现出了类似特征.因此, 污水厂尾水排放对受纳河段沉积物磷形态存在较为明显的影响.
|
|
表 3 沉积物不同形态磷含量/mg ·kg-1 Table 3 Phosphorus form contents in sediments/mg ·kg-1 |
表 3中各采样点底质TP含量均显著高于加拿大安大略省环境和能源部发布指南中可能引起最低级别生物毒性效应的TP含量阈值(600mg ·kg-1)[14], 也明显超过了美国国家环保署湖泊沉积物污染状况评价标准的重度污染标准(650mg ·kg-1)[15].因此, 可以认为板桥河沉积物磷污染较为严重, 生态风险水平较高.
Ex-P和Fe/Al-P易释放于水体, 属于可供水生植物及其他生物利用的潜在活性磷, 因此常被称作生物有效性磷[16].板桥河4个采样点Fe/Al-P的均值分别为290.34、314.11、310.68和319.94mg ·kg-1, 占TP的36.78%、35.60%、37.19%和37.84%;4个采样点Ex-P的均值分别为24.05、25.95、32.80和36.75mg ·kg-1, 占TP的3.05%、2.94%、3.93%和4.35%, 即Fe/Al-P和Ex-P占TP的百分比, 均表现为SP1处相对最小.Fe/Al-P含量在10月份随河流走向呈不断降低趋势, 即表现为CP>SP1>SP2>SP3, 而在2月和4月均表现为随河流走向呈不断增加的趋势, 即表现为SP3>SP2>SP1>CP.除2018年12月以外, Ex-P含量均表现出沿河水行进方向不断增加的趋势, 即表现为SP3>SP2>SP1>CP.
总体上, 对照点CP生物有效性磷占TP比重的均值为39.77%, 排放口下方3个采样点占TP比重均值为40.62%.显然, 尽管排污口上、下方沉积物的生物有效性磷量存在差异, 但占TP比重则基本相当.
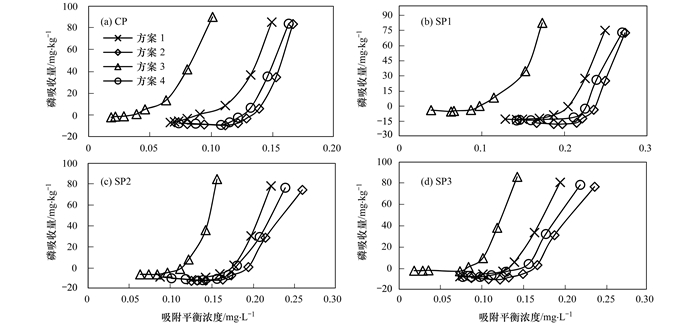
3.2 EPC0对外源碳的响应图 2为2019年4月各采样点沉积物对磷的等温吸附曲线, 相应地EPC0值及其线性拟合的可决系数R2见表 4.由图 2可知, 外源碳的添加使得各采样点的EPC0整体向左发生了偏移, 并以SP1处向左偏移最为明显.其它3次采样也都获得了与图 2相似的结果, 相应地EPC0值及其线性拟合可决系数R2, 见表 4.显然, 乙酸钠的添加显著降低了各采样点的EPC0值.
|
图 2 沉积物对磷等温吸附曲线 Fig. 2 Isothermal adsorption curve of phosphorus in sediments |
|
|
表 4 沉积物磷平衡浓度/mg·L-1 Table 4 Phosphorus equilibrium concentration of sediments/mg ·L-1 |
由表 4可见, 整个采样期间方案1的EPC0均值为0.126 mg ·L-1, 方案3为0.061 mg ·L-1, 明显低于方案1.方案2和方案4添加了抑制剂氯仿, 相应地EPC0均值分别为0.157 mg ·L-1和0.140 mg ·L-1, 两种方案EPC0值均高于方案1.总体上, 方案3均值比方案1低52%, 而方案2相较于方案1高出了25%. 4个采样点中, 各方案EPC0都表现出了相同的排序规律, 即方案3 < 方案1 < 方案4 < 方案2.
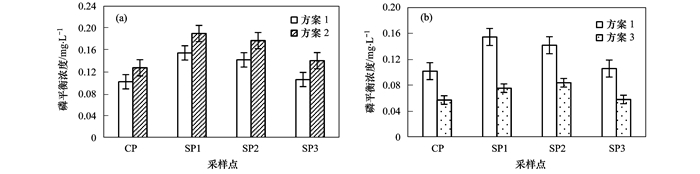
图 3为整个采样期间4个采样点位EPC0值的变化情况.其中, 图 3(a)为各采样点位EPC0值在方案1、方案2中的统计描述和比较.显然, 抑制剂的添加导致了EPC0值的增大, 并且排放口下游各采样点的绝对增幅略高于对照点CP.由于方案1的EPC0值是生物和非生物因素共同作用的结果, 而方案2仅是非生物因素的作用, 因此方案1与方案2的EPC0差值体现的正是生物作用结果.由于该差值在数值上明显低于方案2的EPC0, 更是低于方案1, 表明在沉积物磷吸收效应中生物因素不占主导地位.Griffiths等[17]在对美国沃克河流沉积物的研究中测得EPC0为0.011 mg ·L-1, 加入抑制剂后EPC0值上升到0.013 mg ·L-1;而对威斯康星州河流沉积物的研究发现, 加入抑制剂与否EPC0值都为0.010 mg ·L-1, 表明来自生物因素的沉积物磷吸收贡献也都相对较小.
|
图 3 各采样点位EPC0值变化情况 Fig. 3 Variations of EPC0 in sediments of each sampling site |
这里, 方案1中对照点CP的EPC0变化范围为0.063~0.131 mg ·L-1, 均值为0.102 mg ·L-1;SP1的EPC0值变化范围为0.111~0.184 mg ·L-1, 均值为0.154 mg ·L-1;采样点SP2和SP3的EPC0均值分别为0.142 mg ·L-1和0.106 mg ·L-1, 也都高于对照点CP.因此, 可以认为污水厂尾水的排入导致受纳河段磷平衡浓度增加.
图 3(b)为各采样点位EPC0值在方案1和方案3中的统计描述和比较.方案1与方案3的差异仅体现在是否添加外源碳, 因此两者的EPC0差值揭示的恰好是外源碳添加与否给各采样点位EPC0带来的影响.在方案3中, 采样点CP、SP1、SP2和SP3的EPC0均值分别为0.057、0.076、0.084和0.058 mg ·L-1, 较对应方案1的绝对下降幅度分别为0.045、0.078、0.058和0.048 mg ·L-1, 即排污口下方EPC0值下降更明显, 特别是采样点SP1.从图 3也可以看出, 在方案1、方案2和方案3中, 同一采样点的CP和SP3的磷平衡浓度已大体相当.
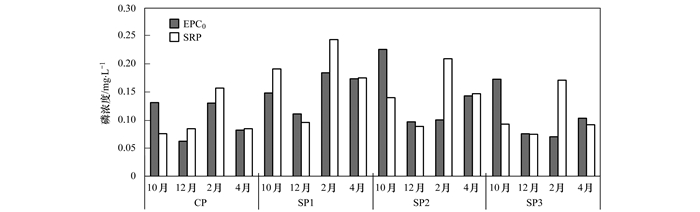
3.3 磷释放风险评估根据EPC0的生态学意义, EPC0值越高意味着沉积物向上覆水释放磷的潜力越大, 当水中SRP浓度高于EPC0时, 沉积物表现出吸附磷的趋势, 反之则表现出磷释放特征[18].因此, 比较SRP和EPC0不仅可以初步估算沉积物向水体释放磷的潜力, 也可以粗略评估磷释放风险.图 4为每个采样点位的方案1中EPC0值及其相应上覆水体SRP浓度情况对比.可以看出, 2月时4个采样点上覆水SRP浓度均明显高于相应地EPC0值, 而在4月时两者基本相当.总体上, 4个采样点沉积物发生磷吸收作用的大约6次, 磷释放作用有6次, 另有4次上覆水SRP与其相应的EPC0值基本相当.而且, 尾水排放口上、下方发生磷释放或吸收的几率大体相当.
|
图 4 各采样点沉积物EPC0与上覆水SRP浓度比较 Fig. 4 Comparison between sediment EPC0 and overlying water SRP concentration |
为更好地展示不同实验方案下各采样点沉积物磷释放风险的相对变化, 不妨以方案1中EPC0为基准, 采用下式计算各采样点位沉积物磷释放风险水平:
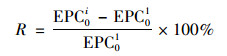
|
式中, R表示磷释放风险的相对变化率(%);EPC0i(i=2, 3, 4)分别代表方案2、方案3和方案4的EPC0值.
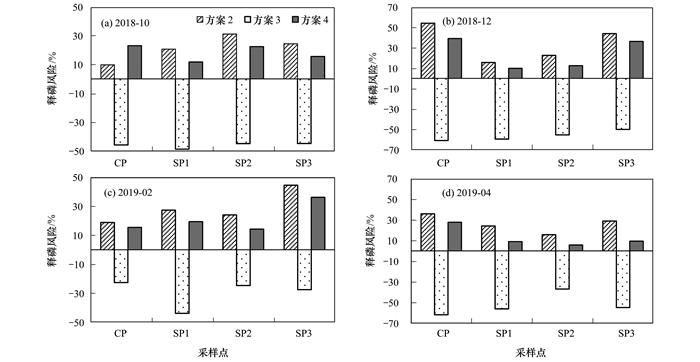
外源碳乙酸钠添加后引起的沉积物磷释放风险变化情况见图 5.在方案3中, 磷释放风险的相对变化率全部是负值, 意味着磷释放风险下降.总体上, 2018年12月各采样点沉积物磷释放风险下降幅度最大, 变化范围为-60.64% ~-49.71%, 均值为-56.15%;2019年2月磷释放风险下降幅度最小, 变化范围为-43.62% ~-22.40%, 均值为-29.44%.显然, 排放口上、下方沉积物磷释放风险变化似乎没有表现出明显的规律性.
|
图 5 各采样点位沉积物磷释放风险变化情况 Fig. 5 Variations of phosphorus release risk in sediments of each sampling site |
在添加抑制剂的方案2和方案4中, 磷释放风险的相对变化率全部为正值, 意味着沉积物磷释放风险加大.总体上, 乙酸钠的添加大幅度降低了沉积物向上覆水体释放磷的风险, 而添加抑制剂则带来沉积物磷释放风险的加大.
4 讨论微生物对碳氮磷等生源物质的吸收利用存在一定的化学计量关系[19, 20].由表 1, 板桥河水体和蔡田铺污水厂尾水的氮磷含量较高, 研究河段沉积物不仅TP含量高, 生物有效磷在TP中所占比例也很大.该河段沉积物有机质含量平均为4.14% ~8.12%, 但与沉积物中相对较高的氮磷含量相比, 有机质相对不充足.众所周知, 城市污水处理厂尾水普遍具有微生物可利用性碳源偏低的特点, 这对受纳河流碳氮磷循环过程无疑将会产生一定的限制性.可以断言, 板桥河水体和沉积物中充足的氮、磷含量, 使得生物可利用碳物质成为了影响沉积物磷生物吸收的限制性因素.这可能是方案3中各采样点EPC0值发生明显变化的主要原因.
Lottig等[21]的研究表明, 外源碳添加可以影响沉积物磷的生物吸收, 而且不同浓度碳的影响效应存在差异.Khoshmanesh等[22]的研究发现, 乙酸钠对促进沉积物的磷吸收超过了葡萄糖或葡萄糖与乙酸钠混合溶液带来的影响.李如忠等[23]在对城市重污染河流十五里河的研究中发现, 外源碳的添加不仅提升了沉积物磷的生物吸收潜力, 也提高了生物因素在沉积物磷吸收中的重要地位, 而且乙酸钠添加所带来的影响效果最显著, 其次是葡萄糖, 乙酸钠与葡萄糖混合溶液则相对较弱.本研究仅选取乙酸钠作为外源碳物质, 解析污水厂尾水受纳水体沉积物EPC0的外源碳响应, 实际上就是借鉴了上述成果.本研究也显示, 乙酸钠的添加明显降低了板桥河沉积物EPC0, 从而可以降低沉积物磷释放风险, 但对板桥河其他河段, 特别是受暗渠排污影响较大的河段是否也具有这一特点, 还需要进一步深入探讨.
本研究中对照点CP位于污水厂尾水排放口的上游, 由于与尾水排放口之间有一座滚水坝阻拦, 因此不会发生尾水上溯影响, 所以该处的各项指标值应该可以代表河流实际状况.实地调查中也发现, 在采样点SP1和SP2之间也存在一个较大的排污暗渠, 存在污水间歇性排入河道现象.在方案1和方案2中, EPC0值总体上表现为SP1>SP2>SP3>CP, 但在方案3中却发生了一些变化, 即表现为SP2>SP1>SP3>CP, 笔者以为这可能与暗渠排污对SP2造成很大影响有一定的关系.这里, 尾水排放口上、下方沉积物磷释放风险变化没有表现出明显的规律性, 可能是因为沉积物磷形态及粒度大小也影响沉积物对磷的吸收和释放[24, 25].需要特别指出的是, 本研究的相关结果仅是基于72 h培养时间而得到的, 更长培养时间可能对评价结果产生何种影响, 也还有待深入探究.
5 结论(1) 板桥河磷污染较为严重, 污水厂尾水排放对受纳河段沉积物磷形态影响明显, 总磷和生物有效性磷含量均表现为排污口下方采样点高于排污口上方的对照点, 且紧邻排污口的采样点沉积物总磷含量最高.
(2) 在污水厂尾水排放口下方沿水流前行方向, 河流沉积物EPC0值递减, 但均高于排污口上方对照点, 表明污水厂尾水提高了受纳河段EPC0水平, 致使河流磷释放风险增大.
(3) 外源碳的添加可以提高板桥河沉积物磷吸附能力、降低沉积物EPC0, 且对紧邻排放口的采样点表现相对最明显, 但总体变化规律似乎并不显著.
| [1] | Haggard B E, Storm D E, Stanley E H. Effect of a point source input on stream nutrient retention[J]. Journal of the American Water Resources Association, 2001, 37(5): 1291-1299. DOI:10.1111/j.1752-1688.2001.tb03639.x |
| [2] |
郑晓英, 朱星, 周翔, 等. 铁炭内电解垂直流人工湿地对污水厂尾水深度脱氮效果[J]. 环境科学, 2017, 38(6): 2412-2418. Zheng X Y, Zhu X, Zhou X, et al. Removal of nitrogen in municipal secondary effluent by a vertical flow constructed wetland associated with iron-carbon internal electrolysis[J]. Environmental Science, 2017, 38(6): 2412-2418. |
| [3] |
李慧, 周易勇, 余能智. 锦江河沉积物磷形态与吸附行为及磷释放风险[J]. 水生态学杂志, 2017, 38(4): 27-35. Li H, Zhou Y Y, Yu N Z. Determination of phosphorus forms and adsorption behavior of sediments in Jinjiang river and the risk of phosphorus release[J]. Journal of Hydroecology, 2017, 38(4): 27-35. |
| [4] |
于佳真, 王晓昌, 薛涛, 等. 不同温度下西安汉城湖沉积物吸附、释放特性和磷形态[J]. 环境工程学报, 2016, 10(11): 6275-6282. Yu J Z, Wang X C, Xue T, et al. Phosphorus sorption, release characteristic under different temperature and phosphorus fractions in sediments of Hancheng Lake in Xi'an[J]. Chinese Journal of Environmental Engineering, 2016, 10(11): 6275-6282. DOI:10.12030/j.cjee.201506085 |
| [5] |
易齐涛, 孙鹏飞, 谢凯, 等. 区域水化学条件对淮南采煤沉陷区水域沉积物磷吸附特征的影响研究[J]. 环境科学, 2013, 34(10): 3894-3903. Yi Q T, Sun P F, Xie K, et al. Impact of regional water chemistry on the phosphorus isothermal adsorption of the sediments in three subsidence waters of the Huainan mine areas[J]. Environmental Science, 2013, 34(10): 3894-3903. |
| [6] | Wang Q R, Li Y C. Phosphorus adsorption and desorption behavior on sediments of different origins[J]. Journal of Soils and Sediments, 2010, 10(6): 1159-1173. DOI:10.1007/s11368-010-0211-9 |
| [7] |
胡洁蕴, 李淑芹, 宋歌, 等. 北京市北运河沉积物对氮、磷的吸附/解吸动力学特征[J]. 湖泊科学, 2018, 30(3): 650-659. Hu J Y, Li S Q, Song G, et al. Adsorption/desorption dynamic characteristic of sediments on nitrogen and phosphorus in the north Grand Canal of Beijing[J]. Journal of Lake Sciences, 2018, 30(3): 650-659. |
| [8] | Pant H K, Reddy K R. Phosphorus sorption characteristics of estuarine sediments under different redox conditions[J]. Journal of Environmental Quality, 2001, 30(4): 1474-1480. DOI:10.2134/jeq2001.3041474x |
| [9] | Stutter M I, Demars B O L, Langan S J. River phosphorus cycling:separating biotic and abiotic uptake during short-term changes in sewage effluent loading[J]. Water Research, 2010, 44(15): 4425-4436. DOI:10.1016/j.watres.2010.06.014 |
| [10] | Li S S, Yuan Z W, Bi J, et al. Anthropogenic phosphorus flow analysis of Hefei City, China[J]. Science of the Total Environment, 2010, 408(23): 5715-5722. DOI:10.1016/j.scitotenv.2010.08.052 |
| [11] |
李如忠, 秦如彬, 黄青飞, 等. 不同水源补给情形的溪流沟渠沉积物磷形态及释放风险分析[J]. 环境科学, 2016, 37(9): 3375-3383. Li R Z, Qin R B, Huang Q F, et al. Fractions and release risk of phosphorus in surface sediments of three headwater streams with different styles of water supply[J]. Environmental Science, 2016, 37(9): 3375-3383. |
| [12] |
李如忠, 叶舟, 高苏蒂, 等. 人为扰动背景下城郊溪流底质磷的生物-非生物吸收潜力分析[J]. 环境科学, 2017, 38(8): 3235-3242. Li R Z, Ye Z, Gao S D, et al. Biotic and abiotic uptake of phosphorus in benthic sediments of suburban streams under intense human disturbance scenario[J]. Environmental Science, 2017, 38(8): 3235-3242. |
| [13] |
李如忠, 鲍琴, 戴源. 巢湖十五里河沉积物磷平衡浓度对外源碳的响应及释放风险[J]. 环境科学, 2019, 40(5): 2178-2185. Li R Z, Bao Q, Dai Y. Effects of exogenous carbon addition on equilibrium phosphate concentration and risk of phosphorus release from sediments in the Shiwuli river, Chaohu lake basin[J]. Environmental Science, 2019, 40(5): 2178-2185. |
| [14] |
李任伟. 沉积物污染和环境沉积学[J]. 地球科学进展, 1998, 13(4): 398-402. Li R W. Contamination of sediments and environmental sedimentology[J]. Advance in Earth Sciences, 1998, 13(4): 398-402. DOI:10.3321/j.issn:1001-8166.1998.04.013 |
| [15] | MacDonald D D, Ingersoll C G, Berger T A. Development and evaluation of consensus-based sediment quality guidelines for freshwater ecosystems[J]. Archives of Environmental Contamination and Toxicology, 2000, 39(1): 20-31. DOI:10.1007/s002440010075 |
| [16] |
李如忠, 李峰, 周爱佳, 等. 巢湖十五里河沉积物氮磷形态分布及生物有效性[J]. 环境科学, 2012, 33(5): 1503-1510. Li R Z, Li F, Zhou A J, et al. Distribution and bioavailability of nitrogen and phosphorus species in the sediments from Shiwuli stream in lake Chaohu[J]. Environmental Science, 2012, 33(5): 1503-1510. |
| [17] | Griffiths N A, Johnson L T. Influence of dual nitrogen and phosphorus additions on nutrient uptake and saturation kinetics in a forested headwater stream[J]. Freshwater Science, 2018, 37(4): 810-825. DOI:10.1086/700700 |
| [18] | 李慧, 余能智. 沉积物磷吸附解吸平衡浓度的测定及其生态学意义[J]. 资源节约与环保, 2016(9): 98-99. DOI:10.3969/j.issn.1673-2251.2016.09.072 |
| [19] | Gibson C A, O'Reilly C M. Organic matter stoichiometry influences nitrogen and phosphorus uptake in a headwater stream[J]. Freshwater Science, 2012, 31(2): 395-407. DOI:10.1899/11-033.1 |
| [20] | Schade J D, MaCneill K, Thomas S A, et al. The stoichiometry of nitrogen and phosphorus spiralling in heterotrophic and autotrophic streams[J]. Freshwater Biology, 2011, 56(3): 424-436. DOI:10.1111/j.1365-2427.2010.02509.x |
| [21] | Lottig N R, Stanley E H. Benthic sediment influence on dissolved phosphorus concentrations in a headwater stream[J]. Biogeochemistry, 2007, 84(3): 297-309. DOI:10.1007/s10533-007-9116-0 |
| [22] | Khoshmanesh A, Hart B T, Duncan A, et al. Biotic uptake and release of phosphorus by a wetland sediment[J]. Environmental Technology, 1999, 20(1): 85-91. DOI:10.1080/09593332008616796 |
| [23] |
李如忠, 鲍琴, 张瑞钢, 等. 巢湖十五里河沉积物磷吸收潜力及对外源碳的响应[J]. 环境科学, 2019, 40(6): 2730-2737. Li R Z, Bao Q, Zhang R G, et al. Potential for phosphorus uptake by bed sediments and its response to carbon additions in the Shiwuli river, Chaohu lake basin[J]. Environmental Science, 2019, 40(6): 2730-2737. |
| [24] |
刘佳, 雷丹, 李琼, 等. 黄柏河流域梯级水库沉积物磷形态特征及磷释放通量分析[J]. 环境科学, 2018, 39(4): 1608-1615. Liu J, Lei D, Li Q, et al. Characteristics of phosphorus fractions and phosphate diffusion fluxes of sediments in cascade reservoirs of the Huangbai river[J]. Environmental Science, 2018, 39(4): 1608-1615. |
| [25] | Bastami K D, Neyestani M R, Raeisi H, et al. Bioavailability and geochemical speciation of phosphorus in surface sediments of the Southern Caspian Sea[J]. Marine Pollution Bulletin, 2018, 126: 51-57. DOI:10.1016/j.marpolbul.2017.10.095 |
 2020, Vol. 41
2020, Vol. 41


