2. 江苏省农业科学院农业资源与环境研究所, 南京 210014
2. Institute of Agricultural Resources and Environment, Jiangsu Academy of Agricultural Sciences, Nanjing 210014, China
磷是生命体中必不可少的元素, 在工农业生产和生活中也占有极其重要的地位.随着经济社会的快速发展, 大量磷排入到水体中, 导致水体富营养化, 进而严重破坏生态系统[1, 2].因此, 开发高效节能的除磷技术势在必行.目前主要的除磷方法有生物除磷法、化学沉淀法、膜分离法、离子交换法和吸附法等[3~7].其中, 吸附法适用范围广, 可以用于高浓度和低浓度磷污水处理, 而且吸附法工艺简单, 成本低廉, 高选择性, 在磷污水处理领域中受到广泛关注.常见的吸附材料有硅酸盐(如蒙脱石[8]和沸石[9])、工业废料(如粉煤灰[10]和炉渣[11])、合成金属氧化物和氢氧化物(如活性氧化铝[12]和氧化铁[13])以及碳材料[14]等, 但是, 大多数吸附剂在吸附性能、可再生性和稳定性等方面存在较多缺陷, 因此, 研发高效能低成本且可回收的新型吸附剂至关重要.有研究表明负载镧的吸附剂有较强的磷吸附能力, 常用的载体材料有沸石、黏土和活性炭等, 如镧改性沸石[15]、镧掺杂二氧化硅球[16]和镧修饰的介孔稻壳生物炭[17]用于去除水体磷酸盐, 均显著增强了吸附效能.近年来, 生物炭因其较大的比表面积、丰富的空隙结构和官能团, 作为吸附剂或者纳米材料的载体方面引起广泛关注[18, 19].生物炭制备主要包括常规裂解生物炭和水热生物炭, 其中与高温裂解炭相比, 水热炭具有以下优势:制备温度低, 原料不受含水量限制, 能耗低, 产率较高, 材料表面保留了更多的含氧、氮官能团[20].目前基于水热炭为载体材料在除磷方面的研究较少.此外, 镧改性材料存在难以回收的问题, 磁性纳米材料具有高效、易分离且具有较好地可持续利用性能, 本研究组前期的工作中[21], 将纳米氧化铁负载于热解生物炭表面, 获得了可回收的除磷吸附剂, 但是吸附受pH值的限制, 且吸附能力比镧材料较低.因此本研究将磁性纳米材料Fe3O4和La(OH)3同时固定于水热炭载体材料表面, 制备了一种吸附容量高、易于磁分离回收的镧改性磁性水热生物炭复合材料(2-La-MHTC), 考察该材料对水中磷酸根吸附过程及其机制, 通过循环再生实验, 验证了该材料的可再生性能, 并考察了其处理实际污水的能力, 以期为含磷废水的处理提供新思路和技术参考.
1 材料与方法 1.1 实验材料六水合三氯化铁(≥99%, 分析纯)、抗坏血酸(99.7%, 分析纯)和氢氧化钠(≥96%, 分析纯), 国药集团化学试剂有限公司;四水合氯化亚铁(≥99%, 分析纯), 上海麦克林生化科技有限公司;七水合氯化镧(≥99%, 分析纯), 上海阿拉丁生化科技股份有限公司;盐酸(36% ~38%, 优级纯)、氨水(25% ~28%, 分析纯)和磷酸二氢钾(99.5%, 分析纯), 南京化学试剂有限公司;钼酸铵(99%, 分析纯), 天津市科密欧化学试剂有限公司;酒石酸锑钾(99%, 分析纯), 西陇化工股份有限公司.
1.2 载镧磁性水热生物炭的制备 1.2.1 秸秆水热炭制备及预处理将洗净烘干的小麦秸秆磨碎, 加入去离子水, 调整物料比为1:6, 充分搅拌后转移至反应釜中, 220℃, 4.5 MPa的条件下反应2 h, 将产物置于80℃烘箱干燥12 h.将烘干后的样品磨碎且过80目(0.178 mm)筛, 用1 mol ·L-1 HCl溶液洗涤数次后, 再用去离子水洗涤至中性, 置于80℃烘箱烘干得到水热生物炭HTC.
1.2.2 La-MHTC复合材料的制备在三颈烧瓶内加入200 mL去离子水, 室温下鼓入氮气30 min以排尽烧瓶内空气.称量2.883 g FeCl3 ·6H2O、1.060 4 g FeCl2 ·4H2O和3.961 3 g LaCl3 ·7H2O加入至水中, 充分溶解后加入0.25 g水热炭, 剧烈搅拌2 h, 再用氨水调整pH至11, 升温至80℃熟化1 h, 然后转移到反应釜中, 180℃下反应10 h, 冷却后用去离子水和无水乙醇洗涤数次, 磁性分离后置于真空烘箱内60℃干燥10 h得到载镧磁性水热炭.为了得到不同镧负载量的磁性水热炭, 调整投入的3种前驱体离子Fe3+、Fe2+和La3+摩尔比分别为2:1:0、2:1:1、2:1:2和2:1:3, 水热炭0.25 g, 得到的样品分别为MHTC、1-La-MHTC/2、2-La-MHTC/2和3-La-MHTC/2. 2-La-MHTC、La-Fe3O4复合材料与2-La-MHTC/2的合成方案基本相同, 2-La-MHTC的合成过程中水热炭添加量增加为0.5 g, La-Fe3O4的合成过程中没有添加水热炭.
1.3 表征与分析采用SmartLab型X射线衍射仪(XRD日本理学公司)分析材料的晶型结构;采用FEI 400FEG型扫描电子显微镜(SEM-EDS美国Thermo Fisher Scientific公司)观察复合材料的表面形貌;采用NicoletS10型的傅里叶红外光谱仪(美国Thermo Scientific公司)测定La-MHTC的特征官能团.采用Zetasizer Nano Zs90型电位仪(英国马尔文公司)测定磷酸盐吸附前后La-MHTC表面电荷;采用PPMS-9T型振动样品磁强计(VSM美国Quantum Design公司)测定材料的磁性;采用ESCALAB250Xi型X射线光电子能谱仪(XPS美国Thermo Fisher Scientific公司)测定材料表面的元素成分;利用720-ES型电感耦合等离子体发射光谱仪(ICP-OES美国Varian公司)和ICS-1100型离子色谱仪(IC美国Dionex公司)测定材料及水体中的元素含量;利用ASAP 3020型物理吸附仪(BET美国Micromeritics公司)测定材料的比表面积及孔径等参数;采用UV-2600型紫外分光光度仪(UV日本岛津公司)测定磷酸盐浓度;采用MS204S型电子天平称量材料质量(万分之一天平瑞士METTLER TOLEDO公司).
1.4 吸附实验用去离子水配制1 000 mg ·L-1的KH2PO4母液, 根据需要可将其稀释至不同质量浓度(实验中提到的磷酸盐浓度均以P进行定量).利用万分之一天平称取材料置于100 mL三角烧瓶中(吸附实验以及脱附实验均在三角烧瓶中进行), 加入50 mL一定浓度的磷酸盐溶液, 用0.1 mol ·L-1的NaOH溶液和0.1 mol ·L-1的HCl溶液调节pH, 置于恒温振荡器内以200 r ·min-1速度振荡3 h, 磁性分离后取上清液, 用钼锑抗分光光度法测定磷酸盐浓度.
1.5 脱附实验精确称取0.005 g吸附剂置于100 mL三角烧瓶中, 加入50 mL初始浓度为4 mg ·L-1的磷酸盐溶液, 调节pH为7, 25℃下置于恒温振荡器内以200 r ·min-1速度振荡3 h后磁性分离, 上清液测定磷酸盐浓度, 收集的吸附剂置于100 mL 1 mol ·L-1的NaOH溶液中脱附1 h, 然后磁性收集吸附剂60℃下真空干燥10 h后用于下一循环, 吸附-脱附循环过程进行5次.
1.6 分析方法 1.6.1 相关参数计算平衡吸附量计算公式:

|
(1) |
式中, qe为平衡吸附量, mg ·g-1;V是溶液的体积, mL;ce和c0分别代表吸附平衡时的磷酸盐浓度和初始磷酸盐浓度, mg ·L-1;m为吸附剂的投加量, g.
磷酸盐去除率和脱附率计算公式:

|
(2) |
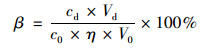
|
(3) |
式中, η和β分别为磷酸盐的去除率和脱附率, %;ce和c0分别代表吸附平衡时的磷酸盐浓度和初始磷酸盐浓度, mg ·L-1;cd为脱附后解吸液的磷酸盐浓度, mg ·L-1;V0和Vd分别为吸附实验和脱附实验中溶液的体积, mL.
1.6.2 吸附等温线模型吸附剂投加量为0.1 g ·L-1, 初始磷酸盐浓度为0.5~15 mg ·L-1, pH为7, 分别在10℃和25℃条件下以200 r ·min-1速度振荡3 h.采用Langmuir和Freundlich模型进行拟合.
Langmuir等温吸附方程:
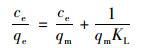
|
(4) |
Freundlich等温吸附方程:

|
(5) |
式中, qm为最大吸附量, mg ·g-1;qe为吸附平衡时的磷酸盐吸附量, mg ·g-1;ce为吸附平衡时的磷酸盐浓度, mg ·L-1;KL(L ·mg-1)和KF(mg ·g-1)分别为Langmuir吸附模型和Freundlich吸附模型的吸附常数, 代表吸附能力的强弱.
Langmuir方程的基本特征可以由无量纲分离因子RL体现, 若0 < RL < 1, 则吸附为优惠吸附[22], 如式(6)所定义:
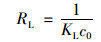
|
(6) |
式中, KL为Langmuir吸附模型的吸附常数, L ·mg-1;c0为最高初始磷酸盐浓度, mg ·L-1.
1.6.3 吸附动力学模型吸附动力学参数决定了磷酸盐回收时间, 对于污水处理系统的设计和运行至关重要.设计实验如下:吸附剂投加量为0.1 g ·L-1, 初始磷酸盐浓度为2 mg ·L-1, 调节pH为7, 温度为25℃, 置于恒温振荡器内以200 r ·min-1速度进行振荡3 h, 固定时间取样测定其磷酸盐浓度.实验数据由两种经典的动力学模型(准一级动力学模型和准二级动力学模型)进行拟合.
准一级动力学模型:

|
(7) |
准二级动力学模型:

|
(8) |
式中, qe为吸附平衡时的磷酸盐吸附量, mg ·g-1;qt为t时刻溶液的磷酸盐含量, mg ·g-1;t为反应时间, h;k1为准一级动力学模型常数, h-1;k2为准二级动力学模型常数, g ·(mg ·h)-1.
2 结果与讨论 2.1 载镧磁性水热生物炭材料表征材料的XRD图谱如图 1所示:在2θ=22°左右时HTC表现出纤维素的特征峰, 为结晶结构.负载Fe3O4后的MHTC在2θ为5°~90°范围内出现了6个明显的特征衍射峰(2θ为30.16°、35.44°、43.21°、53.44°、57.16°和62.75°), 与氧化铁立方晶系JCPDS card 19-629的数据一致[23], 分别对应了Fe3O4的(220)、(311)、(400)、(422)、(511)和(440)晶面的衍射峰.MHTC的XRD谱图中没有出现秸秆HTC的特征峰, 这是由于Fe3O4晶体相对于HTC的结晶度更高, 从而掩盖掉其衍射峰.除了Fe3O4的特征峰外, 2-La-MHTC的XRD谱图中又出现了La(OH)3的特征衍射峰, 与氢氧化镧六方晶系JCPDS 36-1481一致[24], 分别对应了La(OH)3的(100)、(110)、(101)、(200)、(201)、(211)、(112)(311)和(302)晶面的衍射峰.XRD图谱表明Fe3O4和La(OH)3成功负载于水热生物炭上.

|
图 1 X射线衍射谱图 Fig. 1 X-ray diffraction patterns |
图 2(a)、图 2(b)和图 2(c)分别对应HTC、MHTC和2-La-MHTC样品的SEM谱图, 可以看出, HTC的表面粗糙且孔径较大;负载Fe3O4和La(OH)3之后, 材料表面更加蓬松;图 2(d)为图 2(c)局部放大后的SEM谱图, 发现水热炭表面负载了致密的Fe3O4和La(OH)3活性层, 为了进一步了解材料表面的成分, 选取图 3(a)的局部区域进行能谱扫描EDS, 图 3(b)可以看出水热炭表面存在La元素和Fe元素, 并且根据半定量分析, La元素的质量分数和原子百分比分别为30.6%和4.67%, Fe元素的质量分数和原子百分比分别为8.45%和3.21%, 表明Fe3O4和La(OH)3成功负载于水热炭载体上.

|
(a)HTC;(b)MHTC;(c)和(d)2-La-MHTC 图 2 材料的SEM谱图 Fig. 2 SEM images of materials |

|
图 3 2-La-MHTC的元素能谱分析 Fig. 3 Elemental energy spectrum analysis of 2-La-MHTC |
根据国际理论与化学应用协会(IUPAC)孔径分类标准, 多孔材料按孔径大小可以划分为微孔(< 2 nm)、中孔(2~50 nm)和大孔(>50 nm).如图 4所示, 所制备材料的N2吸附脱附等温线符合“Ⅰ”和“Ⅳ”型等温线的特征, 表明HTC和2-La-MHTC表面可能存在一定的微孔和介孔结构[25~27].图 5材料的孔径分布结果进一步证明上述推测.定量分析材料的结构特征, 得到以下数据:HTC的BET比表面积为13.29 m2 ·g-1, 孔容为0.069 cm3 ·g-1, 孔径为18.49 nm;负载Fe3O4和La(OH)3后, 2-La-MHTC的BET比表面积增加为86.08 m2 ·g-1, 因此在磷酸根的吸附过程中可提供更多的吸附位点, 孔容为0.43 cm3 ·g-1, 孔径为16.21 nm.

|
图 4 材料N2吸附脱附等温线 Fig. 4 Nitrogen absorption-desorption isotherms of materials |

|
图 5 材料的孔径分布 Fig. 5 Pore size distributions in materials |
MHTC、1-La-MHTC/2、2-La-MHTC/2、3-La-MHTC/2和2-La-MHTC样品的VSM谱图如图 6所示.这一系列磁性复合材料的剩余磁性和矫顽力为0, 表明材料具有超顺磁性;MHTC、1-La-MHTC/2、2-La-MHTC/2、3-La-MHTC/2和2-La-MHTC磁性材料的饱和磁场强度分别为61.94、40.86、33.34、27.72和15.55 emu ·g-1, 有利于实现材料在污水处理中的快速回收.饱和磁场强度逐渐降低是因为添加的水热炭和La(OH)3使磁性有了一定程度地衰减.材料的优良磁性使其在水处理中具备快速回收特性, 大大提高了粉末吸附剂的应用性能.

|
图 6 载镧磁性复合材料的磁滞回线谱图 Fig. 6 Magnetization curves for La-loaded magnetic materials |
吸附剂的表面电荷性质对于磷酸盐的去除具有重要意义, 利用Zeta电位仪对2-La-MHTC的表面电性进行了测定, 结果如图 7所示. 2-La-MHTC的零电荷点为7.19, 在pH小于7.19时材料表面带正电, 通过静电作用促进了吸附反应的进行.下文将利用Zeta电位仪继续探讨吸附过程的pH效应及机制.

|
图 7 不同pH下2-La-MHTC的Zeta电位谱图 Fig. 7 Zeta potential of 2-La-MHTC at different pH values |
考察了Fe3+、Fe2+和La3+前驱体量比和水热炭添加量对吸附剂除磷性能的影响.条件为:吸附剂投加量为0.1 g ·L-1, 初始磷酸盐浓度为12 mg ·g-1, 调节pH为7, 温度为25℃, 置于恒温振荡器内以200 r ·min-1速度进行振荡3 h, 取样测定磷酸盐含量.结果如图 8所示, 载镧的磁性水热炭具有最佳的除磷能力, 其对磷酸根的吸附量大于HTC和La-Fe3O4, 同时, 随着镧含量的增加, 材料对磷酸盐吸附能力增加.以0.25 g HTC为载体, 载镧量在比例为25.57%(2-La-MHTC/2)时对磷酸根的吸附达到最大, 为65.45 mg ·g-1;继续增加La的负载量, 吸附能力反而略有下降, 可能是由于材料表面负载了过多的镧, 与文献报道相似[28].在2-La-MHTC/2的基础上提高HTC添加量得到2-La-MHTC, 磷吸附能力大大提高, 达到了100.25 mg ·g-1.可能是由于HTC表面存在丰富的羟基、羰基等基团, 可以与La形成C—O—La化学键, 一方面提高了La的负载量(2-La-MHTC的La含量较2-La-MHTC/2提高了39.7%), 另一方面也有效提高了La(OH)3的分散性(2-La-MHTC的La含量与La-Fe3O4基本相同, 但是前者的磷酸盐吸附能力较后者提高了34.2%), 使得亲磷活性位点充分暴露于磷酸盐环境中, 进而大大提高吸附能力.因此选择2-La-MHTC进行下一步研究.

|
图 8 吸附剂的磷酸盐吸附能力和镧含量对比 Fig. 8 Comparison of phosphate adsorption capacity and lanthanum content of adsorbents |
图 9是2-La-MHTC对磷酸盐的等温吸附线, 表 1为相关系数分析, Langmuir等温模型更加适合用于描述2-La-MHTC对于磷酸盐的吸附过程, 表明2-La-MHTC对于磷酸盐的吸附为单层均相吸附过程.经计算, 2-La-MHTC在10℃和25℃的理论最大磷酸盐吸附量分别为21.68 mg ·g-1和100.61 mg ·g-1, 与已有报道的载镧材料相比磷吸附能力有所提高(表 2).最大吸附量qmax随温度的升高而变大, 表明吸附过程为吸热反应.结果也表明2-La-MHTC在低温下也具有一定的除磷能力, 可以应用于秋冬季节较低温度下水体磷酸盐的去除.经计算, 无量纲分离因子RL为0.003, 表明材料对于磷酸盐的吸附为优惠吸附.

|
图 9 2-La-MHTC对于磷酸盐的吸附等温线 Fig. 9 Phosphate absorption isotherms of 2-La-MHTC |
|
|
表 1 2-La-MHTC吸附磷酸盐的热力学参数 Table 1 Isotherm parameters of phosphate adsorption on 2-La-MHTC |
|
|
表 2 载镧材料磷吸附能力对比 Table 2 Comparison of phosphate adsorption capacity of lanthanum-loaded materials |
2.4 反应动力学研究
磷酸盐吸附动力学参数见表 3.与准一级动力学模型拟合相关系数(R2=0.66)相比, 准二级动力学拟合相关系数(R2=0.98)更高, 图 10为用准二级动力学模型拟合的反应动力学曲线, 表明磷酸盐吸附过程主要是化学吸附.从中可以看出, 79.1%的磷酸盐可以在5 min内去除, 30 min时吸附基本达到平衡, 去除率高达95.7%.
|
|
表 3 2-La-MHTC吸附磷酸盐的动力学参数 Table 3 Kinetic parameters of phosphate adsorption on 2-La-MHTC |

|
图 10 2-La-MHTC对于磷酸盐的反应动力学曲线 Fig. 10 Phosphate absorption kinetic of 2-La-MHTC |
溶液pH对于吸附过程至关重要, 一方面会改变磷酸盐的存在状态, 另一方面会决定材料的表面电荷及本身稳定性.因此, 本研究考察了不同pH体系中2-La-MHTC的稳定性及吸附性能.现设计方案如下:固液比为0.1 g ·L-1, 初始磷酸根浓度为2 mg ·L-1, 用0.1 mol ·L-1的HCl和NaOH溶液调节体系pH为2~10, 温度设置为25℃, 置于恒温振荡器内以200 r ·min-1速度振荡3 h, 磁性分离后测出溶液的磷酸盐浓度、Fe3+浓度和La3+浓度.结果如图 11所示, 2-La-MHTC在pH值为3~10范围内体现出较强的pH稳定性, 磷酸盐去除率达到98%以上.在pH值处于酸性或中性时, 磷酸盐主要存在方式为H2PO4-[35], 此时材料表面质子化带正电, 因此二者可以发生较强的静电吸附作用.值得注意的是, 当溶液pH值大于7.19时吸附剂表面带负电荷(pHpzc=7.19), 磷酸盐主要存在方式为HPO42-, 静电排斥对于磷酸盐吸附产生阻碍作用.但是, 2-La-MHTC在中性及弱碱性条件下依然表现出较好的磷酸盐去除效果, 原因应该是材料表面覆盖了丰富的氢氧化镧活性层(材料中La含量达到0.36 g ·g-1), 对于磷酸盐的亲和作用充分补偿了静电排斥力, 因而仍能保持良好的吸附性能, 同时也证明了2-La-MHTC与磷酸盐并不是单纯的静电吸引作用, 还包括化学键作用.下文将对吸附机制进行详细探讨.

|
图 11 pH对于磷酸盐吸附的影响 Fig. 11 The pH effect on phosphate absorption |
本研究同时进一步评估了pH值为3~10环境中材料自身的稳定性.从图 11中发现, 材料在pH值为3时La释放量达到39%, 当pH值大于4的条件下La释放量基本忽略不计, 因而载镧磁性复合材料的适用pH值范围应该是4~10(Fe释放量在pH值为3~10基本可以忽略). 2-La-MHTC对酸碱有一定的耐受性, 具有良好地应用潜力.
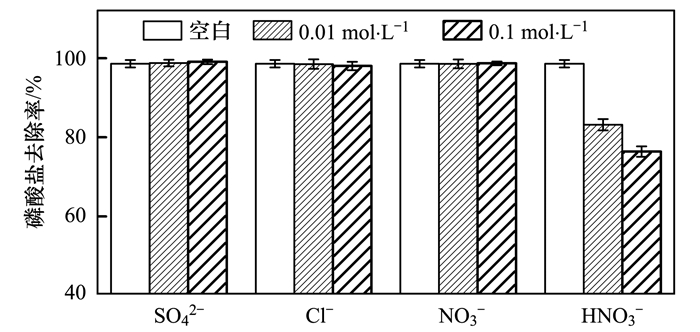
2.6 共存离子效应实际污水中均会存在一定浓度的共存离子如Cl-、NO3-、HCO3-和SO42-等, 这些离子的存在可能会对吸附剂除磷过程产生影响, 因此研究考察了吸附过程中的共存离子效应.设计方案如下:吸附剂投加量为0.1 g ·L-1, 初始磷酸盐浓度为2 mg ·L-1, 添加一定量的SO42-、Cl-、HCO3-和NO3-.共存离子分别设置空白(0 mol ·L-1)、低浓度(0.01 mol ·L-1)和高浓度(0.1 mol ·L-1)这3组实验, 置于恒温振荡器内以200 r ·min-1速度振荡3 h, 磁性分离后测定磷酸盐浓度.如图 12所示, Cl-、NO3-和SO42-对于磷酸盐吸附的影响基本可以忽略(磷酸盐去除率超过97.5%), 只有HCO3-对于吸附过程有一定的抑制作用(在HCO3-浓度为0.1 mol ·L-1时磷酸盐去除率为76.35%), 体现出载镧材料对于磷酸盐的高度选择性, 同时也表明离子强度对于吸附过程影响不大(共存离子浓度达到磷酸盐浓度的1 550倍).共存离子与2-La-MHTC之间的范德华力和化学键力的强弱是其是否产生影响的主要因素, PO43-的离子半径(nm)、相对原子质量和电荷量均大于Cl-、NO3-、SO42-和HCO3-, 因此共存离子在物理吸附方面不会对PO43-产生影响, 而HCO3-会与La形成La2(CO3)3, 可能对PO43-的化学吸附作用产生影响[36].
|
图 12 共存离子效应 Fig. 12 Effects of coexisting ions |
5次吸附-脱附实验用于评估2-La-MHTC的重复利用性及磷回收性能, 图 13表明, 5次循环实验磷酸盐去除率均在94%之上, 脱附率为65%左右, 实现了材料可再生和磷酸盐回收性能.图 14考察了吸附-脱附实验中材料的稳定性, 吸附剂在回收过程中的损失可忽略不计, 且5次循环使用后饱和磁场强度为11.45 emu ·g-1(图 6), 充分体现出2-La-MHTC的优良性能.为进一步考察材料应用性, 探究了载镧磁性复合材料对于实际污水的处理效果.设计实验方案如下:实际污水取自江苏省南京市玄武区某池塘, 初步过滤不溶性杂质和水面漂浮物后, 准确量取50 mL用于实验;吸附剂投加量为0.04~1 g ·L-1, 温度设置为25℃, 置于恒温振荡器内以200 r ·min-1速度振荡3 h, 磁性分离后测定磷酸盐浓度.结果如图 15所示, 当吸附剂投加量达到0.1 g ·L-1时, 可将磷酸盐浓度从0.87 mg ·L-1降低到0.05 mg ·L-1, 吸附过程中镧释放量忽略不计(吸附后溶液的La3+浓度由ICP-OES测得), 充分体现出2-La-MHTC作为一种可回收选择性吸附剂的应用潜力.

|
图 13 吸附-脱附实验 Fig. 13 Absorption-desorption experiments |

|
图 14 吸附-脱附实验中吸附剂质量变化 Fig. 14 Quality changes of absorbent in absorption-desorption experiments |

|
图 15 实际污水处理实验 Fig. 15 Actual sewage treatment experiments |
对载镧复合材料的表面官能团使用FTIR进行表征, 图 16(a)为HTC、MHTC和2-La-MHTC材料的红外谱图, 3种材料均表现出以下几种特征峰:3 420 cm-1处的特征峰归属于吸附到材料表面水分子中O—H键的伸缩振动;2 848 cm-1和2 920 cm-1处特征峰分别对应C—H键的的不对称伸缩振动和对称伸缩振动;1 622 cm-1处特征峰属于C= O键的伸缩振动, 表明材料表面可能含有一定的羰基基团;1 049 cm-1处特征峰对应C—O键的伸缩振动.载镧复合材料共有的特征峰归属于水热生物炭表面存在的丰富的羟基、羰基等基团.除此之外, MHTC和2-La-MHTC的谱图在579 cm-1左右出现的特征峰对应Fe—O键的振动[37, 38], 2-La-MHTC的谱图中在469 cm-1处出现的特征峰对应La—O键的振动[29, 39], 表明2-La-MHTC材料表面形成Fe—O—C键和La—O—C键, 也进一步证明了Fe3O4和La(OH)3成功负载于载体上.磷酸盐吸附前后的FTIR谱图如图 16(b)所示, 2-La-MHTC-P谱图中出现了几个新的特征峰:1 053 cm-1处对应P—O键的非对称伸缩振动, 617 cm-1和540 cm-1特征峰对应O—P—O基团的弯曲振动, 表明磷酸盐以化学键的方式结合到材料表面.这与文献报道中镧可与磷通过配位体交换形成La—O—P键的吸附机制一致[28].

|
(a)HTC、MHTC和2-La-MHTC的红外谱图;(b)吸附磷酸盐前后2-La-MHTC的红外谱图 图 16 材料的红外谱图 Fig. 16 FTIR spectra of materials |
另外通过Zeta电位对除磷后的材料进行了表征, 图 17表明吸附前2-La-MHTC材料的pHPZC为7.19, 吸附后2-La-MHTC-P材料的pHPZC为6.21, 吸附后材料pHPZC的降低应该是由于静电吸附作用.结合图 11中的结果发现, 磷酸盐吸附后溶液pH值略有上升, 原因应该是配体交换后的OH-进入到溶液中使得pH值上升.以上结果说明2-La-MHTC吸附磷的机制既有静电吸引又有配位体交换.

|
图 17 吸附磷酸盐前后2-La-MHTC的Zeta电位谱图 Fig. 17 Zeta potential of 2-La-MHTC before and after phosphate absorption |
为了进一步证明以上机制推测, 研究利用X射线光电子能谱考察了材料吸附前后元素化学状态的变化情况.所制备的2-La-MHTC在吸附磷前后的XPS谱图和吸附前后O、La和Fe元素的XPS谱图如图 18所示.图 18(a)为2-La-MHTC吸附磷酸盐前后的XPS全谱图, 从中可以看出, 主峰对应的分别是La 3d、Fe 2p、O 1s和C 1s, 表明Fe3O4和La(OH)3成功负载于HTC上;吸附后出现了P 2p, 表明磷酸盐被吸附到材料上.图 18(b)、图 18(c)和图 18(d)为2-La-MHTC吸附前后O 1s、La 3d和Fe 2p的XPS谱图.图 18(b)中, 经拟合后O 1s可以分为O2-(Fe—O和La—O)、—OH和吸附的H2O, 结合能分别位于530.72、531.51和532.9 eV[35, 40], 显然, 吸附磷酸盐之后, 结合能531.51 eV处的—OH相对含量由38.44%减小为32.28%, 暗示磷酸盐取代了—OH基团与La通过络合作用形成内层配合物.图 18(c)中吸附磷酸盐之后, La 3d5/2由834.91 eV转移为835.59 eV, La 3d3/2由851.81 eV转移到852.38 eV, 表明价带上的电子转移和La—O—P内层络合物的形成, 而图 18(d)中Fe 2p在磷酸盐吸附前后的结合能没有明显变化.XPS表征结果同前面机制分析基本一致.

|
图 18 吸附前后2-La-MHTC的X射线光电子能谱图 Fig. 18 XPS spectra of 2-La-MHTC before and after phosphate absorption |
(1) 通过一步共沉淀法制备的2-La-MHTC具有高效的除磷能力, 最大吸附量可达100.25 mg ·g-1.
(2) 2-La-MHTC具有良好的实际应用前景, 基本不受pH和其它离子的影响, 而且具有一定的可再生性.
(3) 吸附机制主要为磷酸盐取代—OH基团形成内层配合物.
| [1] | Zeng L, Li X M, Liu J D. Adsorptive removal of phosphate from aqueous solutions using iron oxide tailings[J]. Water Research, 2004, 38(5): 1318-1326. DOI:10.1016/j.watres.2003.12.009 |
| [2] | Conley D J, Paerl H W, Howarth R W, et al. Controlling eutrophication:nitrogen and phosphorus[J]. Science, 2009, 323(5917): 1014-1015. DOI:10.1126/science.1167755 |
| [3] | Awual R, Jyo A. Assessing of phosphorus removal by polymeric anion exchangers[J]. Desalination, 2011, 281: 111-117. DOI:10.1016/j.desal.2011.07.047 |
| [4] | Gao Q, Wang C Z, Liu S, et al. Ultrafiltration membrane microreactor (MMR) for simultaneous removal of nitrate and phosphate from water[J]. Chemical Engineering Journal, 2019, 355: 238-246. DOI:10.1016/j.cej.2018.08.137 |
| [5] | Guisasola A, Chan C, Larriba O, et al. Long-term stability of an enhanced biological phosphorus removal system in a phosphorus recovery scenario[J]. Journal of Cleaner Production, 2019, 214: 308-318. DOI:10.1016/j.jclepro.2018.12.220 |
| [6] | Huang H M, Liu J H, Zhang P, et al. Investigation on the simultaneous removal of fluoride, ammonia nitrogen and phosphate from semiconductor wastewater using chemical precipitation[J]. Chemical Engineering Journal, 2017, 307: 696-706. DOI:10.1016/j.cej.2016.08.134 |
| [7] | Su Y, Cui H, Li Q, et al. Strong adsorption of phosphate by amorphous zirconium oxide nanoparticles[J]. Water Research, 2013, 47(14): 5018-5026. DOI:10.1016/j.watres.2013.05.044 |
| [8] | Chen L, Chen X L, Zhou C H, et al. Environmental-friendly montmorillonite-biochar composites:facile production and tunable adsorption-release of ammonium and phosphate[J]. Journal of Cleaner Production, 2017, 156: 648-659. DOI:10.1016/j.jclepro.2017.04.050 |
| [9] | 林建伟, 王虹, 詹艳慧, 等. 氢氧化镧-天然沸石复合材料对水中低浓度磷酸盐的吸附作用[J]. 环境科学, 2016, 37(1): 208-219. |
| [10] | Dhanke P, Patil A, Kore V, et al. Phosphate removal from waste effluent using improved fly ash[J]. Materials Today:Proceedings, 2018, 5(9): 17889-17894. DOI:10.1016/j.matpr.2018.06.116 |
| [11] | Fang D X, Huang L P, Fang Z Y, et al. Evaluation of porous calcium silicate hydrate derived from carbide slag for removing phosphate from wastewater[J]. Chemical Engineering Journal, 2018, 354: 1-11. DOI:10.1016/j.cej.2018.08.001 |
| [12] | 孟文娜, 谢杰, 吴德意, 等. 活性氧化铝对水中磷的去除与回收研究[J]. 环境科学, 2013, 34(1): 231-236. |
| [13] | Ajmal Z, Muhmood A, Usman M, et al. Phosphate removal from aqueous solution using iron oxides:adsorption, desorption and regeneration characteristics[J]. Journal of Colloid and Interface Science, 2018, 528: 145-155. DOI:10.1016/j.jcis.2018.05.084 |
| [14] | Khalil A M E, Eljamal O, Amen T W M, et al. Optimized nano-scale zero-valent iron supported on treated activated carbon for enhanced nitrate and phosphate removal from water[J]. Chemical Engineering Journal, 2017, 309: 349-365. DOI:10.1016/j.cej.2016.10.080 |
| [15] | Pham T H, Lee K M, Kim M S, et al. La-modified ZSM-5 zeolite beads for enhancement in removal and recovery of phosphate[J]. Microporous and Mesoporous Materials, 2019, 279: 37-44. DOI:10.1016/j.micromeso.2018.12.017 |
| [16] | Huang W Y, Yu X, Tang J P, et al. Enhanced adsorption of phosphate by flower-like mesoporous silica spheres loaded with lanthanum[J]. Microporous and Mesoporous Materials, 2015, 217: 225-232. DOI:10.1016/j.micromeso.2015.06.031 |
| [17] |
许润, 石程好, 唐倩, 等. 氢氧化镧改性介孔稻壳生物炭除磷性能[J]. 环境科学, 2019, 40(4): 1834-1841. Xu R, Shi C H, Tang Q, et al. Phosphate removal using rice husk biochars modified with lanthanum hydroxide[J]. Environmental Science, 2019, 40(4): 1834-1841. |
| [18] | Tan X F, Liu Y G, Gu Y L, et al. Biochar-based nano-composites for the decontamination of wastewater:a review[J]. Bioresource Technology, 2016, 212: 318-333. DOI:10.1016/j.biortech.2016.04.093 |
| [19] | Li H B, Dong X L, Da Silva E B, et al. Mechanisms of metal sorption by biochars:biochar characteristics and modifications[J]. Chemosphere, 2017, 178: 466-478. DOI:10.1016/j.chemosphere.2017.03.072 |
| [20] | Sevilla M, Fuertes A B. The production of carbon materials by hydrothermal carbonization of cellulose[J]. Carbon, 2009, 47(9): 2281-2289. DOI:10.1016/j.carbon.2009.04.026 |
| [21] | 胡小莲, 杨林章, 何世颖, 等. Fe3O4/BC复合材料的制备及其吸附除磷性能[J]. 环境科学研究, 2018, 31(1): 143-153. |
| [22] | Zhao Y F, Zhang B, Zhang X, et al. Preparation of highly ordered cubic NaA zeolite from halloysite mineral for adsorption of ammonium ions[J]. Journal of Hazardous Materials, 2010, 178(1-3): 658-664. DOI:10.1016/j.jhazmat.2010.01.136 |
| [23] | Liu J, Sun Z K, Deng Y H, et al. Highly water-dispersible biocompatible magnetite particles with low cytotoxicity stabilized by citrate groups[J]. Angewandte Chemie International Edition, 2009, 48(32): 5875-5879. DOI:10.1002/anie.200901566 |
| [24] | Hu C G, Liu H, Dong W T, et al. La(OH)3 and La2O3 nanobelts-synthesis and physical properties[J]. Advanced Materials, 2007, 19(3): 470-474. |
| [25] | Yoshida N, Hirota Y, Uchida Y, et al. Solvent-free synthesis and KOH activation of mesoporous carbons using resorcinol/Pluronic F127/hexamethylenetetramine mixture and their application to EDLC[J]. Microporous and Mesoporous Materials, 2018, 272: 217-221. DOI:10.1016/j.micromeso.2018.06.028 |
| [26] | Tang Q, Shi C H, Shi W M, et al. Preferable phosphate removal by nano-La(Ⅲ) hydroxides modified mesoporous rice husk biochars:role of the host pore structure and point of zero charge[J]. Science of the Total Environment, 2019, 662: 511-520. DOI:10.1016/j.scitotenv.2019.01.159 |
| [27] | Lin L, Zhai S R, Xiao Z Y, et al. Dye adsorption of mesoporous activated carbons produced from NaOH-pretreated rice husks[J]. Bioresource Technology, 2013, 136: 437-443. DOI:10.1016/j.biortech.2013.03.048 |
| [28] | Wu B L, Fang L P, Fortner J D, et al. Highly efficient and selective phosphate removal from wastewater by magnetically recoverable La(OH)3/Fe3O4 nanocomposites[J]. Water Research, 2017, 126: 179-188. DOI:10.1016/j.watres.2017.09.034 |
| [29] | Liao T W, Li T, Su X D, et al. La(OH)3-modified magnetic pineapple biochar as novel adsorbents for efficient phosphate removal[J]. Bioresource Technology, 2018, 263: 207-213. DOI:10.1016/j.biortech.2018.04.108 |
| [30] | Hao H T, Wang Y L, Shi B Y. NaLa(CO3)2 hybridized with Fe3O4 for efficient phosphate removal:synthesis and adsorption mechanistic study[J]. Water Research, 2019, 155: 1-11. DOI:10.1016/j.watres.2019.01.049 |
| [31] | Koilraj P, Sasaki K. Selective removal of phosphate using La-porous carbon composites from aqueous solutions:batch and column studies[J]. Chemical Engineering Journal, 2017, 317: 1059-1068. DOI:10.1016/j.cej.2017.02.075 |
| [32] | Chen L, Li Y Z, Sun Y B, et al. La(OH)3 loaded magnetic mesoporous nanospheres with highly efficient phosphate removal properties and superior pH stability[J]. Chemical Engineering Journal, 2019, 360: 342-348. DOI:10.1016/j.cej.2018.11.234 |
| [33] | Dong S X, Wang Y L, Zhao Y W, et al. La3+/La(OH)3 loaded magnetic cationic hydrogel composites for phosphate removal:effect of lanthanum species and mechanistic study[J]. Water Research, 2017, 126: 433-441. DOI:10.1016/j.watres.2017.09.050 |
| [34] | Liu T, Chen X, Wang X, et al. Highly effective wastewater phosphorus removal by phosphorus accumulating organism combined with magnetic sorbent MFC@La(OH)3[J]. Chemical Engineering Journal, 2018, 335: 443-449. DOI:10.1016/j.cej.2017.10.117 |
| [35] | Fang L P, Wu B L, Lo I M C. Fabrication of silica-free superparamagnetic ZrO2@Fe3O4 with enhanced phosphate recovery from sewage:performance and adsorption mechanism[J]. Chemical Engineering Journal, 2017, 319: 258-267. DOI:10.1016/j.cej.2017.03.012 |
| [36] | 戴敏, 王建国, 巢军委, 等. 镧生物质炭对磷酸根离子的吸附特性[J]. 生态与农村环境学报, 2015, 31(3): 372-379. |
| [37] | Li R H, Wang J J, Zhou B Y, et al. Recovery of phosphate from aqueous solution by magnesium oxide decorated magnetic biochar and its potential as phosphate-based fertilizer substitute[J]. Bioresource Technology, 2016, 215: 209-214. DOI:10.1016/j.biortech.2016.02.125 |
| [38] | Chen B L, Chen Z M, Lv S F. A novel magnetic biochar efficiently sorbs organic pollutants and phosphate[J]. Bioresource Technology, 2011, 102(2): 716-723. DOI:10.1016/j.biortech.2010.08.067 |
| [39] | Salavati-Niasari M, Hosseinzadeh G, Davar F. Synthesis of lanthanum hydroxide and lanthanum oxide nanoparticles by sonochemical method[J]. Journal of Alloys and Compounds, 2011, 509(10): 4098-4103. DOI:10.1016/j.jallcom.2010.07.083 |
| [40] | Mallet M, Barthélémy K, Ruby C, et al. Investigation of phosphate adsorption onto ferrihydrite by X-ray photoelectron spectroscopy[J]. Journal of Colloid and Interface Science, 2013, 407: 95-101. DOI:10.1016/j.jcis.2013.06.049 |
 2020, Vol. 41
2020, Vol. 41


