全氟化合物(PFASs)是一类碳原子连接的氢原子全部被氟原子取代的有机化合物, 主要包括全氟羧酸类(PFCAs)和全氟磺酸类(PFSAs)等.由于PFASs具有化学性质稳定、热稳定、高表面活性及疏水疏油等性能, 被广泛应用于化工、纺织、皮革、消防、日用洗涤剂、炊具制造、杀虫剂、医药、石油化工和铬雾抑制剂等[1]诸多与人们日常生活息息相关的领域并排放到环境中去. PFASs已在全球不同环境介质中(如水、土壤和大气等)被广泛检出[2~4], 成为公认的全球性有机污染物.有研究表明, PFOS和PFOA都可能对生物体的生长、发育、生殖系统等产生毒害作用, 而PFOA可能诱发生物体发生癌变[5~8].因此, 2009年5月PFOS及其相关产品全氟辛基磺酰氟(PFOSF)被《斯德哥尔摩公约》第四次缔约方大会列为新增的持久性有机污染. 2015年欧盟将PFOA列为高关注度物质, 自2020年起, 该物质不得生产或投放市场.
国内外有关于PFASs污染现状的研究主要集中于如沉积物、土壤、水、植物、动物及人体[9~15], 而有关城市道路积尘中的PFASs污染特征的研究非常匮乏.城市道路积尘含有重金属和一些有机污染物[16, 17], 会随着风、汽车等外力作用下重新进入大气, 成为二次污染源.因此, 本研究通过采集成都市道路积尘, 分析了道路积尘中PFASs的污染特征, 并对其进行健康风险评估, 以期为后期PFASs的管控提供基础数据.
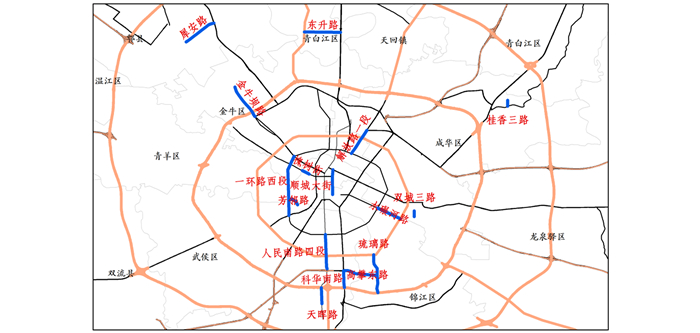
1 材料与方法 1.1 样品采集本文于2016年1月采用吸尘器收集成都市区主干道路及支路上路边的道路积尘, 样品采集期间均无降雨过程发生.采集样品过200目筛子除去石子和毛发等杂质, 过筛后样品用铝箔纸包装保存.样品采集主干道路包括顺城大街、水碾河路、科华南路、高攀东路段、人民南路四段、一环路西段、金牛坝路及解放路一段;支干道路包括槐树街、桂香三路、双城三路、天晖路、琉璃路、芳龄路、东升路及犀安路.每条路段连续采集样品, 由于主干道路车流量较大, 考虑到采样人员的安全性, 道路积尘统一从最右边车道采集.采样点位如图 1所示.
|
图 1 成都市道路积尘采样点位示意 Fig. 1 Map of road in Chengdu City and sampling sites |
甲醇(色谱纯/99.8%, 成都市科龙化工试剂厂)、氨水(25%, 成都市科龙化工试剂厂)、Milli-Q超纯水.
实验标准品:本研究中的标准样品为高纯度混合标准品PFAC-MXB(Wellington公司), 含有全氟羧酸类和全氟磺酸类化合物.其中, 羧酸类包括:全氟丁烷羧酸(PFBA)、全氟戊烷羧酸(PFPeA)、全氟己烷羧酸(PFHxA)、全氟庚烷羧酸(PFHpA)、全氟辛烷羧酸(PFOA)、全氟壬烷羧酸(PFNA)、全氟癸烷羧酸(PFDA)、全氟十一烷羧酸(PFUnDA)和全氟十二烷羧酸(PFDoDA).磺酸类包括:全氟丁烷磺酸(PFBS)、全氟己烷磺酸(PFHxS)和全氟辛烷磺酸(PFOS).另外, PFAC-MXA为高纯度混合碳同位素标记品(Wellington公司), 包括:13 C4-PFBA、13 C2-PFHxA、13 C4-PFOA、13 C5-PFNA、13 C2-PFDA、13 C2-PFUnDA、13 C2-PFDoDA、13O2-PFHxS和13 C4-PFOS.
1.3 样品前处理准确称取5.000 g的道路积尘, 转移至50 mL PP离心管中, 加入2 ng混合内标PFAC-MXA, 涡旋30 s, 充分混合后再静置2 h.然后加入5 mL MeOH, 涡旋30 s, 使其充分混匀.在摇床上于250 r ·min-1下振荡10 min, 然后超声萃取10 min, 5 000 r ·min-1离心5 min.上清液转移到新的PP管中.按上述方法重复萃取一次, 上清液合并到同一PP管中.萃取液氮吹浓缩至2mL.浓缩液用超纯水稀释至200 mL, 以1滴·s-1的速度过活化后的Cleanert PEP柱子[500 mg ·(6 mL)-1, 天津博纳艾杰尔科技有限公司]纯化.活化步骤如下:先用10 mL甲醇溶液活化, 然后用10 mL超纯水活化.活化速度均为1滴·s-1.样品过完柱后, 调节真空泵压力将PEP柱子中水份抽干, 放置平衡2 h后, 先用10 mL 20% MeOH/H2 O洗杂质, 并抽干.最后用10 mL甲醇溶液洗脱目标分析物至15 mL离心管中, 氮吹近干, 用0.6 mL甲醇和0.4 mL H2 O复溶, 复溶液过0.22 μm滤膜后转移到进样小瓶中, -20℃保存待UPLC-MS/MS分析.
1.4 仪器分析采用超高效液相色谱-串联质谱(安捷伦1290- 6470), C18色谱柱(Zorbax SB-C18, 2.1 mm×50 mm, 1.8 μm)对目标化合物进行定性及定量分析(ESI源, 负离子模式), 柱温维持在35.00℃.样品进样量为5 μL, 在水(A相)和甲醇(B相)二元流动相的作用下进行分离, 流速为0.4 mL ·min-1, 流动相梯度为:0.00~0.10 min, A相比例为90%;0.10~6.00 min, A相比例由90%降为5.00%;6.00~8.00 min, A相比例保持为5.00%, 保持运行2 min.质谱条件的设定如下:毛细管出口电压3 000 V;雾化气压力241.5 kPa(35 psi);干燥气温度250℃.
1.5 质量控制和质量保证为了监测预处理过程中的污染, 每处理10个实际样品设置2个空白实验.为观测仪器的稳定性, 每12个实际样品测定两个浓度分别为1 ng ·mL-1和5 ng ·mL-1的标准样品.结果显示, 仪器波动的标准偏差(RSD)为4.0%~9.8%, 处于可接受范围.标准曲线浓度为0、0.1、0.2、1、5和10 ng ·mL-1, 线性关系系数均大于0.99.对于没有在空白样品中检测出的PFASs, 方法检测限设定为3倍信噪比时的浓度, 而在空白样品中检测到的PFASs, 其方法检测限为空白样品中浓度的均值加上3倍的标准偏差.在处理数据时, 检测值低于MDLs值时, 用MDLs值除以2代替, 未检出时, 用零代替.另外, 由于关于道路积尘中PFASs的研究较少, 而城市土壤与道路积尘污染来源较为接近, 因此, 本文参考已有研究中报道的土壤中的PFASs的含量水平, 对道路积尘进行了0.5 ng ·g-1的回收率实验, 回收率为71.1%~93.5%(表 1), 结果比较满意.
|
|
表 1 道路积尘PFASs的方法检出限和回收率 Table 1 Method detection limits and recoveries in road dust |
数据统计分析及作图采用IBM SPSS Statistics 22 software(International Business Machines Corporation, 美国), Origin 8.5(Origin Lab, 美国)和ArcMap 10.2(ESRI, 美国).
1.6 风险评估灰尘是人体暴露于污染物的一个重要途径, 尤其是儿童, 在玩耍的过程中接触到灰尘, 而后无意识地把手放到嘴里或者在吃东西的时候粘到食物上进入体内, 进而使机体暴露于污染物中.由于现有的研究已经表明, PFASs具有肝脏毒性、遗传毒性、免疫毒性等生物毒性效应[18, 19], 因此, 很有必要通过计算当地居民通过灰尘暴露于PFASs的量, 然后对当地居民进行健康风险评估.人体暴露于灰尘的3种主要途径为呼吸摄入、皮肤接触摄入和经口摄入, 本文根据美国EPA推荐方法进行风险评估[20], 具体公式如下:

|
(1) |

|
(2) |

|
(3) |
式中, cd为各PFASs在灰尘中的含量(ng ·kg-1), 本文采用95分位数含量进行最大暴露风险评估;其它各暴露参数如表 2所示.
|
|
表 2 儿童及成人健康风险暴露评价参数 Table 2 Exposure parameters of health risk assessment for children and adults |
2 结果与讨论 2.1 成都市道路积尘中PFASs的分布特征
12种目标化合物在成都市道路积尘中均有不同程度地检出, 说明了PFASs在成都市道路灰尘中的普遍存在.其中, 检出频率最高的为PFOA和PFOS, 检出率均为94%, 然后依次为PFHxA=PFBS(88%)>PFUnDA(81%)>PFBA=PFDA=PFDoDA(69%)>PFNA (63%)>PFHpA(50%)>PFPeA(31%)>PFHxS(6%). PFOA和PFOS在室内灰尘、土壤、水体及人体中均呈现出较高的检出频率[27~31], 被认为是环境中最常见的全氟化合物.成都市道路积尘中总PFASs的含量为0.95~111 ng ·g-1, 平均含量为(25.6±37.2)ng ·g-1, 说明存在较大的空间差异性.如图 2所示, 主干道路上PFASs的总含量显著高于支干道路(独立样本T检验, P<0.05). PFASs被广泛应用于汽油、润滑油和汽车轮胎等[32, 33], 而主干道路车流量大, 交通高峰期道路拥堵, 汽车排放尾气及刹车启动过程中会向环境中释放PFASs, 因此, 主干道路积尘中PFASs含量高于支干道路.其中, 含量最高的出现在主干道路金牛坝路, 为111 ng ·g-1, 该路段沿路有较多的汽车维修商铺、汽车销售中心, 尤其是在汽车维修过程中, 如喷漆等工艺会向环境中释放PFASs[32], PFASs进入土壤或大气, 在人类活动的干扰下进入道路积尘.含量最低的路段在桂香三路(0.95 ng ·g-1), 该路段位于成都市东三环以外, 车辆较少, 污染源排放较低.且周围公园较多, 植被绿化较好, 减少了扬尘等的排放.另外, 对于支干道路来说, 市区道路积尘中的含量[(5.36±4.80)ng ·g-1]要高于周围郊区道路积尘中[(1.06±0.12)ng ·g-1]PFASs的含量.这是由于PFASs被广泛应用于洗涤剂、纺织品、纸张、油墨等与人们日常生活息息相关的消费品[34], 成都市区人口密度远高于郊区人口密度, 消费的相关产品也多于郊区, 从而导致市区支干道路上PFASs的含量高于郊区. Li等[35]对道路积尘中有机磷酸酯的研究结果同样显示, 有机磷酸酯在人口密集的市区道路积尘中呈现出较高的含量, 且含量从市区到郊区呈现出降低的趋势.说明人类活动是影响有机物在道路积尘中分布的主要因素.

|
图 2 成都市道路积尘中PFASs的含量 Fig. 2 Concentrations of PFASs in road dust collected in Chengdu City |
如图 3所示, PFASs的比例特征在成都市道路积尘中存在较大的差异, 说明不同路段PFASs的来源不同.解放路一段、金牛坝路及水碾河路段, PFBA为主要的全氟化合物, 所占比例高达95%, 说明有PFBA污染源的存在. Yao等[27]和路程等[36]发现PFBA是天津市和北京市居民区及商铺空气及灰尘中主要的PFASs.解放路一段及水碾河路段居民及商业区密集, 居民及商业区PFBA通过大气沉降进入道路积尘, 从而导致道路积尘中PFBA比例较高.金牛坝路汽车维修商铺及家具城林立, 涂料和油漆助剂等中的PFBA通过大气沉降或者雨水冲刷进入道路积尘.在其它道路中, 主要的PFASs为PFOA(24.8%)和PFOS(24.1%), 然后依次为PFBS(18.4%)>PFHxA(8.1%)≈PFBA(7.0%)>PFNA(5.4%)>PFHpA(3.8%)>PFDA(2.6%)≈PFUnDA(2.1%)≈PFDoDA(2.3%)>PFPeA(1.0%)>PFHxS (0.1%).这与成都市饮食及自来水中比例特征较为一致, 均以PFOA和短碳链的PFASs为主[37, 38], 说明成都市使用的PFASs已经向短碳链转变.现有的研究结果显示, 相较于短碳链的PFASs, 长碳链的PFASs具有更强的生物富集性及生物毒性[39, 40].美国国家环保署于2010年宣布, 到2015年逐步消除PFOA及长碳链的PFCAs[41].针对全氟化合物的管控, 我国也采取了一系列措施, 将短碳链的PFASs及C6调聚物作为PFOA(C8)替代品, 应用于油墨、半导体材料灭火剂等领域, 从而导致近年来短碳链PFASs在环境中呈现出较高的含量和比例.

|
图 3 成都市道路积尘中PFASs的比例特征 Fig. 3 Proportion profiles of PFASs in road dust of Chengdu City |
如表 3所示, 儿童经口摄入、皮肤摄入及呼吸摄入的PFASs的每日最大摄入量分别为0.166、1.55 ×10-3和1.55×10-5 ng ·(kg ·d)-1, 成人对应的分别为2.77×10-2、3.69×10-4和8.70×10-6 ng ·(kg ·d)-1.其中, 经口摄入的PFAS的量远高于其它两个途径, 说明人体暴露于道路积尘的主要途径是经口摄入.另外, 在同一暴露途径下, 儿童的暴露量均要高于成人, 经口摄入的约为成人的6倍, 皮肤摄入的约为成人的4倍, 呼吸摄入的约为成人的2倍.因此, 人们应该更加关注道路积尘中污染物对于儿童健康的影响.另外, 对于总摄入量来说, PFBA的日摄入量最高[儿童:0.12 ng ·(kg ·d)-1;成人:2.01×10-2 ng ·(kg ·d)-1], 然后为PFOA[儿童:1.46×10-2 ng ·(kg ·d)-1;成人:2.45×10-3 ng ·(kg ·d)-1]和PFNA[儿童:1.05×10-2 ng ·(kg ·d)-1;成人:1.76×10-3 ng ·(kg ·d)-1].与道路积尘的暴露特征不同, 成都市居民饮食暴露的主要化合物为PFOA[4.38 ng ·(kg ·d)-1]和PFOS[85.6 ng ·(kg ·d)-1][38].说明不同的暴露途径, 人体暴露于PFASs的风险及特征存在较大差异.已有的研究结果显示[38], 成都市居民每日通过饮食摄入PFASs的量为98.0 ng ·(kg ·d)-1, 远高于暴露于道路积尘中的含量.这与Zhang等[42]对天津、沈阳和武汉等地区的研究结果一致.天津、沈阳和武汉等地居民通过饮食摄入的PFASs的量远远高于通过灰尘摄入的量.欧盟针对PFOA和PFOS进行了风险评估, 提出了PFOS和PFOA的最大日耐受量分别为150 ng ·(kg ·d)-1和1 500 ng ·(kg ·d)-1 [43].本研究中, 成都市居民暴露于PFOS和PFOA的最大剂量均低于日最高耐受剂量, 说明道路积尘中PFASs不会对成都市居民造成即时伤害.虽然如此, 由于近年来道路积尘污染严重, 除PFASs外, 道路积尘中的重金属、多环芳烃、有机磷阻燃剂等[16, 17, 35]也会对居民带来潜在的健康风险, 因此, 人们应继续关注道路积尘中污染物对人体带来的健康风险.
|
|
表 3 经口摄入、呼吸摄入及皮肤接触摄入的PFASs的日最大摄入量/ng ·(kg ·d)-1 Table 3 High-level daily dose (ADD) for PFASs via ingestion, inhalation and dermal contact of road dust/ng ·(kg ·d)-1 |
3 结论
(1) 成都市道路积尘中PFASs的含量范围是0.95~111 ng ·g-1, 主干道路上PFASs含量显著高于支干道路, 且对于支干道路来说, 市区含量高于郊区含量.
(2) 解放路一段、金牛坝路及水碾河路段, PFBA为主要的全氟化合物, 所占比例高达95%.而其它道路中主要的PFASs为PFOA(24.8%)和PFOS(24.1%).说明成都市道路积尘中PFASs的污染特征存在较大差异.
(3) 成都市儿童和成人通过道路积尘摄入的PFASs分别为0.168 ng ·(kg ·d)-1和0.028 ng ·(kg ·d)-1, 儿童摄入量高于成人.根据欧盟推荐每日最大允许摄入量, 道路积尘中PFOS和PFOA的暴露量不会对成都市居民造成即时伤害.
| [1] | Wiliiam A. EPA and 3M announce phase out of PFOS[EB/OL]. US Environmental Protection Agency. https://archive.epa.gov/epapages/newsroom_archive/newsreleases/33aa946e6cb11f35852568e1005246b4.html,2000-05-16. |
| [2] | Song X W, Vestergren R, Shi Y L, et al. Emissions, transport, and fate of emerging per-and polyfluoroalkyl substances from one of the major fluoropolymer manufacturing facilities in China[J]. Environmental Science & Technology, 2018, 52(17): 9694-9703. |
| [3] | Chen H, Yao Y M, Zhao Z, et al. Multimedia distribution and transfer of per-and polyfluoroalkyl substances (PFASs) surrounding two fluorochemical manufacturing facilities in Fuxin, China[J]. Environmental Science & Technology, 2018, 52(15): 8263-8271. |
| [4] | Wong F, Shoeib M, Katsoyiannis A, et al. Assessing temporal trends and source regions of per-and polyfluoroalkyl substances (PFASs) in air under the Arctic Monitoring and Assessment Programme (AMAP)[J]. Atmospheric Environment, 2018, 172: 65-73. DOI:10.1016/j.atmosenv.2017.10.028 |
| [5] | Yu W G, Liu W, Jin Y H, et al. Prenatal and postnatal impact of perfluorooctane sulfonate (PFOS) on rat development:a cross-foster study on chemical burden and thyroid hormone system[J]. Environmental Science & Technology, 2009, 43(21): 8416-8422. |
| [6] | Wang F Q, Liu W, Jin Y H, et al. Transcriptional effects of prenatal and neonatal exposure to PFOS in developing rat brain[J]. Environmental Science & Technology, 2010, 44(5): 1847-1853. |
| [7] | Newsted J L, Jones P D, Coady K, et al. Avian Toxicity reference values for perfluorooctane sulfonate[J]. Environmental Science & Technology, 2005, 39(23): 9357-9362. |
| [8] | Taniyasu S, Kannan K, So M K, et al. Analysis of fluorotelomer alcohols, fluorotelomer acids, and short-and long-chain perfluorinated acids in water and biota[J]. Journal of Chromatography A, 2005, 1093(1-2): 89-97. DOI:10.1016/j.chroma.2005.07.053 |
| [9] | Zhou Z, Liang Y, Shi Y L, et al. Occurrence and transport of perfluoroalkyl acids (PFAAs), including short-chain PFAAs in Tangxun Lake, China[J]. Environmental Science & Technology, 2013, 47(16): 9249-9257. |
| [10] | Yu N Y, Shi W, Zhang B B, et al. Occurrence of perfluoroalkyl acids including perfluorooctane sulfonate isomers in Huai River Basin and Taihu Lake in Jiangsu Province, China[J]. Environmental Science & Technology, 2013, 47(2): 710-717. |
| [11] | Zushi Y, Ye F, Motegi M, et al. Spatial distribution and loading amounts of particle sorbed and dissolved perfluorinated compounds in the basin of Tokyo Bay[J]. Chemosphere, 2012, 88(11): 1353-1357. DOI:10.1016/j.chemosphere.2012.05.038 |
| [12] | Myers A L, Crozier P W, Helm P A, et al. Fate, distribution, and contrasting temporal trends of perfluoroalkyl substances (PFASs) in Lake Ontario, Canada[J]. Environment International, 2012, 44: 92-99. DOI:10.1016/j.envint.2012.02.002 |
| [13] | Liu W, Jin Y L, Quan X, et al. Perfluorosulfonates and perfluorocarboxylates in snow and rain in Dalian, China[J]. Environment International, 2009, 35(4): 737-742. DOI:10.1016/j.envint.2009.01.016 |
| [14] | Zhang Z, Peng H, Wan Y, et al. Isomer-specific trophic transfer of perfluorocarboxylic acids in the marine food web of Liaodong Bay, North China[J]. Environmental Science & Technology, 2015, 49(3): 1453-1461. |
| [15] | Zhang Y F, Beesoon S, Zhu L Y, et al. Biomonitoring of perfluoroalkyl acids in human urine and estimates of biological half-life[J]. Environmental Science & Technology, 2013, 47(18): 10619-10627. |
| [16] | Li H H, Chen L J, Yu L, et al. Pollution characteristics and risk assessment of human exposure to oral bioaccessibility of heavy metals via urban street dusts from different functional areas in Chengdu, China[J]. Science of the Total Environment, 2017, 586: 1076-1084. DOI:10.1016/j.scitotenv.2017.02.092 |
| [17] | Ma Y K, Liu A, Egodawatta P, et al. Quantitative assessment of human health risk posed by polycyclic aromatic hydrocarbons in urban road dust[J]. Science of The Total Environment, 2017, 575: 895-904. DOI:10.1016/j.scitotenv.2016.09.148 |
| [18] | Borg D, Lund B O, Lindquist N G, et al. Cumulative health risk assessment of 17 perfluoroalkylated and polyfluoroalkylated substances (PFASs) in the Swedish population[J]. Environment International, 2013, 59: 112-123. DOI:10.1016/j.envint.2013.05.009 |
| [19] | Kristensen S L, Ramlau-Hansen C H, Ernst E, et al. Long-term effects of prenatal exposure to perfluoroalkyl substances on female reproduction[J]. Human Reproduction, 2013, 28(12): 3337-3348. DOI:10.1093/humrep/det382 |
| [20] | U.S. EPA. Exposure factors handbook 2011 Edition (Final Report)[EB/OL]. https://cfpub.epa.gov/ncea/risk/recordisplay.cfm?deid=236252,2011-10-03. |
| [21] | U.S.EPA. Supplemental guidance for developing soil screening levels for superfund sites[EB/OL]. Solid Waste and Emergency Response. https://nepis.epa.gov/Exe/ZyNET.exe/91003IJK.TXT?ZyActionD=ZyDocument&Client=EPA&Index=2000+Thru+2005&Docs=&Query=&Time=&EndTime=&SearchMethod=1&TocRestrict=n&Toc=&TocEntry=&QField=&QFieldYear=&QFieldMonth=&QFieldDay=&IntQFieldOp=0&ExtQFieldOp=0&XmlQuery=&File=D%3A%5Czyfiles%5CIndex%20Data%5C00thru05%5CTxt%5C00000023%5C91003IJK.txt&User=ANONYMOUS&Password=anonymous&SortMethod=h%7C-&MaximumDocuments=1&FuzzyDegree=0&ImageQuality=r75g8/r75g8/x150y150g16/i425&Display=hpfr&DefSeekPage=x&SearchBack=ZyActionL&Back=ZyActionS&BackDesc=Results%20page&MaximumPages=1&ZyEntry=1&SeekPage=x&ZyPURL,2002-12. |
| [22] | U.S.EPA. Risk assessment guidance for superfund volume I: Human health evaluation manual (Part E, supplemental guidance for dermal risk assessment)[EB/OL]. Washington, DC: Office of Superfund Remediation and Technology Innovation. https://www.epa.gov/sites/production/files/2015-09/documents/part_e_final_revision_10-03-07.pdf,2004-07. |
| [23] | U.S.EPA. Child-specific exposure scenarios examples[EB/OL]. Washington, D.C: National Center for Environmental Assessment. https://cfpub.epa.gov/ncea/risk/recordisplay.cfm?deid=262211,2014-09. |
| [24] | Li J F, Zhang Z Z, Ma L Y, et al. Implementation of USEPA RfD and SFO for improved risk assessment of organophosphate esters (organophosphate flame retardants and plasticizers)[J]. Environment International, 2018, 114: 21-26. DOI:10.1016/j.envint.2018.02.027 |
| [25] | Li X D, Poon C S, Liu P S. Heavy metal contamination of urban soils and street dusts in Hong Kong[J]. Applied Geochemistry, 2001, 16(11-12): 1361-1368. DOI:10.1016/S0883-2927(01)00045-2 |
| [26] | U.S.EPA. Exposure Factors Handbook Chapter 5(Update): soil and dust ingestion[EB/OL]. https://cfpub.epa.gov/ncea/risk/recordisplay.cfm?deid=337521,2017-09. |
| [27] | Yao Y M, Zhao Y Y, Sun H W, et al. Per-and polyfluoroalkyl substances (PFASs) in indoor air and dust from homes and various microenvironments in China:implications for human exposure[J]. Environmental Science & Technology, 2018, 52(5): 3156-3166. |
| [28] | Hurley S, Goldberg D, Wang M M, et al. Time trends in per-and polyfluoroalkyl substances (PFASs) in California women:declining serum levels, 2011-2015[J]. Environmental Science & Technology, 2018, 52(1): 277-287. |
| [29] | Zhang S Y, Kang Q Y, Peng H, et al. Relationship between perfluorooctanoate and perfluorooctane sulfonate blood concentrations in the general population and routine drinking water exposure[J]. Environment International, 2019, 126: 54-60. DOI:10.1016/j.envint.2019.02.009 |
| [30] |
孙殿超, 龚平, 王小萍, 等. 拉萨河全氟化合物的时空分布特征研究[J]. 中国环境科学, 2018, 38(11): 4298-4306. Sun D C, Gong P, Wang X P, et al. Special distribution and seasonal variation of perfluoroalkyls substances in Lhasa River Basin, China[J]. China Environmental Science, 2018, 38(11): 4298-4306. DOI:10.3969/j.issn.1000-6923.2018.11.040 |
| [31] |
李法松, 倪卉, 黄涵宇, 等. 安徽省部分城市土壤中全氟化合物空间分布及来源解析[J]. 环境科学, 2017, 38(1): 327-332. Li F S, Ni H, Huang H Y, et al. Spatial distribution and source of perfluorinated compounds in urban soil from part of cities in Anhui Province, China[J]. Environmental Science, 2017, 38(1): 327-332. |
| [32] | Prevedouros K, Cousins I T, Buck R C, et al. Sources, fate and transport of perfluorocarboxylates[J]. Environmental Science & Technology, 2006, 40(1): 32-44. |
| [33] | Lau C, Anitole K, Hodes C, et al. Perfluoroalkyl acids:a review of monitoring and toxicological findings[J]. Toxicological Sciences, 2007, 99(2): 366-394. DOI:10.1093/toxsci/kfm128 |
| [34] | Lindstrom A B, Strynar M J, Libelo E L. Polyfluorinated compounds:past, present, and future[J]. Environmental Science & Technology, 2011, 45(19): 7954-7961. |
| [35] | Li W H, Shi Y L, Gao L H, et al. Occurrence, distribution and risk of organophosphate esters in urban road dust in Beijing, China[J]. Environmental Pollution, 2018, 241: 566-575. DOI:10.1016/j.envpol.2018.05.092 |
| [36] |
路程.全氟化合物在典型使用行业中污染特征研究[D].杨陵: 西北农林科技大学, 2014. 27-35. Lu C. The characteristic of perfluorinated compounds contamination in typical industries of China[D]. Yangling: Northwest A&F University, 2014. 27-35. |
| [37] |
方淑红, 岳月, 李成, 等. 四川省不同地区自来水中全氟化合物的污染特征及健康风险评估[J]. 环境科学学报, 2019, 39(4): 1234-1240. Fang S H, Yue Y, Li C, et al. Health risk assessment and pollution characteristics of perfluoroalkyl substances in tap water of Sichuan Province[J]. Acta Scientiae Circumstantiae, 2019, 39(4): 1234-1240. |
| [38] |
方淑红, 彭光垣, 印红玲, 等. 成都饮食中全氟化合物的污染特征及健康风险评估[J]. 环境科学学报, 2019, 39(5): 1708-1716. Fang S H, Peng G Y, Yin H L, et al. Pollution characteristics and human health risk of perfluoroalkyl substance exposure through the diet in Chengdu City[J]. Acta Scientiae Circumstantiae, 2019, 39(5): 1708-1716. |
| [39] | Fang S H, Zhang Y F, Zhao S Y, et al. Bioaccumulation of perfluoroalkyl acids including the isomers of perfluorooctane sulfonate in carp (Cyprinus carpio) in a sediment/water microcosm[J]. Environmental Toxicology and Chemistry, 2016, 35(12): 3005-3013. DOI:10.1002/etc.3483 |
| [40] | Fuentes S, Vicens P, Colomina M T, et al. Behavioral effects in adult mice exposed to perfluorooctane sulfonate (PFOS)[J]. Toxicology, 2007, 242(1-3): 123-129. DOI:10.1016/j.tox.2007.09.012 |
| [41] | U.S.EPA. 2010/15 PFOA Stewardship Program Commitments[EB/OL]. https://19january2017snapshot.epa.gov/sites/production/files/2015-10/documents/dupont.pdf,2006-01-25. |
| [42] | Zhang T, Sun H W, Wu Q, et al. Perfluorochemicals in meat, eggs and indoor dust in China:assessment of sources and pathways of human exposure to perfluorochemicals[J]. Environmental Science & Technology, 2010, 44(9): 3572-3579. |
| [43] | European Food Safety Authority (EFSA). Perfluorooctane sulfonate (PFOS), perfluorooctanoic acid (PFOA) and their salts Scientific Opinion of the Panel on Contaminants in the Food chain[J]. The EFSA Journal, 2008, 653: 1-131. |
 2019, Vol. 40
2019, Vol. 40

