2. 陕西省环境工程重点实验室, 西安 710055
2. Shaanxi Key Laboratory of Environmental Engineering, Xi'an 710055, China
工业的快速发展使石油污染情况日益严重.石油开采、运输、储存等过程中的泄漏问题, 使得全世界每年就有约8×106 t石油进入环境, 造成了很大的环境问题[1~3].其中土壤污染问题尤其突出[4, 5].石油进入土壤后会改变土壤的物理和化学性质, 降低土壤的通透性, 同时也会使土壤中的磷和氮含量减少.由于这些变化, 一方面会造成土样中微生物的栖息地的恶化, 另一方面对土壤微生物本身也有一定的负面影响[6~8].当前对于石油污染土壤, Fenton预氧化联合生物修复是一种有效地修复手段[9~14].
现有研究报道较多的Fenton氧化法大多数是通过加大双氧水(H2O2)浓度[15~17]和铁浓度[14, 18, 19]来提高羟基自由基(·OH)的产量, 从而提高石油污染土壤中TPH的氧化效果.然而由于Fenton氧化过程会对土壤中的土著细菌造成伤害, 且H2O2的浓度越高对土著细菌的伤害越严重, 这并不利于后续生物修复.以往研究中是在Fenton预氧化后外加营养[20~22]或者外加菌源[23]提高后续生物修复效率, 如Gao等[22]的生物修复实验加菌加营养后TPH降解率提高了10%左右.但这些方法会提高造价, 还可能会破坏生态和造成二次污染.为此, 本研究设想是否可以通过低浓度双氧水条件下的Fenton预氧化来实现后续生物的高效降解, 得出一种不用外加菌源也能有效地修复石油污染土壤的低成本的处理方式.这种处理方式称为温和预氧化处理, 它贯彻了低消耗低成本的理念, 增加了工程实际应用的可能性.
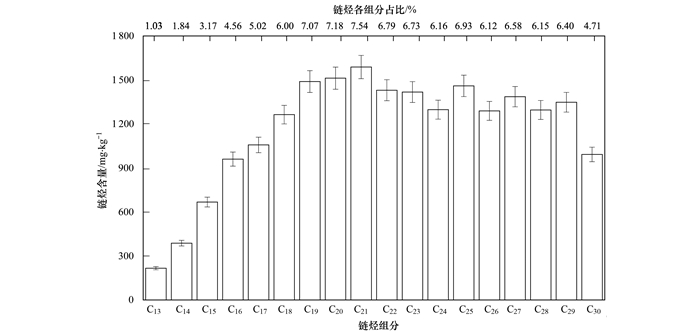
1 材料与方法 1.1 土样本实验所用的石油污染土样取自陕北某油田, 土壤石油烃(total petroleum hydrocarbon, TPH)总量为21 056 mg·kg-1, 土壤有机物(soil organic matter, SOM)占比5.2%, 总铁含量为48.30 g·kg-1, 含水率为18.91%, pH值为7.5. TPH各组分含量及比例见图 1.实验前, 土样需经过碎散, 去除杂质, 用0.45 mm的筛网筛过后, 混匀, 在冰箱(4℃)中密闭保存.
|
图 1 污染土壤中各链烃的含量(18种链烃) Fig. 1 Concentration of alkanes in the contaminated soil sample (a total of 18 alkanes) |
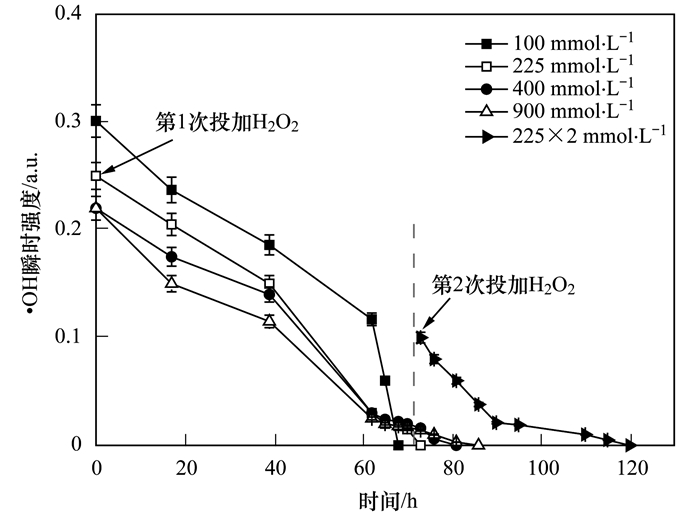
称取5 g筛选的石油污染土样置于250 mL锥形瓶中, 再分别加入柠檬酸-Fe2+、H2O2及蒸馏水, 使得最终液体体积为60 mL, pH为7.2左右.反应体系中柠檬酸-Fe2+的浓度5.8 mmol·L-1, H2O2分别以5种不同的方式加入到体系:①投加5.4 mL 30%的H2O2(900 mmol·L-1); ②投加2.7 mL 30%的H2O2(450 mmol·L-1); ③投加1.35 mL 30%的H2O2(225 mmol·L-1); ④投加2.7 mL 30%的H2O2(450 mmol·L-1), 平分成2次投加, 待前一次投加的H2O2分解完后再进行下一次投加; ⑤投加0.6 mL 30%的H2O2(100 mmol·L-1).反应在开口瓶中进行, 直至检测不到残余H2O2为止.同时做不投加H2O2及其柠檬酸-Fe2+的对照实验.实验中取少量上清液置于试管中, 加入10%硫酸钛溶液通过观察其颜色(碘量法)判断H2O2是否分解完成, 若溶液呈黄色表示仍有H2O2残余, 呈无色说明分解完成.另外在实验过程中测定反应前后上清液中的DOC和NH4+-N的浓度、TPH浓度、土著菌数量和活性.同时做一组平行实验, 向250 mL锥形瓶中仅加入柠檬酸-Fe2+、H2O2溶液和蒸馏水, 反应体系为60 mL, 用于测定氧化过程中的·OH强度.每组实验做3个平行样.
1.2.2 后续生物修复实验每一种Fenton预氧化实验设置3组平行样进行后续为期80 d的生物实验.第一组反应瓶中接种1号菌(土著菌, 筛选自延安的石油污染土壤), 第二组反应瓶中接种2号菌(外源菌, 筛选自西安的石油污染土壤), 第三组反应瓶中不接种菌.通过比较三组反应瓶的反应效果来评价Fenton氧化后残留的土著菌对营养消耗和生物降解的影响.在后期生物修复过程中, 如果不加菌组可以达到和加菌组相近的修复效果, 就达到了前期Fenton预氧化促进后续生物降解TPH的目的.生物修复过程在有氧条件下进行(氧浓度不低于10%).所有反应在20℃、黑暗条件下转速为120 r·min-1的摇床上进行.在本实验过程中测定20、40、60和80 d的TPH、DOC和NH4+-N浓度.另外, 对于不进行Fenton预处理的纯生物实验(加入0.2 mol·L-1 NaN3以考虑挥发的影响), 同样设置3组平行样进行加菌和不加菌的生物修复实验.每组实验做3个平行样, 每个样品测量1次.
1.3 分析方法 1.3.1 土壤中石油烃(TPH)含量的测定土壤中TPH的测定遵循US EPA 3550B[24]测定法, 往待测的石油污染的土样悬浊液中加入20 mL二氯甲烷, 置于摇床振荡过夜(125 r·min-1), 超声15 min, 机械振荡30 min(250 r·min-1), 然后用带聚四氟乙烯活塞的分液漏斗分离, 连续萃取3次, 后续2次每次加入10 mL二氯甲烷, 每次的萃取液收集前过干燥无水硫酸钠(预先在105℃烘箱中烘2 h)的层析柱中干燥脱水, 柱下出口处用50 mL锥形瓶接, 萃取液最终定容至50 mL.之后使用安捷伦6890N气相色谱仪(美国)分析测定样品(单检)[25].
1.3.2 羟基自由基产量的测定取待测液20 μL, 150 mmol·L-1的DMPO 10 μL加于2 mL的离心管中混合均匀, 10 000 r·min-1离心30 s后, 用毛细管吸取长度约1 cm的混合液, 利用电子顺磁共振(EPR)波谱仪测定[26], 而DMPO可以捕捉到很微弱的·OH.每个实验做3个平行样. ·OH单位为a.u.[27, 28].
1.3.3 营养、微生物数量和呼吸活性的测定反应瓶中的上清液经过0.45 μm的滤膜过滤, NH4+-N采用分光光度计法进行测定; 溶解性TOC采用TOC分析仪测定(日本岛津)[29], 使用TOC分析仪测量TC和IC; 溶解性有机碳(DOC)为TC与IC的差值[19]; 微生物数量采用平板计数法和流式细胞仪进行测定[12, 30, 31].
呼吸活性通过CO2产量进行评价, CO2产量采用安捷伦6890N气相色谱仪(双检)进行检测.
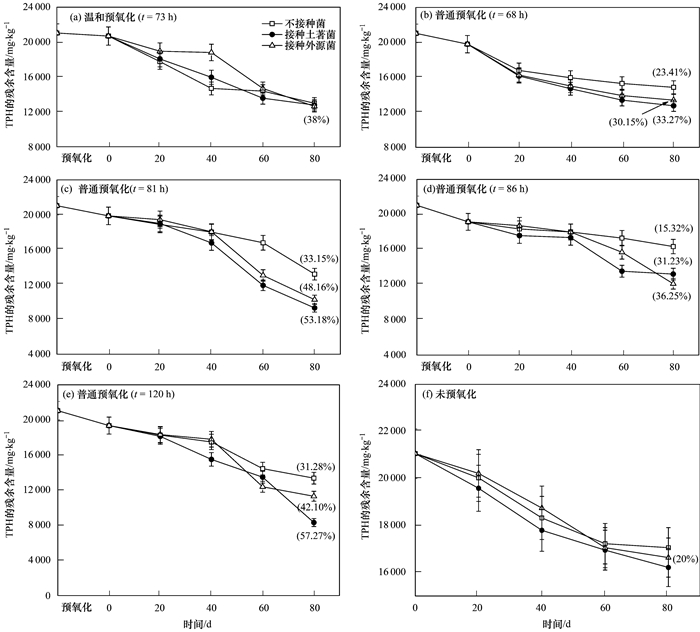
2 结果与讨论 2.1 温和预氧化提高后续生物修复石油污染土壤效果分析 2.1.1 修复TPH效果分析本实验中各组Fenton预氧化·OH特性见表 1.经温和预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)处理, 无论是不接种菌还是接种土著菌(1号)或外源菌(2号), 后期80 d生物修复阶段TPH去除率相似, 为38%左右, 不加菌就能够达到加菌的修复效果.对于普通预氧化处理的, 当·OH存在时间为68 h(H2O2浓度:100 mmol·L-1)、81 h(H2O2浓度:450 mmol·L-1)、86 h(H2O2浓度:900 mmol·L-1)和120 h(H2O2浓度:450 mmol·L-1, 分2次投加)时(图 2), 在后续生物阶段, 不接菌组TPH去除率分别为23.41%、33.15%、15.32%和31.28%, 均低于相应条件下接菌组的TPH去除率(33.27%、53.18%、36.25%和57.27%), 同时也低于经温和预氧化处理的TPH去除率(38%).温和预氧化中·OH存在时间短且H2O2用量少, 但其联合生物修复TPH的效果比普通预氧化联合生物修复TPH效果都要好.对于未经预氧化的纯生物实验组, 不接菌组TPH去除率为19.53%, 低于接种菌的23.49%(图 3), 且这两者都低于温和预氧化联合生物修复的TPH去除率(38%).这说明温和预氧化提高后续生物修复石油TPH效果.
|
|
表 1 Fenton预氧化后·OH特性对TPH氧化、营养产生和残余土著细菌数量的影响1) Table 1 Effects of ·OH on TPH removal, nutrients, and the population of residual indigenous bacteria after Fenton pre-oxidation |
|
图 2 ·OH瞬时强度曲线 Fig. 2 Change curves of instantaneous intensity of ·OH over time |
|
图中括号内百分比为80 d生物修复的生物降解率 图 3 温和预氧化生物修复80 d后残余TPH含量 Fig. 3 Residual TPH during 80 days of incubation after different Fenton pre-oxidation |
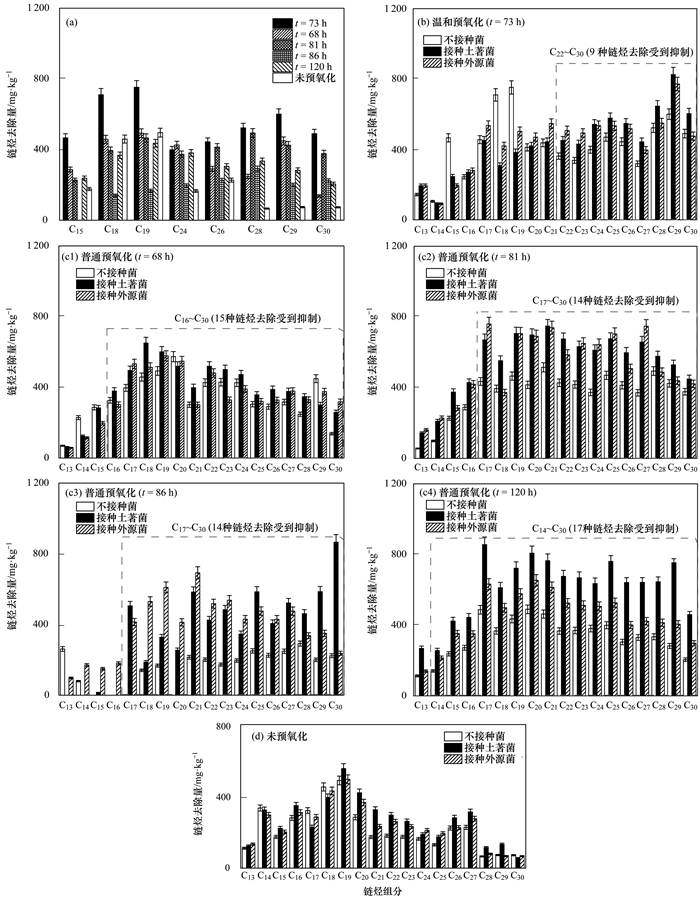
由图 4(a)可知, 在不加菌的条件下, 在后续生物修复阶段, 温和预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)联合生物修复有8种链烃的去除效果比普通预氧化联合生物修复的要好, 其中C15、C18、C19、C29和C30的去除量分别为466.08、710.26、752.62、600.67和490.15 mg·kg-1, 是普通预氧化联合生物修复的1.1~5.0倍, 可见温和预氧化能提高后续生物修复石油链烃的效果.由图 4(b)和4(c)可知, 在经过预氧化处理后, 后续生物修复过程中部分链烃的去除受到抑制.温和预氧化处理后, 后续生物修复中有9种链烃组分(C22~C30)的去除受到了抑制, 其去除量为3 944.98 mg·kg-1, 加菌处理后的链烃C22~C30去除量提高了1.3倍(5 068.35 mg·kg-1).对于普通预氧化处理, 当·OH持续时间分别为68、81、86和120 h时, 在不接种菌的条件下分别有15(C16~C30)、14(C17~C30)、14(C17~C30)和17(C14~C30)种链烃组分受到抑制.其均少于不进行Fenton预氧化处理的.而Mohanty等[32]研究长链烃的去除比短链烃更难, 且随着·OH持续时间的增加, 土著菌活性受到抑制的时间越长, 尤其是降解长链烃的土著菌[13, 33].而未经Fenton预氧化处理的纯生物实验组, 受抑制的链烃组分数也比·OH持续时间短时的要多, 这是由于原本石油污染土壤中土著菌的活性就不高.通常, 在进行Fenton预氧化后, 土著菌的活性大大降低, 需要在后续生物处理过程中进行生物强化或生物刺激才能达到期望的生物处理效果[23, 34, 35].
|
图 4 温和预氧化生物修复80 d内链烃的去除(P < 0.05) Fig. 4 Removal of alkanes during 80 days of incubation after different Fenton pre-oxidation (P < 0.05) |
因此, 本研究中温和预氧化联合生物修复使更多组分链烃的去除不受抑制, 不接种菌就能达到接种菌的去除效果, 为一种有效可行且低消耗的修复方式.
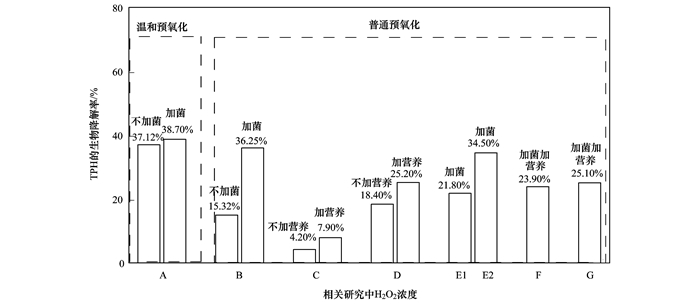
2.2 温和预氧化提高后续生物修复石油污染土壤机制分析由已有研究对比可知(图 5), 本研究中, 在不加菌的条件下温和预氧化联合80 d生物修复在生物阶段的TPH降解率为37.12%, 加菌后为38.70%, TPH去除效果相差不大, 且H2O2用量仅225 mmol·L-1.但普通预氧化中, H2O2用量高达900 mmol·L-1, 但是相应地后续生物阶段TPH去除率仅为15.32%, 是经温和预氧化处理条件下的2/5, 加菌以后的去除率(36.25%)还比温和预氧化处理不加菌(37.12%)的还要低.而在Sutton[19]预氧化联合生物修复实验中, H2O2用量为1 470 mmol·L-1(5%), 是本研究温和预氧化用量的6.5倍, 但在加营养后的后续生物阶段TPH去除率却很低, 仅为7.90%;将H2O2(1 470 mmol·L-1)分3次投加后生物修复效果有所提高, TPH去除率升为25.20%, 仍低于本研究不加菌时经温和预氧化处理的去除效果(37.12%). Xu[13]的研究中发现, 在加菌的条件下, 将900 mmol·L-1 H2O2分别分2次投加和分4次投加在后续生物阶段的TPH去除率分别为21.80%和34.50%.在Bajagain[36]预氧化联合生物修复实验中, 当投加H2O2为1 470 mmol·L-1(5%)时, 在加菌加营养的条件下, 后续生物阶段TPH去除率仅为23.90%, 这可能是由于大量的H2O2对土著菌的伤害很大.根据Xu[37]的研究结果, 发现当在预氧化阶段只加H2O2(900 mmol·L-1), 而未加柠檬酸-Fe2+时, 在加菌加营养的条件下, 后续生物阶段TPH去除率为25.10%.这些Fenton预氧化联合生物修复实验研究在生物部分的TPH去除率均低于本研究温和预氧化组的TPH去除率.
|
A:225 mmol·L-1(本研究); B:900 mmol·L-1(本研究); C:1 470 mmol·L-1(5%) 1次性投加, 引自文献[19]; D:1 470 mmol·L-1(5%)分3次投加, 引自文献[19]; E1:900 mmol·L-1分2次投加, E2:900 mmol·L-1分4次投加, 引自文献[13]; F:1 470 mmol·L-1(5%), 引自文献[36]; G:900 mmol·L-1, 预氧化时未加柠檬酸-Fe2+, 引自文献[37] 图 5 关于生物降解效果本研究与已有研究的对比 Fig. 5 Comparison of different studies on the subsequent bioremediation phase |
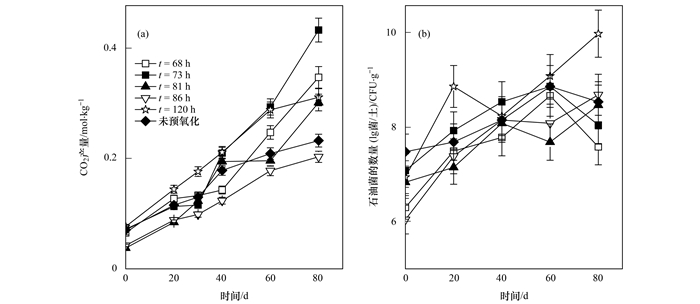
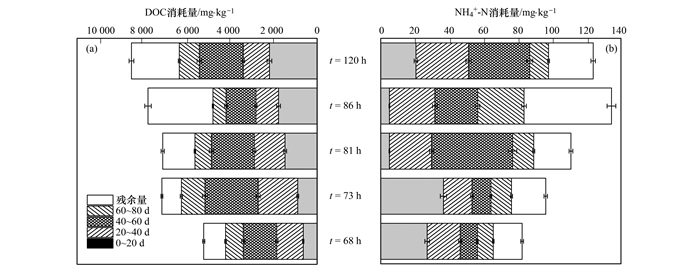
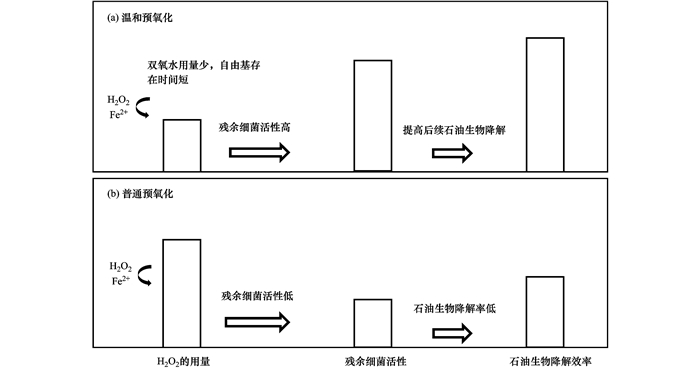
由图 6(a)和图 6(b)可知, 经温和预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)处理后, 土著菌活性在后续生物修复40 d时超过经普通预氧化处理的, 并且在80 d时达到最高, 为0.43 mol·kg-1, 是普通预氧化处理的1.4~2.2倍.对于石油菌数量, 温和预氧化组在40 d时较高, 为108.53CFU·g-1, 是普通氧化组的1.1倍左右; 在60~80 d时温和预氧化组的土著菌数量有所降低, 在80 d时仅为108.04 CFU·g-1, 是普通预氧化组(·OH存在时间:120 h; H2O2浓度:450 mmol·L-1)的4/5(109.97 CFU·g-1).这说明在本研究中去除TPH的关键因素并不是石油菌数量, 而是土著菌活性.可知当·OH存在时间短时, 对土著菌的伤害较低, 生物修复前期土著菌能够恢复到一定数量, 在后期能够快速恢复活性.温和预氧化处理后, 生物修复前20 d的NH4+-H消耗最高, 为36.57 mg·kg-1, 是相应条件下普通预氧化处理后的1.8~7.2倍[图 7(b)], 这是温和预氧化后微生物恢复活性的关键.而在不加菌处理生物修复后40 d, 未经Fenton预氧化处理的土著菌CO2产量很低, 为0.18~0.23 mol·kg-1, 仅为温和预氧化处理的0.8~0.5倍(0.21~0.43 mol·kg-1).这说明原本石油污染土壤中的微生物活性确实不高.温和预氧化·OH存在时间短H2O2用量少, 而且可以适当刺激土著微生物并提高土著微生物的活性, 进而减少对链烃组分的抑制, 有利于TPH的去除, 使得在后期生物修复阶段不加菌处理就能够达到加菌处理的效果, 这就是温和预氧化提高后续生物修复石油的机制(原理见图 8).
|
图 6 温和预氧化生物修复阶段的生物呼吸活性和土壤中石油菌的数量变化 Fig. 6 production and the population of hydrocarbon degraders during biodegradation |
|
图 7 温和预氧化生物修复阶段的营养消耗 Fig. 7 Available nutrients consumed during biodegradation |
|
图 8 温和预氧化提高后续生物修复污染土壤效果的机制 Fig. 8 Mechanism improving the effect of subsequent bioremediation of contaminated soil by mild |
(1) 采用Fenton预氧化联合生物修复石油污染土壤时, 经温和Fenton预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)处理后, 无论是不接种菌还是接种土著菌(1号)或外源菌(2号), 后期生物阶段的TPH的去除相近, 为38%左右, 高于普通预氧化(·OH存在时间:68 h; H2O2浓度:100 mmol·L-1、·OH存在时间:81 h; H2O2浓度:450 mmol·L-1、·OH存在时间:86 h; H2O2浓度:900 mmol·L-1和·OH存在时间:120 h; H2O2浓度:450 mmol·L-1; 分两次投加)处理后的TPH去除率(23.41%、33.15%、15.32%和31.28%), 也高于未经Fenton预氧化的纯生物实验组的TPH去除率(19.53%).温和预氧化中·OH存在时间短H2O2用量少, 在后期生物修复阶段不加菌就能够达到加菌的修复效果, 是一种低成本可行的修复石油污染土壤的方式.
(2) 采用温和Fenton预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)联合生物修复石油污染土壤时, 有9种链烃组分(C22~C30)的去除受到了抑制, 去除量为3 944.98 mg·kg-1, 加菌处理后的链烃C22~C30去除量提高了1.3倍(5 068.35 mg·kg-1).对于普通Fenton预氧化处理, 当·OH存在时间为68、81、86和120 h时, 在不接种菌的条件下分别有15、14、14和17种链烃的去除受到抑制.对于未进行预氧化处理的, 在不接种菌的条件下有13种链烃组分(C17~C29)的去除受到了抑制.这说明温和预氧化能够减少后续生物修复中受抑制的链烃组分, 进而提高TPH的去除效果.
(3) 进一步分析微生物活性发现温和Fenton预氧化(·OH存在时间:73 h; H2O2浓度:225 mmol·L-1)处理后, 土著菌活性在生物修复40~80 d达到最高而石油菌数量却不是最高的, CO2产量最高为0.43 mol·kg-1, 是普通预氧化处理的1.4~2.2倍, 是未经Fenton预氧化处理的1.9倍.而营养消耗表明, 温和预氧化后, 土著微生物能够快速恢复活性的关键是生物修复前20 d的NH4+-H消耗高(36.57 mg·kg-1).这说明温和预氧化后可以适当刺激土著菌的生长并提高其活性, 有利于TPH的去除.因此温和预氧化后在生物修复阶段对TPH的处理效果不加菌与加菌处理相似.
| [1] |
杜卫东, 万云洋, 钟宁宁, 等. 土壤和沉积物石油污染现状[J]. 武汉大学学报(理学版), 2011, 57(4): 311-322. Du W D, Wan Y Y, Zhong N N, et al. Current status of petroleum-contaminated soils and sediments[J]. Journal of Wuhan University:Natural Science Edition, 2011, 57(4): 311-322. |
| [2] |
陆秀君, 郭书海, 孙清, 等. 石油污染土壤的修复技术研究现状及展望[J]. 沈阳农业大学学报, 2003, 34(1): 63-37. Lu X J, Guo S H, Sun Q, et al. Current situation of remediating techniques of petroletum contaminated soil and its prospects[J]. Journal of Shenyang Agricultural University, 2003, 34(1): 63-37. |
| [3] |
李永霞, 郑西来, 马艳飞. 石油污染物在土壤中的环境行为研究进展[J]. 安全与环境工程, 2011, 18(4): 43-47. Li Y X, Zheng X L, Ma Y F. Advance in environmental behavior of petroleum pollutants in soil[J]. Safety and Environmental Engineering, 2011, 18(4): 43-47. DOI:10.3969/j.issn.1671-1556.2011.04.011 |
| [4] | Liu B Q, Liu J P, Ju M T, et al. Purification and characterization of biosurfactant produced by Bacillus licheniformis Y-1 and its application in remediation of petroleum contaminated soil[J]. Marine Pollution Bulletin, 2016, 107(1): 46-51. DOI:10.1016/j.marpolbul.2016.04.025 |
| [5] | Tsai T T, Kao C M, Yeh T Y, et al. Remediation of fuel oil-contaminated soils by a three-stage treatment system[J]. Environmental Engineering Science, 2009, 26(3): 651-659. DOI:10.1089/ees.2008.0008 |
| [6] |
杨萌青, 李立明, 李川, 等. 石油污染土壤微生物群落结构与分布特性研究[J]. 环境科学, 2013, 34(2): 789-794. Yang M Q, Li M L, Li C, et al. Microbial community structure and distribution characteristics in oil contaminated Soil[J]. Environmental Science, 2013, 34(2): 789-794. |
| [7] | Liu R Y, Zhang Y, Ding R, et al. Comparison of archaeal and bacterial community structures in heavily oil-contaminated and pristine soils[J]. Journal of Bioscience and Bioengineering, 2009, 108(5): 400-407. DOI:10.1016/j.jbiosc.2009.05.010 |
| [8] |
蔡萍萍, 宁卓, 何泽, 等. 采油井场土壤微生物群落结构分布[J]. 环境科学, 2018, 39(7): 3329-3338. Cai P P, Ning Z, He Z, et al. Microbial community distributions in soils of an oil exploitation site[J]. Environmental Science, 2018, 39(7): 3329-3338. |
| [9] | Pardo F, Rosas J M, Santos A, et al. Remediation of a biodiesel blend-contaminated soil by using a modified Fenton process[J]. Environmental Science and Pollution Research, 2014, 21(21): 12198-12207. DOI:10.1007/s11356-014-2997-2 |
| [10] | Xu J L, Xin L, Huang T L, et al. Enhanced bioremediation of oil contaminated soil by graded modified Fenton oxidation[J]. Journal of Environmental Sciences, 2011, 23(11): 1873-1879. DOI:10.1016/S1001-0742(10)60654-7 |
| [11] | Goi A, Kulik N, Trapido M. Combined chemical and biological treatment of oil contaminated soil[J]. Chemosphere, 2006, 63(10): 1754-1763. DOI:10.1016/j.chemosphere.2005.09.023 |
| [12] | Gong X B. Remediation of weathered petroleum oil-contaminated soil using a combination of biostimulation and modified Fenton oxidation[J]. International Biodeterioration & Biodegradation, 2012, 70: 89-95. |
| [13] | Xu J L, Deng X, Cui Y W, et al. Impact of chemical oxidation on indigenous bacteria and mobilization of nutrients and subsequent bioremediation of crude oil-contaminated soil[J]. Journal of Hazardous Materials, 2016, 320: 160-168. DOI:10.1016/j.jhazmat.2016.08.028 |
| [14] | Sutton N B, Langenhoff A A M, Lasso D H, et al. Recovery of microbial diversity and activity during bioremediation following chemical oxidation of diesel contaminated soils[J]. Applied Microbiology and Biotechnology, 2014, 98(6): 2751-2764. DOI:10.1007/s00253-013-5256-4 |
| [15] | Martínez-Pascual E, Grotenhuis T, Solanas AM, et al. Coupling chemical oxidation and biostimulation:Effects on the natural attenuation capacity and resilience of the native microbial community in alkylbenzene-polluted soil[J]. Journal of Hazardous Materials, 2015, 300: 135-143. DOI:10.1016/j.jhazmat.2015.06.061 |
| [16] | Xu J L, Cui Y W, Huang F, et al. Effect of the ratio of crude oil to soil organic matter on H2O2 decomposition and oxidation of crude oil in contaminated soils[J]. Journal of Advanced Oxidation Technologies, 2016, 19(1): 113-118. |
| [17] | Xu J L, Pancras T, Grotenhuis T. Chemical oxidation of cable insulating oil contaminated soil[J]. Chemosphere, 2011, 84(2): 272-277. DOI:10.1016/j.chemosphere.2011.03.044 |
| [18] | Sutton N B, Grotenhuis J T C, Langenhoff A A M, et al. Efforts to improve coupled in situ chemical oxidation with bioremediation:a review of optimization strategies[J]. Journal of Soils and Sediments, 2011, 11(1): 129-140. DOI:10.1007/s11368-010-0272-9 |
| [19] | Sutton N B, Grotenhuis T, Rijnaarts H H M. Impact of organic carbon and nutrients mobilized during chemical oxidation on subsequent bioremediation of a diesel-contaminated soil[J]. Chemosphere, 2014, 97(1): 64-70. |
| [20] | Suja F, Rahim F, Taha M R, et al. Effects of local microbial bioaugmentation and biostimulation on the bioremediation of total petroleum hydrocarbons (TPH) in crude oil contaminated soil based on laboratory and field observations[J]. International Biodeterioration & Biodegradation, 2014, 90: 115-122. |
| [21] | Shahi A, Aydin S, Ince B, et al. Evaluation of microbial population and functional genes during the bioremediation of petroleum-contaminated soil as an effective monitoring approach[J]. Ecotoxicology and Environmental Safety, 2016, 125: 153-160. DOI:10.1016/j.ecoenv.2015.11.029 |
| [22] | Gao Y C, Guo S H, Wang J N, et al. Effects of different remediation treatments on crude oil contaminated saline soil[J]. Chemosphere, 2014, 117: 486-493. DOI:10.1016/j.chemosphere.2014.08.070 |
| [23] | Xu Y H, Lu M. Bioremediation of crude oil-contaminated soil:Comparison of different biostimulation and bioaugmentation treatments[J]. Journal of Hazardous Materials, 2010, 183(1-3): 395-401. DOI:10.1016/j.jhazmat.2010.07.038 |
| [24] | Lin T C, Pan P T, Cheng S S. Ex situ bioremediation of oil-contaminated soil[J]. Journal of Hazardous Materials, 2010, 176(1-3): 27-34. DOI:10.1016/j.jhazmat.2009.10.080 |
| [25] | Sirguey C, De Souza E Silva P T, Schwartz C, et al. Impact of chemical oxidation on soil quality[J]. Chemosphere, 2008, 72(2): 282-289. DOI:10.1016/j.chemosphere.2008.01.027 |
| [26] | Margesin R, Hammerle M, Tscherko D. Microbial activity and community composition during bioremediation of diesel-oil-contaminated soil:effects of hydrocarbon concentration, fertilizers, and incubation time[J]. Microbial Ecology, 2007, 53(2): 259-269. DOI:10.1007/s00248-006-9136-7 |
| [27] | Chen L W, Ma J, Li X C, et al. Strong enhancement on Fenton oxidation by addition of hydroxylamine to accelerate the ferric and ferrous iron cycles[J]. Environmental Science & Technology, 2011, 45(9): 3925-3930. |
| [28] | Chen L W, Li X C, Zhang J, et al. Production of hydroxyl radical via the activation of hydrogen peroxide by hydroxylamine[J]. Environmental Science & Technology, 2015, 49(17): 10373-10379. |
| [29] | Kim I, Lee M. Pilot scale feasibility study for in-situ chemical oxidation using H2O2 solution conjugated with biodegradation to remediate a diesel contaminated site[J]. Journal of Hazardous Materials, 2012, 241-242: 173-181. DOI:10.1016/j.jhazmat.2012.09.022 |
| [30] | Jho E H, Ryu H, Shin D, et al. Prediction of landfarming period using degradation kinetics of petroleum hydrocarbons:test with artificially contaminated and field-aged soils and commercially available bacterial cultures[J]. Journal of Soils and Sediments, 2014, 14(1): 138-145. DOI:10.1007/s11368-013-0786-z |
| [31] | Lu M, Zhang Z Z, Qiao W, et al. Remediation of petroleum-contaminated soil after composting by sequential treatment with Fenton-like oxidation and biodegradation[J]. Bioresource Technology, 2010, 101(7): 2106-2113. DOI:10.1016/j.biortech.2009.11.002 |
| [32] | Mohanty G, Mukherji S. Biodegradation rate of diesel range n-alkanes by bacterial cultures Exiguobacterium aurantiacum and Burkholderia cepacia[J]. International Biodeterioration & Biodegradation, 2008, 61(3): 240-250. |
| [33] | Seklemova E, Pavlova A, Kovacheva K. Biostimulation-based bioremediation of diesel fuel:field demonstration[J]. Biodegradation, 2001, 12(5): 311-316. DOI:10.1023/A:1014356223118 |
| [34] | Silva-Castro G A, Rodelas B, Perucha C, et al. Bioremediation of diesel-polluted soil using biostimulation as post-treatment after oxidation with Fenton-like reagents:Assays in a pilot plant[J]. Science of the Total Environment, 2013, 445-446: 347-355. DOI:10.1016/j.scitotenv.2012.12.081 |
| [35] | Silva-Castro G A, Santacruz-Calvo L, Uad I, et al. Treatment of diesel-polluted clay soil employing combined biostimulation in microcosms[J]. International Journal of Environmental Science and Technology, 2012, 9(3): 535-542. DOI:10.1007/s13762-012-0060-8 |
| [36] | Bajagain R, Park Y, Jeong S W. Feasibility of oxidation-biodegradation serial foam spraying for total petroleum hydrocarbon removal without soil disturbance[J]. Science of the Total Environment, 2018, 626: 1236-1242. DOI:10.1016/j.scitotenv.2018.01.212 |
| [37] | Xu J L, Kong F X, Song S H, et al. Effect of Fenton pre-oxidation on mobilization of nutrients and efficient subsequent bioremediation of crude oil-contaminated soil[J]. Chemosphere, 2017, 180: 1-10. DOI:10.1016/j.chemosphere.2017.03.087 |
 2019, Vol. 40
2019, Vol. 40

