2. 生态环境部华南环境科学研究所, 广州 510530;
3. 深圳市市政设计研究院有限公司, 深圳 518029;
4. 南京大学环境学院, 污染控制与资源化研究国家重点实验室, 南京 210093
2. South China Institute of Environmental Science, Ministry of Ecology and Environment, Guangzhou 510530, China;
3. Shenzhen Municipal Design & Research Institute Co., Ltd., Shenzhen 518029, China;
4. State Key Laboratory of Pollution Control and Resource Reuse, School of the Environment, Nanjing University, Nanjing 210093, China
丝状菌污泥膨胀是污水处理厂常见的问题.通常需要耗时较长时间恢复膨胀污泥的良好沉降性能[1, 2], 期间水厂出水水质难以达到排放标准并且存在污泥流失的风险, 如Nakhla等[3, 4]调控膨胀污泥, 污泥体积指数(sludge volume index, SVI)历时两周从170 mL ·g-1降低至79 mL ·g-1, 同时污泥浓度从4 363 mg ·L-1降低至3 960 mg ·L-1.
投加絮凝剂快速增大污泥沉降速率以防止污泥流失, 是污水处理厂运行管理时应急性调控污泥膨胀的常用技术[5, 6], 但是实践效果差并且成本昂贵, 如Hawalli污水处理厂投加大量高分子聚合物控制出水悬浮物, 投加药剂时间长达两年, 期间药剂购置费不菲[7]. FeCl3是常用的絮凝剂之一[8, 9], 被广泛应用于调控污泥膨胀的实践中. Gregorio等[9]连续投加FeCl3至膨胀污泥, 4~5 d后SVI从550 mL ·g-1降低至150 mL ·g-1, 镜检结果表明FeCl3降低了丝状菌丰度, 认为FeCl3可以抑制丝状菌繁殖; 但是Pradhan等[10]使用PCR技术测试FeCl3投加前后污泥中的丝状菌数量, 数据表明FeCl3无抑制丝状菌繁殖的效果.虽然FeCl3调控污泥膨胀的机理目前尚不明确, 但是一般认为停止投加FeCl3后污泥沉降性能存在“反弹”现象[11].因此, 单独投加FeCl3控制污泥膨胀并非良策.
调试运行参数的生化技术也被广泛应用于调控污泥膨胀. Huang等[12]将连续曝气模式调控成交替曝气, SVI从350 mL ·g-1降低至140 mL ·g-1, 证明了交替曝气调控污泥膨胀的有效性.洪颖等[13]控制SBR反应器的DO浓度从0.5 mg ·L-1增大到3 mg ·L-1, 110 d后SVI从300 mL ·g-1稳定至70 mL ·g-1, 引起污泥膨胀的丝孢菌属(Trichosporon)相对丰度从94.82%降低至2.32%, 污泥的菌群多样性增加, 证明了调节DO浓度虽然能够实现调控污泥膨胀的本质目标——抑制丝状菌繁殖的同时促进菌胶团细菌生长, 但是见效慢, 耗时长.已有报道证明其他生化技术存在相同特点, 如刘佩等[14]增大COD浓度使有机负荷(以VSS计, 下同)从0.14 kg ·(kg ·d)-1增大至0.4 kg ·(kg ·d)-1, 虽然镜检结果显示丝状菌大量减少, 但是SVI从467 mL ·g-1降低到240 mL ·g-1共耗时35 d.单一的生化技术还具有通用性差的弊端, 如调节有机负荷、DO浓度等参数调控营养物失衡诱发的污泥膨胀往往没有效果.污水处理厂运行中, 通常对污泥膨胀的诱因不甚明了, “试错性”地应用单一生化技术调控污泥膨胀亦非工程管理的良策.
截止日前, 大部分研究者通过调节单一的生化参数诱导丝状菌膨胀[1, 12~14], 然后针对性地采用单一技术恢复污泥沉降性能, 这些研究的主要目的是为了证实单一技术调控已知诱因污泥膨胀的有效性和可逆性.研究者们甚少关注污水处理厂调控膨胀污泥的最迫切需求:实现调控的本质目标、有效预防污泥流失和保证出水水质达到排放标准.现有的污泥膨胀调控技术存在见效慢、耗时长和通用性差等共同缺点, 研究耦合技术避免“试错性”的工程应用, 是符合生产需求的研究趋势.
另外, 虽然Candidatus Saccharibacteria常见于地表环境[15]、动物人体[16]和活性污泥, 是污水处理厂常见的丝状菌[17], 但是高效调控由Candidatus Saccharibacteria引起的污泥膨胀鲜见报道.
本文以未知原因滋生大量Candidatus Saccharibacteria细菌的膨胀污泥为研究对象, 将反应器应急性地运行SBR工艺, 沉淀工序中投加FeCl3、提高DO和COD初始浓度形成FeCl3-生化耦合技术, 验证了耦合技术调控污泥膨胀的有效性, 分析了调控过程中污染物去除性能和微生物群落结构演替, 以期为应急性调控未知诱因的污泥膨胀提供工程应用依据.
1 材料与方法 1.1 实验装置和运行工况设计规格为500 mm×100 mm×250 mm(L×B×H)的反应器运行三段A/O工艺, 反应器介绍详见项目组已有报道[18].运行一段时间后系统发生未知诱因的污泥膨胀, 膨胀前一周内出水水质如表 1所示.
|
|
表 1 原三段A/O工艺一周内污染物处理性能 Table 1 Performance of the original step-feed A/O process within one week |
污泥膨胀后三段A/O反应器应急性运行SBR工艺, 1 d运行2个周期, 周期内工序是:①5 min完成进水, 进水量10 L; ②曝气180 min后关闭曝气装置, 间隔50 min后继续曝气, 反复3次, 即反应工序共历时690 min; ③为了缩短沉降工序的时间, 加入20 mL FeCl3溶液(60g ·L-1), 污泥历时20 min沉降至反应器底部; ④排除反应器上清液, 排水比80%.
实验中通过电磁式空气泵充气, 采用微孔曝气头做曝气器, 由转子流量计控制风量, 以维持曝气时DO为(7.45±0.49) mg ·L-1.反应工序结束时直接排放500 mL混合液, 控制平均污泥龄20 d.反应器中污泥浓度为3 143~3 856 mg ·L-1.
1.2 实验水质及分析方法本实验种泥取自于某城市污水处理厂, 三段A/O工艺运行过程中, 污泥掉落地面后SVI升高至274 mL ·g-1, 推测受地表Candidatus Saccharibacteria细菌感染而诱发污泥膨胀, 遂应用FeCl3-生化耦合技术调控污泥.调控过程采用模拟废水, 投加葡萄糖使COD初始浓度提升至(332.73±106.06) mg ·L-1.除葡萄糖用量差异, 模拟废水其他成分与运行三段A/O工艺时相同.实验用水成分详见表 2所示.
|
|
表 2 模拟废水组成成分 Table 2 Composition of the synthetic wastewater |
分析项目包括DO、COD、NH4+-N、NO3--N和PO43--P等水质指标.投加FeCl3前取泥水混合液测定污泥浓度和SV30. DO采用HQ30d型溶解氧仪(HACH, 美国)测定, 其他指标检测均采用国家标准方法[19].采用荧光倒置显微镜(TI-FL, Nikon, 日本)进行污泥镜检.
膨胀污泥调控前后(第1和18 d), 采用FastDNA® Spin Kit土壤试剂盒(MP Biomedicals, 美国)提取活性污泥微生物的DNA, 置于-80℃保存, 供高通量测序使用.委托上海美吉生物医药科技有限公司完成PCR扩增, 并基于Illumina MiSeq平台对扩增产物进行高通量测序. PCR扩增具体参考Wang等[20]的方法, 高通量测序数据处理具体参考徐伟超等[21]的方法, 完成可操作分类单元(operational taxonomic units, OTU)的计算.根据OTU值, 统计分析了门、属分类水平的微生物相对丰度, 计算公式如下:

|
污泥发生丝状菌膨胀后, SVI达274 mL ·g-1, 远高于正常值(50~150 mL ·g-1).反应器应急性运行SBR工艺、提高COD初始浓度至(332.73±106.06) mg ·L-1、反应工序引入交替曝气技术, 曝气时提高DO浓度至(7.45±0.49) mg ·L-1、沉淀工序开始投加FeCl3使之在混合液中浓度达120mg ·L-1, 形成的FeCl3-生化耦合技术调控污泥.根据污泥沉降性能, 调控过程分3个阶段, 如图 1所示.阶段Ⅰ(第1~8 d) SVI大于150mg ·L-1, 污泥沉降性能差.阶段Ⅱ(第9~13 d)污泥沉降性能恢复至正常水平但是仍未稳定, 随着耦合技术的持续应用, SVI呈现继续下降趋势.阶段Ⅲ(第14~18 d)污泥的沉降性能稳定, SVI稳定在56 mL ·g-1.说明FeCl3-生化耦合技术对丝状菌膨胀有良好地调控效果, 历时8 d SVI恢复至正常值, 14 d污泥沉降性能恢复至稳定状态.

|
图 1 污泥沉降性能恢复过程中SVI和SV30的时间变化 Fig. 1 Temporal variation of SVIs and SV30 during the process of restoring sludge settleability |
图 2是应用FeCl3-生化耦合技术前后污泥的镜检图.丝状菌膨胀暴发伊始, 丝状菌从菌胶团伸展开来, 污泥絮凝体松散而不规则[图 2(a)].持续应用耦合技术后, 虽然仍有少量丝状菌从菌胶团伸展开来, 但是污泥呈现浓厚紧密状态.推断认为FeCl3-生化耦合技术能高效抑制丝状菌繁殖同时促进菌胶团细菌生长.
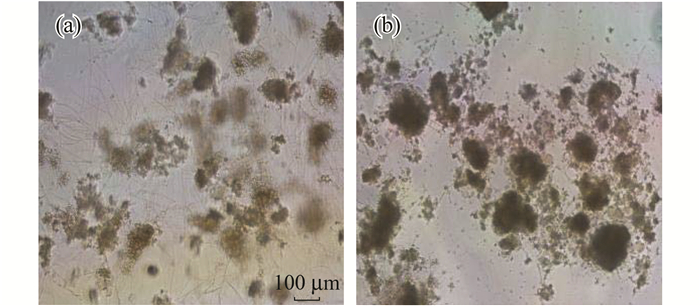
|
(a)第1 d; (b)第18 d 图 2 污泥显微镜镜检图 Fig. 2 Microscopic images of sludge |
已有研究证明高底物或DO浓度条件有利于菌胶团细菌对有机物的储存和利用, 其生长速率常数大于丝状菌, 既促进了菌胶团细菌的生长又抑制了丝状菌的过量生长[13, 22].推断认为调控过程中有机负荷和DO浓度增加促进了菌胶团细菌的快速繁殖, 是FeCl3-生化耦合技术有效调控污泥膨胀的根本原因.需要注意的是过量提高COD浓度致使有机负荷大于生化系统承受能力时存在进一步恶化污泥沉降性能的风险[1]; 又有研究证明可生化的颗粒态有机基质有利于丝状菌繁殖, 交替曝气过程中停止曝气阶段系统呈现还原环境, 颗粒态有机基质发生水解作用将减缓丝状菌的繁殖速率[3], 推断认为FeCl3-生化耦合技术因为引入了交替曝气技术可降低高有机负荷恶化污泥沉降性能的风险.鉴于模拟废水的有机基质是不可水解的葡萄糖, 交替曝气在耦合技术中的作用需进一步实验验证.反应器沉淀工序伊始投加FeCl3, 排出上清液后部分残留FeCl3进入下一周期混合液, 因为反应器重新进水对残留FeCl3具有稀释作用, 混合液FeCl3浓度小于100mg ·L-1(稀释前120mg ·L-1), 不大于100mg ·L-1的FeCl3增强了细菌对DO的摄取速率[5], 提高DO浓度至(7.45±0.49) mg ·L-1保障了DO的充足供应, 促进菌胶团细菌生长.
2.2 污染物去除性能图 3分析了调控污泥膨胀过程中主要污染物的去除性能.前2个周期, 出水COD浓度略高于其他周期[图 3(a)], 这是污泥中微生物适应新的工艺和进水COD浓度导致的.微生物适应后, 出水COD浓度在3个阶段均稳定达标, 阶段Ⅰ、Ⅱ和Ⅲ的平均去除率依次是97.50%、97.92%和98.54%, 说明污泥膨胀对COD去除无明显影响, 与其他研究结论一致[12], 同时也证明FeCl3-生化耦合技术对COD去除无负面影响.
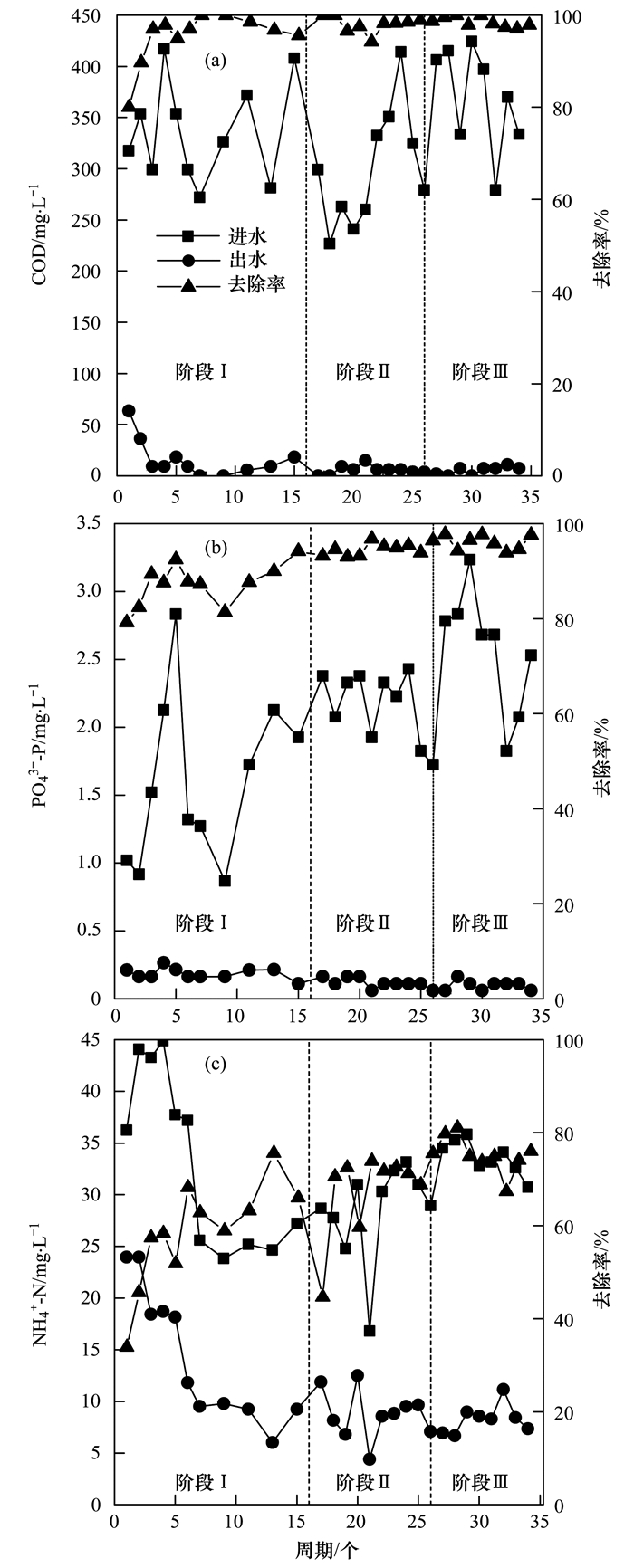
|
(a) COD; (b) PO43--P; (c) NH4+-N 图 3 膨胀污泥调控过程中污染物去除性能 Fig. 3 Performance of contaminant removal during the process of filamentous bulking control |
出水PO43--P浓度均低于0.50mg ·L-1[图 3(b)], 达到《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准[23]. 3个阶段20 min时PO43--P去除率达80%, 除磷速率大于正常的生物除磷速率[24, 25], 这是因为PO43-与残留Fe3+共沉淀而被迅速去除.为了进一步研究除磷机理, 反应工序曝气阶段60 min取样一次, 停止曝气阶段25 min取样一次分析混合液中PO43--P的浓度变化, 图 4(a)分析了阶段Ⅰ、Ⅱ和Ⅲ的PO43--P去除情况.反应器停止曝气, 混合液PO43--P浓度略微升高[图 4(a)], 推断认为反应器中进行厌氧释磷的生化反应, 说明反应器内同时发生了生物除磷.生物除磷的存在, 导致了调控过程中3个阶段PO43--P平均去除率的差异, 阶段Ⅰ、Ⅱ和Ⅲ中PO43--P平均去除率依次是87.22%、94.58%和95.88%.生物除磷效率随剩余污泥排放量的增大而增大, 3个阶段平均污泥浓度分别是3 524, 3 776和3 710 mg ·L-1, 从反应器直接排放500 mL混合液的实质是阶段Ⅱ和Ⅲ排放的剩余污泥相近, 略大于阶段Ⅰ, 所以随着污泥沉降性能的恢复, 阶段Ⅱ和Ⅲ的PO43--P去除率相近, 略高于阶段Ⅰ.

|
(a) PO43--P; (b)NH4+-N; (c) NO3--N on:曝气启动off:曝气停止 图 4 典型周期内污染物去除特征 Fig. 4 Typical cycle profiles of contaminants |
如图 3(c), 前5个周期NH4+-N的高浓度进水导致出水浓度相较其他周期高.不考虑此5个周期, 阶段Ⅰ、Ⅱ和Ⅲ出水NH4+-N平均质量浓度依次是(8.76±2.75)、(8.40±4.08)和(8.32±2.82) mg ·L-1, 出水NH4+-N略大于一级A标准[23], 推测主要是因为:没有脱氮功能的丝状菌是阶段Ⅰ中污泥的主要微生物, NH4+-N无法被顺利转化成N2而残留水中; 阶段Ⅱ和Ⅲ虽然污泥的沉降性能良好, 但是参与去除NH4+-N的微生物数量依然较少, 所以NH4+-N去除量有限.实验中混合液温度(12±2)℃, 低于微生物脱氮的最佳温度(15~20℃)[26], 推断温度低也是NH4+-N出水不达标的原因之一.阶段Ⅰ、Ⅱ和Ⅲ出水NH4+-N质量浓度相近, 但是去除率依次增加[图 3(c)], 3个阶段NH4+-N平均去除率依次是65.33%、70.33%和74.65%.为了研究NH4+-N去除率增大的原因, 分析了3个阶段内典型周期内NH4+-N和NO3--N随时间的变化, 分别如图 4(b)和4(c)所示.各阶段NH4+-N去除速率相等[图 4(b)], 但是阶段Ⅱ(第21周期)NO3--N明显随时间累积[图 4(c)], 阶段Ⅰ(第3周期)和阶段Ⅲ(第32周期)无NO3--N积累现象, 推断3个阶段中NH4+-N的有效去除并非均依赖于硝化-反硝化作用. NH4+-N的硝化-反硝化生化途径如方程式(1)~(4)所示.阶段Ⅱ发现NO3--N随时间在反应器中积累, 说明污泥膨胀导致方程式(3)和(4)表示的反硝化生化体系中断.假设污泥膨胀后仍然可以顺利进行方程式(1)和(2)表示的硝化反应, 考虑高浓度DO(cDO≥2mg ·L-1)条件下NO2--N无法积累在反应器中[27], 则阶段Ⅰ应该可以发现如阶段Ⅱ相似的NO3--N积累现象.阶段Ⅰ无NO3--N积累, 说明假设不成立, 推断认为污泥膨胀后微生物的硝化生化体系中断.阶段Ⅰ至阶段Ⅱ期间重建了硝化体系, 阶段Ⅱ至阶段Ⅲ时间内重建了反硝化体系, 所以NO3--N的积累现象从无到有, 然后再次消失.
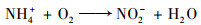
|
(1) |

|
(2) |

|
(3) |

|
(4) |
图 5分析了污泥样品中门分类水平微生物群落(相对丰度≥1%), BS是膨胀污泥样品, AS是恢复良好沉降性能的活性污泥样品. Candidatus Saccharibacteria是BS样品最主要的门水平细菌, 相对丰度达97.64%(图 5).鉴于BS样品中未检测出其他丝状菌, 说明Candidatus Saccharibacteria菌门是引起污泥丝状菌膨胀的唯一原因.污泥沉降性能稳定后, Candidatus Saccharibacteria菌门的相对丰度降低至32.67%(AS样品), 说明FeCl3-生化耦合技术可以抑制丝状菌的生长.
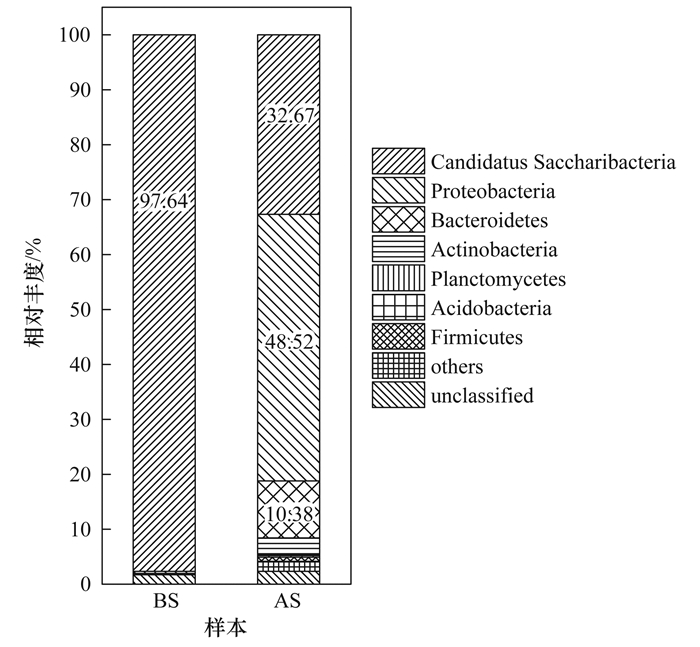
|
图 5 膨胀污泥(BS)和活性污泥(AS)中微生物门水平群落分布 Fig. 5 Community distribution of microorganism on phylum level in bulking sludge(BS) and activated sludge(AS) |
应用FeCl3-生化耦合技术前后, 污泥样品最大相对丰度的菌属均是Candidatus Saccharibacteria.样品BS和AS中Candidatus Saccharibacteria占比分别是97.64%和32.67%. Ma等[28]同样发现Candidatus Saccharibacteria在具有良好沉降性能的活性污泥中成为优势菌属, 说明Candidatus Saccharibacteria虽然是丝状菌, 其相对丰度不超过一定限值时并不会引起污泥膨胀. AS样品中还繁殖有球衣细胞菌属(Sphaerotilus), 是一种常见的丝状菌[29], 其在AS样品的相对丰度是12.46%.球衣细胞菌属(Sphaerotilus)也被分类为铁细菌(iron bacteria), FeCl3絮凝剂的投加可能是球衣细胞菌属(Sphaerotilus)滋生的原因之一. Mulder等[30]进行对比实验, 发现在简单有机基质和营养物中球衣细胞菌属(Sphaerotilus)的生物量是复杂基质中的2.82倍, 说明本研究简单的有机基质和营养物质是促进球衣细胞菌属(Sphaerotilus)滋生的另外一个原因.
样品BS和AS分别检测出70种和188种属分类水平微生物群落, 说明应用FeCl3-生化耦合技术后污泥的物种丰富度变大.恢复良好沉降性能后, 污泥主要菌属(相对丰度≥1%)还包括动胶菌属(Zoogloea)占比14.06%, 铁杆菌属(Ferribacterium)占比1.95%, Tolumonas占比4.62%, 黄杆菌属(Flavobacterium)占比1.90%, Ohtaekwangia占比1.27%, Nakamurella占比1.19%和紫色杆菌属(Janthinobacterium)占比1.05%.说明FeCl3-生化耦合技术可以促进菌胶团细菌的繁殖.
分析Illumina MiSeq测序数据, BS样品无硝化菌检出, AS样品繁殖了少量硝化菌, 硝化螺菌属(Nitrospira)和亚硝化单胞菌属(Nitrosomonas)相对丰度分别是0.25%和0.003%.污泥中硝化菌从无到有, 印证了FeCl3-生化耦合技术调控丝状菌污泥膨胀过程中重建了硝化体系的推测.硝化菌是高效去除NH4+-N的重要菌属, 具有世代时间长和生长速率慢的特征[31], 调控过程历时18 d, 时间短是AS样品中硝化菌数量少的原因.
如表 3主要参照Shapleigh[32]归纳总结的84种反硝化菌分析了调控前后污泥样品的反硝化菌及丰度. BS样品反硝化菌相对丰度总和仅有0.20%, AS样品反硝化菌相对丰度总和是20.78%(表 3), 说明FeCl3-生化耦合技术促进了反硝化菌繁殖.调控过程第3周期无NO3--N积累, 第21周期发现大量NO3--N积累而不能进一步转化成N2, 第32周期NO3--N的积累现象消失[图 4(c)], 结合反硝化菌相对丰度的增加, 印证了反应器重建了反硝化生化体系的推断.
|
|
表 3 污泥样品中反硝化菌属相对丰度统计 Table 3 Relative abundance of putative denitrifying genera detected in sludge samples |
3 结论
(1) 三段A/O反应器应急性运行SBR工艺、交替曝气中提高DO浓度至(7.45±0.49) mg ·L-1、提高COD初始浓度至(332.73±106.06) mg ·L-1、沉淀工序中投加FeCl3使之在混合液中浓度达120mg ·L-1, 形成的FeCl3-生化耦合技术快速调控未知诱因的丝状菌污泥膨胀, SVI在8d恢复至正常值(≤150mg ·L-1), 14 d稳定至56mg ·L-1.
(2) 调控过程出水COD和PO43--P浓度均稳定达到《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准, NH4+-N去除率从65.33%增加至74.65%, 重建了硝化-反硝化生化体系.
(3) FeCl3-生化耦合技术有效抑制Candidatus Saccharibacteria繁殖并且促进菌胶团细菌生长, Candidatus Saccharibacteria细菌的属水平及门水平相对丰度均从97.64%降低至32.67%.
| [1] | Palm J C, Jenkins D, Parker D S. Relationship between organic loading, dissolved oxygen concentration and sludge settleability in the Completely-Mixed activated sludge process[J]. Journal (Water Pollution Control Federation), 1980, 52(10): 2484-2506. |
| [2] | Tsang Y F, Chua H, Sin S N, et al. A novel technology for bulking control in biological wastewater treatment plant for pulp and paper making industry[J]. Biochemical Engineering Journal, 2006, 32(3): 127-134. DOI:10.1016/j.bej.2006.08.014 |
| [3] | Nakhla G, Lugowski A. Control of filamentous organisms in food-processing wastewater treatment by intermittent aeration and selectors[J]. Journal of Chemical Technology & Biotechnology, 2003, 78(4): 420-430. |
| [4] | Al-Mutairi N Z. Aerobic selectors in slaughterhouse activated sludge systems:a preliminary investigation[J]. Bioresource Technology, 2009, 100(1): 50-58. DOI:10.1016/j.biortech.2007.12.030 |
| [5] | Al-Mutairi N Z, Hamoda M F, Al-Ghusain I. Coagulant selection and sludge conditioning in a slaughterhouse wastewater treatment plant[J]. Bioresource Technology, 2004, 95(2): 115-119. DOI:10.1016/j.biortech.2004.02.017 |
| [6] | Philips S, Rabaey K, Verstraete W. Impact of iron salts on activated sludge and interaction with nitrite or nitrate[J]. Bioresource Technology, 2003, 88(3): 229-239. DOI:10.1016/S0960-8524(02)00314-0 |
| [7] | Oladoja N A, Aliu Y D. Snail shell as coagulant aid in the alum precipitation of malachite green from aqua system[J]. Journal of Hazardous Materials, 2009, 164(2-3): 1496-1502. DOI:10.1016/j.jhazmat.2008.09.114 |
| [8] | Guo W S, Ngo H H, Vigneswaran S, et al. Effect of different flocculants on short-term performance of submerged membrane bioreactor[J]. Separation and Purification Technology, 2010, 70(3): 274-279. DOI:10.1016/j.seppur.2009.10.003 |
| [9] | De Gregorio C, Caravelli A H, Zaritzky N E. Performance and biological indicators of a laboratory-scale activated sludge reactor with phosphate simultaneous precipitation as affected by ferric chloride addition[J]. Chemical Engineering Journal, 2010, 165(2): 607-616. DOI:10.1016/j.cej.2010.10.004 |
| [10] | Pradhan S K, Torvinen E, Siljanen H M P, et al. Iron flocculation stimulates biogas production in Microthrix parvicella-spiked wastewater sludge[J]. International Journal of Environmental Science and Technology, 2015, 12(9): 3039-3046. DOI:10.1007/s13762-014-0733-6 |
| [11] | Martins A M P, Pagilla K, Heijnen J J, et al. Filamentous bulking sludge-a critical review[J]. Water Research, 2004, 38(4): 793-817. DOI:10.1016/j.watres.2003.11.005 |
| [12] | Huang L, Ju L K. Sludge settling and online NAD(P)H fluorescence profiles in wastewater treatment bioreactors operated at low dissolved oxygen concentrations[J]. Water Research, 2007, 41(9): 1877-1884. DOI:10.1016/j.watres.2007.01.040 |
| [13] |
洪颖, 姚俊芹, 马斌, 等. 基于高通量测序的SBR反应器丝状膨胀污泥菌群分析[J]. 环境科学, 2018, 39(7): 3279-3285. Hong Y, Yao J Q, Ma B, et al. Filamentous sludge microbial community of a SBR reactor based on high-throughput sequencing[J]. Environmental Science, 2018, 39(7): 3279-3285. |
| [14] |
刘珮, 袁林江, 陈希, 等. 低负荷氧化沟系统中EPS与活性污泥沉降性能的关系[J]. 环境科学学报, 2013, 33(6): 1611-1615. Liu P, Yuan L J, Chen X, et al. Relationship between EPS and activated sludge sedimentation performance in the low-load oxidation ditch system[J]. Acta Scientiae Circumstantiae, 2013, 33(6): 1611-1615. |
| [15] | Borneman J, Triplett E W. Molecular microbial diversity in soils from eastern Amazonia:evidence for unusual microorganisms and microbial population shifts associated with deforestation[J]. Applied and Environmental Microbiology, 1997, 63(7): 2647-2653. |
| [16] | He X S, McLean J S, Edlund A, et al. Cultivation of a human-associated TM7 phylotype reveals a reduced genome and epibiotic parasitic lifestyle[J]. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(1): 244-249. DOI:10.1073/pnas.1419038112 |
| [17] | Hugenholtz P, Tyson G W, Webb R I, et al. Investigation of candidate division TM7, a recently recognized major lineage of the domain Bacteria with no known pure-culture representatives[J]. Applied and Environmental Microbiology, 2001, 67(1): 411-419. DOI:10.1128/AEM.67.1.411-419.2001 |
| [18] |
肖才林, 沈建华, 杨洋, 等. 三段A/O工艺处理发制品产业集聚区综合废水[J]. 中国环境科学, 2018, 38(4): 1304-1311. Xiao C L, Shen J H, Yang Y, et al. Utilizing three step feed A/O process to treate comprehensive wastewater from hair product production cluster area[J]. China Environmental Science, 2018, 38(4): 1304-1311. |
| [19] |
国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002: 211-281. The State Environmental Protection Administration. Water and wastewater monitoring and analysis method[M]. 4th ed.. Beijing: China Environmental Science Press, 2002: 211-281. |
| [20] | Wang Z B, Miao M S, Kong Q, et al. Evaluation of microbial diversity of activated sludge in a municipal wastewater treatment plant of northern China by high-throughput sequencing technology[J]. Desalination and Water Treatment, 2016, 57(50): 23516-23521. DOI:10.1080/19443994.2015.1137232 |
| [21] |
徐伟超, 蒙小俊, 尹莉, 等. 焦化废水活性污泥中降解硫氰化物细菌种群多样性分析[J]. 环境科学, 2016, 37(7): 2689-2695. Xu W C, Meng X J, Yin L, et al. Biodiversity of thiocyanate-degrading bacteria in activated sludge from coking wastewater[J]. Environmental Science, 2016, 37(7): 2689-2695. |
| [22] |
杨雄, 彭永臻, 宋姬晨, 等. 进水中碳水化合物分子大小对污泥沉降性能的影响[J]. 中国环境科学, 2015, 35(2): 448-456. Yang X, Peng Y Z, Song J C, et al. Effect of influent carbohydrates with different molecule-size on sludge settleability[J]. China Environmental Science, 2015, 35(2): 448-456. |
| [23] | GB 18918-2002, 城镇污水处理厂污染物排放标准[S]. |
| [24] | Chen H B, Wang D B, Li X M, et al. Effect of dissolved oxygen on biological phosphorus removal induced by aerobic/extended-idle regime[J]. Biochemical Engineering Journal, 2014, 90: 27-35. DOI:10.1016/j.bej.2014.03.004 |
| [25] | Wang D B, Li X M, Yang Q, et al. Biological phosphorus removal in sequencing batch reactor with single-stage oxic process[J]. Bioresource Technology, 2008, 99(13): 5466-5473. DOI:10.1016/j.biortech.2007.11.007 |
| [26] | Zhu R, Wu M, Yang J. Effect of sludge retention time and phosphorus to carbon ratio on biological phosphorus removal in HS-SBR process[J]. Environmental Technology, 2013, 34(4): 429-435. DOI:10.1080/09593330.2012.698650 |
| [27] | Fillos J, Diyamandoglu V, Carrio L A, et al. Full-scale evaluation of biological nitrogen removal in the step-feed activated sludge process[J]. Water Environment Research, 1996, 68(2): 132-142. |
| [28] | Ma S J, Ding L L, Huang H, et al. Effects of DO levels on surface force, cell membrane properties and microbial community dynamics of activated sludge[J]. Bioresource Technology, 2016, 214: 645-652. DOI:10.1016/j.biortech.2016.04.132 |
| [29] | Richard M, Hao O, Jenkins D. Growth kinetics of Sphaerotilus Species and their significance in activated sludge bulking[J]. Journal (Water Pollution Control Federation), 1985, 57(1): 68-81. |
| [30] | Mulder E G. Iron Bacteria, particularly those of the Sphaerotilus-Leptothrix group, and industrial problems[J]. Journal of Applied Microbiology, 1964, 27(1): 151-173. |
| [31] | Gee C S, Pfeffer J T, Suidan M T. Nitrosomonas and nitrobacter interactions in biological nitrification[J]. Journal of Environmental Engineering, 1990, 116(1): 4-17. |
| [32] | Shapleigh J P. The denitrifying prokaryotes[A]. In: Dworkin M, Stanley F, Rosenberg E, et al (Eds.). The Prokaryotes[M]. New York, NY: Springer, 2006. 769-792. |
| [33] | Tabassum S, Wang Y, Zhang X J, et al. Novel mass bio system (MBS) and its potential application in advanced treatment of coal gasification wastewater[J]. RSC Advances, 2015, 5(108): 88692-88702. DOI:10.1039/C5RA11506J |
| [34] | Tian H L, Zhao J Y, Zhang H Y, et al. Bacterial community shift along with the changes in operational conditions in a membrane-aerated biofilm reactor[J]. Applied Microbiology and Biotechnology, 2015, 99(7): 3279-3290. DOI:10.1007/s00253-014-6204-7 |
| [35] | McIlroy S J, Starnawska A, Starnawski P, et al. Identification of active denitrifiers in full-scale nutrient removal wastewater treatment systems[J]. Environmental Microbiology, 2016, 18(1): 50-64. DOI:10.1111/1462-2920.12614 |
| [36] | Yu Z, Yang J, Liu L M. Denitrifier community in the oxygen minimum zone of a subtropical deep reservoir[J]. PLoS One, 2014, 9(3). |
| [37] | Di Capua F. Nitrogen removal in low pH and heavy metal contaminated mine wastewaters[D]. Italy: University of Napoli "Federico Ⅱ" Napoli, 2012. |
 2019, Vol. 40
2019, Vol. 40


