2. 华中科技大学能源与动力工程学院新能源科学与工程系, 武汉 430074;
3. 深圳市水务(集团)有限公司, 深圳 518031
2. Department of New Energy Science and Engineering, School of Energy and Power Engineering, Huazhong University of Science and Technology, Wuhan 430074, China;
3. Shenzhen Water Group Co., Ltd., Shenzhen 518031, China
湖泊富营养化问题是我国亟待解决的重大环境问题之一[1], 在近30年来, 快速的城市化、工业化和农业集约化对水资源造成严重污染[2].水体富营养化会使有害藻类和其他水生微生物快速生长繁殖, 大量消耗水中的氧气, 导致水体缺氧, 严重危害其他水生动植物的生存繁殖, 造成河流湖泊的生态破坏, 进而对人类的生产与生活造成严重影响[3].水体富营养化的主要成因是磷营养盐浓度过高, 因此处理水体富营养化的关键在于控制磷的含量[4~6].在众多除磷方法中, 吸附法具有工艺简单、选择性好、经济性高等特点, 得到广泛关注和使用[7].
吸附法使用的吸附剂包括硅胶、氧化铝、活性炭、沸石和生物炭等, 其中生物炭具有可再生, 来源广, 成本低等优势而成为研究和应用的热点.而直接热解得到的生物炭比表面积往往较低, 吸附活性位点较少, 表面官能团不够丰富, 因此有必要对生物炭进行活化改性[8]. Alvarez等[9]用H2O和CO2作为活化剂快速热解稻壳制备高BET比表面积生物炭, 并且CO2活化炭比水蒸气活化炭具有更发达的微孔结构. Chen等[10]利用毛竹制备了环保型蒙脱石-生物炭复合材料, 其Langmuir最大吸附量为105.28 mg ·g-1, 吸附之后得到的样品可以作为N、P的有效缓释肥料. Zhang等[11]用液相沉积法制备了生物炭/MgAl-layered double hydroxides(LDHs)超细复合材料, 结果表明, MgAl-LDHs表现出对磷酸根极强的吸附能力, 最大吸附量为410 mg ·g-1, 并且能在1 h内达到吸附平衡. Jung等[12]采用MgCl2、FeCl3前改性裙带菜根的方法制备MgFe2O4/生物炭磁性复合材料, 具有显著的吸附性能, 吸附理论值达487.99 mg ·g-1.然而, MgCl2、FeCl3在热解过程中会生成MgO、Fe2O3晶体[13]和污染性的HCl气体[14].负载在炭表面的MgO可以和磷酸盐形成表面沉淀, 从而大大提高磷吸附量[11].
莲是一种水生植物, 其中的莲蓬壳除了较少部分用于食品和药材[15]之外, 绝大部分被当作垃圾和低热值燃料处理.事实上, 莲蓬壳经过热解活化得到的高比表面积材料, 可以应用于超级电容的电极材料[16]和CO2捕集[17].
然而, Mg改性莲蓬壳基生物炭对富营养化水体磷的吸附研究还鲜有报道, 因此本文选用莲蓬壳作为生物炭前驱体, 混合一定比例的纳米MgO, 通适量的N2和CO2载气, 通过快速热解制纳米MgO负载的生物炭(MBC), 旨在获得高效去除水体中磷的吸附剂.本实验研究了MgO负载量对MBC吸附磷的影响, 通过BET、XRD、SEM和TEM等表征分析了MBC的理化特性, 探讨了MBC对磷酸根的吸附动力学特性和等温吸附特性.
1 材料与方法 1.1 实验原料以湖北省武汉市周边收集的废弃莲蓬壳为研究对象, 对莲蓬壳水洗、干燥, 粉碎过筛, 得到60~120目颗粒作为实验原料, 其工业分析和元素分析见表 1.纳米MgO(50 nm, 99.9%)购自阿拉丁试剂, 二水合磷酸二氢钠(NaH2PO4 ·2H2O)购自国药集团化学试剂有限公司.
|
|
表 1 莲蓬壳工业分析及元素分析 Table 1 Proximate analysis and ultimate analysis of lotus shells |
1.2 纳米MgO-生物炭吸附剂的制备
纳米MgO-生物炭吸附剂(MBC)的制备分预混浸渍与热解两个步骤.首先将纳米MgO和莲蓬壳按不同质量比例(0 :10、1 :9、3 :7、5 :5、7 :3、9 :1和10 :0)置于烧杯中, 加入50 mL去离子水, 搅拌8 h(磁力搅拌器), 抽滤后放入105℃烘箱中干燥24 h后, 放置于干燥皿中备用.
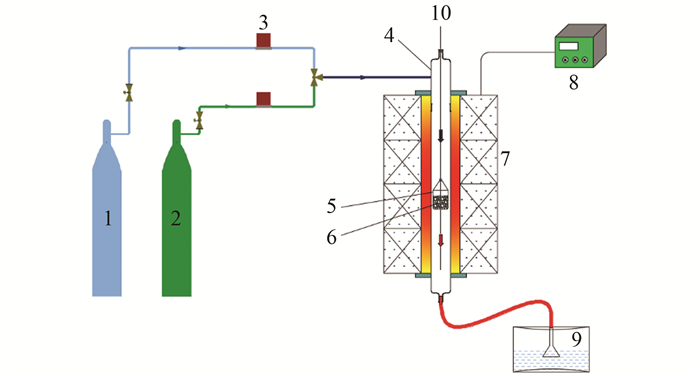
莲蓬壳的快速热解制炭实验在立式炉固定床反应系统(图 1)中进行, 反应器内径42 mm, 长690 mm.
|
1. N2; 2. CO2; 3.质量流量计; 4.固定床反应器; 5.石英吊篮; 6.样品; 7.加热炉; 8.温度控制器; 9.尾气处理单元; 10.铁丝 图 1 立式炉固定床反应系统示意 Fig. 1 Vertical fixed bed reaction system |
本实验分A、B两组进行. A组实验中样品为不同比例预混浸渍后的纳米MgO/莲蓬壳粉末, 样品量为2g.载气为高纯N2(99.99%), 流量为200 mL ·min-1, 热解温度为700℃, 保温2h, 反应后冷却至室温, 得到纳米MgO负载生物炭吸附剂, 分别记为MBC1、MBC2、MBC3、MBC4、MBC5、MBC6和MBC7. B组实验样品中纳米MgO与莲蓬壳的混合比例为0 :10、1 :9、3 :7和5 :5, 载气为高纯N2和高纯CO2混合气氛, 载气流量分别为180 mL ·min-1与20 mL ·min-1, 其他条件与A组实验相同, 得到的纳米MgO负载生物炭吸附剂, 分别记为MBC8、MBC9、MBC10和MBC11.
1.3 纳米MgO-生物炭的特性分析采用全自动比表面积吸附仪(BET, 美国麦克仪器公司, ASAP-2020)测MBC的比表面积等孔隙结构; 通过X型射线衍射仪(XRD, 荷兰帕纳科公司, X'Pert PRO)对MgO-生物炭复合材料的晶体成分进行分析; 采用扫描电镜(SEM荷兰FEI公司, Quanta 200)观察MBC的微观形貌; 通过透射电子显微镜(TEM荷兰FEI公司, Tecnai G2 20)观察纳米MgO晶体在生物炭上的负载情况.溶液中磷酸根离子浓度用紫外/可见分光光度计(上海翱艺仪器有限公司, A系列)测量.
1.4 吸附实验模拟含磷水溶液是通过将1 200 mg NaH2PO4 ·2H2O溶于1 L去离子水制备1 200 mg ·L-1的磷酸盐原溶液, 吸附实验在20℃室温下进行, 将30 mL磷酸盐原溶液与0.050 g各吸附剂加入离心管, 通过加入0.1 mol ·L-1的NaOH溶液或0.1 mol ·L-1的盐酸溶液来调节pH至5.0±0.1, 密封后置于旋转振荡仪上振荡24 h后, 取下离心管, 用0.22 μm的水系一次性针头过滤器将混合物过滤, 将滤液稀释一定倍数, 借助紫外分光光度计, 通过钼酸铵法(GB 11893-89)测定磷酸根离子浓度.
吸附动力学实验方法与上述实验相同, 分别在10、30、60、120、240、480、720和1 440 min取样, 测定溶液浓度; 在等温吸附实验中, NaH2PO4 ·2H2O溶液初始浓度为50~2 500 mg ·L-1.
2 结果与讨论 2.1 孔隙结构分析MBC的孔隙结构参数如表 2所示.在A组中, 根据平均孔径来看, MBC主要为介孔材料, 随着MgO比例的增加, 平均孔径逐渐变大, 微孔体积和比表面积减小, 总孔体积增大. MBC6微孔消失不见, 转化为介孔和大孔.在B组中, 未负载MgO的莲蓬壳炭MBC8主要为微孔, 比表面积为752.749 m2 ·g-1, 是MBC1的2.48倍, 这归因于10% CO2载气作为一种改性剂, 起到了良好的扩微孔作用, 微孔比面积和体积分别增加了1.75倍和1.05倍; 值得注意的是, 负载MgO后, B组MBC9~MBC11分别对应于A组MBC2~MBC4, 由于纳米MgO颗粒堵塞了微孔和部分介孔, 导致微孔体积和比表面积大幅减小[18], 其中MBC10微孔面积为零, 比表面积仅为27.699 m2 ·g-1.
|
|
表 2 纳米MgO-生物炭孔隙结构特性 Table 2 Pore structure characteristics of MBC |
2.2 MBC晶体成分分析
MBC的X射线衍射分析图谱如图 2所示.在A组MBC中, 整体来看, 除了明显的特征衍射峰外, 没有观察到杂峰.原始莲蓬壳生物炭MBC1在2θ为28.346°和40.509°位置可观察到KCl衍射特征峰.说明莲蓬壳中存在K和Cl元素.随着MgO比重的增加, 特征峰强度逐渐降低, KCl质量分数减少, MBC5之后基本观察不到; 从MBC2开始可以在2θ为36.889°、42.856°、62.217°、74.578°和78.510°的位置观察到MgO晶体的特征峰, 并且峰的强度逐渐增大.

|
图 2 X射线衍射图谱 Fig. 2 Wide angle XRD patterns of MBC |
在B组中, 热解气氛为10% CO2和90% N2, 可以观察到莲蓬壳生物炭MBC8的XRD图在2θ为29.5°处有CaCO3的特征峰, 这可能是因为在热解结束后的冷却过程中CO2与CaO生成CaCO3, 随着MgO比重的增加, MBC8~MBC11的CaCO3特征峰的强度减弱; KCl特征峰在MBC8的XRD曲线上不明显, 在MBC9~MBC11的XRD曲线中的峰强减弱; MgO特征峰强度先增加后不变.
2.3 MBC微观形貌分析为了更好地分析MgO-生物炭的形态结构, 对MBC进行了扫描电镜(SEM-EDS)和透射电镜(TEM)分析. 图 3为MBC样品的扫描电镜图, MgO在生物炭表面主要呈现为颗粒状和薄片状, 在A组的MBC2中MgO为颗粒状晶体形态, 随着MgO比例的增加, 在MBC3、MBC4中MgO呈晶体薄片均匀地沉积在炭表面, 可以从MBC4的X射线能谱分析(EDS)可以得到证明; 在B组MBC9~MBC11中, 可以观察到大多是颗粒状MgO晶体, 而在MBC11中可以观察到少量的薄片状MgO.

|
图 3 MBC的扫描电镜SEM图 Fig. 3 SEM image of MBC |
透射电镜TEM图(图 4)观察到的MgO形貌与SEM图具有相同的特征.可以看到, 在CO2的活化下, 未混合MgO的MBC8相对于MBC1表面更加粗糙, 孔隙率高.随着MgO比例的增加, MBC3中可观察到一簇簇和一片片的晶体, 而在MBC4、MBC5中观察到的是一片片的晶体, 这是因为观察角度的不同.透射图中颜色较深部位是MgO发生团聚的结果. MgO/莲蓬壳混合比例越高, 团聚越严重, MBC10相对于MBC9来说团聚较为严重, 这是因为MBC10中莲蓬壳生物质质量分数低于MBC9, 另外CO2与生物炭发生反应消耗了部分炭.

|
图 4 MBC的TEM透射电镜图 Fig. 4 TEM image of MBC |
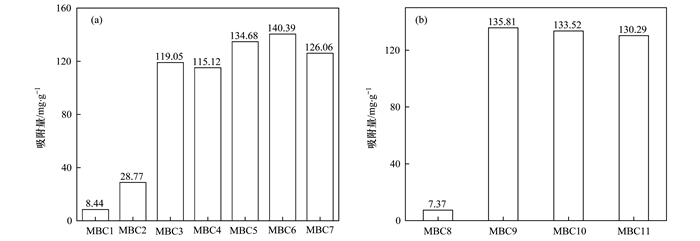
通过一系列的吸附实验得到了11种MgO-生物炭吸附剂的磷吸附量(单位以P计), 如图 5所示.
|
图 5 MBC的磷吸附量 Fig. 5 Effects of MgO/biochar ratio on adsorption |
可以看出, 莲蓬壳生物炭负载MgO可以大大提高对磷酸根的吸附量, 在A组中, 未负载MgO的MBC1的吸附量仅为8.44 mg ·g-1, 负载纳米MgO的MBC3和MBC9的磷吸附量分别达到119.05 mg ·g-1和135.81 mg ·g-1, 分别是MBC1的14倍和16倍左右.结合孔隙特征和微观形貌分析来看, 莲蓬壳炭表面负载上大量薄片状MgO晶体, 这种薄片状结构增加了吸附位点, 更容易传质, 有利于增加对磷酸根吸附量[13].随着MgO/生物质比例的增加, MBC总孔体积增加, 这有利于容纳更多的磷酸根离子, 同时MgO在莲蓬壳炭上的团聚程度不断提高, MBC的磷酸根吸附量不断增加, MBC6吸附量达到最大.在B组中, 未负载MgO的MBC8的磷吸附量为7.37 mg ·g-1, MBC9的吸附量最大, 为135.81 mg ·g-1, 是MBC8的18倍左右.随着MgO/生物质比重增加, MBC的吸附量迅速增加, MBC9的吸附量达到最大值, 而在MBC10的TEM和SEM图中, 观察到MgO团聚程度过高, MgO晶体相互覆盖, 有效的吸附活性位点减少, 吸附量略有降低.
A、B组比较来看, MBC8孔隙率比MBC1的更加发达, 但是二者吸附量都很低且相差不大, 说明在莲蓬壳炭未负载纳米MgO时, 孔隙率不是影响磷吸附的主导因素; 莲蓬壳炭负载MgO时, 由于CO2的扩孔作用, 比表面积增加, 使得MgO更好地负载在炭表面, 有效吸附活性位点增加, 因此B组中MBC吸附量要普遍高于A组.
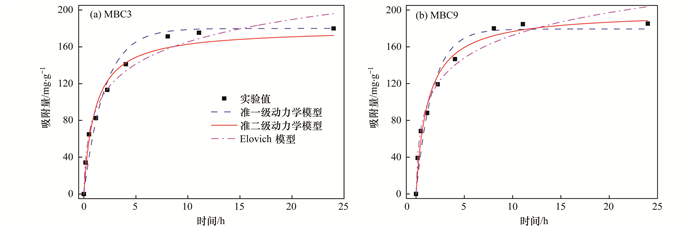
2.5 吸附动力学在A和B组分别选择了磷吸附量较高, 同时MgO混合比例低的MBC3和MBC9进行吸附动力学实验, 实验测得了MBC3和MBC9在不同时间的吸附量, 如图 6所示, 二者的吸附可分为快速吸附阶段和缓慢吸附阶段.吸附的前4 h为快速吸附阶段, 生物炭与溶液中磷浓度相差较大, 吸附势大, MgO-生物炭表面的活性吸附位点丰富, 吸附速率较快; 4 h之后为慢速吸附阶段, 吸附位点减少, 吸附速率逐渐变慢, 吸附逐渐达到饱和值.
|
图 6 MBC3和MBC9吸附动力学拟合 Fig. 6 Adsorption kinetic data and modeling for phosphate on MBC3 |
为了研究吸附机制, 使用常见的准一级动力学模型、准二级动力学模型和Elovich模型来对实验值进行拟合[11, 19, 20], 准一级动力学模型是理想模型, 假设吸附速率与被吸附物浓度呈线性关系, 准二级动力学方程假设吸附速率主要受化学吸附机制控制[21, 22], Elovich模型是考虑了吸附剂脱附因素的经验公式.模型方程分别为公式(1)~(3).
准一级动力学模型:
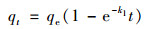
|
(1) |
准二级动力学模型:

|
(2) |
Elovich模型:

|
(3) |
式中, t表示吸附时间(h); qt和qe分别表示吸附剂在t时刻和吸附平衡时的吸附量(mg ·g-1); k1为准一级动力学模型平衡常数(h-1); k2为准二级动力学模型平衡常数[g ·(mg ·min)-1]; α是吸附速率(mg ·g-1); β是解吸常数(g ·mg-1).
通过3种吸附动力学方程拟合得到吸附动力学吸附参数及相关系数见表 3.从相关系数R2来看, MBC3和MBC9的准二级动力学模型的拟合度要优于准一级动力学模型和Elovich模型, 准二级动力学模型能更好地描述生物炭对磷的吸附, 这也与很多研究结果一致[11, 12, 23], 表明了磷酸根离子在MBC上的吸附过程受化学吸附机制控制[24, 25], 比如化学沉淀[26].
|
|
表 3 吸附动力学模型的吸附参数及相关系数 Table 3 Best-fit parameter values for models of kinetic data |
2.6 吸附等温线
吸附等温线是用来描述吸附平衡时溶液浓度与吸附量关系的曲线, 常见的吸附等温线方程有Langmuir、Freundlich和Redlich-Peterson[10, 27].
Langmuir方程:

|
(4) |
Freundlich方程:
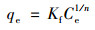
|
(5) |
Redlich-Peterson方程:

|
(6) |
Langmuir等温线方程假设吸附剂具有若干个相同的结合位点, 每个吸附物与每个结合位点的结合是相同的, 并且互不干扰[28], qmax表示最大吸附容量(mg ·g-1); Kl表示Langmuir等温线常数; Freundlich等温吸附方程为经验方程, 适用于异质表面吸附, 并能预测当液相中的离子浓度增加时, 吸附在固体表面的吸附质的增加情况[29]. Kf为与吸附容量和吸附强度有关的常数, 1/n为Freundlich常数, Kf、n值越大表明吸附剂的吸附性能越好; Redlich-Peterson等温线模型将Langmuir和Freundlich方程整合为一个方程, 当n=1和1/Kr=0时, 它分别等于Langmuir方程和Freundlich方程, 因此Redlich-Peterson拟合度最好. Kr和a为Redlich-Peterson等温线常数, g为Redlich-Peterson模型指数(通常0 < g < 1).
本实验测得MBC3和MBC9在不同初始浓度下的磷吸附量, 并通过方程(4)~(6)拟合实验数据得到的结果如图 7和表 4所示, 从吸附方程的相关系数R2来看, MBC3和MBC9的3个吸附等温线拟合度趋势相同(R2:Redlich-Peterson方程>Langmuir方程>Freundlich方程). Redlich-Peterson方程和Langmuir方程较好地描述了磷酸根在MBC3和MBC9上的吸附, g的值分别为0.884和0.916, 接近于1, 表明磷是被单层吸附在炭表面; MBC3和MBC9的Langmuir方程的理论最大吸附量分别为283.26 mg ·g-1和297.96 mg ·g-1, 与实验值283.10 mg ·g-1和296.23 mg ·g-1吻合较好. MBC9的Kf、n值均大于MBC3, 表明MBC9比MBC3具有更好的吸附性能.

|
图 7 MBC3和MBC9吸附等温线拟合 Fig. 7 Adsorption isotherm for phosphates on MBC3 |
|
|
表 4 等温线模型的吸附参数及相关系数 Table 4 Best-fit parameter values for models of isotherm data |
MgO-生物炭的磷吸附量比很多研究的磷吸附量都要高(见表 5), 说明MgO-生物炭可以有效去除水体中磷元素, 是一种非常有潜力的富营养水体污染吸附剂.
|
|
表 5 磷酸盐在各类吸附剂上的最大吸附量 Table 5 Maximum adsorption capacity of phosphate on various adsorbents |
3 结论
通过莲蓬壳混合纳米MgO快速热解制备了高吸附性能的MgO-生物炭吸附剂, MgO主要以薄片状和颗粒状的形态负载在炭表面, 增加了吸附活性位点. MgO-生物炭MBC3吸附量是未负载MgO生物炭MBC1的14倍, 热解通10% CO2载气, MBC9的吸附量进一步增加为MBC1的16倍.但孔隙率对吸附影响较小.准二级动力学方程能更好地描述吸附过程, 磷酸根在MgO-生物炭上的吸附是以化学吸附为主导. MgO-生物炭MBC3和MBC9的Langmuir理论最大吸附量为283.26 mg ·g-1和297.96 mg ·g-1. MgO-生物炭是一种高效的磷吸附剂, 具有改善水体富营养化问题的巨大潜力.
| [1] |
商东耀, 肖启涛, 胡正华, 等. 富营养化湖区CH4排放特征及其影响因素[J]. 环境科学, 2018, 39(11): 5227-5236. Shang D Y, Xiao Q T, Hu Z H, et al. CH4 emissions characteristics and its influencing factors in an eutrophic lake[J]. Environmental Science, 2018, 39(11): 5227-5236. |
| [2] |
王圣瑞, 倪兆奎, 席海燕. 我国湖泊富营养化治理历程及策略[J]. 环境保护, 2016, 44(18): 14-19. Wang S R, Ni Z K, Xi H Y. Management process and strategy of lake eutrophication in China[J]. Environmental Protection, 2016, 44(18): 14-19. |
| [3] |
吴锋, 战金艳, 邓祥征, 等. 中国湖泊富营养化影响因素研究——基于中国22个湖泊实证分析[J]. 生态环境学报, 2012, 21(1): 94-100. Wu F, Zhan J Y, Deng X Z., et al. Influencing factors of lake eutrophication in China——A case study in 22 lakes in China[J]. Ecology and Environmental Sciences, 2012, 21(1): 94-100. DOI:10.3969/j.issn.1674-5906.2012.01.018 |
| [4] | Conley D J, Paerl H W, Howarth R W, et al. Controlling eutrophication:nitrogen and phosphorus[J]. Science, 2009, 323(5917): 1014-1015. DOI:10.1126/science.1167755 |
| [5] |
周启星, 俞洁, 陈剑, 等. 某城市湖泊中磷的循环特征及富营养化发生潜势[J]. 环境科学, 2004, 25(5): 138-142. Zhou Q X, Yu J, Chen J, et al. Cycling characteristics of phosphorus in a urban lake and its eutrophication potentiality[J]. Environmental Science, 2004, 25(5): 138-142. DOI:10.3321/j.issn:0250-3301.2004.05.030 |
| [6] |
桂安, 毛献忠, 陶益, 等. 深圳荔枝湖富营养化成因和总磷模型分析[J]. 环境科学, 2008, 29(4): 874-878. Gui A, Mao X Z, Tao Y, et al. Pollutant loading analyses and TP model calculation for eutrophication in lichee lake in Shenzhen[J]. Environmental Science, 2008, 29(4): 874-878. DOI:10.3321/j.issn:0250-3301.2008.04.005 |
| [7] | Loganathan P, Vigneswaran S, Kandasamy J, et al. Removal and recovery of phosphate from water using sorption[J]. Critical Reviews in Environmental Science and Technology, 2014, 44(8): 847-907. DOI:10.1080/10643389.2012.741311 |
| [8] | Sizmur T, Fresno T, Akgül G, et al. Biochar modification to enhance sorption of inorganics from water[J]. Bioresource Technology, 2017, 246: 34-47. DOI:10.1016/j.biortech.2017.07.082 |
| [9] | Alvarez J, Lopez G, Amutio M, et al. Physical activation of rice husk pyrolysis char for the production of high surface area activated carbons[J]. Industrial & Engineering Chemistry Research, 2015, 54(29): 7241-7250. |
| [10] | Chen L, Chen X L, Zhou C H, et al. Environmental-friendly montmorillonite-biochar composites:Facile production and tunable adsorption-release of ammonium and phosphate[J]. Journal of Cleaner Production, 2017, 156: 648-659. DOI:10.1016/j.jclepro.2017.04.050 |
| [11] | Zhang M, Gao B, Yao Y, et al. Phosphate removal ability of biochar/MgAl-LDH ultra-fine composites prepared by liquid-phase deposition[J]. Chemosphere, 2013, 92(8): 1042-1047. DOI:10.1016/j.chemosphere.2013.02.050 |
| [12] | Jung K W, Lee S, Lee Y J. Synthesis of novel magnesium ferrite (MgFe2O4)/biochar magnetic composites and its adsorption behavior for phosphate in aqueous solutions[J]. Bioresource Technology, 2017, 245: 751-759. DOI:10.1016/j.biortech.2017.09.035 |
| [13] | Zhang M, Gao B, Yao Y, et al. Synthesis of porous MgO-biochar nanocomposites for removal of phosphate and nitrate from aqueous solutions[J]. Chemical Engineering Journal, 2012, 210: 26-32. DOI:10.1016/j.cej.2012.08.052 |
| [14] | Liu W J, Jiang H, Tian K, et al. Mesoporous carbon stabilized MgO nanoparticles synthesized by pyrolysis of MgCl2 preloaded waste biomass for highly efficient CO2 capture[J]. Environmental Science & Technology, 2013, 47(16): 9397-9403. |
| [15] | Zeng H Y, Cai L H, Cai X L, et al. Amino acid profiles and quality from lotus seed proteins[J]. Journal of the Science of Food and Agriculture, 2013, 93(5): 1070-1075. DOI:10.1002/jsfa.5848 |
| [16] | Wang X, Wang M J, Zhang X M, et al. Low-cost, green synthesis of highly porous carbons derived from lotus root shell as superior performance electrode materials in supercapacitor[J]. Journal of Energy Chemistry, 2016, 25(1): 26-34. DOI:10.1016/j.jechem.2015.10.012 |
| [17] | Wu X X, Zhang C Y, Tian Z W, et al. Large-surface-area carbons derived from lotus stem waste for efficient CO2 capture[J]. New Carbon Materials, 2018, 33(3): 252-261. DOI:10.1016/S1872-5805(18)60338-5 |
| [18] | Micháleková-Richveisová B, Frišták V, Pipíška M, et al. Iron-impregnated biochars as effective phosphate sorption materials[J]. Environmental Science and Pollution Research, 2017, 24(1): 463-475. DOI:10.1007/s11356-016-7820-9 |
| [19] | Liu S B, Tan X F, Liu Y G, et al. Production of biochars from Ca impregnated ramie biomass (Boehmeria nivea (L.) Gaud.) and their phosphate removal potential[J]. RSC Advances, 2016, 6(7): 5871-5880. DOI:10.1039/C5RA22142K |
| [20] | Gerente C, Lee V K C, Le Cloirec P, et al. Application of chitosan for the removal of metals from wastewaters by adsorption-mechanisms and models review[J]. Critical Reviews in Environmental Science and Technology, 2007, 37(1): 41-127. DOI:10.1080/10643380600729089 |
| [21] |
易蔓, 李婷婷, 李海红, 等. Ca/Mg负载改性沼渣生物炭对水中磷的吸附特性[J]. 环境科学, 2019, 40(3): 1318-1327. Yi M, Li T T, Li H H, et al. Characteristics of phosphorus adsorption in aqueous solution by Ca/Mg-loaded biogas residue biochar[J]. Environmental Science, 2019, 40(3): 1318-1327. |
| [22] |
吴露, 刘锋, 龙睿, 等. 3种吸附剂对污水磷污染去除性能与机制比较[J]. 环境科学, 2019, 40(2): 677-684. Wu L, Liu F, Long R, et al. Removal performance and mechanism for treating phosphorus in agricultural wastewater by three adsorbents[J]. Environmental Science, 2019, 40(2): 677-684. |
| [23] | Cai R, Wang X, Ji X H, et al. Phosphate reclaim from simulated and real eutrophic water by magnetic biochar derived from water hyacinth[J]. Journal of Environmental Management, 2017, 187: 212-219. |
| [24] | Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+ sorption mechanisms by sludge-derived biochar[J]. Water Research, 2012, 46(3): 854-862. DOI:10.1016/j.watres.2011.11.058 |
| [25] | Mohan D, Pittman C U Jr, Bricka M, et al. Sorption of arsenic, cadmium, and lead by chars produced from fast pyrolysis of wood and bark during bio-oil production[J]. Journal of Colloid and Interface Science, 2007, 310(1): 57-73. DOI:10.1016/j.jcis.2007.01.020 |
| [26] | Li R H, Wang J J, Zhou B Y, et al. Recovery of phosphate from aqueous solution by magnesium oxide decorated magnetic biochar and its potential as phosphate-based fertilizer substitute[J]. Bioresource Technology, 2016, 215: 209-214. DOI:10.1016/j.biortech.2016.02.125 |
| [27] | Rangabhashiyam S, Anu N, Giri Nandagopal M S, et al. Relevance of isotherm models in biosorption of pollutants by agricultural byproducts[J]. Journal of Environmental Chemical Engineering, 2014, 2(1): 398-414. DOI:10.1016/j.jece.2014.01.014 |
| [28] | Saleh T A. Isotherm, kinetic, and thermodynamic studies on Hg(Ⅱ) adsorption from aqueous solution by silica-multiwall carbon nanotubes[J]. Environmental Science and Pollution Research, 2015, 22(21): 16721-16731. DOI:10.1007/s11356-015-4866-z |
| [29] | Vassileva P S, Radoykova T H, Detcheva A K, et al. Adsorption of Ag+ ions on hydrolyzed lignocellulosic materials based on willow, paulownia, wheat straw and maize stalks[J]. International Journal of Environmental Science and Technology, 2016, 13(5): 1319-1328. DOI:10.1007/s13762-016-0970-y |
| [30] | Jung K W, Hwang M J, Jeong T U, et al. A novel approach for preparation of modified-biochar derived from marine macroalgae:dual purpose electro-modification for improvement of surface area and metal impregnation[J]. Bioresource Technology, 2015, 191: 342-345. DOI:10.1016/j.biortech.2015.05.052 |
| [31] | Jung K W, Kim K, Jeong T U, et al. Influence of pyrolysis temperature on characteristics and phosphate adsorption capability of biochar derived from waste-marine macroalgae (Undaria pinnatifida roots)[J]. Bioresource Technology, 2016, 200: 1024-1028. DOI:10.1016/j.biortech.2015.10.016 |
| [32] |
赵钰颖, 林建伟, 张宏华, 等. 钙预处理对磁性锆铁改性膨润土吸附水中磷酸盐的影响[J]. 环境科学, 2019, 40(2): 658-668. Zhao Y Y, Lin J W, Zhang H H, et al. Influence of calcium ion pre-treatment on phosphate adsorption onto magnetic zirconium/iron-modified bentonite[J]. Environmental Science, 2019, 40(2): 658-668. |
 2019, Vol. 40
2019, Vol. 40


