2. 首都师范大学资源环境与旅游学院, 北京 100048
2. College of Resource, Environment and Tourism, Capital Normal University, Beijing 100048, China
随着我国经济的快速发展, 大气污染问题日趋严重.生物质燃烧过程会排放多种污染物[1], 如硝基酚类化合物[2]、芳香醛以及芳香酸[3, 4]等, 是大气气溶胶的重要一次人为源, 严重危害空气质量和生态环境.
硝基酚类物质是苯环上至少连有一个硝基和羟基官能团的芳香族化合物, 具有一定的毒性、致突变和致癌性, 少量的摄入会对植物[5]、水生生物[6]以及人体健康[7]产生危害, 已被我国列为严格控制的有毒物质.作为棕碳的成分之一, 硝基酚类化合物对300~400 nm的近紫外光和可见光具有明显的吸收效应, 进而影响大气辐射平衡、大气光化学、区域大气质量和全球气候变化[8~10].大气中硝基酚类化合物的一次排放源主要包括生物质燃烧[11]、燃煤[12]以及机动车尾气[13]等.有研究表明, 农业生产活动中杀虫剂和除草剂的使用也会排放少量的硝基酚类化合物, 但对环境中浓度的贡献很小[7].此外, 活泼的挥发性有机前体物(如苯和苯酚等)会与氧化剂反应生成硝基酚类化合物.气相体系中白天由·OH引发, 继而和NOx或NO2反应生成硝基酚类化合物[14]; 夜间由NO3 ·引发, 和NOx或NO2发生硝化反应生成硝基酚类物质[15].气相色谱-质谱联用(GC-MS)技术可用于定性定量分析大气中硝基酚类化合物, Morville等[13]使用GC-MS检测了大气中20种苯酚及硝基苯酚类化合物, 发现N-(t-butyldimethylsilyl)-N-methyltrifluoroacetamide (MTBSTFA)衍生化后的碎片离子中[M-57]+的信号响应最强, 可作为特征离子; Cecinato等[16]使用GC-MS分析了罗马地区气相及颗粒相中的6种单硝基苯酚类化合物, 4-硝基苯酚和2-硝基苯酚在两相中浓度最高.
芳香醛和芳香酸是大气中的痕量有机物[17], Wang等[18]使用GC-MS检测到南京地区冬季PM2.5中的香草酸和丁香酸总浓度为8.36 ng·m-3, 高于夏季的1.43 ng·m-3, 并且表现出明显的夜间浓度高于日间的趋势.大气中的芳香醛和芳香酸主要来自于木质素的降解[3], 如松树、草、硬木以及软木的燃烧[19, 20].有研究表明褐煤的燃烧也会排放一定量的香草酸、水杨酸、丁香酸以及香草醛[3].
除自身造成的污染外, 芳香族化合物还会与氧化剂反应, 生成更具有污染性的物质[21~23].基于现今的研究结果发现, 定量分析主要集中在硝基酚类化合物, 对芳香酸和芳香醛的研究主要针对其来源, 定量研究较少.因此, 本研究使用GC-MS对石家庄地区PM2.5中的芳香族化合物(硝基酚类、芳香醛类及芳香酸类)进行了定性定量检测, 通过8种物质的浓度水平、昼夜变化特征进行污染情况分析, 结合与左旋葡聚糖的相关性以及污染时段的后向轨迹对芳香族化合物的来源进行分析, 以期为获取石家庄地区芳香族化合物的污染特征及来源情况提供参考依据.
1 材料与方法 1.1 样品采集使用天虹中流量(TH-150, 武汉市天虹仪表有限责任公司, 中国)采样器于2016年9月18日至10月17日于石家庄地区进行为期30 d的昼夜采样, 采集时间分别为08:00~20:00(日)和20:00~次日08:00(夜).采样流量为100 L ·min-1.采样使用石英纤维滤膜, 其有机物本底含量低、热稳定性强, 对大气有机物分析造成的影响较小.采样前将滤膜放在马弗炉(KSL-1200X, 合肥科晶材料技术有限公司, 中国)中灼烧3 h(500℃), 除去可能的有机杂质.采样前后分别置于恒温恒湿箱(AT-330, 无锡索亚特, 中国)中(温度:25℃, 湿度50%)干燥24 h后称重, -4℃冷冻保存备用.
采样地点位于石家庄市中心广场(E114°28′, N38°04′), 海拔15 m, 周围人口密集, 交通状况良好, 大气环境受人类活动影响较大, 为典型的城市地区.
1.2 分析方法切取1/4采样膜剪碎放入10 mL玻璃瓶中, 加入内标物后分别使用二氯甲烷、正己烷混合液(1 :1, 体积比)和二氯甲烷、甲醇混合液(1 :1, 体积比)各超声提取两次(40 Hz, 15 min), 滤液转移至鸡心瓶.使用旋转蒸发仪旋蒸至1 mL左右, 转移至1.5 mL的反应瓶中氮吹至干燥.加入50 μL 99%BSTFA-1%TMCS和10 μL吡啶, 置于烘箱(70℃)中衍生化反应3 h.冷却至室温后定容到400 μL.
使用GC-MS联用仪(TQ8040, 岛津, 日本)进行样品分析.气相色谱柱型号为HP-5MS(30 m, 0.25 mm, 0.25 μm).初始温度为50℃, 保持2 min, 以5℃ ·min-1的速率升温至290℃, 保持20 min.采用不分流方式进样, 进样量为1 μL.质谱离子源为EI源(70 eV), 采用全扫模式(50~550 u).设置滤膜空白和试剂空白的对比分析, 扣除背景干扰.二氯甲烷、正己烷、甲醇试剂的纯度均超过99.8%.
表 1为目标化合物的相关信息, 包括化学式、结构式、衍生物相对分子质量及衍生物的碎片离子, 其中带有下划线部分为定量离子.对提取过程的回收率及仪器分析方法性能(保留时间、检出限、线性范围及其标准曲线拟合系数R2)进行测定, 结果列于表 2.定量方式采用标准曲线法, 浓度梯度分别为0.2、0.4、0.6、0.8、1.0、1.5和2.0 mg ·L-1, 各物质的线性均高于0.99.通过内标物的回收率进行校正, 尽可能地减少人为操作及仪器分析带来的误差.
|
|
表 1 目标化合物的化学式、结构式、衍生物相对分子质量和衍生物碎片离子 Table 1 Chemical formula, structure, derivative relative molecular weight, and derivative fragment ions of target compounds |
|
|
表 2 实验方法评估及仪器性能分析1) Table 2 Experimental method of evaluation and instrument performance analysis |
2 结果与讨论 2.1 浓度水平
2016年秋季石家庄地区8种芳香族化合物和左旋葡聚糖的平均质量浓度见表 3.可以看出, 芳香族化合物的总浓度(33.5 ng ·m-3)明显低于左旋葡聚糖(487 ng ·m-3), 这是由于左旋葡聚糖为纤维素热解产物, 芳香族化合物为木质素热解产物[19], 生物质燃料中纤维素占总量的40%~50%, 半纤维素占20%~40%, 木质素仅占10%~25%[24].
|
|
表 3 石家庄地区芳香族化合物的平均质量浓度水平/ng ·m-3 Table 3 Average mass concentration of aromatic compounds in Shijiazhuang/ng ·m-3 |
将8种物质分为硝基酚类化合物(4-硝基苯酚、4-硝基儿茶酚、3-甲基-6-硝基儿茶酚)、芳香醛类(对羟基苯甲醛、香草醛)和芳香酸类(4-羟基苯甲酸、香草酸、丁香酸).可以看出, 硝基酚类化合物总平均浓度最高, 为20.4 ng ·m-3, 其次为芳香酸类和芳香醛类, 分别为9.94 ng ·m-3和3.14 ng ·m-3, 说明大气中硝基酚类化合物的污染程度高于芳香酸和芳香醛, 与其复杂的来源有关.生物质燃烧、燃煤、机动车尾气等重要的人为活动都是硝基酚类化合物的一次来源[11~13], 大气中活泼的挥发性有机物(如苯、苯酚等)与氧化剂反应是其重要的二次来源[14, 15], 而芳香醛和芳香酸作为典型的木质素降解产物[3, 4], 来源相对单一, 浓度偏低.
4-硝基儿茶酚[(9.57±14.2)ng ·m-3]在硝基酚类化合物中浓度最高, 4-硝基苯酚[(7.76±9.09)ng ·m-3)]次之, 3-甲基-6-硝基儿茶酚[(3.02±4.79)ng ·m-3]最低, 明显低于4-硝基儿茶酚, 说明在同类别的硝基儿茶酚中4-硝基儿茶酚的污染最为严重, 这与Wang等[25]的研究结果一致.芳香酸类化合物中4-羟基苯甲酸[(6.98±7.17)ng ·m-3]的浓度最高, 香草酸[(1.57±1.55)ng ·m-3]次之, 丁香酸[(1.39±1.76)ng ·m-3]最低.对羟基苯甲醛的浓度高于香草醛, 分别为(2.02±1.94)ng ·m-3和(1.12±1.03)ng ·m-3.
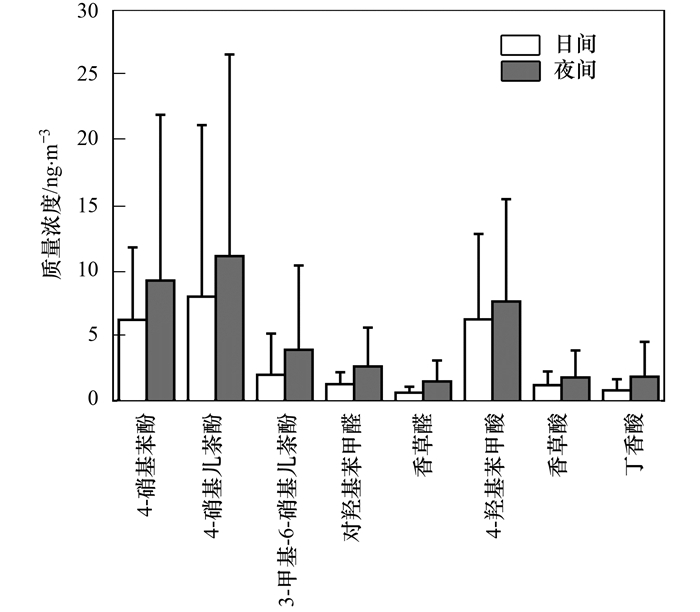
2.2 昼夜变化特征对比石家庄地区的昼夜浓度可以看出(图 1), 8种化合物夜间浓度高于日间. 4-硝基苯酚、4-硝基儿茶酚和3-甲基-6-硝基儿茶酚的夜间浓度分别是日间的1.48、1.39和1.93倍; 4-羟基苯甲酸、香草酸和丁香酸分别是1.22、1.45和2.18倍; 对羟基苯甲醛和香草醛分别是2.01和2.24倍, 为三类化合物中相差最多的物质.夜间浓度升高主要受边界层高度的影响, 边界层高度降低导致污染物累积, 并且夜间的静稳天气条件不利于物质的扩散.秋季昼夜温差较大, 夜间温度的降低导致更多污染物分配在颗粒相中, 从而表现出浓度抬升的趋势.
|
图 1 石家庄地区采样期间8种芳香族化合物的昼夜浓度对比 Fig. 1 Diurnal concentrations of eight aromatic compounds during sampling in Shijiazhuang |
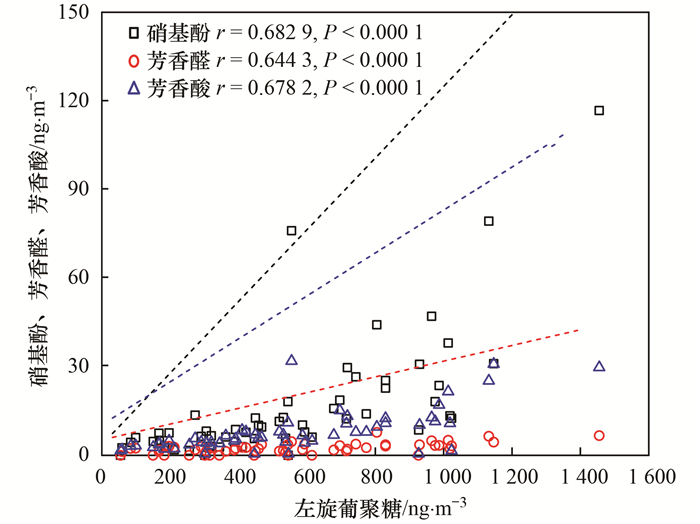
左旋葡聚糖在大气中具有良好的光化学稳定性, 被视为生物质燃烧示踪物[26].将硝基酚类、芳香醛类和芳香酸类化合物与左旋葡聚糖进行相关性分析, 探讨生物质燃烧活动对其大气浓度水平的影响.通过图 2可以看出, 3类化合物与左旋葡聚糖的相关性P值均小于0.000 1, 表明二者存在显著性相关关系.硝基酚类、芳香醛类和芳香酸类化合物与左旋葡聚糖的相关系数(r)分别为0.682 9、0.644 3和0.678 2, 呈现显著的正相关关系, 表明生物质燃烧作为3类物质的重要一次来源, 直接影响其在大气中的浓度水平.因此, 减少生物质燃烧活动可以有效控制芳香族化合物以及其他污染物的排放, 不仅改善当地的空气质量, 也有利于受区域传输影响的周边地区的大气环境.
|
图 2 石家庄地区3类芳香族化合物与左旋葡聚糖的相关性分析 Fig. 2 Correlation analysis of three kinds of aromatic compounds with levoglucosan in Shijiazhuang |
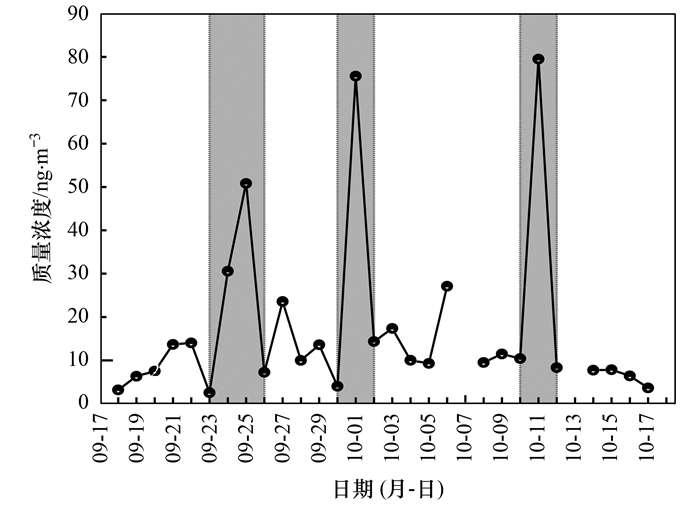
结合8种芳香族化合物总浓度的日变化趋势(图 3)和后向轨迹模型(图 4), 对采样期间芳香族化合物的污染来源进行分析.通过图 3可以看出, 采样期间出现3次严重的污染时段, 分别为09-24、09-25、10-01和10-11, 8种芳香族化合物总质量浓度分别为30.6、50.8、75.6和79.5 ng ·m-3.对污染前、污染时和污染后做同等时长的后向轨迹模型分析, 可以看出, 第一次污染时段[09-24~09-25, 图 4(b)]气团主要来自采样点南部方向的低空传输, 途经农业城市山东聊城, 污染前[09-22~09-23, 图 4(a)]和污染后[09-26~09-27, 图 4(c)]的气团分别来自西部和西北部地区的远距离传输, 以高空传输为主.受区域传输影响, 来自南部的低空气团在途经农业地区后携带生物质燃烧气溶胶到达石家庄, 加剧了芳香族化合物的污染.第二次污染时段[10-01, 图 4(e)]气团主要来自南部的低空近距离传输, 途经工业城市邢台, 污染前[09-30, 图 4(d)]同样是南部低空近距离传输气团, 因此推测该方向气团不会影响石家庄地区的芳香族化合物浓度水平, 本次污染为本地排放引起.第三次污染时段[10-11, 图 4(h)]有大量途经农业城市沧州的低空气团, 污染前[10-10, 图 4(g)]气团主要来自西南方向, 途经太原等城市, 推测本次污染过程依然为区域传输的影响.因此, 受区域传输和本地排放的综合影响, 秋季石家庄芳香族化合物污染呈周期性变化.
|
图 3 石家庄地区8种芳香族化合物总浓度日变化趋势(2016) Fig. 3 Diurnal variation of total concentration of 8 aromatic compounds in Shijiazhuang (2016) |

|
图 4 3个污染时段的后向轨迹模型 Fig. 4 Backward trajectory model of three pollution periods |
(1) 8种芳香族化合物的总浓度水平明显低于左旋葡聚糖, 其中硝基酚类化合物浓度最高, 芳香酸类次之, 芳香醛类最低.
(2) 受夜间边界层高度降低、静稳天气条件以及温度的影响, 8种化合物呈现夜间浓度高于日间的趋势.
(3) 硝基酚、芳香醛、芳香酸类化合物与左旋葡聚糖的相关性分析表明, 生物质燃烧直接影响其在大气中的浓度水平, 需要有效控制本地及周边地区的生物质燃烧活动.
(4) 结合芳香族化合物总浓度的日变化趋势和后向轨迹模型分析发现, 石家庄地区秋季芳香族化合物的污染程度受区域传输和本地排放的综合影响.
| [1] |
田贺忠, 赵丹, 王艳. 中国生物质燃烧大气污染物排放清单[J]. 环境科学学报, 2011, 31(2): 349-357. Tian H Z, Zhao D, Wang Y. Emission inventories of atmospheric pollutants discharged from biomass burning in China[J]. Acta Scientiae Circumstantiae, 2011, 31(2): 349-357. |
| [2] | Wang X F, Gu R R, Wang L W, et al. Emissions of fine particulate nitrated phenols from the burning of five common types of biomass[J]. Environmental Pollution, 2017, 230: 405-412. DOI:10.1016/j.envpol.2017.06.072 |
| [3] | Fabbri D, Torri C, Simoneit B R T, et al. Levoglucosan and other cellulose and lignin markers in emissions from burning of Miocene lignites[J]. Atmospheric Environment, 2009, 43(14): 2286-2295. DOI:10.1016/j.atmosenv.2009.01.030 |
| [4] | Kawamura K, Izawa Y, Mochida M, et al. Ice core records of biomass burning tracers (levoglucosan and dehydroabietic, vanillic and p-hydroxybenzoic acids) and total organic carbon for past 300 years in the Kamchatka Peninsula, Northeast Asia[J]. Geochimica et Cosmochimica Acta, 2012, 99: 317-329. DOI:10.1016/j.gca.2012.08.006 |
| [5] | Hinkcel M, Reischl A, Schramm K W, et al. Concentration levels of nitrated phenols in conifer needles[J]. Chemosphere, 1989, 18(11-12): 2433-2439. |
| [6] |
陆光华, 袁星, 赵元慧. 苯酚、苯胺及其衍生物对斜生栅列藻的急性毒性及QSAR研究[J]. 环境化学, 2000, 19(3): 225-229. Lu G H, Yuan X, Zhao Y H. The acute toxicity of aniline, phenol derivatives to the scenedesmus obliquus and qsar study[J]. Environmental Chemistry, 2000, 19(3): 225-229. DOI:10.3321/j.issn:0254-6108.2000.03.006 |
| [7] | Harrison M A J, Barra S, Borghesi D, et al. Nitrated phenols in the atmosphere:a review[J]. Atmospheric Environment, 2005, 39(2): 231-248. DOI:10.1016/j.atmosenv.2004.09.044 |
| [8] | Lin P, Bluvshtein N, Rudich Y, et al. Molecular chemistry of atmospheric brown carbon inferred from a nationwide biomass burning event[J]. Environmental Science & Technology, 2017, 51(20): 11561-11570. |
| [9] | Teich M, van Pinxteren D, Wang M, et al. Contributions of nitrated aromatic compounds to the light absorption of water-soluble and particulate brown carbon in different atmospheric environments in Germany and China[J]. Atmospheric Chemistry and Physics, 2017, 17(3): 1653-1672. DOI:10.5194/acp-17-1653-2017 |
| [10] | Chen Y F, Ge X L, Chen H, et al. Seasonal light absorption properties of water-soluble brown carbon in atmospheric fine particles in Nanjing, China[J]. Atmospheric Environment, 2018, 187: 230-240. DOI:10.1016/j.atmosenv.2018.06.002 |
| [11] | Claeys M, Vermeylen R, Yasmeen F, et al. Chemical characterisation of humic-like substances from urban, rural and tropical biomass burning environments using liquid chromatography with UV/vis photodiode array detection and electrospray ionisation mass spectrometry[J]. Environmental Chemistry, 2012, 9(3): 273-284. |
| [12] | Lüttke J, Scheer V, Levsen K, et al. Occurrence and formation of nitrated phenols in and out of cloud[J]. Atmospheric Environment, 1997, 31(16): 2637-2648. DOI:10.1016/S1352-2310(96)00229-4 |
| [13] | Morville S, Scheyer A, Mirabel P, et al. A multiresidue method for the analysis of phenols and nitrophenols in the atmosphere[J]. Journal of Environmental Monitoring, 2004, 6(12): 963-966. DOI:10.1039/b408756a |
| [14] | Xu C, Wang L M. Atmospheric oxidation mechanism of phenol initiated by OH radical[J]. The Journal of Physical Chemistry A, 2013, 117(11): 2358-2364. DOI:10.1021/jp308856b |
| [15] | Bolzacchini E, Bruschi M, Hjorth J, et al. Gas-phase reaction of phenol with NO3[J]. Environmental Science & Technology, 2001, 35(9): 1791-1797. |
| [16] | Cecinato A, Di Palo V, Pomata D, et al. Measurement of phase-distributed nitrophenols in Rome ambient air[J]. Chemosphere, 2005, 59(5): 679-683. DOI:10.1016/j.chemosphere.2004.10.045 |
| [17] | Rousová J, Chintapalli M R, Lindahl A, et al. Simultaneous determination of trace concentrations of aldehydes and carboxylic acids in particulate matter[J]. Journal of Chromatography A, 2018, 1544: 49-61. DOI:10.1016/j.chroma.2018.02.026 |
| [18] | Wang G H, Kawamura K. Molecular characteristics of urban organic aerosols from Nanjing:a case study of a mega-city in China[J]. Environmental Science & Technology, 2005, 39(19): 7430-7438. |
| [19] | Simoneit B R T. Biomass burning-a review of organic tracers for smoke from incomplete combustion[J]. Applied Geochemistry, 2002, 17(3): 129-162. |
| [20] | Oros D R, Abas M R B, Omar N Y M J, et al. Identification and emission factors of molecular tracers in organic aerosols from biomass burning:part 3. Grasses[J]. Applied Geochemistry, 2006, 21(6): 919-940. DOI:10.1016/j.apgeochem.2006.01.008 |
| [21] | Yee L D, Kautzman K E, Loza C L, et al. Secondary organic aerosol formation from biomass burning intermediates:phenol and methoxyphenols[J]. Atmospheric Chemistry and Physics, 2013, 13(16): 8019-8043. DOI:10.5194/acp-13-8019-2013 |
| [22] | Santos P S M, Duarte A C. Fenton-like oxidation of small aromatic acids from biomass burning in water and in the absence of light:implications for atmospheric chemistry[J]. Chemosphere, 2015, 119: 786-793. DOI:10.1016/j.chemosphere.2014.08.024 |
| [23] | Santos G T A D, Santos P S M, Duarte A C. Vanillic and syringic acids from biomass burning:behaviour during Fenton-like oxidation in atmospheric aqueous phase and in the absence of light[J]. Journal of Hazardous Materials, 2016, 313: 201-208. DOI:10.1016/j.jhazmat.2016.04.006 |
| [24] | Scurlock J M O, Dayton D C, Hames B. Bamboo:an overlooked biomass resource?[J]. Biomass and Bioenergy, 2000, 19(4): 229-244. DOI:10.1016/S0961-9534(00)00038-6 |
| [25] | Wang L W, Wang X F, Gu R R, et al. Observations of fine particulate nitrated phenols in four sites in Northern China:concentrations, source apportionment, and secondary formation[J]. Atmospheric Chemistry and Physics, 2018, 18(6): 4349-4359. DOI:10.5194/acp-18-4349-2018 |
| [26] | Caseiro A, Marr I L, Claeys M, et al. Determination of saccharides in atmospheric aerosol using anion-exchange high-performance liquid chromatography and pulsed-amperometric detection[J]. Journal of Chromatography A, 2007, 1171(1-2): 37-45. DOI:10.1016/j.chroma.2007.09.038 |
 2019, Vol. 40
2019, Vol. 40



