2. 农业部西北植物营养与农业环境重点实验室, 杨凌 712100
2. Key Laboratory of Plant Nutrition and Agro-environment in Northwest China, Ministry of Agriculture, Yangling 712100, China
重金属复合污染是土壤及水环境污染的主要形式之一[1, 2], 共存的不同重金属离子之间具有相互作用, 从而表现出与单一离子不同的吸附特性[3, 4].因此, 研究重金属复合污染对于保护环境和人体健康具有重要意义.
共存重金属离子之间交互作用的研究已有较多报道, 共存的竞争性离子是影响吸附的重要因子, 黏土矿物对多种重金属离子共存时的吸附具有选择性, 这与重金属离子本身的性质(电荷、离子半径)和矿物种类有关[5], 当多种金属阳离子共存时它们将竞争矿物表面的吸附点位, 导致吸附量下降.同时温度、pH和背景离子等环境因素也不同程度地影响着多重金属离子共同吸附时的竞争效应[6~8].
利用表面活性剂改性黏土使其成为有机黏土矿物, 增强其对污染物的吸附固定能力的研究已有报道, 两性修饰土具有对重金属和有机物良好的同时吸附能力[9].两性表面修饰剂BS- 12修饰塿土后对镉离子、苯酚的吸附分别能达到未修饰土样的1.3~1.8倍和4.0~8.3倍[10], 而采用两性复配修饰能够进一步增强对污染物的吸附[11].李婷[12]的研究发现, 两性修饰剂的碳链长度在一定程度上影响修饰土对金属离子的吸附, 对Cd(Ⅱ)的吸附量在高修饰比例下与两性修饰剂的碳链长度呈正相关.对于有机物和重金属的同时吸附, Ma等[13]的实验结果表明, 苯酚和Cu2+对彼此在阳离子和两性修饰土上的吸附不产生影响.而张斌[14]的研究得出苯酚的存在对Cd(Ⅱ)在两性修饰土上的吸附有一定的阻碍作用.当前的研究主要针对单一重金属或有机污染物, 由于两性修饰改变了黏土矿物的表面特征, 使黏土矿物表面的亲水负电荷表面转变为疏水、正电荷和负电荷共存表面, 进而也改变对有机、重金属污染物的吸附机制[15, 16], 这种吸附机制的变化对于多种重金属复合污染体系中, 不同重金属之间的吸附及其交互作用有何影响, 相关研究目前还未见报道.
本文以批处理法研究了BS- 12两性修饰膨润土在单一及Cu-Pb复合体系中对Cu2+和Pb2+的吸附特征和差异, 同时考察了温度、修饰比例、pH、离子强度对重金属吸附的影响, 并探讨了两性修饰膨润土中Cu2+和Pb2+吸附的相互作用机制, 以期为两性修饰黏土矿物的应用提供理论依据.
1 材料与方法 1.1 实验材料供试黏土矿物采用钠基膨润土(购自河南信阳同创膨润土公司), 经水洗提纯、干燥、研磨、过60目筛后备用.
两性修饰剂采用十二烷基二甲基甜菜碱(BS- 12, 缩写为BS, AR, 天津兴光助剂厂).
重金属污染物Cu2+和Pb2+, 分别以Cu(NO3)2 ·3H2O(AR, 天津市大茂化学试剂厂)和Pb(NO3)2(AR, 天津市恒兴化学试剂制造有限公司)配制.
1.2 修饰土样的制备及表征采用湿法[17]制备BS- 12两性修饰膨润土, 于60℃下烘干、研磨、过60目筛备用.表面修饰剂的用量通过以下公式计算:

|
(1) |
式中, W为称取表面修饰剂的质量, g; m为土样质量, g; CEC为修饰土样的阳离子交换量, mmol ·kg-1; M为相应表面修饰剂的摩尔质量, g ·mol-1; R为表面修饰剂的修饰比例; b为修饰剂产品的含量(质量分数).
采用Nicolet5DX型傅立叶变换红外光谱仪(FTIR)对CK和150BS- 12吸附单一Cu2+和Pb2+前后的有机官能团进行鉴定.
1.3 实验设计BS- 12修饰比例按膨润土CEC设50%、100%和150% 3个比例(分别以50BS- 12、100BS- 12和150BS- 12表示), 以未修饰原土(CK)为对照.以下实验每个实验处理均设置3个重复.
单一Cu2+、Pb2+溶液浓度均设为5、10、20、50、100、200、300、400和500 mg ·L-1这9个浓度梯度, Cu-Pb复合溶液的浓度设为(5+5)、(10+10)、(20+20)、(50+50)、(100+100)、(200+200)、(300+300)、(400+400)和(500+500) mg ·L-1这9个浓度梯度, 此时实验温度设为20℃, pH值设为5, 以0.1 mol ·L-1KNO3溶液作为背景离子强度.
温度对吸附的影响, 供试土样选用150BS- 12, 以CK为对照, 单一Cu2+、Pb2+以及Cu-Pb复合溶液的浓度分别为500 mg ·L-1和(500+500) mg ·L-1, 实验温度设20℃和40℃, 此时溶液初始pH值设为5, 背景离子强度为0.1 mol ·L-1 KNO3溶液.
pH对吸附的影响, 供试土样选用150BS- 12, 以CK为对照, 单一Cu2+、Pb2+以及Cu-Pb复合溶液的浓度分别为500 mg ·L-1和(500+500) mg ·L-1, 溶液初始pH值均设为2、3、4和5, 温度为30℃, 背景离子强度为0.1 mol ·L-1 KNO3溶液.
背景离子强度对吸附的影响, 供试土样选用150BS- 12, 以CK为对照, 背景离子强度设为0.001、0.01、0.1和0.5 mol ·L-1 KNO3溶液, 温度为30℃, 单一Cu2+、Pb2+以及Cu-Pb复合溶液的浓度分别为500 mg ·L-1和(500+500) mg ·L-1, pH值均设为5.
1.4 实验方法平衡吸附实验以批处理法(Batch)进行.分别称取0.2000 g供试土样于9只50 mL具塞塑料离心管中, 并用移液管分别加入20.00 mL上述不同浓度梯度的Cu2+和Pb2+溶液, 恒温振荡24 h, 4800 r ·min-1离心10 min, 取上清液, 测定重金属离子浓度, 差减法确定供试土样中Cu2+和Pb2+的吸附量.
Cu2+和Pb2+的测定采用HITACHIZ-5000型原子吸收分光光度计, 以火焰法测定, Zeeman效应校正背景吸收, 以上测定均插入标准溶液进行分析质量控制.
1.5 数据处理Cu2+和Pb2+的平衡吸附量按式(2)计算:

|
(2) |
式中, c0为溶液中Cu2+和Pb2+的初始浓度(mg ·L-1); ce为溶液的平衡浓度(mg ·L-1); V为加入溶液的体积(mL); m为土样的质量(g); Qe为Cu2+和Pb2+在土样上的平衡吸附量(mg ·g-1).
Cu2+和Pb2+的吸附等温线的拟合采用Langmuir和Freundlich模型.
Langmuir等温吸附方程为:
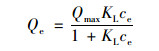
|
(3) |
式中, Qmax(mg ·g-1)为最大吸附容量, KL为吸附平衡常数, 可以衡量吸附亲和力的大小;
Freundlich等温吸附方程为:
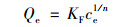
|
(4) |
式中, KF为与吸附容量有关的参数; 1/n代表吸附强度, 表示吸附剂对吸附质束缚力的强弱.
模型拟合及绘图均采用Origin 9软件.
2 结果与分析 2.1 BS- 12修饰土样的表征有研究表明, 膨润土经BS- 12修饰后其结构及表面特性发生变化[18].电镜显示BS- 12修饰土相对CK其层间空隙明显增大且其表面结构由平坦规整变为卷曲松散, 凹凸不平.且随BS- 12修饰比例的增加, BS- 12修饰膨润土的有机碳含量增加, CEC下降, 层间距不断增大, 比表面积的减小, 证实BS- 12通过插层的方式进入到膨润土层间.
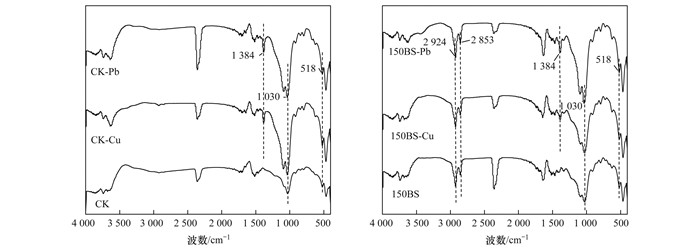
图 1为CK及150BS- 12吸附Cu2+和Pb2+前后的红外光谱图.从中可知, 与CK相比, 150BS- 12在2 924 cm-1和2 853 cm-1处出现了—CH2—的反对称和对称振动吸收峰[19], 说明长碳链的BS- 12修饰到膨润土上. 1 030 cm-1和518 cm-1对应膨润土中Si—O伸缩振动和Al—O—Si弯曲振动吸收峰[20], CK和150BS- 12吸附金属离子前后此处吸附峰的位置无明显变化, 说明BS- 12的修饰和金属离子的吸附并没有改变膨润土的层状硅酸盐结构.而CK和150BS- 12吸附Cu2+和Pb2+后, 均在1 384 cm-1处出现了新的吸收峰, 这可能是由于金属离子与膨润土上硅(铝)羟基以及BS- 12的羧基基团发生反应生成了新的化学键所致.
|
图 1 CK和150BS- 12吸附Cu2+和Pb2+前后的FTIR图谱 Fig. 1 FTIR spectra of CK and 150BS- 12 before and after adsorption of Cu2+ and Pb2+ |
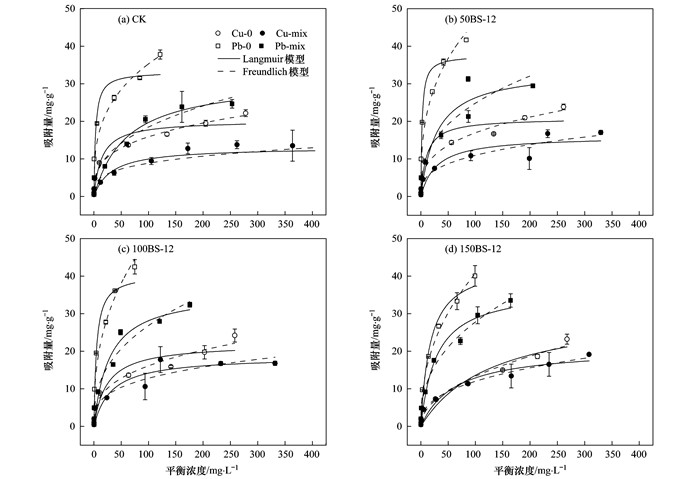
温度为20℃时, BS- 12修饰膨润土对Cu2+和Pb2+的吸附等温线见图 2.从中可知, 各供试土样对Cu2+和Pb2+的吸附等温线均随着平衡浓度的增大而增加, 且吸附等温线呈L型, 在实验浓度范围内Cu2+和Pb2+的吸附量均未达到最大值.
|
Cu-0、Pb-0表示单组分体系中金属离子的吸附量; Cu-mix、Pb-mix表示复合体系中的吸附量, 下同 图 2 BS- 12修饰土对Cu2+和Pb2+的吸附等温线 Fig. 2 Adsorption isotherms of Cu2+ and Pb2+ on BS- 12-modified bentonite |
单一体系中各修饰土样对Cu2+和Pb2+的Langmuir模型最大吸附量Qmax值较CK均有提高, 并随修饰比例的增加呈150BS- 12>100BS- 12>50BS- 12>CK的大小顺序, 显示出不同修饰比例的BS- 12修饰膨润土对于不同的单一金属离子吸附的影响具有一致性, 这和笔者前期BS- 12修饰膨润土吸附Cd2+[22]的顺序一致. BS- 12修饰膨润土对Cu2+和Pb2+的最大吸附量Qmax值较CK分别提高2.9%~56.3%和13.1%~31.8%, 总体上BS- 12修饰对Cu2+的吸附更具有促进作用.但比较BS- 12修饰膨润土对Cu2+和Pb2+的吸附, 表 1显示4种供试土样对Pb2+的Qmax值是Cu2+的1.39~1.84倍, 说明BS- 12修饰膨润土对Pb2+的绝对吸附量高于Cu2+.
|
|
表 1 20℃时不同修饰土样对Cu2+和Pb2+吸附等温线的拟合参数1) Table 1 Fitting parameters for Cu2+ and Pb2+ adsorption isotherms on different modified bentonites (20℃) |
Cu-Pb复合体系中, 各修饰土样对Cu2+和Pb2+的吸附与单一处理具有一致性, 同样显示最大吸附量均表现为Pb2+>Cu2+, 最大吸附量Qmax值随BS- 12修饰比例增加而增加, 且BS- 12修饰更有利于Cu2+的吸的规律.
2.3 Cu2+和Pb2+在BS- 12修饰土上的交互作用及选择系数图 2显示, 相比单一吸附, 4种修饰土样对Cu-Pb复合体系中两种金属离子的吸附量均有所下降, 表现为QCu-0>QCu-mix和QPb-0>QPb-mix的顺序, 说明Cu2+和Pb2+共存时具有相互拮抗的作用.
以复合体系相比单一体系某种金属离子饱和吸附量下降的比例定量表示金属离子间的相互拮抗作用[23].吸附量下降的比例ΔY使用以下公式计算:

|
(5) |
两种金属离子在4种供试土样上的ΔY见图 3. 4种土样对Cu2+吸附的ΔY均显著大于Pb2+, 说明Cu-Pb共存体系中, Pb2+对Cu2+的拮抗作用强于Cu2+对Pb2+的拮抗作用, Pb2+具有较强的吸附竞争性, 与2.2节所得的结果一致.

|
图 3 Cu-Pb复合体系中金属离子间的交互作用 Fig. 3 Interaction between metal ions in Cu-Pb mixed system |
相同金属离子下比较4种土样的ΔY, 经BS- 12修饰后, Cu2+的ΔY小于CK, 而Pb2+的ΔY则大于CK, 说明BS- 12修饰在减弱Pb2+对Cu2+的拮抗作用的同时也增强了Cu2+对Pb2+的拮抗作用, 与2.2节中BS- 12修饰更有利于Cu2+的吸附相呼应.
定义复合体系中某种金属离子的最大吸附量占两种金属离子最大吸附总量的比例为该金属离子的选择性系数, 定量表示两种金属离子在4种土样上的竞争效应与选择性顺序.选择系数可以根据下式计算:
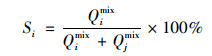
|
(6) |
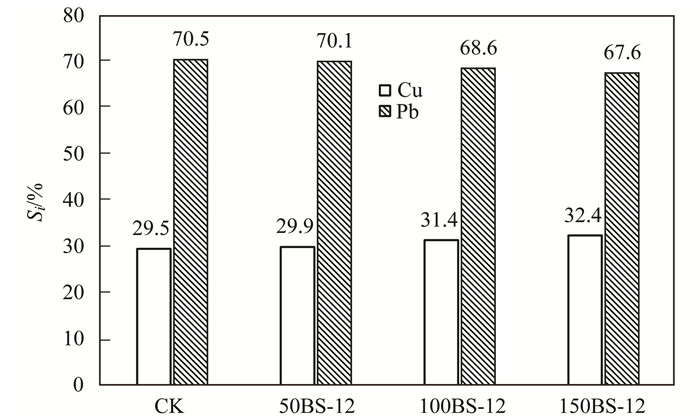
图 4显示4种供试土样对复合体系中两种金属离子的选择系数Si.从中可知, Pb2+的选择系数显著大于Cu2+, CK及BS- 12修饰土规律一致, 说明两性修饰膨润土对Pb2+的吸附具有偏好性; 但Cu2+、Pb2+在4种土样上的选择系数分别为:150BS- 12(32.4%)>100BS- 12(31.4%)>50BS- 12(29.9%)>CK(29.5%)、CK(70.5%)>50BS- 12(70.1%)>100BS- 12(68.6%)>150BS- 12(67.6%).说明随着修饰比例的增加, BS- 12修饰对Cu2+在复合体系中的竞争有所促进, 但对Pb2+的竞争有所抑制.
|
图 4 复合体系中Cu2+和Pb2+的选择系数 Fig. 4 Selection coefficient of Cu2+ and Pb2+ in mixed system |
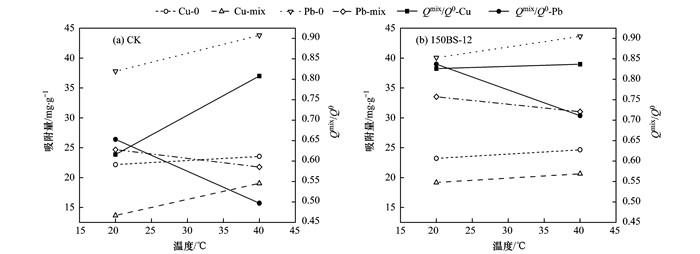
温度对Cu2+和Pb2+的吸附影响见图 5.从中可知, 单一体系中, 两种金属离子的吸附量均随着温度的升高而上升.以40℃与20℃时金属离子吸附量的比值Q40/Q20考察其温度效应, CK对Cu2+和Pb2+的吸附温度效应比值分别为:1.06和1.16, 而150BS- 12则分别为:1.05和1.09.总体看来, 两种土样对两种金属离子的温度效应值较接近1且呈现微弱的增温正效应.
|
图 5 不同温度下Cu2+和Pb2+的吸附量及Qmix/Q0值 Fig. 5 Adsorption capacity and Qmix/Q0values for Cu2+and Pb2+ at different temperatures |
Cu-Pb复合体系中, Cu2+的吸附量随温度升高而上升, CK及150BS- 12对Cu2+的Q40/Q20值分别为:1.39和1.08, 与单一体系中规律一致; 但Pb2+的吸附量则随温度的升高而下降, 其Q40/Q20值分别为:0.88和0.93.说明温度升高, 更有利于Cu2+的吸附, 也意味着Cu2+和Pb2+的吸附具有不同的机制.单一和复合体系中, Cu2+和Pb2+在150BS- 12上的Q40/Q20均比CK接近于1, 进一步证实了有机修饰对于重金属离子的吸附具有“感温钝化”效应[24].
进一步比较Cu2+和Pb2+的Qmix/Q0值随温度的变化, Cu2+的Qmix/Q0值随温度升高而增大, 而Pb2+的Qmix/Q0值则随着温度的升高而减小, 说明温度升高, Cu2+对Pb2+的拮抗作用增强, 而Pb2+对Cu2+的拮抗作用减弱, 温度升高更有利于Cu2+的吸附.
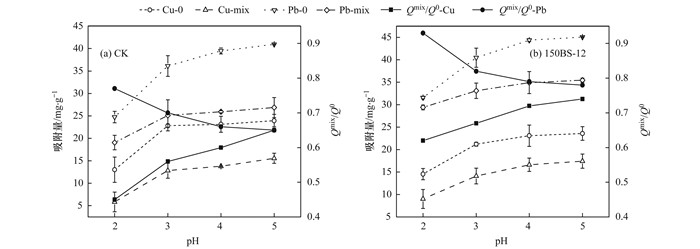
2.5 pH对Cu2+和Pb2+吸附的影响图 6为Cu2+和Pb2+的吸附量以及Qmix/Q0值随pH变化的趋势.两种金属离子的吸附量均随着pH的升高而增加.单一体系中, pH由2增至5, Cu2+在CK和150BS- 12上的吸附量分别增加84.01%和62.13%, 而Pb2+则为65.44%和42.76%. Cu2+的吸附量随pH升高而增加的比例均大于Pb2+, 说明pH升高更有利于Cu2+的吸附. Cu2+和Pb2+在两种土样上的吸附量随pH而增加的比例均为:CK>150BS- 12, 说明150BS- 12修饰减弱了金属离子的吸附量随pH升高而增加的比例.复合体系中, 随pH增加Cu2+和Pb2+在CK和150BS- 12上的吸附量增加的规律与单一吸附时一致.
|
图 6 不同pH值下Cu2+和Pb2+的吸附量及Qmix/Q0值 Fig. 6 Adsorption capacity and Qmix/Q0 values for Cu2+ and Pb2+ at different pH values |
随着pH的升高, CK及150BS- 12对Cu2+的Qmix/Q0值均升高, 而Pb2+的Qmix/Q0值则均下降, 说明随pH升高Cu2+对Pb2+的拮抗作用增强, 而Pb2+对Cu2+的拮抗作用减弱, pH升高更有利于Cu2+的吸附.
2.6 离子强度对Cu2+和Pb2+吸附的影响离子强度对Cu2+和Pb2+的影响见图 7, 结果表明随着离子强度的增加, Cu2+和Pb2+的吸附量均有所降低, 复合体系中Cu2+在CK和150BS- 12上的吸附量下降的比例分别为44.99%和38.41%, 而Pb2+则为62.73%和32.62%, 下降的比例均呈现CK>150BS- 12的顺序, 说明150BS- 12修饰减弱了Cu2+和Pb2+的吸附量下降的比例. Cu-Pb复合后, CK对Pb2+的吸附量随离子强度增加而下降的比例显著大于Cu2+, 说明两种金属离子共存时, 离子强度增加对Pb2+的吸附影响更明显.

|
图 7 不同离子强度下Cu2+和Pb2+的吸附量及Qmix/Q0值 Fig. 7 Adsorption capacity andQmix/Q0 values for Cu2+and Pb2+ at different ionic strengths |
比较两种金属离子的Qmix/Q0值随离子强度变化的趋势, CK对Cu2+的Qmix/Q0值随离子强度变化不明显, 而Pb2+则呈明显地下降趋势, 说明离子强度对Pb2+在CK上吸附的影响更大.而Cu2+和Pb2+在150BS- 12上随离子强度的变化趋势相对较小, 且Cu2+和Pb2+相对接近, 说明150BS- 12修饰减弱了离子强度对金属离子交互作用的影响.
3 讨论膨润土对单一及复合体系中Pb2+的吸附量均显著大于Cu2+, 这是由两种金属离子本身的性质、膨润土表面特性以及其对金属离子的吸附形式决定的.膨润土可以通过静电引力、离子交换和表面络合吸附金属阳离子[25].对于静电引力吸附, 离子的电荷越高, 离子半径越小, 则正、负电荷间吸引力越强[26]. Cu2+、Pb2+同为二价阳离子, 其电荷数相同, 但金属离子在水溶液中通常以水合金属离子的形式存在, 而Pb2+(0.401 nm)的水合离子半径小于Cu2+(0.419 nm), 因此负电荷吸附点位对Pb2+的吸附亲和力更强.
膨润土经BS- 12修饰后对两种金属离子的吸附量均有提高, 均呈现150BS- 12>100BS- 12>50BS- 12>CK的大小顺序, 且单一及复合体系中规律一致.有研究表明[10], 随着修饰比例的增加, 以疏水键合形式修饰到膨润土表面的BS- 12, 其疏水碳链形成的有机相会覆盖一部分负电荷吸附点位, 同时疏水碳链会对亲水性阳离子产生斥力, 这一点和有机碳、CEC、比表面的变化趋势相吻合.但另一方面, BS- 12亲水端所带正、负电荷向外伸展, 其所带羧基负电荷与膨润土上未被覆盖的负电荷继续以静电引力的形式吸附金属离子, 同时金属离子可能与BS- 12上所带胺基及羧基共同反应生成稳定的五元环络合物[9], 所以BS- 12修饰对两种金属离子的吸附较CK均有不同程度的提高. BS- 12修饰对Cu2+的吸附量提升效果较Pb2+更为显著, 且复合体系中随BS- 12修饰比例的增加, Cu2+的竞争效应有所增强而Pb2+的竞争效应有所减弱, 以上结果均表明BS- 12修饰更有利于Cu2+的吸附.这与BS- 12对膨润土的修饰机制及两种金属离子的吸附形式有关.吸附温度效应显示, 单一体系中两种金属单一的吸附量均随着温度的升高而增加, 呈增温正效应, 说明二者的吸附是吸热过程, 均表现出化学吸附的特征.但Cu-Pb复合后, Cu2+的吸附继续呈现增温正效应且增温正效应增强, 而Pb2+的吸附温度效应则由增温正效应转变为增温负效应.以上结果说明温度升高对Cu2+的影响更大, 即Cu2+的吸附以化学吸附为主, 这与许多文献报道的Cu2+容易与羟基、羧基等官能团发生络合吸附相一致[27], 也和红外研究结果相一致, 而Pb2+的吸附则主要为静电引力吸附.由于BS- 12修饰主要是通过形成五元环络合物从而增强膨润土对金属离子的化学吸附, 所以导致其对Cu2+的吸附增强作用较Pb2+更为显著.但BS- 12修饰土对Pb2+的吸附量仍显著大于Cu2+, 且Pb2+在复合条件下的选择系数及竞争效应也大于Cu2+, 说明静电引力依然是Pb2+与Cu2+吸附的主要因素, 但BS- 12的两性修饰具有增强Cu2+化学吸附的作用.
BS- 12修饰膨润土表面的吸附点位是一定的, Cu2+和Pb2+共存会竞争修饰土表面的吸附点位, 因此两种金属离子的吸附量较单一吸附时均有所下降, 表现为相互拮抗的作用, 且随着金属离子初始浓度的增加, 金属离子间的拮抗作用增强.复合体系中Cu2+的吸附量较单一吸附时下降的趋势显著大于Pb2+, 说明水合离子半径较小的Pb2+在静电引力为主要机制的吸附中显然具有更强的竞争性, 这一点在CK和修饰土中具有共性. BS- 12修饰更有利于Cu2+的吸附, 因此BS- 12修饰能够减弱Pb2+对Cu2+的拮抗作用, 同时增强Cu2+对Pb2+的拮抗作用.
背景溶液中的K+主要通过参与竞争修饰土表面的电性吸附位点而减弱对金属阳离子的吸附[28]. Cu-Pb复合后, Pb2+在CK上吸附量随离子强度增加而下降的比例大于Cu2+, 说明Cu2+和Pb2+共存时, K+对Pb2+的竞争作用更强, 也反映出Pb2+更倾向于以静电引力作用吸附到膨润土表面, 而Cu2+更倾向于静电和络合共同的吸附.同时两种土样之间比较, 两种金属离子的吸附量随离子强度的增加而下降的比例均呈CK>150BS- 12的顺序, 这显然是膨润土经BS- 12修饰后, 其表面的负电荷吸附点位减少而BS- 12所带羧基、以及羧基、胺基的五元环络合吸附作用增强的结果, 因此导致K+竞争负电荷吸附点位的作用减弱.
pH升高对金属离子吸附的影响主要由于溶液中H+浓度降低、对负电荷吸附点位的竞争作用减弱以及pH升高也促进了金属离子的水解, 水解生成的羟基金属离子相比自由离子更易被吸附, 因此供试土样对单一及复合溶液中的Cu2+和Pb2+的吸附量均随pH的升高而增加.但Cu2+随pH增大而增加的幅度大于Pb2+, 这是由于2种金属离子的水解常数为KCu(10-7)>KPb(10-11)[29], 水解常数越大, 水解能力越强, 所以Cu2+比Pb2+易于生成金属羟基离子, 这也导致随pH升高, Cu2+的竞争效应增强.
4 结论BS- 12两性修饰土对Cu2+和Pb2+的吸附等温线符合Langmuir和Freundlich模型, 供试土样对单一及复合溶液中Cu2+和Pb2+的最大吸附量均呈150BS- 12>100BS- 12>50BS- 12>CK的顺序, BS- 12修饰对Cu2+吸附的影响比Pb2+更显著, 但其对Pb2+的吸附量仍大于Cu2+; 复合体系中, 共存阳离子Cu2+和Pb2+具有相互拮抗的作用, BS- 12修饰导致Pb2+对Cu2+的拮抗作用增强而Cu2+对Pb2+的拮抗作用减弱, 但Pb2+对Cu2+的拮抗作用仍大于Cu2+对Pb2+的拮抗作用; 温度、pH升高以及离子强度降低均能增加Cu2+和Pb2+的吸附, 但其对两种金属的影响程度不同, 也导致对金属离子间的交互作用产生影响.
| [1] |
串丽敏, 赵同科, 郑怀国, 等. 土壤重金属污染修复技术研究进展[J]. 环境科学与技术, 2014, 37(120): 213-222. Chuan L M, Zhao T K, ZhengH G, et al. Research advances in remediation of heavy metal contaminated soils[J]. Environmental Science & Technology, 2014, 37(120): 213-222. |
| [2] | Anna B, Kleopas M, Constantine S, et al. Adsorption of Cd(Ⅱ), Cu(Ⅱ), Ni(Ⅱ) and Pb(Ⅱ) onto natural bentonite:study in mono- and multi-metal systems[J]. Environmental Earth Sciences, 2015, 73(9): 5435-5444. DOI:10.1007/s12665-014-3798-0 |
| [3] | Du H H, Chen W L, Cai P, et al. Competitive adsorption of Pb and Cd on bacteria-montmorillonite composite[J]. Environmental Pollution, 2016, 218: 168-175. DOI:10.1016/j.envpol.2016.08.022 |
| [4] | Sheikhhosseini A, Shirvani M, Shariatmadari H. Competitive sorption of nickel, cadmium, zinc and copper on palygorskite and sepiolite silicate clay minerals[J]. Geoderma, 2013, 192: 249-253. DOI:10.1016/j.geoderma.2012.07.013 |
| [5] | Liu X F, Hicher P, Muresan B, et al. Heavy metal retention properties of kaolin and bentonite in a wide range of concentration and different pH conditions[J]. Applied Clay Science, 2016, 119: 365-374. DOI:10.1016/j.clay.2015.09.021 |
| [6] |
孟昭福, 满楠, 邓晶, 等. 几种土壤在单一Zn及Cd Cu共存条件下对Zn的吸附[J]. 土壤通报, 2012, 43(2): 379-385. Meng Z F, Man N, Deng J, et al. Adsorption of Zn in different soils with single Zn or Zn in combination with Cd and Cu[J]. Chinese Journal of Soil Science, 2012, 43(2): 379-385. |
| [7] | He S R, Li Y T, Weng L P, et al. Competitive adsorption of Cd2+, Pb2+, and Ni2+ onto Fe3+-modified argillaceous limestone:influence of pH, ionic strength and natural organic matters[J]. Science of the Total Environment, 2018, 637-638: 69-78. DOI:10.1016/j.scitotenv.2018.04.300 |
| [8] | Wang T, Liu W, Xiong L, et al. Influence of pH, ionic strength and humic acid on competitive adsorption of Pb(Ⅱ), Cd(Ⅱ) and Cr(Ⅲ) onto titanate nanotubes[J]. Chemical Engineering Journal, 2013, 215-216: 366-374. DOI:10.1016/j.cej.2012.11.029 |
| [9] | Meng Z F, Zhang Y P, Zhang Z Q. Simultaneous adsorption of phenol and cadmium on amphoteric modified soil[J]. Journal of Hazardous Materials, 2008, 159(2-3): 492-498. DOI:10.1016/j.jhazmat.2008.02.045 |
| [10] | Meng Z F, Zhang Y P, Wang G D. Sorption of heavy metal and organic pollutants on modified soils[J]. Pedosphere, 2007, 17(2): 235-245. DOI:10.1016/S1002-0160(07)60030-7 |
| [11] |
王建涛, 孟昭福, 杨亚提, 等. SDS对两性修饰膨润土吸附Cd2+的影响[J]. 环境科学, 2014, 35(7): 2596-2603. Wang J T, Meng Z F, Yang Y T, et al. Effect of SDS on the adsorption of Cd2+ onto amphoteric modified bentonites[J]. Environmental Science, 2014, 35(7): 2596-2603. |
| [12] |
李婷.两性修饰膨润土对苯酚和Cd(Ⅱ)的平衡吸附特征[D].杨凌: 西北农林科技大学, 2012. 5-10. Li T. Equilibrium adsorption characteristics of amphoteric modified bentonites to Cd(Ⅱ) and phenol[D]. Yangling: Northwest A&F University, 2012. 5-10. http://cdmd.cnki.com.cn/Article/CDMD-10712-1012436814.htm |
| [13] | Ma L Y, Chen Q Z, Zhu J X, et al. Adsorption of phenol and Cu(Ⅱ) onto cationic and zwitterionic surfactant modified montmorillonite in single and binary systems[J]. Chemical Engineering Journal, 2016, 283: 880-888. DOI:10.1016/j.cej.2015.08.009 |
| [14] |
张斌.两性修饰膨润土对苯酚、Cd2+复合污染吸附动力学研究[D].杨凌: 西北农林科技大学, 2012. 52-55. Zhang B. Studies on the adsorption kinetics of phenol and Cd2+ in amphoteric modified bentonites[D]. Yangling: Northwest A&F University, 2012. 52-55. http://cdmd.cnki.com.cn/Article/CDMD-10712-1012436756.htm |
| [15] | Zhu J X, Zhang P, Qing Y H, et al. Novel intercalation mechanism of zwitterionic surfactant modified montmorillonites[J]. Applied Clay Science, 2017, 141: 265-271. DOI:10.1016/j.clay.2017.03.002 |
| [16] | Li W B, Liu Z, Meng Z F, et al. Composite modification mechanism of cationic modifier to amphoteric modified kaolin and its effects on surface characteristics[J]. International Journal of Environmental Science and Technology, 2016, 13(11): 2639-2648. DOI:10.1007/s13762-016-1091-3 |
| [17] |
谢婷, 李文斌, 孟昭福, 等. BS-12+DTAB复配修饰膨润土吸附Cr(Ⅵ)和Cd2+的研究[J]. 农业环境科学学报, 2017, 36(9): 1778-1786. Xie T, Li W B, Meng Z F, et al. Studies on Cr(Ⅵ)and Cd2+ adsorption onto bentonite modified by a BS-12+DTAB complex[J]. Journal of Agro-Environment Science, 2017, 36(9): 1778-1786. |
| [18] |
李文斌.两性-阴(阳)离子复配修饰黏土的修饰机制及其对菲、Cr(Ⅵ)的吸附[D].杨凌: 西北农林科技大学, 2016. 50-54. Li W B. Modification mechanism of amphiphilic-cationic and amphiphilic-anionic modified clay and its adsorption to phenanthrene and Cr(Ⅵ)[D]. Yangling: Northwest A&F University, 2016. 50-54. |
| [19] |
任爽, 孟昭福, 王腾, 等. 阳(阴)离子复配修饰两性磁性膨润土的表面特征差异及对苯酚吸附的影响[J]. 环境科学, 2018, 39(1): 187-194. Ren S, Meng Z F, Wang T, et al. Comparison of amphoteric-cationic and amphoteric-anionic modified magnetic bentonites:characterization and sorption capacity of Phenol[J]. Environmental Science, 2018, 39(1): 187-194. DOI:10.3969/j.issn.1673-1212.2018.01.042 |
| [20] | Zhu K C, Jia H Z, Wang F, et al. Efficient removal of Pb(Ⅱ) from aqueous solution by modified montmorillonite/carbon composite:equilibrium, kinetics, and thermodynamics[J]. Journal of Chemical & Engineering Data, 2017, 62(1): 333-340. |
| [21] | Arfaoui S, Frini-Srasra N, Srasra E. Modelling of the adsorption of the chromium ion by modified clays[J]. Desalination, 2008, 222(1-3): 474-481. DOI:10.1016/j.desal.2007.03.014 |
| [22] | 孟昭福, 李婷, 杨淑英, 等. BS-12两性修饰膨润土对Cd(Ⅱ)的吸附[A].见: 农业环境与生态安全——第五届全国农业环境科学学术研讨会论文集[C].南京: 农业部环境保护科研监测所, 中国农业生态环境保护协会, 2013. 150-157. |
| [23] |
刘娟娟, 梁东丽, 吴小龙, 等. Cr(Ⅵ)对两种黏土矿物在单一及复合溶液中Cu(Ⅱ)吸附的影响[J]. 环境科学, 2014, 35(1): 254-262. Liu J J, Liang D L, Wu X L, et al. Effect of Cr(Ⅵ) anions on the Cu(Ⅱ) adsorption behavior of two kinds of clay minerals in single and binary solution[J]. Environmental Science, 2014, 35(1): 254-262. |
| [24] |
孟昭福, 张一平. 有机修饰改性土对镉离子的吸附及温度效应[J]. 土壤学报, 2005, 42(2): 238-246. Meng Z F, Zhang Y P. Cd2+ adsorption of organic modified soils and its temperature effect[J]. Acta Pedologica Sinica, 2005, 42(2): 238-246. DOI:10.3321/j.issn:0564-3929.2005.02.010 |
| [25] |
张雪萍.膨润土的改性及其对部分重金属离子的吸附研究[D].湘潭: 湘潭大学, 2014. 25-32. Zhang X P. Adsorption of some heavy metal ions from aqueous solution by modified bentonite[D]. Xiangtan: Xiangtan University, 2014. 25-32. http://d.wanfangdata.com.cn/Thesis_D589257.aspx |
| [26] |
刘晶晶. Pb(Ⅱ)、Cu(Ⅱ)、Cd(Ⅱ)在黄土上竞争吸附及解吸特性研究[D].杭州: 浙江大学, 2014. 88-90. Liu J J. Competitive adsorption and desorption behavior of loess soil towards Pb(Ⅱ), Cu(Ⅱ) and Cd(Ⅱ)[D]. Hangzhou: Zhejiang University, 2014. 88-90. http://cdmd.cnki.com.cn/Article/CDMD-10335-1014171134.htm |
| [27] | Li Y R, Bai P, Yan Y, et al. Removal of Zn2+, Pb2+, Cd2+, and Cu2+ from aqueous solution by synthetic clinoptilolite[J]. Microporous and Mesoporous Materials, 2019, 273: 203-211. DOI:10.1016/j.micromeso.2018.07.010 |
| [28] | Wang X K, Liu X P. Effect of pH and concentration on the diffusion of radiostrontium in compacted bentonite-a capillary experimental study[J]. Applied Radiation and Isotopes, 2004, 61(6): 1413-1418. DOI:10.1016/j.apradiso.2004.04.012 |
| [29] |
徐仁扣, 肖双成, 蒋新, 等. pH对Cu(Ⅱ)和Pb(Ⅱ)在可变电荷土壤表面竞争吸附的影响[J]. 土壤学报, 2006, 43(5): 871-874. Xu R K, Xiao S C, Jiang X, et al. Effect of pH on competitive adsorption of Cu(Ⅱ) and Pb(Ⅱ) on variable charge soils[J]. Acta Pedologica Sinica, 2006, 43(5): 871-874. DOI:10.3321/j.issn:0564-3929.2006.05.025 |
 2019, Vol. 40
2019, Vol. 40


