2. 中国环境科学研究院环境基准与风险评估国家重点实验室, 北京 100012;
3. 北京师范大学水科学学院, 北京 100875
2. State Key Laboratory of Environment Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;
3. College of Water Sciences, Beijing Normal University, Beijing 100875, China
电导率是地表水体最基本的水质参数, 是水体水质的重要衡量指标之一, 同时也是评价水环境健康的重要参数[1], 因此是国内外水质监测中重要的监测指标.电导率可以反映水体可溶性固体的总量(total dissolved solids, TDS)[2~4], 通常用于推测水中TDS的含量, 尤其是水体各溶解固形物数据缺失的情况下.此外, 由于溶解离子的导电性, 电导率也可作为水体盐度的度量指标[5].天然淡水体电导率一般在50~500 μS·cm-1之间, 矿化水可达500~1 000 μS·cm-1, 海水电导率则可达30 000 μS·cm-1以上.在没有人为影响的情况下, 天然水体的电导率主要反映流域岩石风化情况[5].但自有人类以来, 人为活动导致的次生盐渍化现象越来越严重, 地表水体电导率或含盐量普遍升高, 对水体生物多样性和生态服务功能产生显著影响[6].国外研究发现氯离子持续输入引起的河流电导率升高会影响鱼类的繁殖、幼苗发育和捕食[1, 7~9]. Biggs指出[10], 电导率在某种程度上也可以反映营养盐的富集情况, 且电导率和流域土地利用密切相关. Leland[11]的研究进一步表明:流域农业活动强度能更好地解释水体电导率的变化, 这与我国黄河流域的情况类似[12].受强烈的人为活动的影响, 我国大部分地表水体也面临类似的问题, 例如陈静生等对黄河和松花江半个世纪水质变化趋势的研究发现:黄河水体有盐渍化趋势, 松花江水体有碱化趋势[12, 13]等, 其根本原因是人为活动引起的水体中各离子组分及TDS的升高, 导致水体电导率发生显著变化, 同时也使水体的物理化学特征发生变化.
湖泊水体通常对人为活动的响应更为敏感[14].已有研究表明中国西北部湖泊存在普遍盐渍化的迹象[15~17].目前蒙新高原湖泊湖水TDS平均值超过10 g·L-1, 相应地湖水电导率也超过了20 000 μS·cm-1, 是北美五大湖区平均电导率的84倍[18].有研究表明长江中下游的太湖水体离子总量和硬度也有显著升高趋势[14].太湖作为我国的第三大淡水湖, 受强烈的人为活动影响, 湖水各主要离子浓度较60年前均呈现数倍增长[14], 湖水电导率也显著升高, 从长远来看, 湖水存在潜在的盐渍化风险.
目前对太湖水环境和污染物方面已经开展了大量的研究, 但尚未见针对太湖电导率变化的专门研究.本文在收集太湖近40年来的电导率和相关历史数据基础上, 同时结合近10年来野外观测数据、太湖水文、水化学等相关数据, 分析太湖不同介质中电导率的时空分布和变化特征, 探究其变化的原因, 以期为预测太湖水体可能的盐渍化进程及湖泊流域的综合管理提供科研依据.
1 材料与方法 1.1 数据收集与野外采样太湖水体电导率和水化学历史数据收集自全球水质监测系统(GEMS, 1980~1999年)和中国生态系统定位观测与研究数据集(2000~2009年)[19], 以及本研究多年来的现场采样监测数据(2009~2018年).历史数据采样频率为每两月一次(1980~1989年)或每月一次(1990~2009年).多年现场监测数据频率为不同水期至少一次.太湖水文数据来源于太湖网的收集(http://www.tba.gov.cn/channels/43.html), 流域污水排放量数据来自太湖流域各省市的统计年鉴.
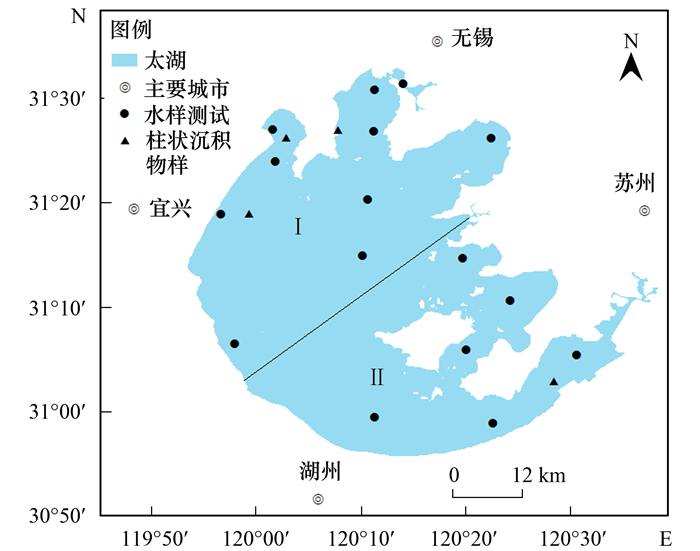
本研究自2015年以来每年于枯水期(11~12月)和丰水期(6~8月)采集太湖不同湖区水和沉积物样品进行测试相关参数, 主要采样湖区为西北湖区(Ⅰ)和东南湖区(Ⅱ)(图 1), 太湖流域雨水主要采集于宜兴市大埔村.水样储存在500 mL预先处理的塑料瓶中; 沉积物使用直径为5 cm, 长度为50 cm柱状采样器进行采集, 并在现场对沉积物按每2 cm进行分割, 分割后的沉积物分别装入聚乙烯密封袋中, 低温冷藏后带回实验室进行下一步处理.
|
图 1 太湖采样点位示意 Fig. 1 Sampling sites in Taihu Lake |
太湖水体电导率使用哈希(HQ30d)水质参数仪现场测试.所有水样在野外经过0.45 μm醋酸纤维滤膜过滤后于4℃保存带回实验室对主要离子和营养盐进行分析测试.其中钾(K+)、钠(Na+)、钙(Ca2+)和镁(Mg2+)采用火焰原子吸收分光光度计法(GB 11904-89, GB 11905-89), 氯(Cl-)采用硝酸银滴定法(GB 11896-89), 硫酸根(SO42-)采用铬酸钡分光光度法(HJ/T 342-2007), 碳酸氢根(HCO3-)和碳酸根(CO3-)采用酸碱指示剂滴定法[20], 氨氮(NH4+)采用纳氏试剂分光光度法(HJ 535-2009), 硝氮(NO3-)采用紫外分光光度法(HJ 346-2007)测试.所有样品均做一组平行实验, 相对误差控制在20%以内.
沉积物分析首先离心获取孔隙水.将现场按2 cm分层的沉积物样装入100 mL离心管中以8 000 r·min-1离心15 min, 取上清液测试孔隙水电导率.离心后固体沉积物经冷冻干燥后研磨, 然后过100目筛子进行筛分.筛分后的每个沉积物样准确称取10 g置于100 mL离心管中, 加入50 mL超纯水(沉积物:水=1:5), 混合物以250 r·min-1振荡24 h, 之后以8 000 r·min-1离心5 min, 取上清液测试沉积物的电导率和pH.沉积物有机质采用重铬酸钾氧化法(NY/T 1121.6-2006)测定.
1.3 数据计算与处理为了分析太湖不同水期电导率的变化, 根据太湖流域情况分为枯水期(1~2月、11~12月)、平水期(3~4月、10月)和丰水期(5~9月)分别讨论.考虑到降雨是太湖水体径流量的重要来源, 对太湖水体离子和电导率可能存在影响, 为估算此可能的影响, 采用如下公式计算2010~2018年直接落入湖泊的年降雨量对太湖水体电导率的平均贡献:
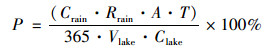
|
(1) |
式中, P为由2010~2018年降水直接输入对太湖水体电导率的平均贡献率, Crain是2010~2018年降水的平均电导率(μS·cm-1), Rrain是2010~2018年平均降雨量(mm), 为1 325 mm, A是太湖水面面积(2 338 km2), T为湖水交换周期(309 d)[14], Vlake是太湖多年平均储水量, 取44.23亿m3, Clake是水体2010~2018年的平均电导率(μS·cm-1), 为465.17 μS·cm-1.
TDS表示水体中可溶性离子总量, 是水体电导率的物质基础.为了探讨对比主要离子和营养盐对太湖水体电导率的贡献, 本研究分别研究了包括和不包括营养盐条件下的TDS与电导率的关系.其中水体中常量离子的TDS计算为:
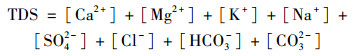
|
(2) |
式中, 离子浓度均以毫克当量计算, 单位meq·L-1.
本研究运用Mann-Kendall趋势检验和突变点分析方法研究太湖水体电导率长期变化趋势, 并用Sen's斜率估计法[21]计算水体电导率变化趋势的斜率.运用SPSS 19.0对数据进行均值、标准差的计算和正态性检验.在正态性检验的基础上选择合适的统计方法, 显著性水平选择0.05.运用Arcgis 10.4进行太湖采样点的绘制, 采用Origin 2015进行绘图.
2 结果与讨论 2.1 太湖水体电导率时空变化特征太湖水体电导率近40年来呈显著上升趋势(P < 0.01, 图 2), 目前水体电导率较1980年相比升高了1.5倍以上, 年平均增长率为10.40 μS·(cm·a)-1.根据Mann-Kendall突变点分析方法, 绘制电导率正向统计量UF和反向统计量UB曲线, 并给出显著性水平α=0.05时的临界值Z=±1.96(具体方法见文献[22]).当UF>0, 表示序列呈上升趋势, 反之则呈下降趋势, 大于或小于±1.96表示上升或下降趋势明显, 趋势不变则为0.如图 2所示:从UF曲线可以看出, 除1984年以外, 1980~2018年的UF值均大于0, 表明太湖水体电导率呈现上升趋势.其中在1994年突破α=0.05的临界值区域, 说明自1994年, UF的值呈现显著的上升趋势.进一步观察UF-UB曲线的交点即突变点, 发现在1996~1997年之间发生突变, 这与太湖水体水化学, 生态系统状况的突变时间基本一致[14].总体来看, 太湖水体电导率变化大致可以分为3个阶段.第一阶段为1996年以前, 水体电导率较低, 平均值为(239.43±70.60)μS·cm-1, 该阶段水体电导率增长较缓慢, 年均增长率为11.79 μS·(cm·a)-1, 可以认为此阶段水体电导率受人为活动影响较小.第二阶段为1996~2006年, 水体电导率增长较快, 年平均增长率为27.77 μS·(cm·a)-1, 处于快速增长阶段.相较于第一阶段, 该阶段水体平均电导率升高了0.87倍, 说明人为活动已成为水体电导率增长的主导因素.第三阶段为2007年至今, 水体电导率增长缓慢, 年平均增长率为3.76 μS·(cm·a)-1, 并处于相对稳定阶段.根据世界卫生组织的水质标准[23, 24], 水体电导率超过800 μS·cm-1就不适合作为饮用水水源.尽管目前太湖水体电导率远未达到此阈值, 但太湖水体电导率的显著升高趋势说明, 太湖也面临潜在的盐渍化趋势, 因此太湖水体电导率的增长应该引起足够的重视.

|
图 2 太湖水体电导率长期变化趋势及其突变性分析 Fig. 2 Long-term trends and mutation analysis of the conductivity of Taihu Lake water |
对太湖不同年代不同湖区水体电导率统计分析发现, 西北湖区水体电导率均大于东南湖区(P < 0.01, 图 3), 这是由于西北湖区是主要的入流区, 受外源输入影响大; 而东南湖区是主要的出流区, 受外源影响小[25], 导致两湖区间水体电导率有明显的差异.这在其它水质特征上也有明显的体现[26].

|
图 3 太湖水体电导率时空变化统计 Fig. 3 Summary statistics for the temporal and spatial variation of conductivity of Taihu Lake water |
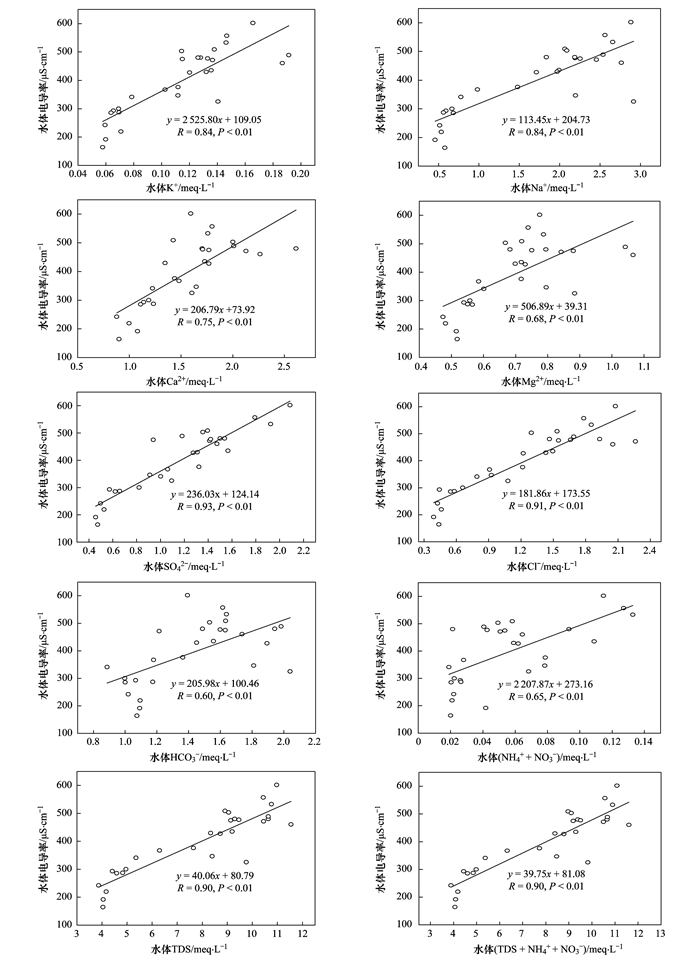
电导率作为水质的基本参数, 可直接反映水体中可溶性离子总量(TDS)[2~4].由图 4可知, 湖水电导率与水体中K+、Na+、Ca2+、Mg2+、SO42-、Cl-、HCO3-和(NH4++NO3-)均呈显著正相关关系(P < 0.01, 图 4), 说明水体中这些离子含量的变化是引起电导率变化的主要原因.值得注意的是, 这些离子和营养盐中K+、Na+、SO42-和Cl-与水体电导率有更高的相关系数(R>0.8), 而这些离子是水体盐渍化过程典型升高速率更快的离子[14].由于太湖富营养化程度较高, 其营养盐含量的升高对水体生态环境产生了显著影响, 但对比氮营养盐和其它主要离子对电导率的贡献发现, 在考虑氮营养盐(TDS+NH4++NO3-)和不考虑的情况下(TDS), 水体TDS和电导率的长期关系(1985~2018年)基本不变(图 4), 说明尽管氮营养盐在太湖水体中含量较高, 但对水体电导率的贡献可以忽略.因此, 可以认为, 太湖水体主要离子变化是电导率变化的主导因素.
|
图 4 水体电导率与主要离子的相关性分析(1985~2018年) Fig. 4 Correlations between conductivity and major ions in water(1985-2018) |
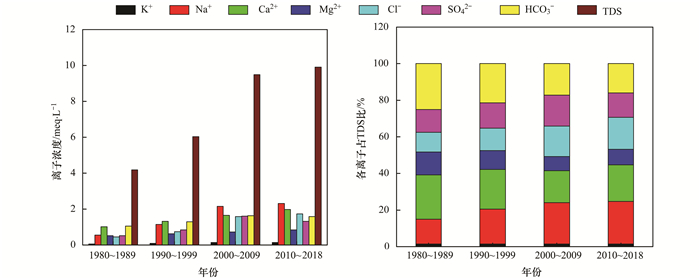
对不同年代水体中各离子浓度和离子浓度占TDS的比值分析发现, 近40年来湖水中各离子浓度均呈现显著的增长趋势(P < 0.05, 图 5), 阳离子中, Na+占TDS的比值增加最为显著, 而Ca2+和Mg2+占TDS比值却有所降低, K+占TDS比值基本不变; 阴离子以Cl-占TDS的比值增加最为显著, HCO3-占TDS比值有所降低, SO42-占TDS的比值在1980~2009年显著增加, 但在2010~2018年占比有所降低(图 5), 说明与湖水中其它离子相比, 水体中Na+和Cl-对电导率的贡献增加最为显著, 这与太湖水体水化学特征的变化相对应[14].同时进一步说明, 这是水体盐渍化趋势的一个重要特征[27, 28].
|
图 5 不同年份各离子浓度及占比分析 Fig. 5 Analysis of major ions concentration and the proportions of major ions in the past decades |
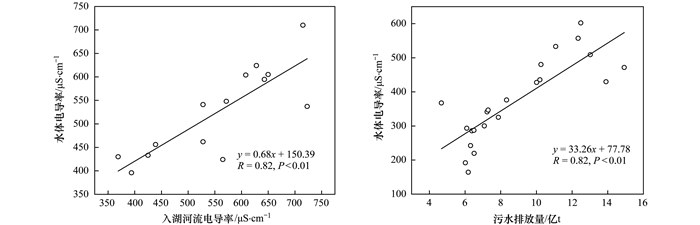
水体中的离子根据其输入途径一般可分为外源性和内源性.其中外源性离子主要通过大气沉降、地表径流和人为排放等途径进入湖泊水体[29, 30].本研究长期监测结果表明:太湖流域雨水电导率(2010~2018年)为(33.61±26.86)μS·cm-1, 变化范围在6.03~93.3 μS·cm-1, 由公式(1)可计算大气沉降对太湖湖水电导率的贡献率仅为4.28%, 说明大气沉降对水体电导率变化影响非常小.此外, 水体电导率与入湖河流电导率、流域污水排放量呈显著正相关(P < 0.01, 图 6), 说明流域人为排放和河流径流输入是引起水体电导率变化的主要外源性因素.
|
图 6 水体电导率与入湖河流电导率(2013~2018年)和污水排放量(1985~2017年)相关性分析 Fig. 6 Correlations between conductivity in the incoming river (2013-2018), the amount of wastewater discharged to the basin (1985-2017), and the conductivity of the water |
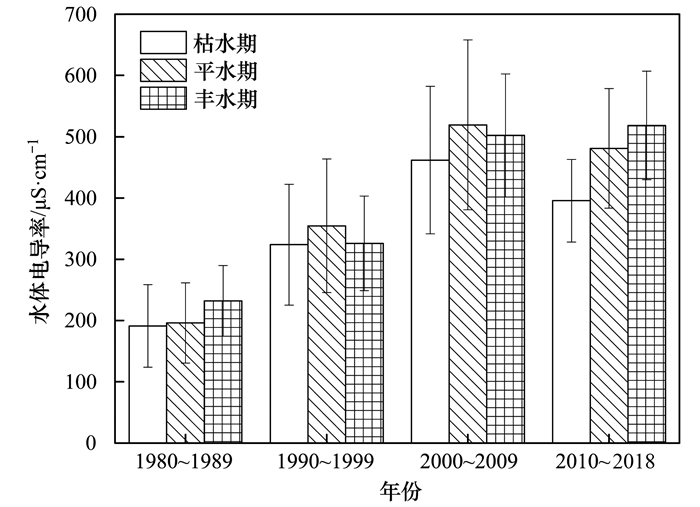
对太湖不同水期电导率的变化对比分析发现, 1980~1999年不同水期湖水电导率不存在显著性差异(图 7), 但之后的2000~2018年不同水期水体电导率存在显著性差异(P < 0.05, 图 7), 其中2000~2009年平水期和丰水期湖水电导率均显著高于枯水期(P < 0.05), 但平水期和丰水期湖水电导率不存在明显变化, 而2010~2018年不同水期间湖水电导率的关系为丰水期>平水期>枯水期, 这说明2010~2018年湖水电导率受季节性径流输入影响更为明显.
|
图 7 不同水期太湖水体电导率变化 Fig. 7 Changes in the conductivity of lake water during different water periods |
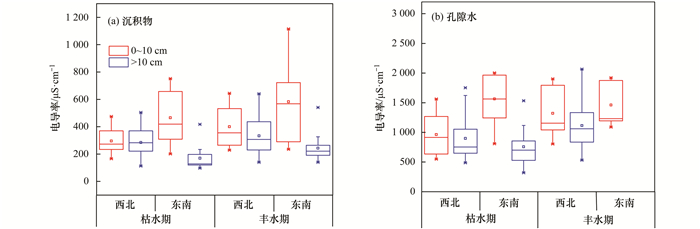
图 8(a)为太湖不同水期和不同湖区沉积物电导率变化情况.空间上, 枯水期西北湖区表层沉积物(0~10 cm)电导率[(295.00±86.77)μS·cm-1]显著低于东南湖区表层沉积物(0~10 cm)电导率[(505.00±190.38)μS·cm-1)][P < 0.05, 图 8(a)], 深层(>10 cm)则相反.剖面上, 枯水期西北湖区表层沉积物(0~10 cm)电导率与深层沉积物(>10 cm)电导率[(284.62±92.24)μS·cm-1]无显著差异, 但东南湖区表层沉积物(0~10 cm)电导率明显高于深层沉积物(>10 cm)电导率[(176.10±97.96)μS·cm-1)][P < 0.05, 图 8(a)], 说明东南湖区表层沉积物(0~10 cm)更易受水体扰动.丰水期沉积物电导率空间和剖面变化规律与枯水期基本相同, 但比较不同水期沉积物电导率发现, 丰水期表层沉积物(0~10 cm)电导率均显著高于枯水期(P < 0.05), 说明丰水期表层沉积物(0~10 cm)更易受水体扰动.
|
图 8 太湖沉积物和孔隙水不同湖区和水期的电导率对比 Fig. 8 Comparison of the conductivity of sediment and pore water in different lake districts and during different water periods |
孔隙水作为沉积物和上覆水进行交换的一个重要通道[31], 在水体扰动的情况下, 最易表现出变化, 因此探究孔隙水电导率时空变化特征对进一步研究水-沉积物界面电导率的关系有重要意义. 图 8(b)为太湖不同水期和不同湖区孔隙水电导率变化情况.空间上, 枯水期西北湖区表层孔隙水(0~10 cm)电导率[(963.33±343.87)μS·cm-1]显著低于东南湖区表层孔隙水(0~10 cm)电导率[(1461.00±424.60)μS·cm-1][P < 0.05, 图 8(b)], 深层(>10 cm)则相反.剖面上, 枯水期西北湖区表层孔隙水(0~10 cm)电导率与深层孔隙水(>10 cm)电导率[(898.02±338.61)μS·cm-1]无显著差异, 但东南湖区表层孔隙水(0~10 cm)电导率明显高于深层孔隙水(>10 cm)电导率[(742.00±385.21)μS·cm-1] [P < 0.05, 图 8(b)].然而对比不同水期孔隙水电导率发现, 丰水期西北湖区表层(0~10 cm)孔隙水电导率高于枯水期.孔隙水电导率在不同水期空间和剖面变化规律与沉积物基本相同, 说明两种介质的电导率之间存在一定关系(具体见2.4节).
沉积物的电导率不仅决定于其主要离子含量, 还受沉积物理化性质的影响.对沉积物电导率与沉积物有机质进行相关性分析发现, 沉积物电导率与有机质呈显著正相关(P < 0.01, 图 9), 说明有机质对沉积物中的离子活化和迁移有显著促进作用.有研究表明沉积物可以通过静电作用吸附金属离子[32, 33], 使其能够带电荷并迁移.沉积物电导率与其pH呈显著负相关(P < 0.05, 图 9), 这是由于酸性条件更易促进金属离子的释放, 促进其迁移性.

|
图 9 沉积物电导率与有机质、pH的相关性分析 Fig. 9 Correlations between conductivity and the organic matter content and pH of lake sediment |
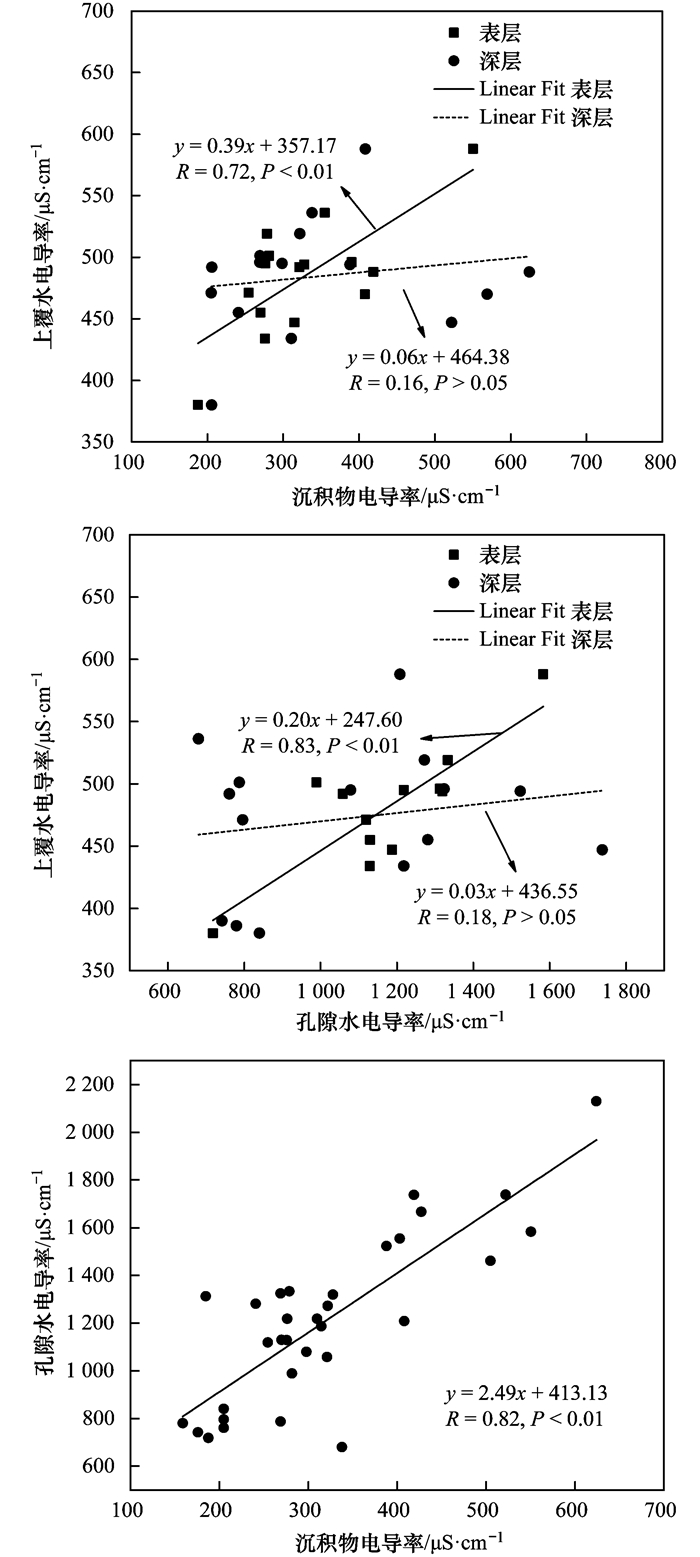
上覆水、孔隙水和沉积物中的离子在不同条件下会进行迁移交换.一方面上覆水中的离子可通过沉淀作用进入沉积物, 另一方面, 沉积物和孔隙水中的离子可通过扩散作用进入上覆水, 因此太湖水体各介质的电导率会通过迁移转化相互影响.对各介质电导率之间相关性分析发现, 表层沉积物、孔隙水(0~10 cm)电导率与上覆水电导率呈显著正相关(P < 0.01, 图 10), 并且孔隙水电导率远高于上覆水(P < 0.05), 说明表层沉积物、孔隙水(0~10 cm)易受水力扰动释放进入上覆水中, 并导致上覆水电导率的升高.但深层沉积物及孔隙水(>10 cm)电导率与上覆水电导率没有相关性(图 10), 说明上覆水电导率受深层孔隙水(>10 cm)影响较小.此外, 整个剖面上(0~50 cm)沉积物电导率和孔隙水电导率呈显著正相关(P < 0.01, 图 10), 说明沉积物和孔隙水之间进行着比较充分的离子迁移交换, 两者之间的相互影响总体上高于对上覆水的影响.
|
图 10 不同介质电导率相关性分析 Fig. 10 Relationship the conductivity of different media |
(1) 太湖水体电导率近40年来呈显著上升趋势, 并在1996~1997年发生突变.总体上由1980~1996年的(239.43±70.60)μS·cm-1增长到目前的(477.31±23.47)μS·cm-1, 年均增长率为10.40 μS·(cm·a)-1.空间上, 西北湖区的水体电导率显著高于东南湖区.水体电导率变化主要由水体主要离子变化导致, 氮营养盐的影响可忽略.流域人为排放和河流径流输入是以引起水体电导率变化的主要外源性因素, 并且水体电导率受季节性径流的影响更为显著.
(2) 孔隙水的电导率显著高于上覆水, 且西北湖区表层沉积物、孔隙水(0~10 cm)电导率低于东南湖区表层沉积物、孔隙水(0~10 cm)电导率, 深层(>10 cm)则相反.剖面上, 西北湖区表层沉积物、孔隙水(0~10 cm)电导率和深层(>10 cm)无显著差异, 但东南湖区表层沉积物、孔隙水(0~10 cm)电导率高于深层(>10 cm).不同水期的变化显示, 丰水期表层沉积物、孔隙水(0~10 cm)电导率高于枯水期, 深层(>10cm)无显著差异.理化性质对沉积物电导率有显著影响, 即沉积物电导率与有机质呈显著正相关(P < 0.01), 与pH呈负相关(P < 0.05).
(3) 太湖不同介质中的电导率存在相互影响的特征.表层沉积物、孔隙水(0~10 cm)电导率与上覆水电导率呈现显著正相关(P < 0.01), 但深层沉积物及孔隙水(>10 cm)电导率与上覆水电导率没有相关性.整个剖面上(0~50 cm)沉积物电导率和孔隙水电导率呈显著正相关(P < 0.01).
| [1] | Morgan II R P, Kline K M, Kline M J, et al. Stream conductivity:relationships to land use, chloride, and fishes in Maryland streams[J]. North American Journal of Fisheries Management, 2012, 32(5): 941-952. DOI:10.1080/02755947.2012.703159 |
| [2] | Rodhe W. The ionic composition of lake waters[J]. SIL Proceedings, 1922-2010, 1949, 10(1): 377-386. |
| [3] | 陈静生. 河流水质原理及中国河流水质[M]. 北京: 科学出版社, 2006. |
| [4] |
李娣, 李旭文, 牛志春, 等. 太湖浮游植物群落结构及其与水质指标间的关系[J]. 生态环境学报, 2014, 23(11): 1814-1820. Li D, Li X W, Niu Z C, et al. Structure of phytoplankton community and relationship between phytoplankton community and water quality in Taihu Lake[J]. Ecology and Environmental Sciences, 2014, 23(11): 1814-1820. DOI:10.3969/j.issn.1674-5906.2014.11.014 |
| [5] | Cañedo-Argüelles M, Kefford B J, Piscart C, et al. Salinisation of rivers:an urgent ecological issue[J]. Environmental Pollution, 2013, 173: 157-167. DOI:10.1016/j.envpol.2012.10.011 |
| [6] | Millennium Ecosystem Assessment. Ecosystems and human well-being:biodiversity synthesis[M]. Washington, DC: Island Press, 2005. |
| [7] | Jackson R B, Jobbágy E G. From icy roads to salty streams[J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(41): 14487-14488. DOI:10.1073/pnas.0507389102 |
| [8] | Megan M H, Nash M S, Neale A C, et al. Biological integrity in mid-atlantic coastal plains headwater streams[J]. Environmental Monitoring and Assessment, 2007, 124(1-3): 141-156. DOI:10.1007/s10661-006-9214-9 |
| [9] | Kelly V R, Lovett G M, Weathers K C, et al. Long-term sodium chloride retention in a rural watershed:legacy effects of road salt on streamwater concentration[J]. Environmental Science & Technology, 2008, 42(2): 410-415. |
| [10] | Biggs B J F. Patterns in benthic algae of streams[A]. In: Stevenson R J, Bothwell M L, Lowe R L (Eds.). Algal Ecology[M]. San Diego, California: Academic Press, 1996. |
| [11] | Leland H V. Distribution of phytobenthos in the Yakima River basin, Washington, in relation to geology, land use and other environmental factors[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1995, 52(5): 1108-1129. DOI:10.1139/f95-108 |
| [12] |
陈静生, 夏星辉, 张利田, 等. 长江、黄河、松花江60-80年代水质变化趋势与社会经济发展的关系[J]. 环境科学学报, 1999, 19(5): 500-505. Chen J S, Xia X H, Zhang L T, et al. Relationship between water quality changes in the Yangtze, Yellow and Songhua rivers and the economic development in the river basins[J]. Acta Scientiae Circumstantiae, 1999, 19(5): 500-505. DOI:10.3321/j.issn:0253-2468.1999.05.007 |
| [13] |
陈静生, 夏星辉, 蔡旭贻. 川贵地区长江干支流河水主要离子含量变化趋势及分析[J]. 中国环境科学, 1998, 18(2): 131-135. Chen J S, Xia X H, Cai X Y. Evolution trend and analysis of major ion contents in the mainstream and some tributaries of Yangtse River in Sichuan and Guizhou Provinces[J]. China Environmental Science, 1998, 18(2): 131-135. DOI:10.3321/j.issn:1000-6923.1998.02.008 |
| [14] | Yu T, Zhang Y, Wu F C, et al. Six-decade change in water chemistry of large freshwater Lake Taihu, China[J]. Environmental Science & Technology, 2013, 47(16): 9093-9101. |
| [15] |
席北斗, 张亚丽, 许秋瑾. 矿化度作为蒙新高原湖泊营养物基准影响指标的可行性[J]. 环境科学, 2012, 33(10): 3308-3313. Xi B D, Zhang Y L, Xu Q J. Possibility of total dissolved solid as one of nutrient baselines in Inner Mongolia-Xinjiang Plateau[J]. Environmental Science, 2012, 33(10): 3308-3313. |
| [16] |
曾海鳌, 吴敬禄. 蒙新高原湖泊水质状况及变化特征[J]. 湖泊科学, 2012, 22(6): 882-887. Zeng H A, Wu J L. Lake status of water quality and the changes in Inner Mongolia-Xinjiang Plateau[J]. Journal of Lake Sciences, 2012, 22(6): 882-887. |
| [17] |
王亚俊, 李宇安, 王彦国, 等. 20世纪50年代以来博斯腾湖水盐变化及趋势[J]. 干旱区研究, 2005, 22(3): 355-360. Wang Y J, Li Y A, Wang Y G, et al. Study on the change of inflow and salt content of the Bosten Lake, Xinjiang since the 1950s[J]. Arid Zone Research, 2005, 22(3): 355-360. |
| [18] | Chapra S C, Dove A, Warren G J. Long-term trends of Great Lakes major ion chemistry[J]. Journal of Great Lakes Research, 2012, 38(3): 550-560. DOI:10.1016/j.jglr.2012.06.010 |
| [19] | 秦伯强, 胡春华. 中国生态系统定位观测与研究数据集:湖泊湿地海湾生态系统卷(江苏太湖站1991-2006)[M]. 第一版. 北京: 中国农业出版社, 2010. |
| [20] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002: 120-121. |
| [21] | Gocic M, Trajkovic S. Analysis of changes in meteorological variables using Mann-Kendall and Sen's slope estimator statistical tests in Serbia[J]. Global and Planetary Change, 2013, 100: 172-182. DOI:10.1016/j.gloplacha.2012.10.014 |
| [22] | Xu D L, Cai Y, Wu X Q, et al. Regime shifts and resilience of the Lake Taihu social-ecological system under long-term external disturbance (1960s-2000s)[J]. Clean-Soil, Air, Water, 2015, 43(4): 561-568. DOI:10.1002/clen.201300870 |
| [23] | MDBMC. The salinity audit of the Murray-darling basin:a 100-year perspective[M]. Canberra: Murray-Darling Basin Commission, 1999. |
| [24] | WHO. Guidelines for drinking water quality[M]. 4th ed.. Geneva: World Health Organization, 2011. |
| [25] |
朱广伟, 秦伯强, 张运林, 等. 2005-2017年北部太湖水体叶绿素a和营养盐变化及影响因素[J]. 湖泊科学, 2018, 30(2): 279-295. Zhu G W, Qin B Q, Zhang Y L, et al. Variation and driving factors of nutrients and chlorophyⅡ-a concentrations in northern region of Lake Taihu, China, 2005-2017[J]. Journal of Lake Sciences, 2018, 30(2): 279-295. |
| [26] | Lei K, Han X J, Zhao J, et al. Characterization of metal kinetics and bioavailability using diffusive gradients in thin films technique in sediments of Taihu Lake, China[J]. Ecotoxicology and Environmental Safety, 2016, 128: 153-160. DOI:10.1016/j.ecoenv.2016.02.019 |
| [27] | Dugan H A, Bartlett S L, Burke S M, et al. Salting our freshwater lakes[J]. Proceedings of the National Academy of Sciences of the United States of America, 2017, 114(17): 4453-4458. DOI:10.1073/pnas.1620211114 |
| [28] | Kaushal S S, Likens G E, Pace M L, et al. Freshwater salinization syndrome on a continental scale[J]. Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(4): E574-E583. DOI:10.1073/pnas.1711234115 |
| [29] |
韩贵琳, 刘丛强. 贵州乌江水系的水文地球化学研究[J]. 中国岩溶, 2000, 19(1): 35-43. Han G L, Liu C Q. Hydrogeochemistry of Wujiang river water in Guizhou Province[J]. Carsologica Sinica, 2000, 19(1): 35-43. DOI:10.3969/j.issn.1001-4810.2000.01.006 |
| [30] |
查慧铭, 朱梦圆, 朱广伟, 等. 太湖出入湖河道与湖体水质季节差异分析[J]. 环境科学, 2018, 39(3): 1102-1112. Zha H M, Zhu M Y, Zhu G W, et al. Seasonal difference in water quality between lake and inflow/outflow rivers of Lake Taihu, China[J]. Environmental Science, 2018, 39(3): 1102-1112. |
| [31] | Yu T, Zhang Y, Meng W, et al. Characterization of heavy metals in water and sediments in Taihu Lake, China[J]. Environmental Monitoring and Assessment, 2012, 184(7): 4367-4382. DOI:10.1007/s10661-011-2270-9 |
| [32] |
张立成, 董文江, 郑建勋, 等. 湘江河流沉积物重金属的形态类型及其形成因素[J]. 地理学报, 1983, 38(1): 55-64. Zhang L C, Dong W J, Zheng J X, et al. The metalform and form factors of heavy metals in the Xiangjiang river sediments[J]. Acta Geographica Sinica, 1983, 38(1): 55-64. DOI:10.3321/j.issn:0375-5444.1983.01.006 |
| [33] |
翟雨翔, 葛淼. 水系沉积物重金属研究进展[J]. 江西农业学报, 2009, 21(1): 127-130. Zhai Y X, Ge M. Research advance in heavy metals in stream sediment[J]. Acta Agriculturae Jiangxi, 2009, 21(1): 127-130. DOI:10.3969/j.issn.1001-8581.2009.01.040 |
 2019, Vol. 40
2019, Vol. 40


