2. 中山大学环境科学与工程学院, 广州 510275;
3. 中山大学深圳研究院, 深圳 518057;
4. 深圳市利赛实业发展有限公司, 深圳 518029;
5. 黑龙江工程学院土木与建筑工程学院, 哈尔滨 150050;
6. 深圳市下坪固体废弃物填埋场, 深圳 518047
2. School of Environmental Science and Engineering, Sun Yat-sen University, Guangzhou 510275, China;
3. Shenzhen Research Institute of Sun Yat-sen University, Shenzhen 518057, China;
4. Shenzhen Lisai Development Co., Ltd., Shenzhen 518029, China;
5. School of Civil and Architecture Engineering, Heilongjiang Institute of Technology, Harbin 150050, China;
6. Shenzhen Xiaping Municipal Solid Waste Landfill Site, Shenzhen 518047, China
垃圾渗滤液是生活垃圾在堆放或填埋过程中产生的高氨氮高有机物废水.在利用传统生物脱氮工艺处理过程中, 具有水力停留时间长, 外加碳源成本高等缺点[1, 2].厌氧氨氧化(anaerobic ammonia oxidation, ANAMMOX)细菌在厌氧的条件下利用NH4+-N作为电子供体, NO2--N为电子受体生成N2, 实现高效自养脱氮[3, 4].近年来利用短程硝化反硝化耦合厌氧氨氧化自养脱氮技术处理垃圾渗滤液逐渐成为行业及学界的热点[5, 6].短程硝化反硝化耦合厌氧氨氧化技术, 不仅无需外加碳源, 而且可大量节省曝气能耗, 具有脱氮负荷高、运行费用低、占地面积小等优点[7~9].垃圾渗滤液低C/N比, 高氨氮的特点, 可以较容易地实现短程硝化, 厌氧氨氧化反应所需要的基质(NH4+-N和NO2--N)可以从短程硝化反应中获得.一般来说, 短程硝化反硝化耦合厌氧氨氧化工艺可以实现垃圾渗滤液的高效脱氮[10].然而, 作为新型的废水脱氮技术, 目前厌氧氨氧化工艺控制技术尚不成熟.厌氧氨氧化菌生长缓慢, 细胞产率低, 易受水质和运行条件影响, 从而导致了厌氧氨氧化工艺在实际废水处理中呈现启动缓慢、稳定性欠缺等问题[11, 12], 影响了组合工艺在工程上的广泛应用.
本研究以某垃圾填埋场将现有垃圾渗滤液短程硝化反硝化脱氮工艺改造为短程硝化反硝化耦合厌氧氨氧化工艺的实际需求为背景, 开展实验室可行性研究.主要分析耦合短程硝化反硝化的厌氧氨氧化垃圾渗滤液处理系统的启动过程、运行控制条件和运行效果.因此, 本实验选用渗滤液处理厂短程硝化反硝化污泥作为接种污泥, 启动厌氧氨氧化反应器, 在系统启动稳定后, 逐渐提高系统氮负荷, 使之贴近渗滤液原水的氨氮浓度.通过考察系统长期运行下脱氮效能及微生物群落变化, 以期为垃圾渗滤液等高氨氮废水脱氮的实际工程应用提供相关实验基础和技术支持.
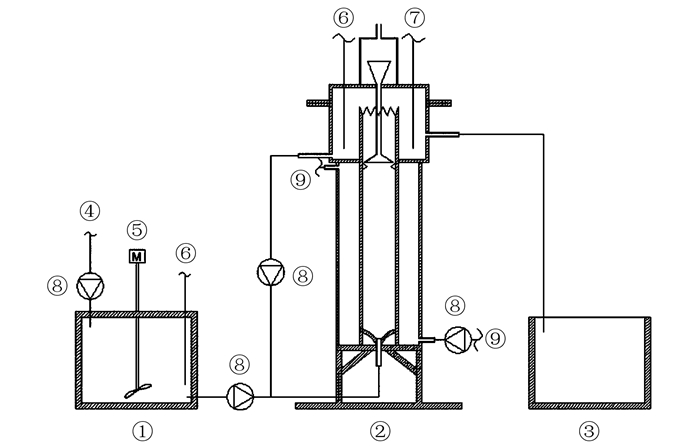
1 材料与方法 1.1 实验装置本研究中采用UASB反应器进行厌氧氨氧化小试, 实验装置如图 1所示.反应器采用有机玻璃制作, 反应区内径6 cm, 高度40 cm, 有效容积为1 L.反应器整体置于遮光保温的环境中, 利用带温度控制的循环水浴装置保持温度在30~35℃.原水通过蠕动泵以连续流形式进入反应器底部, 通过污泥层后再经反应器顶端的三相分离器实现泥、水、气分离, 最后在顶端溢流出反应器进入出水池.
|
图 1 实验装置示意 Fig. 1 Schematic diagram of ANAMMOX-UASB reactor |
本研究采用模拟垃圾渗滤液废水, 其中NH4+-N和NO2--N分别由NH4Cl和NaNO2按需添加.其余主要成分为:NaHCO3 (1 250 mg·L-1), MgSO4·7H2O (300 mg·L-1), KH2PO4(100 mg·L-1), CaCl2·H2O (4.3 mg·L-1), 微量元素浓缩液Ⅰ(1.25 mL·L-1)和微量元素浓缩液Ⅱ (1.25 mL·L-1).微量元素浓缩液Ⅰ组成为:EDTA (5 000 mg·L-1), FeSO4 (5 000 mg·L-1).微量元素浓缩液Ⅱ组成为:EDTA (1 000 mg·L-1), H3BO4 (14 mg·L-1), MnCl2·4H2O (990 mg·L-1), ZnSO4·7H2O (430 mg·L-1), NiCl2·6H2O (190 mg·L-1), NaSeO4·H2O (210 mg·L-1), NaMoO4·2H2O (220 mg·L-1).
1.3 接种污泥厌氧氨氧化系统中接种的污泥取自某垃圾填埋场渗滤液处理车间中的短程硝化反硝化池.该污泥的MLSS、MLVSS质量浓度分别为5 396 mg·L-1和3 342 mg·L-1, 颜色呈棕黄色.
1.4 分析项目和方法实验期间定期采样, 水样沉淀30 min后取上清液用0.45 μm微孔滤膜过滤, 再测定相关水质指标.常规指标检测方法均按照文献[13]操作. NH4+-N:纳氏试剂分光光度法;NO2--N:N-(1-萘基)-乙二胺光度法;NO3--N:紫外分光光度法;MLVSS/MLSS:重量法. pH值由pH计(JENCO 3675, 美国)测定, DO含量采用溶解氧仪(JENCO 6308DT, 美国)检测.
微生物群落多样性的样品分别取自接种后第50 d和250 d反应器内的混合污泥.利用Illumina MiSeq PE300测序平台对样品中的16S rRNA局部区域进行高通量的扩增子测序, 完成微生物群落结构及多样性研究.包括DNA提取、PCR扩增、MiSeq文库构建和MiSeq测序[14].
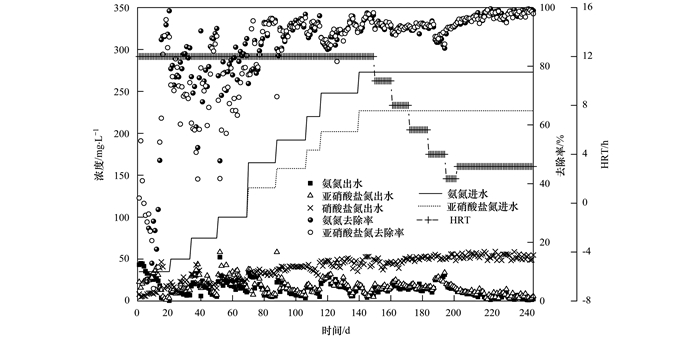
2 结果与讨论 2.1 厌氧氨氧化系统启动根据脱氮规律, 可将UASB反应器内厌氧氨氧化的启动分为3个阶段(图 2):菌体自溶阶段、活性迟滞阶段和活性提高阶段.在整个启动期内, 反应器内保持HRT=12 h.进水总氮浓度从菌体自溶阶段的70 mg·L-1(NO2--N:NH4+-N=1:1);逐渐提升至活性迟滞阶段的100、150和200 mg·L-1, NO2--N:NH4+-N比值保持1:1;在活性提高阶段, 对进水总氮浓度进行300、350、400、450和500 mg·L-1的推进(NO2--N:NH4+-N=1.2:1).每个负荷阶段在系统出水氨氮或亚硝酸盐氮的浓度稳定低于10 mg·L-1后, 进入下一阶段.
|
图 2 UASB厌氧氨氧化反应器启动及长期运行性能(1~250 d) Fig. 2 Start-up and long-term performance of ANAMMOX-UASB reactor(1-250 d) |
由于接种的短程硝化反硝化原污泥中有较多的氨氧化细菌和反硝化异养菌[15], 对反应器内黑暗且厌氧的新环境极为敏感而发生自溶解, 释放出氨和有机物.所以反应器启动初期(1~4 d)出水NH4+-N浓度高于进水NH4+-N浓度, 接种污泥中的反硝化菌消耗NO2--N和NO3--N, 利用菌体自溶提供的有机物进行反硝化脱氮反应.但随着菌体自溶强度减弱, 厌氧氨氧化细菌活性逐渐变强, 反硝化作用由于反硝化菌缺少有机物和反应底物而逐渐减弱, 因此出水NO2--N浓度出现上升情况[16].在第11~12 d时, 出现了出水NO2--N浓度高于进水的情况.第13 d时, 系统出水NH4+-N浓度和NO2--N浓度均低于进水值, 可认为此时菌体自溶的高峰期已过, 系统开始脱离短程硝化反硝化状态.
2.1.2 活性迟滞阶段由于此阶段(14~69 d)进水总氮负荷的逐渐增加, 且反应器内厌氧氨氧化菌的活性也有明显增强.负荷每一次提升后, 由于初期微生物对环境的改变还未适应, 致使脱氮效率短暂降低, 但经过10 d左右NH4+-N和NO2--N的去除率即可达到80%以上, 对应总氮去除负荷也随之增大.系统的容积氨氮去除负荷、容积亚硝酸盐氮去除负荷、容积总氮去除负荷分别由第14 d的33.53、37.89和71.42 mg·(L·d)-1, 达到了第69 d的175.27、159.09和334.36 mg·(L·d)-1, 提升倍数分别为4.2、3.2和3.6.这一变化规律与汪瑶琪等[17]的研究相一致, 在反应器容积负荷提高的同时, 氮素去除负荷也对应地提高.
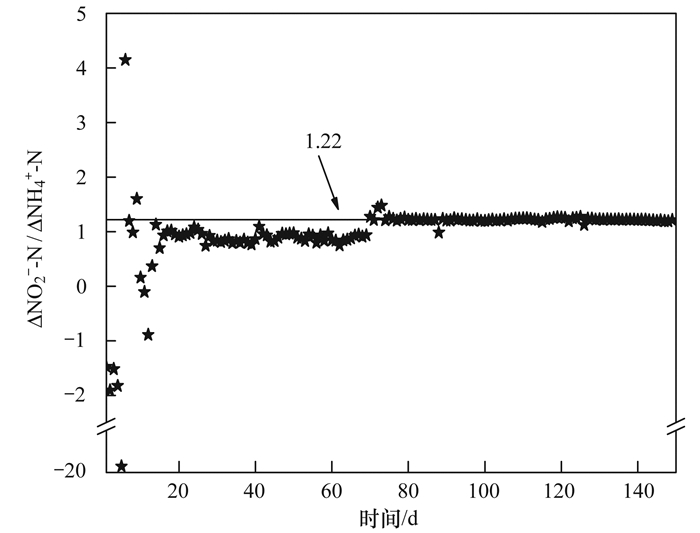
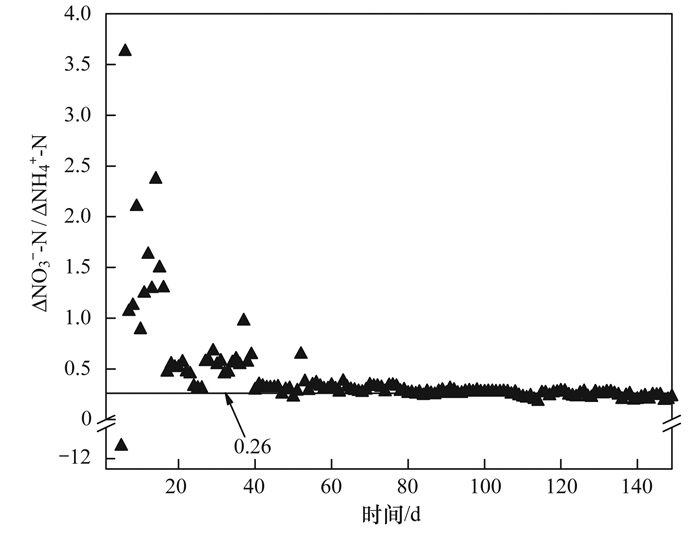
待负荷提高后氮素去除达到稳定, 计算系统中亚硝酸盐氮去除量/氨氮去除量(ΔNO2--N/ΔNH4+-N)和硝酸盐氮生成量/氨氮去除量(ΔNO3--N/ΔNH4+-N)的平均值.当系统容积负荷提高时, 氮素去除比例也随之发生变化.由图 3和图 4可知, 系统ΔNO2--N/ΔNH4+-N和ΔNO3--N/ΔNH4+-N平均值从启动初期的波动状态逐渐趋于稳定.其中, ΔNO3--N/ΔNH4+-N由2.37(第14 d)基本稳定至本阶段后期的0.30左右.此时系统内的短程硝化反硝化反应逐渐减弱, 厌氧氨氧化反应已经较为稳定, 且已经占据主导地位, 系统且具有了一定的脱氮能力.
|
图 3 UASB厌氧氨氧化反应器第1~149 d的亚硝酸盐氮去除量/氨氮去除量 Fig. 3 Value of ΔNO2--N/ΔNH4+-N in the ANAMMOX-UASB reactor(1-149 d) |
|
图 4 UASB厌氧氨氧化反应器第1~149 d的硝酸盐氮生成量/氨氮去除量 Fig. 4 Value of ΔNO3--N/ΔNH4+-N in the ANAMMOX-UASB reactor(1-149 d) |
虽然系统进水已经通过曝氮气脱氧至DO < 0.2 mg·L-1, 但反应器连续进水过程中难免会有溶解氧的增加, 系统内不可避免地会存在硝化反应.考虑到系统内并不是单一的进行厌氧氨氧化反应, 未被厌氧氨氧化反应消耗的基质会被系统中存在的硝化细菌所消耗, 且系统内可能对厌氧氨氧化菌产生抑制的有机物可以被反硝化菌消耗, 因此, 将此阶段的进水NO2--N/NH4+-N值调整为1.2左右, 略低于厌氧氨氧化反应中的理论值1.32.
此阶段(70~149 d)系统内NH4+-N和NO2--N实现同步高效去除(图 2), 脱氮效果良好, 系统平均NH4+-N去除率为91%, 平均NO2--N去除率为92%.从图 3和图 4可看出, 将进水NO2--N/NH4+-N比值进行调整之后, 系统的ΔNO2--N/ΔNH4+-N平均值(1.22)及ΔNO3--N/ΔNH4+-N平均值(0.26)接近厌氧氨氧化反应的理论值1.32和0.26.对于不同的接种污泥、原水水质和实验方法, 学者们启动成功的厌氧氨氧化反应器具有不同的ΔNO2--N/ΔNH4+-N和ΔNO3--N/ΔNH4+-N[17, 18], 主要因为不同的条件下, 系统内与厌氧氨氧化共存的反应不同所致[19].
第149 d时, 系统的容积氨氮去除负荷、容积亚硝酸盐氮去除负荷、容积总氮去除负荷分别为442.09、536.24和978.33 mg·(L·d)-1, 与第70 d时的200.08、254.39和454.46 mg·(L·d)-1相比均提高了1倍以上.可见此时UASB反应器的厌氧氨氧化特性已经全部显现, 由此判断厌氧氨氧化系统启动成功.
2.2 HRT调整在保证厌氧氨氧化系统运行稳定的前提下, UASB反应器内ANAMMOX启动成功后第150 d时, 对反应器的HRT进行梯度调整, 保持进水TN浓度和NO2--N/NH4+-N比值不变.与此同时, 系统的进水总氮负荷得到提升, 也使反应器上部的污泥可以获得足够的反应基质, 促进系统成熟.在第150~250 d, 系统经历了6个阶段的HRT调整, 依次为10、8、6、4、2和3 h.
由图 2可见, 每次缩短HRT后, 系统中NH4+-N和NO2--N的出水浓度略有波动, 呈现先上升后下降的趋势, 但总体上NH4+-N去除率和NO2--N去除率均在80%以上, 系统的去除效果相对稳定.在HRT为10、8、6和4 h时, 系统的容积总氮平均去除速率分别达到了1 123.63、1 409.85、1 890.62和2 748.69 mg·(L·d)-1.但是当HRT调到2 h时, 系统NH4+-N和NO2--N的出水浓度明显上升, 处理效果出现恶化趋势. NH4+-N去除率和NO2--N去除率处于持续下降的状态, 均降至70%以下.尽管此时系统的TN去除率有一定的提高, 但是容积总氮去除负荷随着系统的恶化而下降至3 887.03 mg·(L·d)-1.由于系统内存在与厌氧氨氧化共存的反硝化反应, 随着HRT的逐渐缩短, 厌氧氨氧化对脱氨的贡献率降低[20].魏琛等[21]的研究也证明系统HRT过短会导致含氮污染物去除不完全.
第203 d时将反应器的HRT调回至3 h, 以避免系统继续恶化.随后, 系统的脱氮性能得到逐渐恢复, 氮去除率达到80%以上.随着反应的继续运行, 系统的进水总氮容积负荷提高到4 000.00 mg·(L·d)-1, 接近垃圾渗滤液原水的氮浓度, 容积总氮平均去除负荷达到3 885.76 mg·(L·d)-1, NH4+-N和NO2--N的平均去除率均达到95%以上.系统脱氮效果较好且稳定.
2.3 系统中微生物群落结构分析 2.3.1 系统微生物群落多样性变化分析本实验中选取的污泥样品分别来自低负荷启动初期(50 d)与高负荷稳定运行期(250 d)时的系统, α多样性参数分析结果如表 1所示. α多样性统计中Chao1指数和OTUs指数是表征菌群丰富度的关键指标, 指数值越高表明物种数越多[22].与启动初期相比, 系统在完全成熟的反应后期时Chao1指数和OTUs数有所下降, 可见随着反应器负荷的不断提高, 微生物种类呈现下降趋势. Simpson指数和Shannon指数受样品群落中物种丰富度和物种均匀度的影响, 可用来表征菌群的多样性.群落多样性越高, 则Simpson指数越大;而Shannon指数越高则表明群落复杂程度越大.由表 1数据可见, 250 d时的样品Shannon指数减小, Simpson指数也同步地减小, 即在系统稳定运行后期, 污泥群落结构复杂性降低, 优势菌群比例增大.
|
|
表 1 样品的α多样性参数 Table 1 The α diversity index of microbial communities in the samples |
2.3.2 微生物群落门水平结构分析
对各样品进行门水平上的分析, 探究不同时期系统中微生物群落组成情况, 统计结果见表 2.在启动初期和完全成熟的反应后期, 系统中微生物群落结构的多样性比较丰富.系统微生物在门水平上主要有浮霉菌门(Planctomycetes)、变形菌门(Proteobacteria)、绿菌门(Chlorobi)、、绿弯菌门(Chloroflexi)和拟杆菌门(Bacteroidetes)等, 其中脱氮功能菌主要有浮霉菌门和变形菌门[17].
|
|
表 2 微生物群落的相对丰度(门水平) Table 2 Abundance of microbial community at phylum level |
厌氧氨氧化菌主要属于浮霉菌门[23].由表中数据可知, 随着厌氧氨氧化反应器的成功启动和稳定运行, 浮霉菌门丰度大幅提高, 在第250 d时丰度达到54.94%.对应反应器的氨氮和亚硝酸盐氮平均去除率均达到95%以上, 与微生物变化规律相一致.反硝化菌属在门水平上属于变形菌门和拟杆菌门[24~26], 他们的丰度在第250 d时较第50 d时明显减少.异养菌所属的绿弯菌门丰度变化不大.绿菌门的丰度则从30.51%减少到10.87%.可见在系统启动后的长期稳定运行条件下, 微生物群落结构发生了显著变化, 厌氧氨氧化菌得到了富集.
2.3.3 脱氮相关的微生物群落属水平结构分析为了对反应器内的脱氮功能菌进行详细分析, 在16S rRNA高通量测序所得的数据当中, 挑选出与系统脱氮相关的主要菌属进行分析比对(表 3).从启动初期到系统完全成熟的反应后期运行过程中, 系统中的脱氮功能菌主要有厌氧氨氧化细菌、反硝化细菌、氨氧化细菌(AOB)和亚硝氮氧化细菌(NOB), 这证实了该反应系统是一个同时具有厌氧氨氧化、硝化和反硝化的综合脱氮系统.
|
|
表 3 脱氮相关的微生物群落序列数及相对丰度(属水平) Table 3 Sequences and abundance of nitrogen removal related to the microbial community in sludge at genera level |
在第50 d和250 d时, 厌氧氨氧化菌属的相对丰度分别为1.97%和49.70%.在运行中, 厌氧氨氧化菌得到了很好地富集, 可知厌氧氨氧化为系统脱氮的主要途径.虽然进水中含有少量未能完全消除的溶解氧, 这为AOB菌属的存活提供了条件, 但厌氧氨氧化细菌在反应过程中的大量增殖, 使得AOB菌在基质争夺上处于劣势.因此, AOB菌属的相对丰度由0.27%(第50 d)减弱为0.03%(第250 d).而NOB菌属在第250 d的相对丰度仅为0.01%以下, 最终被淘汰出本系统.由于反硝化细菌可以在厌氧条件下利用细菌死亡释放的有机物发生反硝化反应, 因此反硝化菌属的相对丰度较为稳定, 由0.37%(第50 d)增至0.88%(第250 d), 仅有小幅增加.这种情况可能是作为一种好氧反硝化细菌如Diaphorobacter属, 可以消耗反应器中残留的溶解氧, 从而提升厌氧氨氧化系统的脱氮能力[27].
目前研究的厌氧氨氧化菌共有5个菌属[28, 29], 属于浮霉菌门.本系统中浮霉菌门检测到了Candidatus Kuenenia、Candidatus Jettenia和Candidatus Brocadia属等.随着系统的负荷提高和稳定运行, Candidatus Kuenenia属的富集程度最为明显, 其相对丰度由第50d的1.97%增至250 d的49.66%.而第250d时, Candidatus Jettenia和Candidatus Brocadia属的相对丰度仅为0.03%和0.01%以下, 数量极微.这是由于本实验的UASB厌氧氨氧化系统进水中含有大量亚硝酸盐, 而Candidatus Brocadia属对亚硝酸盐的存在极为敏感, 因此该菌属难以富集成功[30].与Candidatus Kuenenia属相比, Candidatus Brocadia属对反应基质的亲和力和耐受性都差得多[31].
在经历了250 d的运行过程之后, UASB厌氧氨氧化系统内生物多样性呈现逐渐减少的现象, 结合门水平和属水平上的群落结构分析, 说明了系统内厌氧氨氧化细菌成功富集, 为系统内的优势群落, 而接种污泥中的硝化细菌和其他微生物均有明显减少, 降低了对系统厌氧氨氧化性能的抑制影响.
3 结论(1) 以短程硝化反硝化污泥为UASB厌氧氨氧化工艺的接种污泥, 以人工配水的方式, 系统在149 d成功启动了厌氧氨氧化.后期阶段通过缩短HRT方式提高负荷, 进水总氮容积负荷达到4 000.00 mg·(L·d)-1, 接近垃圾渗滤液原水的氮浓度.总氮容积平均去除速率达到3 885.76 mg·(L·d)-1, 系统氨氮和亚硝酸盐氮的平均去除率均超过95%.说明本系统已经可以稳定且长期运行厌氧氨氧化, 在短程硝化反硝化基础上耦合厌氧氨氧化实现垃圾渗滤液深度处理的升级改造工艺具有可行性.
(2) 经过250 d的运行之后, 系统中生物多样性逐渐减少, 厌氧氨氧化细菌占据了主要菌群的位置.在门水平上厌氧氨氧化主要菌群为Planctomycetes, 其相对丰度达到了54.94%.在属水平上Candidatus Kuenenia为厌氧氨氧化主要菌属, 其相对丰度达到了49.66%.
| [1] | Shalini S S, Joseph K. Nitrogen management in landfill leachate:application of SHARON, ANAMMOX and combined SHARON-ANAMMOX process[J]. Waste Management, 2012, 32(12): 2385-2400. DOI:10.1016/j.wasman.2012.06.006 |
| [2] | Jokela J P Y, Kettunen R H, Sormunen K M, et al. Biological nitrogen removal from municipal landfill leachate:low-cost nitrification in biofilters and laboratory scale in-situ denitrification[J]. Water Research, 2002, 36(16): 4079-4087. DOI:10.1016/S0043-1354(02)00129-X |
| [3] | Kartal B, Maalcke W J, de Almeida N M, et al. Molecular mechanism of anaerobic ammonium oxidation[J]. Nature, 2011, 479(7371): 127-130. DOI:10.1038/nature10453 |
| [4] | Ali M, Chai L Y, Tang C J, et al. The increasing interest of ANAMMOX research in China:bacteria, process development, and application[J]. BioMed Research International, 2013, 2013: 134914. |
| [5] | Wen X, Gong B Z, Zhou J, et al. Efficient simultaneous partial nitrification, anammox and denitrification (SNAD) system equipped with a real-time dissolved oxygen (DO) intelligent control system and microbial community shifts of different substrate concentrations[J]. Water Research, 2017, 119: 201-211. DOI:10.1016/j.watres.2017.04.052 |
| [6] | Azari M, Walter U, Rekers V, et al. More than a decade of experience of landfill leachate treatment with a full-scale anammox plant combining activated sludge and activated carbon biofilm[J]. Chemosphere, 2017, 174: 117-126. DOI:10.1016/j.chemosphere.2017.01.123 |
| [7] | Jetten M S M, Cirpus I, Kartal B, et al. 1994-2004:10 years of research on the anaerobic oxidation of ammonium[J]. Biochemical Society Transactions, 2005, 33(1): 119-123. |
| [8] | Joss A, Salzgeber D, Eugster J, et al. Full-scale nitrogen removal from digester liquid with partial nitritation and anammox in one SBR[J]. Environmental Science & Technology, 2009, 43(14): 5301-5306. |
| [9] | Ma B, Wang S Y, Cao S B, et al. Biological nitrogen removal from sewage via anammox:recent advances[J]. Bioresource Technology, 2016, 200: 981-990. DOI:10.1016/j.biortech.2015.10.074 |
| [10] | Wang G, Xu X C, Zhou L, et al. A pilot-scale study on the start-up of partial nitrification-anammox process for anaerobic sludge digester liquor treatment[J]. Bioresource Technology, 2017, 241: 181-189. DOI:10.1016/j.biortech.2017.02.125 |
| [11] | Chen H, Hu H Y, Chen Q Q, et al. Successful start-up of the anammox process:influence of the seeding strategy on performance and granule properties[J]. Bioresource Technology, 2016, 211: 594-602. DOI:10.1016/j.biortech.2016.03.139 |
| [12] | Miao L, Yang G Q, Tao T, et al. Recent advances in nitrogen removal from landfill leachate using biological treatments-A review[J]. Journal of Environmental Management, 2019, 235: 178-185. |
| [13] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002: 88-284. |
| [14] |
陈重军, 张海芹, 汪瑶琪, 等. 基于高通量测序的ABR厌氧氨氧化反应器各隔室细菌群落特征分析[J]. 环境科学, 2016, 37(7): 2652-2658. Chen C J, Zhang H Q, Wang Y Q, et al. Characteristics of microbial community in each compartment of ABR ANAMMOX reactor based on high-throughput sequencing[J]. Environmental Science, 2016, 37(7): 2652-2658. |
| [15] |
梁俊宇, 周鸿, 赵晴, 等. 垃圾渗滤液部分亚硝化的启动运行及菌群分析[J]. 水处理技术, 2018, 44(3): 99-103, 108. Liang J Y, Zhou H, Zhao Q, et al. Analysis of start-up, operation and microbial community during landfill leachate partial nitritation[J]. Technology of Water Treatment, 2018, 44(3): 99-103, 108. |
| [16] | Wang T, Zhang H M, Gao D W, et al. Enrichment of anammox bacteria in seed sludges from different wastewater treating processes and start-up of Anammox process[J]. Desalination, 2011, 271(1-3): 193-198. DOI:10.1016/j.desal.2010.12.034 |
| [17] |
汪瑶琪, 张敏, 姜滢, 等. 厌氧氨氧化启动过程及微生物群落结构特征[J]. 环境科学, 2017, 38(12): 5184-5191. Wang Y Q, Zhang M, Jiang Y, et al. Start-up and characteristics of the microbial community structure of ANAMMOX[J]. Environmental Science, 2017, 38(12): 5184-5191. |
| [18] |
陈胜, 孙德智, 遇光禄. 填充床快速启动厌氧氨氧化反应器及其脱氮性能研究[J]. 环境科学, 2010, 31(3): 691-696. Chen S, Sun D Z, Yu G L. Rapid startup and nitrogen removal characteristic of anaerobic ammonium oxidation reactor in packed bed biofilm reactor with suspended carrier[J]. Environmental Science, 2010, 31(3): 691-696. |
| [19] |
黄曦, 张雁秋, 李开銮. 浅谈ANAMMOX反应的启动研究[J]. 污染防治技术, 2010, 23(1): 74-77. Huang X, Zhang Y Q, Li K L. Studies on the start-up of ANAMMOX[J]. Pollution Control Technology, 2010, 23(1): 74-77. |
| [20] |
安芳娇, 赵智超, 黄利, 等. HRT对厌氧氨氧化协同异养反硝化脱氮的影响[J]. 环境科学, 2018, 39(9): 4302-4309. An F J, Zhao Z C, Huang L, et al. Effect of HRT on nitrogen removal using ANAMMOX and heterotrophic denitrification[J]. Environmental Science, 2018, 39(9): 4302-4309. |
| [21] |
魏琛, 陆天友, 钟仁超, 等. HRT及氮素负荷对厌氧氨氧化系统的影响[J]. 环境科学学报, 2010, 30(4): 749-755. Wei C, Lu T Y, Zhong R C, et al. Influence of HRT and nitrogen load on an ANAMMOX system[J]. Acta Scientiae Circumstantiae, 2010, 30(4): 749-755. |
| [22] | Ma J X, Wang Z W, Yang Y, et al. Correlating microbial community structure and composition with aeration intensity in submerged membrane bioreactors by 454 high-throughput pyrosequencing[J]. Water Research, 2013, 47(2): 859-869. DOI:10.1016/j.watres.2012.11.013 |
| [23] |
王亚宜, 黎力, 马骁, 等. 厌氧氨氧化菌的生物特性及CANON厌氧氨氧化工艺[J]. 环境科学学报, 2014, 34(6): 1362-1374. Wang Y Y, Li L, Ma X, et al. Bio-characteristics of anammox bacteria and CANON anammox process[J]. Acta Scientiae Circumstantiae, 2014, 34(6): 1362-1374. |
| [24] | Luo J H, Liang H, Yan L J, et al. Microbial community structures in a closed raw water distribution system biofilm as revealed by 454-pyrosequencing analysis and the effect of microbial biofilm communities on raw water quality[J]. Bioresource Technology, 2013, 148: 189-195. DOI:10.1016/j.biortech.2013.08.109 |
| [25] | Xia Y, Kong Y H, Thomsen T R, et al. Identification and ecophysiological characterization of epiphytic protein-hydrolyzing Saprospiraceae ("Candidatus Epiflobacter" spp.) in activated sludge[J]. Applied and Environmental Microbiology, 2008, 74(7): 2229-2238. DOI:10.1128/AEM.02502-07 |
| [26] | Lu H J, Chandran K, Stensel D. Microbial ecology of denitrification in biological wastewater treatment[J]. Water Research, 2014, 64: 237-254. DOI:10.1016/j.watres.2014.06.042 |
| [27] |
曹雁.厌氧氨氧化与反硝化协同脱氮及微生物特性研究[D].广州: 华南理工大学, 2018. Cao Y. Study on performance and microbial characteristics of co-existence of anammox and denitrification for simultaneous nitrogen removal[D]. Guangzhou: South China University of Technology, 2018. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y3166923 |
| [28] | Kuenen J G. Anammox bacteria:from discovery to application[J]. Nature Reviews Microbiology, 2008, 6(4): 320-326. DOI:10.1038/nrmicro1857 |
| [29] | Kartal B, van Niftrik L, Keltjens J T, et al. Anammox-growth physiology, cell biology, and metabolism[J]. Advances in Microbial Physiology, 2012, 60: 211-262. DOI:10.1016/B978-0-12-398264-3.00003-6 |
| [30] | Gaul T, Märker S, Kunst S. Start-up of moving bed biofilm reactors for deammonification:the role of hydraulic retention time, alkalinity and oxygen supply[J]. Water Science & Technology, 2003, 52(7): 127-133. |
| [31] | van der Star W R L, Abma W R, Blommers D, et al. Startup of reactors for anoxic ammonium oxidation:experiences from the first full-scale anammox reactor in Rotterdam[J]. Water Research, 2007, 41(18): 4149-4163. DOI:10.1016/j.watres.2007.03.044 |
 2019, Vol. 40
2019, Vol. 40


