2. 北京工业大学城镇污水深度处理与资源化利用技术国家工程实验室, 北京 100124
2. National Engineering Laboratory for Advanced Municipal Wastewater Treatment and Reuse Technology, Beijing University of Technology, Beijing 100124, China
氮元素的大量排放所导致的自然水体污染已经日益成为人们关注的重点, 传统生物脱氮工艺能耗高, 并且产生的大量剩余污泥处置困难.研究人员将目光投向新型生物脱氮工艺技术, 在短程硝化反硝化(short-cut nitrification and denitrification, SNAD)和厌氧氨氧化(anaerobic ammonium oxidation, ANAMMOX)等脱氮技术取得了进展[1, 2].厌氧氨氧化是指在厌氧或缺氧的条件下, 厌氧氨氧化菌(anaerobic ammonium oxidizing bacteria, AnAOB)以亚硝酸盐为电子受体, 将氨氮转为氮气或少量硝酸盐的过程[3].相比于传统工艺, ANAMMOX工艺无需供氧, 无需添加有机碳源, 同时污泥产量减少了90%, 是目前已知的最简洁和最经济的生物脱氮途径之一[1].
AGS具有良好的沉降性能, 抗冲击负荷能力强, 可有效减少细菌流失, 保证反应器高效稳定运行.但AnAOB作为自养型细菌, 生长缓慢, 世代周期长达11 d, 且对生存环境要求较严格[4], 这给驯化FAS和培养AGS带来极大困难.因此, 如何加快培养AGS, 成为了国内外研究的热点. López等[5]用高负荷废水培养得到AGS, 但时间较长, 大于200 d;唐崇俭等[6]通过接种比厌氧氨氧化活性(specific ANAMMOX activity, SAA)为1.9 kg·(kg·d)-1的FAS, 经过230 d的稳定培养, 得到粒径为2~4 mm的AGS;丛岩等[7]把好氧硝化颗粒污泥与ANAMMOX生物膜作为接种污泥, 经过80 d得到平均直径0.556 mm的成熟颗粒污泥, 但总氮去除负荷较低;陈光辉等[8]通过包埋固定化技术, 以ANAMMOX包埋菌颗粒代替ANAMMOX污泥, 在短时间内成功启动ANAMMOX;刘晓宇等[9]利用反硝化颗粒污泥掺杂少量ANAMMOX污泥, 反应器连续运行60 d, 成功培养出AGS.
这些研究表明通过不同的培养方法, ANAMMOX污泥均可实现颗粒化, 但存在不同的缺陷, 如培养过程耗时较长或颗粒污泥杂质和杂菌较多, 不利于实际工程的应用.本研究利用少量ANAMMOX污泥为接种污泥, 在反应器中放置生物流离球, 逐步提高进水基质浓度和缩短水力停留时间(hydraulic retention time, HRT), 旨在启动ANAMMOX反应器, 进一步加快培养AGS.同时, 为了研究AGS的脱氮性能, 以基质抑制动力学模型为基础, 分析其动力学特性, 以期为实际的工程优化提供理论依据.
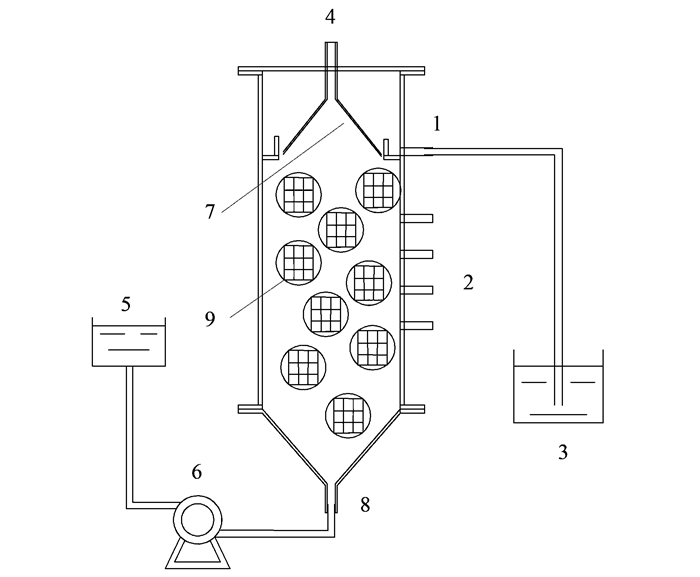
1 材料与方法 1.1 实验装置及运行方式采用UASB完成主体实验, 如图 1所示.反应器由有机玻璃制成, 上部设有三相分离器, 外面用锡纸包裹以避光, 底部进水, 上部出水.反应器的有效容积为8 L, 进水pH控制在7.4~8.0, 水温控制在32℃, 在不同阶段控制不同HRT.本实验所用生物流离球为聚乙烯材质, 直径80 mm, 球内填充大孔径黑色长方体海绵, 可有效截留微生物, 防止菌体流失, 加快反应器启动.
|
1.出水口; 2.取样口; 3.出水桶; 4.排气口; 5.进水桶; 6.蠕动泵; 7.三相分离器; 8.进水口; 9.生物流离球 图 1 ANAMMOX UASB反应器示意 Fig. 1 Schematic diagram of ANAMMOX UASB reactor system |
本实验主要分为两个阶段:①AnAOB富集阶段.启动UASB反应器的接种污泥共计1 L, 取自实验室SBR反应器内长期稳定运行的FAS, 反应器初始阶段污泥浓度(mixed liquid suspended solids, MLSS)为750 mg·L-1. ②AnAOB快速增殖与颗粒化阶段.生物流离球被放置在UASB反应器内, 水体可以均匀地从流离球内部经过, 从而保证AnAOB被流离球截留并附着在流离球内部, 实现AnAOB的增殖和AGS的快速形成.
1.2 实验水质UASB反应器和动力学测定的实验用水采用人工模拟配水, 主要成分组成见表 1[10].同时补充微量元素(微量元素Ⅰ、Ⅱ事先配成浓溶液, 配水时按1 mg·L-1取用), 微量元素Ⅰ的主要成分为(g·L-1):EDTA 15、MnCl2·4H2O 0.99、CuSO4·5H2O 0.25、(NH4)6MoO·4H2O 0.16、H3BO3 0.011、NaSeO3·5H2O 0.159 6、ZnSO4·7H2O 0.43、NiCl2·6H2O 0.19、CoCl2·6H2O 0.24;微量元素Ⅱ的主要成分为(g·L-1):EDTA 5、FeSO4·7H2O 5[11].由NH4Cl和NaNO2提供NH4+-N和NO2--N, 浓度按需所配, 比例为1:1.32[12].
|
|
表 1 模拟废水的主要成分组成 Table 1 Main components of simulated wastewater |
1.3 指标测定方法
NH4+-N:纳氏试剂分光光度法[13];NO2--N:N-(1-萘基)-乙二胺分光光度法[13];NO3--N:麝香草酚分光光度法[13];污泥浓度MLSS:重量法[13]. pH:雷磁PHS-3C型pH计;温度与溶解氧(dissolved oxygen, DO)值:雷磁便携式溶解氧测定仪;颗粒污泥粒径:奥利巴斯CX-31显微镜配合目镜十字标尺;扫描电镜(SEM):JSM-6390LV.
1.4 动力学测定从反应器中取适量直径1~3 mm的AGS分装在两个300 mL的锥形瓶中, 并将锥形瓶放在35℃恒温振荡箱中培养, 控制摇床转速为120 r·min-1.进水NH4+-N和NO2--N按实验要求调整浓度, 其他同表 1.进水之后, 用氮气吹脱3 min, 以去除锥形瓶内的DO.定时取样测定水中NH4+-N和NO2--N浓度, 锥形瓶内初始污泥浓度为1 020 mg·L-1.由于实验时间较短, 可假设在实验期间污泥浓度无较大变化, 由基质浓度降解曲线, 计算出AGS的SAA[6], 单位为kg·(kg·d)-1.
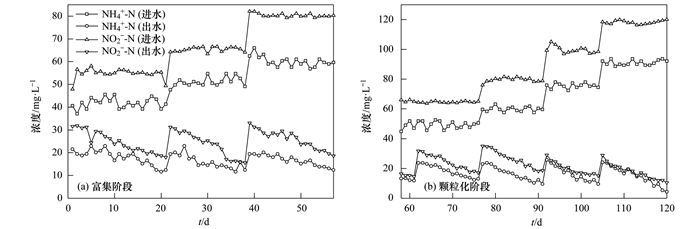
2 结果与分析 2.1 ANAMMOX启动 2.1.1 AnAOB富集阶段反应器接种阶段, 加入1 L接种污泥, 设置NH4+-N和NO2--N的初始进水浓度为40 mg·L-1和55 mg·L-1, HRT控制在12 h.如图 2(a)所示, 反应器运行20 d, NH4+-N和NO2--N出水浓度降低至10~20 mg·L-1, 提高进水基质浓度, 使NH4+-N和NO2--N的进水浓度分别达到50 mg·L-1和65mg·L-1, 保持较高的负荷, 促进AnAOB的生长和繁殖.当系统运行至第38 d, 再次提高进水基质浓度, 使NH4+-N和NO2--N的进水浓度分别达到60 mg·L-1和80 mg·L-1.当系统运行至第57 d, NH4+-N和NO2--N的出水浓度降低至10~20 mg·L-1, 完成AnAOB的富集.此时, 反应器内的MLSS=1 723 mg·L-1, 较培养初期的750 mg·L-1有大幅度提高.提高进水基质浓度的初期, 出水浓度出现跃升现象, 这是由于反应器内微生物量较少, 处理能力不足造成的, 经过一段时间的运行, 系统中微生物增殖, 去除负荷增加, NH4+-N和NO2--N去除率提高.
|
图 2 运行过程中NH4+-N和NO2--N的浓度变化曲线 Fig. 2 Concentration curves of NH4+-N and NO2--N during operation |
系统运行至第58 d, 在反应器内加入生物流离球填料.由图 2(b)可知, 反应器运行前4 d, 继续保持HRT=12 h, NH4+-N和NO2--N的初始浓度分别控制在50 mg·L-1和65 mg·L-1左右, NH4+-N和NO2--N的出水浓度均在10~15 mg·L-1.将HRT缩短至6 h, NH4+-N和NO2--N的出水浓度跃升到23.6 mg·L-1和31.8 mg·L-1.第76 d, NH4+-N和NO2--N的出水浓度降低至10~20 mg·L-1时, 提高NH4+-N和NO2--N的进水至60 mg·L-1和80 mg·L-1;第91天, NH4+-N和NO2--N的出水浓度降低至较低浓度, 再次提高NH4+-N和NO2--N的进水浓度至75 mg·L-1和100 mg·L-1, 第104 d, 出水浓度分别降低至9.5 mg·L-1和18.6 mg·L-1.第105 d时, NH4+-N和NO2--N的进水浓度提高至90 mg·L-1和120 mg·L-1, 第120 d, NH4+-N的出水浓度为2~3mg·L-1, NO2--N的出水浓度稳定在8~10 mg·L-1, NO3--N的出水浓度稳定在15~25 mg·L-1.
流离球加入到反应器之后, 每隔两周观察外观和污泥形态.第71 d [图 3(a)], 白色塑料上已经附着了红棕色AnAOB, 黑色海绵附着生长不明显;反应器运行至第85 d [图 3(b)], 塑料球表面已经大面积附着暗红色AnAOB, 形成一层生物膜, 黑色海绵上的AnAOB聚集为直径0.2~0.5 mm的圆形颗粒, 颜色为暗红色;运行至第99 d [图 3(c)], 塑料球表面的AnAOB继续生长, 黑色海绵的内部孔隙几乎被AnAOB充满, 颗粒直径增长至0.3~0.8 mm;第113 d[图 3(d)], AnAOB的总量明显增多, 颗粒直径增长至0.5~1.5 mm, 少量颗粒达到2 mm;第127 d [图 3(e)], 白色塑料球表面覆盖了厚度0.1~0.3 mm的生物膜, 黑色海绵孔隙内充满了AnAOB, 颗粒直径达到1.0~3.0 mm.

|
图 3 生物琉璃球外观变化 Fig. 3 Changes in appearance of the filler |
把黑色海绵部分从流离球中取出, 如图 4(a)所示, 海绵的尖端挂载着红色的AGS;散落在反应器底部的AnAOB也生长为直径1.0~3.0 mm的AGS. AGS预处理[14]之后, 做扫描电镜, 在5 000和10 000倍条件下得到颗粒污泥电镜图[图 4(c)].有研究表明, AnAOB是具有红色细胞色素的一类细菌, AnAOB比例越高, AGS呈现的红色越深[15]. 图 4(b)中, AGS的颜色呈暗红色, 形状近似圆形, 颗粒表面光滑;图 4(c)中, 球形的细菌占据了绝大多数, 细胞壁上有呈“火山口状”的两面凹陷, 这是较为典型的AnAOB[16].因此, 可以说明颗粒污泥中AnAOB已经占据优势地位. AGS内部布满孔隙和无细胞的通道网络结构, 微小聚集体通过蛋白质和多糖形成的胞外聚合物(extracellular polymeric substances, EPS)[15]、丝状菌[17]等骨架聚合在一起形成球状颗粒污泥.

|
图 4 AGS外观图和扫描电镜图 Fig. 4 Appearance diagram and SEM image of AGS |
用于动力学测试的AGS取自本研究的UASB反应器中生长良好的颗粒污泥, 直径1~3 mm.取出的颗粒污泥, 在均匀状态下, 分装在300 mL的锥形瓶中, MLSS=1 020 mg·L-1.初始NH4+-N和NO2--N浓度都为70 mg·L-1[18], 分别提高NH4+-N和NO2--N的进水浓度, 用于完成NH4+-N和NO2--N对ANAMMOX反应的影响研究.
ANAMMOX动力学过程受NH4+-N浓度和NO2--N浓度两个因素的限制, 进水基质浓度过高, 会抑制微生物的生长和代谢.常用基质抑制动力学模型——Haldane模型[19, 20]研究AGS动力学过程.

|
(1) |
式中, V为反应速率, Vmax为最大反应速率, 单位为kg·(kg·d)-1;S为基质浓度, Km为半速率常数、Ki为半抑制常数, 单位为mmol·L-1.
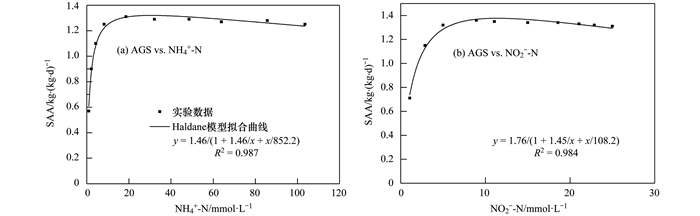
如图 5所示, 通过Origin Pro 2017, 以基质浓度为横坐标, 以SAA为纵坐标, 对表 2实验数据进行Haldane模型拟合, 得到AGS对NH4+-N [图 5(a)]和NO2--N[图 5(b)]的动力学方程.拟合常数R2分别为0.987和0.984, 表现出良好的相关性, 说明Haldane模型可以较好地描述两种基质对ANAMMOX的抑制动力学行为.
|
图 5 颗粒污泥的动力学特性 Fig. 5 Kinetic characteristics of AGS |
|
|
表 2 基质浓度对ANAMMOX反应的影响 Table 2 Effects of substrate concentration on ANAMMOX |
由图 5(a)可知, 当NH4+-N为抑制剂时, 得到AGS的最大氨反应速率(SAA-NH4+-N)为1.46 kg·(kg·d)-1, AGS对氨的半速率常数(Km)为1.46 mmol·L-1, 氨对AGS的半抑制常数(Ki)为852.2 mmol·L-1;由图 5(b)可知, 当NO2--N为抑制剂时, 得到AGS的最大亚硝酸盐反应速率(SAA-NO2--N)为1.76 kg·(kg·d)-1, AGS对亚硝酸盐的半速率常数(Km)为1.45mmol·L-1, 亚硝酸盐对AGS的半抑制常数(Ki)为108.2 mmol·L-1.动力学实验结果表明, 低浓度时, NH4+-N和NO2--N浓度的升高, 能促进厌氧氨氧化的进行;高浓度时, NH4+-N和NO2--N浓度的继续升高, 会抑制厌氧氨氧化的反应速率, 且高浓度NO2--N更容易对厌氧氨氧化反应产生抑制作用[21, 22].
3 讨论影响厌氧氨氧化颗粒污泥形成的因素有很多, 如运行方式、接种污泥、废水性质、污泥负荷和HRT等, 最主要的因素在于AnAOB自身缓慢的繁殖速度且对环境较为敏感, 以及在系统中的大量流失.于鹏飞等[23]考察不同氮负荷及冲击条件下AGS可颗粒化程度, 发现保持较高的氮负荷和上升流速, 有助于污泥颗粒化, 但条件较难控制.李惠娟等接种A/A/O系统的活性污泥, 在经历停滞期、提高期和稳定期之后, 用时160 d才完成厌氧氨氧化的启动和颗粒污泥的培养[24].
第一阶段少量的FAS投加到反应器之后, 系统运行前10 d, 出水的NH4+-N和NO2--N的浓度较不稳定, 主要是AnAOB处于适应阶段.在转移到反应器的过程中, AnAOB接触大量的氧气;进入反应器之后, 反应器内存在少量溶解氧, 都会抑制AnAOB对NH4+-N和NO2--N的处理能力.不稳定的生存条件, 导致部分细菌死亡, 出现菌体自溶现象[25], 死亡的菌体释放出NH4+-N, 也会导致NH4+-N和NO2--N的出水浓度不稳定.经过57 d的富集培养, 反应器出水NH4+-N和NO2--N的浓度同步降低, 去除率分别达到83.3%和75%, 去除的NH4+-N:去除的NO2--N:生成的NO3--N=1:1.2:0.2, 与理论上的1:1.32:0.26较为接近.因此可以认为在第一阶段结束时, UASB反应器内ANAMMOX工艺运行良好.
第二阶段, AnAOB开始在填料上附着生长和繁殖.加入填料之后, AnAOB几乎均匀分布在反应器的内部, 很大程度上改善了基质的传质速率, 使NH4+-N和NO2--N的去除率迅速升至78%左右.接着将HRT缩短为6 h, NH4+-N和NO2--N的去除率回落到50%左右, 说明在AnAOB量不足和未形成颗粒污泥的情况下, HRT对出水水质影响较大.运行至第120 d, NH4+-N和NO2--N的进水浓度分别为90 mg·L-1和120 mg·L-1, 去除的NH4+-N:去除的NO2--N:生成的NO3--N=1:1.23:0.27.氨氮的去除率为97%, 亚氮的去除率为91%~95%, 总氮的去除率达到85%以上, 总氮容积负荷为0.72 kg·(m3·d)-1, 可以说明ANAMMOX工艺成功启动.
AnAOB在填料上以生物膜形式生长良好, 能够均匀地分布在流离球内部, 形成红色的生物膜和颗粒污泥杂菌和杂质较少.于英翠等[26]利用高密度聚乙烯和生物酶作为增强成分的环形填料, 启动ANAMMOX, 但形成的生物膜颜色暗黄, 推测杂菌和杂质较多, AnAOB量不足.相比而言, 以填充了大孔径海绵的流离球作为生物膜载体, 利用悬浮物在流体的流动中, 总是由流速快的一侧向流速慢的一侧集聚的原理, 能够让AnAOB在流离球内停留聚集[27].在菌群生长过程中, 细菌会释放出一种被称作自诱导物(auto-inducer, Ai)的胞外信号因子, 当信号因子在其微环境中达到一个阈值时, 信号被菌群接收并开始调节特定基因的表达, 这一过程称为群体感应(quorum sensing, QS)[28, 29]. AnAOB在流离球内聚集之后, Ai的浓度迅速升高, 诱发群体感应, 促进EPS的形成, 强化菌群的生物聚团行为[30].丛岩等[7]和刘晓宇等[9]利用硝化颗粒和反硝化颗粒, 在80 d和60 d内培养出AGS, 虽用时较短, 但硝化颗粒和反硝化颗粒本身就很难获得, 不利于大规模应用;李海玲等[31]通过调控温度和沉降时间, 30 d就实现了ANAMMOX的启动和AGS的快速培养, 但颗粒的平均直径仅0.430 mm, 总氮容积负荷仅为0.24 kg·(m3·d)-1, 低于本实验的0.72 kg·(m3·d)-1.用生物流离球为聚乙烯材料, 化学稳定性好, 耐酸碱侵蚀, 成本低廉, 有较好的应用价值.在反应器中加入生物流离球, 能够更好地启动ANAMMOX, 加快AGS的形成, 提高AnAOB的生物活性和脱氮效率.
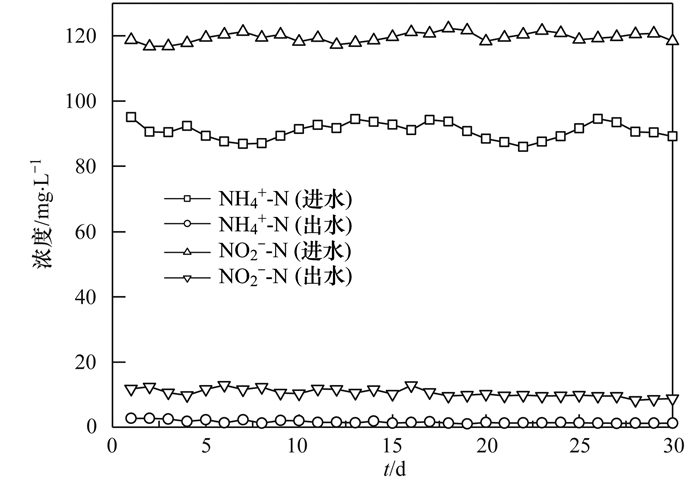
为考察反应器长期的运行效果, 在AGS培养成功之后, 继续监测反应器的进出水数据, 见图 6.保持反应器NH4+-N和NO2--N的进水浓度为90 mg·L-1和120 mg·L-1, HRT为6 h;NH4+-N和NO2--N的出水浓度为1~2 mg·L-1和8~9 mg·L-1, NO2--N的出水浓度较AGS培养成功的初期有少量下降, 脱氮能力进一步提高.
|
图 6 NH4+-N和NO2--N的浓度变化曲线 Fig. 6 Concentration curves of NH4+-N and NO2--N |
本实验与其他研究人员对AGS和絮状污泥的动力学特性的研究结果相比见表 3, 发现动力学特性参数差别较大. Tang等[32]利用UASB工艺, 在高负荷条件下, 通过缩短HRT培育得到AGS;祖波等[33]利用膨胀颗粒污泥床(EGSB)中培育好的颗粒污泥完成动力学特性的研究, 陈光辉等[8]以水性聚氨酯为材料, 得到AnAOB包埋颗粒.不同的运行方式和控制条件, 会影响颗粒污泥的组成成分, 进而影响动力学特性的测定.本实验的AGS最大氨反应速率和最大亚硝酸盐反应速率明显高于FAS, 但和其他AGS的最大反应速率略有差异, 分析其原因主要是由于颗粒污泥的菌种组分不同, 包括胞外聚合物含量不同, 影响了SAA的测定结果.较高的反应速率能够促进基质的降解速度, 能促进AnAOB的生长和繁殖, 有利于ANAMMOX的进行.本实验培养的AGS对氨和亚硝酸盐的半速率常数低于包埋颗粒和FAS, 高于其他研究中的AGS.结合AGS电镜图[图 4(c)], EPS中有大小不一的孔隙, 表明附着在塑料大孔球上生长的AGS具有良好的传质效果, 对基质的亲和力也相对较大, 更容易在竞争环境中竞争基质.氨对本实验AGS的半抑制常数远高于包埋颗粒和FAS, 略高于其他研究中的AGS;亚硝酸盐对AGS的半抑制常数远高于包埋颗粒、FAS和其他AGS.表明本实验培养的AGS能承受更高的NH4+-N和NO2--N浓度, 具有更强耐冲击负荷能力, 有助于ANAMMOX反应器的高效、稳定运行.
|
|
表 3 不同ANAMMOX污泥的动力学特性 Table 3 Comparison of kinetic parameters of different ANAMMOX sludge contents |
4 结论
(1) 接种少量FAS对加快ANAMMOX的启动作用是明显的, 可以跳过污泥的驯化阶段, 直接进入AnAOB的富集阶段, 缩短ANAMMOX的启动时间.经过120 d的培养, 氨氮的去除率为97%~99%, 亚氮的去除率为91%~95%, 总氮的去除率达85%以上, 总氮容积负荷为0.72 kg·(m3·d)-1.
(2) 加入生物流离球, 为AnAOB的生长提供了载体, 使其聚集在流离球内. AnAOB均匀分布在反应器内, 提高基质的传质效率, 进而提高脱氮效率.同时, AnAOB分泌的自我诱导物Ai达到一定浓度之后, 强化菌群的生物聚团行为, 加快颗粒污泥的形成.经过127 d, 培养出直径1~3 mm的厌氧氨氧化颗粒污泥, 脱氮效率良好.
(3) 动力学结果表明, AGS对氨和亚硝酸盐的最大反应速率分别为1.46 kg·(kg·d)-1和1.76 kg·(kg·d)-1, 高于FAS和大部分AGS, 有更高的脱氮效率.对氨和亚硝酸盐的半抑制速率(Ki)分别是852.2 mmol·L-1和108.2 mmol·L-1, 高于FAS和其他AGS的对应值, 能承受更高的基质浓度, 有利于反应器的稳定运行.
| [1] | Ni L F, Wang Y Y, Lin X M, et al. Enhancement of the adaptability of anammox granules to zinc shock by appropriate organic carbon treatment[J]. Bioresource Technology, 2018, 268: 496-504. DOI:10.1016/j.biortech.2018.08.035 |
| [2] | Yang S, Yang F L. Nitrogen removal via short-cut simultaneous nitrification and denitrification in an intermittently aerated moving bed membrane bioreactor[J]. Journal of Hazardous Materials, 2011, 195: 318-323. DOI:10.1016/j.jhazmat.2011.08.045 |
| [3] | Ma H Y, Niu Q G, Zhang Y L, et al. Substrate inhibition and concentration control in an UASB-Anammox process[J]. Bioresource Technology, 2017, 238: 263-272. DOI:10.1016/j.biortech.2017.04.017 |
| [4] | Wang T, Zhang H M, Gao D W, et al. Comparison between MBR and SBR on anammox start-up process from the conventional activated sludge[J]. Bioresource Technology, 2012, 122: 78-82. DOI:10.1016/j.biortech.2012.02.069 |
| [5] | López H, Puig S, Ganigué R, et al. Start-up and enrichment of a granular anammox SBR to treat high nitrogen load wastewaters[J]. Journal of Chemical Technology and Biotechnology, 2008, 83(3): 233-241. DOI:10.1002/jctb.1796 |
| [6] |
唐崇俭, 熊蕾, 王云燕, 等. 高效厌氧氨氧化颗粒污泥的动力学特性[J]. 环境科学, 2013, 34(9): 3544-3551. Tang C J, Xiong L, Wang Y Y, et al. Kinetic characteristics of high-rate Anammox granules[J]. Environmental Science, 2013, 34(9): 3544-3551. |
| [7] |
丛岩, 黄晓丽, 王小龙, 等. 厌氧氨氧化颗粒污泥的快速形成[J]. 化工学报, 2014, 65(2): 664-671. Cong Y, Huang X L, Wang X L, et al. Faster formation of Anammox granular sludge[J]. CIESC Journal, 2014, 65(2): 664-671. DOI:10.3969/j.issn.0438-1157.2014.02.042 |
| [8] |
陈光辉, 李军, 邓海亮, 等. 包埋菌启动厌氧氨氧化反应器及其动力学性能[J]. 化工学报, 2015, 66(4): 1459-1466. Chen G H, Li J, Deng H L, et al. Performance and kinetic characteristics of immobilized granules on start-up of Anammox bioreactor[J]. CIESC Journal, 2015, 66(4): 1459-1466. |
| [9] |
刘晓宇, 王思慧, 薛耀琦, 等. 厌氧氨氧化颗粒污泥的快速培养与形成机理[J]. 环境工程学报, 2016, 10(3): 1223-1227. Liu X Y, Wang S H, Xue Y Q, et al. Rapid cultivation and formation mechanism of anammox granular sludge[J]. Chinese Journal of Environmental Engineering, 2016, 10(3): 1223-1227. |
| [10] |
冯平, 周少奇. 常温下厌氧氨氧化生物膜反应器的启动研究[J]. 环境科学与技术, 2010, 33(6): 19-22, 34. Feng P, Zhou S Q. Experimental study on start-up of UASB-Anammox biofilm reactor at ordinary temperature[J]. Environmental Science & Technology, 2010, 33(6): 19-22, 34. |
| [11] | Strous M, van Gerven E, Zheng P, et al. Ammonium removal from concentrated waste streams with the anaerobic ammonium oxidation (Anammox) process in different reactor configurations[J]. Water Research, 1997, 31(8): 1955-1962. DOI:10.1016/S0043-1354(97)00055-9 |
| [12] |
曹天昊, 王淑莹, 苗蕾, 等. 不同基质浓度下SBR进水方式对厌氧氨氧化的影响[J]. 中国环境科学, 2015, 33(8): 2334-2341. Cao T H, Wang S Y, Miao L, et al. Influence of feeding modes on anammox under different influent substrate concentration in SBR[J]. China Environmental Science, 2015, 33(8): 2334-2341. DOI:10.3969/j.issn.1000-6923.2015.08.011 |
| [13] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002. |
| [14] | Chen G H, Li J, Tabassum S, et al. Anaerobic ammonium oxidation (ANAMMOX) sludge immobilized by waterborne polyurethane and its nitrogen removal performance-a lab scale study[J]. RSC Advances, 2015, 5(32): 25372-25381. DOI:10.1039/C4RA14451A |
| [15] |
丁爽, 郑平, 张萌, 等. 厌氧氨氧化菌群体感应系统研究[J]. 生态学报, 2012, 32(8): 2581-2587. Ding S, Zheng P, Zhang M, et al. Quorum sensing in anaerobic ammonium oxidation bacteria[J]. Acta Ecologica Sinica, 2012, 32(8): 2581-2587. |
| [16] |
沈冰洁, 王荣昌. 厌氧氨氧化菌富集培养技术关键与影响因素[J]. 工业水处理, 2013, 33(10): 6-10. Shen B J, Wang R C. Technical essentials and influencing factors of the enrichment of anaerobic ammonia oxidation(ANAMMOX) bacteria[J]. Industrial Water Treatment, 2013, 33(10): 6-10. |
| [17] | Fan N S, Wang R F, Qi R, et al. Control strategy for filamentous sludge bulking:bench-scale test and full-scale application[J]. Chemosphere, 2018, 210: 709-716. DOI:10.1016/j.chemosphere.2018.07.028 |
| [18] |
郑照明, 李军, 马静, 等. SNAD生物膜厌氧氨氧化活性的氨氮抑制动力学研究[J]. 中国环境科学, 2016, 36(10): 2957-2963. Zheng Z M, Li J, Ma J, et al. The kinetic coefficients of ammonium inhibition on the Anammox activity of SNAD biofilm[J]. China Environmental Science, 2016, 36(10): 2957-2963. DOI:10.3969/j.issn.1000-6923.2016.10.015 |
| [19] |
李伟刚, 于德爽, 李津. ASBR反应器厌氧氨氧化脱氮Ⅱ:反应动力学[J]. 中国环境科学, 2013, 33(12): 2191-2200. Li W G, Yu D S, Li J. Nitrogen removal in the Anammox sequencing batch reactor Ⅱ:kinetics characteristics[J]. China Environmental Science, 2013, 33(12): 2191-2200. |
| [20] | Gee C S, Suidan M T, Pfeffer J T. Modeling of nitrification under substrate-inhibiting conditions[J]. Journal of Environmental Engineering, 1990, 116(1): 18-31. DOI:10.1061/(ASCE)0733-9372(1990)116:1(18) |
| [21] | Qin Y J, Han B, Cao Y, et al. Impact of substrate concentration on anammox-UBF reactors start-up[J]. Bioresource Technology, 2017, 239: 422-429. DOI:10.1016/j.biortech.2017.04.126 |
| [22] |
陈永, 张树德, 张杰, 等. 亚硝酸盐氮浓度对厌氧氨氧化反应的影响[J]. 中国给水排水, 2006, 22(17): 74-76. Chen Y, Zhang S D, Zhang J, et al. Influence of nitrite nitrogen concentration on ANAMMOX process[J]. China Water & Wastewater, 2006, 22(17): 74-76. DOI:10.3321/j.issn:1000-4602.2006.17.020 |
| [23] |
于鹏飞, 周明俊, 孙明, 等. 氮负荷对厌氧氨氧化污泥颗粒化的影响[J]. 水处理技术, 2016, 42(7): 25-29, 34. Yu P F, Zhou M J, Sun M, et al. Nitrogen load effects on anaerobic ammonia oxidation granular sludge[J]. Technology of Water Treatment, 2016, 42(7): 25-29, 34. |
| [24] |
李惠娟, 彭党聪, 陈国燕, 等. ANAMMOX的快速启动及EPS在ANAMMOX颗粒污泥中的空间分布[J]. 环境科学, 2017, 38(7): 2931-2940. Li H J, Peng D C, Chen G Y, et al. Fast start-up of ANAMMOX and the spatial distribution of EPS in ANAMMOX granules[J]. Environmental Science, 2017, 38(7): 2931-2940. |
| [25] | Wang Q T, Wang Y L, Lin J B, et al. Selection of seeding strategy for fast start-up of Anammox process with low concentration of Anammox sludge inoculum[J]. Bioresource Technology, 2018, 268: 638-647. DOI:10.1016/j.biortech.2018.08.056 |
| [26] |
于英翠, 高大文, 陶彧, 等. 利用序批式生物膜反应器启动厌氧氨氧化研究[J]. 中国环境科学, 2012, 32(5): 843-849. Yu C Y, Gao D W, Tao Y, et al. Start-up of anammox in a sequencing batch biofilm reactor (SBBR)[J]. China Environmental Science, 2012, 32(5): 843-849. DOI:10.3969/j.issn.1000-6923.2012.05.011 |
| [27] | Wei L P, Lu Y J, Wei J J. Flow separation from a spherical particle in supercritical water[J]. Chemical Engineering Research and Design, 2014, 92(11): 2273-2282. DOI:10.1016/j.cherd.2014.03.007 |
| [28] | Tang X, Liu S T, Zhang Z T, et al. Identification of the release and effects of AHLs in anammox culture for bacteria communication[J]. Chemical Engineering Journal, 2015, 273: 184-191. DOI:10.1016/j.cej.2015.03.045 |
| [29] |
彭永臻, 张向晖, 马斌, 等. 厌氧氨氧化菌群体感应机制[J]. 北京工业大学学报, 2018, 44(3): 449-454. Peng Y Z, Zhang X H, Ma B, et al. Mechanism of quorum sensing in anaerobic ammonium oxidation (Anammox) bacteria[J]. Journal of Beijing University of Technology, 2018, 44(3): 449-454. |
| [30] | Zhao R, Zhang H M, Zhang F, et al. Fast start-up anammox process using Acyl-homoserine lactones (AHLs) containing supernatant[J]. Journal of Environmental Sciences, 2018, 65: 127-132. DOI:10.1016/j.jes.2017.03.025 |
| [31] |
李海玲, 李冬, 张杰, 等. 调控温度和沉降时间实现ANAMMOX颗粒快速启动及其稳定运行[J]. 环境科学, 2019, 40(2): 837-844. Li H L, Li D, Zhang J, et al. Adjusting temperature and settling time to achieve ANAMMOX particles rapid start-up and stable operation[J]. Environmental Science, 2019, 40(2): 837-844. |
| [32] | Tang C J, Zheng P, Wang C H, et al. Performance of high-loaded ANAMMOX UASB reactors containing granular sludge[J]. Water Research, 2011, 45(1): 135-144. DOI:10.1016/j.watres.2010.08.018 |
| [33] |
祖波, 张代钧, 阎青. 颗粒污泥厌氧氨氧化动力学特性及微量NO2的影响[J]. 环境科学, 2008, 29(3): 683-687. Zu B, Zhang D J, Yan Q. Effect of trace NO2 and kinetic characteristics for anaerobic ammonium oxidation of granular sludge[J]. Environmental Science, 2008, 29(3): 683-687. DOI:10.3321/j.issn:0250-3301.2008.03.024 |
 2019, Vol. 40
2019, Vol. 40


