2. 陕西朗正环保科技有限公司, 西安 710065
2. Shaanxi Langzheng Environmental Protection Technology Co., Ltd., Xi'an 710065, China
传统的生物脱氮除磷技术(biological nutrient removal, BNR)作为应用最广泛的污水处理技术之一, 多年来一直备受关注.然而, 低C/N比的城市污水无法满足传统BNR中聚磷菌和反硝化细菌的碳源需求, 从而导致其生物脱氮除磷性能难以进一步提升[1, 2].城市污水处理厂进水碳源不足导致低脱氮除磷效率的难题一直是传统BNR难以突破的瓶颈[3]. “十三五”以来, 随着国家水体治理的稳步推进, 城市污水处理厂势必将面临更为严格的出水水质标准, 这其中氮和磷的降低至关重要.因此, 有必要寻找进一步提升传统BNR脱氮除磷效率的方法, 为实现传统BNR工艺强化脱氮除磷奠定理论与技术基础.
面对进水碳源不足的问题, 传统BNR城市污水处理厂通常的处理对策是外加优质碳源, 如乙酸钠、葡萄糖、甲醇和乙醇等[4].但是, 高昂的药品费用会给城市污水处理厂带来更大的经济负担, 而且外加优质碳源也会产生更多的剩余污泥, 因此, 这种方法在实际应用中受到了一定程度的限制[5].除此之外, 研发能降低碳源需求的新型工艺(短程硝化反硝化、厌氧氨氧化)也是污水处理厂解决进水碳源不足的另一条途径[6, 7].然而, 由于各种原因的限制, 致使新型工艺在国内城市污水处理厂中几乎没有成功应用的案例.
除了上述两种对策以外, 面对城市污水处理厂进水碳源不足的问题, 具有针对性地改造、优化现有污水处理厂结构和工艺也是提高城市污水处理厂脱氮除磷性能的有效途径, 且相对而言更加经济、现实.比如Cao等[8]应用改良四段式分段进水工艺处理低C/N城市污水, 其研究表明当4段A/O的流量分配比例为20:35:35:10时, 系统处理效率达到最佳, 此时系统平均出水COD、NH4+-N、TN和TP浓度分别为33.05、0.58、9.26和0.46mg·L-1;Peng等[9]在三段式分段进水工艺中同样实现了深度脱氮除磷的目的.大量研究表明, 流量分配对生物脱氮除磷性能有着重要的影响[10, 11].然而, 究竟是哪些微生物在发挥着至关重要的作用却鲜见报导.基于此, 本文以低C/N(C/N<5)实际城市生活污水为研究对象, 通过由传统式厌氧段进水向预缺氧和厌氧两段及预缺氧、厌氧和缺氧3段进水方式的转变, 探讨分段进水对改良A2/O工艺脱氮除磷和污泥沉降性能的影响;除此之外, 还分析了不同进水流量分配比例下系统内部分微生物种群结构的变化规律, 以期建立分段进水改良A2/O工艺宏观表现与微观结构的内在关联.
1 材料与方法 1.1 试验装置及运行方式中试反应器的平面示意如图 1所示. A2/O反应器由厚约10 mm的方形钢板焊接制成, 其整体尺寸为长3.7 m, 宽1.5 m, 高2.0 m, 有效容积为7.8 m3;反应器内部设置了数块隔板, 将反应器分割成11块相连的区域, 依次为预缺氧区、厌氧区、缺氧区和好氧区, 体积比为1:1:2:3;通过对隔板上下开孔的方式, 保证了反应器内部污水的流态;反应器不同区域的进水流量通过阀门与电磁流量计控制, 溶解氧浓度通过转子流量计控制.

|
图 1 中试反应器平面示意 Fig. 1 Schematic diagram of the step-feed A2/O process |
中试反应器持续运行120 d, 共分为以下5个阶段:阶段Ⅰ(0~23 d), 传统式厌氧进水;阶段Ⅱ(24~47 d), 预缺氧区与厌氧区两段进水, Q预缺:Q厌=0.3:0.3;阶段Ⅲ(48~71 d), 预缺氧区、厌氧区与缺氧区3段进水, Q预缺:Q厌:Q缺=0.2:0.2:0.2;阶段Ⅳ(72~95 d), Q预缺:Q厌:Q缺=0.1:0.2:0.3;阶段Ⅴ(96~119 d), Q预缺:Q厌:Q缺=0.1:0.1:0.4.整个试验过程中, 总进水流量控制在0.6 m3·h-1, 温度采用恒温器维持在25℃±1℃.反应器的其它工况参数如表 1所示.
|
|
表 1 中试反应器工况控制参数 Table 1 Operational conditions for this study |
1.2 试验用水及接种污泥
中试反应器的进水为西安市某污水处理厂曝气沉砂池的出水, 该城市污水处理厂的处理规模为20万m3·d-1, 采用的污水处理工艺为传统A2/O工艺, 其进水水质如表 2所示.反应器活性污泥取自该污水处理厂好氧池的活性污泥, 污泥维持了较高的活性, 经过30d的驯化与适应, 系统对各项污染物的去除性能趋于稳定状态.
|
|
表 2 中试反应器进水水质 Table 2 Influent characteristics of the pilot-scale step-feed A2/O plant |
1.3 试验指标及测定方法
污泥体积指数(SVI)、混合液悬浮固体浓度(MLSS)、混合液挥发性悬浮固体浓度(MLVSS)、COD、NH4+-N、NO3--N、TN、PO43--P和TP浓度的测定方法均采用标准方法[12]. DO、pH和水温监测均采用哈希公司WTW多功能自动测定仪.快速易生物降解COD组分(Ss)和慢速可生物降解COD组分(Xs)的测定方法见文献[13], 可生物降解COD(BCOD)即为Ss与Xs之和.系统缺氧区活性污泥反硝化速率的测定方法见文献[14]. PAOs/DPAOs的测定方法见文献[2].
不同试验阶段的污泥样均取自该阶段后3 d的好氧池, 经离心机分离去除上清液后置于-20℃保存备用.采用CTAB或SDS方法对样本的基因组DNA进行提取, 之后利用琼脂糖凝胶电泳检测DNA的纯度和浓度, 取适量的样品于离心管中, 使用无菌水稀释样品至1 ng·μL-1.以稀释后的基因组DNA为模板, 根据测序区域的选择, 使用带Barcode的特异引物, New England Biolabs公司的Phusion® High-Fidelity PCR Master Mix with GC Buffer和高效高保真酶进行PCR, 确保扩增效率和准确性.引物对应区域:16S V4区引物(515F和806R);16S V3-V4/16S V4-V5区.使用Thermofisher公司的Ion Plus Fragment Library Kit 48 rxns建库试剂盒进行文库的构建, 构建好的文库经过Qubit定量和文库检测合格后, 使用Thermofisher的Life Ion S5TM或Ion S5TMXL进行上机测序.使用Cutadapt先对reads进行低质量部分剪切, 再根据Barcode从得到的reads中拆分出各样品数据, 截去Barcode和引物序列初步质控得到原始数据, 经过以上处理后得到的reads需要进行去除嵌合体序列的处理, reads序列通过与数据库(gold database)进行比对, 检测嵌合体序列, 并最终去除其中的嵌合体序列, 得到最终的有效数据.
2 结果与讨论 2.1 不同进水流量下污染物的去除性能不同进水比例下系统对污染物的去除效果如图 2所示.从图 2(a)中可以看出, 5种流量分配比例下, 系统各阶段出水COD平均浓度分别为31.74、30.97、30.21、30.10和30.49mg·L-1, 平均去除率分别为88.78%、89.38%、89.06%、89.41%和89.08%, 由此可见不同进水流量比例对系统COD的去除效果影响不大, 系统在5个阶段均有较好的COD去除效率, 这与南彦斌等[2]的研究成果相符.从图 2(b)中可以看出, 系统各阶段出水NH4+-N浓度变化不大, 平均出水浓度分别为1.16、1.15、1.18、1.85和1.23mg·L-1, 平均去除率分别为97.14%、97.32%、97.23%、95.30%和96.82%, 整个试验过程中系统均具有较强的硝化性能, 这与系统好氧区具有充足的水力停留时间(5.25 h)和溶解氧浓度(2~3mg·L-1)直接相关[15].从图 2(c)和2(d)中可以看出, 进水流量分配比例对系统TN和TP的去除均有着较明显的影响.系统出水TN平均浓度分别为14.49、13.48、11.74、9.41和9.05mg·L-1, 平均去除率分别为73.63%、76.17%、79.66%、83.00%和83.68%;系统平均出水TP浓度分别为0.86、0.57、0.72、0.71和1.10mg·L-1, 平均去除率分别为88.04%、91.97%、89.58%、90.09%和81.97%.从以上数据可以看出, 在改良A2/O工艺其它条件不变的情况下, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可以提高系统脱氮除磷的性能;然而, 进一步降低厌氧段进水流量会使PAOs厌氧释磷所需的碳源匮乏, 从而降低系统除磷性能.因此, 从阶段Ⅰ~Ⅴ, TN去除率呈上升的趋势, TP去除率呈先上升后降低的趋势.综合考虑下, 系统在阶段Ⅳ(Q预缺:Q厌:Q缺=0.1:0.2:0.3)对污染物的去除效果达到最佳状态, 此时出水COD、NH4+-N、TN和TP的平均浓度分别为30.10、1.85、9.41和0.71mg·L-1, 去除率分别为89.41%、95.30%、83.00%和90.09%.

|
图 2 各阶段下系统对污染物的去除效果 Fig. 2 Removal performance of nutrients in each stage |
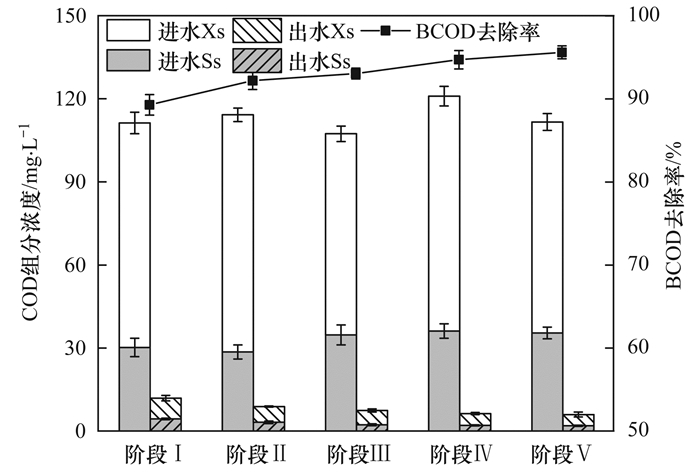
不同进水比例下COD在反应器内的沿程变化如图 3所示.可以看出, 不同阶段下反应器内各个功能区对COD的去除情况变化不大, COD主要在系统厌氧和缺氧区去除.通过物料衡算分析可得, 各阶段下厌氧和缺氧区对COD的去除量分别占COD去除总量的74.56%、78.22%、81.60%、84.58%和86.72%, 因此COD的主要去除途径是通过聚磷菌、反硝化细菌及其他异养型细菌代谢活动的有效利用. 图 4为各阶段系统进出水COD组分浓度变化及BCOD去除情况, 可以看出, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可在一定程度上提高微生物对BCOD的利用效率, 从而改善不同微生物的活性.

|
图 3 各阶段COD的沿程变化规律 Fig. 3 Variation of COD concentrations in different sections of the reactor in each stage |
|
图 4 各阶段进出水BCOD浓度及BOCD去除率 Fig. 4 Concentration and removal efficiency of BCOD in each stage |
通过对各阶段好氧区活性污泥16S rRNA基因测序数据的梳理, 可以发现系统内大量异养型细菌在属水平上的相对丰度都随着试验的进行而得到不同程度的提升, 其中较为公认的且相对丰度变化规律较为明显的6类异养型菌属及所属菌门如表 3所示.可以看出, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可提高原水中碳源的利用效率, 从而使Thauera[16]、Dechloromonas[17]、Candidatus_Accumulibacter[18]、Bacillus[19]、Flavobacterium[20]和Denitratisoma[21]在属水平上的相对丰度得到不同程度提高.阶段Ⅴ的进水模式更有利于这6类异养型菌属的富集, 其相对丰度总和与阶段Ⅰ相比提高了31.23%.因此, 预缺氧、厌氧及缺氧三段进水的模式更有利于这6类异养型菌属的富集, 这与系统较高的COD去除效率密切相关.
|
|
表 3 各阶段下系统内异养型菌属的相对丰度 Table 3 Relative abundance of heterotrophic bacteria at genus level in each stage |
2.3 氮去除机制及相关菌属相对丰度变化
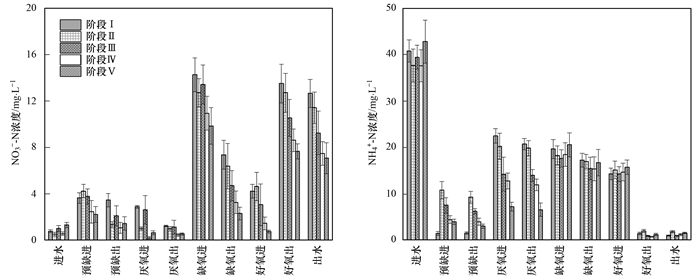
不同进水比例下NO3--N和NH4+-N在反应器内的沿程变化如图 5所示.从图 5(a)中可以看出, NO3--N的去除主要发生在反应器内缺氧区, 且在相同的HRT(3.5 h)内, 缺氧区去除的NO3--N随着其进水流量分配比例的增大而增加.通过反硝化速率测定试验可以得出, 从阶段Ⅰ~Ⅴ系统缺氧区反硝化速率分别为2.14、2.44、3.15、3.56和3.86mg·(g·h)-1.因此, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可极大程度地提高A2/O系统的反硝化性能, 从而保证系统TN的去除效率.从图 5(b)中可以看出, NH4+-N的去除主要发生在反应器内好氧区, 且不同的进水模式对A2/O系统的硝化性能影响不大, 系统在各个阶段均具有较强的硝化性能.结果表明, 氮在系统内的去除主要是通过传统的好氧硝化作用和缺氧反硝化作用完成的, 预缺氧、厌氧及缺氧三段进水的模式可极大程度地提高A2/O系统的反硝化性能, 从而保证了TN的去除效率.
|
图 5 各阶段下NO3--N和NH4+-N的沿程变化规律 Fig. 5 Variations of NO3--N and NH4+-N concentrations in different sections of the reactor in each stage |
通过对各阶段好氧区活性污泥16S rRNA基因测序数据的梳理, 发现了系统内有4类反硝化细菌在属水平上的相对丰度随着试验的进行而得到较明显的提升, 如表 4所示.可以看出, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可提高缺氧区反硝化细菌的代谢活性, 从而使Pseudomonas[22]、Thauera、Denitratisoma和Thermomonas[23]在属水平上的相对丰度得到不同程度提高.阶段Ⅴ的进水模式更有利于这4类反硝化菌属的富集, 其相对丰度总和与阶段Ⅰ相比提高了42.86%.因此, 预缺氧、厌氧及缺氧三段进水的模式更有利于这4类反硝化菌属的富集, 这与系统较强的反硝化性能密切相关.
|
|
表 4 各阶段下系统内反硝化菌属的相对丰度 Table 4 Relative abundance of denitrification bacteria at genus level in each stage |
2.4 磷去除机制及相关菌属相对丰度变化
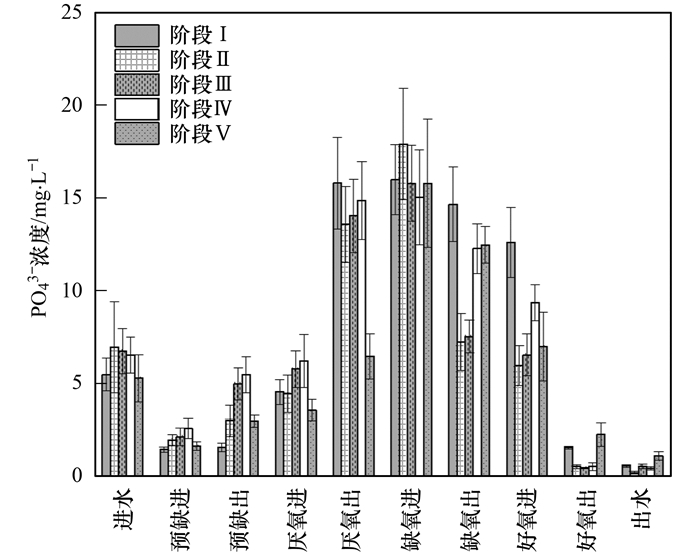
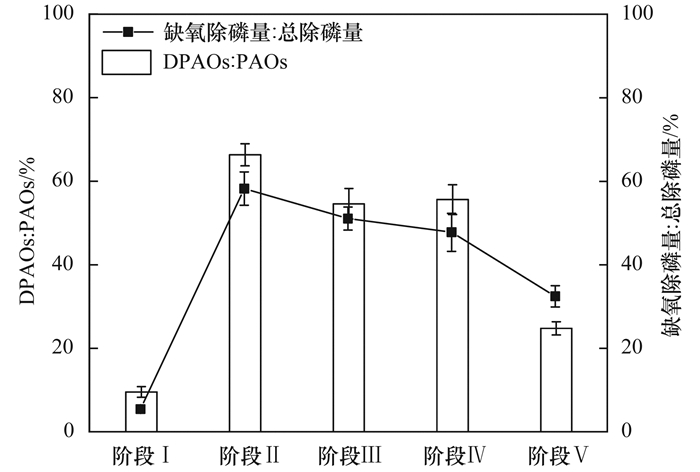
不同进水比例下PO43--P在反应器内的沿程变化如图 6所示.从中可以看出, 在传统厌氧区单段进水的模式下, 系统对PO43--P的去除是通过PAOs的厌氧释磷和好氧摄磷实现的;而预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式将PO43--P的去除途径改变为厌氧释磷和缺氧、好氧摄磷. 图 7为各阶段下DPAOs/PAOs和缺氧除磷量/总除磷量的变化规律, 可以看出多段进水的模式给预缺氧和厌氧段的PAOs分配了更多的碳源, 使其充分释磷并合成大量内碳源, 为反硝化除磷的发生创造了必要条件.在三段进水的模式下, 缺氧段除磷量随着缺氧段进水比例的增加而减少, 这是因为更多的NO3--N被反硝化细菌去除, 降低了DPAOs反硝化除磷所需的电子受体, 从而降低了系统反硝化除磷的性能[24].
|
图 6 各阶段PO43--P沿程变化规律 Fig. 6 Variation of PO43--P concentrations in different sections of the reactor in each stage |
|
图 7 各阶段DPAOs与PAOs和缺氧除磷量与总除磷量比值变化规律 Fig. 7 Variations of DPAOs/PAOs and QDP/QTP in different sections of the reactor in each stage |
通过对各阶段好氧区活性污泥16S rRNA基因测序数据的梳理, 发现了系统内有5类PAOs在属水平上的相对丰度随着试验的进行表现出较明显的规律, 如表 5所示.可以看出, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可提高系统PAOs的代谢活性, 从而使Dechloromonas、Candidatus_Accumulibacter、Acinetobacter[25]、Tetrasphaera[26]和Aeromonas[21]在属水平上的相对丰度得到不同程度提高.阶段Ⅱ的进水模式更有利于这5类PAOs的富集, 其相对丰度总和与阶段Ⅰ和Ⅲ相比分别提高了32.07%和13.99%.因此, 预缺氧、厌氧两段进水的模式更有利于这5类PAOs的富集, 这与系统在阶段Ⅱ较强的除磷性能密切相关.
|
|
表 5 各阶段下系统内聚磷菌属的相对丰度 Table 5 Relative abundance of PAOs at genus level in each stage |
2.5 污泥性状及相关菌属丰度变化
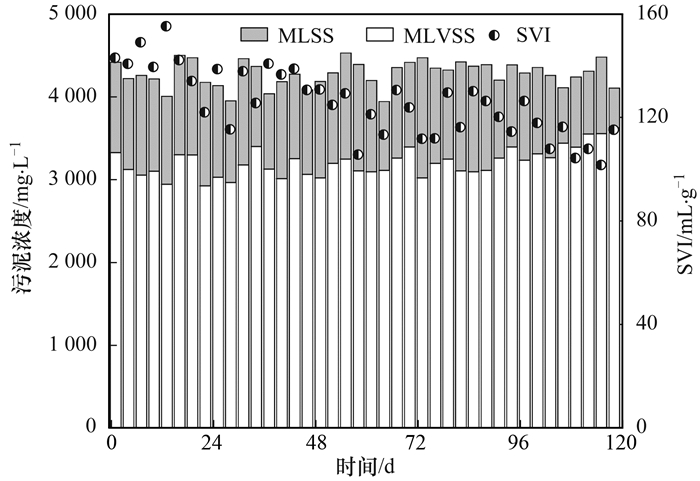
不同进水比例下系统好氧池内MLSS、MLVSS和SVI如图 8所示.据相关资料显示良好的活性污泥SVI一般在130 mL·g-1以下[8].从中可以看出, 随着试验的进行, 系统好氧池活性污泥平均SVI由阶段Ⅰ的140.66 mL·g-1降至阶段Ⅴ的112.09 mL·g-1;与此同时, 好氧池活性污泥平均VSS/TSS由阶段Ⅰ的0.73升至0.84. 结果表明, 预缺氧、厌氧及缺氧三段进水的模式可以改善系统活性污泥的沉降性能与活性.分析原因是三段进水的模式, 增大了系统内底物浓度梯度, 菌胶团能够迅速利用底物并将大量底物以PHA的形式贮存起来, 较高的底物贮存能力有利于抑制丝状菌在好氧条件下的优势生长[27], 从而能够维持系统良好的沉降性能;好氧段适宜的HRT、SRT及DO浓度也为菌胶团的生长提供了有利的生存环境.因此, 随着试验的进行, 系统活性污泥的沉降性能也在逐渐改善, 整个试验阶段均未发生污泥膨胀现象.
|
图 8 各阶段污泥性状 Fig. 8 Characteristics of activated sludge in each stage |
通过对各阶段好氧区活性污泥16S rRNA基因测序数据的梳理, 发现了系统内分别有3类丝状菌和2类菌胶团在属水平上的相对丰度随着试验的进行表现出较明显的规律, 如表 6所示.可以看出, 与传统厌氧区单段进水的模式相比, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式更有利于丝状菌的淘汰、菌胶团的富集, 从而使Thiothrix[28]、Candidatus_Microthrix[29]和Trichococcus[30]在属水平上的相对丰度得到不同程度的降低;Zoogloea[30]和Acidaminobacter[30]在属水平上的相对丰度得到不同程度的提高.因此, 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式更有利于这3类丝状菌的淘汰、2类菌胶团的富集, 这与系统较好的污泥沉降性能密切相关.
|
|
表 6 各阶段下系统内丝状菌属和菌胶团属的相对丰度 Table 6 Relative abundance of filamentous bacteria and zooglea at genus level in each stage |
3 结论
(1) 预缺氧、厌氧两段和预缺氧、厌氧及缺氧三段进水的模式可有效提高A2/O系统的脱氮除磷性能, 最佳进水比例为Q预缺:Q厌:Q缺=0.1:0.2:0.3, 此时出水COD、NH4+-N、TN和TP的平均浓度分别为30.10、1.85、9.41和0.71 mg·L-1, 去除率分别为89.41%、95.30%、83.00%和90.09%.
(2) 多段进水优化了A2/O系统厌氧段和缺氧段中碳源的供给, 从而提高了系统BCOD的去除效率、反硝化脱氮和反硝化除磷性能, 这分别与6类异养型菌属、4类反硝化菌属及5类聚磷菌属的富集密切相关.
(3) 多段进水可改善A2/O系统活性污泥的沉降性能与活性, 系统阶段Ⅴ的SVI和VSS/TSS分别为112.09 mL·g-1、0.84, 这与3类丝状菌属的淘汰和2类菌胶团菌属的富集密切相关.
| [1] | Zhao W H, Huang Y, Wang M X, et al. Post-endogenous denitrification and phosphorus removal in an alternating anaerobic/oxic/anoxic (AOA) system treating low carbon/nitrogen (C/N) domestic wastewater[J]. Chemical Engineering Journal, 2018, 339: 450-458. DOI:10.1016/j.cej.2018.01.096 |
| [2] |
南彦斌, 彭永臻, 曾立云, 等. 分段进水对改良A2/O-BAF双污泥系统反硝化除磷脱氮的影响[J]. 环境科学, 2018, 39(4): 1704-1712. Nan Y B, Peng Y Z, Zeng L Y, et al. Effect of step feed on denitrifying phosphorus and nitrate removal in a modification of the two sludge A2/O-BAF system[J]. Environmental Science, 2018, 39(4): 1704-1712. |
| [3] | Zhang W, Peng Y, Ren N, et al. Improvement of nutrient removal by optimizing the volume ratio of anoxic to aerobic zone in AAO-BAF system[J]. Chemosphere, 2013, 93: 2859-2863. DOI:10.1016/j.chemosphere.2013.08.047 |
| [4] | Gao Y Q, Peng Y Z, Zhang J Y, et al. Biological sludge reduction and enhanced nutrient removal in a pilot-scale system with 2-step sludge alkaline fermentation and A2O process[J]. Bioresource Technology, 2011, 102(5): 4091-4097. DOI:10.1016/j.biortech.2010.12.051 |
| [5] | Zhang T, Wang B, Li X Y, et al. Achieving partial nitrification in a continuous post-denitrification reactor treating low C/N sewage[J]. Chemical Engineering Journal, 2018, 335: 330-337. DOI:10.1016/j.cej.2017.09.188 |
| [6] | Voets J P, Vanstaen H, Verstraete W. Removal of nitrogen from highly nitrogenous wastewaters[J]. Journal (Water Pollution Control Federation), 1975, 47(2): 394-398. |
| [7] | Lackner S, Gilbert E M, Vlaeminck S E, et al. Full-scale partial nitritation/anammox experiences-An application survey[J]. Water Research, 2014, 55: 292-303. DOI:10.1016/j.watres.2014.02.032 |
| [8] | Cao G H, Wang S Y, Peng Y Z, et al. Biological nutrient removal by applying modified four step-feed technology to treat weak wastewater[J]. Bioresource Technology, 2013, 128: 604-611. DOI:10.1016/j.biortech.2012.09.078 |
| [9] | Peng Y Z, Ge S J. Enhanced nutrient removal in three types of step feeding process from municipal wastewater[J]. Bioresource Technology, 2011, 102(11): 6405-6413. DOI:10.1016/j.biortech.2011.03.043 |
| [10] | Zhu G B, Peng Y Z, Wang S Y, et al. Effect of influent flow rate distribution on the performance of step-feed biological nitrogen removal process[J]. Chemical Engineering Journal, 2007, 131(1-3): 319-328. DOI:10.1016/j.cej.2006.12.023 |
| [11] | Ge S J, Peng Y Z, Wang S Y, et al. Enhanced nutrient removal in a modified step feed process treating municipal wastewater with different inflow distribution ratios and nutrient ratios[J]. Bioresource Technology, 2010, 101(23): 9012-9019. DOI:10.1016/j.biortech.2010.06.151 |
| [12] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002. |
| [13] |
金鹏康, 常晋, 王先宝, 等. 不同碳源在污水处理过程中的变化规律研究[J]. 环境科学, 2014, 35(9): 3443-3448. Jin P K, Chang J, Wang X B, et al. Variation of different carbon sources in the sewage treatment process[J]. Environmental Science, 2014, 35(9): 3443-3448. |
| [14] | Jin P K, Wang X B, Wang X C, et al. A new step aeration approach towards the improvement of nitrogen removal in a full scale Carrousel oxidation ditch[J]. Bioresource Technology, 2015, 198: 23-30. DOI:10.1016/j.biortech.2015.08.145 |
| [15] |
李红岩, 张昱, 高峰, 等. 水力停留时间对活性污泥系统的硝化性能及其生物结构的影响[J]. 环境科学, 2006, 27(9): 1862-1865. Li H Y, Zhang Y, Gao F, et al. Effects of hydraulic retention time (HRT) on nitrification performance and microbial community of conventional activated sludge (CAS)[J]. Environmental Science, 2006, 27(9): 1862-1865. DOI:10.3321/j.issn:0250-3301.2006.09.030 |
| [16] | Liu B B, Mao Y J, Bergaust L, et al. Strains in the genus Thauera exhibit remarkably different denitrification regulatory phenotypes[J]. Environmental Microbiology, 2013, 15(10): 2816-2828. |
| [17] | Coates J D, Chakraborty R, Lack J G, et al. Anaerobic benzene oxidation coupled to nitrate reduction in pure culture by two strains of Dechloromonas[J]. Nature, 2001, 411(6841): 1039-1043. DOI:10.1038/35082545 |
| [18] | Kim B C, Kim S, Shin T, et al. Comparison of the bacterial communities in anaerobic, anoxic, and oxic chambers of a pilot A2O process using pyrosequencing analysis[J]. Current Microbiology, 2013, 66(6): 555-565. DOI:10.1007/s00284-013-0311-z |
| [19] |
温洪宇, 杨洋, 贾新宇, 等. 4株细菌处理乳品废水效果的比较研究[J]. 环境科学与技术, 2009, 32(8): 127-129. Wen H Y, Yang Y, Jia X Y, et al. Dairy wastewater treated by 4 bacteria with different methods[J]. Environmental Science & Technology, 2009, 32(8): 127-129. DOI:10.3969/j.issn.1003-6504.2009.08.032 |
| [20] |
胡正嘉, 李科德. 焦化废水活性污泥中的主要细菌类群和优良菌株的选育[J]. 华中农业大学学报, 1991, 10(1): 52-57. Hu Z J, Li K D. Major bacterial genera of activated sludge treated coking wastewaterd and seclection of good strains[J]. Journal of Huazhong Agricultural University, 1991, 10(1): 52-57. |
| [21] |
赵诗惠.基于短程反硝化除磷的ABR-MBR工艺处理生活污水微生物种群分析[D].苏州: 苏州科技大学, 2017. Zhao S H. Analysis of microbial population of denitrifying phosphorus removal from domestic sewage in ABR-MBR process[D]. Suzhou: Suzhou University of Science and Technology, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10332-1018031948.htm |
| [22] | Kong Q X, Wang X W, Jin M, et al. Development and application of a novel and effective screening method for aerobic denitrifying bacteria[J]. FEMS Microbiology Letters, 2006, 260(2): 150-155. DOI:10.1111/j.1574-6968.2006.00306.x |
| [23] |
张楠, 初里冰, 丁鹏元, 等. A/O生物膜法强化处理石化废水及生物膜种群结构研究[J]. 中国环境科学, 2015, 35(1): 80-86. Zhang N, Chu L B, Ding P Y, et al. Enhanced treatment of petrochemical wastewater by using A/O biofilm reactor and analysis of biofilm community[J]. China Environmental Science, 2015, 35(1): 80-86. |
| [24] | Kuba T, Van Loosdrecht M C M, Heijnen J J, et al. Biological dephosphatation by activated sludge under denitrifying conditions pH influence and occurrence of denitrifying dephosphatation in a full-scale waste water treatment plant[J]. Water Science and Technology, 1997, 36(12): 75-82. DOI:10.2166/wst.1997.0433 |
| [25] | Fuhs G W, Chen M. Microbiological basis of phosphate removal in the activated sludge process for the treatment of wastewater[J]. Microbial Ecology, 1975, 2(2): 119-138. |
| [26] | Maszenan A M, Seviour R J, Patel B K C, et al. Three isolates of novel polyphosphate-accumulating gram-positive cocci, obtained from activated sludge, belong to a new genus, Tetrasphaera gen. nov., and description of two new species, Tetrasphaera japonica sp. nov. and Tetrasphaera australiensis sp. nov.[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50(2): 593-603. DOI:10.1099/00207713-50-2-593 |
| [27] |
王杰, 薛同来, 彭永臻, 等. A/O系统中不同缺氧/好氧体积比对活性污泥沉降性能的影响[J]. 中国环境科学, 2016, 36(2): 443-452. Wang J, Xue T L, Peng Y Z, et al. Effect of different anoxic/aerobic volume ratio on activated sludge settleability in A/O system[J]. China Environmental Science, 2016, 36(2): 443-452. DOI:10.3969/j.issn.1000-6923.2016.02.021 |
| [28] | Sarvajith M, Reddy G K K, Nancharaiah Y V. Textile dye biodecolourization and ammonium removal over nitrite in aerobic granular sludge sequencing batch reactors[J]. Journal of Hazardous Materials, 2018, 342: 536-543. DOI:10.1016/j.jhazmat.2017.08.064 |
| [29] | Rossetti S, Christensson C, Blackall L L, et al. Phenotypic and phylogenetic description of an Italian isolate of "Microthrix parvicella"[J]. Journal of Applied Microbiology, 1997, 82(4): 405-410. DOI:10.1046/j.1365-2672.1997.00334.x |
| [30] | Li J R, Burrell P, Seviour E M, et al. The filamentous bacterial morphotype 'Nostocoida limicola' Ⅰ contains at least two previously described genera in the low G+C gram positive bacteria[J]. Systematic and Applied Microbiology, 2000, 23(4): 528-534. DOI:10.1016/S0723-2020(00)80027-2 |
 2019, Vol. 40
2019, Vol. 40


