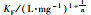2. 清华大学水质与水生态研究中心, 北京 100084;
3. 中国科学院生态环境研究中心, 北京 100085
2. Center for Water and Ecology, Tsinghua University, Beijing 100084, China;
3. Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
20世纪以来由于矿冶、机械制造、化工和电子等工业活动造成的重金属水体污染[1]呈愈演愈烈之势, 常见的重金属包括铅、汞、镉和铬等.其中, 重金属铅离子(Pb2+)可通过皮肤、呼吸道和消化道在人体和动物组织中蓄积, 严重威胁人类健康[2], 控制水体铅污染刻不容缓.目前, 常见的含铅废水处理方法包括化学沉淀法、吸附法、离子交换法等[3].在现有基础上, 开发高效、低成本、高能量利用率的环境友好型重金属去除技术十分关键[4].电吸附, 又称电容去离子技术(capacitive deionization, CDI), 是一种利用外加电压使离子在静电力作用下向带相反电荷的电极移动, 在电极表面形成双电层、富集, 从而实现吸附去除的脱盐技术[5~7].电吸附具有电极可循环再生和无二次污染等优点, 可用于废水中低浓度Pb2+的高效去除.
电极材料是电吸附技术的核心, 良好的电极材料应具有比表面积大、孔道结构丰富、电化学性能稳定等优点.碳材料储量丰富、成本低廉, 在电吸附Pb2+方面表现出巨大的应用潜力[8~10], 种类包括活性炭(activated carbon powder)[11]、碳气凝胶(carbon aerogel)[12]、有序介孔碳(ordered mesoporous carbons)[13]、碳纳米管(carbon nanotubes)[14]和石墨烯(graphene)[15, 16]等.经过掺杂[17]和改善电极表面特性[18, 19]等手段, 多孔碳材料的电容和电吸附性能可进一步提高.醌类化合物分子内的C=O基团可通过氧化还原反应发生蒽醌和氢醌的可逆互变, 从而为体系提供法拉第赝电容[20~22].但是, 因其导电性较差, 比表面积较低, 难以直接用作电极材料.因此, 本研究将电容较大的醌类化合物修饰具有较大比表面积和优异电化学性能的石墨烯材料, 从而强化电吸附Pb2+性能.
本研究通过高温溶剂热法合成了2,6-二氨基蒽醌/石墨烯(DA@rGO)复合电极, 分析其对Pb2+的电吸附性能.对rGO和DA@rGO的形貌、组成表征及电化学性能测试表明, DA修饰明显提高了复合电极赝电容, 导致复合电极饱和吸附量增加.本研究可为开发高性能电极用于电吸附去除水体重金属离子提供依据.
1 材料与方法 1.1 实验材料天然鳞片石墨(青岛天元石墨有限公司)、2,6-二氨基蒽醌(DA, Sigma-Aldrich)、Nafion溶液(质量分数5%, Sigma-Aldrich)、碳纤维布(日本东丽)、N,N-二甲基乙酰胺(DMA)、硫酸(H2SO4)、过硫酸钠(Na2S2O8)、五氧化二磷(P2O5)、高锰酸钾(KMnO4)、硝酸钠(NaNO3)、硝酸铅[Pb(NO3)2]、磷酸二氢钾(KH2PO4)、氢氧化钠(NaOH)和乙醇(CH3CH2OH)等均为分析纯, 购于国药集团化学试剂有限公司.实验用水均为超纯水.
1.2 rGO及DA@rGO复合电极的制备采用改良Hummers法[23]制备氧化石墨(GO), 将制得的GO分散液在水中透析15 d左右至pH呈中性, 稀释至浓度为1 mg·L-1备用.采用高温水热法[24]制备还原氧化石墨烯(rGO)水凝胶:取30 mL GO分散液, 超声30 min, 在鼓风干燥箱中于180℃下反应12 h. 2,6-二氨基蒽醌/石墨烯(DA@rGO)的制备:取30 mg DA溶于1 mL DMA中, 分散均匀后溶于GO分散液, 0℃下超声90 min, 于180℃下反应12 h.将所合成的两种材料分别压片制得rGO和DA@rGO复合电极, 尺寸为25 mm×25 mm×1 mm.
1.3 电化学性质测试电化学测试使用三电极体系, 工作电极为rGO或DA@rGO复合电极, 对电极为铂丝电极, 参比电极为Ag/AgCl电极.工作电极制备方法为:将干燥后的rGO及DA@rGO电极材料分别取5 mg, 溶于由500 μL乙醇, 500 μL超纯水, 5 μL Nafion溶液混合而成的分散液中, 超声30 min, 取5 μL滴加在处理后的玻碳电极上.电解液为1 mol·L-1 H2SO4.
1.4 电吸附Pb2+性能测试采用双电极体系, 将钛钌网作为电极片载体, rGO或DA@rGO作为工作电极, 预处理后的碳纤维布为对电极.配置一定浓度的Pb2+溶液, 以NaNO3为电解液, 研究不同电压下的吸附效果以及最大吸附量.在最优条件下测试DA@rGO电吸附Pb2+去除率, 通电60 min后将工作电极和对电极反接施加反向电压或用0.5 mol·L-1硝酸处理, 使吸附在电极表面的Pb2+脱附.重复电吸附-脱附实验10次, 测试电极的循环稳定性.
1.5 电极材料表征采用场发射扫描电子显微镜(FE-SEM, SU8020, 日本日立)对材料的形貌进行表征, 傅里叶变换红外光谱仪(FT-IR, Nicolet 6700, 美国赛默飞世尔)、X射线粉末衍射仪(XRD, X'Pert PRO MPD, 荷兰帕纳科)、显微共焦拉曼光谱仪(Raman, inVia-Reflex, 英国雷尼绍)、X射线光电子能谱仪(XPS, ESCALAB 250Xi, 美国赛默飞世尔)用于测定材料组成与结构, 比表面积孔隙率分析仪(BET, ASAP 2460, 美国麦克)用于测定材料的比表面积及孔径分布.
2 结果与讨论 2.1 电极表面形貌与组成分析rGO和DA@rGO的SEM照片如图 1所示. rGO表现出结构平整的片状结构, 表面富含褶皱, 同时存在无卷曲的片层相互搭接而形成的大尺寸楔形空隙. DA@rGO呈疏松多孔结构, 表面折叠和褶皱增加, 表明DA修饰增大了材料的比表面积, 利于电解液与电极材料的接触;丰富的孔隙可作为离子缓冲存储层, 减小电解质离子扩散距离, 利于离子在薄层石墨烯中的快速传输.

|
图 1 rGO和DA@rGO的SEM照片 Fig. 1 SEM images of rGO and DA@rGO |
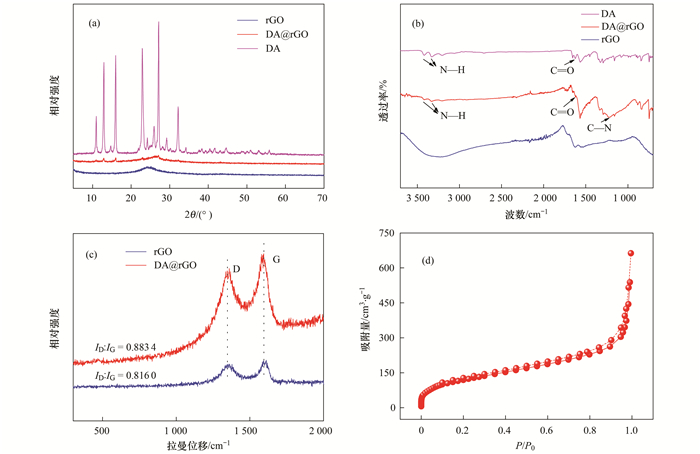
rGO和DA@rGO的XRD谱图如图 2(a)所示, rGO在24.5°出现一个宽化的衍射特征峰, 对应(002)晶面.经过DA修饰后该特征峰移动至25.6°, 表明由于DA修饰, 与还原氧化石墨烯之间产生新的共价键, 使得石墨烯插层的层间距减小.此外, 复合材料DA@rGO在12.98°和16.1°处出现两个微弱的归属于DA的衍射峰, 表明DA分子成功负载于rGO得到复合材料.
|
图 2 rGO和DA@rGO的XRD、FT-IR、拉曼谱图和DA@rGO的氮气吸脱附曲线 Fig. 2 XRD pattern, FT-IR, Raman spectra of rGO and DA@rGO and nitrogen adsorption/desorption isotherm of DA@rGO |
对DA、rGO和DA@rGO的红外光谱进行分析, 进一步验证DA是否成功修饰并与rGO结合. 图 2(b)中DA@rGO的傅里叶变换红外光谱图显示, 波数3 420 cm-1和3 318 cm-1附近出现两个N—H伸缩振动的特征峰, 波数1 250 cm-1处出现C—N伸缩振动特征峰. DA在波数为1 626 cm-1处对应C=O伸缩振动的特征峰, 而DA@rGO中C=O特征峰向低波数发生了偏移(约1 620 cm-1), 原因可能是材料复合之后形成了分子内氢键使得吸收峰发生了红移, 进一步说明成功合成了DA@rGO复合材料.
图 2(c)为rGO和DA@rGO的拉曼光谱图. D带峰强度可反映碳材料基底面内和边缘由于基团、缺陷等因素引起的无序度, G带峰反映石墨烯sp2杂化碳原子的面内伸缩振动. D峰和G峰的峰强比(ID:IG)越大, 表明材料无序程度越高.与rGO相比, DA@rGO的D峰和G峰均增强, 且ID:IG值(0.88)大于rGO(0.81), 表明DA修饰引起复合材料的无序程度增加.
图 2(d)为材料DA@rGO的N2吸附-脱附等温曲线, N2吸附-脱附等温线出现一个微弱的回滞环. DA@rGO复合材料的BET比表面积达到461.24 m2·g-1, 较大的比表面积有利于电吸附Pb2+.
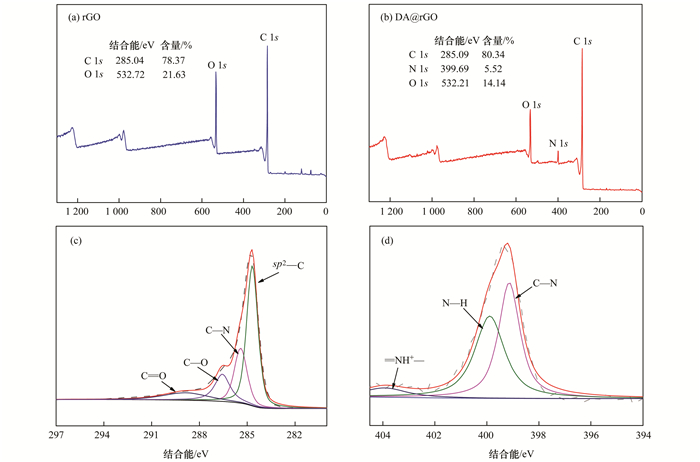
利用XPS分析DA修饰前后rGO和DA@rGO的元素组成和化学键变化. XPS全谱扫描结果显示[图 3(a)和3(b)], rGO仅含有C、O元素, DA@rGO复合材料在285、399和532 eV分别对应C 1s、N 1s和O 1s的结合能.对DA@rGO的C 1s谱图进行分峰拟合结果如图 3(c), 在284.6、285.4、286.6和289.1 eV分别对应sp2—C、C—N、C—O和C=O键, N元素含量为5.52%.对其N 1s谱图进行分峰拟合如图 3(d), N元素的成键形式包括C—N(399.1 eV)、N—H(399.9 eV)和=NH+ (404 eV), 说明DA中的一部分—NH2可能与rGO中的—COOH发生了反应, 以共价键的形式负载到石墨烯上.
|
(c)和(d)为DA@rGO的XPS C 1s谱图和N 1s谱图 图 3 rGO和DA@rGO的XPS分析 Fig. 3 XPS analysis of rGO and DA@rGO |
多孔材料的电容大小与电吸附能力关系密切[25]. rGO及DA@rGO的循环伏安曲线(CV)如图 4(a)所示, 在电压窗口-0.5~0.5 V范围内, rGO的CV曲线呈标准矩形, 表现出优异的双电层电容. DA@rGO的CV曲线在-0.1~0 V左右出现一组对称的氧化峰和还原峰, 原因是DA分子发生了可逆的蒽醌与氢醌的氧化还原反应. DA@rGO复合材料表现出优异的电化学性质, 其CV曲线闭合面积显著大于rGO, 表明DA的修饰明显提高了复合材料的电容, 增加部分来源于DA分子的蒽醌基团提供的赝电容.不同电流密度下DA@rGO的GCDC曲线如图 4(b)所示, 通过计算可知在电流密度分别为0.5、1和2 A·g-1时相应的比电容为302.5、304.4和215.4 F·g-1.

|
图 4 rGO及DA@rGO复合电极循环伏安曲线和恒电流充放电曲线 Fig. 4 CV curves of rGO and DA@rGO and galvanostatic charge-discharge curves of DA@rGO |
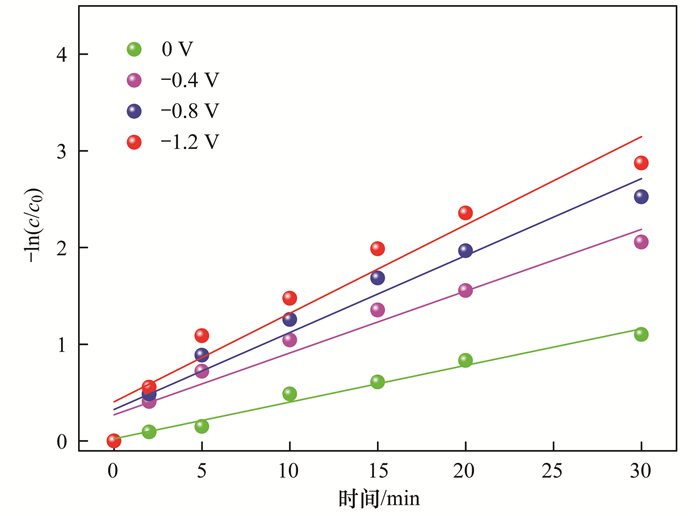
对不同电压下电极材料DA@rGO电吸附Pb2+的吸附过程进行一级动力学方程拟合[26].如图 5所示, 随着外加电压的负向移动, 电吸附过程的Pb2+去除率提高, 说明增加负向电压有利于Pb2+向电极的迁移和吸附.随着外加电压由0 V负向增加至-1.2 V, 表 1中拟合得到的速率常数由0.038 min-1增大到0.091 min-1.
|
图 5 不同电压下DA@rGO复合电极对Pb2+的电吸附动力学曲线 Fig. 5 Pb2+ electrosorption kinetics of the DA@rGO composite electrode at different potentials |
|
|
表 1 不同电压下DA@rGO复合电极对Pb2+的电吸附动力学参数 Table 1 First order kinetics of electrosorption of Pb2+ at different potentials of DA@rGO composite electrode |
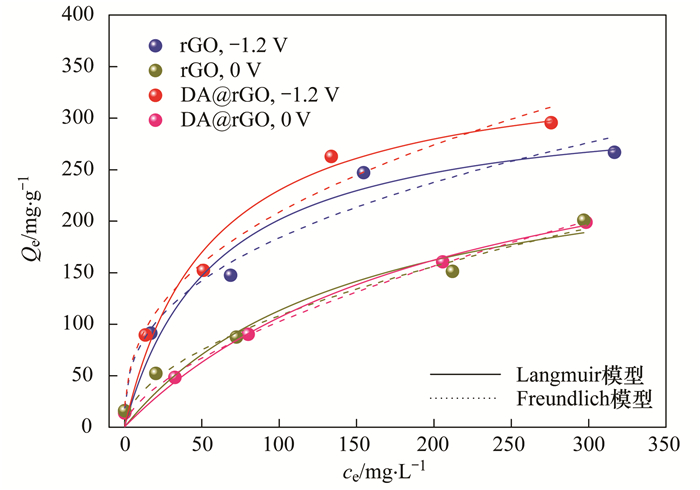
采用Langmuir和Freundlich两种吸附模型拟合吸附等温线[27]. 图 6为rGO及DA@rGO复合电极分别在施加-1.2 V和0 V(对照)下的吸附等温线, 两电极在电压-1.2 V下电吸附Pb2+的最大吸附量分别是0 V时的1.1倍和1.2倍, 说明静电力作用促进两种材料对Pb2+的吸附. 0 V时, 两种电极材料的平衡吸附量接近;-1.2 V时DA@rGO复合电极电吸附Pb2+的平衡吸附量高于rGO, 较高的比电容是其电吸附效果越好的重要原因. 表 2为Langmuir和Freundlich吸附等温线模型拟合的相关参数.吸附平衡时Langmuir模型拟合得到的rGO和DA@rGO电极材料的饱和吸附量分别为319.4 mg·g-1和356.66 mg·g-1.参照Freundlich模型拟合所得的K值, 可验证两种材料在加电条件下均可以促进吸附[28].
|
图 6 rGO和DA@rGO复合电极的吸附等温线 Fig. 6 Adsorption isotherms of Pb2+ on rGO and DA@rGO composite electrode |
|
|
表 2 Langmuir和Freundlich吸附等温线的拟合参数 Table 2 Fitting parameters of Langmuir and Freundlich adsorption models |
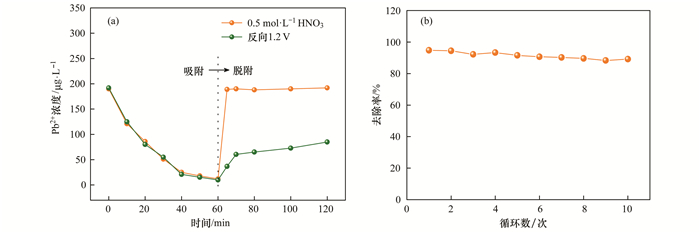
在外加电压为-1.2 V的最佳条件下, 对DA@rGO复合电极进行60 min吸附实验后, 分别比较接反向1.2 V电压、0.5 mol·L-1硝酸处理两种条件下的脱附60 min的效果, 如图 7(a)所示.最佳电吸附条件下, 反应60 min后溶液中的Pb2+浓度由192 μg·L-1降至10 μg·L-1左右, Pb2+去除率达到94.8%.硝酸处理条件下5 min内脱附效果显著, 溶液中的Pb2+浓度迅速升高至190 μg·L-1左右, 其机制是电极表面吸附的Pb2+由于与硝酸溶液中的H+发生交换[29], 从而被释放到溶液中达到脱附.接反向1.2 V电压60 min后, 溶液中的Pb2+浓度由10 μg·L-1升高至84.9 μg·L-1, Pb2+的脱附率为41.6%. 图 7(b)为电极材料DA@rGO吸附Pb2+的循环性能测试, 保持吸附时间为60 min, 在最佳条件下重复电吸附-酸处理脱附10次循环后, 电极的Pb2+去除率保持在88%左右, 表明电极循环性能稳定.
|
图 7 DA@rGO电极吸脱附曲线及吸脱附循环测试 Fig. 7 Electrosorption-desorption equilibrium curves and electrosorption-desorption cycles of the DA@rGO electrode |
(1) 通过高温溶剂热法成功将DA分子修饰于rGO上制备了DA@rGO复合电极. DA分子内蒽醌-氢醌互变反应提供的赝电容使得复合电极电容量增加.
(2) 对电吸附过程分析表明, 电吸附Pb2+符合一级动力学方程, 热力学符合Langmuir和Freundlich吸附等温线模型. DA@rGO复合电极在最佳条件(外加电压-1.2 V)下Pb2+去除率达到94.8%, 饱和吸附量(356.66 mg·g-1)明显高于rGO电极(319.40 mg·g-1).
(3) 0.5 mol·L-1硝酸处理可以使DA@rGO表面吸附的Pb2+在5 min内脱附, 实现电极再生.经过10次电吸附-脱附循环后Pb2+去除率仍保持在88%左右, 电极循环性能稳定.
| [1] |
王海东, 方凤满, 谢宏芳. 中国水体重金属污染研究现状与展望[J]. 广东微量元素科学, 2010, 17(1): 14-18. Wang H D, Fang F M, Xie H F. Research situation and outlook on heavy metal pollution in water environment of China[J]. Guangdong Trace Elements Science, 2010, 17(1): 14-18. DOI:10.3969/j.issn.1006-446X.2010.01.002 |
| [2] | Emmanuel E, Angerville R, Joseph O, et al. Human health risk assessment of lead in drinking water:a case study from Port-au-Prince, Haiti[J]. International Journal of Environment and Pollution, 2007, 31(3-4): 280-291. |
| [3] | Acharya J, Sahu J N, Mohanty C R, et al. Removal of lead(Ⅱ) from wastewater by activated carbon developed from Tamarind wood by zinc chloride activation[J]. Chemical Engineering Journal, 2009, 149(1-3): 249-262. DOI:10.1016/j.cej.2008.10.029 |
| [4] | Subramani A, Jacangelo J G. Emerging desalination technologies for water treatment:a critical review[J]. Water Research, 2015, 75: 164-187. DOI:10.1016/j.watres.2015.02.032 |
| [5] | Jia B P, Zhang W. Preparation and application of electrodes in capacitive deionization (CDI):a state-of-art review[J]. Nanoscale Research Letters, 2016, 11(1): 64. DOI:10.1186/s11671-016-1284-1 |
| [6] | Porada S, Zhao R, Van Der Wal A, et al. Review on the science and technology of water desalination by capacitive deionization[J]. Progress in Materials Science, 2013, 58(8): 1388-1442. DOI:10.1016/j.pmatsci.2013.03.005 |
| [7] | Ji Q H, An X Q, Liu H J, et al. Electric double-layer effects induce separation of aqueous metal ions[J]. ACS Nano, 2015, 9(11): 10922-10930. DOI:10.1021/acsnano.5b04027 |
| [8] | Bansal R C, Goyal M. Activated carbon adsorption[J]. Environmental Science & Technology, 1995, 29(3): 109A. |
| [9] | Peng Z, Zhang D S, Shi L Y, et al. Comparative electroadsorption study of mesoporous carbon electrodes with various pore structures[J]. The Journal of Physical Chemistry C, 2011, 115(34): 17068-17076. DOI:10.1021/jp2047618 |
| [10] | Huang Z H, Yang Z Y, Kang F Y, et al. Carbon electrodes for capacitive deionization[J]. Journal of Materials Chemistry A, 2017, 5(2): 470-496. DOI:10.1039/C6TA06733F |
| [11] | Hou C H, Huang J F, Lin H R, et al. Preparation of activated carbon sheet electrode assisted electrosorption process[J]. Journal of the Taiwan Institute of Chemical Engineers, 2012, 43(3): 473-479. DOI:10.1016/j.jtice.2011.12.003 |
| [12] | Yang C M, Choi W H, Na B K, et al. Capacitive deionization of NaCl solution with carbon aerogel-silicagel composite electrodes[J]. Desalination, 2005, 174(2): 125-133. DOI:10.1016/j.desal.2004.09.006 |
| [13] | Peng Z, Zhang D S, Shi L Y, et al. High performance ordered mesoporous carbon/carbon nanotube composite electrodes for capacitive deionization[J]. Journal of Materials Chemistry, 2012, 22(14): 6603-6612. DOI:10.1039/c2jm16735b |
| [14] | Gao Y, Pan L K, Li H B, et al. Electrosorption behavior of cations with carbon nanotubes and carbon nanofibres composite film electrodes[J]. Thin Solid Films, 2009, 517(5): 1616-1619. DOI:10.1016/j.tsf.2008.09.065 |
| [15] | Wang H, Zhang D S, Yan T T, et al. Graphene prepared via a novel pyridine-thermal strategy for capacitive deionization[J]. Journal of Materials Chemistry, 2012, 22(45): 23745-23748. DOI:10.1039/c2jm35340g |
| [16] | Lei H, Yan T T, Wang H, et al. Graphene-like carbon nanosheets prepared by a Fe-catalyzed glucose-blowing method for capacitive deionization[J]. Journal of Materials Chemistry A, 2015, 3(11): 5934-5941. DOI:10.1039/C4TA05713A |
| [17] | Lai L F, Yang H P, Wang L, et al. Preparation of supercapacitor electrodes through selection of graphene surface functionalities[J]. ACS Nano, 2012, 6(7): 5941-5951. DOI:10.1021/nn3008096 |
| [18] | Choi J H. Fabrication of a carbon electrode using activated carbon powder and application to the capacitive deionization process[J]. Separation and Purification Technology, 2010, 70(3): 362-366. DOI:10.1016/j.seppur.2009.10.023 |
| [19] | Park B H, Choi J H. Improvement in the capacitance of a carbon electrode prepared using water-soluble polymer binder for a capacitive deionization application[J]. Electrochimica Acta, 2010, 55(8): 2888-2893. DOI:10.1016/j.electacta.2009.12.084 |
| [20] |
曾汉民.水热/溶剂热法还原氧化石墨烯及其蒽醌复合物的电化学性能研究[D].广州: 华南理工大学, 2014.46-52. Zeng H M. Synthesis and electrochemical performance of hydrothermal/solvothermal reduced graphene oxide and its anthraquinone composite[D]. Guangzhou: South China University of Technology, 2014.46-52. http://cdmd.cnki.com.cn/article/cdmd-10561-1014064641.htm |
| [21] | Liu H Y, Zhang G Q, Zhou Y F, et al. One-step potentiodynamic synthesis of poly(1, 5-diaminoanthraquinone)/reduced graphene oxide nanohybrid with improved electrocatalytic activity[J]. Journal of Materials Chemistry A, 2013, 1(44): 13902-13913. DOI:10.1039/c3ta13600k |
| [22] | Wu Q, Sun Y Q, Bai H, et al. High-performance supercapacitor electrodes based on graphene hydrogels modified with 2-aminoanthraquinone moieties[J]. Physical Chemistry Chemical Physics, 2011, 13(23): 11193-11198. DOI:10.1039/c1cp20980a |
| [23] | Hummers Jr W S, Offeman R E. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 1958, 80(6): 1339. DOI:10.1021/ja01539a017 |
| [24] | Xu Y X, Sheng K X, Li C, et al. Self-assembled graphene hydrogel via a one-step hydrothermal process[J]. ACS Nano, 2010, 4(7): 4324-4330. DOI:10.1021/nn101187z |
| [25] |
李海波.基于石墨烯及其复合物电极的电容去离子技术研究[D].上海: 华东师范大学, 2012.2-77. Li H B. Study of graphene and its composite as electrodes for capacitive deionization[D]. Shanghai: East China Normal University, 2012.2-77. http://www.cnki.com.cn/Article/CJFDTotal-WGCL201602002.htm |
| [26] | Zhou Y J, Ji Q H, Liu H J, et al. Pore structure-dependent mass transport in flow-through electrodes for water remediation[J]. Environmental Science & Technology, 2018, 52(13): 7477-7485. |
| [27] | Tan I A W, Ahmad A L, Hameed B H. Adsorption isotherms, kinetics, thermodynamics and desorption studies of 2,4,6-trichlorophenol on oil palm empty fruit bunch-based activated carbon[J]. Journal of Hazardous Materials, 2009, 164(2-3): 473-482. DOI:10.1016/j.jhazmat.2008.08.025 |
| [28] |
王瑶, 吉庆华, 李永峰, 等. 石墨烯凝胶电极的制备及电吸附Pb2+的性能[J]. 环境科学, 2017, 38(9): 3747-3754. Wang Y, Ji Q H, Li Y F, et al. Preparation and Pb2+ electrosorption characteristics of graphene hydrogels electrode[J]. Environmental Science, 2017, 38(9): 3747-3754. |
| [29] | Liu Y X, Yan J M, Yuan D X, et al. The study of lead removal from aqueous solution using an electrochemical method with a stainless steel net electrode coated with single wall carbon nanotubes[J]. Chemical Engineering Journal, 2013, 218: 81-88. DOI:10.1016/j.cej.2012.12.020 |
 2019, Vol. 40
2019, Vol. 40