2. 中国水产科学研究院黄海水产研究所, 青岛 266071;
3. 农业农村部水产品质量安全检测与评价重点实验室, 青岛 266071
2. Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Qingdao 266071, China;
3. Key Laboratory of Testing and Evaluation for Aquatic Product Safety and Quality, Ministry of Agriculture and Rural Affairs, Qingdao 266071, China
全氟烷基物质(perfluorinated alkyl substances, PFASs)是一类新兴的持久性有机污染物(persistent organic pollutant, POPs), 因其具有极强的稳定性、良好的疏水疏油性和表面活性, 广泛应用于各种工业生产和消费品中[1, 2].目前, 已在大气[3]、水体[4]、沉积物[5]、土壤[6]及动植物体内[7]等多种环境介质中发现PFASs的存在.毒理学研究表明, PFASs具有肝脏毒性、生殖毒性、发育毒性、免疫毒性、内分泌干扰作用和潜在的致癌性[8].在2009年召开的“关于持久性有机污染物的斯德哥尔摩公约”第四次缔约方大会上, 限制了全氟辛烷磺酸(perfluorooctane sulfonate, PFOS)及其盐在全球范围内的使用[9];2015年缔约方大会又通过了全氟辛酸(perfluorooctanoic acid, PFOA)及相关物质的特性筛选审查并提交限制议案, 建议其在全球范围内禁止使用[10].此外, 前驱物作为PFASs的重要来源之一, 已有相关研究证实其同样具有生物毒性[11, 12], 在环境中也普遍存在[13~15].因此, PFASs及其前驱物的安全风险已成为国际研究热点和管控重点.
胶州湾位于中国黄海中部、胶东半岛南部, 为青岛市境内典型的半封闭海湾, 湾口与黄海直接相连, 并有多条河流汇入, 是青岛市各种陆源排放物的汇集地.胶州湾为我国有名的贝类养殖基地, 其盛产的菲律宾蛤仔肉质鲜嫩、营养丰富, 深受消费者喜爱, 是胶州湾浅海底播增殖贝类的代表[16].近年来, 人类活动的不断增加使胶州湾水域面积减少, 净化能力下降, 部分河口海域污染严重.目前, 针对胶州湾POPs污染的相关研究涉及邻苯二甲酸酯[17]、多溴联苯醚[18]和多环芳烃[19]等, 而PFASs作为一类新型POPs, 其污染情况的研究鲜有报道, 仅有的相关研究[20]只分析了胶州湾表层海水及水生生物中的14种PFASs, 未涵盖前驱物的污染情况.
本文从海水、沉积物和菲律宾蛤仔多种环境介质入手, 通过对胶州湾PFASs污染情况的调查, 分析了PFASs的污染水平及分布特征, 以期为胶州湾区域PFASs的污染控制及生态风险评价提供一定的数据基础和科学依据.
1 材料与方法 1.1 仪器与试剂仪器:Q-Exactive四极杆-静电场轨道阱高分辨质谱系统及Dionex UltiMate 3000超高效液相色谱系统(美国Thermo fisher公司), 真空冷冻干燥机(丹麦Scanlaf公司), XW-80A旋涡混合器(上海医大仪器厂), Himac CR 22GⅡ高速离心机(日本Hitachi公司), N-EVAP 112氮吹仪(美国Organomation公司), 57250-U固相萃取装置(美国Supelco公司).
试剂:PFASs标准溶液纯度均>99%(加拿大Wellington Laboratories公司), 35种PFASs物质包括全氟丁酸(perfluorobutanoic acid, PFBA)、全氟戊酸(perfluoropentanoic acid, PFPeA)、全氟己酸(perfluorohexanoic acid, PFHxA)、全氟庚酸(perfluoroheptanoic acid, PFHpA)、全氟辛酸(perfluorooctanoic acid, PFOA)、全氟壬酸(perfluorononanoic acid, PFNA)、全氟癸酸(perfluorodecanoic acid, PFDA)、全氟十一烷酸(perfluoroundecanoic acid, PFUdA)、全氟十二烷酸(perfluorododecanoic acid, PFDoA)、全氟十三烷酸(perfluorotridecanoic acid, PFTrDA)、全氟十四烷酸(perfluorotetradecanoic acid, PFTeDA)、全氟十六烷酸(perfluorohexadecanoic acid, PFHxDA)、全氟十八烷酸(perfluorooctadecanoic acid, PFODA)、全氟丁烷磺酸(perfluorobutanesulfonic acid, PFBS)、全氟己烷磺酸(perfluorohexanesulfonic acid, PFHxS)、全氟庚烷磺酸(perfluoroheptanesulfonic acid, PFHpS)、全氟辛烷磺酸(perfluorooctanesulfonic acid, PFOS)、全氟癸烷磺酸(perfluorodecanesulfonic acid, PFDS)、全氟辛烷磺酰胺(, PFOSA)、6:2氟调聚酸(2-Perfluorohexyl ethanoic acid, 6:2 FTCA)、10:2氟调聚酸(2-Perfluorodecyl ethanoic acid, 10:2 FTCA)、3:3氟调聚酸(3-Perfluoropropyl propanoic acid, 3:3 FTCA)、5:3氟调聚酸(3-Perfluoropentyl propanoic acid, 5:3 FTCA)、7:3氟调聚酸(3-perfluoroheptyl propanoic acid, 7:3 FTCA)、6:2氟调聚不饱和酸(2H-Perfluoro-2-octenoic acid, 6:2 FTUCA)、8:2氟调聚不饱和酸(2H-Perfluoro-2-decenoic acid, 8:2 FTUCA)、10:2氟调聚不饱和酸(2H-Perfluoro-2-dodecenoic acid, 10:2 FTUCA)、6:2全氟辛烷二磷酸酯[bis-(1H, 1H, 2H, 2H-perfluorooctyl) phosphate, 6:2 diPAP]、N-甲基全氟辛烷磺酰胺(N-methyl perfluorooctane sulfonamide, N-MeFOSA)、N-乙基全氟辛烷磺酰胺(N-ethyl perfluorooctane sulfonamide, N-EtFOSA)、N-甲基全氟辛烷磺酰胺乙醇(N-methyl perfluorooctane sulfonamidoethanol, N-MeFOSE)、N-乙基全氟辛烷磺酰胺乙醇(N-ethyl perfluorooctane sulfonamidoethanol, N-EtFOSE)、全氟辛烷磺酰胺乙酸(perfluorooctane sulfonamidoacetic acid, PFOSAA)、N-甲基全氟辛烷磺酰胺乙酸(N-methyl perfluorooctane sulfonamidoacetic acid, N-MeFOSAA)和N-乙基全氟辛烷磺酰胺乙酸(N-ethyl perfluorooctane sulfonamidoacetic acid, N-EtFOSAA), 12种内标物质包括13C4-全氟辛酸(Perfluoro-n-[1, 2, 3, 413C4]octanoic acid, MPFOA)、13C4-全氟辛烷磺酸(Perfluoro-1-[1, 2, 3, 413C4]octanesulfonate, MPFOS)、13C8-全氟辛烷磺酰胺(Perfluoro-1-[13C8]octanesulfonamide, M8FOSA)、[13C2]6:2氟调聚酸(2-Perfluorohexyl-[1, 2-13C2]-ethanoic acid, M6:2 FTCA)、[13C2]8:2氟调聚酸(2-Perfluorooctyl-[1, 2-13C2]-ethanoic acid, M8:2 FTCA)、[13C2]10:2氟调聚酸(2-Perfluorodecyl-[1, 2-13C2]-ethanoic acid, M10:2 FTCA)、[13C2]6:2氟调聚不饱和酸(2H-Perfluoro-[1, 2-13C2]-2-octenoic acid, M6:2 FTUCA)、[13C2]8:2氟调聚不饱和酸(2H-Perfluoro-[1, 2-13C2]-2-decenoic acid, M8:2 FTUCA)、[13C2]6:2全氟辛烷二磷酸酯[bis (1H, 1H, 2H, 2H-〔1, 2-13C2〕perfluorooctyl)-phosphate, M4-6:2 diPAP]、N-甲基全氟辛烷磺酰胺-D3(N-methyl-d3-, D3-N-MeFOSA)和N-甲基全氟辛烷磺酰胺乙酸-D3(N-methyl-d3-perfluorooctanesulfonamidoacetic acid, D3-N-MeFOSAA).
甲醇、乙腈、水(质谱级, 美国Merck公司)、乙酸铵(HPLC级, 美国Sigma公司)、氨水(ACS级, 美国Sigma公司);C18填料(40 μm, 美国Agilent公司)、石墨化碳黑(ENVI Carbon-GCB, 120-400目, 美国Sigma公司);Waters Oasis WAX固相萃取柱(6 cc, 150 mg, 美国Waters公司)、Waters Oasis PRiME HLB固相萃取柱(6 cc, 200 mg, 美国Waters公司), 其他未作特殊说明的试剂均为分析纯.
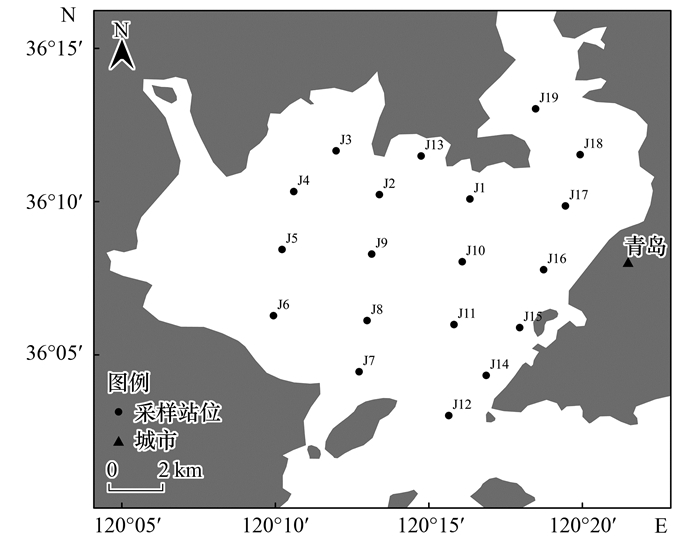
1.2 样品采集2018年4月在胶州湾近岸海域采集样品, 采样点分布如图 1所示.使用1 L聚丙烯(PP)瓶采集海水样品(n=19), 低温保存运回实验室, 过滤后置于4℃储存, 在同一采样点采集沉积物(n=18)和菲律宾蛤仔(n=25), 储存在PP样品袋中, 密封运回实验室, 冷冻干燥后置于-20℃储存.为避免污染, 采样过程中严禁使用含氟材料的器皿.
|
图 1 胶州湾采样点分布示意 Fig. 1 Distribution of sampling points in Jiaozhou Bay |
海水中PFASs的提取参考文献[21]的方法, 水样经0.45 μm玻璃纤维滤膜去除颗粒物质, 取100 mL样品加入内标物(2 ng), 室温下静置10 min, 过Waters Oasis WAX固相萃取柱(使用前依次用5 mL 0.1%氨水甲醇溶液、5 mL甲醇和5 mL水活化), 然后用5 mL 20%甲醇淋洗, 4 mL 2.5%氨水甲醇溶液重复洗脱两次.洗脱液于35℃氮吹至略低于0.5 mL, 用50%甲醇水溶液定容至1 mL, 12 000 r·min-1高速离心10 min, 将上清液过0.22 μm滤膜, 待测.
沉积物中PFASs的提取参考文献[22]的方法, 样品冷冻干燥后, 准确称取1.0 g于15 mL PP离心管中, 加入内标物(5 ng), 室温下静置10 min, 加入5 mL 90%乙腈水溶液, 涡旋混匀1 min, 超声提取10 min, 8 000 r·min-1离心5 min, 再加入4 mL 90%乙腈水溶液重复提取1次, 合并上清液定容至10 mL.向提取液中加入100 mg C18填料和50 mg石墨化碳黑(GCB), 充分涡旋后, 8 000 r·min-1离心5 min, 取5 mL上清液于35℃氮吹至略低于0.5 mL, 用50%甲醇水溶液定容至0.5 mL, 12 000 r·min-1高速离心10 min, 将上清液过0.22 μm滤膜, 待测.
菲律宾蛤仔中PFASs的提取参考文献[23]的方法, 准确称取0.5 g冻干样品于15 mL PP离心管中, 加入内标物(10 ng), 室温下静置10 min, 加入9 mL 90%乙腈水溶液, 涡旋混匀1 min, 超声提取10 min, 8 000 r·min-1离心5 min, 移取上清液并用90%乙腈水溶液定容至10 mL.取约1 mL上述提取液润洗Oasis PRiME HLB固相萃取柱, 自然流速流干, 再准确移取2 mL提取液加载至SPE小柱上, 保持流速为每秒1滴, 收集流出液, 于35℃氮气吹至略低于0.5 mL, 用50%甲醇水溶液定容至1 mL, 12 000 r·min-1高速离心10 min, 将上清液过0.22 μm滤膜, 待测.
1.4 液相色谱/质谱条件液相色谱条件:Phenomenex Kinetex XB-C18色谱柱(2.1×100 mm, 2.6 μm), 柱温为40℃, 流动相A为5%甲醇水溶液(含5 mmol·L-1乙酸铵缓冲液), B为95%甲醇水溶液(含5 mmol·L-1乙酸铵缓冲液), 进样量为10 μL, 流速为0.25 mL·min-1;洗脱梯度:初始流动相为10% B, 0.5~3.0 min升至70% B, 3.0~5.0 min升至80% B, 5.0~8.0 min保持80% B, 8.0~10.0 min升至100% B, 10.0~13.0 min保持100% B, 13.1~15.0 min恢复至初始流动相.
质谱条件:加热电喷雾离子源(HESI), 负离子模式, 扫描模式为Full MS/dd-MS2;喷雾电压:-3.0 kV;毛细管和加热器温度分别为320℃和50℃;鞘气和辅助气为40 arb和5 arb;采集范围m/z为150~1 000;一级全扫描(Full MS)分辨率为70000 FWHM, C-trap最大容量(AGC target):3×106, C-trap最大注入时间:200 ms;数据依赖二级子离子扫描(dd-MS2)分辨率为17500 FWHM, C-trap最大容量(AGC target):1×105, C-trap最大注入时间:50 ms, 其他质谱参数参考文献[23].
1.5 质量控制与保证为避免外源性污染, 全程避免使用聚四氟乙烯材质的色谱管路和器皿, 实验器皿均采用聚丙烯材质, 使用前用甲醇充分清洗.样品检测的同时做试剂空白, 所有实验数据均扣除空白值.
在空白样品中加入待测物的标准溶液, 按1.3节和1.4节进行回收率分析. 35种PFASs线性范围为0.100~20.0 μg·L-1, 相关系数(R2)在0.992~0.999之间, 海水加标回收率为60.0%~118%, 相对标准偏差为2.06%~14.6%(加标量分别为0.5、2、10 ng·L-1);沉积物加标回收率为67.8%~112%, 相对标准偏差为1.01%~14.6%, (加标量分别为0.1、0.5、2 μg·kg-1);菲律宾蛤仔加标回收率为60.9%~119%, 相对标准偏差为1.35%~14.4%(加标量分别为0.5、2和10 μg·kg-1).各化合物的回收率与检出限见表 1.
|
|
表 1 目标化合物的回收率与检出限 Table 1 Recoveries and detection limits of target compounds |
1.6 数据分析
本文采用软件Origin 8.5、SPSS 13.0及Excel 2016等对实验数据进行分析, 若PFASs含量低于检出限或未检出时, 在数据处理过程中其含量数值以0进行计算.
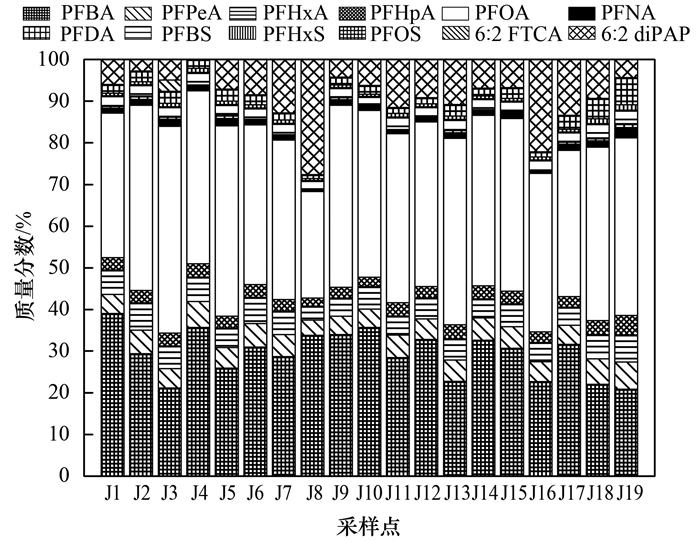
2 结果与讨论 2.1 胶州湾海水及沉积物中PFASs的含量水平与组成海水样品共检出12种PFASs, 包括C4~C10全氟羧酸(perfluorocarboxylic acids, PFCAs)、C4, C6, C8全氟磺酸(perfluorosulfonic acids, PFSAs)、6:2 FTCA和6:2 diPAP(图 2). PFOA在海水样品中均有检出, 占PFASs总质量浓度(ΣPFASs)的40.1%, 明显高于其他组分, 为主要污染物, 其次是PFBA(29.2%)、PFHxA(5.25%)和PFPeA(5.12%);前驱物6:2 FTCA仅在J3站点被检出, 而6:2 diPAP是胶州湾海水首次检出的前驱物, 检出率为94.7%, 平均质量浓度为2.51 ng·L-1(表 2), 低于香港维多利亚港[13]及波罗的海[14]的污染水平. ΣPFASs范围为21.1~38.0 ng·L-1, 均值为26.6 ng·L-1, 与国内黄河中游[24]污染成分组成基本相同, 总污染水平低于太湖[25]、天津[26]地区, 但高于深圳近岸[27]及渤海[28]地区, 这可能与地域差异、人类活动及工业发展等因素有关;与国外地区相比, ΣPFASs污染水平高于西班牙[5]及日本[29]海域, 低于韩国西海岸[30]及南非瓦尔河[31].
|
图 2 不同采样点海水中PFASs组成及质量分数 Fig. 2 Compositions and mass fractions of PFASs in seawater at different sampling points |
|
|
表 2 胶州湾海水和沉积物中PFASs的含量 Table 2 Contents of PFASs in seawater and sediments from Jiaozhou Bay |
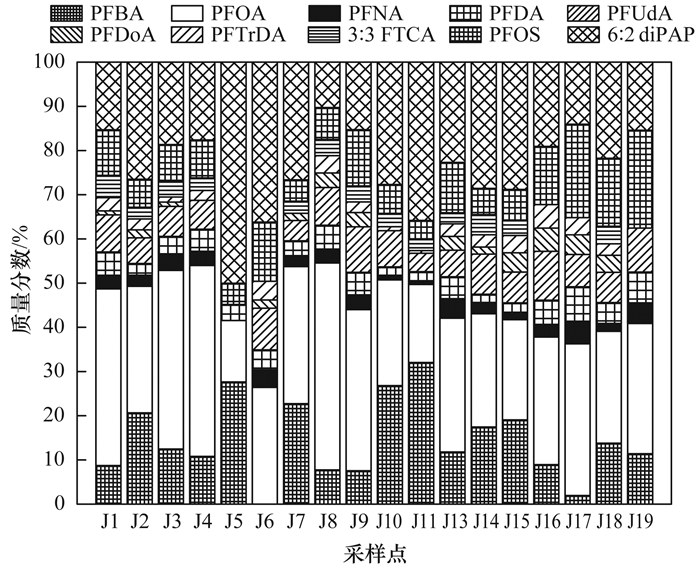
沉积物样品共检出10种PFASs, 包括C4, C8~C13 PFCAs、PFOS、3:3 FTCA和6:2 diPAP(图 3). PFOA同样是沉积物中最主要的污染物, 检出率为100%, 占ΣPFASs的30.1%, 其次是PFBA(15.4%)、PFOS(9.50%)和PFUdA(6.98%);前驱物3:3 FTCA的检出率为72.0%, 占ΣPFASs的2.54%, 6:2 diPAP在沉积物中均有检出, 占ΣPFASs的24.5%, 平均含量(以干重计)为0.183 μg·kg-1, 低于黄河中游三门峡和小浪底镇[24]颗粒相中的含量, 但高于五大湖[15]沉积物的污染程度. diPAP属于双酯类的多氟烷基磷酸酯(polyfluoroalkyl phosphates, PAPs), 主要用于食品包装材料中, 海水及沉积物中普遍检出6:2 diPAP, 而位于胶州湾北部的多家食品厂可能是污染源之一.沉积物中ΣPFASs含量范围为0.459~1.20 μg·kg-1, 均值为0.745 μg·kg-1, 总污染水平与国内黄浦江地区[32]相当, 但明显高于五大湖[15]、珠江[32]及西班牙[5]地区, 与天津[26]及韩国西海岸[30]相比, 总污染水平相对较低.
|
图 3 不同采样点沉积物中PFASs组成及质量分数 Fig. 3 Compositions and mass fractions of PFASs in sediments at different sampling points |
以上结果表明, 海水与沉积物中PFASs的污染组分有所差异, 短链PFASs(C5~C7)仅在海水中检出, 长链PFASs(C11~C13)仅在沉积物中检出, C8~C10 PFASs虽均有检出, 但在ΣPFASs中的占比有所差异(如PFOA占海水ΣPFASs的40.1%, 占沉积物ΣPFASs的30.1%), 这说明碳链长度影响PFASs在沉积物与海水之间的分配行为.
2.2 PFASs在沉积物与海水之间的分配采用同一采样点的海水及沉积物中PFASs含量计算其分配系数(Kd), 有研究表明沉积物对PFASs的吸附作用与有机碳含量密切相关[33, 34], 因此有机碳归一化分配系数(KOC)可以更好地反映分配行为, 计算公式如下[33]:
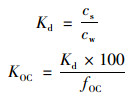
|
式中, cs是PFASs在沉积物中的含量(μg·kg-1, 以干重计);cw是PFASs在海水中的质量浓度(μg·L-1);fOC是沉积物中有机碳的质量分数(%), 采用Elementar VARIO EL元素分析仪测定了胶州湾沉积物中fOC均值为0.708%;Kd及KOC的单位是L·kg-1.
表 3结果显示, lg Kd及lg KOC值的变化范围分别为1.09±0.417(PFBA)~2.22±0.093 5(PFDA)和5.24±0.404(PFBA)~6.37±0.083 6(PFDA), 其中PFBA、PFOA、PFNA、PFDA和PFOS的lg KOC值及PFOA的lg Kd值高于其他地区[33~37], 可能是由不同地区沉积物性质(如粒径和有机碳含量等)及水质(如pH和Ca2+浓度等)差异造成的. lg KOC值呈现随碳链增加而增加的趋势, 且每增加一个碳链(PFOA~PFDA), lg KOC值增加约0.4个单位, 与之前报道的研究结果[34, 37]相符. Labadie等[33]及Higgins[36]认为对于一类特定的PFASs, 碳链长度是影响沉积物吸附作用的主要结构特征, 随着碳链的增长, PFASs的疏水作用增强, 溶解度减小, 更易被固体吸附, 这可以解释本研究海水及沉积物中PFASs组成差异明显的现象.此外, PFOS的lgKd值较PFOA高0.7个单位, 6:2 diPAP碳链较长, 但其Kd及KOC值均小于PFDA, 与刘宝林[27]及Chen等[37]的研究结果一致, 这说明除疏水作用外, 沉积物对PFASs的吸附作用还可能与官能团、氢键或静电作用力有关.
|
|
表 3 不同地区PFASs的lg Kd与lg KOC值 Table 3 The lg Kd and lg KOC values of PFASs in different regions |
2.3 胶州湾生物样品中PFASs的含量水平与组成
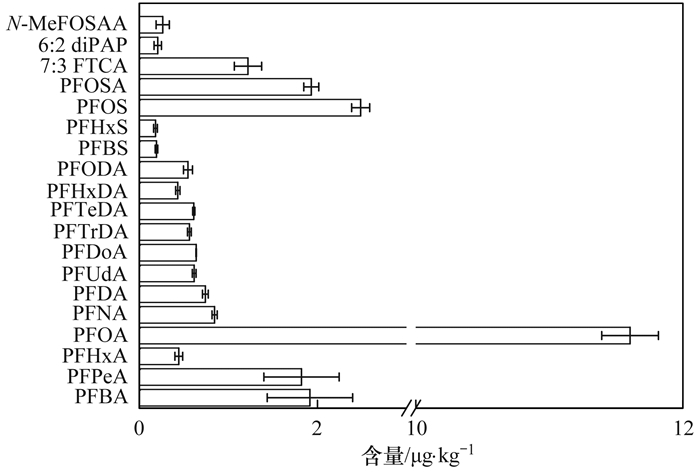
菲律宾蛤仔是胶州湾主要水产养殖品种之一, 本研究以其作为胶州湾生物样品代表, PFASs含量及组成如图 4所示.菲律宾蛤仔共检出19种PFASs, 包括C4~C6、C8~C16PFCAs、C4、C6、C8PFSAs、PFOSA、N-MeFOSAA、7:3 FTCA及6:2 diPAP. ΣPFASs含量(以干重计)范围为15.5~27.5 μg·kg-1, 其中PFOA普遍检出, 含量为5.32~17.4 μg·kg-1(均值11.6 μg·kg-1), 占ΣPFASs的56.9%, 是菲律宾蛤仔中首要的PFAS, 其次是PFOS(12.2%), 这与渤海文蛤[38]污染情况类似, 但韩国[39]、日本[40]及西班牙[5]海域中双壳贝类体内的首要PFAS为PFOS, 且PFOA含量低于本研究.菲律宾蛤仔中检出的PFSAs前驱物有PFOSA及N-MeFOSAA, PFOSA的检出率为93.8%, 占ΣPFASs含量的8.88%, 郭萌萌等[23]同样发现鱼肉的PFOS阳性样品存在其前驱物PFOSA的复合污染;N-MeFOSAA的检出率为25.0%, 仅占ΣPFASs的0.160%. PFCAs前驱物7:3 FTCA的检出率为43.7%, 占ΣPFASs的2.62%, 6:2 diPAP在菲律宾蛤仔样品中也有检出, 检出率仅为18.7%, 低于海水及沉积物中的检出率, 仅占ΣPFASs的0.190%, 可能是6:2 diPAP在生物体内转化成PFHxA和PFHpA等其它PFASs[11].
|
图 4 菲律宾蛤仔中PFASs含量水平及组成 Fig. 4 Contents and compositions of PFASs in Ruditapes philippinarum |
除C7(PFHpA)外, C4~C16PFASs在菲律宾蛤仔体内均有检出, 基本包含海水及沉积物中的PFASs组分, 表明海水和沉积物是水产生物体内PFASs的重要来源, PFOA、PFNA和PFOS在生物体内ΣPFASs的占比高于海水及沉积物, 说明PFASs在菲律宾蛤仔体内可能具有生物累积能力.
2.4 PFASs的生物累积特征用同一采样点的生物及海水中PFASs含量来计算生物累积因子(bioaccumulation factors, BAF), 而沉积物作为某些水生生物PFASs的来源之一, 生物-沉积物累积因子(bioaccumulation factors between organism and sediment, BSAF)是描述沉积物中PFASs生物累积的相关参数, 计算公式如下[41]:
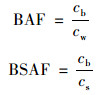
|
式中, cb是PFASs在菲律宾蛤仔中的含量(μg·kg-1, 以湿重计);cw是PFASs在海水中的质量浓度(μg·L-1);cs是PFASs在沉积物中的含量(μg·kg-1, 以干重计).如表 4所示, PFASs在菲律宾蛤仔体内的lg BAF及lg BSAF值变化范围分别为2.53±0.061 4(PFBA)~4.32±0.284(PFDA)和1.30±0.487(PFBA)~2.50±0.077 9(PFOA), C4~C10PFASs的lg BAF值大于lg BSAF值, 表明菲律宾蛤仔体内的短链PFASs(C4~C10)更易通过海水富集.
|
|
表 4 PFASs在生物体内的lg BAF和lg BSAF值 Table 4 The lg BAF and lg BSAF values of PFASs in organisms |
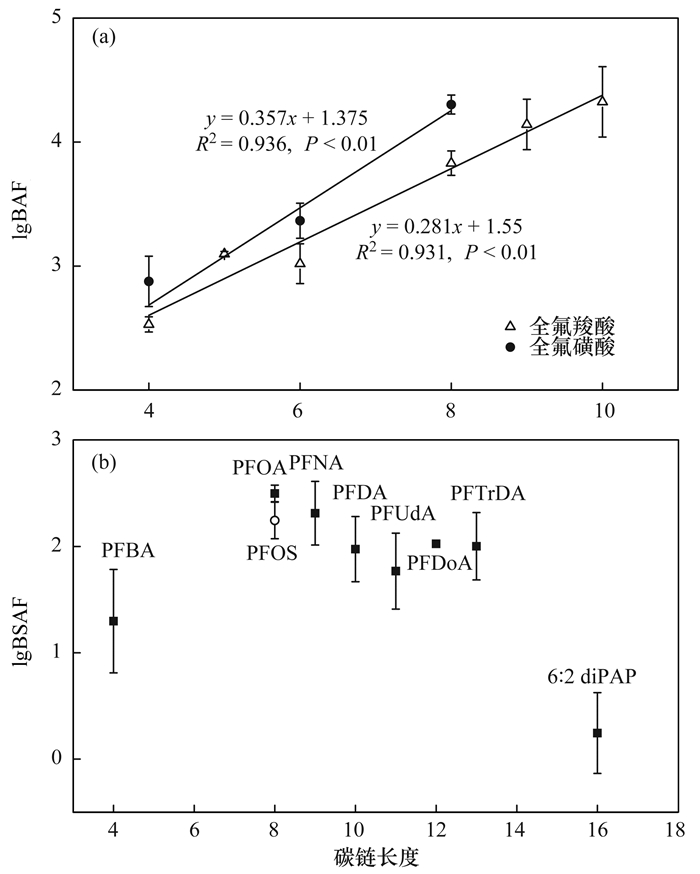
PFCAs和PFSAs的lg BAF值呈现随碳链长度增加而增加的趋势, 且具有显著的相关性[图 5(a)], 这与长链PFASs表现出更高的蛋白质-水分配系数(Kpw)的事实相一致[42]. PFSAs的lg BAF值大于具有相同碳链长的PFCAs(如PFOS比PFOA高0.473个单位), 符合Labadie[33]及Chen等[37]的研究结果, 但lg BAF值有所差异, 可能由物种差异及生活习性不同造成的, 另一种原因可能是不同地区水体PFASs污染水平不同. 6:2 diPAP的碳链较长, 但lg BAF值仅为2.24, 推测可能的原因为6:2 diPAP在生物体内发生转化, 或者6:2 diPAP分子质量较大导致难以穿透细胞膜, 限制其生物累积能力[43]. PFASs的lg BSAF值不同于lg BAF值随碳链的增加而增加, 而是随碳链的增加呈现下降趋势[图 5(b)], PFOA的lg BSAF值最大. Labadie等[33]同样发现鱼肉和沉积物之间的lg BSAF值与碳链长度呈负相关(C10~C14), 且PFDA为最大值;Higgins等[44]报道了夹杂带丝蚓的BSAF值随着碳链长度(C8~C14)的增加趋于下降, 但这一过程的机制尚不清楚.
|
图 5 生物体中PFASs的lg BAF值和lg BSAF值与碳链长度的关系 Fig. 5 Correlation between lg BAF, lg BSAF values, and length of carbon chain of PFASs in organisms |
(1) 胶州湾海水、沉积物及生物体(菲律宾蛤仔)内普遍检出PFASs.海水中ΣPFASs含量范围为21.1~38.0 ng·L-1, 沉积物中ΣPFASs含量(以干重计)范围为0.459~1.20 μg·kg-1, 菲律宾蛤仔中ΣPFASs含量(以干重计)范围为15.5~27.5 μg·kg-1;与国内外报道的其他地区相比, 胶州湾ΣPFASs污染处于中等或偏高水平.胶州湾首要污染物为PFOA, 6:2 diPAP是海水及沉积物中检出率及含量最高的前驱物, 而PFOSA则是菲律宾蛤仔体内检出率及含量最高的前驱物.
(2) 短链PFASs易存在于海水中, 长链PFASs易存在于沉积物中, lg Kd与lg KOC值呈现随碳链增加而增加的趋势.
(3) lg BAF值与PFASs碳链长度呈显著线性正相关;lg BSAF值随PFASs碳链的增加(C8~C13)呈现下降趋势, PFOA的lg BSAF值最大.
| [1] | Paul A G, Jones K C, Sweetman A J. A first global production, emission, and environmental inventory for perfluorooctane sulfonate[J]. Environmental Science & Technology, 2009, 43(2): 386-392. |
| [2] | Prevedouros K, Cousins I T, Buck R C, et al. Sources, fate and transport of perfluorocarboxylates[J]. Environmental Science & Technology, 2006, 40(1): 32-44. |
| [3] | Dreyer A, Weinberg I, Temme C, et al. Polyfluorinated compounds in the atmosphere of the atlantic and southern oceans:evidence for a global distribution[J]. Environmental Science & Technology, 2009, 43(17): 6507-6514. |
| [4] | Ahrens L. Polyfluoroalkyl compounds in the aquatic environment:a review of their occurrence and fate[J]. Journal of Environmental Monitoring, 2011, 13(1): 20-31. DOI:10.1039/C0EM00373E |
| [5] | Gómez C, Vicente J, Echavarri-Erasun B, et al. Occurrence of perfluorinated compounds in water, sediment and mussels from the Cantabrian Sea (North Spain)[J]. Marine Pollution Bulletin, 2011, 62(5): 948-955. DOI:10.1016/j.marpolbul.2011.02.049 |
| [6] | Kim E J, Park Y M, Park J E, et al. Distributions of new Stockholm Convention POPs in soils across South Korea[J]. Science of the Total Environment, 2014, 476-477: 327-335. DOI:10.1016/j.scitotenv.2014.01.034 |
| [7] | Pignotti E, Casas G, Llorca M, et al. Seasonal variations in the occurrence of perfluoroalkyl substances in water, sediment and fish samples from Ebro Delta (Catalonia, Spain)[J]. Science of the Total Environment, 2017, 607-608: 933-943. DOI:10.1016/j.scitotenv.2017.07.025 |
| [8] | Lau C, Anitole K, Hodes C, et al. Perfluoroalkyl acids:a review of monitoring and toxicological findings[J]. Toxicological Sciences, 2007, 99(2): 366-394. DOI:10.1093/toxsci/kfm128 |
| [9] | Zhao Z, Tang J H, Mi L J, et al. Perfluoroalkyl and polyfluoroalkyl substances in the lower atmosphere and surface waters of the Chinese Bohai Sea, Yellow Sea, and Yangtze River estuary[J]. Science of the Total Environment, 2017, 599-600: 114-123. DOI:10.1016/j.scitotenv.2017.04.147 |
| [10] | Wang Y, Sun Y Z. The causes of the scientific and regulatory gap in the listing of new persistent organic pollutants into the Stockholm Convention[J]. Environmental Science & Technology, 2016, 50(12): 6117-6118. |
| [11] | Chen M, Guo T T, He K Y, et al. Biotransformation and bioconcentration of 6:2 and 8:2 polyfluoroalkyl phosphate diesters in common carp (Cyprinus carpio):Underestimated ecological risks[J]. Science of the Total Environment, 2019, 656: 201-208. DOI:10.1016/j.scitotenv.2018.11.297 |
| [12] | Liu C S, Deng J, Yu L Q, et al. Endocrine disruption and reproductive impairment in zebrafish by exposure to 8:2 fluorotelomer alcohol[J]. Aquatic Toxicology, 2010, 96(1): 70-76. |
| [13] | Loi E I H, Yeung L W Y, Mabury S A, et al. Detections of commercial fluorosurfactants in Hong Kong marine environment and human blood:a pilot study[J]. Environmental Science & Technology, 2013, 47(9): 4677-4685. |
| [14] | Gebbink W A, Bignert A, Berger U. Perfluoroalkyl acids (PFAAs) and selected precursors in the Baltic Sea environment:do precursors play a role in food web accumulation of PFAAs?[J]. Environmental Science & Technology, 2016, 50(12): 6354-6362. |
| [15] | Guo R, Megson D, Myers A L, et al. Application of a comprehensive extraction technique for the determination of poly-and perfluoroalkyl substances (PFASs) in Great Lakes Region sediments[J]. Chemosphere, 2016, 164: 535-546. DOI:10.1016/j.chemosphere.2016.08.126 |
| [16] | 刘增胜, 柳正. 中国渔业年鉴[M]. 北京: 中国农业出版社, 2007: 51-52. |
| [17] |
刘成, 孙翠竹, 张哿, 等. 胶州湾表层水体中邻苯二甲酸酯的污染特征和生态风险[J]. 环境科学, 2019, 40(4): 1726-1733. Liu C, Sun C Z, Zhang G, et al. Pollution characteristics and ecological risk assessment of phthalate esters (PAEs) in the surface water of Jiaozhou Bay[J]. Environmental Science, 2019, 40(4): 1726-1733. |
| [18] |
鞠婷, 葛蔚, 柴超. 胶州湾沉积物中多溴联苯醚的污染特征及风险评价[J]. 环境化学, 2017, 36(4): 839-848. Ju T, Ge W, Chai C. Pollution and ecological risk assessment of polybrominated diphenyl ethers in the sediments of Jiaozhou Bay[J]. Environmental Chemistry, 2017, 36(4): 839-848. |
| [19] |
刘娜, 印萍, 朱志刚, 等. 胶州湾大沽河河口表层沉积物中多环芳烃分布特征、来源及生态风险评价[J]. 海洋环境科学, 2016, 35(6): 831-837. Liu N, Yin P, Zhu Z G, et al. Distribution, sources and ecological risk assessment of PAHs in surface sediments from the Dagu River estuary in Jiaozhou Bay, China[J]. Marine Environmental Science, 2016, 35(6): 831-837. |
| [20] |
韩同竹.胶州湾海水和生物体中全氟化合物的分布特征及来源解析[D].青岛: 国家海洋局第一海洋研究所, 2018.27-54. Han T Z. Distribution and potential sources of perfluoroalkyl substances (PFASs) in Jiaozhou bay[D]. Qingdao: The First Institute of Oceanography, SOA, 2018.27-54. |
| [21] |
张明, 唐访良, 俞雅雲, 等. 固相萃取-超高效液相色谱-电喷雾串联质谱法同时测定地表水中16种全氟有机化合物[J]. 色谱, 2014, 32(5): 472-476. Zhang M, Tang F L, Yu Y Y, et al. Simultaneous determination of sixteen perfluorinated organic compounds in surface water by solid phase extraction and ultra performance liquid chromatography with electrospray ionization tandem mass spectrometry[J]. Chinese Journal of Chromatography, 2014, 32(5): 472-476. |
| [22] |
郭萌萌, 吴海燕, 李兆新, 等. 超快速液相色谱-串联质谱法检测水产品中23种全氟烷基化合物[J]. 分析化学, 2013, 41(9): 1322-1327. Guo M M, Wu H Y, Li Z X, et al. Determination of 23 perfluorinated alkyl substances in fishery products by ultra fast liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2013, 41(9): 1322-1327. |
| [23] |
郭萌萌, 国佼, 吴海燕, 等. 通过式固相萃取-液相色谱-四极杆/静电场轨道阱高分辨质谱快速筛查鱼肉中全氟化合物及其前体物质[J]. 分析化学, 2016, 44(10): 1504-1513. Guo M M, Guo J, Wu H Y, et al. Rapid screening and confirmation of perfluorinated compounds and their precursors in fish muscle by solid phase extraction purification and liquid chromatography coupled with Quadrupole/Exactive Orbitrap mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2016, 44(10): 1504-1513. DOI:10.11895/j.issn.0253-3820.160333 |
| [24] |
李琦路, 程相会, 赵祯, 等. 黄河中游(渭南——郑州段)全/多氟烷基化合物的分布及通量[J]. 环境科学, 2019, 40(1): 228-238. Li Q L, Cheng X H, Zhao Z, et al. Distribution and fluxes of perfluoroalkyl and polyfluoroalkyl substances in the middle reaches of the Yellow River (Weinan-Zhengzhou section)[J]. Environmental Science, 2019, 40(1): 228-238. |
| [25] | Mak Y L, Taniyasu S, Yeung L W Y, et al. Perfluorinated compounds in tap water from China and several other countries[J]. Environmental Science & Technology, 2009, 43(13): 4824-4829. |
| [26] | Li F S, Sun H W, Hao Z N, et al. Perfluorinated compounds in Haihe River and Dagu Drainage Canal in Tianjin, China[J]. Chemosphere, 2011, 84(2): 265-271. DOI:10.1016/j.chemosphere.2011.03.060 |
| [27] |
刘宝林, 张鸿, 谢刘伟, 等. 深圳近岸海域全氟化合物的污染特征[J]. 环境科学, 2015, 36(6): 2028-2037. Liu B L, Zhang H, Xie L W, et al. Pollution characteristics of perfluorinated compounds in offshore marine area of Shenzhen[J]. Environmental Science, 2015, 36(6): 2028-2037. |
| [28] | Wang T Y, Lu Y L, Chen C L, et al. Perfluorinated compounds in estuarine and coastal areas of north Bohai Sea, China[J]. Marine Pollution Bulletin, 2011, 62(8): 1905-1914. DOI:10.1016/j.marpolbul.2011.05.029 |
| [29] | Taniyasu S, Kannan K, Horii Y, et al. A survey of perfluorooctane sulfonate and related perfluorinated organic compounds in water, fish, birds, and humans from Japan[J]. Environmental Science & Technology, 2003, 37(12): 2634-2639. |
| [30] | Naile J E, Khim J S, Hong S, et al. Distributions and bioconcentration characteristics of perfluorinated compounds in environmental samples collected from the west coast of Korea[J]. Chemosphere, 2013, 90(2): 387-394. DOI:10.1016/j.chemosphere.2012.07.033 |
| [31] | Groffen T, Wepener V, Malherbe W, et al. Distribution of perfluorinated compounds (PFASs) in the aquatic environment of the industrially polluted Vaal River, South Africa[J]. Science of the Total Environment, 2018, 627: 1334-1344. DOI:10.1016/j.scitotenv.2018.02.023 |
| [32] | Bao J, Liu W, Liu L, et al. Perfluorinated compounds in urban river sediments from Guangzhou and Shanghai of China[J]. Chemosphere, 2010, 80(2): 123-130. DOI:10.1016/j.chemosphere.2010.04.008 |
| [33] | Labadie P, Chevreuil M. Partitioning behaviour of perfluorinated alkyl contaminants between water, sediment and fish in the Orge River (nearby Paris, France)[J]. Environmental Pollution, 2011, 159(2): 391-397. DOI:10.1016/j.envpol.2010.10.039 |
| [34] | Guo C S, Zhang Y, Zhao X, et al. Distribution, source characterization and inventory of perfluoroalkyl substances in Taihu Lake, China[J]. Chemosphere, 2015, 127: 201-207. DOI:10.1016/j.chemosphere.2015.01.053 |
| [35] | Zhu Z Y, Wang T Y, Wang P, et al. Perfluoroalkyl and polyfluoroalkyl substances in sediments from South Bohai coastal watersheds, China[J]. Marine Pollution Bulletin, 2014, 85(2): 619-627. DOI:10.1016/j.marpolbul.2013.12.042 |
| [36] | Higgins C P, Luthy R G. Sorption of perfluorinated surfactants on sediments[J]. Environmental Science & Technology, 2006, 40(23): 7251-7256. |
| [37] | Chen M, Wang Q, Shan G Q, et al. Occurrence, partitioning and bioaccumulation of emerging and legacy per-and polyfluoroalkyl substances in Taihu Lake, China[J]. Science of the Total Environment, 2018, 634: 251-259. DOI:10.1016/j.scitotenv.2018.03.301 |
| [38] | Pan Y Y, Shi Y L, Wang Y W, et al. Investigation of perfluorinated compounds (PFCs) in mollusks from coastal waters in the Bohai Sea of China[J]. Journal of Environmental Monitoring, 2010, 12(2): 508-513. DOI:10.1039/B909302H |
| [39] | Naile J E, Khim J S, Wang T Y, et al. Perfluorinated compounds in water, sediment, soil and biota from estuarine and coastal areas of Korea[J]. Environmental Pollution, 2010, 158(5): 1237-1244. DOI:10.1016/j.envpol.2010.01.023 |
| [40] | Nakata H, Kannan K, Nasu T, et al. Perfluorinated contaminants in sediments and aquatic organisms collected from shallow water and tidal flat areas of the Ariake Sea, Japan:environmental fate of perfluorooctane sulfonate in aquatic ecosystems[J]. Environmental Science & Technology, 2006, 40(16): 4916-4921. |
| [41] | Jacobson T, Holmström K, Yang G D, et al. Perfluorooctane sulfonate accumulation and parasite infestation in a field population of the amphipod Monoporeia affinis after microcosm exposure[J]. Aquatic Toxicology, 2010, 98(1): 99-106. |
| [42] | Kelly B C, Ikonomou M G, Blair J D, et al. Perfluoroalkyl contaminants in an arctic marine food web:trophic magnification and wildlife exposure[J]. Environmental Science & Technology, 2009, 43(11): 4037-4043. |
| [43] | Conder J M, Hoke R A, de Wolf W, et al. Are PFCAs bioaccumulative? A critical review and comparison with regulatory criteria and persistent lipophilic compounds[J]. Environmental Science & Technology, 2008, 42(4): 995-1003. |
| [44] | Higgins C P, McLeod P B, Macmanus-Spencer L A, et al. Bioaccumulation of perfluorochemicals in sediments by the aquatic oligochaete Lumbriculus variegates[J]. Environmental Science & Technology, 2007, 41(13): 4600-4606. |
 2019, Vol. 40
2019, Vol. 40


