2. 住房和城乡建设部村镇建设司, 农村生活垃圾处理技术研究与培训中心, 上海 200092;
3. 同济大学固体废物处理与资源化研究所, 上海 200092
2. Centre for the Technology Research and Training on Household Waste in Small Towns & Rural Area, Ministry of Housing Urban-Rural Development, Shanghai 200092, China;
3. Institute of Waste Treatment and Reclamation, Tongji University, Shanghai 200092, China
生物炭是一种富含碳的细粒多孔物质, 是指生物质在无氧或缺氧及相对较低温(250~700℃)条件下热解的产物[1, 2].其来源广泛, 木材废物、玉米棒等农业废弃物、茶叶废料、动物粪便、城市污泥等废弃生物质都可作为生物炭的原材料[3, 4].
由于生物炭来源广, 比表面积相对较大, 表面官能团丰富, 近年来广泛应用于土壤改良、储能、环境污染修复等场合[5~8], 以及厌氧消化和好氧堆肥等废物生物转化过程[9]. Lü等[10]和Luo等[11]发现投加生物炭可以有效缓解厌氧消化过程中的氨抑制和酸抑制; 粒径为75 μm的生物炭, 可缩短反应迟滞期38.0%, 提高最大产甲烷速率70.6%. Awasthi等[12]将生物炭投加到好氧堆肥体系, 发现生物炭不仅缩短了反应的嗜热期, 而且减少了CH4和N2O等温室气体的排放.
但是, 由于复杂的高温制备过程, 生物炭可能会残留一些有毒有害物质, 如痕量金属、多环芳烃(PAHs)、挥发性有机物(VOCs), 以及被羟基和羧基取代的小分子芳香族化合物等[4, 6, 13~15].生物炭表面残留的化合物种类主要与生物质原料和热解温度有关[15~17]. Oleszczuk等发现[18], 采用甲苯提取4种不同原料制得生物炭表面的PAHs总量相差较大, 范围为1 124~28 339 μg·kg-1, 当生物炭提取物PAHs总量越高时, 与之接触的甲壳类动物大型蚤死亡率越高, 最高可达80%. Smith等[19]用蒸馏水浸出松木生物炭, 并将生物炭浸出液用于培养水生光合微生物蓝绿藻类, 发现浸出液对微生物的生长表现出了明显的抑制作用.因此, 在厌氧消化等生物反应过程中, 生物炭中的有毒有害物质若被浸出, 可能会对反应体系中的微生物产生危害.另外, 如果这些有毒有害物质进入沼渣、沼液等处理残余物, 当残余物用于后续土地利用时也可能会造成不利的环境影响.
目前, 大量关于生物炭浸出液成分及其相关毒性的研究多聚焦于生物炭在蒸馏水或甲苯中的浸出[14, 18~20], 鲜有研究关注在实际不同环境应用体系中的溶解性有机物(dissolved organic matters, DOM)组成.而在厌氧消化[21]、发酵产氢[22, 23]过程中, 随着反应的进行, 在中期阶段可能会产生挥发性脂肪酸(VFAs)、醇类等中间产物, 在反应后期会累积腐殖质等物质. Zheng等[24]研究了在厌氧消化过程中29种可生物降解固体废物光谱特性的演变规律, 结果表明, 在产甲烷过程结束后, 沼液中富里酸类化合物荧光峰的丰度提高了0.01~0.54倍, 说明厌氧消化系统生成了一定量的腐殖类物质. Tang等[25]的研究发现, 在厌氧消化过程中污泥中的腐殖质成分发生了再聚合, 能提供更多芳香族富电子位点从而形成新的腐殖质聚合物, 在厌氧消化后期腐殖酸浓度达到最高.因此, 生物炭在厌氧消化过程中的实际应用环境较为复杂, 仅以蒸馏水或甲苯作为浸提剂不足以正确评估生物炭可能造成的影响.另外, 传统研究中测试浸出液中有机物组成的方法, 常见有气质联用(GC-MS)[14]、13C核磁共振、红外光谱[20]等.而大分子化合物沸点高, 难以气化, 从而不能通过GC-MS被检测到.因此, GC-MS检测到的物质大多为小分子物质, 忽略了大分子物质和复杂物质的存在; 13C核磁共振、红外光谱[20]等手段虽然能提供一些结构信息, 但无法准确鉴别物质成分.
本文以4种浸提剂模拟厌氧消化不同阶段的液相环境, 采用高分辨液质联用仪的鉴定方法, 探究了生物炭在厌氧消化不同典型反应阶段浸出液中溶解性有机物的分子成分, 以研讨生物炭浸出液化合物组成可能对反应过程产生的影响.
1 材料与方法 1.1 生物炭本实验用生物炭为购自大连群芳园艺公司的果木炭, 热解温度为400~500℃.原始尺寸为8~12 mm, 使用前进行破碎筛分得到粒径为1~2 mm的生物炭颗粒.
1.2 浸出过程采用4种代表厌氧消化典型液相环境的浸提剂, 包括作为反应体系初始阶段的水和缓冲盐溶液, 作为反应中期的甲醇和作为反应后期的腐殖酸(humic acid, HA)溶液.
1.2.1 浸提剂HA溶液:将HA固体(购自上海巨枫化学科技有限公司), 用0.1 mol·L-1的NaOH溶解, 然后, 用HCl调节pH到5.0; HA溶液用0.45 μm滤膜过滤, 滤液保存于4℃冰箱作为储备液.
缓冲盐溶液:参考Lin等[26]启动厌氧消化批次反应的方法, 配制代表厌氧消化初期液相环境的缓冲盐溶液, 其组成包括0.1g·L-1 MgCl2·6H2O、0.53 g·L-1 NH4Cl、0.075 g·L-1 CaCl2·2H2O、0.1 g·L-1 Na2S·9H2O、2.77 g·L-1 K2HPO4、2.8 g·L-1 KH2PO4和0.02 g·L-1 FeCl2·4H2O.
甲醇:购自Sigma, HPLC, >99.9%.
1.2.2 浸出实验取10 g破碎筛分后的生物炭颗粒于500 mL浸提剂中, 在25℃、150 r·min-1的转速下振荡72 h.浸出液用0.45 μm混合纤维素酯滤膜过滤, 滤液保存于4℃冰箱作为储备液.
1.3 测试指标与分析方法用固相萃取法提取在不同浸提剂中生物炭的DOM, 采用高分辨液相色谱质谱联用仪测试浸出液中DOM的组成.
1.3.1 固相萃取固相萃取流程参考Dittmar等[27]萃取海水中DOM的方法.首先, 用甲醇活化固相萃取小柱(安捷伦, Bond Elut-PPL, 100 mg, 3 mL), 然后, 使浸出液匀速流过萃取柱, 流速不超过40 mL·min-1; 其后, 用pH=2的HCl清洗萃取小柱, 除去柱内的盐分, 并用空气干燥5 min; 最后, 用甲醇洗脱萃取小柱, 得萃取后的浸出液.除了将4种浸出液进行固相萃取之外, 将4种空白浸提剂也分别进行固相萃取, 并进行后续测试, 作为生物炭浸出前浸提剂的系统空白, 以扣除实验流程带来的误差.每种工况设置3平行.
1.3.2 仪器测试仪器:采用高分辨液相色谱质谱联用仪(Q-Exactive plus, Thermo), 分别用电喷雾正离子模式[ESI(+)]和电喷雾负离子模式[ESI(-)]测试浸出液中的DOM, 测试前仪器用校准溶液进行外部校准.
液相条件:扫描质量范围为100~1 500 m/z, 分辨率为70 000, 进样量为5 μL, 流速为0.3 mL·min-1, 选取甲醇和乙酸溶液为流动相.
1.3.3 软件分析使用Past3软件(http://folk.uio.no/ohammer/past/), 对不同浸出液中DOM利用进行主成分分析, 以比较DOM之间的差异.利用Compounds discover 2.1(Thermo)软件将DOM与物质数据库进行对比检索, 以鉴别DOM成分.
2 结果与分析结合电喷雾正离子[ESI(+)]和负离子[ESI(-)]两种模式下的原始数据, 共检测到2 690种物质.对原始数据进行数据筛选, 3个平行中至少有两平行检测到的物质才认为有效, 剔除无效数据[28], 剩下共有536种物质.
2.1 不同浸提剂体系DOM主成分分析对不同浸出液进行基于Bray-Curtis距离的主成分分析(principle component analysis, PCA), 如图 1(a)所示, 不同样品间的差异程度通过点与点间的距离体现[29].

|
(a)4种浸出液及其对应浸提剂DOM差异; (b)蒸馏水、缓冲盐溶液和HA溶液浸出液及其对应浸提剂DOM差异 图 1 不同浸出液中DOM组成主成分分析 Fig. 1 Principal component analysis on DOM composition in different leachates |
从图 1(a)中可以看出, 主成分1的占比为96.57%, 而主成分2的占比仅为2.76%.因此, 主成分1在DOM中所占比重较大, DOM组成差异主要由横轴的差距体现.蒸馏水浸出液和缓冲盐浸出液与对应空白相距较近, 即物质组成较为相似; HA溶液与HA溶液浸出液的距离相对较远, 这说明HA溶液和HA溶液浸出液之间DOM组成存在差异; 距离最远的是甲醇和甲醇浸出液, 即甲醇浸出液中DOM组成与甲醇有着较大差异.
由于甲醇的浸出液与甲醇空白之间的差异太大, 可能会影响其它组别之间的比较.因此, 将甲醇空白及甲醇浸出液从主成分分析图中去除, 对比剩余组别之间的差异. 图 1(b)列出了除甲醇浸出液外的3个浸出液及其空白的主成分分析图.从图中可以看出, 蒸馏水浸出液和蒸馏水空白距离极为接近, 说明生物炭在蒸馏水中浸出的DOM相对较少; 缓冲盐溶液浸出液和缓冲盐溶液空白距离最远, 即相比蒸馏水, 缓冲盐溶液能浸出更多的DOM; HA溶液浸出液和HA溶液空白在水平距离上基本无差异, 但在主成分2差异较大.
2.2 不同浸出液的DOM分子特征在正离子模式[ESI(+)]的测试结果中, 生物炭浸出液共检索到419种物质, 在负离子模式[ESI(-)]共检测到117种物质.结合ESI(+)和ESI(-)的质谱分析结果, 可得到浸出液中所有DOM的分子式.依据分子式中H/C和O/C原子数个数比的大小, 可将物质分为不饱和烃、木质素、脂类和脂肪族及蛋白质类物质, 绘制成Van Krevelen图[30].按此分类, 在蒸馏水和缓冲盐溶液中生物炭的浸出液DOM分布如图 2所示.

|
图 2 生物炭在蒸馏水和缓冲盐溶液浸出液DOM的Van Krevelen图 Fig. 2 Van Krevelen diagram of DOM in the water and the buffer salt solution leachates of biochar |
HA原溶液和生物炭的HA溶液浸出液中DOM组成和分布如图 3所示.从中可以看出, 投加生物炭到HA溶液中后, 溶液中DOM物质数量有所减少, 从113种减少到47种, 主要为木质素和脂类物质减少, 这与图 1的结果相一致.

|
图 3 HA溶液和HA溶液浸出液中DOM的Van Krevelen图 Fig. 3 Van Krevelen diagram of DOM in the humic acid solution and the humic acid solution leachate of biochar |
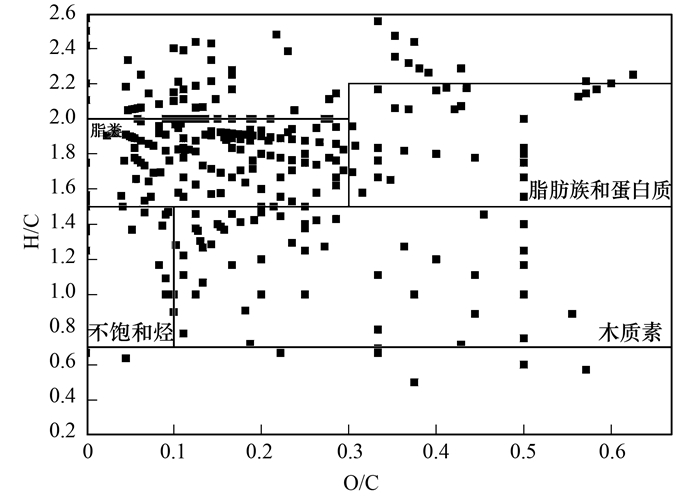
图 4是生物炭在甲醇浸出液中DOM的组成.可以看到, 甲醇浸出液中DOM各个种类有机物的数量相比其它浸出液都大幅增加, 尤其是脂类、木质素、脂肪族及蛋白质类物质的数量, 一共检测到381种物质.
|
图 4 生物炭在甲醇浸出液中DOM的Van Krevelen图 Fig. 4 Van Krevelen diagram of DOM in the methanol leachate of biochar |
不同于2.2节按DOM分子式中H/C和O/C的原子数个数比值差异对物质进行分类, 本节将测得物质质谱谱图与参考物质数据库mzCloud (www. mzCloud. org)进行对比检索, 保留匹配度超过70%的物质, 剩下共有100种物质.将这100种物质按结构进行分类, 主要可分为芳香族化合物和脂肪族化合物.芳香族化合物主要包括酚、芳香酸、芳香醛和酮、芳香酯和其它化合物, 其它化合物包括芳香醇、芳香醚和一些结构复杂的芳香族物质; 脂肪族化合物包括脂肪酸、酯、醇和其它化合物, 其它化合物包括酮、酰胺、杂环化合物等物质.检测到的DOM相对分子质量分布在109~458范围内, 平均相对分子质量为290.2.
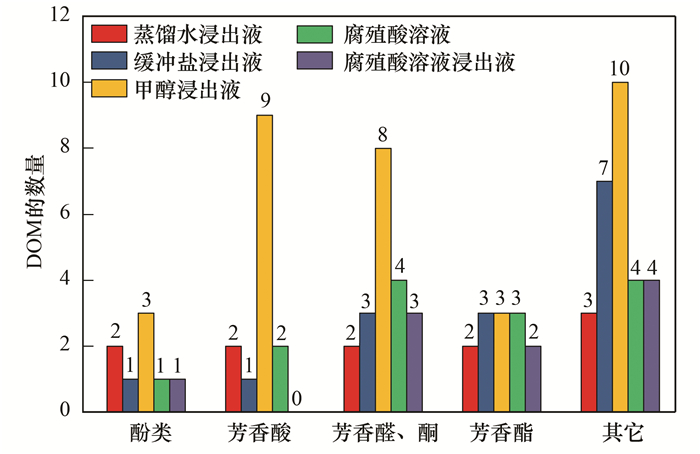
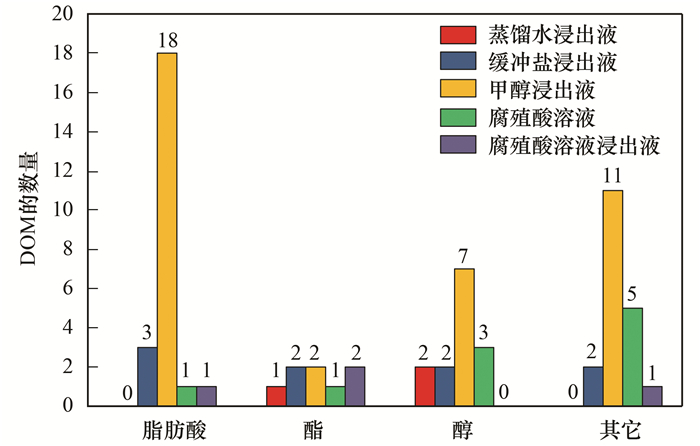
图 5和图 6分别为各个浸出液中芳香族化合物和脂肪族化合物种类的数量.在脂肪酸和芳香族化合物的其它物质这两个类别中, 缓冲盐溶液比蒸馏水多浸出了7种物质.甲醇浸出液在每个类别的DOM数量都是最多的, 尤其是脂肪酸和芳香酸这两类物质的数量远多于其它浸出液. HA溶液浸出液中的DOM在每个类别的数量都略少于HA溶液, 总体共少了10种物质.
|
图 5 不同浸出液中的芳香族化合物数量 Fig. 5 Number of aromatic compounds in different leachates |
|
图 6 不同浸出液中的脂肪族化合物数量 Fig. 6 Number of aliphatic compounds in different leachates |
不同浸出液中物质的含量存在差异, 表 1列出了各浸出液中相对丰度较高几种物质的峰面积.尽管图 3显示HA溶液中部分木质素和脂类物质被生物炭吸附, 但从表 1中可以看出, 生物炭在HA溶液中仍有部分物质浸出, 如4-硝基苯酚等.
|
|
表 1 各浸出液中部分物质的峰面积 Table 1 Peak area of some substances in each leachate |
3 讨论 3.1 蒸馏水与缓冲盐溶液条件下的浸出
在固相萃取过程中, 尽管空白对照会不可避免地遭受污染, 但其所含DOM物质极少, 所以, 可以认为蒸馏水和缓冲盐溶液中不含DOM.因此, 图 2浸出液中的DOM均来自生物炭.从中可以看出, 两种浸出液中的DOM物质种类近似, 多为脂类、木质素和不饱和烃类物质; 但是, 缓冲盐溶液浸出的DOM有93种物质, 多于蒸馏水浸出液中的37种物质, 这与图 1(b)主成分分析的结果一致.造成这种现象的原因, 可能是缓冲盐溶液中的金属离子与生物炭上的有机物竞争生物炭表面吸附位点[31], 即在浸出过程中金属离子可能占据了生物炭表面的吸附位点, 而使得生物炭上的有机物溶解到溶液中. 图 5和图 6中, 在脂肪酸和芳香族化合物的其它物质这两个类别中, 缓冲盐溶液比蒸馏水多浸出了7种物质, 与图 2的结论一致.
目前, 大量研究用生物炭在蒸馏水的浸出液来评估生物炭浸出液的毒性, 而实际应用场合如厌氧消化初始阶段的环境可能会浸出更多物质, 给反应过程带来更复杂的影响.由于缓冲盐溶液浸出液中DOM组成复杂, 物质类别分布较为均匀, 没有明显的高浸出组分, 给反应带来的影响是未知的, 比如是否浸出的DOM化合物反而起到了电子传递介体的有益作用.因此, 生物炭在厌氧消化初期的浸出液带来的实际影响尚需要进行毒性研究进一步确认.
3.2 甲醇条件下的浸出厌氧消化中期阶段可能会产生挥发性脂肪酸(VFAs)和醇类等中间产物.甲醇极性强, 相较乙醇可以溶解更多的化合物. Patra等[32]的研究发现用甲醇提取丁香和大蒜相比乙醇和水有更好的提取效果.因此, 选择甲醇为浸提剂可以浸出更多的DOM.乙酸是厌氧消化中期最常见的挥发性脂肪酸, 其极性与甲醇相近, 但由于其余组别固相萃取最后以甲醇为溶剂, 为减小误差和减少溶剂转化时的损失, 本文选择甲醇为浸提剂.实际的厌氧消化环境中, 甲醇浓度最高约为100~200 mg·L-1[23, 33], 本研究选用纯甲醇为浸提剂是为了获得最多的可浸出DOM种类, 即为了评估生物炭的DOM最大可浸出程度.因此, 甲醇浸出也是其它组别的对照组.从图 4与图 2、3的对比中可以看出, 作为厌氧消化反应中期的代表性醇类浸提剂, 甲醇比反应初期的蒸馏水和缓冲盐溶液浸出了更多的DOM种类.造成这种现象的原因, 可能是生物炭中DOM在甲醇中的辛醇-水分配系数大于蒸馏水和缓冲盐溶液, 有机物更易在甲醇中溶解.
根据图 5和图 6物质结构分类结果, 表明甲醇浸出液在芳香族化合物和脂肪族化合物中每个类别的DOM数量都是最多的, 尤其是脂肪酸和芳香酸这两类物质的数量远多于其它浸出液. Buss等[14]和Hao等[6]在用蒸馏水浸出生物炭和水热炭的相关研究中也检测到了大量的有机酸和酚类物质, 并提到这些物质可能会对微生物的生长造成威胁.因此, 在厌氧消化中期生成大量中间产物醇的环境下, 大量的有机酸、酚类和其它有机物可能会从生物炭表面浸出, 前二者可能会对厌氧反应体系中的微生物形成抑制.所以, 生物炭浸出液在反应中期可能产生比初期更大的危害.
3.3 腐殖酸从图 3可以看出, 投加生物炭到HA溶液后, 溶液中的DOM物质数量从113种减少到47种, 这可能是由于生物炭的吸附作用, 即由于生物炭丰富的孔隙, HA溶液中部分物质被吸附到生物炭表面[34]. 图 5和图 6中, HA溶液浸出液中的DOM在芳香族化合物和脂肪族化合物中每个类别的数量都略少于HA溶液, 这与图 3的结果是一致的.
Buss等[14]用蒸馏水浸出生物炭, 采用气相色谱-质谱联用(6890 GC-5975c MS, Agilent)测试浸出液成分, 发现浸出液中主要包括醇、小分子脂肪酸、酚类和多环芳烃(PAHs)等共34种物质, 相对分子质量分布在32~278范围内.与Buss等的研究结论相比, 本文测得的物质共100种, 相对分子质量分布在109~458范围内, 物质的相对分子质量总体要更大, 且种类更多.与其重合的物质种类主要包括酚、脂肪酸、醇和酮等物质, 在这些物质中, 本文测得的物质种类相对分子质量更大, 且数量更多.例如, 脂肪酸类中, 其研究主要包含甲酸、乙酸、丙酸和丁酸共4种酸, 相对分子质量范围为46~88, 而本文中的脂肪酸类物质主要包括壬二酸、十二烷二酸、十五烷酸和十六烷二酸等21种相对分子质量更大的脂肪酸, 相对分子质量分布在131~392范围内.因此, 传统的气相质谱测试方法测得的物质结构较为简单, 可能低估了生物炭浸出液中DOM组成的复杂性.
4 结论(1) 在厌氧消化不同阶段, 生物炭浸出液中的DOM组成存在较大差异.与目前大量研究所使用的蒸馏水浸出液相比, 代表厌氧消化初期环境的缓冲盐溶液能浸出生物炭中更多的脂肪酸和一些芳香族化合物; 代表厌氧消化中期环境的甲醇溶液溶剂浸出了大量的有机酸和苯酚类物质, 已有研究证明有机酸和苯酚类物质会对微生物形成抑制; 在代表厌氧消化后期环境的HA溶液中, 尽管生物炭能吸附部分木质素类物质, 但是仍有毒性强的酚类物质浸出.
(2) 本文结果表明, 应关注生物炭在环境及农业等相关修复场合应用的安全性.尽管生物炭表现出了优异的环境修复改善性能, 但应用生物炭后的浸出液及残余物也可能给反应过程带来不确定性, 给后续应用带来环境风险.因此, 后续研究和应用时应充分考虑生物炭浸出的DOM在其中所起的作用.
| [1] | Lehmann J, Joseph S. Biochar for environmental management: science, technology and implementation[M]. 2nd ed.. London: Routledge, 2015. |
| [2] | Manyà J J. Pyrolysis for biochar purposes: a review to establish current knowledge gaps and research needs[J]. Environmental Science & Technology, 2012, 46(15): 7939-7954. |
| [3] | Van Zwieten L, Kimber S, Morris S, et al. Effects of biochar from slow pyrolysis of papermill waste on agronomic performance and soil fertility[J]. Plant and Soil, 2010, 327(1-2): 235-246. DOI:10.1007/s11104-009-0050-x |
| [4] | Zielińska A, Oleszczuk P. The conversion of sewage sludge into biochar reduces polycyclic aromatic hydrocarbon content and ecotoxicity but increases trace metal content[J]. Biomass and Bioenergy, 2015, 75: 235-244. DOI:10.1016/j.biombioe.2015.02.019 |
| [5] |
赵华轩, 郎印海. 磁性生物炭对水中CIP和OFL的吸附行为和机制[J]. 环境科学, 2018, 39(8): 3729-3735. Zhao H X, Lang Y H. Behaviors and mechanisms of CIP and OFL adsorption by magnetic biochar[J]. Environmental Science, 2018, 39(8): 3729-3735. |
| [6] | Hao S L, Zhu X D, Liu Y C, et al. Production temperature effects on the structure of hydrochar-derived dissolved organic matter and associated toxicity[J]. Environmental Science & Technology, 2018, 52(13): 7486-7495. |
| [7] | Gai X P, Wang H Y, Liu J, et al. Effects of feedstock and pyrolysis temperature on biochar adsorption of ammonium and nitrate[J]. PLoS One, 2014, 9(12): e113888. DOI:10.1371/journal.pone.0113888 |
| [8] |
徐国鑫, 王子芳, 高明, 等. 秸秆与生物炭还田对土壤团聚体及固碳特征的影响[J]. 环境科学, 2018, 39(1): 355-362. Xu G X, Wang Z F, Gao M, et al. Effects of straw and biochar return in soil on soil aggregate and carbon sequestration[J]. Environmental Science, 2018, 39(1): 355-362. |
| [9] | Zhang J N, Lü F, Shao L M, et al. The use of biochar-amended composting to improve the humification and degradation of sewage sludge[J]. Bioresource Technology, 2014, 168: 252-258. DOI:10.1016/j.biortech.2014.02.080 |
| [10] | Lü F, Luo C H, Shao L M, et al. Biochar alleviates combined stress of ammonium and acids by firstly enriching Methanosaeta and then Methanosarcina[J]. Water Research, 2016, 90: 34-43. DOI:10.1016/j.watres.2015.12.029 |
| [11] | Luo C H, Lü F, Shao L M, et al. Application of eco-compatible biochar in anaerobic digestion to relieve acid stress and promote the selective colonization of functional microbes[J]. Water Research, 2015, 68: 710-718. DOI:10.1016/j.watres.2014.10.052 |
| [12] | Awasthi M K, Wang M J, Chen H Y, et al. Heterogeneity of biochar amendment to improve the carbon and nitrogen sequestration through reduce the greenhouse gases emissions during sewage sludge composting[J]. Bioresource Technology, 2017, 224: 428-438. DOI:10.1016/j.biortech.2016.11.014 |
| [13] | Keiluweit M, Kleber M, Sparrow M A, et al. Solvent-extractable polycyclic aromatic hydrocarbons in biochar: influence of pyrolysis temperature and feedstock[J]. Environmental Science & Technology, 2012, 46(17): 9333-9341. |
| [14] | Buss W, Mašek O, Graham M, et al. Inherent organic compounds in biochar--their content, composition and potential toxic effects[J]. Journal of Environmental Management, 2015, 156: 150-157. DOI:10.1016/j.jenvman.2015.03.035 |
| [15] | Kloss S, Zehetner F, Dellantonio A, et al. Characterization of slow pyrolysis biochars: effects of feedstocks and pyrolysis temperature on biochar properties[J]. Journal of Environmental Quality, 2012, 41(4): 990-1000. DOI:10.2134/jeq2011.0070 |
| [16] | Lyu H H, He Y H, Tang J C, et al. Effect of pyrolysis temperature on potential toxicity of biochar if applied to the environment[J]. Environmental Pollution, 2016, 218: 1-7. DOI:10.1016/j.envpol.2016.08.014 |
| [17] | Zhao L, Cao X D, Mašek O, et al. Heterogeneity of biochar properties as a function of feedstock sources and production temperatures[J]. Journal of Hazardous Materials, 2013, 256-257: 1-9. DOI:10.1016/j.jhazmat.2013.04.015 |
| [18] | Oleszczuk P, Jośko I, Kuśmierz M. Biochar properties regarding to contaminants content and ecotoxicological assessment[J]. Journal of Hazardous Materials, 2013, 260: 375-382. DOI:10.1016/j.jhazmat.2013.05.044 |
| [19] | Smith C R, Buzan E M, Lee J W. Potential impact of biochar water-extractable substances on environmental sustainability[J]. ACS Sustainable Chemistry & Engineering, 2013, 1(1): 118-126. |
| [20] | Qu X L, Fu H Y, Mao J D, et al. Chemical and structural properties of dissolved black carbon released from biochars[J]. Carbon, 2016, 96: 759-767. DOI:10.1016/j.carbon.2015.09.106 |
| [21] | He P J, Lü F, Shao L M, et al. Effect of alkali metal cation on the anaerobic hydrolysis and acidogenesis of vegetable waste[J]. Environmental Technology, 2006, 27(3): 317-327. DOI:10.1080/09593332708618646 |
| [22] | Ghimire A, Frunzo L, Pirozzi F, et al. A review on dark fermentative biohydrogen production from organic biomass: process parameters and use of by-products[J]. Applied Energy, 2015, 144: 73-95. DOI:10.1016/j.apenergy.2015.01.045 |
| [23] | Sivaramakrishna D, Sreekanth D, Himabindu V, et al. Biological hydrogen production from probiotic wastewater as substrate by selectively enriched anaerobic mixed microflora[J]. Renewable Energy, 2009, 34(3): 937-940. DOI:10.1016/j.renene.2008.04.016 |
| [24] | Zheng W, Lü F, Phoungthong K, et al. Relationship between anaerobic digestion of biodegradable solid waste and spectral characteristics of the derived liquid digestate[J]. Bioresource Technology, 2014, 161(161): 69-77. |
| [25] | Tang Y F, Li X W, Dong B, et al. Effect of aromatic repolymerization of humic acid-like fraction on digestate phytotoxicity reduction during high-solid anaerobic digestion for stabilization treatment of sewage sludge[J]. Water Research, 2018, 143: 436-444. DOI:10.1016/j.watres.2018.07.003 |
| [26] | Lin Y C, Lü F, Shao L M, et al. Influence of bicarbonate buffer on the methanogenetic pathway during thermophilic anaerobic digestion[J]. Bioresource Technology, 2013, 137: 245-253. DOI:10.1016/j.biortech.2013.03.093 |
| [27] | Dittmar T, Koch B, Hertkorn N, et al. A simple and efficient method for the solid-phase extraction of dissolved organic matter (SPE-DOM) from seawater[J]. Limnology and Oceanography Methods, 2008, 6(6): 230-235. DOI:10.4319/lom.2008.6.230 |
| [28] | Lucas J, Koester I, Wichels A, et al. Short-term dynamics of north sea bacterioplankton-dissolved organic matter coherence on molecular level[J]. Frontiers in Microbiology, 2016, 7: 321. |
| [29] | Beals E W. Bray-curtis ordination: an effective strategy for analysis of multivariate ecological data[J]. Advances in Ecological Research, 1984, 14: 1-55. DOI:10.1016/S0065-2504(08)60168-3 |
| [30] | Yuan Z W, He C, Shi Q, et al. Molecular insights into the transformation of dissolved organic matter in landfill leachate concentrate during biodegradation and coagulation processes using ESI FT-ICR MS[J]. Environmental Science & Technology, 2017, 51(14): 8110-8118. |
| [31] | Uchimiya M, Lima I M, Klasson K T, et al. Contaminant immobilization and nutrient release by biochar soil amendment: Roles of natural organic matter[J]. Chemosphere, 2010, 80(8): 935-940. DOI:10.1016/j.chemosphere.2010.05.020 |
| [32] | Patra A K, Kamra D N, Agarwal N. Effect of spices on rumen fermentation, methanogenesis and protozoa counts in in vitro gas production test[J]. International Congress Series, 2006, 1293: 176-179. DOI:10.1016/j.ics.2006.01.025 |
| [33] | Revilla I, González-Sanjosé M L. Methanol release during fermentation of red grapes treated with pectolytic enzymes[J]. Food Chemistry, 1998, 63(3): 307-312. DOI:10.1016/S0308-8146(98)00049-1 |
| [34] | He P J, Yu Q F, Zhang H, et al. Removal of copper (Ⅱ) by biochar mediated by dissolved organic matter[J]. Scientific Reports, 2017, 7(1): 7091. DOI:10.1038/s41598-017-07507-y |
 2019, Vol. 40
2019, Vol. 40