2. 苏州高新区浒墅关镇安全环保办公室, 苏州 215009;
3. 苏州净研环保科技有限公司, 苏州 215009;
4. 同济大学环境科学与工程学院, 上海 200092
2. Safety and Environmental Protection Office of Xushuguan Town, Suzhou High-tech Zone, Suzhou 215009, China;
3. Suzhou Jingyan Environmental Protection Technology Co., Ltd., Suzhou 215009, China;
4. School of Environmental Science and Engineering, Tongji University, Shanghai 200092, China
目前, 污水处理仍属于能耗密集型行业, 污水处理过程的节能降耗是污水处理厂实现可持续发展的一个重要环节.据统计, 现行市政污水处理厂有超过50%的能耗用于污水的好氧生物处理[1].特别地, 氨氮的硝化过程是污水好氧生物处理的重要组成部分, 为了保证良好的硝化效果, 现行污水处理厂在运行控制时一般维持硝化池中溶解氧(DO)浓度不低于2.0 mg·L-1[2].
特定条件下(如氧分压、气压、水温及水质等), 硝化过程对供氧的要求主要取决于两个方面, 即微生物实际消耗量和氧传质效率[3].基于低DO浓度条件下更高的氧传质效率(DO浓度为0.5 mg·L-1时氧传质效率比2.0 mg·L-1时提高16%[4])和微生物细胞产率[5], 有研究者致力于研究和开发低氧硝化工艺, 即在DO浓度不高于0.5 mg·L-1的条件下完成硝化过程[6, 7], 从而实现硝化反应能耗的节省.目前, 有关低氧硝化的研究主要集中在工艺效能、功能种群鉴定及其响应特征等方面[6~10], 结果表明低氧硝化工艺虽然可以实现与高氧(DO浓度>2.0 mg·L-1)硝化工艺相似的硝化效能, 其涉及的硝化功能种群类别或代谢特征却与高氧硝化工艺有显著差异.
污水生物处理工艺(包括硝化工艺)作为多物种共存的复杂生态系统, 其所表现出的系统功能不仅受特定功能菌群的影响, 还与共存的其他物种有关[11, 12].如有研究证实活性污泥系统的功能稳定性与其所含微生物种群的多样性[13, 14]和均匀性[15]密切相关. DO浓度作为硝化工艺一个重要的运行控制参数, 可以推测DO浓度变化不仅仅影响氨氧化细菌(AOB)和亚硝酸盐氧化细菌(NOB)的种类、数量和代谢特征, 亦会对系统中其他共存物种产生显著影响.了解低DO浓度下硝化工艺中微生物种群结构有助于深入掌握低氧硝化工艺的功能特征.遗憾的是, 现有研究对低氧硝化工艺中微生物种群结构及组成关注较少.
因此, 本研究借助高通量测序技术, 通过对比分析不同DO浓度下硝化工艺中的微生物种群组成, 重点揭示低氧硝化工艺中的微生物结构特征, 以期为低氧硝化工艺的开发和应用提供理论支持.
1 材料与方法 1.1 试验装置如图 1所示, 两个相同的全混式反应器(CSTR)并列运行, 每个反应器的反应区和沉淀区有效容积分别为2.4 L和0.6 L.反应区底部装有曝气砂盘, 并连通空气泵用于反应区供氧, 曝气速率根据运行情况通过气体流量计进行调节, 保证两个反应器中DO浓度分别维持在0.2~0.3 mg·L-1(RL)和(2.0±0.1)mg·L-1(RH).反应区均设有机械搅拌装置, 搅拌强度控制在60 r·min-1, 辅助实现进水与污泥的均匀混合.两反应器水力停留时间(HRT)和污泥停留时间(SRT)均分别控制在8 h和20 d.两反应器中pH均通过外加NaHCO3缓冲液维持在7.5左右.本研究期间, 整个反应器置于同一恒温水浴中, 反应器中温度在20~22℃.

|
图 1 工艺装置示意 Fig. 1 Schematic diagram of the experimental equipment |
反应器进水为人工配制低浓度NH4+-N污水(以N计约为50 mg·L-1), 具体组成如下:NH4Cl 190 mg·L-1(N约50 mg·L-1), K2HPO4 50 mg·L-1, CaCl2·2H2O 20 mg·L-1, MgSO4·7H2O 25 mg·L-1以及1 mL·L-1的微量元素, 微量元素配方见文献[16].为了降低异养菌的影响, 所配制污水中不外加任何有机物质.接种污泥来源于某城市污水处理厂A2O工艺中的好氧池(污泥浓度约3.6 g·L-1, 污泥SVI为95 mL·g-1), 该A2O工艺SRT为10 d, HRT为8 h.接种后两反应器初始污泥浓度(以MLVSS计)均约为2.2 g·L-1.
1.3 分析方法NH4+-N、NO2--N、NO3--N、TN和MLSS/MLVSS等水质指标分别按文献[17]中规定的纳氏试剂光度法、N-(1-萘基)-乙二胺光度法、紫外分光光度法、过硫酸钾氧化法、重量法等进行测定; pH由雷磁PHSJ-4A型pH计测定; 温度和DO浓度采用哈希便携式溶解氧测定仪(HQ30d)分析; 污泥形态通过OLYMPUS CX41型显微镜及数码相机观察.
采用Illumina PE250测序平台进行生物信息学分析, 包括DNA抽提、PCR扩增、PE文库构建和Illumina测序, 具体分析步骤参见文献[18].
2 结果与讨论 2.1 反应器硝化效能及污泥形态整个研究过程中, 两反应器均维持稳定的进水容积负荷[约为150 g·(m3·d)-1].因RH和RL中DO浓度不同, 二者所表现出的硝化效能亦有不同. RH中NH4+-N去除率始终保持在约100%, 即本研究期间RH的硝化能力受进水负荷限制而维持在约150 g·(m3·d)-1; 对于RL, 因硝化菌活性受低氧环境抑制, RL的初始硝化效能较RH显著下降, 即出水中有较高浓度的NH4+-N存在, 但持续运行约三周之后, RL中NH4+-N去除负荷开始呈上升趋势, 第70 d时其数值达88.5 g·(m3·d)-1(表 1).需要指出的是, 本研究期间RH和RL中均无NO2--N累积的现象, 表明了单纯低氧控制难以用于短程硝化工艺的启动.
|
|
表 1 第70 d时RH和RL的运行状况 Table 1 Performance of the RH and RL reactors at day 70 |
污泥表观特征的观察结果也表明了不同溶氧条件下硝化污泥形态的不同.如图 2所示, RH中污泥形态多以边缘清晰、结构致密的微聚体为主, 这亦与其良好的污泥沉降性能(SVI=82 mL·g-1)相符; 而RL中污泥形态则以松散且无规则构型的絮体为主.污泥形态的不同表明了物质(如O2)传质阻力的不同[19, 20], 即RL中DO浓度较低(O2扩散驱动力低), 松散的絮体结构有利于絮体内好氧微生物对O2的获取.需要指出的是, 不同于污泥微膨胀技术[21], 本研究中长期低DO浓度下运行的RL中并无丝状菌产生.

|
(a)RH中污泥形态; (b)RL中污泥形态 图 2 第70 d时的污泥形态 Fig. 2 Microscopic images of the sludge at day 70 |
表 2为第70 d时两反应器内细菌多样性的特征.从OUT数以及ACE和Chao1指数可知RL比RH具有更高的物种丰度; 由Shannon和Simpson指数也显示RL中种群多样性显著高于RH.低氧环境较高氧环境具有更高的物种多样性亦被其他研究者证实[22, 23].正如Girvan等[13]报道:高的物种多样性往往表明了该生物系统(或工艺)具有较高的功能稳定性.因此, 成熟的低氧硝化工艺可能比高氧硝化工艺表现出更高的功能稳定性.
|
|
表 2 第70 d时RH和RL中细菌多样性指数 Table 2 Diversity estimators of the bacterial phylotypes in the RH and RL reactors at day 70 |
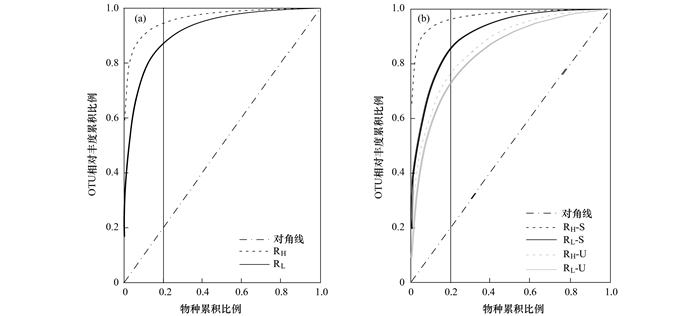
如前所述, 微生物种群与系统功能之间的关系除了与所含物种丰富度密切相关, 还受微生物组成的均匀性或功能组织性(Fo)显著影响[15, 24].如Wittebolle等[15]指出的微生物种群的均匀性越高, 该系统在应对环境冲击时的功能稳定性越好. Pareto-Lorenz(PL)曲线常被用于描述微生物种群的功能组织性特征, 如图 3所示.从中可以看出, 尽管两个反应器中的微生物种群都具有较好的功能组织性(Fo>0.8), 但RL与RH相比仍然表现出更好的微生物组成均匀性, 尤其针对二者共有的物种[图 3(b)].因此, 基于上述结果可以推测低氧条件下运行的硝化工艺其功能稳定性可能更高.
|
(a) RH和RL中总OUTs; (b)RH和RL共有的OUTs(R-S)与独有的OUTs(R-U) 图 3 RH和RL中OUTs的Pareto-Lorenz曲线 Fig. 3 Pareto-Lorenz curves derived from RH and RL OTUs |
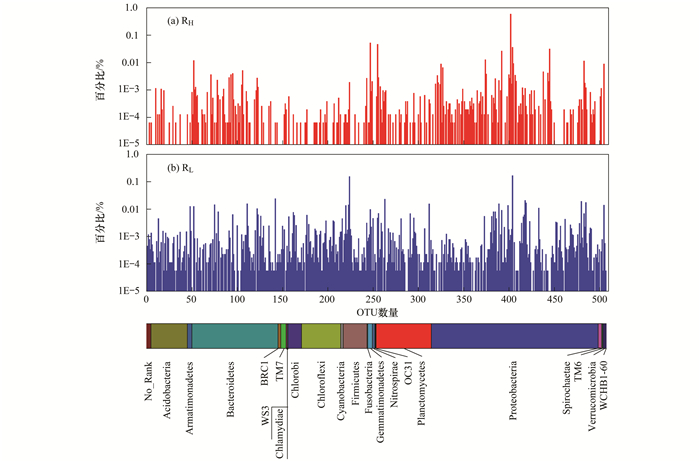
图 4显示了不同DO浓度条件下微生物种群在门分类水平上的组成特征.两个反应器中总共包含21个可被鉴定的门类, 尽管从门的种类上来看, RL与RH的微生物种群组成基本相同.但是从单个门类的相对丰度或构成来看, RL与RH中的微生物种群组成存在显著的差异.例如, RH中以Proteobacteria门为绝对优势种群, 其相对丰度占RH中总物种的百分比高达80.7%;而在RL中则以Proteobacteria (43.8%), Firmicutes (20.0%)以及Bacteroidetes (15.1%)为共同主导者.因此, 从图 4中亦可看出RL中微生物种群组成比RH更加丰富、均匀.
|
图 4 RH和RL中微生物种群的系统发育光谱图 Fig. 4 Phylogenetic spectra of microbial communities from RH and RL |
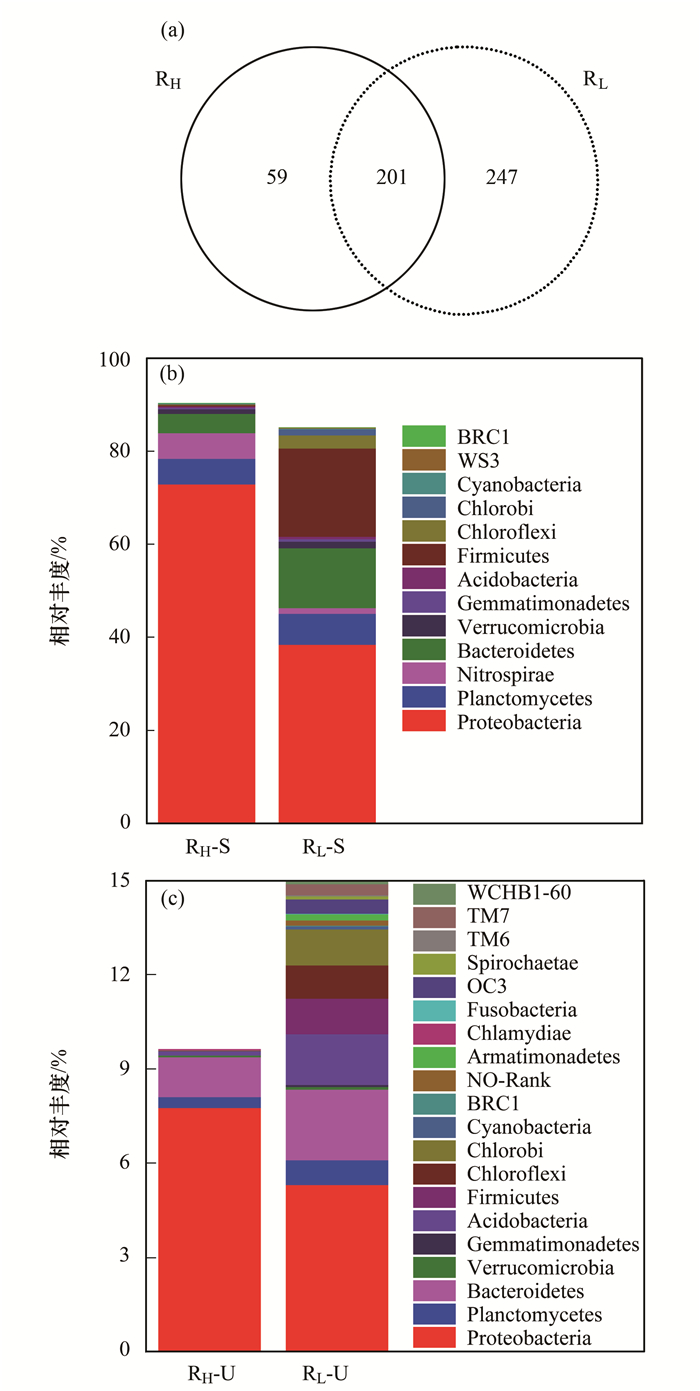
为了揭示RL与RH之间微生物种群的异同, 本文进一步对所得微生物种群信息进行了对比分析, 结果如图 5所示.两反应器中有201种OTUs属于共有[图 5(a)], 这些共用OTUs占两反应器中总微生物信息量的85%以上[图 5(b)], 如此高比例的共有信息亦表明了两反应器中微生物的同源性.然而, 部分共有物种在相对丰度上的显著差异也说明了在不同DO浓度形成的选择压驱动下这些物种不同的生活特性, 如Firmicutes与Bacteroidetes在RH-S与RL-S中的相对丰度分别为0.3%与4.1%和20.0%与12.9%, 表明了隶属于Firmicutes与Bacteroidetes的共有物种更倾向于在低DO浓度环境下生存; 而Proteobacteria与Nitrospirae在RH-S与RL-S中的相对丰度分别为72.9%与5.5%和38.4%与1.2%, 表明Proteobacteria与Nitrospirae的部分种群更趋于在较高DO浓度条件下繁殖.而对于独有物种, 尽管RL中新生了大量的独有物种(占RL中所有OTUs的55%), 但它们所含细菌序列信息仅占RL中总序列信息的15%以下[图 5(c)], 同时, RH与RL所含独有物种的功能组织性基本一致[图 3(b)], 说明这些独有物种对两反应器所表现出的微生物种群组成分化贡献较小.换言之, 由于DO浓度不同造成的RH与RL之间微生物种群分化演变主要发生在共有物种之间, 这一结论与Ma等[22]的报道一致.
|
(a)OTUs韦恩图; (b)共有物种组成; (c)独有物种组成 图 5 RH与RL中微生物种群演化 Fig. 5 Microbial evolution between RH and RL |
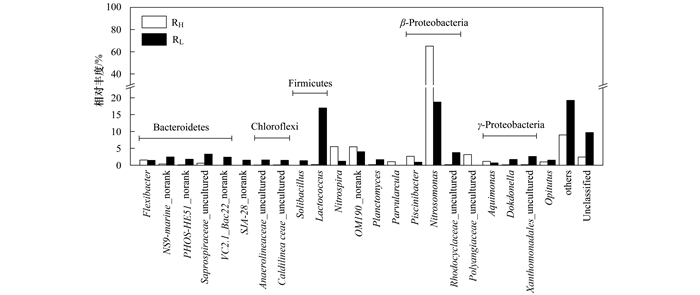
为了获得更加深入的对比信息, 本研究从属水平上对RH与RL所含主要物种(相对丰度>1%)进行了对比分析, 如图 6所示.可以看出RH与RL所含主要物种在属水平上的差异更加明显.在高DO浓度下运行的RH中Nitrosomonas菌属被高度富集, 相对丰度达65.1%, 除Nitrospira、OM190_norank、Polyangiaceae_uncultured、Flexibacter及Aquimonas之外, 其他菌属相对丰度均在1%以下, 即RH中微生物种群组成表现出极高的不均匀性.对于RL中微生物种群, 尽管以Nitrosomonas (18.7%)和Lactococcus (17.0%)占据主导, 但其中相对丰度>1%的菌属高达18类之多, 整体微生物种群均匀性显著高于RH中微生物种群.此外, 从所含菌属代谢特征上而言, 除了大量共有的好氧细菌(如Nitrosomonas和Nitrospira), 与RH相比RL中还含有大量可进行水解发酵作用的菌属, 如Lactococcus、Anaerolineaceae以及Rhodocyclaceae等, 这亦和RL中较低的DO浓度运行环境相呼应(尽管絮体结构较为松散).
|
图 6 RH和RL中微生物种群在属水平上的相对丰度 Fig. 6 Relative abundances of the predominant phylogenetic groups of RH and RL at the genus level |
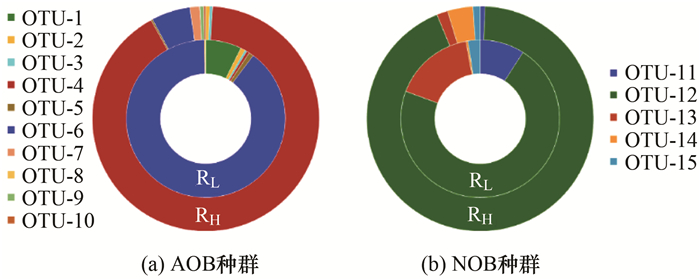
图 7展示了两反应器中硝化功能菌群的组成, 尽管RH与RL所含硝化菌OTUs种类基本一致, 但在个别OUT的相对丰度上差异显著.如图 7(a)所示, RH与RL中AOB种群所含OTUs均为8个, 但优势物种各不相同, 即OUT-4(Nitrosomonas oligotropha)为RH中优势AOB物种, 而RL中AOB则以OUT-6(Nitrosomonas europaea)为主导.然而, RH与RL中NOB种群不仅所含OTUs数目相同(5个)且主导物种也一致, 即均为OTU-12(Nitrospira defluvii)[图 7(b)].有趣的是RH和RL中AOB/NOB相对丰度之比基本一致(11.6和12.3).
|
图 7 RL和RH中AOB和NOB的种群组成 Fig. 7 Community structure of AOB and NOB in the RL and RH reactors |
根据生态学r/K对策理论, Nitrosomonas oligotropha一般被认为属于K-AOB(即具有高基质亲和性和低生长速率), 而Nitrosomonas europaea则被归为r-AOB(即具有低基质亲和性和高生长速率)[25].因此, DO浓度或NH4+-N浓度高低是筛选不同类型AOB的关键环境因子.针对DO浓度高低与AOB种群的关系已有大量研究, 但所得结果不尽一致, 如Bellucci等[10]报道在高低DO条件下Nitrosomonas oligotropha-AOB均占据优势, 而Liu等[6]发现Nitrosomonas europaea-AOB在并行的高低DO浓度硝化工艺中均是优势物种, 更有Park等[8]报道DO浓度由高到低的变化导致了AOB优势物种由Nitrosomonas oligotropha转变为Nitrosomonas europaea, 并且上述有关DO浓度与AOB种群关系的报道均与本研究结果不符.综上可知, NH4+-N浓度(< 0.3 mg·L-1)应是造成RH与RL中富集出不同AOB优势种群的关键因素, 即RH始终在极低NH4+-N浓度条件下运行从而筛选出对NH4+-N有较高亲和力的Nitrosomonas oligotropha-AOB, 而RL中长期拥有较高浓度的剩余NH4+-N得以使r-AOB Nitrosomonas europaea被富集.正如Bollmann等[26, 27]证实的Nitrosomonas oligotropha比Nitrosomonas europaea具有更高的NH4+-N亲和性.
Nitrospira defluvii作为Nitrospira-NOB的一个重要分支, 其生态学特征属于典型的K对策者[28].因此, 研究者对Nitrospira defluvii的富集亦多是在持续低DO浓度和低NO2--N的环境下实现的[29, 30], Lücker等[31]甚至通过宏基因组技术发现所富集的Nitrospira defluvii细胞内缺乏超氧化物歧化酶(SOD).然而, 有别于上述报道, 本研究结果显示Nitrospira defluvii可以同时在高低DO浓度条件下被富集.基于以上论述可以推测, 控制环境中较低的NO2--N浓度(< 0.5 mg·L-1), 而非DO浓度才是筛选Nitrospira defluvii的关键因子.如前文所述, 尽管RH与RL分别在不同的DO浓度下运行, 两反应器却表现出了相似的硝化特征, 即均无NO2--N累积现象的发生, 从而导致RH与RL中NOB优势种群均为Nitrospira defluvii.至于为何RH与RL两反应器在AOB数量是NOB十几倍之多的前提下均未发生NO2--N的显著累积有待深入研究.
3 结论(1) 分别在高DO浓度(2.0±0.1 mg·L-1)和低DO浓度(0.2~0.3 mg·L-1)条件下运行的RH和RL均可实现有效的硝化过程, 但低DO浓度导致RL启动缓慢.
(2) 与RH相比, RL中微生物种群具有更高的多样性和均匀性, 表明了低氧硝化工艺应有更高的功能稳定性.
(3) DO浓度的不同造成了RH和RL中微生物种群组成的分化, 该分化主要表现为共有物种在相对丰度上的差异. Proteobacteria(80.7%)在RH中被高度富集, 而在RL中则以Proteobacteria (43.8%), Firmicutes (20.0%)以及Bacteroidetes (15.1%)为共同主导者; 与RH相比RL中含有大量可进行水解发酵作用的菌属.
(4) RH和RL中的AOB分别以Nitrosomonas oligotropha和Nitrosomonas europaea为优势物种, 而NOB均以Nitrospira defluvii为主导.反应器中NH4+-N和NO2--N浓度(而非DO浓度)是上述硝化菌群被选择性富集的关键因素.
| [1] | McCarty P L, Bae J, Kim J. Domestic wastewater treatment as a net energy producer-Can this be achieved[J]. Environmental Science & Technology, 2011, 45(17): 7100-7106. |
| [2] | 张自杰, 林荣忱, 金儒霖. 排水工程下册[M]. 第四版. 北京: 中国建筑工业出版社, 2000. |
| [3] | Arnaldos M, Pagilla K R. Implementation of a demand-side approach to reduce aeration requirements of activated sludge systems:directed acclimation of biomass and its effect at the process level[J]. Water Research, 2014, 62: 147-155. DOI:10.1016/j.watres.2014.05.040 |
| [4] | Metcalf & Eddy. Wastewater engineering:treatment and reuse[M]. 4th ed. Boston: McGraw-Hill, 2003. |
| [5] | Abbassi B, Dullstein S, Räbiger N. Minimization of excess sludge production by increase of oxygen concentration in activated sludge flocs; Experimental and theoretical approach[J]. Water Research, 2000, 34(1): 139-146. DOI:10.1016/S0043-1354(99)00108-6 |
| [6] | Liu G Q, Wang J M. Long-term low do enriches and shifts nitrifier community in activated sludge[J]. Environmental Science & Technology, 2013, 47(10): 5109-5117. |
| [7] | Fitzgerald C M, Camejo P, Oshlag J Z, et al. Ammonia-oxidizing microbial communities in reactors with efficient nitrification at low-dissolved oxygen[J]. Water Research, 2015, 70: 38-51. DOI:10.1016/j.watres.2014.11.041 |
| [8] | Park H D, Noguera D R. Evaluating the effect of dissolved oxygen on ammonia-oxidizing bacterial communities in activated sludge[J]. Water Research, 2004, 38(14-15): 3275-3286. DOI:10.1016/j.watres.2004.04.047 |
| [9] | Arnaldos M, Kunkel S A, Stark B C, et al. Characterization of heme protein expressed by ammonia-oxidizing bacteria under low dissolved oxygen conditions[J]. Applied Microbiology and Biotechnology, 2014, 98(7): 3231-3239. DOI:10.1007/s00253-013-5400-1 |
| [10] | Bellucci M, Ofiţeru I D, Graham D W, et al. Low-dissolved-oxygen nitrifying systems exploit ammonia-oxidizing bacteria with unusually high yields[J]. Applied and Environmental Microbiology, 2011, 77(21): 7787-7796. DOI:10.1128/AEM.00330-11 |
| [11] | Wagner M, Loy A. Bacterial community composition and function in sewage treatment systems[J]. Current Opinion in Biotechnology, 2002, 13(3): 218-227. DOI:10.1016/S0958-1669(02)00315-4 |
| [12] | Ju F, Zhang T. Bacterial assembly and temporal dynamics in activated sludge of a full-scale municipal wastewater treatment plant[J]. The ISME Journal, 2015, 9(3): 683-695. DOI:10.1038/ismej.2014.162 |
| [13] | Girvan M S, Campbell C D, Killham K, et al. Bacterial diversity promotes community stability and functional resilience after perturbation[J]. Environmental Microbiology, 2005, 7(3): 301-313. DOI:10.1111/emi.2005.7.issue-3 |
| [14] | Briones A, Raskin L. Diversity and dynamics of microbial communities in engineered environments and their implications for process stability[J]. Current Opinion in Biotechnology, 2003, 14(3): 270-276. DOI:10.1016/S0958-1669(03)00065-X |
| [15] | Wittebolle L, Marzorati M, Clement L, et al. Initial community evenness favours functionality under selective stress[J]. Nature, 2009, 458(7238): 623-626. DOI:10.1038/nature07840 |
| [16] | van de Graaf A A, de Bruijn P, Robertson L A, et al. Autotrophic growth of anaerobic ammonium-oxidizing micro-organisms in a fluidized bed reactor[J]. Microbiology, 1996, 142(8): 2187-2196. DOI:10.1099/13500872-142-8-2187 |
| [17] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002. |
| [18] | Liu W R, Yang D H, Chen W J, et al. High-throughput sequencing-based microbial characterization of size fractionated biomass in an anoxic anammox reactor for low-strength wastewater at low temperatures[J]. Bioresource Technology, 2017, 231: 45-52. DOI:10.1016/j.biortech.2017.01.050 |
| [19] | Manser R, Gujer W, Siegrist H. Consequences of mass transfer effects on the kinetics of nitrifiers[J]. Water Research, 2005, 39(19): 4633-4642. DOI:10.1016/j.watres.2005.09.020 |
| [20] | Arnaldos M, Amerlinck Y, Rehman U, et al. From the affinity constant to the half-saturation index:understanding conventional modeling concepts in novel wastewater treatment processes[J]. Water Research, 2015, 70: 458-470. DOI:10.1016/j.watres.2014.11.046 |
| [21] |
王中玮, 彭永臻, 王淑莹, 等. 不同运行方式下低溶解氧污泥微膨胀的可行性研究[J]. 环境科学, 2011, 32(8): 2347-2352. Wang Z W, Peng Y Z, Wang S Y, et al. Feasibility study for limited filamentous bulking under low dissolved oxygen at different operation regimes[J]. Environmental Science, 2011, 32(8): 2347-2352. |
| [22] | Ma J X, Wang Z W, Yang Y, et al. Correlating microbial community structure and composition with aeration intensity in submerged membrane bioreactors by 454 high-throughput pyrosequencing[J]. Water Research, 2013, 47(2): 859-869. DOI:10.1016/j.watres.2012.11.013 |
| [23] | Gao D W, Fu Y, Tao Y, et al. Linking microbial community structure to membrane biofouling associated with varying dissolved oxygen concentrations[J]. Bioresource Technology, 2011, 102(10): 5626-5633. DOI:10.1016/j.biortech.2011.02.039 |
| [24] | Marzorati M, Wittebolle L, Boon N, et al. How to get more out of molecular fingerprints:practical tools for microbial ecology[J]. Environmental Microbiology, 2008, 10(6): 1571-1581. DOI:10.1111/emi.2008.10.issue-6 |
| [25] | Dytczak M A, Londry K L, Oleszkiewicz J A. Activated sludge operational regime has significant impact on the type of nitrifying community and its nitrification rates[J]. Water Research, 2008, 42(8-9): 2320-2328. DOI:10.1016/j.watres.2007.12.018 |
| [26] | Bollmann A, Bär-Gilissen M J, Laanbroek H J. Growth at low ammonium concentrations and starvation response as potential factors involved in niche differentiation among ammonia-oxidizing bacteria[J]. Applied and Environmental Microbiology, 2002, 68(10): 4751-4757. DOI:10.1128/AEM.68.10.4751-4757.2002 |
| [27] | Bollmann A, Laanbroek H J. Continuous culture enrichments of ammonia-oxidizing bacteria at low ammonium concentrations[J]. FEMS Microbiology Ecology, 2001, 37(3): 211-221. |
| [28] | Nowka B, Daims H, Spieck E. Comparison of oxidation kinetics of nitrite-oxidizing bacteria:nitrite availability as a key factor in niche differentiation[J]. Applied and Environmental Microbiology, 2015, 81(2): 745-753. DOI:10.1128/AEM.02734-14 |
| [29] | Park M R, Park H, Chandran K. Molecular and kinetic characterization of Planktonic nitrospira spp. selectively enriched from activated sludge[J]. Environmental Science & Technology, 2017, 51(5): 2720-2728. |
| [30] | Spieck E, Hartwig C, McCormack I, et al. Selective enrichment and molecular characterization of a previously uncultured Nitrospira-like bacterium from activated sludge[J]. Environmental Microbiology, 2006, 8(3): 405-415. DOI:10.1111/emi.2006.8.issue-3 |
| [31] | Lücker S, Wagner M, Maixner F, et al. A Nitrospira metagenome illuminates the physiology and evolution of globally important nitrite-oxidizing bacteria[J]. Proceedings of the National Academy of Sciences of the United States of America, 2010, 107(30): 13479-13484. DOI:10.1073/pnas.1003860107 |
 2019, Vol. 40
2019, Vol. 40

