2. 忻州师范学院地理系, 忻州 034000
2. Department of Geography, Xinzhou Teachers University, Xinzhou 034000, China
亚高山淡水湖蕴含着巨大的微生物资源, 在调节气候变化、调控生物地球化学循环和维持生态系统稳定方面发挥重要作用[1].相比于平原湖, 亚高山湖泊中的微生物通常对光照、pH、温度等环境梯度的耐受幅较窄[2], 对气候变化和人为干扰更敏感, 即使是很小的环境改变也能够显著影响亚高山湖泊水体的理化性质, 引起水体生物群落组成和结构的变化, 进而影响水生生态系统的功能[3, 4].细菌群落作为水生微生物食物网的重要组成部分, 在淡水湖生态系统中的营养循环和物质转化过程中发挥着重要作用[5].由于亚高山湖泊位于林线附近, 气候的小幅波动会引起林线上下迁移, 同时会伴随入湖营养盐、溶解有机碳等关键环境因子变化, 最终可能会引起湖泊生态系统的显著变化[6].因此研究细菌群落时空分布格局的形成机制及其对环境变化的响应有助于揭示湖泊生态系统功能的变化, 最终预测生态系统对当前以及未来环境变化的响应[7].目前, 大量的研究表明在湖泊水体中, 细菌群落的组成和多样性受到环境因素的影响, 如温度[8]、溶解氧[9]、营养物质[10]等; 同时季节变化和水体深度也是影响细菌群落多样性格局的重要因子[11, 12].虽然, 针对环境变化和时空变异对水体细菌群落结构影响的相对重要性已有初步研究[13, 14], 但是就亚高山湖中细菌群落时空格局维持机制的研究还较少.
宁武天池湖泊群位于山西省管涔山麓地, 是华北地区唯一的亚高山湖泊群[15].张俊芳等[16]通过调查该湖群中浮游植物群落, 发现由于气候变化和人类活动的影响, 湖水受到碳、氮和磷的污染, 呈现酸化的趋势, 引起湖水中浮游植物群落多样性的显著变化.天池群共有大小不一的15个湖泊, 多数湖泊已经干涸, 目前常年有水的公海湖, 水位也在逐年下降.公海是天池湖泊群中海拔最高、最深的湖泊, 周围地势高耸, 湖水主要靠降水和地下水补给, 属完全封闭的小型淡水湖泊.随着全球气候变化和旅游开发的扩展, 湖水可能受到大气氮干沉降、雨水冲刷引起的氮湿沉降和人类旅游导致的垃圾污染, 但人们没有对这些指标进行直接测量; 公海湖周围遍布水草, 其根系分泌物和凋落物也可能对湖泊生态系统产生影响; 而周围少农田, 不存在施肥导致的面源污染.因此, 公海湖是评估人为干扰对微观生态系统影响的理想环境[17].那么, 湖泊中微生物群落的多样性和结构动态有什么样的特征呢?本研究通过分析公海湖中细菌群落的丰度变化和多样性格局, 旨在探讨以下问题:①影响水体细菌群落丰度和α多样性变化的原因; ②不同季节湖内不同深度的细菌群落的空间分布格局差异及影响机制.
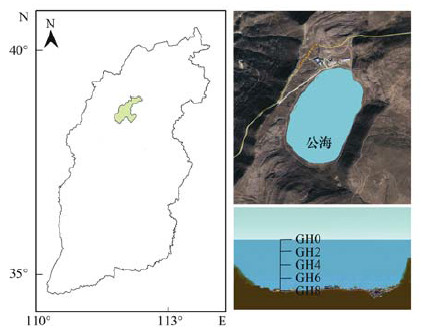
1 材料与方法 1.1 研究区概况与样品采集宁武天池湖泊群总面积约4 km2, 处于海拔1 771~1 849 m之间, 属典型季风边缘区, 是黄土高原和浑善达克沙地的过渡地带.年均气温7.7℃, 年降水量约460 mm. 2017年4~12月进行野外调查取样.本实验所用样品采集于常年有水的公海(GH)(38.91°N, 112.23°E), 面积0.36 km2, 水深8 m左右, 蓄水540万m3(图 1).在GH中心区域, 沿垂直方向从表层到湖底每隔2 m为一个采样点, 共有5个采样点(GH0、GH2、GH4、GH6和GH8), 在每个采样点取3个重复.利用采水器收集水样3 L, 装于无菌的塑料桶中运回实验室.通过聚碳酸酯膜(0.2 μm, ϕ 50 mm, Millipore, 津腾, 天津)过滤2.5 L, 然后将粘附微生物的滤膜置于无菌离心管中, 保存于-20℃冰箱, 用于微生物DNA的提取, 剩余的0.5 L用于水样理化性质分析.
|
GH0、GH2、GH4、GH6、GH8为不同深度的采样点 图 1 样地示意和采样点设置 Fig. 1 Schematic diagram of sampling site and the sampling depth profile |
用便携式水质监测仪(Aquread AP-2000, UK)原位测定水体温度(T)、酸碱度(pH)、溶解氧(DO)、电导率(EC), 盐度(SAL), 硝氮(NO3-)和铵态氮(NH4+); 用TOC分析仪(Shimadzu, TOC-VCPH, Japan)测定总碳(TC)、总有机碳(TOC)和无机碳(IC)含量; 亚硝氮(NO2-)、硫酸盐(SO42-)和磷酸盐(PO43-)含量用全自动间断化学分析仪(Cleverchem Anna, DeChem-Tech, Germany)测定.
1.3 样品DNA提取和PCR扩增水样宏基因组DNA提取:先用1×PBS缓冲液洗脱滤膜上的微生物, 然后利用水体快速提取试剂盒(MP Biomedicals, Solon, OH, USA)提取样本的DNA, 用ddH2O溶解, 作为实时荧光定量PCR和变性梯度凝胶电泳-基因扩增(DGGE-PCR)的模板, -20℃保存.DGGE-PCR的正向引物为带有GC夹子的341F(5′-CGCCCGCCGCGCGCGGCGGGCGGG GCGGGGGCACGGGGGGCCTACGGGAGGCAGCAG-3′), 反向引物为534R(5′-TTACCGCGGCTGCTGG CAC-3′), 扩增细菌的16S rDNA V3区片段, 扩增产物进行DGGE分析.扩增体系和反应条件详见文献[18]的描述.实时荧光定量PCR扩增细菌的16S rDNA V3区片段, 正向引物为338F (5′-ACTCCTA CGGGAGGCAGCA-3′), 反向引物为534R(5′-TTAC CGCGGCTGCTGGCAC-3′).扩增体系和反应条件参照Liu等[19]的方法进行.
1.4 DGGE分析实验PCR扩增产物先通过2%的凝胶电泳鉴定, 条带清晰、无明显的引物二聚体, 然后继续进行DGGE分析, 变性胶的质量分数为10%(质量浓度), 变性梯度是45%~65%, 然后用DCode DGGE电泳仪(Bio-Rad, USA)跑胶.电泳在电压65 V, 温度60℃的1×TAE缓冲液中进行, 电泳时间为12 h.电泳完成后, 凝胶用硝酸银溶液染色10 min, 然后加入预冷的氢氧化钠溶液, 在摇床上缓慢振荡15 min, 用去离子水冲洗掉过量的染色和显色液, 然后用凝胶成像系统(Gel Doc TM XR, Bio-Rad, USA)扫描染色的凝胶, 获得DGGE条带图像, 并通过图像处理软件(Quantity one v4.62, Bio-Rad, USA)分析DGGE条带图像.通过软件半自动识别每个泳道DNA条带的数量、宽度和亮度.在每个泳道中具有相同迁移距离的条带被认为代表相同的操作分类单元.
1.5 数据分析对同一个月份不同深度间水体的理化参数差异和群落拷贝数变化采用SPSS 20.0软件的one-way ANOVA分析, 并通过LSD检验进行多重比较, 最后通过SigmaPlot 14.0软件作图.通过R软件分析群落α多样性(vegan程序包)并作图(ggplot2程序包).用CANOCO软件的PCoA(主坐标分析)分析群落的空间分布格局.在R软件中对所有理化因子进行了膨胀因子筛选(vegan程序包), 消除了共线性高的理化因子, 然后通过前选择筛选出对群落结构有显著影响的理化因子, 通过Pearson相关性(psych程序包)分析不同环境因子对群落多样性的影响.通过冗余分析(RDA)(vegan程序包)分析不同环境因子对群落结构的影响程度, 并通过方差分解(VPA)(vegan程序包)进一步验证环境因子和空间距离对群落构建影响的相对贡献.所有统计分析过程的置信区间均为95% (P < 0.05).
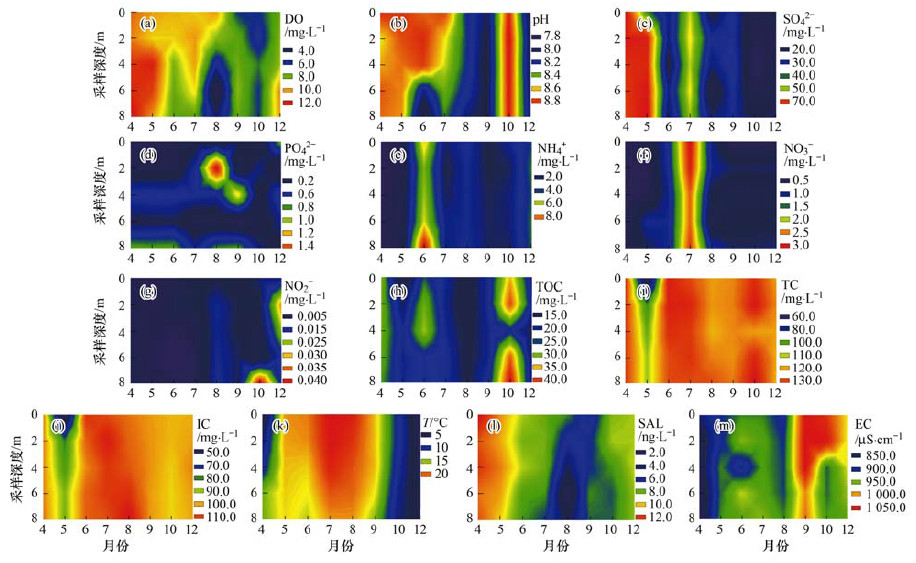
2 结果与分析 2.1 水体理化性质的时空动态水体理化参数在各采样深度间存在差异, 且不同因子的变化趋势不同(图 2), 形成一定的生境梯度.所有月份的T、pH、DO、EC、SAL和NH4+在不同的采样深度间差异显著.在6月和12月, 其它7个理化因子(SO42-、PO43-、NO3-、NO2-、TOC、TC和IC)在不同采样深度间也存在显著差异(P < 0.05).T表现出显著的季节性变化, 从4~8月逐渐升高, 在8月达到最大值而后降低, 其中5~10月的T随着采样深度的增加而降低, 而在4月和12月随着采样深度的增加而增加.pH从4~12月整体呈逐渐下降的趋势, 其中5~8月随着采样深度的增加而降低; SAL从4月开始逐月降低, 到9月达到最小值, 之后开始升高, 其中除了4月和6月随着采样深度的增加呈先下降后升高的趋势, 其余月份均是先增加后减小.而NO2-的浓度在4、5、8和9月不同深度没有显著的变化; TOC和IC的浓度在8月和9月不同深度没有显著的变化; NO3-的浓度只在8月不同深度间没有显著的变化, 其它月份变化显著(P>0.05).
|
图 2 湖泊水体理化参数的时空动态 Fig. 2 Spatio-temporal dynamics of water physiochemical parameters for Gonghai Lake |
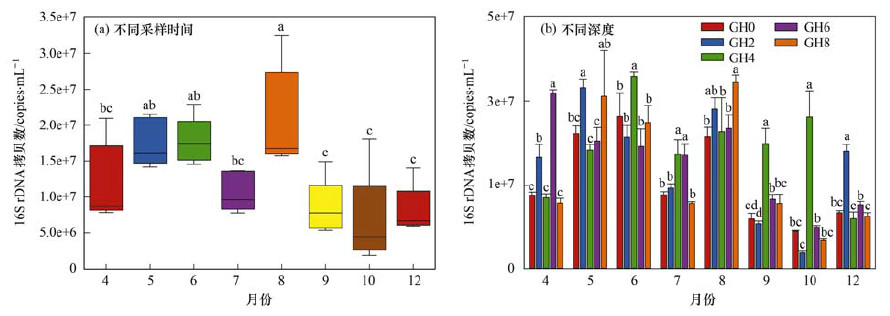
Q-PCR结果显示, 从4~12月细菌群落的丰度有显著变化(时间动态以不同深度的细菌群落丰度为重复), 从4~6月逐渐增加, 但是在7月却突然降低, 在8月达到峰值, 而后逐渐降低[图 3(a)].各月份不同深度的细菌丰度均有显著性差异, 表现为中层水细菌的丰度(2、4和6 m)较高, 除5月和8月外, 均表现为表层和底层水中细菌的丰度(0 m和8 m)相对较低[图 3(b)].
|
图 3 不同采样时间和不同深度水体细菌丰度的变化 Fig. 3 Dynamics of bacterial abundance in the water of Gonghai Lake at different depths and times |
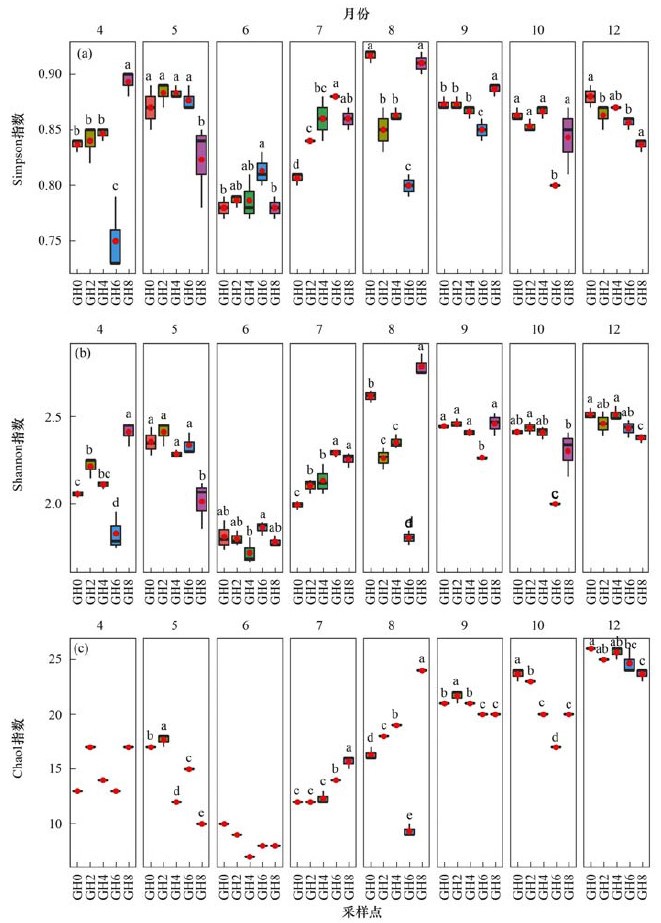
经DGGE分析获得各采样点细菌群落的丰富度和多样性指数.结果表明, 各月份不同深度间群落多样性指数(Simpson和Shannon指数)均有显著性差异, 说明细菌群落的α多样性在不同深度之间有明显的变化[图 4(a)和4(b)], 其中在5~7月的中层水中多样性相对较高; 12月份随着采样深度增加逐渐降低, 其它4个月在中层水中多样性均较低.丰富度指数(Chao1)除了4月和6月外, 其它月份在不同深度取样点均有显著性差异, 其中7、8月沿取样深度有增加的趋势, 并在底层达到最大, 其它月份均是表层水(0 m)较高.从4~12月整体上呈现先减小后增加的趋势[图 4(c)].
|
图 4 不同采样时间和不同深度间细菌群落的α多样性指数 Fig. 4 Phylotype richness and α diversity estimators of the bacteria communities at different depths and times |
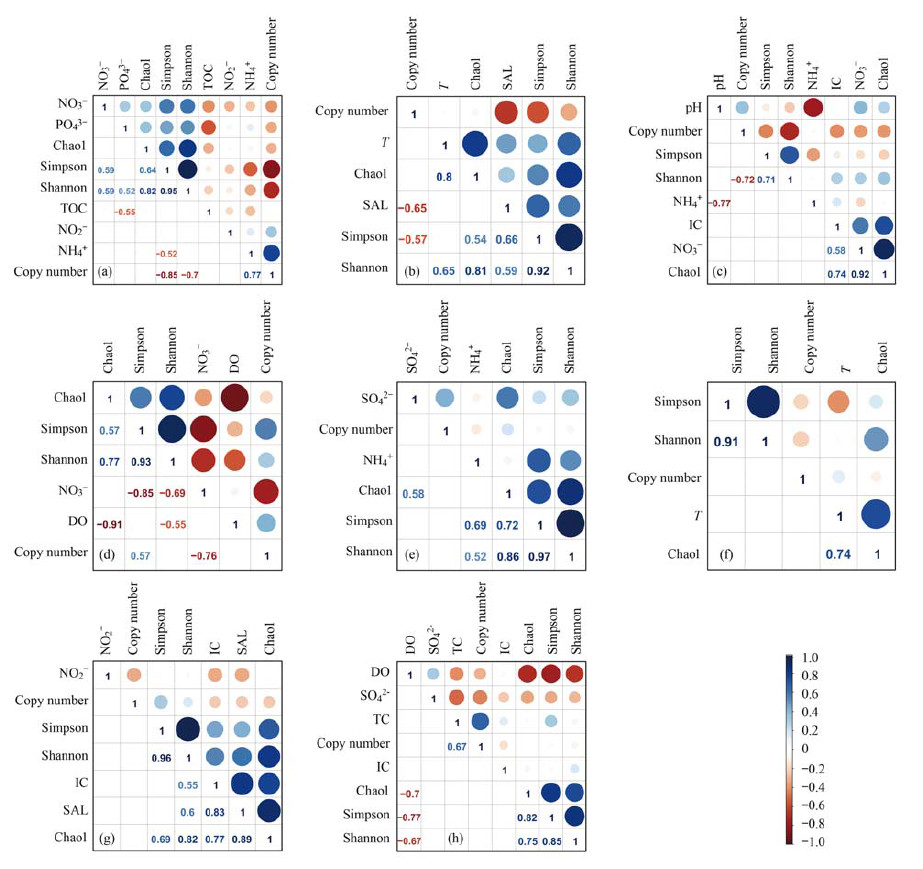
细菌群落α多样性与环境因子的相关性分析表明, 不同深度细菌群落的α多样性主要与水体T、DO和SAL浓度显著相关(图 5).其中, 4月和12月的细菌丰度分别与NH4+和TC浓度显著正相关, 而在5月和7月细菌丰度分别与SAL和NO3-显著负相关[图 5(a)、5(b)、5(d)和5(h)]; Simpson和Shannon指数在4月和8月均与NH4+显著相关, 而5月份和10月份主要与SAL显著相关[图 5(a)、5(b)、5(e)和5(g)]; Chao1指数在5月份和9月份与T显著正相关, 在6月和10月与IC显著正相关[图 5(b)、5(c)、5(f)和5(g)]; 在12月, 多样性指数与丰富度指数均与DO显著负相关[图 5(h)].
|
(a)~(h)分别为不同的采样月份:4、5、6、7、8、9、10和12月, 下同; 数字代表显著相关系数, 红色表示负相关, 蓝色表示正相关, 颜色越深相关性越大, P < 0.05 图 5 理化因子与细菌群落α-多样性的相关性分析 Fig. 5 Correlation analysis between physicochemical factors and bacterial community diversity |
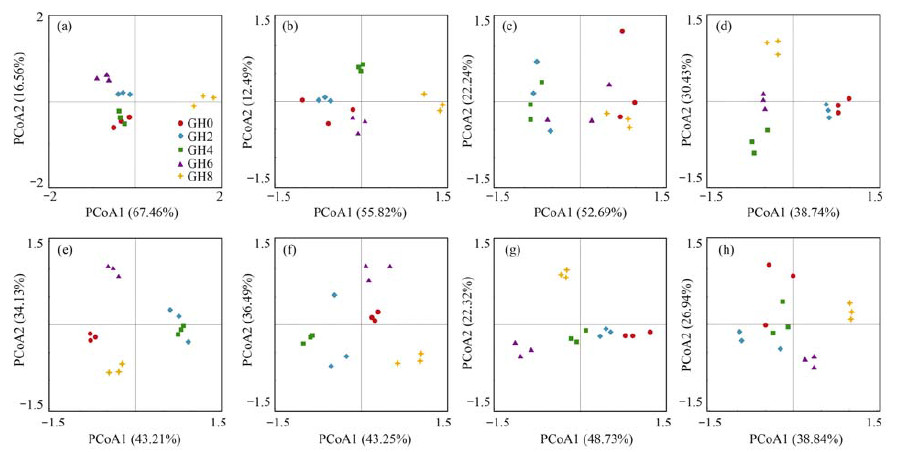
基于Bray-Curtis的PCoA排序结果显示, 在不同采样时间和不同深度间细菌群落的空间分布格局具有明显的差异(图 6).除6月外, 其余7个月细菌群落的分布格局在不同深度间均存在差异, 尤其是底层水体中的细菌群落格局明显与其它水层不同.通过PERMANOVA组间差异检验进一步表明, 不同深度间的细菌群落具有明显不同的空间分布格局(P < 0.001), 见表 1.
|
图 6 PCoA排序分析不同月份水体细菌群落的分布格局 Fig. 6 Principal coordinates analysis indicating the distribution patterns of bacterial communities at different times |
|
|
表 1 PERMANOVA组间差异检验1) Table 1 Inter-group difference test of PERMANOVA |
2.4 细菌群落空间格局多样性的驱动因素
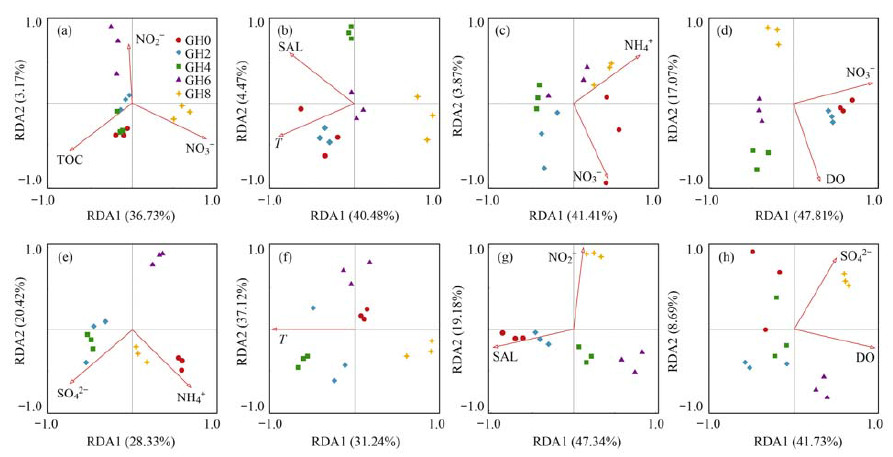
通过前选择筛选出对细菌群落空间分布有显著影响的环境因子, 这些环境因子对不同深度的群落空间结构的影响在每个月份均显著(P < 0.05).RDA分析结果表明, 不同的环境因子对不同深度细菌群落结构的影响程度和方式不一样, 其中无机氮(NO3-、NO2-和NH4+)浓度对细菌群落结构影响较大, 但是在不同月份间主要的影响因子存在差异(图 7).
|
图 7 细菌群落与环境因子的RDA分析 Fig. 7 RDA showing the relationship between environmental parameters and bacterial communities |
空间距离对细菌空间分布影响很小, 并且在个别月份中影响不显著(P>0.05)(表 2).4月不同深度细菌群落的空间分布格局受到NO3-、NO2-和TOC的显著影响[图 7(a)](F=2.503, P=0.047), 理化因子对群落分布格局的解释率为26%, 总解释率为49%(P < 0.05)(表 2).5月不同深度细菌群落的空间分布格局受到T、SAL的显著影响[图 7(b)](F=4.900, P=0.006), 理化因子和空间距离的共同解释率为35%, 总解释率为40%(表 2).6月不同深度细菌群落的空间分布格局受到NO3-和NH4+的显著影响[图 7(c)](F=4.964, P=0.005), 所有理化因子对群落分布格局的解释率为50%, 总解释率为59%(表 2).7月不同深度细菌群落的空间分布格局受到NO3-和DO的显著影响[图 7(d)](F=11.084, P=0.001), 理化因子对群落分布格局的解释率为34%, 总解释率为67%(表 2).8月不同深度细菌群落的空间分布格局受到NH4+和SO42-的显著影响[图 7(e)](F=5.708, P=0.003), 理化因子对群落分布格局的解释率为63%, 总解释率为72%(表 2).9月不同深度细菌群落的空间分布格局受T的显著影响[图 7(f)], 解释率为43%(F=5.905, P=0.002), 总解释率为45%(表 2).10月不同深度细菌群落的空间分布格局受到NO2-和SAL的显著影响[图 7(g)](F=11.922, P=0.001), 理化因子对群落分布格局的解释率为24%, 总解释率为61%(表 2).12月不同深度细菌群落的空间分布格局受到DO、SO42-的显著影响[图 7(h)](F=6.103, P=0.001), 所有理化因子对群落分布格局的解释率为23%, 总解释率为43%(表 2).
|
|
表 2 单独的环境因子(E)、单独的空间因素(S)、环境因子和空间因素的交互作用(E∩S)以及环境因子和空间因素的总和(E∪S)对细菌群落多样性分布格局解释率的方差分解结果1) Table 2 Variation partitioning results showing the contribution of environmental (E), spatial (S) and interaction effects (E∩S) as well as the total effect (E∪S) components of the bacterial communities based on the Bray-Curtis distance |
3 讨论 3.1 细菌群落的α多样性及其对环境变化的响应
细菌在湖泊生态系统中有着非常重要的作用, 不仅是淡水生态系统中微生物群落的重要组成部分, 也是湖泊物质能量循环的主要参与者[20].湖泊中的细菌驱动着湖泊生态系统中的生物地球化学循环, 其数量众多且种类丰富[21].细菌还可在一定程度上反映水体污染特征及其生态功能演变[22], 因此可以通过研究其在不同深度及季节下的细菌群落多样性格局, 来反映水体生态系统结构和功能的变化.
本研究中, PO43-的浓度在7~9月表层水体中高于其它月, 通常高浓度的磷是水体污染的标志[23]; 8月水体的NO3-、NO2-、TOC和IC等理化参数在不同深度之间没有显著差异(图 2).细菌丰度在4~12月整体呈现先增加后减少的趋势, 在8月显著高于其它月的细菌丰度, 而7月略有下降, 通过分析表明这种差异性主要与水体营养状况相关(图 5), 这可能是因为夏季降雨量大, 将周边土壤中的营养物质带入水体从而改变了湖泊的环境因子[24], 环境因子的变化使细菌群落的结构特征与功能特征发生变化, 从而对细菌群落的丰度造成了影响[25].7月和9月细菌群落丰度的降低可能是由于旅游旺季导致的人为干扰强烈, 这种物理干扰破坏了湖泊水体的群落结构[26], 进而改变了细菌的丰度.
在不同月份的不同取样深度下, 群落α多样性指数(丰富度和多样性指数)具有显著差异.结果表明, 影响细菌群落α多样性的环境因子主要包括T、DO和其它理化因子(图 5), 说明微生物群落的多样性会受多种环境因子的共同影响而呈现不同的变化.这是因为细菌群落组成和多样性随湖泊深度的变化与环境异质性密切相关, 例如:光照、溶解氧和温度随着水深增加而变化(图 2); 水体初级生产力、营养盐浓度等也沿着水深而发生相应地变化, 这与已有研究结果一致.Adams等[27]的研究表明温度可以增加生态系统中细菌的代谢能力, 湖泊细菌群落组成更多受到了温度的驱动; 而营养盐对于湖泊生态系统来说, 可通过“上行效应”直接影响水体细菌群落的组成和分布[28], 也可通过影响水体细菌的捕食者(异样鞭毛虫和纤毛虫)的组成和丰度, 间接影响水体细菌群落结构和多样性[5].
3.2 细菌群落的空间分布格局和适应机制群落空间分布格局的形成是物种被逐层筛选的结果, 确定性过程和随机过程是微生物群落多样性维持机制的重要原因, 它们的相对重要性决定了微生物群落的分布格局[29].不同生境中的细菌群落多样性维持机制和群落分布格局明显不同[30, 31], 确定和随机过程的相对重要性取决于环境类型、环境条件以及生物体特性.本研究表明, 不同月份以及不同深度间的细菌群落具有明显不同的空间分布格局(图 6), 细菌群落结构均具有显著性差异(P < 0.001), 见表 1, 这种多样性格局受到环境选择(P < 0.01)和扩散限制的双重影响(表 2), 环境选择是主要的驱动力.
空间距离对细菌群落多样性格局的影响很小, 而不同的环境因子对不同深度细菌群落结构的影响程度和方式不同, 说明环境选择在细菌群落构建过程中有重要的作用(图 7).这是由于湖泊(水深≤200 m)水体在垂直层温差较大(ΔT>0.2℃·m-1)的情况下产生的水体分层现象[32, 33], 阻碍了不同深度水体间的垂直物质交换, 进而对湖泊内各种理化过程、生物的新陈代谢和物质分解产生影响[34], 而浅水湖通常被认为是没有产生分层现象的均一体[35].本研究中, 在不同深度的取样点较接近(间隔为2 m), 湖泊不同深度之间的温差小[0~2.5℃·m-1, 图 2(k)], 细菌群落在不同深度间的扩散阻力小, 物种均匀分布, 物种多样性格局只在一定程度受到了空间分布的调控作用(表 3).而6月在不同深度水体中细菌群落空间分布没有明显的分层现象, 这可能是因为在6月频繁的人类活动, 破坏了水体固有的分层现象, 因此不同深度细菌群落的空间分布较其它月份的差异要小; 另一个可能的原因是在6月充沛的降雨附带更多的营养物质流入湖泊, 从而降低了不同深度水体间的营养物质差异, 因此细菌群落的差异性减小[图 6(c)].从方差分解的结果来看, 空间距离和环境因子的交互作用对细菌群落结构的构建也有重要作用, 这是由于空间分布影响了环境因子, 进而改变了细菌群落结构.对于未解释的部分, 可能受到微生物群落种间关系或其他未测量的环境因子的影响.总之, 在GH中确定性过程和随机过程对细菌群落的构建都有影响, 且影响强度在不同月份间存在差异.
就湖泊生态系统而言, 其内部的细菌群落结构及多样性受多种因素制约.本研究结果显示, 无机氮(NO3-、NO2-和NH4+)浓度是驱动细菌群落空间分布格局形成的重要因素, 但是在不同月份间主要的影响因子存在差异(图 7).这可能是由于底物浓度的变化导致参与水体氮循环不同过程的细菌类群的比例发生了变化, 因为细菌群落在不同环境中可表现为不同的生活策略[31], 从而环境因子的变化引起细菌群落结构的变化.随着各种测序技术的进一步发展, 为人们认识湖泊水体细菌的相关功能提供了有利的支持, 也大大促进了人们对湖泊水体细菌生态功能的认识[5].将细菌群落结构和特定生态功能联系起来, 一直是众多微生物生态学家努力解决的问题, 这也是本课题组下一步要解决的问题.
4 结论(1) 在宁武GH亚高山湖泊的细菌群落中(不同月份的不同深度之间), 细菌群落丰度和α多样性(丰富度和多样性指数)具有显著差异, 这种差异性主要与水体营养状况相关.
(2) GH不同深度之间的细菌群落具有明显不同的空间分布格局, 这种多样性格局受到环境选择和扩散限制的双重影响, 而环境选择是主要的驱动力.无机氮(NO3-、NO2-和NH4+)浓度是影响GH亚高山湖泊细菌群落多样性格局的主导因子.
| [1] | Salmaso N. Long-term phytoplankton community changes in a deep subalpine lake:responses to nutrient availability and climatic fluctuations[J]. Freshwater Biology, 2010, 55(4): 825-846. DOI:10.1111/(ISSN)1365-2427 |
| [2] | Battarbee R W, Grytnes J A, Thompson R, et al. Comparing palaeolimnological and instrumental evidence of climate change for remote mountain lakes over the last 200 years[J]. Journal of Paleolimnology, 2002, 28(1): 161-179. DOI:10.1023/A:1020384204940 |
| [3] | Pernthaler J. Competition and niche separation of pelagic bacteria in freshwater habitats[J]. Environmental Microbiology, 2017, 19(6): 2133-2150. DOI:10.1111/1462-2920.13742 |
| [4] | Zaharescu D G, Burghelea C I, Hooda P S, et al. Small lakes in big landscape:Multi-scale drivers of littoral ecosystem in alpine lakes[J]. Science of the Total Environment, 2016, 551-552: 496-505. DOI:10.1016/j.scitotenv.2016.02.066 |
| [5] | Ma Y T, Li J Q, Wu J, et al. Bacterial and fungal community composition and functional activity associated with lake wetland water level gradients[J]. Scientific Reports, 2018, 8: 760. DOI:10.1038/s41598-018-19153-z |
| [6] |
彭佳, 黄春玲, 陈旭. 沉积物记录的亚高山湖泊环境变化——以鄂东南云中湖为例[J]. 地理研究, 2017, 37(1): 220-230. Peng J, Huang C L, Chen X. Sedimentary records of environmental changes of subalpine lakes:A case study of Yunzhong Lake in the southeastern Hubei province[J]. Geographical Research, 2017, 37(1): 220-230. |
| [7] | Bier R L, Voss K A, Bernhardt E S. Bacterial community responses to a gradient of alkaline mountaintop mine drainage in Central Appalachian streams[J]. The ISME Journal, 2015, 9(6): 1378-1390. DOI:10.1038/ismej.2014.222 |
| [8] | Roguet A, Laigle G S, Therial C, et al. Neutral community model explains the bacterial community assembly in freshwater lakes[J]. FEMS Microbiology Ecology, 2015, 91(11): fiv125. DOI:10.1093/femsec/fiv125 |
| [9] | Missaghi S, Hondzo M, Herb W. Prediction of lake water temperature, dissolved oxygen, and fish habitat under changing climate[J]. Climatic Change, 2017, 141(4): 747-757. DOI:10.1007/s10584-017-1916-1 |
| [10] | Vander Zanden M J, Chandra S, Park S K, et al. Efficiencies of benthic and pelagic trophic pathways in a subalpine lake[J]. Canadian Journal of Fisheries and Aquatic Sciences, 2006, 63(12): 2608-2620. DOI:10.1139/f06-148 |
| [11] | Gilbert J A, Steele J A, Caporaso J G, et al. Defining seasonal marine microbial community dynamics[J]. The ISME Journal, 2012, 6(2): 298-308. DOI:10.1038/ismej.2011.107 |
| [12] | Di Cesare A, Eckert E M, Teruggi A, et al. Constitutive presence of antibiotic resistance genes within the bacterial community of a large subalpine lake[J]. Molecular Ecology, 2015, 24(15): 3888-3900. DOI:10.1111/mec.2015.24.issue-15 |
| [13] | Genitsaris S, Monchy S, Viscogliosi E, et al. Seasonal variations of marine protist community structure based on taxon-specific traits using the eastern English Channel as a model coastal system[J]. FEMS Microbiology Ecology, 2015, 91(5): fiv034. |
| [14] | Suh S S, Park M, Hwang J, et al. Characterization of bacterial communities associated with seasonal water masses from Tongyoung in South Sea of Korea[J]. Ocean Science Journal, 2014, 49(3): 193-200. DOI:10.1007/s12601-014-0019-4 |
| [15] |
王鑫, 王宗礼, 陈建徽, 等. 山西宁武天池区高山湖泊群的形成原因[J]. 兰州大学学报(自然科学版), 2014, 50(2): 208-212. Wang X, Wang Z L, Chen J H, et al. Origin of the upland lake group in Ningwu Tianchi Region, Shanxi Province[J]. Journal of Lanzhou University (Natural Sciences), 2014, 50(2): 208-212. |
| [16] |
张俊芳, 冯佳, 谢树莲, 等. 山西宁武亚高山湖群浮游植物群落结构特征[J]. 湖泊科学, 2012, 24(1): 117-122. Zhang J F, Feng J, Xie S L, et al. Characteristics of phytoplankton community structures in Ningwu subalpine lakes, Shanxi Province[J]. Journal of Lake Sciences, 2012, 24(1): 117-122. DOI:10.3969/j.issn.1003-5427.2012.01.016 |
| [17] | Chen F H, Liu J B, Xu Q H, et al. Environmental magnetic studies of sediment cores from Gonghai Lake:implications for monsoon evolution in North China during the late glacial and Holocene[J]. Journal of Paleolimnology, 2013, 49(3): 447-464. DOI:10.1007/s10933-012-9677-3 |
| [18] |
景炬辉.中条山铜尾矿库坝面土壤微生物群落结构特征[D].太原: 山西大学, 2017. Jing J H. The structural characteristics of soil microbial community in dam of copper mine tailings in Zhongtiaoshan Mountains, Shanxi[D]. Taiyuan: Shanxi University, 2017. |
| [19] | Liu J X, Li C, Jing J H, et al. Ecological patterns and adaptability of bacterial communities in alkaline copper mine drainage[J]. Water Research, 2018, 133: 99-109. DOI:10.1016/j.watres.2018.01.014 |
| [20] | Garcia S L, Salka I, Grossart H P, et al. Depth-discrete profiles of bacterial communities reveal pronounced spatio-temporal dynamics related to lake stratification[J]. Environmental Microbiology Reports, 2013, 5(4): 549-555. DOI:10.1111/1758-2229.12044 |
| [21] | Reche I, Pulido-Villena E, Morales-Baquero R, et al. Does ecosystem size determine aquatic bacterial richness?[J]. Ecology, 2005, 86(7): 1715-1722. DOI:10.1890/04-1587 |
| [22] |
寇文伯, 黄正云, 张杰, 等. 鄱阳湖湖泊细菌群落组成及结构——以松门山为例[J]. 生态学报, 2015, 35(23): 7608-7614. Kou W B, Huang Z Y, Zhang J, et al. Bacterial community structure and composition in Lake Poyang:a case study in the Songmenshan Region, China[J]. Acta Ecologica Sinica, 2015, 35(23): 7608-7614. |
| [23] | Novais S V, Zenero M D O, Barreto M S C, et al. Phosphorus removal from eutrophic water using modified biochar[J]. Science of the Total Environment, 2018, 633: 825-835. DOI:10.1016/j.scitotenv.2018.03.246 |
| [24] |
苟婷, 马千里, 许振成, 等. 贝江浮游藻类群落特征及富营养化风险分析[J]. 环境科学, 2015, 36(3): 946-954. Gou T, Ma Q L, Xu Z C, et al. Phytoplankton community structure and eutrophication risk assessment of Beijiang River[J]. Environmental Science, 2015, 36(3): 946-954. |
| [25] | Wong W H, Dudula J J, Beaudoin T, et al. Declining ambient water phosphorus concentrations in Massachusetts' rivers from 1999 to 2013:Environmental protection works[J]. Water Research, 2018, 139: 108-117. DOI:10.1016/j.watres.2018.03.053 |
| [26] |
李玉凤, 刘红玉, 蔡春晓, 等. 城市湿地公园周边干扰对其水环境健康的影响——以西溪国家湿地公园为例[J]. 地理研究, 2015, 34(5): 851-860. Li Y F, Liu H Y, Cai C X, et al. The disturbance effect of the surroundings on the water environmental health of urban wetland park:A case study on Xixi Wetland Park, China[J]. Geographical Research, 2015, 34(5): 851-860. |
| [27] | Adams H E, Crump B C, Kling G W. Temperature controls on aquatic bacterial production and community dynamics in arctic lakes and streams[J]. Environmental Microbiology, 2010, 12(5): 1319-1333. DOI:10.1111/emi.2010.12.issue-5 |
| [28] | Bouvy M, Bettarel Y, Bouvier C, et al. Trophic interactions between viruses, bacteria and nanoflagellates under various nutrient conditions and simulated climate change[J]. Environmental Microbiology, 2011, 13(7): 1842-1857. DOI:10.1111/j.1462-2920.2011.02498.x |
| [29] |
李毳, 马转转, 乔沙沙, 等. 原位微宇宙法研究温带森林土壤真菌群落构建的驱动机制[J]. 生态环境学报, 2018, 27(5): 811-817. Li C, Ma Z Z, Qiao S S, et al. Analysis of driving forces underlying the structure of fungal community in temperate forest soils based on microcosm experiments[J]. Ecology and Environmental Sciences, 2018, 27(5): 811-817. |
| [30] | Dong C M, Sheng H F, Wang W G, et al. Bacterial distribution pattern in the surface sediments distinctive among shelf, slope and basin across the western Arctic Ocean[J]. Polar Biology, 2017, 40(2): 423-436. DOI:10.1007/s00300-016-1970-6 |
| [31] | Xiong J B, Ye X S, Wang K, et al. Biogeography of the sediment bacterial community responds to a nitrogen pollution gradient in the East China Sea[J]. Applied and Environmental Microbiology, 2014, 80(6): 1919-1925. DOI:10.1128/AEM.03731-13 |
| [32] | Li J B, Li P Y, Shang C, et al. Series of national standards on specifications for oceanographic survey[J]. China Standardization, 2011(2): 34-38. |
| [33] | Jones J R, Knowlton M F, Obrecht D V, et al. Temperature and oxygen in Missouri reservoirs[J]. Lake and Reservoir Management, 2011, 27(2): 173-182. DOI:10.1080/07438141.2011.583713 |
| [34] | Allen J I, Siddorn J R, Blackford J C, et al. Turbulence as a control on the microbial loop in a temperate seasonally stratified marine systems model[J]. Journal of Sea Research, 2004, 52(1): 1-20. DOI:10.1016/j.seares.2003.09.004 |
| [35] | Nixdorf B, Deneke R. Why 'very shallow' lakes are more successful opposing reduced nutrient loads[J]. Hydrobiologia, 1997, 342-343: 269-284. DOI:10.1023/A:1017012012099 |
 2019, Vol. 40
2019, Vol. 40


