2. 重庆市农业资源与环境研究重点实验室, 重庆 400716
2. Chongqing Key Laboratory of Agricultural Resources and Environment, Chongqing 400716, China
随着我国城市化进程加快, 城市人工湿地数量也显著增多.与自然湿地相比, 城市湿地有着众多其他自然湿地不可替代的生态功能, 比如调节城市气候、提供城市景观娱乐、保护城市生物多样性、城市防洪泄洪、污染物净化和降解等, 具有生态价值和社会价值, 是城市可持续发展所依赖的生态系统[1~7].但是人工湿地中的各类污染物, 包括氮磷污染物、有机污染物、重金属污染物等对人类生活有一定潜在危害[8].汞(Hg)作为一种具有稳定性、高毒性、生物累积性的重金属污染物之一[9, 10], 在氧化还原条件下能与水体中微生物、可溶性碳等作用后产生毒性更强的甲基汞(MeHg), 使湿地成为汞敏感生态系统[11~13].
尤其是近年来, 我国重视城市生态文明建设, 城市湿地成为城市环境很重要的一部分.但城市湿地研究却滞后于城市发展, 影响到城市生态安全和社会经济健康.由于城市湿地的生态服务功能与乡野湿地有着明显的不同, 存在受人为活动干扰强烈、面积变小、功能减弱、污染加剧等问题.这些特征使得汞在城市湿地水体中的迁移转化具有区别于其他生态系统的特殊性.城市湿地的建设、维护对环境汞的分布及转化影响还不清楚.特别地, 纳污是城市湿地的一个重要生态功能, 由于城市污水水质及污水处理工艺的复杂, 城市污水经污水厂处理排入城市湿地后可能影响受纳水体中总汞及甲基汞质量浓度.
鉴于此, 本文以重庆某城市湿地公园为例, 对水体中总汞与甲基汞的含量进行研究, 通过找出城市湿地水体中汞分布特征及其源汇关系, 以期保证湿地公园的生态环境安全提供科学支持.
1 研究区概况该城市湿地公园湿地面积47 hm2, 蓄水达168万m3.水源主要来自一日处理量1.7万t的城市生活污水处理厂出水, 另有一部分来自上游水库.该湿地公园在设计上以“立体湿地”为主要风格, 形成溪流、池塘、梯田式人工湿地水体净化系统的组合.该城市湿地公园集接纳生活污水处理厂出水、水质净化、休闲娱乐等多功能, 周围以居民生活区为主, 人口密度大, 人为活动较为频繁.
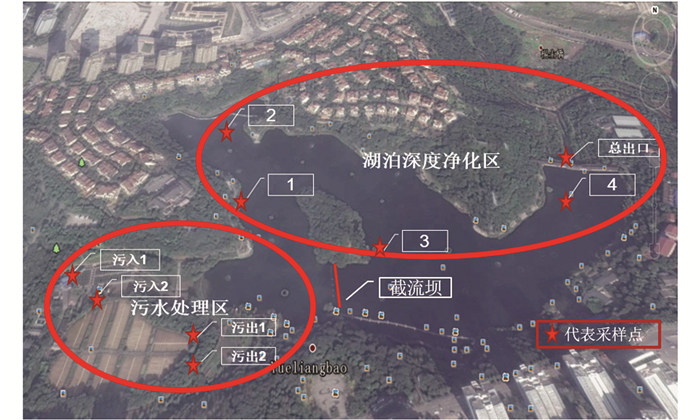
2 材料与方法 2.1 采样点设置和样品采集根据湿地公园区域功能差异, 分为两个区域:污水处理区和湖泊深度净化区.在两个区域内共布设9个采样点(图 1).其中, 污水处理区设置4个采样点, 分别为:污水入口1、污水入口2、污水出口1、污水出口2;湖泊深度净化区设置5个采样点为:C1、C2、C3、C4、总出口.研究区水体流向如下:污水入口1、2→污水出口1、2→ C1→ C2→ C3→ C4→总出口.每个采样点环境有所区别, C1、C2附近岸边种有大量水生植物且有供游客行走的步道, C3位于湖泊中心但附近有曝气装置, C4和总出口之间设有桥体, 游客会长时间聚集于此.
|
图 1 采样点分布示意 Fig. 1 Location of sampling sites |
于2017年3月~2018年2月期间, 每月用卡盖式采水器, 在湖泊深度净化区4个采样点(C1、C2、C3、C4)处按照表层和深层(>8 m)采集水样, 在污水处理区4个采样点(污入1、污入2、污出1、污出2)出水口接取样品; 此外, 分季节于3月、6月、9月和12月在湖泊深度净化区4个采样点各采集一次分层样品(表层、4 m、8 m、12 m).将采集的水样转移至已进行超净处理的硼硅玻璃瓶中, 放入冷藏箱中运回实验室待测.为避免污染, 在所有的操作过程中均佩戴一次性聚乙烯手套.
2.2 样品分析与质量控制水样汞参照阎海鱼等[14]和蒋红梅[15]建立的天然水中痕量汞的分析方法测定:总汞(THg)用金汞齐-冷原子荧光光谱法进行测定; 总甲基汞(MeHg)用蒸馏-乙基化结合GC-CVAFS法进行测定.
本实验用水均为超纯水(18.2Milli-Q).所有样品测定通过标准样测定、平行样控制及加标回收率(80%~120%)进行质量控制, 并对5%的样品进行重复测定, 相对标准偏差<15%.
2.3 物料计算与数据分析人工湿地污染物负荷总量与去除总量计算公式[16]:

|
式中, WL为人工湿地污染物负荷总量(mg ·d-1), WR为人工湿地污染物去除总量(mg ·d-1), ICWi、ECWi分别为人工湿地每天的进、出水污染物质量浓度(ng ·L-1), Qi为每天的进水流量.本文Qi取17 000 m3 ·d-1, 为污水厂每日处理水量.
本实验数据用Microsoft Excel、SPSS等软件进行数理统计分析, 用Origin 8.6等进行图的绘制.
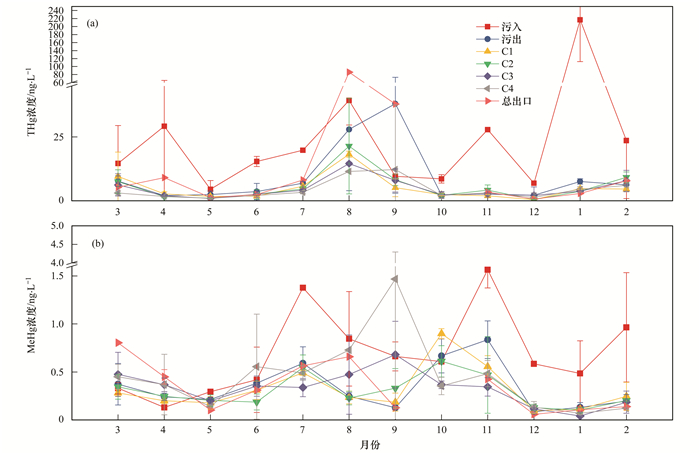
3 结果与讨论 3.1 水体汞的时间分布于2017年3月~2018年2月进行为期1a的定点采样.分析结果显示(图 2), 城市生活污水经该污水厂处理后, 出水THg质量浓度范围为1.98~38.03 ng ·L-1, 平均值为(9.10±5.84) ng ·L-1.除9月以外, 污水经污水厂处理后的总汞均有所降低, 去除率范围为29.0%~96.5%, 平均去除率达69.2%, 这表明城市生活污水处理厂能有效去除一定THg; 出水MeHg质量浓度范围为0.09~0.84 ng ·L-1, 平均值为(0.34±0.08)ng ·L-1.该污水处理厂对MeHg也起到一定的去除效果(除3、4、10月以外), 去除率范围8.5%~85.4%, 平均去除率为58.8%.这与李花等人的研究一致[17, 18], 发现污水处理工艺对THg及MeHg的去除有一定效果, 主要由于二沉池和氧化沟对汞起到吸附和沉积的作用, 且污水处理过程中发生了去甲基化, 之后大部分汞进入污泥, 只有一部分汞随出水排入受纳水体[19~21], 这些共同导致污水出口汞质量浓度降低.
|
图 2 不同采样点不同月份THg和MeHg质量浓度 Fig. 2 Concentration of THg and MeHg in different months at different sampling points |
湖泊深度净化区THg质量浓度范围为0.37~85.69 ng ·L-1[平均质量浓度为(6.76±2.29)ng ·L-1], MeHg质量浓度范围为0.04~1.47 ng ·L-1[平均质量浓度为(0.35±0.17) ng ·L-1].从季节分布来看, THg质量浓度在夏季高于其它季节, 并且各采样点THg质量浓度均在8月出现峰值, 这主要可能与8月人为活动较频繁有关.其游客数量约是其它月份的2~10倍, 特别是总出口处的观赏桥附近, 游客与车辆较多, 停留时间较长, 人为干扰较剧烈, 导致该月份总出口处THg质量浓度达到了85.69 ng ·L-1.
从图 2(b)可以得到, 各个采样点MeHg质量浓度变化趋势没有明显规律.这主要是由于本研究区域体系复杂, 污水厂和湿地公园一体化, 影响甲基汞生成的因素较多.一方面, 污水厂的氧化沟工艺会影响甲基汞的生成, 而二沉池对流经的污染物起到吸附去除的作用等[17, 18]; 另一方面, 湿地环境也有利于甲基汞的形成[22].
在春、夏两季, 湖泊深度净化区C1采样点THg质量浓度分别为4.84 ng ·L-1和6.31 ng ·L-1, 随水流流动, THg质量浓度呈现出降低的趋势, 到C4采样点时分别为1.87 ng ·L-1和3.54 ng ·L-1, 比C1采样点分别下降了61.4%和43.9%.而在秋、冬两季, C1采样点水体THg浓度分别为3.61 ng ·L-1和2.51 ng ·L-1, 随水流流动, THg质量浓度呈现出增加的趋势, 流至C4采样点时质量浓度分别达到14.01 ng ·L-1和3.26 ng ·L-1, 比C1采样点分别增加了2.88倍和0.30倍.在总出口处, THg质量浓度在春、夏、秋、冬四季都有一个上升趋势, 夏季达到最高值32.06 ng ·L-1.
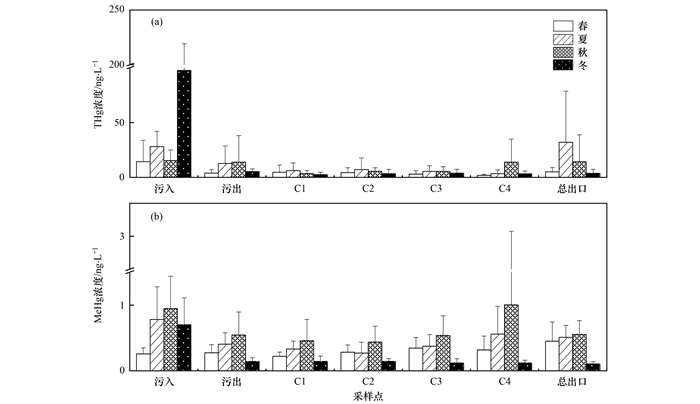
湖泊深度净化区C1~C4采样点MeHg质量浓度表现为:秋季>夏季>春季>冬季.在春、夏、秋、冬四季C1点MeHg质量浓度分别为0.22、0.33、0.46和0.14 ng ·L-1, 而到C4点分别为0.32、0.56、1.00和0.12 ng ·L-1.从图 2(b)可以看出, 温度对甲基汞的分布影响较大, 气温低的月份甲基汞含量较低, 正如不同季节甲基汞分布所示[图 3(b)], 各采样点甲基汞在冬季呈现最低值(除污入外).有研究表明[23, 24], 水温升高, 可以促进汞的甲基化过程.四季湖泊水体各采样点在甲基汞质量浓度变化趋势上相似, 但差异并不明显.这可能由两个原因造成, 第一, 底泥中的汞释放到水相中的速度十分缓慢, 有研究表明[25]底泥沉积物是表层水体汞的重要储存库, 但沉积物中的汞重新释放进入水相环境是一个特别缓慢的过程, 需要十年甚至更久的时间.第二, 进入到水相中的汞可能被生物体所吸收.
|
图 3 不同季节随水流流向各采样点水体THg和MeHg质量浓度 Fig. 3 Concentration of THg and MeHg in water at different sampling points in different seasons |
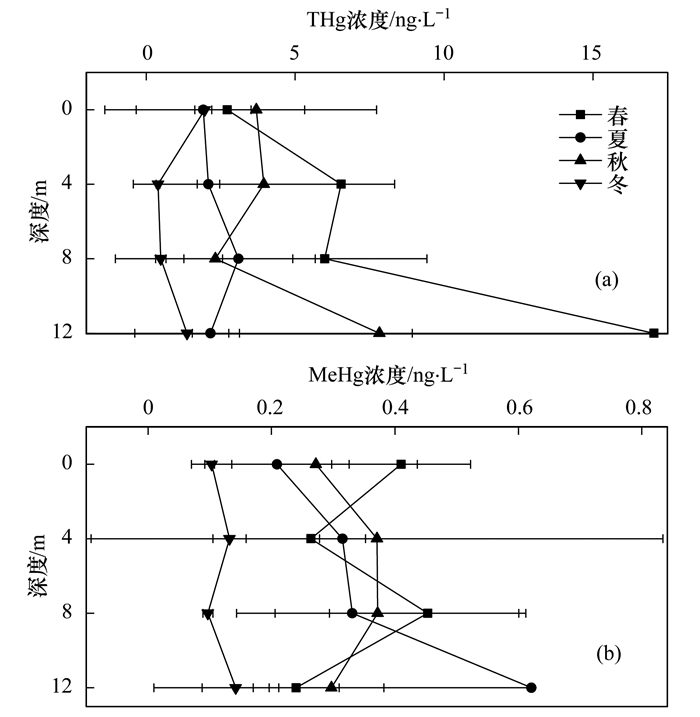
该湿地公园湖泊水体THg和MeHg的垂直变化范围分别为0.07~23.11 ng ·L-1和0.05~1.52 ng ·L-1.如图 4所示, 各采样点水体THg和MeHg在剖面上具有较强的波动性, 并没有表现出明显的规律性.由于人工湿地受人为活动影响较大, 水体汞的来源复杂, 除了沉积物再悬浮外, 生活污水、土壤侵蚀和地表径流的贡献也不容忽视.
|
图 4 不同季节不同采样点垂直断面水体THg和MeHg质量浓度 Fig. 4 Concentrations of THg and MeHg in vertical section of different sampling points in different seasons |
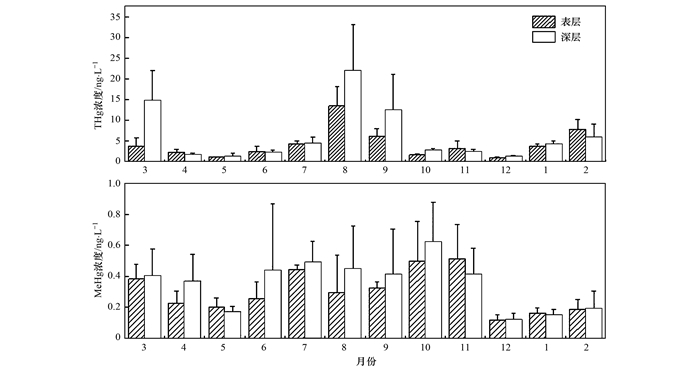
受环境因素影响, 水体表层和底层汞的来源和形态转化是不同的, 因而对表层和底层水体汞的分布分别进行了研究.结果发现, 表层水体THg平均浓度在8月最高, 为13.42ng ·L-1, 而在12月最低, 为0.95 ng ·L-1; MeHg平均浓度在11月最高, 达到0.51 ng ·L-1, 在12月最低, 仅为0.12 ng ·L-1.对于底层水体, THg平均浓度在8月最高, 达到22.04 ng ·L-1, 5月最低, 为1.27 ng ·L-1; MeHg平均浓度在10月最高, 达到0.62 ng ·L-1, 12月最低, 为0.12 ng ·L-1.从图 5可以看出, 除少数月份外, 表层THg和MeHg含量小于底层, 这说明沉积物可能是上覆水中汞的重要来源.有研究表明[26, 27], 厌氧微生物的汞甲基化是水生环境中MeHg产生的主要途径.与水体相比, 水体-沉积物界面形成的低氧和强还原状态有利于提高厌氧汞甲基化微生物的活性, 进行汞甲基化, 形成的MeHg会向上覆水释放, 导致上覆水MeHg浓度要高于表层水体[28~30].另外, 被湖泊底泥吸附的汞在一系列物理、化学或生物的作用下(如颗粒物再悬浮、底栖生物扰动等)再次进入水体, 导致水体深层甲基汞浓度较高[31].湖泊的水源虽然是经污水厂处理后汇入的城镇生活污水, 但其有机质、富营养化程度依然较高, 而有机质的腐解是一个耗氧过程, 会消耗水体内大量氧气, 使湖底成为一个有利于汞甲基化的厌氧环境[32].
|
图 5 不同月份水体表层、深层THg、MeHg质量浓度 Fig. 5 Concentrations of THg and MeHg in the surface and deep layers of water in different months |
水生环境系统中, 物料平衡是估算污染源的重要方法, 能够为化学污染物浓度监测提供有效信息, 有利于水环境质量的评价[33].目前, 人工湿地中汞的迁移转化途径尚无定论, 仍需进行讨论和深入研究.本文在探讨了汞浓度变化的基础上, 基于汞的地球化学循环平衡模型, 量化分析汞在人工湿地中的动态变化特征.
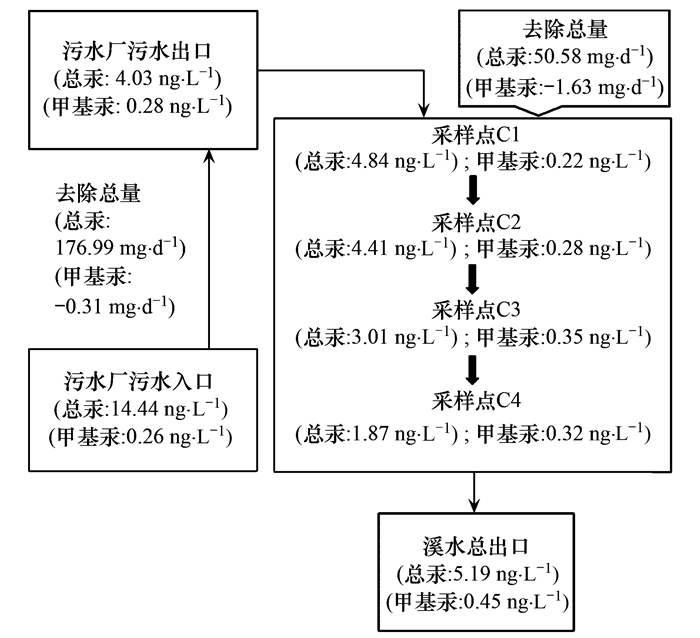
因此, 根据人工湿地污染物负荷总量与去除总量计算公式, 笔者定量分析了春、夏、秋、冬四季该城市湿地公园水体汞的迁移特征.以春季为例, 图 6展示了该季节水体汞随水流方向(污水入口1、2→污水出口1、2→ C1→ C2→ C3→ C4→总出口)的分布以及迁移量.
|
负值代表增加 图 6 春季湿地水体物料衡算示意 Fig. 6 Schematic diagram of water balance in the wetland in spring |
从污水处理区和湖泊深度净化区两个区域来看, 在春季污水处理区, 城市污水经污水厂处理后THg总量减少了176.99 mg ·d-1, 而MeHg总量增加了0.31 mg ·d-1.之后, 水体流经湖泊深度净化区, 经湖泊环境净化后THg总量减少了50.58 mg ·d-1, 而MeHg总量增加了1.63mg ·d-1.最后, 水体汇入溪流时, THg和MeHg平均质量浓度分别为5.19 ng ·L-1和0.45 ng ·L-1.如果将污水进入污水厂, 最终流向小溪看作一个整体, 经该系统处理净化后, THg降低了157.25 mg ·d-1, 而MeHg增加了3.30 mg ·d-1.
对于不同季节而言, 不同水体区域对THg和MeHg的源汇归趋行为有所差异(表 1).在污水处理区, 4个季节的水体经污水厂工艺处理后THg均有所下降, 冬季减少最多(1 567.98 mg ·d-1); MeHg在夏、秋、冬三季均呈现降低趋势, 冬季降低值最大(9.50 mg ·d-1), 而春季略有升高(0.31 mg ·d-1).这可能是由于春节期间饮食丰富造成污水厂中有机质含量增加, 因而春季污水处理区MeHg增加.对于湖泊深度净化区, 水体THg在不同季节具有不同特征.在春、夏两季, 湖泊环境对水体THg有去除效果, 而秋、冬两季则相反; 对于甲基汞而言, 湖泊环境除了在冬季对水体MeHg有去除效果外(0.39 mg ·d-1), 在其它3个季均表现出MeHg增加趋势.这可能是由于冬季温度较低, 湖泊内MeHg的原位生成较弱.对于整个湿地公园来说, 从水体进入污水厂至流入溪流, 除夏季水体THg质量浓度略有增加以外, 其余3个季节均有所减少; 而水体MeHg质量浓度除春季略有升高, 另外3个季节均呈下降趋势.
|
|
表 1 不同季节不同系统THg、MeHg去除总量1)/mg ·d-1 Table 1 Total removal of THg and MeHg in different seasons and systems/mg ·d-1 |
通过物料衡算得出了研究期间该湿地公园汞迁移与变动情况(表 2), 在污水处理系统, 水体THg每年降低184.99 g, 水体MeHg每年降低2.04 g; 而在湖体系统, 水体THg每年增加8.38 g, 水体MeHg每年增加1.31 g.总体而言, 尽管湿地中湖体有净甲基汞的产生, 而对于整个湿地公园, 水体THg每年降低155.50 g, 水体MeHg每年降低1.65 g, 对下游水体具有保护作用.
|
|
表 2 不同系统THg、MeHg日去除总量/mg ·d-1 Table 2 Daily removal amount of THg and MeHg in different systems/mg ·d-1 |
4 结论
该城市湿地中的污水处理区对流入的城市生活污水中无机汞和甲基汞均具有去除作用.城市湿地系统可消纳进入系统中的汞和甲基汞, 对下游水体具有保护作用.
| [1] |
殷康前, 倪晋仁. 湿地研究综述[J]. 生态学报, 1998, 18(5): 539-546. Yin K Q, Ni J R. Review of wetland studies[J]. Acta Ecologica Sinica, 1998, 18(5): 539-546. DOI:10.3321/j.issn:1000-0933.1998.05.014 |
| [2] | 葛继稳. 湿地资源及管理实证研究——以"千湖之省"湖北省为例[M]. 北京: 科学出版社, 2007. |
| [3] |
傅娇艳, 丁振华. 湿地生态系统服务、功能和价值评价研究进展[J]. 应用生态学报, 2007, 18(3): 681-686. Fu J Y, Ding Z H. Research progress on wetland ecosystem service and its valuation[J]. Chinese Journal of Applied Ecology, 2007, 18(3): 681-686. DOI:10.3321/j.issn:1001-9332.2007.03.037 |
| [4] |
俞孔坚, 李迪华, 潮洛蒙. 城市生态基础设施建设的十大景观战略[J]. 规划师, 2001, 17(6): 9-13, 17. Yu K J, Li D H, Chao L M. Ten landscape strategies to build urban ecological infrastructure[J]. Planners, 2001, 17(6): 9-13, 17. DOI:10.3969/j.issn.1006-0022.2001.06.002 |
| [5] |
曹鹏飞. 浅谈城市湿地生态功能退化的原因及其恢复与保护[J]. 福建林业科技, 2008, 35(1): 176-179, 196. Cao P F. Preliminary study on the cause of the city wetland ecology function degradation and its restoration with the protection[J]. Journal of Fujian Forestry Science and Technology, 2008, 35(1): 176-179, 196. DOI:10.3969/j.issn.1002-7351.2008.01.041 |
| [6] |
崔保山, 杨志峰, 李英华, 等. 城市拓展中湿地的综合保护与发展[J]. 自然资源学报, 2004, 19(4): 462-471. Cui B S, Yang Z F, Li Y H, et al. The integrated wetland conservation and development in the context of city expansion[J]. Journal of Natural Resources, 2004, 19(4): 462-471. DOI:10.3321/j.issn:1000-3037.2004.04.008 |
| [7] |
吴晓磊. 人工湿地废水处理机理[J]. 环境科学, 1995, 16(3): 83-86. Wu X L. Mechanism of wastewater treatment in constructed wetlands[J]. Environmental Science, 1995, 16(3): 83-86. DOI:10.3321/j.issn:0250-3301.1995.03.024 |
| [8] |
刘超翔, 胡洪营, 张建, 等. 不同深度人工复合生态床处理农村生活污水的比较[J]. 环境科学, 2003, 24(5): 92-96. Liu C X, Hu H Y, Zhang J, et al. Rural sewage treatment performance of constructed wetlands with different depths[J]. Environmental Science, 2003, 24(5): 92-96. DOI:10.3321/j.issn:0250-3301.2003.05.017 |
| [9] | Orihel D M, Paterson M J, Blanchfield P J, et al. Temporal changes in the distribution, methylation, and bioaccumulation of newly deposited mercury in an aquatic ecosystem[J]. Environmental Pollution, 2008, 154(1): 77-88. |
| [10] | Celo V, Lean D R S, Scott S L. Abiotic methylation of mercury in the aquatic environment[J]. Science of the Total Environment, 2006, 368(1): 126-137. DOI:10.1016/j.scitotenv.2005.09.043 |
| [11] | Lindqvist O, Johansson K, Bringmark L, et al. Mercury in the Swedish environment-Recent research on causes, consequences and corrective methods[J]. Water, Air, and Soil Pollution, 1991, 55(1-2): xi-261. |
| [12] |
王娅, 赵铮, 木志坚, 等. 三峡库区典型农田小流域水体汞的时空分布特征[J]. 环境科学, 2014, 35(11): 4095-4102. Wang Y, Zhao Z, Mu Z J, et al. Spatial and temporal distribution of mercury in water of a small typical agricultural watershed in the three gorges reservoir region[J]. Environmental Science, 2014, 35(11): 4095-4102. |
| [13] |
白薇扬, 张成, 唐振亚, 等. 长寿湖水库垂直剖面不同形态汞的季节变化特征及其影响因素[J]. 环境科学, 2015, 36(10): 3649-3661. Bai W Y, Zhang C, Tang Z Y, et al. Seasonal variations in vertical profile of Hg species and the influential factors in Changshou reservior[J]. Environmental Science, 2015, 36(10): 3649-3661. |
| [14] |
闫海鱼, 冯新斌, 商立海, 等. 天然水体中痕量汞的形态分析方法研究[J]. 分析测试学报, 2003, 22(5): 10-13. Yan H Y, Feng X B, Shang L H, et al. Speciation analysis of ultra trace levels of mercury in natural waters[J]. Journal of Instrumental Analysis, 2003, 22(5): 10-13. DOI:10.3969/j.issn.1004-4957.2003.05.003 |
| [15] |
蒋红梅, 冯新斌, 粱琏, 等. 蒸馏-乙基化GC-CVAFS法测定天然水体中的甲基汞[J]. 中国环境科学, 2004, 24(5): 568-571. Jiang H M, Feng X B, Liang L, et al. Determination of methyl mercury in waters by distillation-GC-CVAFS technique[J]. China Environmental Science, 2004, 24(5): 568-571. DOI:10.3321/j.issn:1000-6923.2004.05.014 |
| [16] | 赵建.人工湿地对污染河水的净化效果及机理研究[D].南京: 河海大学, 2006. 43-45. http://cdmd.cnki.com.cn/article/cdmd-10294-2006076883.htm |
| [17] |
李花, 毛宇翔, 李永, 等. 汞在城市污水处理厂的赋存特征及质量平衡——总汞[J]. 环境化学, 2014, 33(7): 1059-1065. Li H, Mao Y X, Li Y, et al. Occurrence and mass balance of mercury at a sewage treatment plant. Part Ⅰ:total mercury[J]. Environmental Chemistry, 2014, 33(7): 1059-1065. |
| [18] |
李花, 毛宇翔, 李永, 等. 汞在城市污水处理厂的赋存特征及质量平衡——甲基汞[J]. 环境化学, 2014, 33(8): 1287-1293. Li H, Mao Y X, Li Y, et al. Occurrence and mass balance of mercury at a sewage treatment plant. Part Ⅱ:methylmercury[J]. Environmental Chemistry, 2014, 33(8): 1287-1293. |
| [19] | Balogh S J, Nollet Y H. Methylmercury input to the Mississippi River from a large metropolitan wastewater treatment plant[J]. Science of the Total Environment, 2008, 406(1-2): 145-153. DOI:10.1016/j.scitotenv.2008.07.039 |
| [20] | Gilmour C C, Bloom N S. A case study of mercury and methylmercury dynamics in a Hg-contaminated municipal wastewater treatment plant[J]. Water, Air, and Soil Pollution, 1995, 80(1-4): 799-803. DOI:10.1007/BF01189731 |
| [21] | Balogh S J, Nollet Y H. Mercury mass balance at a wastewater treatment plant employing sludge incineration with offgas mercury control[J]. Science of the Total Environment, 2008, 389(1): 125-131. DOI:10.1016/j.scitotenv.2007.08.021 |
| [22] |
刘汝海, 刘诗璇, 王杰, 等. 秋夏季黄河三角洲湿地土壤汞和甲基汞的变化[J]. 环境科学学报, 2017, 37(1): 272-279. Liu R H, Liu S X, Wang J, et al. Change of mercury and methylmercury in Yellow River Delta wetlands from autumn to summer[J]. Acta Scientiae Circumstantiae, 2017, 37(1): 272-279. |
| [23] | Nguyen H L, Leermakers M, Kurunczi S, et al. Mercury distribution and speciation in Lake Balaton, Hungary[J]. Science of the Total Environment, 2005, 340(1-3): 231-246. DOI:10.1016/j.scitotenv.2004.08.016 |
| [24] | Hall B D, Manolopoulos H, Hurley J P, et al. Methyl and total mercury in precipitation in the Great Lakes region[J]. Atmospheric Environment, 2005, 39(39): 7557-7569. DOI:10.1016/j.atmosenv.2005.04.042 |
| [25] |
李永华, 王五一, 杨林生, 等. 汞的环境生物地球化学研究进展[J]. 地理科学进展, 2004, 23(6): 33-40. Li Y H, Wang W Y, Yang L S, et al. A review of mercury in environmental biogeochemistry[J]. Progress in Geography, 2004, 23(6): 33-40. DOI:10.3969/j.issn.1007-6301.2004.06.004 |
| [26] | Ullrich S M, Tanton T W, Abdrashitova S A. Mercury in the auqatic environment:A review of factors affecting methylation[J]. Critical Reviews in Environmental Science & Technology, 2001, 31(3): 241-293. |
| [27] |
冯新斌, 仇广乐, 付学武, 等. 环境汞污染[J]. 化学进展, 2009, 21(2-3): 436-457. Feng X B, Qiu G L, Fu X W, et al. Mercury pollution in the environment[J]. Progress in Chemistry, 2009, 21(2-3): 436-457. |
| [28] | Bloom N. Determination of picogram levels of methylmercury by aqueous phase ethylation, followed by cryogenic gas chromatography with cold vapour atomic fluorescence detection[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1989, 46(7): 1131-1140. DOI:10.1139/f89-147 |
| [29] | Regnell O, Elert M, Höglund L O, et al. Linking cellulose fiber sediment methyl mercury levels to organic matter decay and major element composition[J]. Ambio, 2014, 43(7): 878-890. DOI:10.1007/s13280-013-0487-2 |
| [30] | Shi J B, Ling L N, Jiang G B, et al. The speciation and bioavailability of mercury in sediments of Haihe River, China[J]. Environment International, 2005, 31(3): 357-365. DOI:10.1016/j.envint.2004.08.008 |
| [31] | Vale C, Ferreira A M, Micaelo C, et al. Mobility of contaminants in relation to dredging operations in a mesotidal estuary (Tagus estuary, Portugal)[J]. Water Science and Technology, 1998, 37(6-7): 25-31. DOI:10.2166/wst.1998.0731 |
| [32] | Yan H Y, Feng X B, Shang L H, et al. The variations of mercury in sediment profiles from a historically mercury-contaminated reservoir, Guizhou province, China[J]. Science of the Total Environment, 2008, 407(1): 497-506. DOI:10.1016/j.scitotenv.2008.08.043 |
| [33] |
刘妍, 张蕴, 韩晓盈, 等. 清洁生产审核中物料平衡的难点及应用实例[J]. 环境科学与管理, 2013, 38(3): 163-168. Liu Y, Zhang Y, Han X Y, et al. Problems and application examples of material balance in cleaner production audits[J]. Environmental Science and Management, 2013, 38(3): 163-168. DOI:10.3969/j.issn.1673-1212.2013.03.039 |
 2019, Vol. 40
2019, Vol. 40


