短程硝化(PN)是指通过控制溶解氧(DO)和污泥龄(SRT)等因素, 抑制亚硝酸盐氧化菌(NOB)的生长, 将硝化过程控制在NO2--N阶段[1], 其具有节约成本、缩短反应时间等优点[2].同步硝化反硝化(SND)是指在空间上没有明显缺氧和好氧分区或者在微溶解氧的条件下, 硝化和反硝化反应在空间和时间上同步进行的生物脱氮过程[3~9].同步短程硝化反硝化(SPND)脱氮就是将PN与SND耦合, 污水中的NH4+-N经氨氧化菌(AOB)氧化为NO2--N后, 直接通过反硝化还原为N2除去[10], 其具有节约成本、缩短反应时间、高效利用碳源等优势.
强化生物除磷技术(EBPR)是指通过微生物大量吸收水中溶解性的磷酸盐从而去除磷的活性生物污泥系统, 其去除量超过自身代谢繁殖所需要的磷酸盐的量[11~14]. EBPR工艺的核心就在于保证聚磷菌(PAOs)的生长, 提高PAOs相对于异养菌所占的比例[15].反硝化除磷(DPR)与传统的好氧除磷菌相比具有相似的除磷机制, 其主要区别在于吸磷过程所利用的电子受体不同, 其利用的是NO2--N和NO3--N[16]. EBPR和DPR的同时存在, 可保证低曝气量下PO43--P的高效去除.
针对传统生物脱氮除磷工艺中存在的碳源不足[17~19]、脱氮菌与除磷菌对溶解氧(DO)的竞争[20, 21]、不同功能菌在污泥龄[22~25]方面存在着矛盾等诸多弊端[26], 结合低C/N城市污水的水质特点提出了一种同步脱氮除磷的新工艺, 即同步短程硝化反硝化除磷(SPNDPR)系统. SPNDPR工艺中好氧吸磷过程与反硝化除磷过程的同时存在, 可在保证系统稳定除磷的基础上, 实现部分氮的去除; 与传统同步硝化反硝化(SND)脱氮工艺相比, SPNDPR工艺中短程硝化反硝化的存在, 实现了“一碳两用”[27], 可进一步降低脱氮过程所需的有机碳源需求, 有利于提高系统的脱氮性能.
目前, 有关SPNDPR系统脱氮除磷的报道[28]主要是启动或典型周期内脱氮除磷特性的研究, 对于SPNDPR工艺进一步的优化运行还未见报道.本研究以低C/N(≤4)城市污水为处理对象, 采用厌氧/低氧运行的序批式活性污泥反应器(SBR), 通过合理控制厌氧/好氧运行时间和SRT, 并联合调控好氧段曝气量[单位体积的反应器在单位时间内通过的气体的体积, 单位为L·(min·L)-1]和曝气时间, 考察了SPNDPR系统的优化运行特性, 并探讨了该系统优化运行后的COD、氮、磷去除特性以及优化运行前后典型周期内基质浓度的变化情况, 以期为了解SPNDPR系统优化运行期间的氮磷去除特性及其在低C/N城市污水的实际工程应用中提供实验数据支撑.
1 材料与方法 1.1 实验装置与运行工序SBR反应器采用有机玻璃制成, 为敞口式反应器, 总体积为13 L, 有效容积为8 L, 采用机械搅拌的方式使泥水混匀, 以曝气砂头作为微孔曝气器, 并以转子流量计调节曝气量.反应器采用厌氧/好氧交替的运行方式, 具体运行参数见表 1. SPNDPR系统初始运行参数:曝气量0.125 L·(min·L)-1、好氧时间3 h; 出水水质: NH4+-N、NO2--N、NO3--N、PO43--P和COD浓度分别为0.35、20.05、0.42、0.47和63.55mg·L-1.
|
|
表 1 SPNDPR系统优化运行期间运行参数1) Table 1 Running parameters during the optimal operation of the SPNDPR system |
1.2 实验用水和接种污泥
本实验用水为青岛市某污水处理厂粗格栅前入口处的生活污水, 具体水质为:COD浓度176.75~572.48 mg·L-1, NH4+-N浓度53.99~92.84 mg·L-1, NO2--N浓度 < 1 mg·L-1, NO3--N浓度 < 1mg·L-1, PO43--P浓度平均3~10.25 mg·L-1, pH值7.2~7.6.接种污泥取自本实验室正常运行的SPNDPR系统的剩余污泥, 具有良好的脱氮除磷能力, 接种到反应器内后MLSS约为4 016 mg·L-1, SV约为21%, SVI约为52.29mL·g-1.
1.3 检测方法 1.3.1 常规检测方法水样经中性滤纸(最大孔径15~20 μm)过滤后测定以下各参数:NH4+-N采用纳氏试剂分光光度法测定, NO2--N采用N-(1-萘基)乙二胺分光光度法测定, NO3--N采用麝香草酚分光光度法测定, PO43--P采用钼酸铵分光光度法测定; COD采用联华5B-3A型COD快速测定仪测定, MLSS采用重量法测定, 温度与DO值采用雷磁便携式溶解氧测定仪测定, pH采用雷磁PHS-3C pH计测定.
1.3.2 CODins计算方法CODins是指在SPNDPR系统的厌氧段, 原水中的COD被PAOs和GAOs储存为内碳源的量.其计算方法如下:
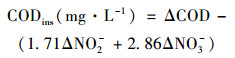
|
式中, ΔCOD、ΔNO2-和ΔNO3-分别为系统厌氧段COD、NO2--N和NO3--N浓度的变化量mg·L-1; 1.71和2.86分别为单位质量浓度的NO2--N和NO3--N被异养反硝化菌利用时所消耗COD的质量浓度.
1.3.3 SND率计算方法SND率用以表示在SPNDPR系统好氧段的氮损失情况, 其计算方法如下:
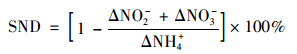
|
式中, ΔNH4+、ΔNO2-和ΔNO3-分别为系统好氧段NH4+-N、NO2--N和NO3--N浓度的变化量, mg·L-1.
2 结果与讨论 2.1 优化运行期间SPNDPR系统的COD去除及厌氧段内碳源贮存特性图 1为SPNDPR系统优化运行期间COD浓度、COD去除率、CODins、COD进水负荷以及COD去除负荷的变化情况.在阶段1[1~28 d, 曝气量由0.125 L·(min·L)-1降低至0.100 L·(min·L)-1], 进水COD浓度约为302.62 mg·L-1, 厌氧末和出水COD浓度分别由75.25 mg·L-1和64.83 mg·L-1逐渐降低至44.64 mg·L-1和33.08 mg·L-1. CODins由26.47 mg·L-1逐渐提高至51.90 mg·L-1.说明降低曝气量有利于提高SPNDPR系统的内碳源贮存性能.此外, COD进水负荷约为151.31 g·(m3·d)-1, COD去除负荷由90.24 g·(m3·d)-1逐渐提高至110.36 g·(m3·d)-1, 且COD去除率由73.57%逐渐提高至86.97%.

|
图 1 优化运行期间SPNDPR系统COD浓度, COD去除率和CODins变化情况 Fig. 1 Variations of COD concentration, removal efficiency, and CODins during the optimal operation of the SPNDPR system |
在阶段2[29~53 d, 曝气量由0.100 L·(min·L)-1降低至0.075 L·(min·L)-1], 进水COD浓度约为293.32 mg·L-1; 厌氧末和出水COD浓度分别由70.59 mg·L-1和58.75 mg·L-1逐渐降低并稳定在44.81 mg·L-1和38.25 mg·L-1.此外, COD进水负荷约为146.66 g·(m3·d)-1, COD去除负荷由103.37g·(m3·d)-1逐渐升高并稳定在124.54 g·(m3·d)-1; COD去除率由77.87%逐渐升高并稳定在84.40%.在阶段3[54~77 d, 曝气量由0.075 L·(min·L)-1降低至0.050 L·(min·L)-1, 好氧时间由3 h延长至5 h], 进水COD浓度约为319.24 mg·L-1; 厌氧末和出水COD浓度分别由56.63 mg·L-1和53.25 mg·L-1逐渐升高至第69 d的71.17 mg·L-1和68.58 mg·L-1, 而后逐渐降低并稳定在45.99 mg·L-1和41.64 mg·L-1.此阶段, COD进水负荷和去除负荷分别由117.08 g·(m3·d)-1和97.11 g·(m3·d)-1逐渐降低至第64 d的97.17 g·(m3·d)-1和79.23 g·(m3·d)-1, 而后逐渐升高并稳定在117.35 g·(m3·d)-1和101.71 g·(m3·d)-1; COD去除率由82.94%逐渐降低至第69 d的78.85%, 而后逐渐升高并稳定在86.43%.在阶段4~5[78~118 d, 曝气量由0.050 L·(min·L)-1降低至0.025 L·(min·L)-1, 好氧时间由5 h延长至6 h], 进水COD浓度约为309.78 mg·L-1; 厌氧末和出水COD浓度维持稳定, 分别平均为41.47 mg·L-1和36.18 mg·L-1; COD去除率由87.30%逐渐升高至90.35%.阶段4和5的COD进水负荷分别约为117.45 g·(m3·d)-1和102.16 g·(m3·d)-1, COD去除负荷分别为104.01 g·(m3·d)-1和91.99 g·(m3·d)-1.说明SPNDPR系统的COD去除性能逐步提高并能维持在较高水平[COD进水负荷102.16 g·(m3·d)-1时, COD去除负荷高达91.99 g·(m3·d)-1, 即COD去除率高达90%以上].此外, 在阶段2~5, CODins缓慢升高, 由64.24 mg·L-1逐步升高至约89.74 mg·L-1.进一步说明降低曝气量[由0.075 L·(min·L)-1逐渐降低至0.025 L·(min·L)-1]和延长好氧时间(由3 h逐渐延长至6 h)有利于提高SPNDPR系统的内碳源贮存性能.
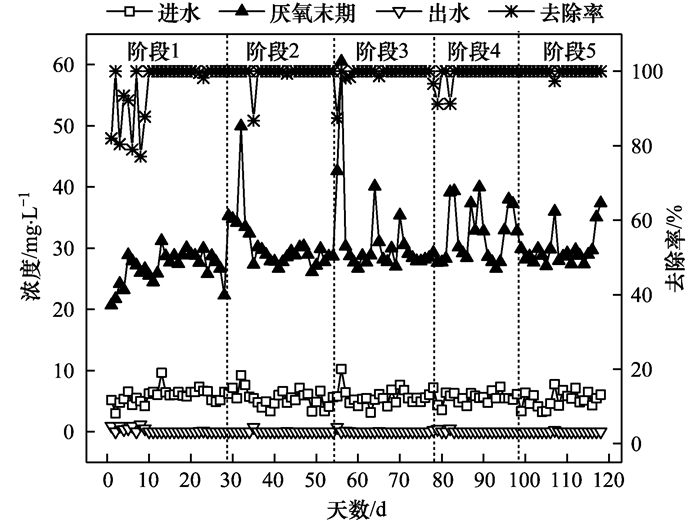
2.2 SPNDPR系统的除磷特性图 2为SPNDPR系统优化运行期间PO43--P浓度及其去除率的变化情况.在阶段1[1~28 d, 曝气量由0.125 L·(min·L)-1降低至0.100 L·(min·L)-1]的第1~19 d, 进水PO43--P浓度约为5.86 mg·L-1; 出水PO43--P浓度和PO43--P去除率均不稳定, 厌氧末PO43--P浓度由20.67 mg·L-1逐渐升高至26.64 mg·L-1.在该阶段的第20~28 d, 厌氧末PO43--P浓度和出水PO43--P浓度均维持稳定, 分别平均为27.65 mg·L-1和0.01 mg·L-1; PO43--P去除率高达99.88%, 说明系统除磷性能较好.在阶段2~5(29~118 d), SPNDPR系统进水PO43--P浓度、厌氧末PO43--P浓度、出水PO43--P浓度和PO43--P去除率均维持稳定, 分别平均为5.51、30.92、0.03 mg·L-1和99.39%.
|
图 2 优化运行期间SPNDPR系统PO43--P浓度及其去除率的变化情况 Fig. 2 Variations of the PO43--P concentration and removal efficiency during the optimal operation of the SPNDPR system |
上述实验结果表明, 改变运行条件[曝气量由0.125 L·(min·L)-1降低至0.100 L·(min·L)-1]后, SPNDPR系统的除磷性能受到影响(PO43--P去除率不稳定), 经过一段时间(约8 d)的运行, 系统除磷性能稳定在较高水平(PO43--P去除率高达99.88%).当曝气量由0.100 L·(min·L)-1降至0.025 L·(min·L)-1过程中, SPNDPR系统的除磷性能几乎不受影响, 表现为PO43--P去除率稳定维持在较高水平(约为99.39%).
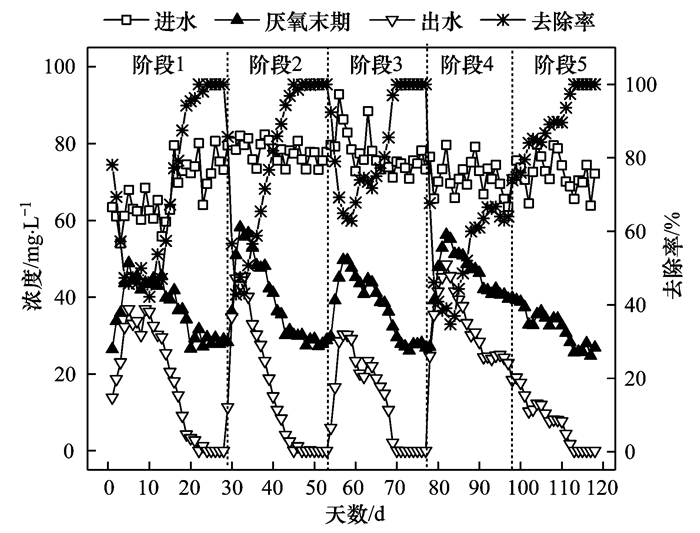
2.3 SPNDPR系统的硝化特性 2.3.1 SPNDPR系统优化运行期间NH4+-N浓度及NH4+-N去除率变化情况图 3为SPNDPR系统优化运行期间NH4+-N浓度及NH4+-N去除率变化情况.在阶段1[1~28 d, 曝气量由0.125 L·(min·L)-1降低至0.100 L·(min·L)-1], 进水NH4+-N浓度约为67.38 mg·L-1; 厌氧末和出水NH4+-N浓度分别由26.47 mg·L-1和13.90 mg·L-1逐渐提高至第5 d的48.91 mg·L-1和36.91 mg·L-1, 而后逐渐降低并稳定维持在28.99 mg·L-1和0.说明曝气量的突降使SPNDPR系统硝化不完全, 但是运行一段时间(21 d左右)后, SPNDPR系统的硝化性能得到提高, 并稳定在较高水平(出水NH4+-N浓度约为0). NH4+-N去除率由100%逐渐降低至第10 d的42.16%, 而后逐渐上升并稳定维持在98%以上.说明降低曝气量引起SPNDPR系统的硝化性能变差(NH4+-N去除率降至50%以下), 但是运行一段时间(21 d左右)之后, 系统的硝化性能逐渐提高并稳定在较高水平(NH4+-N去除率高达98%以上).
|
图 3 优化运行期间SPNDPR系统NH4+-N浓度及其去除率的变化情况 Fig. 3 Variations of NH4+-N concentration and removal efficiency during the optimal operation of the SPNDPR system |
在阶段2[29~53 d, 曝气量由0.100 L·(min·L)-1降低至0.075 L·(min·L)-1], 进水NH4+-N浓度约为77.91 mg·L-1; 厌氧末和出水NH4+-N浓度分别由28.30 mg·L-1和11.36 mg·L-1逐渐升高至第32 d的58.23 mg·L-1和45.36 mg·L-1, 而后逐渐降低并稳定维持在28.72 mg·L-1和0.18 mg·L-1. NH4+-N去除率由100%逐渐下降至第44 d的43.06%, 而后逐渐升高并稳定维持在99.80%.
在阶段3[54~77 d, 曝气量由0.075 L·(min·L)-1降低至0.050 L·(min·L)-1, 好氧时间由3 h延长至5 h], 进水NH4+-N浓度约为77.43 mg·L-1; 厌氧末和出水NH4+-N浓度由29.71 mg·L-1和6.00 mg·L-1逐渐升高至第57 d的49.68 mg·L-1和30.31 mg·L-1, 而后逐渐降低并稳定维持在27.39 mg·L-1和0. NH4+-N去除率由100%逐渐下降至第69 d的62.89%, 而后逐渐升高并稳定维持在100%.
在阶段4[78~97d, 曝气量由0.050 L·(min·L)-1降低至0.025 L·(min·L)-1, 好氧时间为5 h], 进水NH4+-N浓度约为71.29 mg·L-1; 厌氧末和出水NH4+-N浓度由27.10 mg·L-1和24.73 mg·L-1逐渐升高至第82 d的56.27 mg·L-1和48.56 mg·L-1, 而后逐渐降低并稳定维持在40.83 mg·L-1和24.19 mg·L-1. NH4+-N去除率由100%逐渐降低至第83 d的34.66%, 而后逐渐升高并稳定维持在64.76%.在阶段5(98~118 d, 好氧时间由5 h延长至6 h), 进水NH4+-N浓度约为72.19 mg·L-1; 厌氧末和出水NH4+-N浓度由39.84 mg·L-1和18.47 mg·L-1逐渐降低并稳定维持在26.27 mg·L-1和0.NH4+-N去除率由73.90%逐渐提高并稳定维持在100%.
上述实验结果表明, 当曝气量由0.125 L·(min·L)-1降至0.100 L·(min·L)-1和由0.100 L·(min·L)-1降至0.075 L·(min·L)-1时, 系统硝化速率均能恢复并稳定维持在0.16 mg·(L·min)-1左右.但曝气量继续降至0.050 L·(min·L)-1和0.025 L·(min·L)-1后, 硝化速率分别降至0.09 mg·(L·min)-1和0.06 mg·(L·min)-1左右.说明曝气量降至0.050 L·(min·L)-1和0.025 L·(min·L)-1时, 系统硝化性能变差.
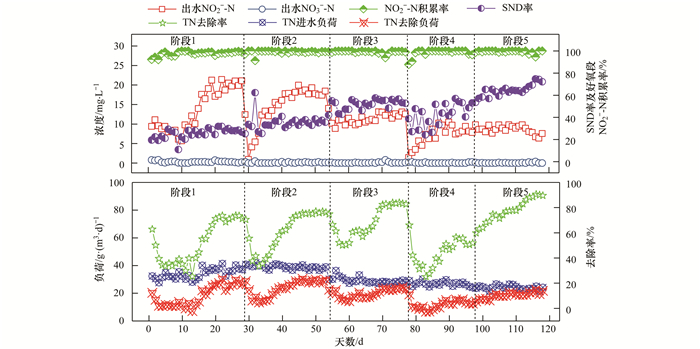
2.3.2 SPNDPR系统优化运行期间出水NO2--N和NO3--N浓度变化情况图 4为SPNDPR系统优化运行期间出水NO2--N和NO3--N浓度变化情况.在阶段1[1~28 d, 曝气量由0.125 L·(min·L)-1降低至0.100 L·(min·L)-1], 出水NO2--N浓度由9.39 mg·L-1逐步降低至第10 d的5.70 mg·L-1, 而后逐渐升高并稳定在19.67 mg·L-1; 出水NO3--N浓度稳定维持在0.31 mg·L-1. NO2--N积累率稳定维持在97.61%.说明SPNDPR系统的短程硝化性能得以稳定维持. TN进水负荷约为34.15 g·(m3·d)-1, TN去除负荷由20.34 g·(m3·d)-1逐渐提高至18 d的22.23 g·(m3·d)-1, 而后稳定维持在26.70 g·(m3·d)-1; TN去除率由62.82%逐渐降低至第18 d的25.34%, 而后逐渐提高并稳定维持在72.06%; SND率由19.57%逐渐提高并稳定维持在28.64%.说明降低曝气量后有利于同步短程硝化反硝化性能的提高.
|
图 4 优化运行期间SPNDPR系统出水NO2--N和NO3--N浓度的变化情况 Fig. 4 Variation of effluent NO2--N and NO3--N concentration during the optimal operation of the SPNDPR system |
在阶段2[29~53 d, 曝气量由0.100 L·(min·L)-1降低至0.075 L·(min·L)-1], 出水NO2--N浓度由12.43 mg·L-1突降至第30 d的0.93 mg·L-1, 而后逐渐升高并稳定在18.19 mg·L-1; 出水NO3--N浓度稳定维持在0.13 mg·L-1. NO2--N积累率稳定维持在99.00%. TN进水负荷约为39.08 g·(m3·d)-1, TN去除负荷由28.80 g·(m3·d)-1逐渐降低至33 d的13.34 g·(m3·d)-1, 而后逐渐升高并稳定在28.99 g·(m3·d)-1; TN去除率由70.47%逐渐降低至第33 d的33.48%, 而后逐渐升高并稳定在75.91%; SND率由25.27%逐渐提高并稳定维持在35.67%.
在阶段3[54~77 d, 曝气量由0.075 L·(min·L)-1降低至0.050 L·(min·L)-1, 好氧时间由3 h延长至5 h], 出水NO2--N浓度由14.01 mg·L-1逐渐降低至第56d的8.87 mg·L-1, 而后逐渐升高并稳定在12.60 mg·L-1; 出水NO3--N浓度稳定维持在0.11 mg·L-1. NO2--N积累率稳定维持在99.12%. TN进水负荷约为29.17 g·(m3·d)-1, TN去除负荷由22.54 g·(m3·d)-1逐渐降低至第60 d的14.22 g·(m3·d)-1, 而后逐渐提高并稳定在22.66 g·(m3·d)-1; TN去除率由74.93%逐渐降低至第60 d的52.05%, 而后逐渐提高并稳定在81.21%; SND率由42.09%逐渐提高并稳定维持在54.21%.与阶段2相比, 阶段3的TN去除性能得到提高(TN去除率由阶段2的75.91%提高至阶段3的81.21%).
在阶段4[78~97 d, 曝气量由0.050 L·(min·L)-1降低至0.025 L·(min·L)-1, 好氧时间为5 h], 出水NO2--N浓度由12.57 mg·L-1降至1.43 mg·L-1, 而后逐渐升高并稳定在8.80 mg·L-1; 出水NO3--N浓度稳定维持在0.07 mg·L-1. NO2--N积累率稳定维持在98.27%. TN进水负荷约为26.87 g·(m3·d)-1, TN去除负荷由19.20 g·(m3·d)-1逐渐降低至第81 d的8.67 g·(m3·d)-1, 而后逐渐提高并稳定维持在13.75 g·(m3·d)-1; TN去除率由66.02%逐渐降低至第81 d的31.24%, 而后逐渐升高并稳定在51.40%; SND率由38.82%逐渐提高并稳定维持在49.48%.
在阶段5(98~118 d, 好氧时间由5 h延长至6 h), 出水NO2--N、NO3--N浓度和NO2--N积累率分别稳定维持在8.62 mg·L-1、0.06 mg·L-1和99.26%.此外, TN进水负荷约为24.09 g·(m3·d)-1, TN去除负荷由14.12 g·(m3·d)-1逐渐提高并稳定维持在20.15 g·(m3·d)-1; TN去除率和SND率分别由59.87%和53.53%逐渐升高并稳定维持在87.08%和72.11%.
上述实验结果表明, 随着曝气量的降低[由0.125 L·(min·L)-1分别降至0.100、0.075、0.050、0.025 L·(min·L)-1], TN去除率逐渐升高(由62.82%升高至87.08%).说明降低曝气量有利于实现SPNDPR系统的深度脱氮.此外, SND率也随曝气量的降低逐渐升高, 由19.57%升高至72.11%.说明降低曝气量可以加强SPND作用.
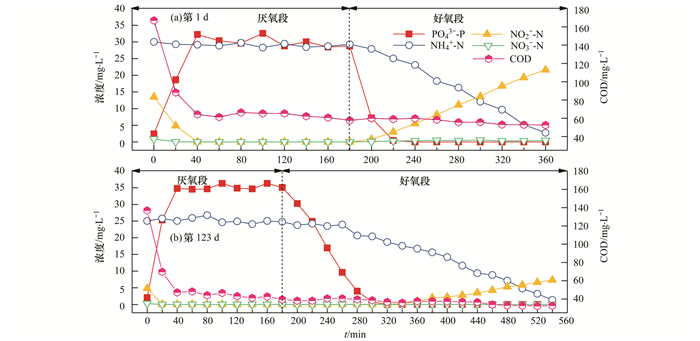
2.4 不同曝气量下SPNDPR系统实现生活污水同步短程硝化反硝化除磷的机制为进一步分析不同曝气量下SPNDPR系统的脱氮除磷机制, 分别对系统第1 d和第123 d典型周期内基质浓度变化情况进行分析, 见图 5.如图 5(a)所示, SPNDPR系统初始COD、NH4+-N、NO2--N、NO3--N和PO43--P浓度分别为167.05、29.49、0、13.51和0.86 mg·L-1.在厌氧段(0~180 min), COD浓度逐渐降低, 并伴随着磷的释放和NOx--N的去除.在0~20 min, NO2--N和NO3--N浓度迅速降至约0, PO43--P浓度呈线性增长趋势, 并伴随着COD浓度的迅速减少.说明0~40min内主要发生NOx--N的外源反硝化作用及PAOs的释磷作用.在40~180 min内, PO43--P浓度维持稳定(约为28.79 mg·L-1), 但COD浓度持续降低了6.56 mg·L-1, 说明40~180 min内仍存在着聚糖菌将外源COD向内碳源转化的过程.在好氧段(180~360 min), COD浓度基本保持不变, PO43--P浓度由28.79 mg·L-1逐渐降至0mg·L-1.证明了好氧吸磷或反硝化除磷的存在.此外, 该阶段NH4+-N浓度由29.29 mg·L-1逐渐降低至0, 减少了29.29 mg·L-1; NO2--N由0逐渐升高至21.61 mg·L-1, NO3--N仅为0.45 mg·L-1; 好氧段氮损失为7.23 mg·L-1.其证明了SPNDPR系统内同步短程硝化反硝化的存在.
|
图 5 优化运行的SPNDPR系统在典型周期内的污染物去除情况 Fig. 5 Pollutant removal in a typical period of optimized operation of the SPNDPR system |
如图 5(b)所示, 初始COD、NH4+-N、NO2--N、NO3--N和PO43--P浓度分别为129.80、24.79、4.81、0.25和2.04 mg·L-1.在厌氧段(0~180 min), COD浓度逐渐降低, 并伴随着磷的释放和NOx--N的去除.在0~20 min, NO2--N和NO3--N浓度迅速降至约0.在0~40 min内, PO43--P浓度成线性增长趋势, 并伴随着COD浓度的迅速降低.说明0~40 min内主要发生NOx--N的外源反硝化作用及PAOs的释磷作用.此外, 考虑到该阶段NOx--N的浓度较低(≤5mg·L-1), 所以COD的去除主要是通过释磷作用实现的.在40~180 min内, PO43--P浓度维持稳定(约为35.07 mg·L-1), COD浓度持续降低了7.59 mg·L-1.在好氧段(180~540 min), COD浓度基本保持不变. PO43--P浓度由35.07 mg·L-1逐渐降至0. NH4+-N浓度由24.77 mg·L-1逐渐降低至0;NO2--N由0逐渐升高至7.30 mg·L-1, NO3--N为0 mg·L-1; 好氧段氮损失高达17.47 mg·L-1.
由典型周期(图 5)对比分析可知, 厌氧段释磷量(PRA)由28.79 mg·L-1提高至35.07 mg·L-1, 即通过厌氧释磷作用去除的COD有所提高.释磷结束后COD的减少量由6.56 mg·L-1提高至7.59 mg·L-1, 说明聚糖菌将外源COD向内碳源转化的性能得到增强.好氧段吸磷速率由0.71 mg·(L·min)-1降低至0.29 mg·(L·min)-1, 硝化速率由0.15 mg·(L·min)-1降低至0.07 mg·(L·min)-1.说明曝气量的降低使得吸磷速率和硝化速率都有所降低.值得注意的是, 通过SND作用去除的NH4+-N浓度由7.23 mg·L-1提高至17.47 mg·L-1, 说明低曝气量下有利于SND作用的进行.此外, 典型周期中, 好氧段基本没有NO3--N生成, 说明改变运行方式[曝气量降至0.025 L·(min·L)-1, 好氧时间延长至6h]并未破坏短程硝化进程.
3 结论(1) 采用延时厌氧(180 min)/好氧的运行方式, 通过优化好氧段曝气量[由0.125 L·(min·L)-1逐渐降低至0.025 L·(min·L)-1]和好氧时间(由3h逐渐延长至6 h), 可以实现SPNDPR系统的深度脱氮除磷.优化后的SPNDPR系统出水NH4+-N、NO2--N、NO3--N和PO43--P浓度分别为0、8.62、0.06和0.03 mg·L-1; 出水TN浓度约为9.22mg·L-1, TN去除率高达87.08%.
(2) 降低曝气量[由0.125 L·(min·L)-1逐渐降低至0.025 L·(min·L)-1]和延长好氧时间(由3 h逐渐延长至6 h)有利于提高SPNDPR系统的内碳源贮存性能(由61.20 mg·L-1逐渐升高至89.74 mg·L-1).优化后SPNDPR系统COD去除率和CODins分别高达90.35%和89.74 mg·L-1.
(3) 当曝气量由0.125 L·(min·L)-1降至0.100 L·(min·L)-1和由0.100 L·(min·L)-1降至0.075 L·(min·L)-1时, 系统硝化速率均能恢复并稳定维持在0.16 mg·(L·min)-1左右.但曝气量继续降至0.050 L·(min·L)-1和0.025 L·(min·L)-1后, 硝化速率分别降至0.09 mg·(L·min)-1和0.06 mg·(L·min)-1左右.说明曝气量降至0.050 L·(min·L)-1和0.025 L·(min·L)-1时, 系统硝化性能变差.
(4) 随着曝气量的降低[由0.125 L·(min·L)-1依次降至0.100、0.075、0.050、0.025 L·(min·L)-1]和好氧时间的延长(由3 h延长至6 h), TN去除率逐渐升高(由62.82%升高至87.08%).说明降低曝气量有利于实现SPNDPR系统的深度脱氮.此外, SND率也随曝气量的降低逐渐升高, 由19.57%升高至72.11%.说明降低曝气量可以加强SPND作用.
| [1] | Fux C, Boehler M, Huber P, et al. Biological treatment of ammonium-rich wastewater by partial nitritation and subsequent anaerobic ammonium oxidation (anammox) in a pilot plant[J]. Journal of Biotechnology, 2002, 99(3): 295-306. DOI:10.1016/S0168-1656(02)00220-1 |
| [2] | 张小玲.短程硝化-反硝化生物脱氮与反硝化聚磷基础研究[D].西安: 西安建筑科技大学, 2004. |
| [3] | Virdis B, Read S T, Rabaey K, et al. Biofilm stratification during simultaneous nitrification and denitrification (SND) at a biocathode[J]. Bioresource Technology, 2011, 102(1): 334-341. DOI:10.1016/j.biortech.2010.06.155 |
| [4] |
马放, 李平, 张晓琦, 等. SBR反应器同步硝化反硝化影响因素及其特性[J]. 哈尔滨工业大学学报, 2011, 43(8): 55-60. Ma F, Li P, Zhang X Q, et al. The influencing factors and the characteristics of simultaneous nitrification-denitrification in SBR[J]. Journal of Harbin Institute of Technology, 2011, 43(8): 55-60. |
| [5] |
彭赵旭, 彭永臻, 左金龙. 同步硝化反硝化的影响因素研究[J]. 给水排水, 2009, 35(5): 167-171. Peng Z X, Peng Y Z, Zuo J L. Study of influence factors on simultaneous nitrification and denitrification[J]. Water Supply and Drainage, 2009, 35(5): 167-171. DOI:10.3969/j.issn.1002-8471.2009.05.049 |
| [6] | Wang X X, Wang S Y, Xue T L, et al. Treating low carbon/nitrogen (C/N) wastewater in simultaneous nitrification-endogenous denitrification and phosphorous removal (SNDPR)systems by strengthening anaerobic intracellular carbon storage[J]. Water Research, 2015, 77: 191-200. DOI:10.1016/j.watres.2015.03.019 |
| [7] | Fu Z M, Yang F L, An Y Y, et al. Simultaneous nitrification and denitrification coupled with phosphorus removal in an modified anoxic/oxic-membrane bioreactor (A/O-MBR)[J]. Biochemical Engineering Journal, 2008, 43(2): 191-196. |
| [8] |
刘春, 年永嘉, 张静, 等. 微气泡曝气生物膜反应器同步硝化反硝化研究[J]. 环境科学, 2014, 35(6): 2230-2235. Liu C, Nian Y J, Zhang J, et al. Simultaneous nitrification and denitrification in a microbubble-aerated biofilm reactor[J]. Environmental Science, 2014, 35(6): 2230-2235. |
| [9] | Münch E V, Lant P, Keller J. Simultaneous nitrification and denitrification in bench-scale sequencing batch reactors[J]. Water Research, 1996, 30(2): 277-284. DOI:10.1016/0043-1354(95)00174-3 |
| [10] |
吕宏德, 张树军, 王伟, 等. A/O短程硝化反应器处理高浓氨氮废水的SND[J]. 中国给水排水, 2008, 24(13): 89-91, 95. Lü H D, Zhang S J, Wang W, et al. Study on SND in A/O shortcut nitrification reactor for treatment of high-concentration ammonia nitrogen wastewater[J]. China Water & Wastewater, 2008, 24(13): 89-91, 95. DOI:10.3321/j.issn:1000-4602.2008.13.024 |
| [11] |
苗志加, 彭永臻, 薛桂松, 等. 强化生物除磷工艺富集聚磷菌及其微生物菌群分析[J]. 北京工业大学学报, 2013, 39(5): 743-748. Mao Z J, Peng Y Z, Xue G S, et al. Enrichment and analysis of the population of phosphate accumulating organisms in enhanced biological phosphorus removal system[J]. Journal of Beijing University of Technology, 2013, 39(5): 743-748. |
| [12] | Zengin G E, Artan N, Orhon D, et al. Population dynamics in a sequencing batch reactor fed with glucose and operated for enhanced biological phosphorus removal[J]. Bioresource Technology, 2010, 101(11): 4000-4005. DOI:10.1016/j.biortech.2010.01.044 |
| [13] | Li N, Ren N Q, Wang X H, et al. Effect of temperature on intracellular phosphorus absorption and extra-cellular phosphorus removal in EBPR process[J]. Bioresource Technology, 2010, 101(15): 6265-6268. DOI:10.1016/j.biortech.2010.03.008 |
| [14] | Wang F, Lu S, Wei Y J, et al. Characteristics of aerobic granule and nitrogen and phosphorus removal in a SBR[J]. Journal of Hazardous Materials, 2009, 164(2-3): 1223-1227. DOI:10.1016/j.jhazmat.2008.09.034 |
| [15] | Ma Y, Peng Y Z, Wang X L. Improving nutrient removal of the AAO process by an influent bypass flow by denitrifying phosphorus removal[J]. Desalination, 2009, 246(1-3): 534-544. DOI:10.1016/j.desal.2008.04.061 |
| [16] | 戴娴.富集聚磷菌的EBPR耦合同步硝化反硝化系统脱氮除磷性能研究[D].北京: 北京工业大学, 2016. |
| [17] |
戴娴, 王晓霞, 彭永臻, 等. 进水C/N对富集聚磷菌的SNDPR系统脱氮除磷的影响[J]. 中国环境科学, 2015, 35(9): 2636-2643. Dai X, Wang X X, Peng Y Z, et al. Effect of influent C/N ratio on simultaneous nitrification-denitrification and phosphorus removal (SNDPR) enriched with phosphorus accumulating organisms (PAOs)[J]. China Environmental Science, 2015, 35(9): 2636-2643. DOI:10.3969/j.issn.1000-6923.2015.09.011 |
| [18] | 张静, 陈洪斌. 低碳源污水的脱氮除磷技术研究进展[J]. 水处理技术, 2014, 40(1): 1-6, 15. |
| [19] |
刘钢, 谌建宇, 黄荣新, 等. 新型后置反硝化工艺处理低C/N(C/P)比污水脱氮除磷性能研究[J]. 环境科学学报, 2013, 33(11): 2979-2986. Liu G, Chen J Y, Huang R X, et al. Nutrient removal performance of a novel post-anoxic process in treating wastewater with low C/N(C/P) ratios[J]. Acta Scientiae Circumstantiae, 2013, 33(11): 2979-2986. |
| [20] |
温沁雪, 唐致文, 陈志强, 等. A2O工艺好氧末段溶解氧变化对脱氮除磷影响[J]. 环境工程学报, 2011, 5(5): 1041-1046. Wen Q X, Tang Z W, Chen Z Q, et al. Effects of dissolved oxygen concentration at the end of aerobic stage in A2O on nitrogen and phosphorus removal[J]. Chinese Journal of Environmental Engineering, 2011, 5(5): 1041-1046. |
| [21] |
操家顺, 陈洵, 方芳. 低溶解氧对改良A/A/O工艺脱氮除磷的影响[J]. 净水技术, 2013, 32(6): 40-44, 63. Cao J S, Chen X, Fang F. Effect of low concentration of dissolved oxygen on nitrogen and phosphorus removal with modified A/A/O processes[J]. Water Purification Technology, 2013, 32(6): 40-44, 63. |
| [22] | 王建龙, 彭永臻, 王淑莹. 污泥龄对A2/O工艺脱氮除磷效果的影响[J]. 环境工程, 2007, 25(1): 16-18. |
| [23] | 徐伟锋, 顾国维, 陈银广. SRT对A2/O工艺脱氮除磷的影响[J]. 水处理技术, 2007, 33(9): 68-71. DOI:10.3969/j.issn.1000-3770.2007.09.017 |
| [24] |
许小平, 陶晓武, 杜敬, 等. 污泥龄对A2/O工艺脱氮除磷的影响分析[J]. 中国给水排水, 2013, 29(21): 69-71. Xu X P, Tao X W, Du J, et al. Effect of SRT on nitrogen and phosphorus removal in A2/O process[J]. China Water & Wastewater, 2013, 29(21): 69-71. |
| [25] |
许劲, 孙俊贻. 生物除磷脱氮系统工程设计中的污泥龄[J]. 重庆建筑大学学报, 2005, 27(5): 86-89. Xu J, Sun J Y. Sludge retention time in design of biological phosphorus and nitrogen removal system[J]. Journal of Chongqing Architecture University, 2005, 27(5): 86-89. |
| [26] | Gieseke A, Arnz P, Amann R, et al. Simultaneous P and N removal in a sequencing batch biofilm reactor:insights from reactor-and microscale investigations[J]. Water Research, 2002, 36(2): 501-509. DOI:10.1016/S0043-1354(01)00232-9 |
| [27] |
戴娴, 彭永臻, 王晓霞, 等. 不同厌氧时间对富集聚磷菌的SNDPR系统处理性能的影响[J]. 中国环境科学, 2016, 36(1): 92-99. Dai X, Peng Y Z, Wang X X, et al. Effect of different anaerobic time on the nutrient removal in simultaneous nitrification-denitrification and phosphorus removal (SNDPR) systems enriched with phosphorus accumulating organisms[J]. China Environmental Science, 2016, 36(1): 92-99. DOI:10.3969/j.issn.1000-6923.2016.01.015 |
| [28] |
于德爽, 袁梦飞, 王晓霞, 等. 厌氧/好氧SPNDPR系统实现低C/N城市污水同步脱氮除磷的优化运行[J]. 环境科学, 2018, 39(11): 5065-5073. Yu D S, Yuan M F, Wang X X, et al. Simultaneous nitrogen and phosphorus removal characteristics of an anaerobic/aerobic operated SPNDPR system treating low C/N urban sewage[J]. Environmental Science, 2018, 39(11): 5065-5073. |
 2019, Vol. 40
2019, Vol. 40


