2. 西南大学资源环境学院, 重庆 400715
2. College of Resources and Environment, Southwest University, Chongqing 400715, China
磷是生命过程中必须元素, 然而, 大量磷素不断从环境过程中流失, 不仅导致水体含氧量降低、毒素增加, 也使水体富营养化问题日趋严重[1, 2].磷酸盐自然回收率很低, 在水体中形成沉淀后, 会再次释放[3, 4].因此, 减少磷流失, 回收磷资源具有重要的研究价值[5].生物体吸附法[6, 7]是近几年兴起的一种经济、环境友好的吸附技术, 具有操作简单、二次污染小等优点, 但仍面临吸附剂成本高、去除率低等问题[8].因此, 寻求低成本、高效的吸附材料具有重要的实际意义.
生物炭是生物残体在缺氧的情况下, 经由高温热解产生的一类难溶的、稳定的、富含碳素的固态物质, 是一种新型、廉价吸附材料[9, 10].迄今为止, 不少研究者利用污泥[11]、松木[12]、落叶[13]、小麦秸秆[14]等材料制备生物炭, 证明了其对氨氮、硫化物、重金属、有机污染物等具有一定吸附作用.但传统生物炭表面带负电, 对磷酸盐吸附存在容量低, 吸附效果差等问题[15].因此, 有学者通过负载金属离子Fe[16, 17]、Bi[18]、Al[17, 19]等对生物炭进行改性来提高其对磷酸盐的吸附容量[20~22].与其他金属改性方法相比, Ca2+、Mg2+是植物所需的中量元素, 吸附磷后的生物炭含有较多的钙镁元素和磷元素, 施入土壤后可作为土壤改良剂, 减小土壤毒性, 不仅有良好的除磷效果, 还具有一定的环境效益.
近年来, 我国沼气工程大规模快速发展, 每年都有大量沼渣产生, 沼渣富含碳源, 是制备生物炭的良好材料[23].若不及时处理, 不仅影响生态环境也浪费资源.但目前利用农业废弃物沼渣制备生物炭的研究还较少.因此, 本研究将沼渣制备成生物炭, 选用Ca2+、Mg2+两种离子对其进行改性, 增强除磷效果, 从影响因素、动力学模型、吸附等温线等方面分析钙镁改性沼渣生物炭对水中磷的吸附特征, 通过获得廉价、高效的吸附剂, 以期为其用于水体除磷提供理论研究和实践基础.
1 材料与方法 1.1 化学试剂与仪器主要化学试剂:磷酸二氢钾(AR)、抗坏血酸(AR)、钼酸铵(AR)、酒石酸锑钾(AR)、过硫酸钾(AR)、无水氯化钙(AR)、六水氯化镁(AR)、氯化钠(AR)、氢氧化钠(AR)、盐酸(AR)、硫酸(AR)等, 溶液采用去离子水配制.
主要仪器:粉碎机(C-800Y, 浙江); 气氛炉(GF11Q-B, 南京); 电子天平(JA2003A, 上海); pH计(PHS-3C, 上海); 紫外可见/分光光度计(T6新世纪, 北京); 恒温振荡器(ZHWY-2102C, 北京); 离心机(TDZ5-WS, 北京); 电热鼓风干燥箱(DHG-9245A, 上海); 扫描电子显微镜(SU8010, 日本); X射线粉末衍射仪(D8 ADVANCE, 德国); 红外光谱仪(Nicolet 6700, 美国); 物理吸附仪(ASAP 2020, 美国).
1.2 材料的制备 1.2.1 生物炭制备原料沼渣(ZZ)取自重庆市巴南区某养牛场.去除大粗粒后制成2.5 cm×2.5 cm×2 cm小块, 去离子水冲洗, 在烘箱中75℃烘24 h.烘干的原料于坩埚中送入气氛炉, 于不同条件(终温分别为350、550和750℃; 升温速率为5℃ ·min-1)在N2(氮气流速为300 mL ·min-1)气氛保护下, 到达目标温度后恒温保持4 h, 待炭化反应结束后, 继续保持炉内N2气氛冷却至室温, 取不同终温下所得固体研磨过40目(0.45 mm)和80目(0.20 mm)筛, 保留两筛网之间截留物, 残余物即为沼渣生物炭, 记为ZZs(不同终温下s分别为350、550、750℃).
1.2.2 改性生物炭的制备分别取上述制备好的ZZ350、ZZ550和ZZ750这3种生物炭各50.0 g浸渍到500 mL CaCl2/MgCl2混合改性反应溶液中, 室温下振荡反应24 h, 用0.45 μm滤膜过滤, 后将负载了Ca2+/Mg2+的ZZ350、ZZ550和ZZ750这3种生物炭用去离子水反复清洗, 至pH值稳定后, 在105℃下烘干至恒重, 所得固体再一次过40目和80目筛, 两筛网之间的截留物装入棕色瓶中保存备用, 记为CMZZs(不同终温下s分别为350、550、750℃).在上述步骤中, 为了比较混合改性溶液中CaCl2和MgCl2的不同浓度比值对生物炭改性效果的影响, 将CaCl2和MgCl2的浓度(mol ·L-1)比值Ca2+/Mg2+分别设置如下:0/3、1/3、2/3、3/3和3/0, 并以磷吸附量为依据, 通过静态吸附实验得到最佳钙镁改性条件.
1.3 实验方法 1.3.1 不同钙镁比对改性生物炭吸附磷的影响为了比较混合改性溶液不同Ca2+/Mg2+比对生物炭吸附磷的影响, 分别投加1 g的ZZ550和CMZZ550生物炭到150 mL锥形瓶中, 加入50 mL浓度为10 mg ·L-1磷溶液, 用0.1 mol ·L-1 HCl和NaOH调节溶液pH为9.0±0.1.在298 K、180 r ·min-1下恒温振荡24 h后, 经0.45 μm滤膜过滤后, 测定其磷浓度.
1.3.2 溶液初始pH对除磷效果的影响分别投加1 g的ZZs和CMZZs生物炭到150 mL锥形瓶中, 加入50 mL浓度为10 mg ·L-1的磷溶液, 用HCl、NaOH调节初始pH分别为4.0~10.0, 在298 K、180 r ·min-1下恒温振荡24 h后, 经0.45 μm滤膜过滤取水样, 测定其磷浓度.
1.3.3 初始浓度和温度对生物炭吸附磷的影响分别投加1 g的ZZs和CMZZs生物炭到150 mL锥形瓶中, 加入1~250 mg ·L-1磷溶液, 固液比1 :50条件下, 用0.1 mol ·L-1 HCl和NaOH调节溶液pH为9.0±0.1.实验温度分别设为288、303和318 K, 在180 r ·min-1下恒温振荡24 h, 0.45 μm滤膜过滤, 测定其磷浓度.
1.3.4 吸附动力学吸附实验采用批处理方法, 分别称取1 g的ZZs和CMZZs生物炭加入150 mL锥形瓶中, 加入10 mg ·L-1磷溶液, 固液比1 :50, 用0.1 mol ·L-1 HCl和NaOH调节溶液pH为9.0±0.1.将锥形瓶置于恒温振荡器中, 转速180 r ·min-1, 分别在振荡第1、3、5、10、15、20、40、70、120、170、250和350 min时取样, 经0.45 μm滤膜过滤后, 测定其磷浓度.
1.3.5 解吸实验称取饱和吸附磷后的生物炭各1 g, 分别加入纯水、0.1 mol ·L-1 HCl、0.1 mol ·L-1 NaOH、1 mol ·L-1 NaCl溶液, 固液比为1 :50, 室温下振荡24 h, 转速180 r ·min-1, 滤取剩余溶液, 测定其磷浓度, 计算生物炭解吸量.
1.4 分析方法 1.4.1 改性前后生物炭的表征采用扫描电镜来观察改性前后生物炭表面和内部结构变化; 比表面积测定仪来测定生物炭的比表面积、孔容和平均孔径; X射线粉末衍射仪和红外光谱仪来测定生物炭表面的物相结构和表面官能团种类.生物炭的等电点pHpzc采用Babic序批平衡法[24]测定.
1.4.2 溶液中磷浓度的测定采用国标(GB 11893-89)钼酸铵分光光度法[25, 26]测定溶液中磷的含量, 每组3个平行, 达到吸附平衡后, 用式(1)计算生物炭的吸附量.
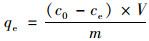
|
(1) |
式中, qe为吸附平衡时生物炭的吸附量, mg ·g-1; c0和ce分别为溶液初始和吸附平衡时磷浓度, mg ·L-1; V为溶液体积, mL; m为生物炭质量, g.
1.4.3 等温吸附模型采用Langmuir和Freundlich[27, 28]方程对生物炭吸附磷的实验数据进行拟合分析, 其表达式如下所示.
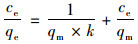
|
(2) |
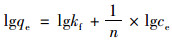
|
(3) |
式中, qe、ce、qm分别表示平衡吸附量、平衡浓度和饱和吸附量, mg ·g-1; k为平衡常数. kf为Freundlich方程吸附速率常数, n表示与吸附强度有关的常数.
1.4.4 动力学模型为分析改性前后生物炭对磷的吸附动力学情况, 采用假一级方程、假二级方程[29~31]和颗粒内扩散方程[32]进行拟合, 并以相关性系数判断各自对方程的适宜性.
假一级方程:

|
(4) |
假二级方程:

|
(5) |
令:
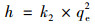
|
(6) |
颗粒内扩散方程:
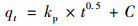
|
(7) |
式中, t为吸附时间, min; qt为t时刻的吸附量, mg ·g-1; qe, exp为实验测得的平衡吸附量, mg ·g-1; qe为理论平衡吸附量, mg ·g-1; k1、k2和kp分别为假一级动力学、假二级动力学和颗粒内扩散速率常数; C是常数, 为颗粒内扩散方程的截距; h为初始吸附速率, g ·(mg ·min)-1.
2 结果与讨论 2.1 不同Ca2+/Mg2+比对生物炭去除磷的影响为了考察改性溶液不同Ca2+ :Mg2+比对生物炭吸附磷的影响, 实验分析了ZZ550和CMZZ550对磷的吸附情况.从图 1中可以看出, ZZ550吸附量最小, 为1.38 mg ·g-1. Ca2+ :Mg2+=2 :3时, CMZZ550吸附量最大, 为25.59 mg ·g-1, 比Ca2+ :Mg2+=1 :3和Ca2+ :Mg2+=3 :3时分别高出5.02 mg ·g-1和11.97 mg ·g-1, 比单独钙和镁改性吸附量分别高出17.06 mg ·g-1和10.28 mg ·g-1.因此, 后续实验均选用改性溶液Ca2+ :Mg2+=2 :3的改性生物炭作为研究对象.

|
图 1 不同钙镁比例复合改性沼渣生物炭对磷吸附的影响 Fig. 1 Removal efficiencies of biochar samples derived from impregnating solutions at different Ca/Mg ratios |
使用扫描电子显微镜比较ZZs、CMZZs表面结构变化, 见图 2.生物炭经过炭化后, 产生丰富的孔隙结构, 炭化温度越高, 呈现更加紊乱无序的排列状态, 与物理吸附测试结果一致(表 1).且通过表 1表面元素分析发现, 改性后生物炭C元素含量降低, Ca2+和Mg2+含量增加, 占元素集合3.36%~5.6%, 分别是改性前的1.3~1.5和8.27~15.42倍, 说明Ca2+和Mg2+占据了生物炭表面C元素, 且Mg2+比Ca2+更好地附着在生物炭表面[16].

|
图 2 不同终温下生物炭的SEM图 Fig. 2 SEM analyses of the ZZs and CMZZs |
|
|
表 1 不同终温下改性前后生物炭的表面元素组成、比表面积和平均孔径 Table 1 Elemental analysis, specific surface area, and average pore size of biochar at different carbonization temperatures |
从表 1还可以看出, 改性前后炭孔径均在20 nm以下, 说明含有大量介孔[33].随炭化温度增加, 改性后生物炭SBET、Vtot、Smic逐渐降低, Dp逐渐增大.可能是因为生物炭微孔被Ca2+、Mg2+或Ca2+、Mg2+氧化物所填充, 造成生物炭内部原有孔隙结构破坏, 内部微孔被堵塞, 同时疏通了中孔和大孔, 因此, SBET、Vtot、Smic等减少, 但是增大了Dp[16].
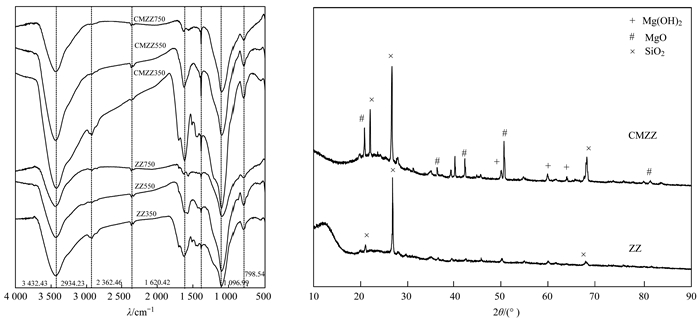
红外光谱图常用来识别炭表面的功能基团, 不同吸收峰代表不同基团.从图 3中可以看出, 改性前后生物炭的红外光谱图趋势基本一致, 说明改性前后生物炭含有丰富相似的化学官能团, 改性未改变官能团种类[32, 34].
|
图 3 改性前后沼渣生物炭FT-IR及XRD图 Fig. 3 FT-IR and XRD analysis of ZZs and CMZZs biochar |
X射线衍射分析(XRD)是晶体结构定性分析的有效方法.如图 3所示, 图谱中各衍射峰尖锐且杂峰较多, 说明生成的非晶胞产物结晶度较高、纯度较低[16]. 2θ在25°附近出现强衍射峰, 对比可以确定是SiO2晶体[34].改性后生物炭2θ在20°、40°、70°附近出现新衍射峰, 对比可能存在MgO、Mg(OH)2等物质[35, 36].改性后生物炭上没有明显钙氧化物[CaO、Ca(OH)2]等特征峰, 这可能与钙氧化物负载量少(表 1)和颗粒尺寸小有关, 且在复合改性材料中复杂的结构也可能会导致其特征峰互相叠加或抵消[16].
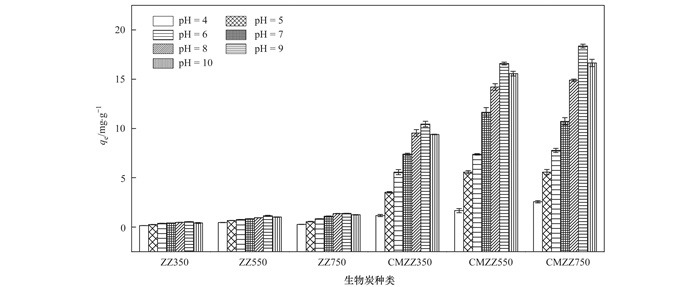
2.3 溶液初始pH对吸附磷的影响溶液初始pH对生物炭除磷效果的影响见图 4.无论是否改性, 生物炭对磷吸附量始终随炭化终温升高而增加, 说明实验范围内终温变化对生物炭除磷性能影响较大.随着初始pH增大, 6种生物炭的吸附量均呈先增大后减少趋势, 且在pH=9时达到最大值.有研究表明, 当溶液pH不同时, 磷存在的形态不同, 主要有H3PO4、H2PO4-、HPO42-和PO43-这4种形态[37].在所研究pH值范围内, 磷主要以H2PO4-、HPO42-两种形式存在.由于生物炭中可能含有MgO微粒, 当pH低于MgO的零点电位时(pHpzc=12), 羟基化后的MgO能与H2PO4-、HPO42-产生静电吸引, 形成非晶体沉淀[38].且CMZZs生物炭表面的Zeta电位为正(pHpzc=10.23), 当pH < 9时, 可通过静电作用吸附H2PO4-、HPO42-[9, 22].其过程如下:
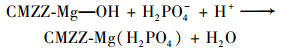
|
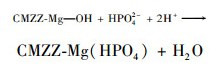
|
|
图 4 溶液pH对改性前后沼渣生物炭吸附磷的影响 Fig. 4 Effect of the solution pH on ZZs and CMZZs adsorption of P |
但MgO含量有限, 与磷之间的反应也十分有限.同时, pH继续增大, OH-浓度迅速增加, 导致静电排斥力增强, 与磷竞争吸附位点, 与Ca2+、Mg2+离子反应生成沉淀, 堵塞孔道, 不利于吸附进行[39].因此, pH对磷吸附是磷形态和生物炭性质综合作用的结果.
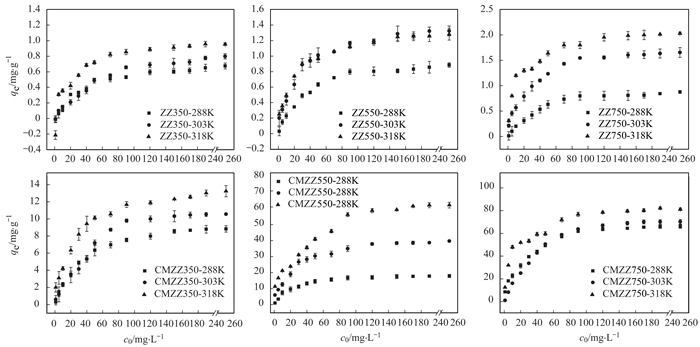
2.4 溶液初始浓度和温度对生物炭吸附磷的影响由图 5可知, 生物炭平衡吸附量随初始磷浓度增加呈先增大后平缓的趋势, 这与初始磷浓度与生物炭表面可吸附利用位点数量比率有关[32].在318 K时, CMZZ750达到吸附量最大值, 为81.23 mg ·g-1, 即, 升高温度有利于生物炭对磷的吸附, 但温度越高能耗越大, 因此综合考虑选择303K为宜.从图 5中还可以看出, 未改性生物炭对磷的吸附效果很差, 在低浓度(1 mg ·L-1和5 mg ·L-1)时吸附量出现了负值, 这是由于ZZ生物炭本身原料含有一定磷, 有磷溶出的现象.
|
图 5 初始浓度和温度对生物炭吸附性能的影响 Fig. 5 Effect of the initial concentration and temperature on the P adsorption of ZZs and CMZZs |
采用Langmuir和Freundlich方程对实验数据进行拟合, 结果如表 2所示. ZZs和CMZZs理论最大饱和吸附量分别为1.27 mg ·g-1和86.92 mg ·g-1. Freundlich方程的回归系数R2均高于Langmuir方程, 说明生物炭对磷的吸附更符合Freundlich等温方程, 表面具有异质性[40], 为多层吸附[41]. 3种温度下Freundlich方程的n-1值均在0~1之间, 说明生物炭对磷的吸附容易进行, 强度较高; qm和k值随温度升高而增大, 说明生物炭的平衡吸附量和吸附速率随温度升高而增大[27].
|
|
表 2 改性前后生物炭对磷吸附等温线的拟合方程参数 Table 2 P adsorption isotherm parameter of ZZs and CMZZs biochar |
2.5 吸附动力学研究
改性前后沼渣生物炭对磷的吸附随时间变化如图 6所示, 前期(1~50 min)生物炭对磷的吸附迅速增加, 50 min后吸附趋势放缓, 所有材料均可在50~100 min内达到吸附平衡.分别采用假一级方程、假二级方程进行拟合.由表 3拟合结果可知, 改性前后生物炭对磷的吸附与假二级动力学拟合程度最好, 相关性系数R2最高, 化学键的形成是影响吸附的主要因素[16, 32]. ZZs和CMZZs对磷的初始吸附速率h随炭化温度升高而增大, 可以解释为炭化温度升高, 增加了吸附质表面积, 从而增加与吸附剂的接触面, 提高其吸附速率[32, 42, 43].

|
图 6 时间对改性前后生物炭吸附P的影响 Fig. 6 Effect of time on the P adsorption of ZZs and CMZZs |
|
|
表 3 改性前后生物炭的动力学模型参数 Table 3 Kinetic parameters of the adsorption models |
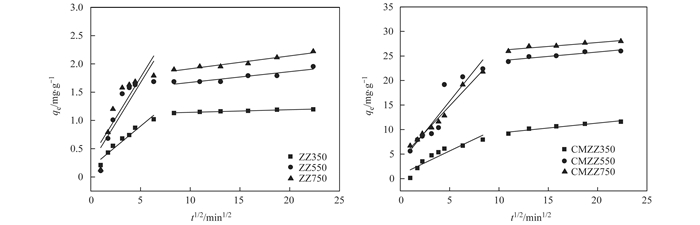
为了确定实验中实际控速步骤, 采用颗粒内扩散方程对动力学数据进行拟合.从图 7可看出, 生物炭改性前后对磷的吸附呈多段性:第一阶段斜率最大, 吸附速率较快; 第二阶段斜率较小, 属于颗粒内扩散阶段[44].拟合直线的反向延长线不通过原点, 说明颗粒内扩散不是唯一的速率控制步骤, 可能是由表面吸附和颗粒内扩散共同控制[16].对所有生物炭的吸附过程(表 3), kp1大于kp2, C1小于C2.说明在开始阶段磷去除率较大, 随着吸附进行, 生物炭表面逐渐形成了边界层, 吸附剂的吸附能力逐渐丧失, 这时吸附速率主要是由吸附质从颗粒外传输至颗粒内的速率决定[32].
|
图 7 生物炭颗粒内扩散吸附曲线 Fig. 7 Intraparticle diffusion curve of ZZs and CMZZs |
为进一步探讨生物炭对磷的吸附机制, 采用FTIR和XRD分析吸附前CMZZ750和吸附磷后生物炭P-CMZZ750.如图 8所示, 以3 428.85 cm-1为中心的FTIR谱带与Mg(OH)2中—OH振动有关[35].位于1 632.48 cm-1处的峰为吸附水的—OH振动峰, 1 371.38 cm-1处为C=C伸缩振动峰, 说明生物炭制备过程中有芳构化过程发生[45]. 900~1 000 cm-1附近的峰为Mg—OH弯曲振动. 500 cm-1附近的峰由Mg—O伸缩振动引起[36].吸附磷后, 464.86 cm-1处Mg—O伸缩振动峰强度下降, 但很容易观察到, 表明可能存在表面MgO与磷(Mg—O—P)之间形成新的颗粒外复合物. 900 cm-1附近Mg—OH振动峰几乎消失, 1 027.20 cm-1处P—O峰强度增加, 意味着Mg—OH和P之间形成颗粒内复合物[35].另外, 从吸附前后XRD图谱可以看出, P-CMZZ750不仅表现出MgO和Mg(OH)2的存在, 还出现了MgHPO4和Mg(H2PO4)2新晶体, 这表明磷与Mg2+之间发生了沉淀反应[17, 35].因此, 综合pH影响及动力学过程, 可以提出磷酸盐的吸附是由表面静电吸引, 颗粒内复合和沉淀过程结合[35].在所研究的pH值范围内, 磷主要是以H2PO4-、HPO42-两种形式存在.反应初始, 由于静电作用H2PO4-、HPO42-和质子化MgOH+相吸附, 随着反应继续进行, 磷酸根离子通过CMZZ750生物炭表面孔隙或间隙, 通过颗粒内扩散和膜扩散过程进一步进入生物炭基质内, 形成颗粒内复合, 并与MgO发生沉淀反应, 形成MgHPO4和Mg(H2PO4)2晶体[17, 35, 36], 见图 9.

|
图 8 吸附前后沼渣生物炭FT-IR及XRD图 Fig. 8 FT-IR and XRD analysis of CMZZ750 and P-CMZZ750 biochar |

|
图 9 P的吸附机制 Fig. 9 Purposed P adsorption mechanism |
改性前后生物炭吸附磷后分别用水、0.1 mol ·L-1 HCl、0.1 mol ·L-1 NaOH、1 mol ·L-1 NaCl作为解吸剂来使已吸附的磷酸根离子解吸出来.从表 4中可看出, ZZs及CMZZs解吸效果均不理想, 解吸率不超过50%.用0.1 mol ·L-1 HCl作为解吸剂时CMZZ750解吸量达到最大, 为5.96 mg ·g-1, 解吸率为46.70%.
|
|
表 4 改性前后生物炭上磷的解吸量/mg ·g-1 Table 4 Data of phosphate desorption capacity on biochar/mg ·g-1 |
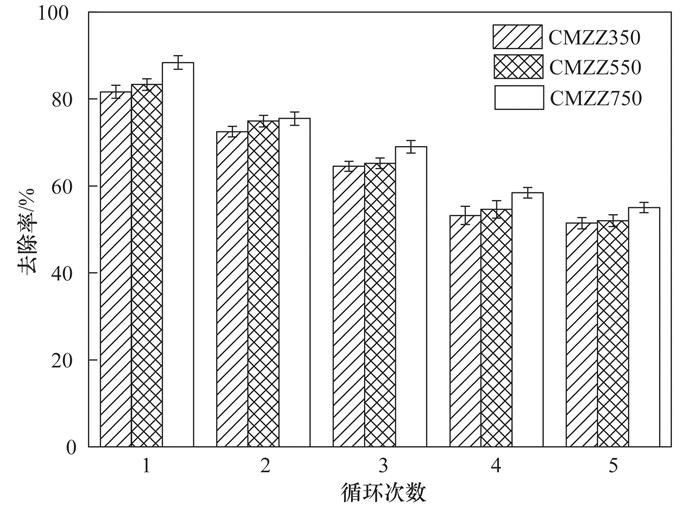
如图 10所示, 把0.1 mol ·L-1 HCl解吸的CMZZs从溶液中分离出来, 并用纯水洗至中性再循环[17].结果如图 10, 经过5次连续循环后, CMZZ350、CMZZ550和CMZZ750对磷去除率分别从81.65%、83.31%和88.38%降至51.45%、52.03%和55.05%.表明改性生物炭中一些活性位点在解吸过程中不能完全逆转[17, 35].虽然生物炭的吸附能力随循环次数的延长而下降, 但经过5次连续循环后, 磷去除率仍高于50%, 表明CMZZs生物炭具有较高的重复使用性, 是一种很有前途的磷去除吸附剂.
|
图 10 CMZZs对P的去除率 Fig. 10 Removal rate of phosphate by CMZZs during five successive cycles |
(1) 钙镁复合改性未改变沼渣生物炭表面化学官能团种类. XRD图谱显示改性后生物炭可能存在Mg(OH)2、MgO等物质, 但钙氧化物[CaO、Ca(OH)2]没有明显特征峰, 这可能与钙的负载量少和颗粒尺寸小有关.
(2) 在中性偏碱的条件下有利于生物炭CMZZs吸附水中磷, 在温度为303 K, pH=9.00时, CMZZ750可达76.92 mg ·g-1.
(3) 吸附符合Freundlich方程, 为多分子层吸附.吸附过程符合假二级动力学方程, 生物炭在100 min内基本达到吸附平衡, 以化学吸附为主.
(4) 用0.1 mol ·L-1 HCl作为解吸剂时, CMZZ750的解吸量为5.96 mg ·g-1大于植物生长所需的磷量(14~50 mg ·kg-1), 经过5次连续循环后, 磷去除率仍高于50%, 说明钙镁复合改性沼渣生物炭对于去除水中磷具有潜在价值.
| [1] | Elser J, Bennett E. Phosphorus cycle:a broken biogeochemical cycle[J]. Nature, 2011, 478(7367): 29-31. DOI:10.1038/478029a |
| [2] | Cordell D, Rosemarin A, Schr?der J J, et al. Towards global phosphorus security:a systems framework for phosphorus recovery and reuse options[J]. Chemosphere, 2011, 84(6): 747-758. DOI:10.1016/j.chemosphere.2011.02.032 |
| [3] | Qiu G L, Law Y M, Das S, et al. Direct and complete phosphorus recovery from municipal wastewater using a hybrid microfiltration-forward osmosis membrane bioreactor process with seawater brine as draw solution[J]. Environmental Science & Technology, 2015, 49(10): 6156-6163. |
| [4] | Loganathan P, Vigneswaran S, Kandasamy J, et al. Removal and recovery of phosphate from water using sorption[J]. Critical Reviews in Environmental Science and Technology, 2014, 44(8): 847-907. DOI:10.1080/10643389.2012.741311 |
| [5] | Bradford-Hartke Z, Lane J, Lant P, et al. Environmental benefits and burdens of phosphorus recovery from municipal wastewater[J]. Environmental Science & Technology, 2015, 49(14): 8611-8622. |
| [6] | Melia P M, Cundy A B, Sohi S P, et al. Trends in the recovery of phosphorus in bioavailable forms from wastewater[J]. Chemosphere, 2017, 186: 381-395. DOI:10.1016/j.chemosphere.2017.07.089 |
| [7] | Fox S, Oren Y, Ronen Z, et al. Ion exchange membrane bioreactor for treating groundwater contaminated with high perchlorate concentrations[J]. Journal of Hazardous Materials, 2014, 264: 552-559. DOI:10.1016/j.jhazmat.2013.10.050 |
| [8] | Zuthi M F R, Guo W S, Ngo H H, et al. Enhanced biological phosphorus removal and its modeling for the activated sludge and membrane bioreactor processes[J]. Bioresource Technology, 2013, 139: 363-374. DOI:10.1016/j.biortech.2013.04.038 |
| [9] |
郑晓青, 韦安磊, 张一璇, 等. 铁锰氧化物/生物炭复合材料对水中硝酸根的吸附特性[J]. 环境科学, 2018, 39(3): 1220-1232. Zheng X Q, Wei A L, Zhang Y X, et al. Characteristic of nitrate adsorption in aqueous solution by iron and manganese oxide/biochar composites[J]. Environmental Science, 2018, 39(3): 1220-1232. |
| [10] |
邱慧, 秦智峰, 刘凤玲, 等. 生物质基纳米HZO杂化材料的研制及其除磷特性[J]. 环境科学, 2018, 39(3): 1212-1219. Qiu H, Qin Z F, Liu F L, et al. Fabrication of a biomass-based hydrous zirconium oxide nanocomposite for advanced phosphate removal[J]. Environmental Science, 2018, 39(3): 1212-1219. |
| [11] | Fan S S, Wang Y, Wang Z, et al. Removal of methylene blue from aqueous solution by sewage sludge-derived biochar:adsorption kinetics, equilibrium, thermodynamics and mechanism[J]. Journal of Environmental Chemical Engineering, 2017, 5(1): 601-611. DOI:10.1016/j.jece.2016.12.019 |
| [12] | Greiner B G, Shimabuku K K, Summers R S. Influence of biochar thermal regeneration on sulfamethoxazole and dissolved organic matter adsorption[J]. Environmental Science:Water Research & Technology, 2018, 4(2): 169-174. |
| [13] | Sahota S, Vijay V K, Subbarao P M V, et al. Characterization of leaf waste based biochar for cost effective hydrogen sulphide removal from biogas[J]. Bioresource Technology, 2018, 250: 635-641. DOI:10.1016/j.biortech.2017.11.093 |
| [14] | Zhou L, Richard C, Ferronato C, et al. Investigating the performance of biomass-derived biochars for the removal of gaseous ozone, adsorbed nitrate and aqueous bisphenol A[J]. Chemical Engineering Journal, 2018, 334: 2098-2104. DOI:10.1016/j.cej.2017.11.145 |
| [15] | Michalekova-Richveisova B, Frišták V, Pipíška M, et al. Iron-impregnated biochars as effective phosphate sorption materials[J]. Environmental Science and Pollution Research, 2017, 24(1): 463-475. DOI:10.1007/s11356-016-7820-9 |
| [16] | Zhou H G, Jiang Z M, Wei S Q. A novel absorbent of nano-Fe loaded biomass char and its enhanced adsorption capacity for phosphate in water[J]. Journal of Chemistry, 2013, 2013: 649868. |
| [17] | Yang Q, Wang X L, Luo W, et al. Effectiveness and mechanisms of phosphate adsorption on iron-modified biochars derived from waste activated sludge[J]. Bioresource Technology, 2018, 247: 537-544. DOI:10.1016/j.biortech.2017.09.136 |
| [18] | Zhu N Y, Yan T M, Qiao J, et al. Adsorption of arsenic, phosphorus and chromium by bismuth impregnated biochar:adsorption mechanism and depleted adsorbent utilization[J]. Chemosphere, 2016, 164: 32-40. DOI:10.1016/j.chemosphere.2016.08.036 |
| [19] | Li R H, Wang J J, Zhou B Y, et al. Enhancing phosphate adsorption by Mg/Al layered double hydroxide functionalized biochar with different Mg/Al ratios[J]. Science of the Total Environment, 2016, 559: 121-129. DOI:10.1016/j.scitotenv.2016.03.151 |
| [20] | Al-Wabel M I, Al-Omran A, El-Naggar A H, et al. Pyrolysis temperature induced changes in characteristics and chemical composition of biochar produced from conocarpus wastes[J]. Bioresource Technology, 2013, 131: 374-379. DOI:10.1016/j.biortech.2012.12.165 |
| [21] | Yao Y, Gao B, Inyang M, et al. Biochar derived from anaerobically digested sugar beet tailings:characterization and phosphate removal potential[J]. Bioresource Technology, 2011, 102(10): 6273-6278. DOI:10.1016/j.biortech.2011.03.006 |
| [22] |
蒋旭涛, 迟杰. 铁改性生物炭对磷的吸附及磷形态的变化特征[J]. 农业环境科学学报, 2014, 33(9): 1817-1822. Jiang X T, Chi J. Phosphorus adsorption by and forms in Fe-modified biochar[J]. Journal of Agro-Environment Science, 2014, 33(9): 1817-1822. |
| [23] | He X M, Zhang T, Ren H Q, et al. Phosphorus recovery from biogas slurry by ultrasound/H2O2 digestion coupled with HFO/biochar adsorption process[J]. Waste Management, 2017, 60: 219-229. DOI:10.1016/j.wasman.2016.08.032 |
| [24] |
唐登勇, 黄越, 胥瑞晨, 等. 改性芦苇生物炭对水中低浓度磷的吸附特征[J]. 环境科学, 2016, 37(6): 2195-2201. Tang D Y, Huang Y, Xu R C, et al. Adsorption behavior of low concentration phosphorus from water onto modified reed biochar[J]. Environmental Science, 2016, 37(6): 2195-2201. |
| [25] | Qi T, Su Z Q, Jin Y, et al. Electrochemical oxidizing digestion using PbO2 electrode for total phosphorus determination in a water sample[J]. RSC Advances, 2018, 8(12): 6206-6211. DOI:10.1039/C8RA00220G |
| [26] | Guo Y J, Tang H, Li G D, et al. Effects of cow dung biochar amendment on adsorption and leaching of nutrient from an acid yellow soil irrigated with biogas slurry[J]. Water, Air, & Soil Pollution, 2014, 225(1): 1820. |
| [27] | Freundlich H M F. Over the adsorption in solution[J]. The Journal of Physical Chemistry, 1906, 57: 385-471. |
| [28] | Stromer B S, Woodbury B, Williams C F. Tylosin sorption to diatomaceous earth described by Langmuir isotherm and Freundlich isotherm models[J]. Chemosphere, 2018, 193: 912-920. DOI:10.1016/j.chemosphere.2017.11.083 |
| [29] | Karunanithi R, Ok Y S, Dharmarajan R, et al. Sorption, kinetics and thermodynamics of phosphate sorption onto soybean stover derived biochar[J]. Environmental Technology & Innovation, 2017, 8: 113-125. |
| [30] | Dawood S, Sen T K, Phan C. Synthesis and characterization of slow pyrolysis pine cone bio-char in the removal of organic and inorganic pollutants from aqueous solution by adsorption:kinetic, equilibrium, mechanism and thermodynamic[J]. Bioresource Technology, 2017, 246: 76-81. DOI:10.1016/j.biortech.2017.07.019 |
| [31] | Yan L G, Yang K, Shan R R, et al. Kinetic, isotherm and thermodynamic investigations of phosphate adsorption onto core-shell Fe3O4 @ LDHs composites with easy magnetic separation assistance[J]. Journal of Colloid and Interface Science, 2015, 448: 508-516. DOI:10.1016/j.jcis.2015.02.048 |
| [32] | Hou J, Huang L, Yang Z M, et al. Adsorption of ammonium on biochar prepared from giant reed[J]. Environmental Science and Pollution Research, 2016, 23(19): 19107-19115. DOI:10.1007/s11356-016-7084-4 |
| [33] | Jung K W, Jeong T U, Kang H J, et al. Preparation of modified-biochar from Laminaria japonica:simultaneous optimization of aluminum electrode-based electro-modification and pyrolysis processes and its application for phosphate removal[J]. Bioresource Technology, 2016, 214: 548-557. DOI:10.1016/j.biortech.2016.05.005 |
| [34] | Tan X F, Liu Y G, Gu Y L, et al. Biochar-based nano-composites for the decontamination of wastewater:a review[J]. Bioresource Technology, 2016, 212: 318-333. DOI:10.1016/j.biortech.2016.04.093 |
| [35] | Li R H, Wang J J, Zhou B Y, et al. Recovery of phosphate from aqueous solution by magnesium oxide decorated magnetic biochar and its potential as phosphate-based fertilizer substitute[J]. Bioresource Technology, 2016, 215: 209-214. DOI:10.1016/j.biortech.2016.02.125 |
| [36] | Li R H, Wang J J, Zhou B Y, et al. Simultaneous capture removal of phosphate, ammonium and organic substances by MgO impregnated biochar and its potential use in swine wastewater treatment[J]. Journal of Cleaner Production, 2017, 147: 96-107. DOI:10.1016/j.jclepro.2017.01.069 |
| [37] | Jung K W, Ahn K H. Fabrication of porosity-enhanced MgO/biochar for removal of phosphate from aqueous solution:application of a novel combined electrochemical modification method[J]. Bioresource Technology, 2016, 200: 1029-1032. DOI:10.1016/j.biortech.2015.10.008 |
| [38] | Jung K W, Jeong T U, Hwang M J, et al. Phosphate adsorption ability of biochar/Mg-Al assembled nanocomposites prepared by aluminum-electrode based electro-assisted modification method with MgCl2 as electrolyte[J]. Bioresource Technology, 2015, 198: 603-610. DOI:10.1016/j.biortech.2015.09.068 |
| [39] | Li S M S, Zeng Z X, Xue W L. Adsorption of lead ion from aqueous solution by modified walnut shell:kinetics and thermodynamics[J]. Environmental Technology, 2018. DOI:10.1080/09593330.2018.1430172 |
| [40] | Gautam S B, Vaishya R C, Devnani G L, et al. Adsorption of As (Ⅲ) from aqueous solutions by iron-impregnated quartz, lignite, and silica sand:kinetic study and equilibrium isotherm analysis[J]. Desalination and Water Treatment, 2014, 52(16-18): 3178-3190. DOI:10.1080/19443994.2013.797182 |
| [41] |
陈靖, 李伟民, 丁文川, 等. Fe/Mg负载改性竹炭去除水中的氨氮[J]. 环境工程学报, 2015, 9(11): 5187-5192. Chen J, Li W M, Ding W C, et al. Removal of ammonia nitrogen by Fe/Mg-modified bamboo charcoal[J]. Chinese Journal of Environmental Engineering, 2015, 9(11): 5187-5192. DOI:10.12030/j.cjee.20151109 |
| [42] | Liu Q, Hu P, Wang J, et al. Phosphate adsorption from aqueous solutions by Zirconium (Ⅳ) loaded cross-linked chitosan particles[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 59: 311-319. DOI:10.1016/j.jtice.2015.08.012 |
| [43] | Mahdi Z, Yu Q J, El Hanandeh A. Investigation of the kinetics and mechanisms of nickel and copper ions adsorption from aqueous solutions by date seed derived biochar[J]. Journal of Environmental Chemical Engineering, 2018, 6(1): 1171-1181. DOI:10.1016/j.jece.2018.01.021 |
| [44] |
马锋锋, 赵保卫, 刁静茹, 等. 牛粪生物炭对水中氨氮的吸附特性[J]. 环境科学, 2015, 36(5): 1678-1685. Ma F F, Zhao B W, Diao J R, et al. Ammonium adsorption characteristics in aqueous solution by dairy manure biochar[J]. Environmental Science, 2015, 36(5): 1678-1685. |
| [45] | Wan S, Wang S S, Li Y C, et al. Functionalizing biochar with Mg-Al and Mg-Fe layered double hydroxides for removal of phosphate from aqueous solutions[J]. Journal of Industrial and Engineering Chemistry, 2017, 47: 246-253. DOI:10.1016/j.jiec.2016.11.039 |
 2019, Vol. 40
2019, Vol. 40


