2. 清华大学水质与水生态研究中心, 北京 100084;
3. 中国科学院生态环境研究中心, 北京 100085
2. Center for Water and Ecology, Tsinghua University, Beijing 100084, China;
3. Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
光催化氧化技术作为高级氧化技术的一种, 在处理难降解有机污染物方面表现良好.而光生电子和空穴的重组, 极大影响了光催化的效率, 从而限制了光催化技术的应用[1].
BiOCl是典型的铋系半导体光催化材料, 具有特殊的晶体和电子结构, [Bi2O2]2+层在两个Cl离子层中间. Cl与Bi原子之间共价作用强, 导致BiOCl极化率强, 从而决定了较强的内部电场, 一定程度上有利于光生电子-空穴有效分离[2, 3], 因此表现出良好的光催化活性.为进一步降低其光生电子和空穴的复合率, 科研人员不断对其进行改性.针对BiOCl的微结构调制, 有一维纳米线(棒)、二维纳米片[2, 4]、三维分层结构[5, 6]和支撑薄膜[7, 8]四大类.针对BiOCl的复合催化剂, 有半导体复合[9, 10]、金属复合[11, 12]、助催化敏化[13, 14]三大类.针对BiOCl的结构设计, 有掺杂或缺陷引入[15, 16]、固溶体光催化剂[17, 18]和其它卤代铋光催化剂[19, 20]三大类.这些改性对光催化活性有了明显的提升.
为了使光生电子得以迅速转移从而降低光生电子和空穴的复合, 人们可以为其添加一种电子受体.多金属氧酸盐分子体积巨大, 结构确定, 并且具有质子储存和转移的能力, 而且还原态和氧化态的多酸不会因为得失电子而导致结构变形, 如已经证实Keggin型结构的[XM12O40]n-能够接受32个电子[21]并保持结构稳定.由于多金属氧酸盐在一定条件下可以进行可逆的、多步的、多电子的氧化还原过程, 因此可以将其作为一类性质优异电子受体. Liu等[22]将磷钨酸与氯化铁形成的Fe(Ⅲ){PO4[WO(O2)2]4}负载到了g-C3N4的表面, 在太阳光照条件下, 对罗丹明B的降解效果良好. Heng等[23]制作的H3PW12O40/TiO2-In2S3复合光催化剂对吡虫啉有良好的降解效果.
受此启发, 人们可以将磷钨酸铵作为氯氧铋的光生电子受体, 制作一种新型的复合光催化剂.近期, 只有Wang等[24, 25]通过沸石负载溴氧铋和磷钨酸, 实现了可见光下良好的催化活性.但是, 复合材料光催化效率提升的机制尚不明确.
本文利用两步水热法, 制备了磷钨酸铵和氯氧铋复合光催化剂.以甲基橙为模拟污染物, 对复合催化剂的光催化活性进行测试.同时研究了元素配比、不同淬灭剂和酸碱性对光催化活性的影响.通过淬灭实验、XPS分析和光电流来对机制进行研究, 表明磷钨酸铵可以接受氯氧铋产生的光生电子, 使得复合光催化剂的光生电子和空穴复合率有了明显的降低.
1 材料与方法 1.1 试剂与仪器主要试剂:硝酸铋Bi(NO3)3 ·5H2O、聚乙烯吡咯烷酮(PVP)、甘露醇、饱和NaCl溶液、磷钨酸(H3PW12O40 ·xH2O)、氯化铵(NH4Cl)、甲基橙(MO)溶液等, 以上试剂均为分析纯, 实验用水为去离子水.
主要仪器:紫外可见分光光度计(U-3900日本Hitachi High-Technologies Co.)、X射线衍射仪(D8 focus德国Bruker公司)、场发射扫描电子显微镜(SU-8020日本日立公司)、透射电子显微镜(JEM-2100日本电子珠式会社)、X射线光电子能谱仪(ESCALAB250Xi赛默飞世尔科技(中国)有限公司)、红外光谱仪(TENSON 27 BRUKEY, Germany)、电化学工作站(Reference 600+GAMRY).
1.2 催化剂制备:磷钨酸铵[(NH4)3PW12O40]制备:将300 mg的H3PW12O40 ·xH2O和110 mg的NH4Cl分别溶于20 mL和10 mL去离子水中, 分别记为A和B溶液(保证NH4Cl和H3PW12O40 ·xH2O的摩尔比大于3 :1).在磁力搅拌的作用下, 将B溶液缓慢滴加至A溶液, 搅拌均匀后放入反应釜中, 在140℃条件下加热12 h.自然冷却后通过离心获得沉淀, 用去离子水清洗3次, 再进行冷冻干燥.
复合催化剂制备:参考Guan等[26]的方式由溶剂热法制备BiOCl.将0.486 g的Bi(NO3)3 ·5H2O和0.400 g的PVP溶于25 mL的0.1mol ·L-1的甘露醇溶液, 通过超声和机械搅拌使其溶解.加入5 mL的饱和NaCl溶液, 产生均一的白色悬浮液.搅拌10 min后, 再加入一定比例的磷钨酸铵, 搅拌均匀后, 倒入到聚四氟乙烯高压反应釜中, 放入烘箱中160℃反应3 h.待反应釜自然冷却到室温后, 离心获得固体沉淀物, 用去离子水洗涤3次以除去多余的离子.样品经过干燥即可使用.
1.3 光催化活性测试催化剂活性以甲基橙(MO)的降解速率来作为评价指标.模拟污染物MO的浓度为10mg ·L-1, 体积为100 mL, 置于300 mL烧杯中, 加入一定量的催化剂.在磁力搅拌的条件下, 利用氙灯模拟太阳光进行光催化实验.反应前, 避光吸附30 min, 达到吸附脱附平衡.光照一定时间后取5 mL反应液, 高速离心分离, 用分光光度计在466 nm处测其上层清液的吸光度.以溶液的降解率来评价光催化剂的活性, 即ct/c0=At/A0(式中, At和A0分别表示t时间和初始溶液的吸光度).在pH条件实验中, 利用0.5mol ·L-1的HNO3溶液和0.5 mol ·L-1的NaOH溶液调节pH值.
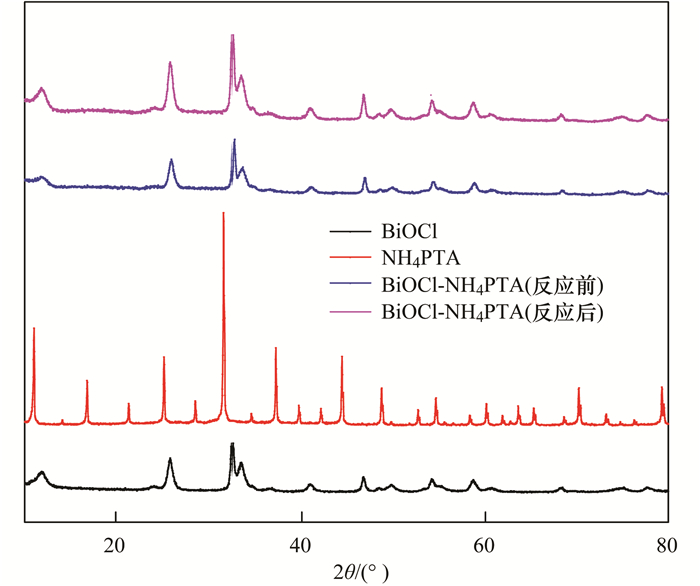
2 结果与讨论 2.1 催化剂理化性质表征利用XRD对BiOCl和复合催化剂进行分析(图 1).水热法制备的BiOCl与JCPDS (No. 82-0485)相对应.主要以001晶面(12.025°)、101晶面(25.905°)、110晶面(32.551°)和102晶面(33.520°)为主.水热法制备的复合催化剂其峰值与BiOCl较为吻合, 但是却无明显的磷钨酸铵的衍射峰.可能是由于磷钨酸铵的含量相对较少, 且分散性较好, 致使其无明显的XRD特征峰.催化剂反应前后的XRD峰值无明显变化, 表明催化剂较为稳定.
|
图 1 样品XRD图 Fig. 1 XRD patterns of samples |
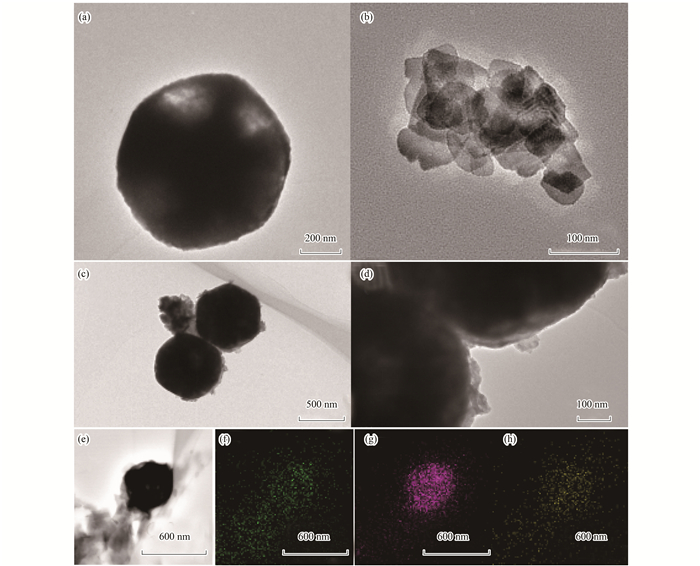
催化剂的微观结构对催化反应有一定的影响.所以通过TEM来对复合催化剂进行微观分析.从图 2(a)看到NH4PTA呈球状, 粒径大约为700 nm; 图 2(b)中的BiOCl呈二维薄片状; 图 2(c)和图 2(d)可以看到BiOCl纳米片在NH4PTA上形成了部分的片层覆盖. 图 2(e)为能谱分析的选定区域, 图 2(f)~2(h)分别表示为选定区域中的Bi、W和P元素.因此可以表明NH4PTA和BiOCl复合良好.
|
(a) NH4PTA透射电镜图; (b) BiOCl透射电镜图; (c)和(d) BiOCl-NH4PTA的透射电镜图; (e)~(h)BiOCl-NH4PTA的元素分布 图 2 催化剂的透射电镜图和元素分布 Fig. 2 TEM images and element mapping of samples |
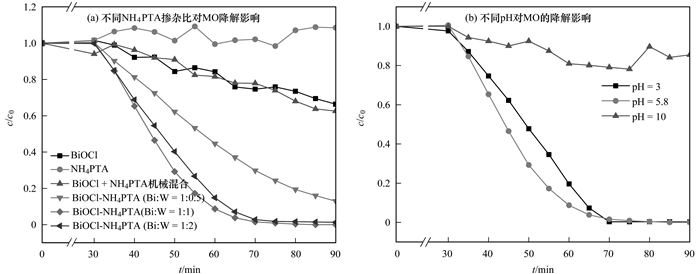
在氙灯模拟的太阳光条件下, 不同掺杂比例的BiOCl-NH4PTA复合光催化剂对MO降解进行了比较实验.如图 3(a)所示, 引入磷钨酸铵后, 催化降解速率较BiOCl有了明显的提升, 当Bi与W的摩尔比1 :1时, 对MO的光催化效果最佳, 在光照0.5 h后, MO的降解率达到了90%以上.不同掺杂比例的BiOCl-NH4PTA, 其降解速率也有所区别.这可能是由于BiOCl过多, 会对NH4PTA过分包裹, 从而降低了光生电子的传递.后续实验中, 均选用催化效果最好的BiOCl-NH4PTA[n(Bi):n(W)=1:1]进行实验.
|
图 3 催化剂对甲基橙的降解效果 Fig. 3 Image of degradation effects of different photocatalysts for MO |
本实验中, 利用0.5mol·L-1的NaOH溶液和0.5mol·L-1的HNO3来调节反应体系的pH值.通过图 3(b)可以看到, 在酸性条件下降解效果较好.但是pH=10时, 催化效率很低.酸碱条件下催化效率的差异是由于酸性条件下, 催化剂表面的正电荷会吸引光生电子迁移到催化剂表面, 一定程度上加强了光生电子和空穴的分离; 同时, 迁移到催化剂表面的电子可以与水中的O2反应生成超氧自由基, 进而提高光催化降解的效率[27, 28].
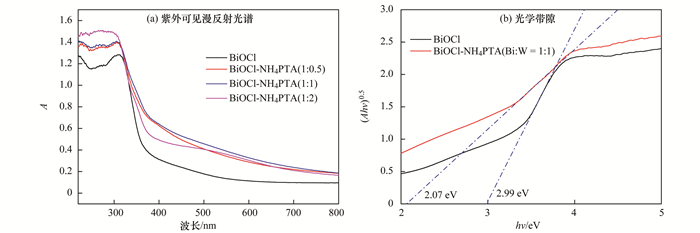
2.3 降解机制讨论紫外可见漫反射吸收光谱可以直观地显示材料在不同波长下的光吸收值.如图 4(a)所示, 复合催化剂较BiOCl发生了明显的红移, 表明复合催化剂增强了可见光区的吸收, 可以利用更多波长范围的光, 进而在实际条件的运用有了一定的基础.异质结的形成, 会对物质的能带产生一定的影响.所以通过计算对比了二者的禁带宽度.根据Tauc plot公式:
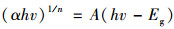
|
|
图 4 BiOCl和NH4PTA-BiOCl的光学性质 Fig. 4 Optical properties of BiOCl and NH4PTA-BiOCl |
式中, α为吸光指数, h为普朗克常数, v为频率, A为常数, Eg为半导体禁带宽度.指数n与半导体类型有关.直接带隙半导体:n=1/2;间接带隙半导体n=2. BiOCl是间接带隙半导体, 故n取2.由此以(Ahv)0.5对hv作图, 其结果如图 4(b)所示, 计算可得BiOCl和复合催化剂的禁带宽度值分别为2.99 eV和2.07 eV.禁带宽度的减小, 可以使催化剂利用更多长波段的光, 进行催化反应.
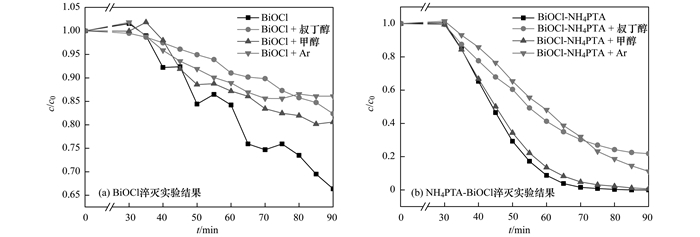
为探究光催化降解MO的内在机制, 通过自由基淬灭实验来对反应过程中的活性物种进行研究.本实验中, 以甲醇为空穴淬灭剂, 叔丁醇作为羟基自由基猝灭剂, Ar曝气来抑制超氧自由基的生成. 图 5分别为BiOCl和复合催化剂的淬灭实验结果.在BiOCl降解MO的过程中, 空穴、羟基自由基和超氧自由淬灭后, 其反应速率均有明显的下降, 说明以上3种活性物种均参与了反应.在复合催化剂的降解MO的过程中, 羟基自由基和超氧自由基淬灭后, 反应速率有明显的下降, 而空穴的淬灭对反应速率的影响较小, 说明BiOCl-NH4PTA复合材料降解MO主要通过羟基自由基和超氧自由基.
|
图 5 BiOCl和NH4PTA-BiOCl光催化氧化MO反应机制 Fig. 5 Reaction mechanism of BiOCl and NH4PTA-BiOCl in the photocatalytic oxidation of MO |
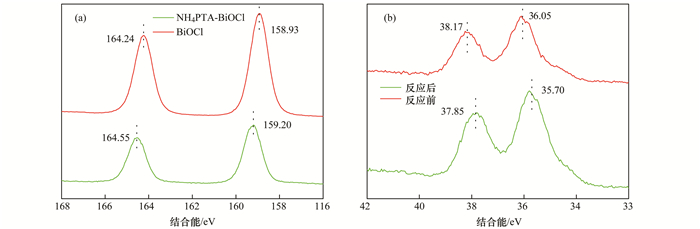
XPS是分析元素价态和化学环境的重要手段之一.为了分析氯氧铋和磷钨酸铵的结合方式, 本研究对BiOCl和复合催化剂中的Bi元素进行了XPS分析, 其结果如图 6(a)所示. 158.93 eV和164.24 eV对应着Bi4f轨道, 表明铋元素为+3价[29].复合催化剂的Bi4f元素的结合能偏移到了159.20 eV和164.55 eV, 表明BiOCl和磷钨酸铵形成了强烈的化学键, 而不是二者简单的机械混合[30, 31].为了验证复合材料反应后磷钨酸铵是否得电子, 本研究对反应前后催化剂的钨元素进行了XPS分析, 如图 6(b)所示, 为催化剂反应前后W4f轨道电子的结合能.反应前的38.17 eV和36.05 eV分别对应着W4f5/2和W4f7/2轨道电子的结合能, 表明钨元素为+6价[32].而反应后, 其对应的峰值偏移到了37.85 eV和35.7 eV. XPS谱图中, 轨道电子向小的结合能方向移动, 表明该元素得电子.测得的这一微小的偏移是由于磷钨酸铵中W元素接收了BiOCl在光照激发下产生的光生电子, 使得其XPS谱图中W元素的结合能降低.
|
(a)BiOCl和NH4PTA-BiOCl中Bi元素; (b)NH4PTA-BiOCl催化剂反应前后W元素 图 6 催化剂XPS谱图 Fig. 6 XPS spectra of samples |
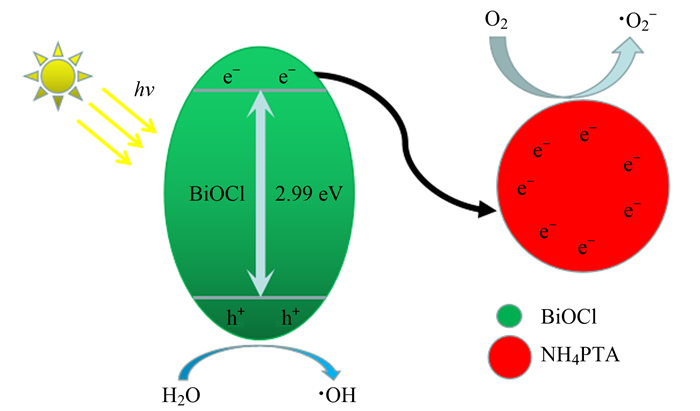
钨元素微弱的偏移并未整体引起化合价的改变.如图 7所示, 在催化反应过程中, 磷钨酸铵接受了来自氯氧铋的光生电子, 传递到磷钨酸铵的电子会迅速与水中的氧气反应, 产生超氧自由基.该体系在加速分离光生电子和空穴的同时, 产生了具有强氧化性的超氧自由基, 从而提高了光催化活性.
|
图 7 光生载流子传递示意 Fig. 7 Photo-induced transfer of electrons and holes at the interface between BiOCl and NH4PTA |
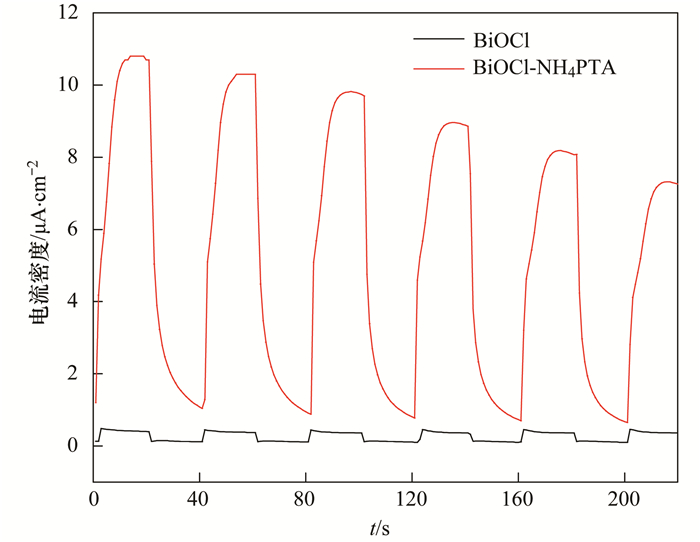
高效的电荷分离和转移是影响光催化的重要因素.可以通过光电流的测试来验证异质结对光生电子的分离和迁移影响[33].在模拟太阳光的照射下, 以0.1mol·L-1的NaSO4溶液为电解液, 在0.8 V电压下对BiOCl和BiOCl-NH4PTA进行光电流测试, 其结果如图 8所示.在光照时, 可以看到两种类型的光电极都产生了均匀稳定的光电流, 同时光响应具有良好的可逆性. BiOCl的光电流密度为0.5 μA·cm-2, 复合催化剂BiOCl-NH4PTA的光电流较BiOCl有了明显的提高, 达到了10 μA·cm-2.光电流的增强是由于复合催化剂的光生电子和空穴可以有效分离[34].
|
图 8 BiOCl和BiOCl-NH4PTA的光电流对比 Fig. 8 Photocurrent of BiOCl and BiOCl-NH4PTA under ultraviolet light |
(1) 通过两步水热法制备了BiOCl-(NH4)3PW12O40复合光催化剂.当Bi与W的摩尔比为1 :1时, 在氙灯模拟的太阳光照射下, 对甲基橙的降解效果最佳.
(2) 通过淬灭实验, 发现羟基自由基和超氧自由基共同作用于光催化氧化过程中. XPS能谱和光电流测试, 证明了磷钨酸铵作为光生电子受体的作用.磷钨酸铵的引入, 使光生电子和空穴得到了有效地分离.
(3) 将杂多酸作为电子受体引入半导体光催化剂, 将会成为降低光生电子和空穴复合率的一种有效方法.
| [1] | Wang H L, Zhang L S, Chen Z G, et al. Semiconductor heterojunction photocatalysts:design, construction, and photocatalytic performances[J]. Chemical Society Reviews, 2014, 43(15): 5234-5244. DOI:10.1039/C4CS00126E |
| [2] | Jiang J, Zhao K, Xiao X Y, et al. Synthesis and facet-dependent photoreactivity of BiOCl single-crystalline nanosheets[J]. Journal of the American Chemical Society, 2012, 134(10): 4473-4476. |
| [3] | Zhao K, Zhang L Z, Wang J J, et al. Surface structure-dependent molecular oxygen activation of BiOCl single-crystalline nanosheets[J]. Journal of the American Chemical Society, 2013, 135(42): 15750-15753. |
| [4] | Chang X F, Huang J, Cheng C, et al. BiOX (X=Cl, Br, I) photocatalysts prepared using NaBiO3 as the Bi source:characterization and catalytic performance[J]. Catalysis Communications, 2010, 11(5): 460-464. |
| [5] | Zhang X, Ai Z H, Jia F L, et al. Generalized one-pot synthesis, characterization, and photocatalytic activity of hierarchical BiOX (X=Cl, Br, I) nanoplate microspheres[J]. The Journal of Physical Chemistry C, 2008, 112(3): 747-753. |
| [6] | Zhu L P, Liao G H, Bing N C, et al. Self-assembled 3D BiOCl hierarchitectures:tunable synthesis and characterization[J]. Crystengcomm, 2010, 12(11): 3791-3796. |
| [7] | Mu Q H, Zhang Q H, Wang H Z, et al. Facile growth of vertically aligned BiOCl nanosheet arrays on conductive glass substrate with high photocatalytic properties[J]. Journal of Materials Chemistry, 2012, 22(33): 16851-16857. |
| [8] | Li Y Y, Liu J P, Jiang J, et al. UV-resistant superhydrophobic BiOCl nanoflake film by a room-temperature hydrolysis process[J]. Dalton Transactions, 2011, 40(25): 6632-6634. DOI:10.1039/c1dt10691k |
| [9] | Cheng H F, Huang B B, Qin X Y, et al. A controlled anion exchange strategy to synthesize Bi2S3 nanocrystals/BiOCl hybrid architectures with efficient visible light photoactivity[J]. Chemical Communications, 2011, 48(1): 97-99. |
| [10] | Zhang J, Xia J X, Yin S, et al. Improvement of visible light photocatalytic activity over flower-like BiOCl/BiOBr microspheres synthesized by reactable ionic liquids[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2013, 420: 89-95. |
| [11] | Li H, Zhang L Z. Oxygen vacancy induced selective silver deposition on the {001} facets of BiOCl single-crystalline nanosheets for enhanced Cr(VI) and sodium pentachlorophenate removal under visible light[J]. Nanoscale, 2014, 6(14): 7805-7810. |
| [12] | Weng S X, Chen B B, Xie L Y, et al. Facile in situ synthesis of a Bi/BiOCl nanocomposite with high photocatalytic activity[J]. Journal of Materials Chemistry A, 2013, 1(9): 3068-3075. |
| [13] | Gao F D, Zeng D W, Huang Q W, et al. Chemically bonded graphene/BiOCl nanocomposites as high-performance photocatalysts[J]. Physical Chemistry Chemical Physics, 2012, 14(30): 10572-10578. |
| [14] | Zhang L, Wang W Z, Sun S M, et al. Water splitting from dye wastewater:a case study of BiOCl/copper (Ⅱ) phthalocyanine composite photocatalyst[J]. Applied Catalysis B:Environmental, 2013, 132-133: 315-320. DOI:10.1016/j.apcatb.2012.12.003 |
| [15] | Pare B, Sarwan B, Jonnalagadda S B. Photocatalytic mineralization study of malachite green on the surface of Mn-doped BiOCl activated by visible light under ambient condition[J]. Applied Surface Science, 2011, 258(1): 247-253. |
| [16] | Ye L Q, Deng K J, Xu F, et al. Increasing visible-light absorption for photocatalysis with black BiOCl[J]. Physical Chemistry Chemical Physics, 2012, 14(1): 82-85. |
| [17] | Liu Y Y, Son W J, Lu J B, et al. Composition dependence of the photocatalytic activities of BiOCl1-xBrx solid solutions under visible light[J]. Chemistry-A European Journal, 2011, 17(34): 9342-9349. DOI:10.1002/chem.v17.34 |
| [18] | Ren K X, Liu J, Liang J, et al. Synthesis of the bismuth oxyhalide solid solutions with tunable band gap and photocatalytic activities[J]. Dalton Transactions, 2013, 42(26): 9706-9712. DOI:10.1039/c3dt50498k |
| [19] | Xiao X Y, Jiang J, Zhang L Z. Selective oxidation of benzyl alcohol into benzaldehyde over semiconductors under visible light:The case of Bi12O17Cl2 nanobelts[J]. Applied Catalysis B:Environmental, 2013, 142-143: 487-493. |
| [20] | Zhai Y F, Zhang A, Teng F, et al. Effect of mixed anion layer on energy band, charge separation and photochemical properties of (BiO)2OHCl[J]. Applied Catalysis B:Environmental, 2018, 224: 116-124. |
| [21] | Launay J P. Reduction de l'ion metatungstate:Stades eleves de reduction de H2W12O406-, derives de l'ion HW12O407- et discussion generale[J]. Journal of Inorganic and Nuclear Chemistry, 1976, 38(4): 807-816. |
| [22] | Liu J H, Xie S Y, Geng Z B, et al. Carbon nitride supramolecular hybrid material enabled high-efficiency photocatalytic water treatments[J]. Nano Letters, 2016, 16(10): 6568-6575. |
| [23] | Heng H M, Gan Q, Meng P C, et al. The visible-light-driven type Ⅲ heterojunction H3PW12O40/TiO2-In2S3:a photocatalysis composite with enhanced photocatalytic activity[J]. Journal of Alloys and Compounds, 2017, 696: 51-59. DOI:10.1016/j.jallcom.2016.11.116 |
| [24] | Wang Q Z, Niu T J, Jiao D H, et al. Preparation of visible-light-driven BiOBr composites with heteropolyacids (H3PW12O40) encapsulated by a zeolite for the photo-degradation of methyl orange[J]. New Journal of Chemistry, 2017, 41(11): 4322-4328. |
| [25] | Wang Q Z, Jiao D H, Bai Y, et al. Immobilized heteropolyacids with zeolite (MCM-41) to enhance photocatalytic performance of BiOBr[J]. Materials Letters, 2015, 161: 267-270. DOI:10.1016/j.matlet.2015.08.111 |
| [26] | Guan M L, Xiao C, Zhang J, et al. Vacancy associates promoting solar-driven photocatalytic activity of ultrathin bismuth oxychloride nanosheets[J]. Journal of the American Chemical Society, 2013, 135(28): 10411-10417. |
| [27] | Hu L X, Chen F Y, Hu P F, et al. Hydrothermal synthesis of SnO2/ZnS nanocomposite as a photocatalyst for degradation of Rhodamine B under simulated and natural sunlight[J]. Journal of Molecular Catalysis A:Chemical, 2016, 411: 203-213. |
| [28] | Aghdam S M, Haghighi M, Allahyari S, et al. Precipitation dispersion of various ratios of BiOI/BiOCl nanocomposite over g-C3N4 for promoted visible light nanophotocatalyst used in removal of acid orange 7 from water[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2017, 338: 201-212. |
| [29] | Yan Y, Sun S F, Song Y, et al. Microwave-assisted in situ synthesis of reduced graphene oxide-BiVO4 composite photocatalysts and their enhanced photocatalytic performance for the degradation of ciprofloxacin[J]. Journal of Hazardous Materials, 2013, 250-251: 106-114. DOI:10.1016/j.jhazmat.2013.01.051 |
| [30] | Duo F F, Wang Y W, Fan C M, et al. Low temperature one-step synthesis of rutile TiO2/BiOCl composites with enhanced photocatalytic activity[J]. Materials Characterization, 2015, 99: 8-16. DOI:10.1016/j.matchar.2014.11.002 |
| [31] | Wang X J, Wang Q, Li F T, et al. Novel BiOCl-C3N4 heterojunction photocatalysts:in situ preparation via an ionic-liquid-assisted solvent-thermal route and their visible-light photocatalytic activities[J]. Chemical Engineering Journal, 2013, 234: 361-371. DOI:10.1016/j.cej.2013.08.112 |
| [32] | Rengifo-Herrera J A, Blanco M, Wist J, et al. TiO2 modified with polyoxotungstates should induce visible-light absorption and high photocatalytic activity through the formation of surface complexes[J]. Applied Catalysis B:Environmental, 2016, 189: 99-109. DOI:10.1016/j.apcatb.2016.02.033 |
| [33] | Zhang G Q, Li X Y, Zheng S Z, et al. Construction of TiO2 nanobelts-Bi2O4 heterojunction with enhanced visible light photocatalytic activity[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2018, 548: 150-157. |
| [34] | Wang Y J, Shi R, Lin J, et al. Enhancement of photocurrent and photocatalytic activity of ZnO hybridized with graphite-like C3N4[J]. Energy & Environmental Science, 2011, 4(8): 2922-2929. |
 2019, Vol. 40
2019, Vol. 40


