2. 西安建筑科技大学环境与市政工程学院, 西安 710055
2. School of Environmental and Municipal Engineering, Xi'an University of Architecture and Technology, Xi'an 710055, China
铬(Cr)是一种广泛用于工业生产且自然界中普遍存在的金属元素.由于冶金、电镀、制革以及印染等行业的迅猛发展, 随之产生具有高毒性、致畸致癌性的含铬废水所造成的环境污染日趋严峻[1, 2].含铬废水的处理方法主要包括离子交换法、化学沉淀法、电解还原法、膜分离法、吸附及光催化还原法等[3].吸附及光催化还原法因效率高、成本低、不易产生二次污染而受到广泛关注[4, 5].铬主要以Cr(Ⅵ)和Cr(Ⅲ)的形式存在于水体环境中[6], 其中Cr(Ⅵ)比Cr(Ⅲ)具有更高的毒性(约100倍)[7], 因此将Cr(Ⅵ)还原为毒性较低的Cr(Ⅲ)再去除被认为是一种有效的含铬废水处理方法.
二氧化钛(TiO2)作为一种吸附催化材料, 因其高效、无毒、化学稳定性好等优点而被广泛应用于环境污染的治理中[8~10].在紫外光(UV)下, TiO2表面可产生具有强烈氧化还原作用的电子-空穴对, 光生电子可将重金属离子, 如Cr、Hg等还原为无毒或低毒性状态; 光生空穴可将常见的有机污染物, 如苯酚、甲醛和染料等矿化成CO2和H2O[11]. Liu等[12]采用直接包裹法和水热蚀刻法制备了石墨烯包裹的TiO2空心核壳结构(TGHMS)光催化剂, TGHMS因可由相互独立暴露的{001}和{101}晶面组成的TiO2芯层形成一种Z型光催化体系, 而兼具较高的电荷分离效率和较强的氧化还原能力, 且在光催化协同去除罗丹明B和Cr(Ⅵ)中表现优异. Lara等[13]通过表面氟化法制备了暴露晶面为{001}的TiO2并用于光催化性能研究, 结果表明, 相较于市售TiO2(P25), {001}晶面的暴露及其表面附着的氟对于光催化氧化苯酚和甲基橙、光催化还原Cr(Ⅵ)所表现出的优越性能起着关键作用.综上所述, TiO2表面对Cr的吸附及光催化还原为水体中Cr的去除提供了有利途径.近期研究结果表明, TiO2表面结构对其吸附及催化性能有显著影响.高指数晶面TiO2{201}因其表面富有高密度的原子台阶、悬空键及未饱和配位的Ti原子, 具有潜在的高吸附能力及催化活性.
本研究以高指数晶面TiO2{201}为吸附催化材料, 通过吸附等温线分析其对Cr(Ⅲ/Ⅵ)的吸附, 并通过光生电子-空穴淬灭实验考察其光催化还原Cr(Ⅵ)的机制, 以期为铬的去除提供理论基础.
1 材料与方法 1.1 实验仪器电感耦合等离子体发射光谱仪(ICP-OES, Optima 2000 DV, Perkin Elmer Co, USA); 紫外可见分光光度计(岛津UV-2550);电子天平(ME104);场发射扫描电子显微镜(FE-SEM, SU-8000, Hitachi); 高分辨透射电镜(HR-TEM, JEM-2100F, JEOL); X'Pert PRO MPDX射线衍射仪(PAN alytical, Netherlands); X射线光电子能谱仪(XPS, Thermo Fisher ESCALAB 250Xi); pH计(FE20);超声机(KH500B); 磁力搅拌器(WIGGENS WH220);真空干燥箱(DZF-6020);汞灯光源系统(中教金源CEL-M500);离心机(Thermo ScientificTM HeraeusTM MultifugeTM X1R).
1.2 实验材料及试剂本实验所用六水合三氯化铬(CrCl3·6H2O, 分析纯)购自天津市津科精细化工研究所; 重铬酸钾(K2Cr2O7, 分析纯)购自天津市化学试剂一厂; 二苯基碳酰二肼(C13H14N4O, 分析纯)购自北京化学试剂公司; N, N-二甲基甲酰胺购自Alfa Aesar(China) Chemicals Co., Ltd.; 钛酸四丁酯及EDTA-2Na (C10H14N2Na2O8·2H2O)购自Sigma-Aldrich; 冰醋酸(C2H4O2, 优级纯)、无水乙醇(C2H6O, 优级纯)、丙酮(C3H6O, 分析纯)、硫酸(H2SO4, 优级纯)、磷酸(H3PO4, 优级纯)、盐酸(HCl, 优级纯)、氢氧化钠(NaOH, 分析纯)及溴酸钾(KBrO3, 分析纯)均购自国药集团化学试剂有限公司.
1.3 溶液配制1 g·L-1 Cr(Ⅵ)溶液:称取于110℃干燥2 h的重铬酸钾(K2Cr2O7) 2.829 g, 用超纯水溶解后, 移入1000 mL容量瓶中, 再用超纯水稀释至标线, 摇匀, 可得浓度为1 g·L-1的Cr(Ⅵ)储备液.
1 g·L-1 Cr(Ⅲ)溶液:称取六水合三氯化铬(CrCl3·6H2O) 5.124 g, 用超纯水溶解后, 移入1000 mL容量瓶中, 再用超纯水稀释至标线, 摇匀, 可得浓度为1 g·L-1的Cr(Ⅲ)储备液.
2 g·L-1二苯基碳酰二肼显色剂溶液:称取0.2 g二苯基碳酰二肼(C13H14N4O), 溶于50 mL丙酮中, 加超纯水定容至100 mL, 摇匀并贮于棕色瓶中, 所得浓度为2 g·L-1的二苯基碳酰二肼溶液于4℃保存.
1+1硫酸:将优级纯浓硫酸缓慢加入到同体积的超纯水中.
1+1磷酸:将优级纯磷酸缓慢加入到同体积的超纯水中.
实验所用超纯水(18.2 MΩ·cm)均由Millipore Milli-Q系统提供.
1.4 实验方法 1.4.1 高指数晶面TiO2{201}的制备采用溶剂热法制备高指数晶面TiO2{201}, 首先开启磁力搅拌, 将8 mL冰醋酸、12 mL N, N-二甲基甲酰胺及0.5 mL钛酸四丁酯依次加入至反应釜中, 混合搅拌5 min, 随后将反应釜置于200℃真空干燥箱中反应10 h.反应结束后, 所得产物经离心和5次无水乙醇清洗后, 再在60℃条件下烘干, 即可获得高指数晶面TiO2{201}.
1.4.2 高指数晶面TiO2{201}的表征采用加速电压为5 kV的场发射扫描电镜(FE-SEM, SU-8000, Hitachi)、加速电压为200 kV的高分辨透射电镜(HR-TEM, JEM-2100F, JEOL)对所制备的高指数晶面TiO2{201}进行形貌表征.采用辐射源为Cu Kα射线、扫描角度2θ为5°~90°、间隔为0.01°、步长为1 s的X'Pert PRO MPDX射线衍射仪(PAN alytical, Netherlands)对所制备的高指数晶面TiO2{201}进行晶体结构表征.
1.4.3 吸附等温线室温条件下, 取浓度为1 g·L-1的Cr(Ⅲ)和Cr(Ⅵ)储备液逐级稀释, 将30 mL浓度为2.5、5、10、15、20、25、35、50、65、80、100、125、150、175、200 mg·L-1的Cr(Ⅲ)和Cr(Ⅵ)溶液分别置于规格为50 mL的聚乙烯离心管中, 并确保每个体系中NaCl背景液浓度为0.04 mol·L-1, 用HCl和NaOH调节溶液pH=5[14], 随后往每个反应体系中投加15 mg TiO2{201}吸附剂, 即体系中TiO2{201}浓度为0.5 g·L-1.将反应体系置于旋转培养器上避光旋转摇匀, 吸附平衡后, 取混合溶液经0.22 μm水系滤膜过滤, 并采用电感耦合等离子体发射光谱仪(ICP-OES, Optima 200F0 DV, Perkin Elmer Co, USA)测定Cr浓度.
1.4.4 光催化还原Cr(Ⅵ)室温条件下, 取浓度为1 g·L-1的Cr(Ⅵ)储备液逐级稀释, 得到浓度为10 mg·L-1的Cr(Ⅵ)溶液.取80 mL浓度为10 mg·L-1的Cr(Ⅵ)溶液于100 mL烧杯中, 用HCl和NaOH调节pH=5, 随后在黑暗条件下加入质量为40 mg的TiO2{201}, 即反应体系中TiO2{201}浓度为0.5 g·L-1, 磁力搅拌30 min以达到吸附-脱附平衡, 再置于波长为254 nm、强度为2000 μW·cm-2的紫外光下照射.按照光照时间0、5、10、15、20、25、30、40 min进行取样, 所取样品经0.22 μm水系滤膜过滤.采用相同的实验方法分别考察浓度为20 mmol·L-1的光生电子淬灭剂(KBrO3)和光生空穴淬灭剂(EDTA-2Na)对TiO2{201}光催化还原Cr(Ⅵ)的影响.
取4 mL滤液于离心管中, 并依次加入1+1硫酸、1+1磷酸各0.04 mL以及0.16 mL二苯基碳酰二肼显色剂溶液, 摇匀, 待10 min后所显紫色稳定, 采用紫外可见分光光度计(岛津UV-2550)于540 nm处测定Cr(Ⅵ)浓度[15].
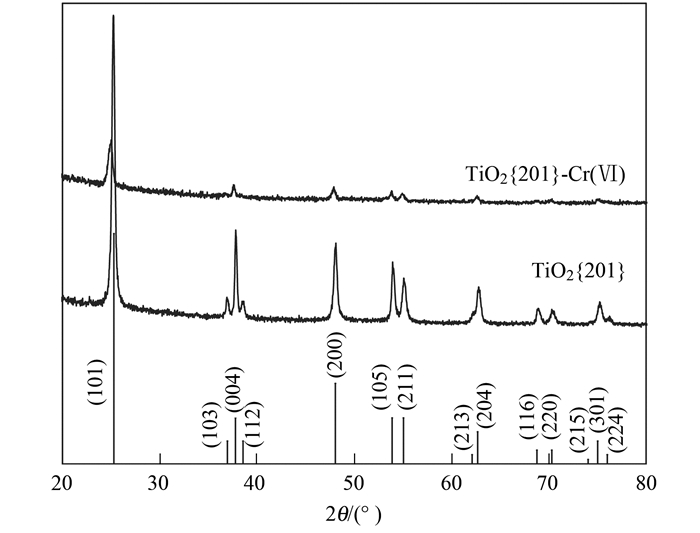
2 结果与讨论 2.1 高指数晶面TiO2{201}的表征高指数晶面TiO2{201}的SEM形貌表征结果如图 1(a)所示, 所制备的TiO2{201}由直径约1 μm的类蒲公英状的层级球形结构组成; TEM及HR-TEM表征结果分别如图 1(b)和1(c)所示, 所制备的TiO2{201}其晶格间距为0.24 nm, 与文献报道一致[16]. TiO2{201}的X射线衍射(XRD)图谱如图 2所示, 所有识别的特征衍射峰均与MDI Jade 6.5软件中的锐钛矿相TiO2标准图谱(JCPDS No. 21-1272)相匹配, 表明所制备的高指数晶面TiO2{201}为锐钛矿相[17].

|
图 1 TiO2{201}的SEM、TEM及HR-TEM表征结果 Fig. 1 SEM, TEM, and HR-TEM characterization of TiO2{201} |
|
图 2 TiO2{201}及TiO2{201}光催化还原Cr(Ⅵ)后所收集固体[TiO2{201}-Cr(Ⅵ)]的XRD表征结果 Fig. 2 XRD patterns of TiO2{201} and the solid[TiO2{201}-Cr(Ⅵ)] collected after photocatalytic reduction of Cr(Ⅵ) by TiO2{201} |
吸附等温线可以用来表征吸附材料的表面性质和吸附亲和性, 被认为是研究吸附理论的最佳途径[18].本项研究采用Langmuir及Freundlich吸附模型对等温吸附结果进行拟合, 如公式(1)~(3)所示:
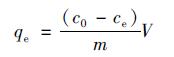
|
(1) |
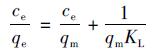
|
(2) |
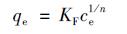
|
(3) |
式中, qe和qm分别为平衡吸附量(mg·g-1)和最大吸附量(mg·g-1), c0和ce分别为吸附质的初始浓度(mg·L-1)和平衡浓度(mg·L-1), m和V分别为吸附剂的质量(mg)与溶液体积(L), KL为与吸附自由能相关的Langmuir吸附平衡常数(L·mg-1); KF与1/n为Freundlich公式中的常数, 当1/n在0.1~0.5范围内时易于吸附, 且1/n越小, 吸附性能越好.
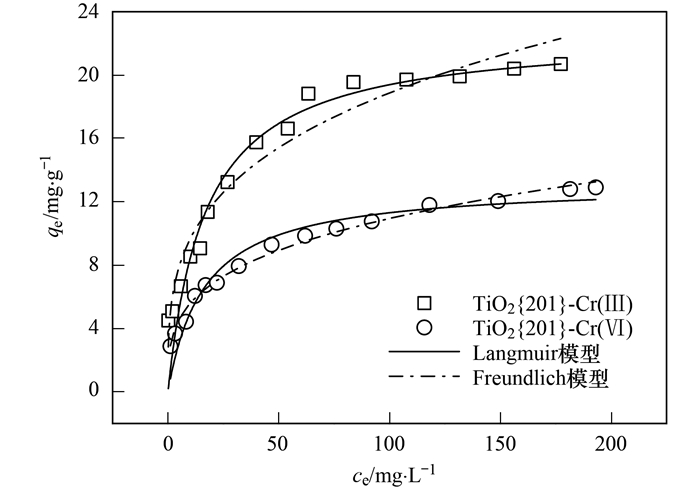
TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的吸附结果、Langmuir及Freundlich拟合结果如图 3和表 1所示, Langmuir吸附模型拟合可得TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的最大吸附量分别为22.7 mg·g-1和13.2 mg·g-1, 且TiO2{201}对Cr(Ⅲ)的吸附效果较好; Freundlich拟合结果表明TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的吸附均易于进行(1/n均小于0.5).
|
图 3 TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的吸附等温线、Langmuir及Freundlich模型拟合 Fig. 3 Langmuir and Freundlich fitting results for adsorption isotherms of Cr(Ⅲ) and Cr(Ⅵ) on TiO2{201} (symbol) |
|
|
表 1 Langmuir和Freundlich模型拟合TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的等温吸附结果 Table 1 Langmuir and Freundlich fitting results for adsorption isotherms of Cr(Ⅲ) and Cr(Ⅵ) on TiO2{201} |
2.3 光催化还原Cr(Ⅵ)
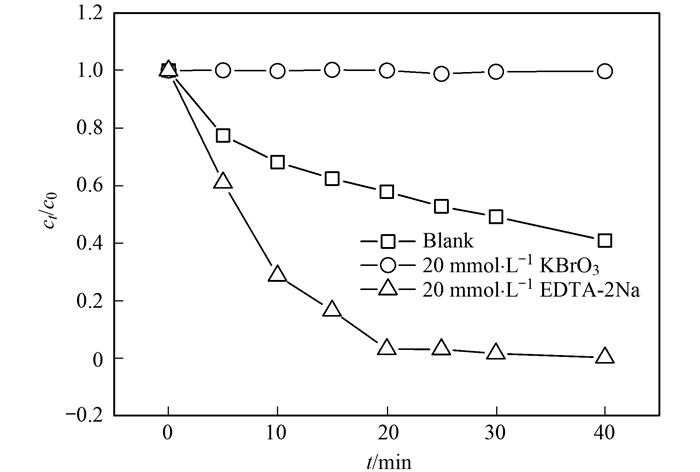
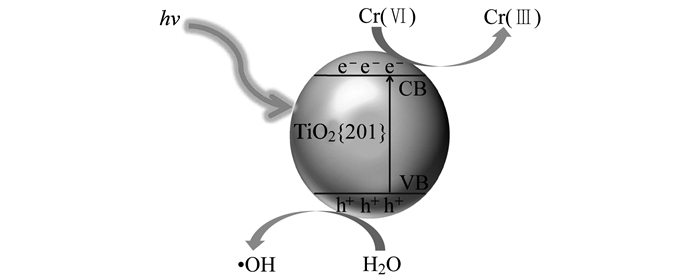
TiO2{201}对Cr(Ⅵ)的光催化还原结果如图 4所示, 其中c0为Cr(Ⅵ)的初始浓度(mg·L-1), ct为光照时间t所测得的Cr(Ⅵ)浓度(mg·L-1).从中可知, 光照40 min时, TiO2{201}对Cr(Ⅵ)的还原率仅为60%;在加入光生空穴淬灭剂EDTA-2Na后, 仅需光照20 min, Cr(Ⅵ)的还原率便可达100%;在加入光生电子淬灭剂KBrO3之后, Cr(Ⅵ)还原率为0.以上结果表明光生电子是TiO2{201}光催化还原Cr(Ⅵ)的主要反应活性物质, 而KBrO3作为一种电子淬灭剂, 将其引入可抑制Cr(Ⅵ)的还原; EDTA-2Na作为一种空穴淬灭剂, 将其引入可促进光生电子和空穴的分离, 从而提高光生电子的利用率, 即提高Cr(Ⅵ)的还原率[19, 20].在投加电子淬灭剂KBrO3的体系中, 光生电子与电子淬灭剂、光生电子与Cr(Ⅵ)之间的反应同时存在, 而在投加空穴淬灭剂EDTA-2Na的体系中, 因空穴被淬灭而产生的大量光生电子则全部作用于Cr(Ⅵ)的还原, 因此空穴淬灭剂对Cr(Ⅵ)还原率的影响比电子淬灭剂更大. TiO2{201}光催化还原Cr(Ⅵ)的机制可表述为图 5及公式(4)~(6):在紫外光照下, TiO2{201}表面产生光生电子(e-)-光生空穴(h+)对, 光生电子将Cr(Ⅵ)还原为Cr(Ⅲ), 光生空穴则将H2O氧化为羟基自由基(·OH)[21, 22].
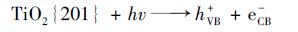
|
(4) |
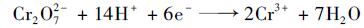
|
(5) |

|
(6) |
|
图 4 不同淬灭剂对TiO2{201}光催化还原Cr(Ⅵ)的影响 Fig. 4 Effect of different scavengers on photocatalytic reduction of Cr(Ⅵ) by TiO2{201} |
|
图 5 TiO2{201}光催化还原Cr(Ⅵ)机制 Fig. 5 Mechanism of photocatalytic reduction of Cr(Ⅵ) by TiO2{201} |
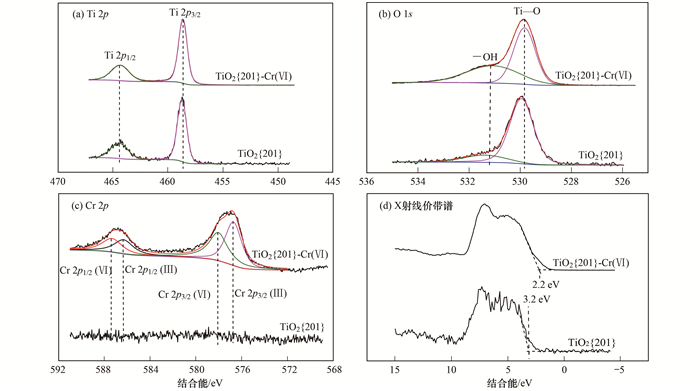
为进一步考察TiO2{201}光催化还原Cr(Ⅵ)的机制, 采用XRD及XPS对TiO2{201}及TiO2{201}光催化还原Cr(Ⅵ)反应结束后所收集的固体TiO2{201}-Cr(Ⅵ)进行表征. XRD表征结果如图 2所示, 表明光催化还原反应结束后, TiO2{201}仍为锐钛矿相, 其晶型未发生变化. XPS表征结果如图 6所示, XPS可检测TiO2{201}与TiO2{201}-Cr(Ⅵ)的表面组成及化学状态.通过XPS获得的结合能, 须以外来污染碳源的结合能(284.6 eV)为基准进行校正. TiO2{201}与TiO2{201}-Cr(Ⅵ)表面Ti 2p的高分辨能谱图如图 6(a)所示, 结果显示在464.4 eV和458.7 eV处出现两个峰, 分别对应氧化态Ti4+的Ti 2p3/2与Ti 2p1/2自旋轨道分裂光电子[23, 24], Ti 2p3/2与Ti 2p1/2两个谱峰的能量差(5.7 eV)反映了锐钛矿相TiO2的Ti4+化学态.
|
图 6 TiO2{201}及TiO2{201}光催化还原Cr(Ⅵ)后所收集固体(TiO2{201}-Cr(Ⅵ))的XPS表征结果 Fig. 6 XPS patterns of TiO2{201} and the solid(TiO2{201}-Cr(Ⅵ)) collected after photocatalytic reduction of Cr(Ⅵ) by TiO2{201} |
O 1s的高分辨能谱图如图 6(b)所示, 结果显示, TiO2{201}在529.9 eV和531.4 eV处出现两个峰, TiO2{201}-Cr(Ⅵ)在529.8 eV和531.1 eV处出现两个峰, 分别对应Ti—O和—OH[25].通过计算Ti—O峰和—OH峰的百分占比, 进一步分析二者含量的变化情况, 计算数据如表 2所示.
|
|
表 2 TiO2{201}和TiO2{201}-Cr(Ⅵ)中的Ti—O与—OH占比情况 Table 2 Contribution of Ti—O and —OH to the O 1s XPS spectra for TiO2{201} and TiO2{201}-Cr(Ⅵ) |
由表 2可知, TiO2{201}光催化还原Cr(Ⅵ)反应结束后所收集的固体, —OH含量约为未经光照的TiO2{201}的2.6倍, 说明TiO2{201}光催化还原Cr(Ⅵ)的过程中伴随着—OH的生成.结合图 6(c), 可知Cr(Ⅵ)被TiO2{201}光催化还原成Cr(Ⅲ), 继而Cr(Ⅲ)以Cr(OH)3沉淀覆盖在TiO2{201}表面, 因此光催化还原结束后表面—OH含量升高.根据XPS中Cr 2p3/2和Cr 2p1/2的谱图对应元素[26], 可判断覆盖在TiO2{201}表面的Cr(Ⅲ)为Cr2O3和Cr(OH)3的混合物, Cr(Ⅵ)主要为CrO3, 其相对应的Cr 2p类型及其结合能如表 3所示.
|
|
表 3 利用Cr 2p的XPS谱对TiO2{201}-Cr(Ⅵ)进行成分分析 Table 3 Components of TiO2{201}-Cr(Ⅵ) analyzed by Cr 2p XPS spectra |
此外, 从TiO2{201}与TiO2{201}-Cr(Ⅵ)的X射线价带谱[图 6(d)]可看出, 由于Cr的引入并在TiO2{201}表面发生了还原反应, TiO2{201}-Cr(Ⅵ)的价带顶相较于TiO2{201}明显下降了1 eV, 说明Cr覆盖在TiO2表面之后, 费米能级更接近价带[27], 形成p型半导体材料, 有望拓展其光催化性能.
3 结论(1) Freundlich模型拟合结果表明TiO2{201}对Cr(Ⅲ)和Cr(Ⅵ)的吸附均易于进行, 其1/n均小于0.5;但Langmuir模型拟合结果表明TiO2{201}对Cr(Ⅲ)的吸附量(22.7 mg·g-1)高于对Cr(Ⅵ)的吸附量(13.2 mg·g-1), 对Cr(Ⅵ)的吸附去除效果较差.
(2) 经比较光生空穴和电子淬灭剂对TiO2{201}光催化还原Cr(Ⅵ)的影响, 发现紫外光照射40 min时, TiO2{201}对Cr(Ⅵ)的还原率为60%, 在加入光生空穴淬灭剂EDTA-2Na之后, 还原率可达100%, 而在加入光生电子淬灭剂KBrO3之后, 还原率为0, 表明光生电子对TiO2{201}光催化还原Cr(Ⅵ)起决定性作用.
(3) 对TiO2{201}光催化还原Cr(Ⅵ)反应结束后所收集的固体TiO2{201}-Cr(Ⅵ)进行XPS及XRD表征. XPS表征结果显示Cr(Ⅵ)在TiO2表面被还原为Cr(Ⅲ)后, 以Cr2O3和Cr(OH)3的形式沉积在TiO2{201}表面; XRD结果表明TiO2{201}仍为锐钛矿相, 其晶型未发生变化, 表明TiO2{201}性质稳定.
| [1] | Chen L, Chen Z H, Chen D, et al. Removal of hexavalent chromium from contaminated waters by ultrasound-assisted aqueous solution ball milling[J]. Journal of Environmental Sciences, 2017, 52: 276-283. DOI:10.1016/j.jes.2016.04.006 |
| [2] | Velegraki G, Miao J W, Drivas C, et al. Fabrication of 3D mesoporous networks of assembled CoO nanoparticles for efficient photocatalytic reduction of aqueous Cr(Ⅵ)[J]. Applied Catalysis B:Environmental, 2018, 221: 635-644. DOI:10.1016/j.apcatb.2017.09.064 |
| [3] | Du Y C, Zhang S H, Wang J S, et al. Nb2O5 nanowires in-situ grown on carbon fiber:a high-efficiency material for the photocatalytic reduction of Cr(Ⅵ)[J]. Journal of Environmental Sciences, 2018, 66: 358-367. DOI:10.1016/j.jes.2017.04.019 |
| [4] | Zhao D L, Gao X, Wu C N, et al. Facile preparation of amino functionalized graphene oxide decorated with Fe3O4 nanoparticles for the adsorption of Cr(Ⅵ)[J]. Applied Surface Science, 2016, 384: 1-9. DOI:10.1016/j.apsusc.2016.05.022 |
| [5] | Li Y, Cui W Q, Liu L, et al. Removal of Cr(Ⅵ) by 3D TiO2-graphene hydrogel via adsorption enriched with photocatalytic reduction[J]. Applied Catalysis B:Environmental, 2016, 199: 412-423. DOI:10.1016/j.apcatb.2016.06.053 |
| [6] | Kumar A, Jena H M. Adsorption of Cr(Ⅵ) from aqueous solution by prepared high surface area activated carbon from Fox nutshell by chemical activation with H3PO4[J]. Journal of Environmental Chemical Engineering, 2017, 5(2): 2032-2041. DOI:10.1016/j.jece.2017.03.035 |
| [7] |
陈心满, 徐明芳. UV/TiO2光催化还原Cr(Ⅵ)过程中吸附作用的影响及其消除[J]. 环境科学, 2006, 27(5): 913-917. Chen X M, Xu M F. Effects of absorption on photo-reduction of Cr(Ⅵ) by UV/TiO2 process and its elimination[J]. Environmental Science, 2006, 27(5): 913-917. DOI:10.3321/j.issn:0250-3301.2006.05.017 |
| [8] | Wei M, Wan J M, Hu Z W, et al. Enhanced photocatalytic degradation activity over TiO2 nanotubes co-sensitized by reduced graphene oxide and copper(Ⅱ) meso-tetra(4-carboxyphenyl)porphyrin[J]. Applied Surface Science, 2016, 377: 149-158. DOI:10.1016/j.apsusc.2016.03.120 |
| [9] | Li Y N, Chen Z Y, Bao S J, et al. Ultrafine TiO2 encapsulated in nitrogen-doped porous carbon framework for photocatalytic degradation of ammonia gas[J]. Chemical Engineering Journal, 2018, 331: 383-388. DOI:10.1016/j.cej.2017.08.119 |
| [10] | Momeni M M, Nazari Z. Preparation of TiO2 and WO3-TiO2 nanotubes decorated with PbO nanoparticles by chemical bath deposition process:a stable and efficient photo catalyst[J]. Ceramics International, 2016, 42(7): 8691-8697. DOI:10.1016/j.ceramint.2016.02.103 |
| [11] | Sun Q, Hu X L, Zheng S L, et al. Influence of calcination temperature on the structural, adsorption and photocatalytic properties of TiO2 nanoparticles supported on natural zeolite[J]. Powder Technology, 2015, 274: 88-97. DOI:10.1016/j.powtec.2014.12.052 |
| [12] | Liu H, Liu S, Zhang Z L, et al. Hydrothermal etching fabrication of TiO2@graphene hollow structures:mutually independent exposed {001} and {101} facets nanocrystals and its synergistic photocaltalytic effects[J]. Scientific Reports, 2016, 6: 33839. DOI:10.1038/srep33839 |
| [13] | Lara M A, Sayagués M J, Navío J A, et al. A facile shape-controlled synthesis of highly photoactive fluorine containing TiO2 nanosheets with high {001} facet exposure[J]. Journal of Materials Science, 2018, 53(1): 435-446. |
| [14] | Lu D Z, Chai W Q, Yang M C, et al. Visible light induced photocatalytic removal of Cr(Ⅵ) over TiO2-based nanosheets loaded with surface-enriched CoOx nanoparticles and its synergism with phenol oxidation[J]. Applied Catalysis B:Environmental, 2016, 190: 44-65. DOI:10.1016/j.apcatb.2016.03.003 |
| [15] | Han J C, Chen G J, Qin L P, et al. Metal respiratory pathway-independent cr isotope fractionation during Cr(Ⅵ) reduction by Shewanella oneidensis MR-1[J]. Environmental Science & Technology Letters, 2017, 4(11): 500-504. |
| [16] | Song J Y, Yan L, Duan J M, et al. TiO2 crystal facet-dependent antimony adsorption and photocatalytic oxidation[J]. Journal of Colloid and Interface Science, 2017, 496: 522-530. DOI:10.1016/j.jcis.2017.02.054 |
| [17] | Chen M, Ma J Z, Zhang B, et al. Facet-dependent performance of anatase TiO2 for photocatalytic oxidation of gaseous ammonia[J]. Applied Catalysis B:Environmental, 2018, 223: 209-215. DOI:10.1016/j.apcatb.2017.04.012 |
| [18] | Kebir M, Trari M, Maachi R, et al. Relevance of a hybrid process coupling adsorption and visible light photocatalysis involving a new hetero-system CuCo2O4/TiO2 for the removal of hexavalent chromium[J]. Journal of Environmental Chemical Engineering, 2015, 3(1): 548-559. DOI:10.1016/j.jece.2014.12.024 |
| [19] | Xue C, Zhang T X, Ding S J, et al. Anchoring tailored low-index faceted BiOBr nanoplates onto TiO2 nanorods to enhance the stability and visible-light-driven catalytic activity[J]. ACS Applied Materials & Interfaces, 2017, 9(19): 16091-16102. |
| [20] | Wu Z B, Yuan X Z, Zeng G M, et al. Highly efficient photocatalytic activity and mechanism of Yb3+/Tm3+ codoped In2S3 from ultraviolet to near infrared light towards chromium (Ⅵ) reduction and rhodamine B oxydative degradation[J]. Applied Catalysis B:Environmental, 2018, 225: 8-21. DOI:10.1016/j.apcatb.2017.11.040 |
| [21] | Wang L, Zhang C B, Gao F, et al. Algae decorated TiO2/Ag hybrid nanofiber membrane with enhanced photocatalytic activity for Cr(Ⅵ) removal under visible light[J]. Chemical Engineering Journal, 2017, 314: 622-630. DOI:10.1016/j.cej.2016.12.020 |
| [22] | Mohamed A, Osman T A, Toprak M S, et al. Visible light photocatalytic reduction of Cr(Ⅵ) by surface modified CNT/titanium dioxide composites nanofibers[J]. Journal of Molecular Catalysis A:Chemical, 2016, 424: 45-53. DOI:10.1016/j.molcata.2016.08.010 |
| [23] | Yan L, Du J J, Jing C Y. How TiO2 facets determine arsenic adsorption and photooxidation:spectroscopic and DFT studies[J]. Catalysis Science & Technology, 2016, 6(7): 2419-2426. |
| [24] | Yan L, Tu H W, Chan T S, et al. Mechanistic study of simultaneous arsenic and fluoride removal using granular TiO2-La adsorbent[J]. Chemical Engineering Journal, 2017, 313: 983-992. DOI:10.1016/j.cej.2016.10.142 |
| [25] | Shi L, Xu C L, Sun X, et al. Facile fabrication of hierarchical BiVO4/TiO2 heterostructures for enhanced photocatalytic activities under visible-light irradiation[J]. Journal of Materials Science, 2018, 53(16): 11329-11342. DOI:10.1007/s10853-018-2442-x |
| [26] | Chidambaram D, Halada G P, Clayton C R. Development of a technique to prevent radiation damage of chromate conversion coatings during X-ray photoelectron spectroscopic analysis[J]. Applied Surface Science, 2001, 181(3-4): 283-295. DOI:10.1016/S0169-4332(01)00433-0 |
| [27] | Cao J Y, Zhang Y J, Liu L Q, et al. A p-type Cr-doped TiO2 photo-electrode for photo-reduction[J]. Chemical Communications, 2013, 49(33): 3440-3442. DOI:10.1039/c3cc40394g |
 2019, Vol. 40
2019, Vol. 40


