2. 清华大学水质与水生态研究中心, 北京 100084;
3. 中国科学院生态环境研究中心, 北京 100085
2. Center for Water and Ecology, Tsinghua University, Beijing 100084, China;
3. Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
随着经济社会的发展, 水污染问题日益严重, 尤为突出的就是水体污染物的种类变得越发繁杂, 染料、抗生素等有机废水已经很难通过简单的生物反应达到良好的降解效果[1].以高效非均相光催化为代表的高级氧化技术, 在降解上述污水方面, 有着显著的效果, 是解决能源问题与环境修复的有效手段之一[2].
1972年, Fujishima等[3]发现受光辐射的TiO2微粒可以使水持续地发生氧化还原反应产生氢气.自此, TiO2作为光催化剂, 因高效廉价, 无毒稳定而被广泛研究[4].但是二氧化钛光生电子和空穴易复合, 导致其量子效率较低[5, 6].通过对二氧化钛的改性, 可以减缓其电子和空穴的复合的速率, 提高光量子效率.如金属离子掺杂[7, 8]、Pt、Pd、Ag、Au等贵金属沉积[9~12]和复合半导体[13, 14]等方法均被广泛研究.钙钛矿型氧化物在紫外光的照射下具有较强的光催化活性和良好的稳定性, 钙钛矿型复合光催化剂如TiO2/SrTiO3[15]、TiO2/LaFeO3[16]等, 均表现出高于TiO2的光催化活性.近些年来, 廉价易得、活性较高的ZnTiO3逐渐引起人们的关注.苏碧桃等[17]利用溶胶凝胶法制作了ZnTiO3/TiO2复合光催化剂; 王爱民等[18]利用均相沉淀制作的氧化锌粉体加入到二氧化钛前驱体中, 制作出类似的异质复合材料, 这些催化剂均对亚甲基蓝有良好的降解效果.虽然研究人员对催化剂制备进行了深入研究, 但是对异质结的生成和分析, 及光催化效果提升的机制未进行深入的研究和探索.
本文利用Sol-Gel法制备了ZnTiO3-TiO2纳米复合光催化剂, 以甲基橙(MO)溶液为模拟污染物, 对该复合材料光催化活性进行测试, 同时研究了前驱体的配比、煅烧温度等条件对光催化性能的影响.通过高分辨透射电镜、光电流测试和自由基分析等方法研究了光催化效率提升的机制.
1 材料与方法 1.1 试剂与仪器主要试剂:钛酸四丁酯Ti(OC4H9)4、冰醋酸和六水合硝酸锌Zn(NO3)2·6H2O等, 以上试剂均为分析纯, 实验用水为去离子水.
主要仪器:紫外可见分光光度计(756PC天津市拓普仪器有限公司)、高压汞灯(RSUV-天津瑞森特紫外线设备有限公司)、马弗炉(SX-GO7103天津市中环实验电炉有限公司)、X射线衍射仪(D8 focus德国Bruker公司)、场发射扫描电子显微镜(SU-8020日本日立公司)、透射电子显微镜(JEM-2100F日本电子珠式会社)、X射线光电子能谱仪(ESCALAB250Xi赛默飞世尔科技(中国)有限公司)、红外光谱仪(TENSON 27 BRUKEY, Germany)、电化学工作站(Reference 600+GAMRY)和电子自旋共振波谱仪(A300-10/12德国布鲁克有限公司).
1.2 催化剂制备将34 mL钛酸丁酯(0.1 mol)溶于35 mL无水乙醇中, 形成溶液A.将5 mL去离子水、15 mL冰醋酸和一定量的Zn(NO3)2·6H2O先后溶于35 mL无水乙醇中, 形成溶液B.在搅拌状态下, 将溶液B缓慢滴加到溶液A中.搅拌30 min后, 溶液呈溶胶状.静置陈化24 h后, 在105℃条件下干燥12 h.所得固体研磨呈粉末状, 在一定温度下煅烧3 h后, 得到不同摩尔比的ZnTiO3-TiO2复合光催化剂.
1.3 光催化活性测试催化剂活性以甲基橙MO的降解速率来作为评价指标.模拟污染物MO的浓度为5mg·L-1, 体积为175 mL, 置于300 mL石英烧杯中, 催化剂用量0.35 g.使用主波长为365 nm的高压汞灯为紫外光源.光催化降解反应前, 避光吸附30 min, 达到吸附脱附平衡.光照一定时间后取2~3 mL反应液, 高速离心分离, 用分光光度计在463 nm处测其上层清液的吸光度.以溶液的降解率来评价光催化剂的活性, 即ct/c0=At/A0, 式中, At和A0分别表示t时间溶液和初始溶液的吸光度.分别利用0.1mol·L-1的HNO3溶液和0.1mol·L-1的NaOH溶液调节pH值.在重复性实验中, 将反应后的溶液离心分离得到催化剂沉淀, 干燥后再次使用.
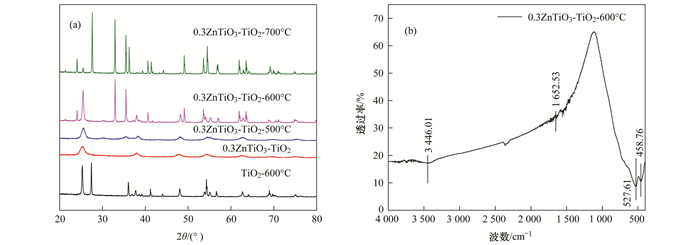
2 结果与讨论 2.1 材料理化性质表征利用X射线衍射(XRD)对不同煅烧温度的复合催化剂进行分析.如图 1(a)所示, 在未煅烧的0.3ZnTiO3-TiO2中, TiO2以锐钛矿晶型(JCPDS No. 9-0008)为主, 在25.303°、37.792°、48.035°、53.884°、62.683°、76.03°和82.67°分别对应锐钛矿的(101)、(004)、(200)、(105)、(204)、(301)和(224)晶面.图谱中未出现明显的锌类化合物的衍射峰, 可能是未煅烧导致的结晶度较差[19], 或者是锌类物质含量少, 且分散到了TiO2表面[20]. 0.3ZnTiO3-TiO2-500℃中, TiO2以锐钛矿(JCPDS No. 9-0008)为主, 同时, 锌元素以ZnTiO3(JCPDS No. 39-0190)的形式存在, 在30.032°、35.379°和62.444°处分别对应着(220)、(311)和(440)晶面. 0.3ZnTiO3-TiO2-600℃中, TiO2以锐钛矿(JCPDS No. 9-0008)为主.锌元素以ZnTiO3(JCPDS No. 26-1500)的形式存在, 在21.182°、23.92°、32.790°、35.307°、40.452°、48.929°、53.445°、61.797°和63.394°处分别对应着(101)、(012)、(104)、(110)、(113)、(024)、(116)、(214)和(300)晶面. 0.3ZnTiO3-TiO2-700℃中, TiO2以金红石(JCPDS No. 77-0441)为主, 在13.693°、18.003°、19.559°、20.578°、27.106°、28.258和34.430°分别对应锐钛矿的(110)、(101)、(200)、(111)、(211)、(220)和(301)晶面.同时, 锌元素以ZnTiO3(JCPDS No. 26-1500)的形式存在.而以上述方法制作的TiO2, 在600℃煅烧后, 存在锐钛矿(JCPDS No. 9-0008)和金红石(JCPDS No. 9-0090)两种晶型, 而通过引入ZnTiO3, 抑制了煅烧时二氧化钛从锐钛矿向金红石的转变, 提高了锐钛矿的热稳定性, 有利于光催化活性的提高[21].
|
(a)不同锌钛比例ZnTiO3-TiO2的XRD图; (b) 0.3ZnTiO3-TiO2的红外谱图 图 1 催化剂材料表征 Fig. 1 Characterization of samples |
通过红外光谱(FT-IR)研究了复合催化剂的化学键和官能团组成.如图 1(b)所示, 400~700 cm-1对应着金属氧化物键. 458.76 cm-1和527.61 cm-1分别对应着ZnTiO3中Zn—O键和Ti—O键[22]. 3446.01 cm-1附近的宽峰为Zn—OH、Ti—OH及吸附水的O—H伸缩振动峰, 1652.53 cm-1附近的峰为催化剂表面结合水的—OH弯曲振动峰[18], 可作为表面羟基多少的近似度量.以上分析说明该催化剂表面存在较丰富的羟基官能团, 而表面羟基的存在有利于捕获光生空穴形成具有氧化活性的羟基自由基, 有利于光催化反应的进行[23].
通过场发射扫描电镜对复合光催化剂进行微观分析.如图 2所示, 分别为未煅烧、500、600和700℃条件下煅烧的复合催化剂的扫描电镜照片.图 2(a)可以看出未煅烧的催化剂颗粒呈不规则形态.图 2(b)中的催化剂在500℃煅烧后, 催化剂由无规则态向球状转变.图 2(c)中的催化剂在600℃煅烧后, 催化剂结晶良好, 呈较完整的球状堆叠.图 2(d)中的催化剂在700℃煅烧后, 球状颗粒堆叠挤压成不规则块状.由此可知, 不同温度的煅烧, 对于催化剂的结晶有较大影响, 进而影响催化剂的光催化活性.

|
图 2 不同煅烧温度的0.3ZnTiO3/TiO2的场发射扫描电镜图 Fig. 2 FE-SEM images of 0.3ZnTiO3/TiO2 with different calcination temperature |
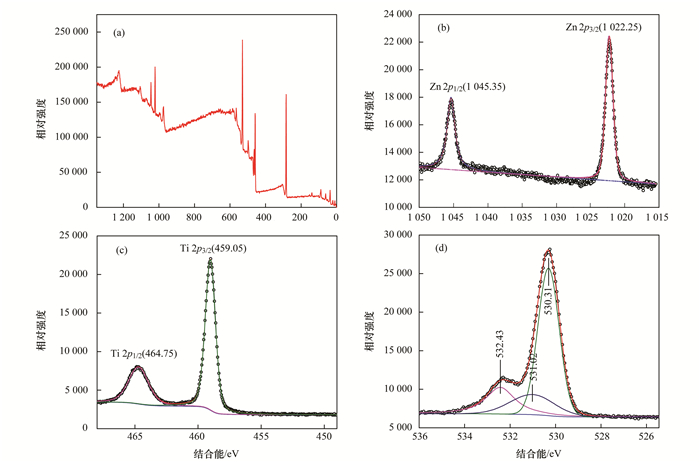
为了分析复合催化剂的化学成分和元素价态分布, 对600℃煅烧的0.3ZnTiO3-TiO2复合光催化剂进行了X射线光电子能谱(XPS)测试, 其结果如图 3所示.图 3(a)为催化剂的谱图, 包含了复合催化剂的元素组成.图 3(b)是复合催化剂中Zn2p轨道的谱图. Zn2p1/2对应的峰值是1045.35 eV, Zn2p3/2对应的峰值是1022.25 eV, 两个特征峰之间结合能相差23.1 eV, 表明复合催化剂中Zn主要以Zn2+的形式存在[24, 25].图 3(c)显示的是复合催化剂中Ti2p轨道的谱图. Ti2p1/2和Ti2p3/2对应的峰值分别是464.75 eV和459.05 eV, 这对应着ZnTiO3中的氧化形式的Ti[24].图 3(d)显示的是复合催化剂中O1s的特征峰. O1s的特征峰是由Ti—O(530.31 eV), Zn—O(531.02 eV)和H—O(532.43 eV)组成[26].由上述XPS谱图可以确定, 复合光催化剂ZnTiO3-TiO2已成功制备.
|
(a) 0.3ZnTiO3-TiO2-600℃总谱; (b) Zn 2p谱图; (c) Ti 2p谱图; (d) O 1s谱图 图 3 0.3ZnTiO3-TiO2-600℃的XPS图谱 Fig. 3 XPS analysis of 0.3ZnTiO3-TiO2-600℃ |
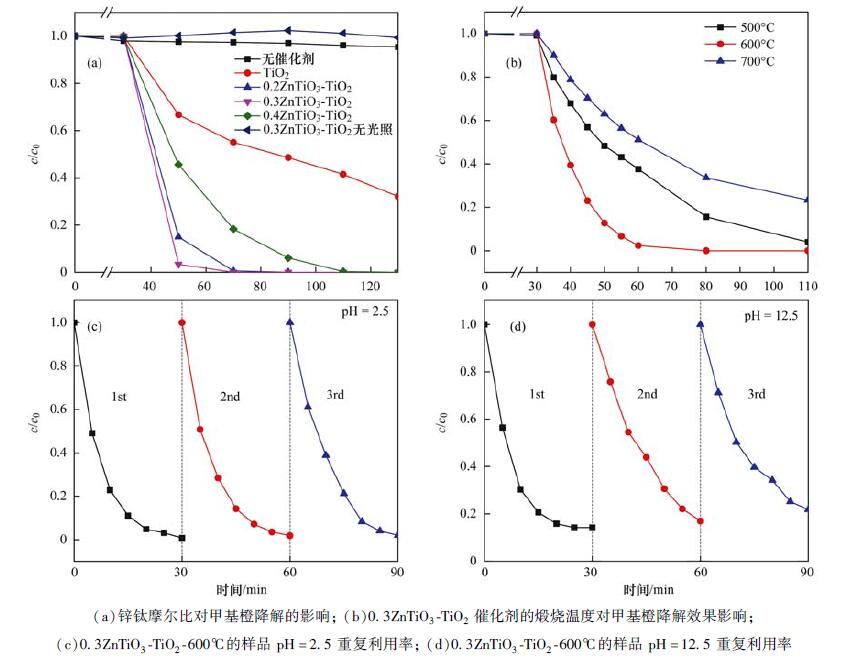
对于ZnTiO3的引入, 催化剂的光催化效果较单纯的TiO2有明显的提升.如图 4(a)所示, 当硝酸锌与钛酸四丁酯的掺杂摩尔比为0.3时, 紫外光下对甲基橙的光降解效果最佳.而掺杂摩尔比过低时, ZnTiO3与TiO2形成异质结较少, 从而减小异质结的作用.掺杂量过多时, 可能是大量的ZnTiO3与TiO2互相包裹, 影响了TiO2的活性位点.
|
图 4 ZnTiO3-TiO2光催化降解甲基橙的性能 Fig. 4 Photocatalytic degradation of methyl orange using ZnTiO3-TiO2 |
本研究发现, 不同煅烧温度对半导体晶型会有巨大影响.如图 4(b)所示, 600℃为最佳的煅烧温度.结合之前XRD分析, 500℃煅烧时, 二氧化钛以锐钛矿形式存在.含锌化合物以钛酸锌形式存在.但是由于温度原因, 导致二氧化钛和钛酸锌结晶度不好, 从而降低了光催化活性. 600℃煅烧时, 二氧化钛以锐钛矿晶型存在, 锌类化合物以钛酸锌形式存在.锐钛矿型TiO2与ZnTiO3形成的异质结有助于光生电子和空穴的分离, 从而提高其光催化活性. 700℃煅烧时, 二氧化钛由锐钛矿转变成了金红石, 因高温处理导致其表面羟基数量较少, 同时高温处理制备金红石相TiO2的过程中往往引起晶粒烧结团聚, 引起比表面积的降低, 均不利于光催化反应活性的提高[27].再者, 锐钛矿TiO2是低温相, 其稳定性低于金红石相, 因此晶格中会存在一些氧缺陷位, 可以捕获光生电子来减少光生电子和空穴的复合几率, 进而提高光催化反应活性.
2.2.3 催化剂耐酸碱性及重复利用率实际印染废水的酸碱性具有不确定性.因此, 为考察该催化剂在实际废水中的应用前景, 分别选择在pH为2.5、7和12.5的反应体系中, 进行了光催化模拟实验.在紫外光照30 min时, 甲基橙的降解分别达到了99.3%、97.6%和85.8%.图 4(c)和4(d), 分别为pH=2.5和pH=12.5的条件下重复降解效果, 酸性重复利用率分别达到了99.3%、92.9%和91.7%;碱性重复利用率分别达到了85.8%、85.5%和83.9%.表明催化剂可以广泛适用于各种酸碱体系中, 而且可以重复回收利用.而酸碱条件下催化效果的差异, 是因为酸性条件会促进光生载流子与溶液中的H+或O2反应, 从而阻止电子和空穴复合, 产生更多的活性自由基(O2-·), 有利于光催化氧化反应的进行[28].
2.3 光催化机制分析催化剂的微观结构对光催化效果有巨大影响.本研究对600℃煅烧的复合催化剂进行TEM分析.图 5(a)和图 5(b)分别为催化剂的低分辨和高分辨投射电镜图; 图 5(c)为能谱分析的选定区域; 图 5(d)~5(f)分别为选定区域中O、Ti和Zn的元素分布.可以发现, Ti和O原子均匀分布, 而Zn原子分布则稍显集中, 表明ZnTiO3成功负载到了TiO2表面.
图 5(b)表明, 复合催化剂结晶度良好, 观察其晶格条纹, 0.352nm和0.273nm分别对应锐钛矿(JCPDS No 99-0008)中的(101)晶面和ZnTiO3(JCPDS No 39-0190)中的(104)晶面, 可以发现两种半导体在晶面处形成了界面区域.二者之间强烈地相互作用, 可能会形成异质结, 异质结的形成会提高光生电子和空穴的分离效率[29].

|
(a) 0.3ZnTiO3-TiO2的透射电镜图(低分辨); (b) 0.3ZnTiO3-TiO2的透射电镜图(高分辨); (c)~(f) 0.3ZnTiO3-TiO2的元素分布 图 5 0.3ZnTiO3-TiO2的透射电镜及元素分布 Fig. 5 HRTEM images and element mapping of 0.3ZnTiO3-TiO2 |
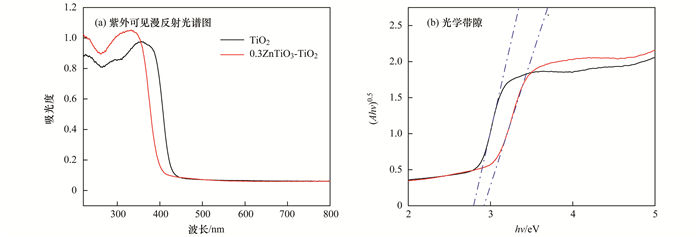
异质结的存在会对光催化剂的能带产生较大影响.为了验证异质结的存在, 本研究对样品进行了紫外可见漫反射的测试.其结果如图 6所示.从图 6(a)中可以发现, 0.3ZnTiO3-TiO2较TiO2发生了一定的蓝移, 同时在紫外光区的光吸收有了一定的增强, 而本研究在紫外光条件下的实验, 从而在一定程度上有利于光催化效率的提升.
|
图 6 TiO2和0.3ZnTiO3-TiO2的光学性质 Fig. 6 Optical properties of TiO2 and 0.3ZnTiO3-TiO2 |
根据Tauc plot公式:
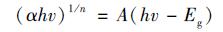
|
式中, α为吸光指数, h为普朗克常数, v为频率, A为常数, Eg为半导体禁带宽度.指数n与半导体类型有关.直接带隙半导体: n=1/2;间接带隙半导体n=2. TiO2是间接带隙半导体, 故n取2).由此以(Ahv)1/n对hv作图, 其结果如图 6(b)所示.计算可得TiO2和0.3ZnTiO3-TiO2的禁带宽度值分别为2.79eV和2.92eV.禁带宽度的变大, 一定程度上使其在光照下产生光生电子与空穴的氧化还原能力提高[30].
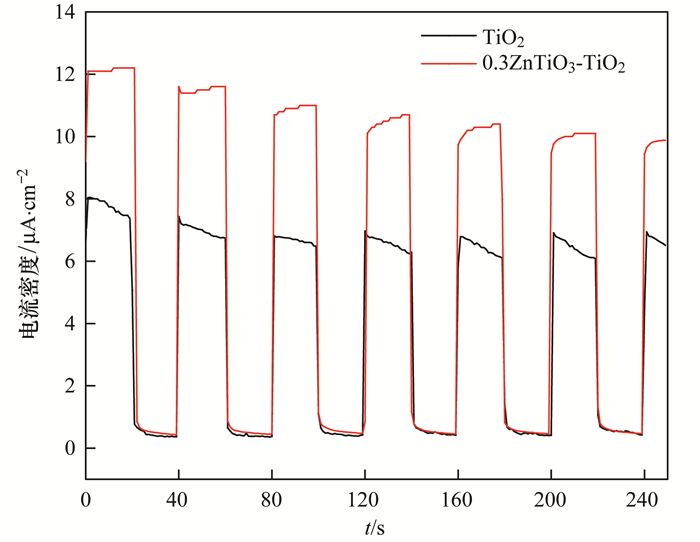
高效的电荷转移和分离是影响光催化的重要因素.本研究可以通过光电流的测试来验证异质结对光生电子的分离和迁移影响[31].在紫外光的条件下, 以0.1mol·L-1的NaSO4溶液为电解液, 在0.5 V电压下对TiO2和0.3ZnTiO3-TiO2进行光电流测试, 其结果如图 7所示.在光照时, 可以看到两种类型的光电极都产生了均匀稳定的光电流, 同时光响应具有良好的可逆性. TiO2的光电流密度为7 μA·cm-2, 复合催化剂0.3ZnTiO3-TiO2的光电流较TiO2有了明显的提高, 达到了11 μA·cm-2.光电流的增强是由于复合催化剂的光生电子和空穴可以有效分离[32].
|
图 7 TiO2和0.3ZnTiO3-TiO2的光电流对比 Fig. 7 Photocurrent of TiO2 and 0.3ZnTiO3-TiO2 under ultraviolet light |
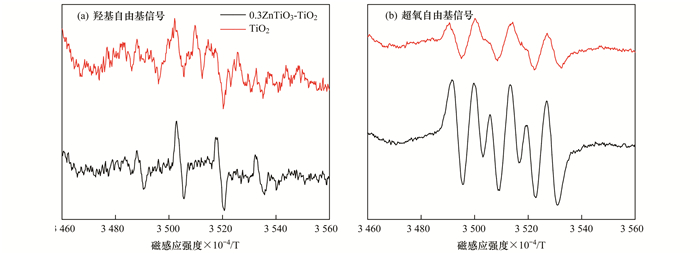
为进一步探究反应体系中羟基自由基和超氧自由基的产生, 本研究利用电子自旋共振波谱仪(ESR)验证笔者的推测.本实验中分别在水和甲醇体系中检测TiO2和0.3ZnTiO3-TiO2的羟基自由基和超氧自由基的产生.图 8分别表示羟基自由基和超氧自由基的信号峰.可以看出复合催化剂较TiO2, 自由基信号有了明显增强, 测试结果与实验结果相符合.正是由于TiO2和ZnTiO3形成了异质结, 在TiO2产生的光生电子转移到ZnTiO3表面, 与O2相结合, 产生了大量的超氧自由基, 同时减少了光生电子和空穴的复合, 从而提高了其光催化活性[33].
|
图 8 TiO2和0.3ZnTiO3-TiO2的光催化反应自由基的ESR图 Fig. 8 ESR spectra of TiO2 and 0.3ZnTiO3-TiO2 |
(1) 利用溶胶凝胶法制备了ZnTiO3-TiO2复合光催化剂, 对甲基橙有良好的降解效果.
(2) 当ZnTiO3/TiO2的摩尔比为0.3, 煅烧温度为600℃时, 产物以锐钛矿TiO2和ZnTiO3为主. 30 min光照后, 对甲基橙降解率为97.6%.在pH为2.5和12.5的条件下进行重复实验, 结果表明催化剂具有良好的光催化活性和化学稳定性.
(3) 将ZnTiO3引入到TiO2, 使其光催化效果有了明显的提升.通过自由基捕获和光电流对催化机制分析发现, ZnTiO3和TiO2两种半导体的复合形成了异质结, 而异质结的存在使得复合催化剂的光生电子和空穴的复合率较单一半导体TiO2有了明显的降低, 体系中的空穴、羟基自由基和超氧自由基含量有了提高, 从而提高了光催化活性.
| [1] | Ribeiro A R, Nunes O C, Pereira M F R, et al. An overview on the advanced oxidation processes applied for the treatment of water pollutants defined in the recently launched Directive 2013/39/EU[J]. Environment International, 2015, 75: 33-51. DOI:10.1016/j.envint.2014.10.027 |
| [2] | Han F, Kambala V S R, Srinivasan M, et al. Tailored titanium dioxide photocatalysts for the degradation of organic dyes in wastewater treatment:A review[J]. Applied Catalysis A:General, 2009, 359(1-2): 25-40. DOI:10.1016/j.apcata.2009.02.043 |
| [3] | Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238(5358): 37-38. DOI:10.1038/238037a0 |
| [4] |
于艳辉, 哈日巴拉, 徐传友, 等. 纳米二氧化钛光催化剂研究进展[J]. 材料导报, 2008, 22(S1): 54-57. Yu Y H, Hari B, Xu C Y, et al. Research progress in Nano TiO2 photocatalyst[J]. Materials Review, 2008, 22(S1): 54-57. |
| [5] | Singh R, Dutta S. A review on H2 production through photocatalytic reactions using TiO2/TiO2-assisted catalysts[J]. Fuel, 2018, 220: 607-620. DOI:10.1016/j.fuel.2018.02.068 |
| [6] | Kumar S G, Devi L G. Review on modified TiO2 photocatalysis under UV/visible light:selected results and related mechanisms on interfacial charge carrier transfer dynamics[J]. The Journal of Physical Chemistry A, 2011, 115(46): 13211-13241. DOI:10.1021/jp204364a |
| [7] | Liu Y, Wei J H, Xiong R, et al. Enhanced visible light photocatalytic properties of Fe-doped TiO2 nanorod clusters and monodispersed nanoparticles[J]. Applied Surface Science, 2011, 257(18): 8121-8126. DOI:10.1016/j.apsusc.2011.04.121 |
| [8] | Nishiyama N, Yamazaki S. Effect of mixed valence states of platinum ion dopants on the photocatalytic activity of titanium dioxide under visible light irradiation[J]. ACS Omega, 2017, 2(12): 9033-9039. DOI:10.1021/acsomega.7b01393 |
| [9] | Xiong Y L, Yang L, Xiao P, et al. Enhanced charge separation and oxidation kinetics by loading Pt nanoparticles with hydrogenated TiO2 nanotubes[J]. Journal of Materials Science, 2018, 53(10): 7703-7714. DOI:10.1007/s10853-018-2079-9 |
| [10] |
刘晴, 喻泽斌, 张睿涵, 等. 钯掺TiO2光催化降解全氟辛酸[J]. 环境科学, 2015, 36(6): 2138-2146. Liu Q, Yu Z B, Zhang R H, et al. Photocatalytic degradation of perfluorooctanoic acid by Pd-TiO2 photocatalyst[J]. Environmental Science, 2015, 36(6): 2138-2146. |
| [11] | Sun C X, He P, Pan G F, et al. Study on preparation and visible-light activity of Ag-TiO2 supported by artificial zeolite[J]. Research on Chemical Intermediates, 2018, 44(4): 2607-2620. DOI:10.1007/s11164-017-3249-0 |
| [12] |
倪冰楠, 陆婷, 刘心娟, 等. 纳米Au/TiO2复合物光催化降解亚甲基蓝[J]. 环境工程学报, 2014, 8(12): 5372-5376. Ni B N, Lu T, Liu X J, et al. UV photocatalytic reduction of methylene blue by Nano Au/TiO2 composites[J]. Chinese Journal of Environmental Engineering, 2014, 8(12): 5372-5376. |
| [13] | Chen Q, Tong R F, Chen X J, et al. Ultrafine ZnO quantum dot-modified TiO2 composite photocatalysts:the role of the quantum size effect in heterojunction-enhanced photocatalytic hydrogen evolution[J]. Catalysis Science & Technology, 2018, 8(5): 1296-1303. |
| [14] | Liao D L, Badour C A, Liao B Q. Preparation of nanosized TiO2/ZnO composite catalyst and its photocatalytic activity for degradation of methyl orange[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2008, 194(1): 11-19. DOI:10.1016/j.jphotochem.2007.07.008 |
| [15] | Su E C, Huang B S, Wey M Y. Enhanced optical and electronic properties of a solar light-responsive photocatalyst for efficient hydrogen evolution by SrTiO3/TiO2 nanotube combination[J]. Solar Energy, 2016, 134: 52-63. DOI:10.1016/j.solener.2016.04.007 |
| [16] | Gao K, Li S D. Multi-modal TiO2-LaFeO3 composite films with high photocatalytic activity and hydrophilicity[J]. Applied Surface Science, 2012, 258(17): 6460-6464. DOI:10.1016/j.apsusc.2012.03.061 |
| [17] |
苏碧桃, 朱平武, 许晶晶, 等. ZnTiO3-TiO2纳米复合材料的光催化性能[J]. 应用化学, 2011, 28(1): 33-38. Su B T, Zhu P W, Xu J J, et al. Photocatalytic property of ZnTiO3-TiO2 Nano-composite materials[J]. Chinese Journal of Applied Chemistry, 2011, 28(1): 33-38. |
| [18] |
王爱民, 白妮, 王金玺, 等. ZnTiO3/TiO2异质复合材料的制备及光催化性能[J]. 人工晶体学报, 2018, 47(2): 382-388. Wang A M, Bai N, Wang J X, et al. Preparation and photocatalytic property of ZnTiO3/TiO2 heterogeneous composite material[J]. Journal of Synthetic Crystals, 2018, 47(2): 382-388. DOI:10.3969/j.issn.1000-985X.2018.02.026 |
| [19] |
郑红娟, 赵志伟, 张琳琪, 等. ZnO-TiO2纳米复合材料的制备及光催化性能研究[J]. 功能材料, 2010, 41(12): 2120-2123. Zheng H J, Zhao Z W, Zhang L Q, et al. Preparation and photocatalytic property of ZnO-TiO2 nanocomposites[J]. Journal of Functional Materials, 2010, 41(12): 2120-2123. |
| [20] |
程刚, 周孝德, 李艳, 等. 纳米ZnO-TiO2复合半导体的La3+改性及其光催化活性[J]. 催化学报, 2007, 28(10): 885-889. Cheng G, Zhou X D, Li Y, et al. La3+ modification of ZnO-TiO2 coupled semiconductors and their photocatalytic activity[J]. Chinese Journal of Catalysis, 2007, 28(10): 885-889. DOI:10.3321/j.issn:0253-9837.2007.10.010 |
| [21] |
邱明艳, 张天永, 李彬, 等. La-TiO2/ZnO异质结纳米复合材料的光催化性能[J]. 人工晶体学报, 2014, 43(7): 1809-1814, 1822. Qiu M Y, Zhang T Y, Li B, et al. Photocatalytic properties of La-TiO2/ZnO heterojunction nanocomposites[J]. Journal of Synthetic Crystals, 2014, 43(7): 1809-1814, 1822. DOI:10.3969/j.issn.1000-985X.2014.07.038 |
| [22] | Salavati-Niasari M, Soofivand F, Sobhani-Nasab A, et al. Synthesis, characterization, and morphological control of ZnTiO3 nanoparticles through sol-gel processes and its photocatalyst application[J]. Advanced Powder Technology, 2016, 27(5): 2066-2075. DOI:10.1016/j.apt.2016.07.018 |
| [23] |
陈小泉, 古国榜. 以钛氧有机物为前驱物制备具有高光催化活性的纳米二氧化钛晶体[J]. 催化学报, 2002, 23(4): 312-316. Chen X Q, Gu G B. Preparation of nanometer crystal TiO2 of high photocatalytic activity with titanyl organic compound as precursor[J]. Chinese Journal of Catalysis, 2002, 23(4): 312-316. DOI:10.3321/j.issn:0253-9837.2002.04.007 |
| [24] | Mofokeng S J, Kumar V, Kroon R E, et al. Structure and optical properties of Dy3+ activated sol-gel ZnO-TiO2 nanocomposites[J]. Journal of Alloys and Compounds, 2017, 711: 121-131. DOI:10.1016/j.jallcom.2017.03.345 |
| [25] | Morozov I G, Belousova O V, Ortega D, et al. Structural, optical, XPS and magnetic properties of Zn particles capped by ZnO nanoparticles[J]. Journal of Alloys and Compounds, 2015, 633: 237-245. DOI:10.1016/j.jallcom.2015.01.285 |
| [26] | 张鹏.钛基复合纳米纤维材料的制备及光催化性质研究[D].长春: 东北师范大学, 2014. |
| [27] | Wang C C, Ying J Y. Sol-gel synthesis and hydrothermal processing of anatase and rutile titania nanocrystals[J]. Chemistry of Materials, 1999, 11(11): 3113-3120. DOI:10.1021/cm990180f |
| [28] | Zhang Y C, Zhang Q, Shi Q W, et al. Acid-treated g-C3N4 with improved photocatalytic performance in the reduction of aqueous Cr(Ⅵ) under visible-light[J]. Separation and Purification Technology, 2015, 142: 251-257. DOI:10.1016/j.seppur.2014.12.041 |
| [29] | Lu L Y, Wang G H, Zou M, et al. Effects of calcining temperature on formation of hierarchical TiO2/g-C3N4 hybrids as an effective Z-scheme heterojunction photocatalyst[J]. Applied Surface Science, 2018, 441: 1012-1023. DOI:10.1016/j.apsusc.2018.02.080 |
| [30] |
张雪, 刘建新, 王雅文, 等. 异质结型AgBr/CuO光催化剂的合成、光催化活性及再生[J]. 高等学校化学学报, 2016, 37(1): 88-93. Zhang X, Liu J X, Wang Y W, et al. Synthesis, photocatalytic activity and regeneration of AgBr/CuO heterojunction photocatalyst[J]. Chemical Journal of Chinese Universities, 2016, 37(1): 88-93. |
| [31] | Zhang C Q, Li X Y, Zheng S Z, et al. Construction of TiO2 nanobelts-Bi2O4 heterojunction with enhanced visible light photocatalytic activity[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2018, 548: 150-157. |
| [32] | Wang Y J, Shi R, Lin J, et al. Enhancement of photocurrent and photocatalytic activity of ZnO hybridized with graphite-like C3N4[J]. Energy & Environmental Science, 2011, 4(8): 2922-2929. |
| [33] |
闫俊青.基于TiO2半导体光生载流子分离、可见光范畴拓展策略探究[D].天津: 南开大学, 2015. Yan J Q. Study of TiO2-based semiconductors: Photo-generated carriers' separation and visible light response[D]. Tianjin: Nankai University, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10055-1017807889.htm |
 2019, Vol. 40
2019, Vol. 40


