2. 石油石化污染物控制与处理国家重点实验室, 北京 102206
2. State Key Laboratory of Petroleum Pollution Control and Treatment, Beijing 102206, China
随着人类在过去几个世纪对传统化石燃料的过度开采使用, 人类目前正在面临严重的能源短缺与环境污染问题, 半导体光催化利用丰富的太阳能光催化分解水产H2、分解有害污染物、选择性转化有机物、转换CO2为碳燃料等, 被认为是应对能源短缺和环境污染的一种高效, 绿色的解决方案.其中, TiO2作为一种处理难降解有机物的光催化材料而得到广泛研究, 而且, 由于其具有3.2 eV的宽带隙能, 仅可在紫外光区吸收光子.目前对于光催化剂的改进多采用贵金属掺杂[1, 2]、形貌改进[2]、负载客体半导体[3]等方法提高光催化性能.而BiOI作为一种带隙能为1.7~1.9 eV的窄带隙光催化材料, 由于其在可见光下对于罗丹明B、甲基橙、亚甲基蓝、对氯苯酚具有较高的光催化活性而得到广泛的研究.
BiOI作为高度各向异性的层状结构间隙半导体, 具有十分优异的光催化性能, 相比于其他的卤氧化铋光催化剂(BiOBr、BiOCl), BiOI具有最窄的禁带宽度, 因此其具有更强的可见光响应, 其独特的层状结构使得BiOX具有足够的空间来极化相应的原子和轨道, 这一诱导偶极矩能有效地分离电子空穴对.另一方面, BiOX是间接跃迁禁带宽, 受激电子必须穿过一定的K层才能被价带所激发, 这样就降低了光致电子空穴对的复合概率[4~6].
MoS2作为一种与石墨烯类似的二维(2D)层状材料, 因其层状结构被高度关注, 其中每层由两层六方紧密堆积的硫原子与中间一层钼原子形成三明治结构, 相邻的层间由较弱的范德华力结合在一起[7], MoS2的层状结构表现出其巨大的比表面积, 较多的活性位点, 使其具有一定的吸附性能, 也为电子的快速迁移提供了可能.作为过渡金属二硫化物中的一员(MX2这里M代表过渡金属, X代表硫族金属诸如S、Se、Te、Po), 作为半导体材料其带隙1.23~1.69 eV, 具有较高的太阳光利用率, 并且带隙与层厚度, 纳米尺寸, 掺杂等因素相关[8].考虑到MoS2与BiOI具有相似的结构, 采用适当的方法以少层MoS2与BiOI复合实现BiOI改性, 会进一步有效提升光催化性能, 成为光催化应用中理想的光催化材料.
通过共沉淀法制备的新型复合材料MoS2/BiOI在降解罗丹明B的过程中表现出高催化性能.通过水热法首先合成MoS2, 然后采用共沉淀法合成BiOI, 在BiOI的合成过程中, 将硝酸铋与碘化钾加入绿色溶剂乙醇中, 并加入表面活性剂PVP, 在室温下反应, 其中PVP作为一种金属纳米材料的水溶性形貌控制剂, 在BiOI的形貌控制中发挥着重要的作用[9].在所有的纳米结构中, PVP扮演着两种角色: ①作为防止纳米粒子团聚的稳定剂; ②作为控制纳米粒子生长的封装剂[10~12].关于BiOI形貌控制与改性研究较多, 但其中有关MoS2与BiOI两者复合的研究相对较少, 本文通过改变MoS2在BiOI中的质量分数, 探究两者复合的最佳比例, 从而有效提高光催化效率, 得到广泛的实际应用.
1 材料与方法 1.1 试剂及仪器五水硝酸铋、硫代乙酰胺、二水钼酸钠、碘化钾、罗丹明B、亚甲基蓝、甲基橙、重铬酸钾、异丙醇、对苯醌、三乙醇胺、乙醇(均为分析纯).
光催化反应仪:南京胥江机电厂; TU-1901双光束紫外可见分光光度计:北京普析通用仪器有限责任公司; XRD-6100型X射线衍射仪:日本岛津公司; 扫描电镜和透射电子显微镜:日本日立公司; 氮气吸附-脱附:美国麦克仪器公司; X射线光电子能谱仪:VG MultiLab 2000型.
1.2 催化剂的制备 1.2.1 二硫化钼(MoS2)的制备分别称取1.5 g二水钼酸钠与2.2 g硫代乙酰胺, 置于50 mL去离子水中, 磁力搅拌2h, 然后将溶液转移至80 mL的聚四氟乙烯坩埚中, 在240℃的条件下反应24 h, 最终得到二硫化钼光催化剂.
1.2.2 MoS2/BiOI复合材料的制备首先称取1.02 g的五水硝酸铋, 溶解在60 mL乙醇中, 磁力搅拌60 min, 然后, 向其中加入一定量的二硫化钼, 磁力搅拌60 min后超声2 h得到稳定均一溶液, 再向其中加入PVP 0.2 g, 搅拌数分钟后加入0.116 2 g KI获得淡黄色沉淀, 搅拌12 h, 离心分离得到橙色沉淀, 用无水乙醇和去离子水反复洗涤多次, 然后放入60℃真空干燥箱中干燥一夜, 得到BiOI/MoS2复合光催化剂, BiOI单体的制备过程与上述制备方法相同.
通过控制MoS2粉末的投加量制备得到不同质量比的复合光催化剂MoS2/BiOI, 分别将质量分数0.5%、1%、2%、4%、8% MoS2投料比的复合物记为B-M-0.5、B-M-1、B-M-2、B-M-4、B-M-8.
1.3 催化剂性能研究及催化剂稳定性评价 1.3.1 催化剂性能研究为了衡量所制备样品的光催化活性, 以罗丹明B(RhB)水溶液与Cr6+水溶液作为目标污染物, 使用XPA光催化反应仪, 光源为1 000 W氙灯, 用滤光片滤去 < 420 nm的紫外光, 称取0.025 mg光催化剂, 置于50 mL浓度为20 mg·L-1的罗丹明B(RhB)水溶液和10 mg·L-1的Cr6+水溶液中, 磁力搅拌, 避光条件下暗处理1 h, 达到吸附解吸平衡, 然后打开氙灯, 光催化降解污染物, 降解RhB过程中每间隔5 min取3 mL溶液, Cr6+水溶液则每间隔10 min取3 mL溶液, 均采用0.45 μm的滤头进行过滤, 滤去固体颗粒后直接测量RhB水溶液的吸光度, 对过滤后的Cr6+水溶液则采用二苯碳酰二肼分光光度法进行显色测试吸光度, 整个反应过程持续2 h.污染物水溶液的降解率为(η), 由以下公式计算:

|
(1) |
式中, c0和c是污染物水溶液的初始浓度和降解后的浓度(mg·L-1), A0与A分别为污染物初始和降解后的吸光度.
1.3.2 催化剂稳定性评价通过循环降解实验考察复合光催化剂的稳定性和可重复利用性, 将0.025 g复合催化剂分散在20 mg·L-1的罗丹明B溶液中, 反应周期为2 h, 反应结束后, 过滤得到复合光催化剂, 用乙醇和去离子水洗涤、60℃真空干燥后, 重复进行降解实验, 保持与1.3.1节相同的实验条件.
1.4 催化剂降解机制研究采用自由基捕获实验研究活性物种对光催化降解的影响, 从而进一步确定MoS2/BiOI复合光催化剂的光催化降解污染物的机制.自由基捕获实验中利用异丙醇、对苯醌、三乙醇胺分别对可能产生的羟基自由基、超氧自由基和空穴等活性物质进行捕获, 研究不同活性物质对于光催化性能的影响, 其中各个捕获剂的浓度为20、0.1和0.2 mmol·L-1.
2 结果与讨论 2.1 红外色谱红外光谱用于研究MoS2/BiOI复合光催化剂的表面化学性质, 如图 1所示, 在480 cm-1和490 cm-1处的红外峰与BiOI中的Bi=O=Bi键的振动有关, 对于B-M-0.5、B-M-1、B-M-2、B-M-4、B-M-8而言, 在1 290 cm-1处的吸收峰主要是由于PVP中的C—N键的红移, 是PVP中的N原子与BiOI样品发生相互作用导致的.红外光谱中在1 400~1 500 cm-1之间出现的一系列微弱的吸收峰主要与芳香吡啶基团中C=C键有关[9~13]; 在PVP和BiOI的光谱中, 在1 660 cm-1处可以观察到强烈的吸收峰, 这个吸收峰来自于PVP中羰基基团的伸缩振动, 而在由PVP合成的BiOI/MoS2复合光催化剂中, 发生了明显的红移, 这是由于MoS2与PVP中的氧原子发生相互作用的结果.此外, 在2 954 cm-1与3 463 cm-1处的宽峰分别来自于C—H键的对称弹性振动和吸收水分子产生的O—H伸缩振动[14].总体来说, 红外光谱证明BiOI纳米粒子、MoS2纳米粒子与PVP之间的相互作用.

|
图 1 BiOI、PVP和不同复合比光催化剂的红外光谱图 Fig. 1 FTIR patterns of BiOI, PVP and different proportions of the photocatalyst |
作为一种有效的表征手段, XRD可以对复合光催化剂的晶相和纯度进行分析, 样品MoS2、BiOI、B-M-0.5、B-M-1、B-M-2、B-M-4、B-M-8的X射线衍射图谱参照图 2.

|
图 2 MoS2单体、BiOI单体和不同复合比光催化剂的XRD图谱 Fig. 2 XRD patterns of MoS2, BiOI, and different proportions of the photocatalyst |
在图 2中, MoS2单体在2θ为39.6°和58.6°的衍射峰分别对应六方相MoS2晶体的(103)和(110)晶面[8, 15], 并无其他杂峰出现, 表明通过水热法制备的MoS2单体具有较好的纯度, 但具有较差的结晶性, 而出现在9°左右的衍射峰相较于(002)晶面对应的14.4°向低角度移动, 这是由于层间距扩大导致的[16], 有利于MoS2后续超声分离.同时, BiOI在29.66°、31.73°、45.45°、55.19°、66.2°分别对应(102)、(110)、(104)、(212)、(220)晶面(JCPDS卡10-0445), 表明制备的BiOI具有较高的纯度与结晶度, 从图 2中可以发现复合材料中并未出现明显的MoS2特征峰, 造成这种现象主要是因为复合材料中MoS2的含量相对较低, 并且与BiOI的特征峰强度相差较大, 导致复合后的材料的特征峰相对不明显或消失.
2.3 XPS表征通过XPS分析了B-M-2的表面化学组成与价态, 结果如图 3所示, 可见B-M-2是由Bi、I、O、Mo、S、C这6种元素组成, 图 3(a)可知, 样品中的Bi元素存在2个不同能带位置的特征峰, 分别对应于158.7 eV的4f7/2与164 eV的4f5/2, 这表明Bi元素在B-M-2中以+3价存在. 图 3(b)与3(d)分别显示了Mo3d与S2p的XPS图谱, 结合能分别为231.7、234.7、158.65和163.95 eV, 表明复合材料B-M-2中存在着Mo4+与S2-, 样品中位于529.8 eV与531 eV的特征峰对应于O1s的结合能, 位于618.8 eV, 630.3 eV则为I3d5/2与I3d3/2的特征峰, 表明I元素在B-M-2中以I-1的形式存在, 而出现在284.8 eV与286.8 eV的特征峰分别对应于C—H与C=O中的C原子, 这可能是由于PVP的加入向B-M-2中引入了次甲基基团与羧酸基团造成的.由图 3中可以看出, S2p与Bi4f的特征峰位置发生了重叠, 但是B-M-2中Mo4+的存在表明MoS2成功与BiOI复合.这与XRD表征结果相吻合, 表明在B-M-2中存在着MoS2与BiOI.

|
图 3 B-M-2的XPS光谱 Fig. 3 XPS spectra of B-M-2 |
BiOI以及MoS2/BiOI复合光催化剂的形貌通过SEM以及TEM表征进行研究, 如图 4(b)可以观察到BiOI呈现纳米微球状结构, 直径在1 μm左右, 而制备的二硫化钼则呈现纳米片层聚集而成的纳米花结构[图 4(a)], 通过TEM图 5(b)可以观察到, BiOI形成的纳米片层透明, 厚度较小, 形状不规则, 尺寸在几十纳米左右, 相比于BiOI, 与二硫化钼复合后, 复合光催化剂呈现纳米花状结构[图 5(a)], 分布具有一定的层次性, 这可能是由于在反应过程中, 超声作用使BiOI前驱体分布于MoS2纳米花结构中, 发生原位反应, 生成了纳米片状结构, 随着反应的进行, 纳米片增多, 后续生成的纳米片原位生长在BiOI纳米片上, 层层包裹直至反应结束, 形成内部致密外部疏松的纳米花状结构, 也可以通过SEM看到, 两者复合后出现了大量的纳米花状结构[图 4(c)], 随着二硫化钼复合量的增加, 纳米花结构消失, 出现了形状不规则的纳米块状结构[图 4(d)], 这主要是因为二硫化钼的加入量增加, 在制备过程中, 超声搅拌对于二硫化钼的分离效果下降, 导致二硫化钼仍存在一定程度的团聚, 而五水硝酸铋进入二硫化钼的花瓣状结构中, 随着碘化钾的加入, 五水硝酸铋与碘化钾发生反应, 原位生成BiOI片状结构, 使二硫化钼原有的纳米花变得更为密实.如图 4(e)、4(f)所示, 随着二硫化钼的加入量越多, 二硫化钼纳米花结构增多, BiOI的原位生长使纳米花结构消失, 孔隙变小, 结构更为致密.

|
图 4 MoS2、BiOI、B-M-2和B-M-8的SEM图 Fig. 4 SEM images of MoS2, BiOI, B-M-2, and B-M-8 |

|
图 5 B-M-2和BiOI的TEM图 Fig. 5 TEM images of B-M-2 and BiOI |
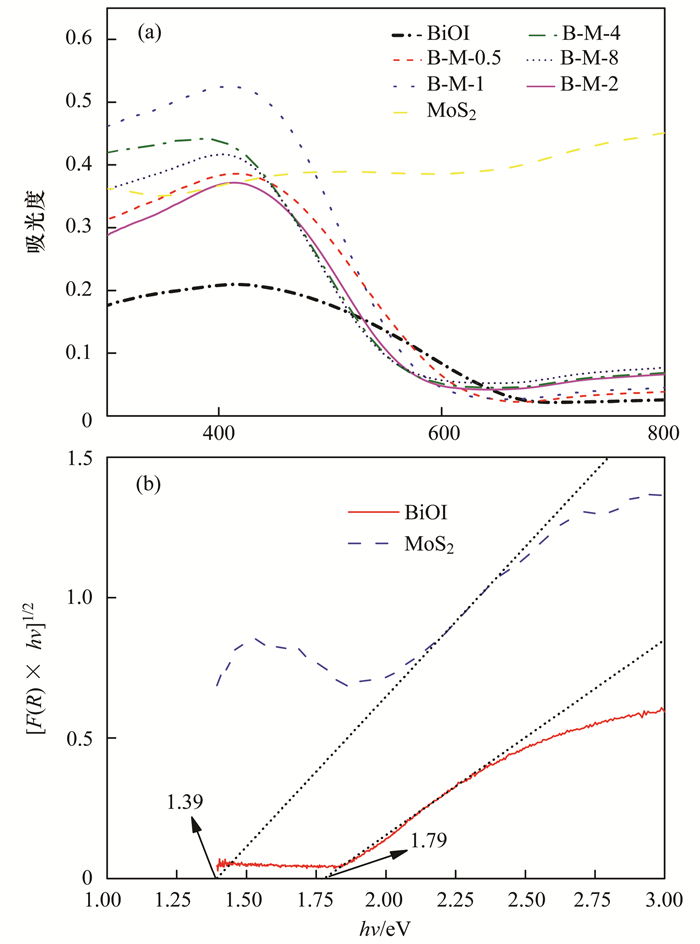
BiOI单体、MoS2单体与B-M-0.5、B-M-1、B-M-2、B-M-4、B-M-8的紫外可见漫反射图谱显示在图 6中, 所有的光催化剂在紫外与可见光区均有较强的响应, BiOI单体的吸收带边在420 nm左右, 复合材料对于可见光表现出了明显增强的吸收, 这主要是由于黑色MoS2的强吸光作用, 表明MoS2与BiOI之间发生了明显的相互作用.光催化剂带隙能可用下列方程计算:
|
图 6 BiOI单体、MoS2单体和不同复合比光催化剂的DRS图谱及以[F(R)×hν]1/2 vs. hν的BiOI单体与MoS2单体禁带宽度 Fig. 6 UV-Vis spectra of the synthesized BiOI samples, MoS2 samples, and different proportions of the photocatalyst and [F(R)×hν]1/2 vs. hν curves of BiOI and the MoS2 catalyst |
根据Kubelka-Muck函数方程:
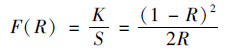
|
(2) |
以[F(R)×hν]n/2 vs. hν作图并做切线可得光催化剂带隙能, 其中K为样品吸收系数; S为样品反射系数; R为样品的漫反射率(%), h为普朗克常量(eV·s), ν为光频率(Hz), 当样品为直接半导体时n=4, 间接半导体时n=1, BiOI为间接半导体, 取n=1, 图 6(b)为[F(R)×hν]1/2 vs. hν拟合带隙能, 切线与X轴的截距与半导体带隙能相近, MoS2与BiOI分别为1.79 eV与1.39 eV.
2.6 Mott-Schottky分析通过Kubelka-Muck方程对紫外可见漫反射光谱进行分析计算得到MoS2与BiOI的带隙能分别为1.39 eV与1.79 eV.通过图 7中的Mott-Schottky可以得到以甘汞电极为参比的MoS2与BiOI导带(CB)位置分别为-0.7 eV与-0.89 eV, 其中C代表半导体的空间电荷层空间电容(F·cm-2), E代表电压(eV), 价带位置可以根据下列公式计算得出:

|
(3) |

|
图 7 BiOI与MoS2的Mott-Schottky导带曲线 Fig. 7 Mott-Schottky conduction band curves of BiOI and MoS2 |
式中, Eg代表半导体带隙能(eV), EVB代表半导体价带电位(eV), ECB代表半导体导带电位(eV), 根据公式可以计算出MoS2与BiOI的价带位置分别为0.69 eV与0.9 eV, 为进一步探究复合光催化剂机制提供了依据.
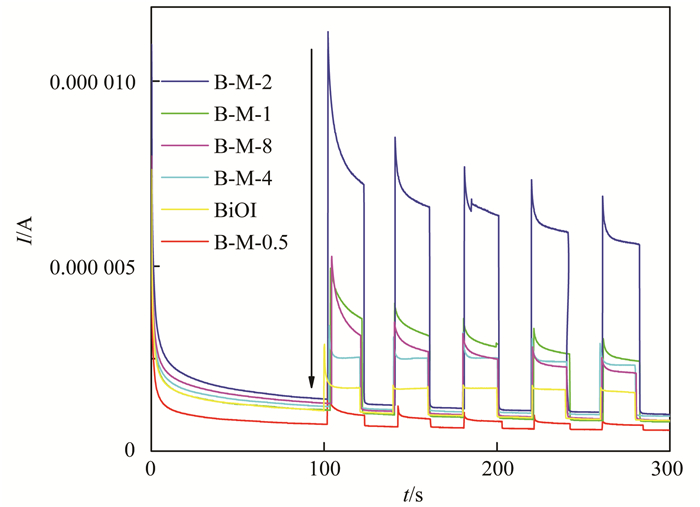
2.7 I-T响应分析光电流响应根据周期性开关氙灯完成测试, 光照结束后, 来自MoS2与BiOI的电子由导带转移到导电玻璃上, 产生响应电流[17], 光电流响应越强, 表明光生电子空穴对的分离效率越高[18].打开氙灯时, 工作电极光电流响应突然增强, 主要与光生载流子的快速分离有关, 关闭氙灯时, 光电流响应保持在较低水平, 与初始电流强度相当.这表明, MoS2/BiOI复合光催化剂与BiOI单体相比具有更强的光电流响应, 其中B-M-2的光电流响应强度明显优于其他MoS2复合量的光催化剂, 说明质量分数为2%的MoS2与BiOI复合具有更高的光生电子空穴分离效率, 更长的光生电子空穴存活时间, 质量分数为2%的MoS2更有利于界面电子的有效转移.由图 8可以看出, B-M-0.5的光电流响应低于BiOI单体, 这是由于制备的MoS2单体为黑色, 复合过少使其对光的吸收能力较弱, 而MoS2过多造成一定程度的团聚, 也限制了复合材料内部对光的吸收, 使产生的响应电流强度较弱.这说明, 过多或过少的复合MoS2可能会对影响光生载流子的生成速率, 进而影响其光催化活性.
|
图 8 BiOI单体、MoS2单体与不同复合比光催化剂光响应图谱 Fig. 8 Photocurrent of BiOI samples, MoS2 samples, and different proportions of the photocatalyst |
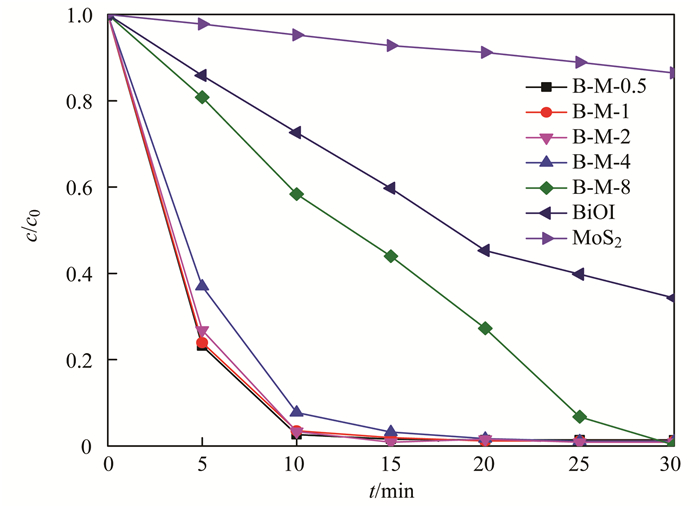
图 9显示了不同质量分数复合比MoS2/BiOI的光催化氧化降解RhB的性能曲线, 从中可以看出复合后的光催化剂与MoS2与BiOI单体相比性能有了较大的提升, 其中B-M-0.5、B-M-1、B-M-2、B-M-4具有较高的光催化活性, 20 min内可以完成污染物的降解, 而B-M-8、MoS2和BiOI分别只降解了92.71%、8.8%和54.72%的RhB, B-M-2的降解率为98.28%, 为BiOI单体降解率的1.79倍. 30 min时除MoS2和BiOI外, 均完成了对RhB的降解, 这是由于MoS2加入过多, 会覆盖在BiOI表面, 限制了光生载流子的分离效率, 也阻碍了其对于可见光的吸收, 从而降低了复合光催化剂降解效率[19].
|
图 9 可见光照射下BiOI单体、MoS2单体与不同复合比光催化剂对RhB降解效率曲线 Fig. 9 Photocatalytic degradation of RhB in the presence of BiOI, MoS2, and the photocatalyst with different proportions catalysts under visible light irradiation |
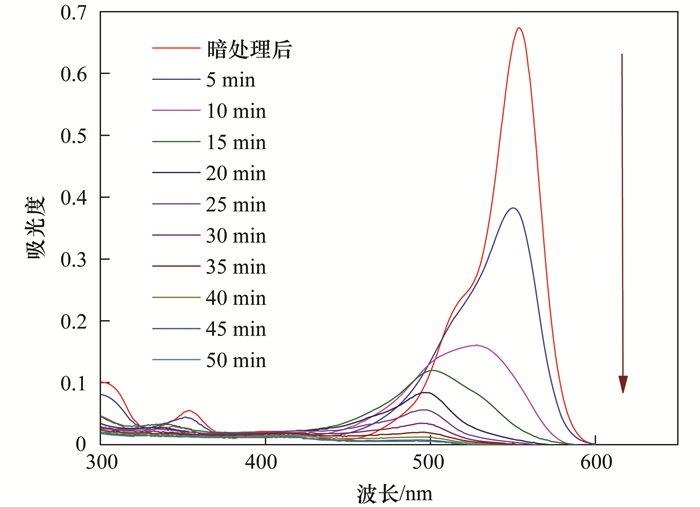
图 10为B-M-2降解RhB过程中的全光谱扫描图, 从中可以看出, 降解过程中, 随着时间的延长, 位于最大波长553 nm处的吸光度逐渐降低, 最后趋于消失, 与此同时, RhB的颜色也由原来明亮的粉红色变为无色, 这表明在可见光下, B-M-2对RhB实现了完全脱色, 在光催化降解过程中, 最大吸收波长在经过10 min的降解后由原来的553 nm移动到500 nm, 这是由于在光催化降解过程中RhB逐渐脱乙基导致的[20].
|
图 10 B-M-2降解RhB过程全光谱图 Fig. 10 Temporal UV-Vis absorption spectral changes during the photocatalytic degradation of RhB using B-M-2 |
当模拟染料废水的浓度较低时, MoS2/BiOI复合材料的光催化反应遵循Langmuir Hinshelwood动力学模型:
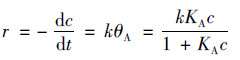
|
(4) |
式中, r为化学反应速率[mol·(L·s)-1], k为反应速率常数, KA为表观速率常数.
由式(4)变形得:
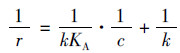
|
(5) |
当浓度c很低时, KAc≤1, 式(5)可简化为式(6), 表现为一级动力学.
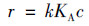
|
(6) |
将式(6)两边积分得:
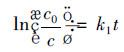
|
(7) |
此时为直线关系, 其中k1=kKA, 为表观一级反应速率常数, 式中, c指t时刻模拟染料废水浓度(mg·L-1), c0指模拟染料废水初始浓度(mg·L-1), t指反应时间(min).
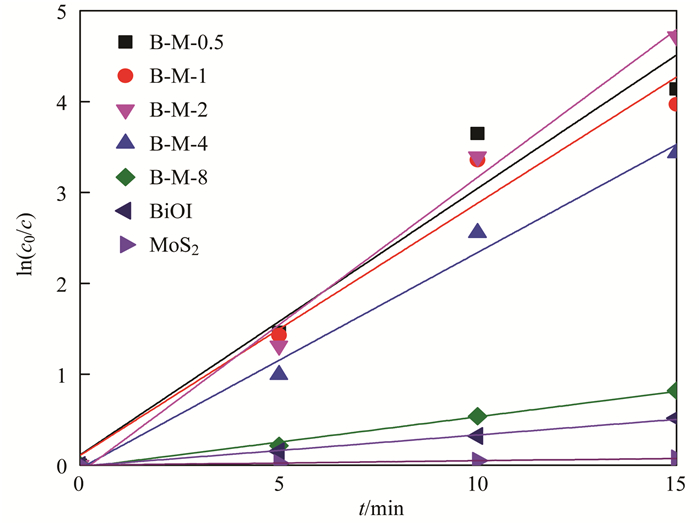
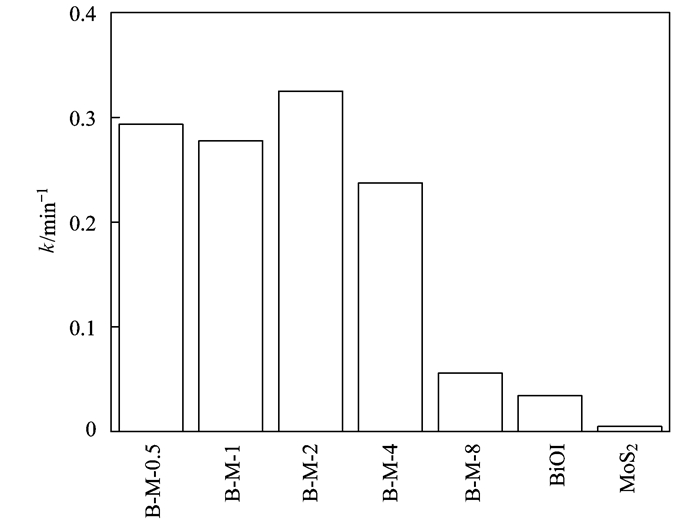
从图 11可以看出, 光催化反应的ln(c0/c)和反应时间呈明显线性关系, 由此可见, MoS2/BiOI纳米复合材料光催化降解符合反应一级动力学方程.由图 12可以看出, 相比于其他光催化剂, B-M-2的一级动力学速率常数最大, k1为0.324 84 min-1, 分别为BiOI和MoS2一级动力学速率常数值的9.5倍与64.7倍, 光催化降解速率得到明显提升.这可能是由于质量分数为2%的MoS2与BiOI复合后, 为复合材料提供了大量的吸附位点与活性位点, 有效吸附了RhB, 将污染物由液相转移至催化剂吸附位点上进行光催化降解; 同时也有效抑制了光生电子空穴对的复合, 增大了光的吸收强度.
|
图 11 光催化降解RhB反应动力学拟合 Fig. 11 Kinetic plots of the photocatalytic degradation of RhB |
|
图 12 光催化降解RhB一级动力学参数 Fig. 12 Pseudo-first-order constants of the photocatalytic degradation of RhB |
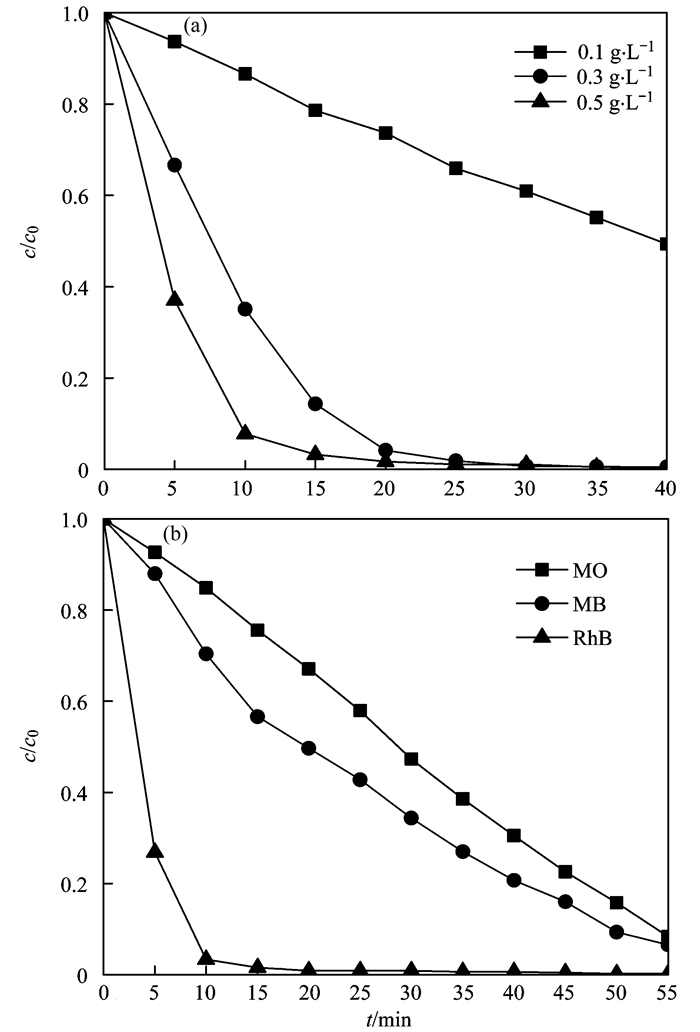
为了进一步研究B-M-2光催化降解RhB的最佳实验条件, 探究了不同催化剂添加量对于光催化降解RhB的影响, 结果如图 13(a)所示, 随着催化剂添加量的减少, 光催化降解效率也逐渐降低, 当催化剂添加量为0.1 g·L-1与0.3 g·L-1时, 10 min时降解率分别为14.5%和65.9%, 但当催化剂浓度增加到0.5 g·L-1时, 其降解率达到了92.3%, 这与降解反应中分布在B-M-2表面的活性位点数量以及光吸收能力有关[21].随着催化剂浓度的增加, 分布于催化剂表面参与降解反应的活性位点的数量也随之增加; 同时, 更高的催化剂添加量也提高了降解反应中催化剂对于可见光的吸收能力, 进而具有更高的光催化活性.在20 min时, 催化剂浓度为0.1、0.3和0.5 g·L-1的降解率分别为26.3%、95.8%与98.2%, 可以看出此时催化剂浓度为0.3 g·L-1与0.5 g·L-1的降解率相差不大, 对RhB基本完成降解脱色.考虑到经济成本与降解效率, 选用0.3 g·L-1的催化剂浓度最佳.
|
图 13 B-M-2添加量与不同染料对于光催化降解RhB的影响 Fig. 13 Effect of the B-M-2 dosage and different dyes on the photocatalytic degradation of RhB |
为了探究B-M-2对不同染料的降解情况, 选取了RhB、MO、MB这3种染料在可见光下进行光催化降解实验, 由图 13(b)可知, 反应进行到60 min时, 3种染料均完成降解过程, RhB、MO和MB的降解率分别为99.8%、98.15%和96.53%.在降解过程中, 3种染料发生了明显的脱色, 说明光催化降解均破坏了染料结构中的发色基团. RhB与MB均属阳离子染料, 分子结构中均不含有偶氮键(—N=N—), 在可见光照射下, 光催化剂吸收能量, 发生电子跃迁, 产生空穴(h+), 此时RhB在光生空穴作用下, 二乙胺基(C2H5)2—N—脱乙基形成氨基—NH2, 经过·OH氧化变为NH4+, 脱离苯环, 同时, ·OH进攻苯环, 使苯环断裂, 最终被氧化成小分子[22]. MB的降解过程与RhB类似, 先发生脱甲基反应, 然后h+与e-会进攻苯环上的N原子和S原子, 使苯环裂解[23].而MO作为阴离子染料, 存在对位取代的—SO3H, 具有吸电子效应和共轭效应, 在光生空穴电子的作用下, 实现偶氮键(—N=N—)的断裂, 进一步进行降解.
从图 14中可以看出, 光催化反应进行到20 min时, RhB降解率达到99.1%, 降解基本完成, 而MB和MO的降解率只有50.3%和32.91%, 这可能是由于光催化剂对于染料的吸附差异造成的. RhB与MB属阳离子染料, MO为阴离子染料, 催化剂对阴阳离子染料电子吸附能力不同, 在降解过程中染料的相转移速率也具有一定差异, 相比于MO 16.1%的吸附率, B-M-2对RhB与MB的吸附性更强, 可以达到78.58%与58.47%的吸附率, 这主要是由于BiOI的生成过程中引入了MoS2, 制备过程中反复的超声处理使MoS2分散较为均匀, 与生成的BiOI充分结合, 减少了MoS2的团聚, 暴露了更多的活性位点, 提高了吸附性能.而在RhB与MB的染料结构中, 存在带有一个正电荷的N原子, 而BiOI表现出了表面负电荷的电性[24], 同时, 所制备的B-M-2暴露了更多的110晶面, 在这个晶面上提供了更多的氧原子[25], 因此BiOI表现了负的电性特征, B-M-2与RhB、MB之间存在的静电作用力导致了RhB和MB相较于MO更容易吸附到B-M-2的表面.

|
图 14 B-M-2对于不同染料的吸附率 Fig. 14 Adsorption rate of B-M-2 for different dyes |
近年来, 光催化剂催化性能与吸附性能的相互作用研究较多, 一般以无水乙醇为溶剂对光催化反应后的催化剂超声处理30 min进行解吸, 以得到经过表面吸附反应后的复合材料脱附率接近100%的混合液, 离心分离对上清液进行分析测定, 结果表明, 脱附后的上清液中的RhB浓度仅仅为吸附总量的13.57%.
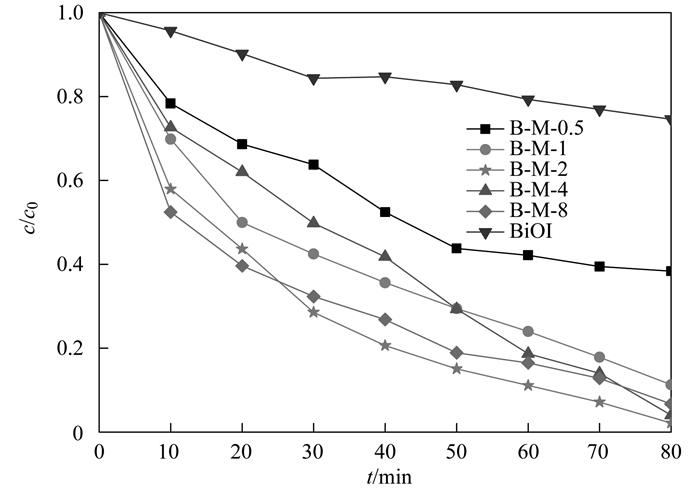
2.9 光催化剂还原性能测试图 15显示了MoS2/BiOI光催化还原Cr6+性能, 从中可以看出, MoS2与BiOI复合后还原Cr6+性能相比于BiOI得到了较大程度的提升, 在可见光照射下, 光催化反应进行到80 min时, B-M-0.5、B-M-1、B-M-2、B-M-4和B-M-8降解率分别达到61.63%、88.75%、97.87%、96%和93.29%, 基本完成将Cr6+还原为Cr3+的光催化反应, 相比于BiOI单体的25.39%, 降解率分别提升了2.43、3.5、3.85、3.78、3.67倍, 进行动力学拟合(图 16), 发现光催化反应的ln(c0/c)和反应时间呈明显线性关系, 由此可见, MoS2/BiOI纳米复合材料光催化降解符合反应一级动力学方程, 从图 17可以看出, 相比于其他光催化剂, B-M-2的一级动力学速率常数最大, k1为0.035 53 min-1, 为BiOI一级动力学速率常数值的10.9倍, 说明BiOI在与MoS2复合后, 光催化还原Cr6+的反应速率得到大幅度提高.这可能是由于在复合MoS2后, 一方面提高了对于Cr6+的吸附率, 另一方面, 复合MoS2后, MoS2出色的电子转移能力有效分离了BiOI在可见光照射下产生的电子空穴对; 利用转移自BiOI的电子与自身产生的电子参与Cr6+的还原反应, 有效降低了Cr6+浓度, 对于光催化处理含Cr6+废水具有一定意义.
|
图 15 BiOI单体与不同复合比光催化剂光催化还原Cr6+活性 Fig. 15 Photocatalytic reduction of Cr6+ over BiOI samples and different proportions of the photocatalyst |

|
图 16 光催化还原Cr6+反应动力学拟合 Fig. 16 Kinetic plots of the photocatalytic reduction of Cr6+ |

|
图 17 光催化还原Cr6+一级动力学参数 Fig. 17 Pseudo-first-order constants of the photocatalytic reduction of Cr6+ |
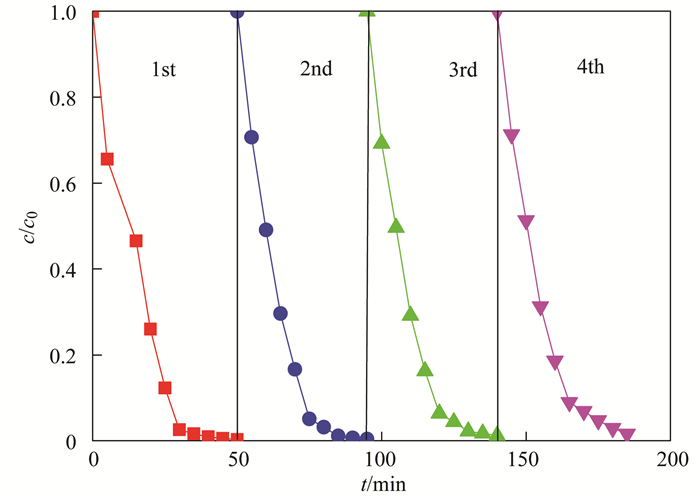
在实际应用中, 光催化剂的稳定性与循环利用能力至关重要, 通过将反应后的光催化剂B-M-2离心分离, 真空干燥后, 在相同的实验条件下降解RhB, 进行了4次循环利用, 以此测试光催化剂可回收利用能力, 由图 18可以发现, 随着回收利用次数的增加, 光催化剂降解RhB性能出现了一定程度的降低, 但在循环使用4次后, 光催化降解效率仍保持在98.39%, 具有较高的光催化活性, 光催化性能出现的这种降低, 有可能是因为在回收过程中催化剂的微量损失或者催化剂表面仍吸附有少量的RhB造成的.总的来说, B-M-2在光催化氧化RhB过程中具有较高的稳定性和可持续利用性, 具有一定的实际应用意义.
|
图 18 可见光照射下B-M-2降解RhB稳定性 Fig. 18 Stability of the B-M-2 catalyst during the degradation of RhB under irradiation with visible light |
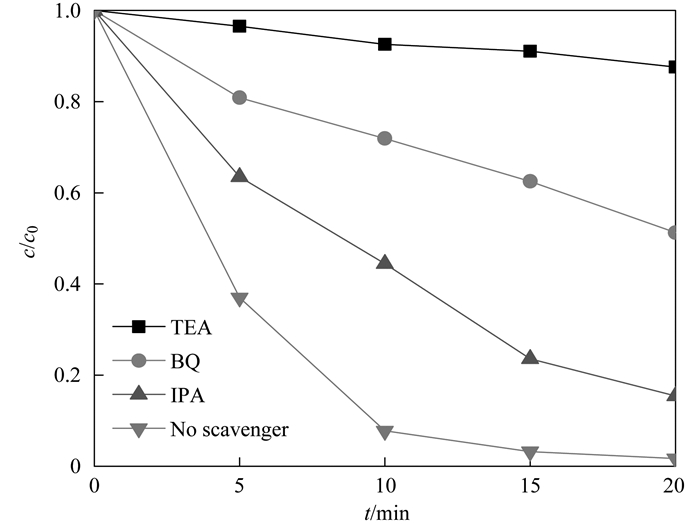
通常来说, 光生电子在光催化还原过程中发挥着主要作用, 同样地, 在光催化氧化过程中也存在着许多氧化自由基, 诸如超氧自由基(·O2-), 羟基自由基(·OH)和空穴(h+), 为了检测光催化氧化降解RhB活性自由基的影响, 选择对苯醌(BQ)作为超氧自由基(·O2-)捕获剂, 三乙醇胺(TEA)作为光生空穴(h+), 异丙醇(IPA)作为羟基自由基(·OH)捕获剂, 在相同实验条件下, 对比实验不加任何捕获剂.由于捕获剂的影响, 光催化氧化反应被部分抑制, 光催化氧化效率降低.从图 19中可以看出, 空穴(h+)在光催化氧化RhB的过程中发挥着决定性的作用, 三乙醇胺加入后光催化降解率只有22.38%, 而对苯醌与异丙醇加入后具有48.76%与84.62%的光催化降解率, 相比于未加捕获剂的98.28%的光催化降解率, 分别降低了75.9%、49.52%与13.66%, 说明羟基自由基在光催化氧化降解RhB的过程中, 只是次要的影响因素.而空穴与超氧自由基发挥着主要作用, 其中又尤以空穴为主.
|
图 19 不同牺牲剂对于光催化氧化RhB的影响 Fig. 19 Effect of different quenchers on the photocatalytic oxidation of RhB |
根据Mott-Schottky与DRS分析, 结合自由基捕获实验, 以及光催化氧化与还原性能, 对光催化机制进行总结如图 20, 从中可以看出, 在可见光照射下, BiOI/MoS2复合光催化剂呈现1型异质结结构, 在可见光照射下, BiOI与MoS2均可被激发产生电子空穴对, 相比于MoS2, BiOI具有更负电位的导带底, 而具有更正电位的价带顶, 因此, 在可见光照射下BiOI产生的电子与空穴会进一步转移到MoS2的导带与价带上.在光催化氧化降解过程中, RhB首先被吸附在催化剂表面, 由于MoS2(0.85 eV)的价带位置相比于·OH/H2O(2.27 eV)和·OH/OH-(2.38 eV)的标准还原电势较低[26], 因此汇集在MoS2价带上的光生空穴无法将H2O与OH-氧化为羟基自由基, 而MoS2(-0.54 eV)导带电位相比于O2/·O2-标准还原电势-0.33 eV较低, 因此具有更强的还原性, 汇集在MoS2导带上的光生电子与氧分子作用生成大量的·O2-, 从而消耗了电子, 减少了MoS2上光生电子空穴对的复合[27].这些产生的超氧自由基与MoS2价带上BiOI与MoS2产生的空穴共同氧化分解RhB生成产物[19].另一方面, 在光催化还原过程中, 由于氧化降解RhB中, 超氧自由基对于催化降解反应的贡献明显低于光生空穴, 因此在MoS2导带上依然存在着丰富的电子无法被氧分子捕获生成超氧自由基, 从而导致较多的电子参与光催化还原反应, 将Cr6+还原产生较低毒性的Cr3+[28].
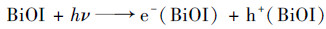
|
(8) |
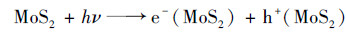
|
(9) |

|
(10) |

|
(11) |
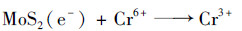
|
(12) |
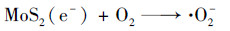
|
(13) |

|
(14) |

|
(15) |

|
图 20 MoS2/BiOI异质结光催化剂光催化反应机制 Fig. 20 Photocatalytic mechanism of the MoS2/BiOI heterojunction photocatalyst |
(1) 通过条件较温和的共沉淀法制备了不同复合比例的光催化剂MoS2/BiOI, 该复合材料对于可见光具有较好的吸收.
(2) 通过降解RhB与Cr6+两种污染物, 分别对复合光催化剂的光催化氧化与还原能力进行考察, 发现复合光催化对两种污染物降解效果均优于BiOI, 其中以B-M-2最为突出, 可在短时间内完成对两种污染物的降解, B-M-2复合光催化剂在循环使用4次后, 仍能在可见光下保持对RhB的高催化降解活性.
(3) 通过对复合光催化剂进行一系列电化学表征及DRS分析, 计算出MoS2与BiOI价带与导带位置, 两者呈现嵌入式能带结构, 为1型异质结, 有效促进了BiOI电子空穴对的分离, 提高了催化剂的光催化活性.同时自由基捕获实验表明在B-M-2降解RhB过程中, 主要活性物种为·O2-与h+, 其中h+影响更为显著.
| [1] |
刘晴, 喻泽斌, 张睿涵, 等. 钯掺TiO2光催化降解全氟辛酸[J]. 环境科学, 2015, 36(6): 2138-2146. Liu Q, Yu Z B, Zhang R H, et al. Photocatalytic degradation of perfluorooctanoic acid by Pd-TiO2 photocatalyst[J]. Environmental Science, 2015, 36(6): 2138-2146. |
| [2] |
黄建辉, 林文婷, 谢丽燕, 等. 石墨相氮化碳-碘氧化铋层状异质结的构建及其光催化杀菌性能[J]. 环境科学, 2017, 38(9): 3979-3986. Huang J H, Lin W T, Xie L Y, et al. Construction of graphitic carbon nitride-bismuth oxyiodide layered heterostructures and their photocatalytic antibacterial performance[J]. Environmental Science, 2017, 38(9): 3979-3986. |
| [3] |
鲍玥, 周旻昀, 邹骏华, 等. C3N4/BiOBr复合可见光催化剂的性能及其作用机制[J]. 环境科学, 2017, 38(5): 2182-2190. Bao Y, Zhou M J, Zou J H, et al. Performance and mechanism study of visible light-driven C3N4/BiOBr composite photocatalyst[J]. Environmental Science, 2017, 38(5): 2182-2190. |
| [4] | Zhao J L, Lv XW, Wang X X, et al. Fabrication of BiOX (X=Cl, Br, and I) nanosheeted films by anodization and their photocatalytic properties[J]. Materials Letters, 2015, 158: 40-44. DOI:10.1016/j.matlet.2015.05.037 |
| [5] | Meng X C, Zhang Z S. New insight into BiOX (X=Cl, Br, and I) hierarchical microspheres in photocatalysis[J]. Materials Letters, 2018, 225: 152-156. DOI:10.1016/j.matlet.2018.04.086 |
| [6] | Yang Y, Zhang C, Cui L, et al. BiOX (X?=-Cl, Br, I) photocatalytic nanomaterials:applications for fuels and environmental management[J]. Advances in Colloid and Interface Science, 2018, 254: 76-93. DOI:10.1016/j.cis.2018.03.004 |
| [7] | Wang C X, Lin H H, Xu Z Z, et al. One-step hydrothermal synthesis of flowerlike MoS2/CdS heterostructures for enhanced visible-light photocatalytic activities[J]. Royal Society of Chemistry Advances, 2015, 5(20): 15621-15626. |
| [8] | Thangavel S, Thangavel S, Raghavan N, et al. Efficient visible-light photocatalytic and enhanced photocorrosion inhibition of Ag2WO4 decorated MoS2 nanosheets[J]. Journal of Physics and Chemistry of Solids, 2017, 110: 266-273. DOI:10.1016/j.jpcs.2017.06.005 |
| [9] | Wang H S, Qiao X L, Chen J G, et al. Mechanisms of PVP in the preparation of silver nanoparticles[J]. Materials Chemistry and Physics, 2005, 94(2-3): 449-453. DOI:10.1016/j.matchemphys.2005.05.005 |
| [10] | Nemamcha A, Moumeni H, Rehspringer J L. PVP Protective mechanism of palladium nanoparticles obtained by sonochemical process[J]. Physics Procedia, 2009, 2(3): 713-717. DOI:10.1016/j.phpro.2009.11.015 |
| [11] | Zhang B C, Yu H Y, Sun D B. Shape-controlled synthesis and formation mechanism of cobalt nanopowders by a PVP-assisted method[J]. Materials Science Forum, 2010, 654-656: 1186-1189. DOI:10.4028/www.scientific.net/MSF.654-656 |
| [12] | Crespo-Quesada M, Yarulin A, Jin M S, et al. Structure sensitivity of alkynol hydrogenation on shape-and size-controlled palladium nanocrystals:which sites are most active and selective?[J]. Journal of the American Chemical Society, 2011, 133(32): 12787-12794. DOI:10.1021/ja204557m |
| [13] | Kaur R, Tripathi S K. Study of conductivity switching mechanism of CdSe/PVP nanocomposite for memory device application[J]. Microelectronic Engineering, 2015, 133: 59-65. DOI:10.1016/j.mee.2014.11.010 |
| [14] | Fu J, Tian Y L, Chang B B, et al. BiOBr-carbon nitride heterojunctions:synthesis, enhanced activity and photocatalytic mechanism[J]. Journal of Materials Chemistry, 2012, 22(39): 21159-21166. DOI:10.1039/c2jm34778d |
| [15] | Bai X, Wan J, Jia J, et al. Simultaneous photocatalytic removal of Cr(Ⅵ) and RhB over 2D MoS2/Red phosphorus heterostructure under visible light irradiation[J]. Materials Letters, 2018, 222: 187-191. DOI:10.1016/j.matlet.2018.04.001 |
| [16] |
周宇, 徐玉福, 胡献国. 铵离子插层MoS2的制备与表征[J]. 应用化学, 2008, 25(1): 5-8. Zhou Y, Xu Y F, Hu X G. Preparation and characterization of molybdenum disulfide with NH4+ interlayer[J]. Chinese Journal of Applied Chemistry, 2008, 25(1): 5-8. DOI:10.3969/j.issn.1000-0518.2008.01.002 |
| [17] | McShane C M, Choi K S. Photocurrent enhancement of n-type Cu2O electrodes achieved by controlling dendritic branching growth[J]. Journal of the American Chemical Society, 2009, 131(7): 2561-2569. DOI:10.1021/ja806370s |
| [18] | Xu H, Yan J, Xu Y G, et al. Novel visible-light-driven AgX/graphite-like C3N4 (X=Br, I) hybrid materials with synergistic photocatalytic activity[J]. Applied Catalysis B:Environmental, 2013, 129: 182-193. DOI:10.1016/j.apcatb.2012.08.015 |
| [19] | Jiang D L, Li J, Xing C S, et al. Two-dimensional CaIn2S4/g-C3N4 heterojunction nanocomposite with enhanced visible-light photocatalytic activities:Interfacial engineering and mechanism insight[J]. ACS Applied Materials & Interfaces, 2015, 7(34): 19234-19242. |
| [20] | Xia J X, Yin S, Li H M, et al. Improved visible light photocatalytic activity of sphere-like BiOBr hollow and porous structures synthesized via a reactable ionic liquid[J]. Dalton Transactions, 2011, 40(19): 5249-5258. DOI:10.1039/c0dt01511c |
| [21] | Wongkalasin P, Chavadej S, Sreethawong T. Photocatalytic degradation of mixed azo dyes in aqueous wastewater using mesoporous-assembled TiO2 nanocrystal synthesized by a modified sol-gel process[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2011, 384(1-3): 519-528. DOI:10.1016/j.colsurfa.2011.05.022 |
| [22] |
李荣荣, 姜恒, 宫红, 等. g-C3N4的制备及其对不同染料光催化降解性能研究[J]. 应用化工, 2016, 45(9): 1700-1704. Li R R, Jang H, Gong H, et al. Simple synthesis of g-C3N4 catalyst for the photocatalytic degradation of different dyes[J]. Applied Chemical Industry, 2016, 45(9): 1700-1704. |
| [23] | Yu Z Q, Chuang S S C. Probing methylene blue photocatalytic degradation by adsorbed ethanol with in situ IR[J]. The Journal of Physical Chemistry C, 2007, 111(37): 13813-13820. DOI:10.1021/jp0715474 |
| [24] | Huang W L, Zhu Q S. DFT calculations on the electronic structures of BiOX (X=F, Cl, Br, I) photocatalysts with and without semicore Bi 5d states[J]. Journal of Computational Chemistry, 2009, 30(2): 183-190. DOI:10.1002/jcc.v30:2 |
| [25] | Yu C L, Fan C F, Yu J C, et al. Preparation of bismuth oxyiodides and oxides and their photooxidation characteristic under visible/UV light irradiation[J]. Materials Research Bulletin, 2011, 46(1): 140-146. DOI:10.1016/j.materresbull.2010.08.013 |
| [26] | Cheng H F, Huang B B, Dai Y, et al. One-step synthesis of the nanostructured AgI/BiOI composites with highly enhanced visible-light photocatalytic performances[J]. Langmuir, 2010, 26(9): 6618-6624. DOI:10.1021/la903943s |
| [27] | Xu M, Han L, Dong S J. Facile fabrication of highly efficient g-C3N4/Ag2O heterostructured photocatalysts with enhanced visible-light photocatalytic activity[J]. ACS Applied Materials & Interfaces, 2013, 5(23): 12533-12540. |
| [28] |
李莉莉, 陈翠柏, 兰华春, 等. g-C3N4协同光催化还原Cr(Ⅵ)及氧化磺基水杨酸[J]. 环境科学, 2017, 38(4): 1483-1489. Li L L, Chen C B, Lan H C, et al. Simultaneous photocatalytic reduction of Cr(Ⅵ) and oxidation of SSA by carbon nitride[J]. Environmental Science, 2017, 38(4): 1483-1489. DOI:10.3969/j.issn.1000-6923.2017.04.036 |
 2019, Vol. 40
2019, Vol. 40


