 唑间接光降解作用
唑间接光降解作用
2. 中国水产科学研究院黄海水产研究所, 农业农村部海洋渔业可持续发展重点实验室, 青岛 266071;
3. 国家海洋局海洋减灾中心, 北京 100194
 唑(SMZ)的间接光解作用和影响因素.结果表明,CDOM对于SMZ具有显著间接光降解作用,这种间接光降解具有双重性,既可以通过生成各种活性中间体来促进SMZ的间接光降解,又可以通过光屏蔽作用以及活性中间体掩蔽作用抑制SMZ的光降解.SMZ的间接光降解主要由CDOM产生的3CDOM*、HO·、1O2等活性中间体控制,其中3CDOM*为SMZ间接光降解的主要参与者.另外,pH、盐度和硝酸根离子对SMZ的间接光降解均具有显著影响作用,而碳酸氢根离子对于SMZ间接光降解的影响作用不明显.
唑(SMZ)的间接光解作用和影响因素.结果表明,CDOM对于SMZ具有显著间接光降解作用,这种间接光降解具有双重性,既可以通过生成各种活性中间体来促进SMZ的间接光降解,又可以通过光屏蔽作用以及活性中间体掩蔽作用抑制SMZ的光降解.SMZ的间接光降解主要由CDOM产生的3CDOM*、HO·、1O2等活性中间体控制,其中3CDOM*为SMZ间接光降解的主要参与者.另外,pH、盐度和硝酸根离子对SMZ的间接光降解均具有显著影响作用,而碳酸氢根离子对于SMZ间接光降解的影响作用不明显.
2. Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture, Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Qingdao 266071, China;
3. National Marine Hazard Mitigation Service, Beijing 100194, China
随着社会经济的不断发展, 越来越多的药物(pharmaceuticals and personal care products, PPCPs)被广泛使用. PPCPs多为水溶性的, 其半衰期较短, 在自然环境中能够发生水解、光降解和微生物降解等过程, 但由于人类自身和养殖业的大量使用, 导致自然界中的PPCPs出现了“假持续现象”, 即自然界中PPCPs浓度基本保持稳定, 对自然环境及人类健康造成威胁[1, 2], 其在环境中的迁移转化及风险评估吸引了全球学者及研究人员的广泛关注.
磺胺类抗生素是使用最为广泛的抗生素之一, 由于其优秀的抗菌性和便宜的价格被广泛用于淡水、海水养殖业中, 与陆源输入叠加, 使得近岸海域海水中的抗生素含量也不断增加.生物体对于磺胺类药物的利用率很低, 受药后约30%~90%的磺胺类药物会以母体或者代谢物的形式排出生物体[3], 同时这些代谢产物在自然环境中也可以通过逆向反应生成母体药物[4], 近年来, 地下水[5]、饮用水[6]、地表水体[7, 8]、甚至是经过处理的水中均检测出了各类磺胺类药物的存在[9].磺胺甲


然而, 目前对于磺胺类抗生素间接光降解机制、特别是海水环境条件下间接光降解作用方面的研究相对较少.本文以磺胺甲
实验设备:Fluorolog3-11荧光分光光度计(Jobin Yvon, France), UV-2550紫外可见分光光度计(日本岛津), XPA-7多试管搅拌式光化学反应仪(南京胥江机电厂), LC-10F高效液相色谱(天津博纳艾杰尔科技有限公司), C18液相色谱柱(Agilent PLRP-S, 5 μm, 150mm×4.60 mm), Agilent1260液相色谱[安捷伦科技(中国)有限公司], 马弗炉(上海意丰电炉有限公司), 0.2μm一次性聚醚砜针头滤器(德国MEMBRANA公司原产膜), 5mL一次性注射器(河南曙光健士医疗器械有限公司), Milli-Q超纯水装置(18.2 MΩ·cm, Milli-Q, Millipore), pH计, 烘箱(上海精宏实验设备有限公司), 超声波清洗器(昆山市超声仪器有限公司).
实验试剂:磺胺甲
取0.050 7 g磺胺甲
(1) CDOM影响探究 取12支石英管各加40 mL不同浓度的CDOM溶液和200 μL的磺胺甲

(2) RIs影响探究 添加·OH淬灭剂的异丙醇(IPA)、1O2捕获剂四氢呋喃和3CDOM*淬灭剂苯酚, 研究反应过程中激发三重态溶解有机物等活性中间体对磺胺甲



(3) pH影响研究 取40 mL、10 mg·L-1 CDOM贮备液, 加200 μL磺胺甲

(4) 盐度影响探究 用Milli-Q水、标准海水以及CDOM母液配制盐度分别为0、5‰、15‰、25‰和35‰, 浓度为10mg·L-1的CDOM溶液, 并加入200 μL磺胺甲


(5) 硝酸根和碳酸氢根离子影响研究 用磺胺甲


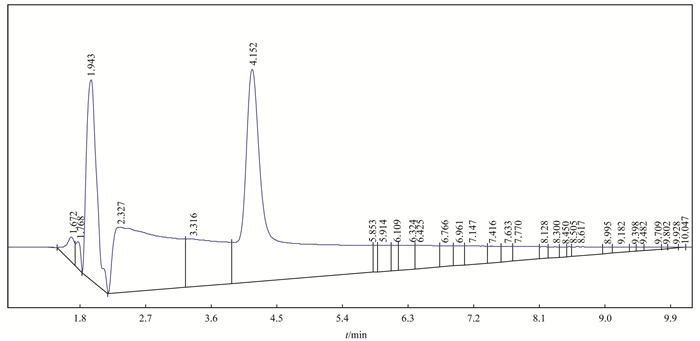
表 1是不同浓度的SRNOM存在下, 分别置于光照和黑暗条件下两组SMZ浓度变化平均值, 各个实验3次平行, 测定的SMZ浓度的相对标准偏差范围为1.4%~6.8%, 实验结果的精密度较高, 重现性较好.可以看出, 相比较于黑暗组, 光照组的SMZ降解速率大大加快, 10 mg·L-1SRNOM溶液中光照组SMZ的24 h降解率达30.9%, 而黑暗组的降解率不足4.1%. 图 1是10 mg·L-1 JKHA存在下SMZ光照40 h的高效液相色谱图, 目标峰SMZ在4.15 min出峰, 峰型良好, 之后无其他产物峰出现.
|
|
表 1 不同浓度SRNOM存在下光照和黑暗条件下的SMZ测定结果 Table 1 Results of SMZ determination under light and dark conditions in the presence of different concentrations of SRNOM |
|
图 1 10 mg·L-1JKHA存在下SMZ光照40 h的液相色谱图 Fig. 1 Chromatogram of SMZ irradiated in the presence of 10mg·L-1JKHA for 40 h |
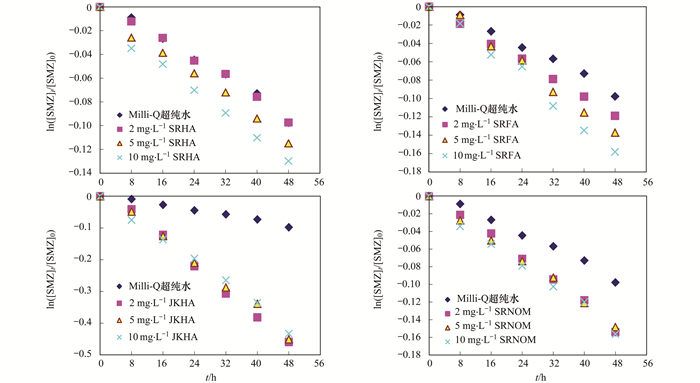
4种CDOM(SRHA、SRFA、JKHA和SRNOM)在SMZ光解中的作用如图 2所示. Milli-Q水对照组中SMZ的浓度随时间延长而降低, 表明照射光波长大于320 nm时直接光解仍在进行, 加入CDOM后增大的部分速率可作为SMZ的间接光降解速率. 4种CDOM对SMZ光降解均具有促进作用, 其中, SRHA和SRFA溶液中, SMZ的间接光解速率随CDOM浓度的增大而增快; 而在JKHA和SRNOM溶液中, SMZ的间接光降解速率在测定范围内CDOM浓度为2 mg·L-1的条件下达到最大, 之后随着CDOM浓度的增大无明显变化.当4种CDOM在2 mg·L-1的低浓度条件下, JKHA、SRNOM对SMZ间接光降解作用最为显著, 当CDOM浓度达到10mg·L-1时, JKHA、SRNOM对SMZ间接光降解作用远大于SRHA和SRFA.各实验平行测定3次, 取平均值, 测得的各SMZ浓度的相对标准偏差均小于7%.
|
[SMZ]t表示t时刻的SMZ浓度; [SMZ]0表示SMZ的初始浓度, 下同
图 2 不同组分不同浓度的CDOM存在下磺胺甲 |
CDOM对于SMZ的间接光降解作用具有双重性.一方面, CDOM光解过程中能够生成活性中间体(RIs), 包括超氧自由基(O2-·)、过氧化氢(H2O2)、羟基自由基(·OH)、单线态氧(1O2)、三线态CDOM(3CDOM*)等, 参与SMZ的间接光降解.另一方面, CDOM会因吸光而屏蔽光辐射, 且浓度越高, 光屏蔽能力越强[7~9], 同时, CDOM作为一种光敏抑制剂, 还可以与RIs发生直接反应, 从而减弱有机污染物的间接光降解[12]. CDOM对SMZ光降解的这种促进或抑制作用的相对强弱变化, 是导致SMZ间接光降解速率随CDOM浓度增加出现非线性变化的主要原因.而不同来源CDOM对SMZ间接光降解作用的不同主要是由于CDOM组成不同、活性中间体的产生效率不同导致的.
2.2 CDOM产生的活性中间体对磺胺甲
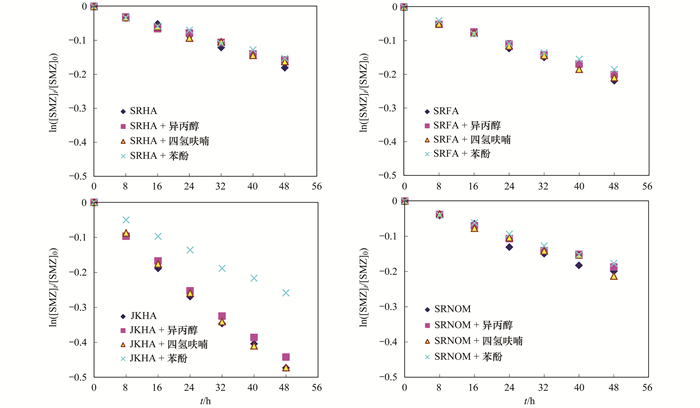
CDOM主要通过生成RIs来促进SMZ间接光降解进程, RIs常被用作衡量水体对于有机污染物间接光降解能力的重要指标[13]. Bahnmüller等[10, 14]发现异丙醇对于·OH的屏蔽率高达98.4%~99.6%, 而苯酚能够有效地抑制由3CDOM*造成的SMZ的转化, 四氢呋喃常被用作1O2的清除剂.本文以异丙醇作为·OH的掩蔽剂, 以苯酚作为3CDOM*的抑制剂, 以四氢呋喃作为1O2的清除剂, 来研究·OH和3CDOM*对SMZ间接光降解的作用, 实验结果如图 3.加入异丙醇和苯酚后, SMZ的间接光降解速率明显降低, 其中, 加入苯酚的反应液中, SMZ的间接光降解速率下降最显著, 这是由于苯酚除了抑制3CDOM*外, 同时也会清除HO·, 加入苯酚与异丙醇后间接光降解速率减小量的差值可作为3CDOM*作用下SMZ间接光解的速率.从图 3可以看出, ·OH和3CDOM*对SMZ的间接光降解均有贡献.在SRHA、SRFA以及SRNOM溶液中, ·OH在SMZ间接光降解中皆处于主导地位, 而在JKHA溶液中, 3CDOM*是SMZ间接光降解的主要贡献者.加入四氢呋喃的CDOM溶液中, SMZ光降解变化不明显, 表明1O2在SMZ间接光转化过程中所起作用较小.
|
图 3 添加不同RIs猝灭剂的CDOM存在下磺胺甲 |
O2是一种典型的三线态抑制剂, 通入O2可使3CDOM*的稳态浓度会被抑制到极小值[15, 16].为了考察HO·和3CDOM*在SMZ间接光降解中的作用, 向CDOM溶液中分别通入O2和N2, N2作为O2的清除剂, 实验结果如图 4所示.

|
图 4 分别同入氧气、氮气的CDOM存在下磺胺甲 |
在4种CDOM溶液中, 充N2(无O2)条件下, SMZ的光降解速率急剧增大, 而充O2条件下, SMZ的光降解速率略有减小, 这种情况说明3CDOM*在SMZ光降解过程中起着重要作用, 是SMZ间接光降解的主要影响因子.·OH对于SMZ的间接光降解作用相对较小.
2.3 溶液pH值对磺胺甲
水体pH值的变化能够改变各种离子、CDOM以及其他溶解物质的存在形态和理化性质, 影响水体中RIs生成及氧化活性, 对水中有机污染物的降解有重要影响[17, 18].为研究pH对于SMZ间接光降解的影响, 配制了不同pH值(5、7、9、11)的10μmol·L-1SMZ溶液进行间接光降解实验, 结果如图 5所示. SMZ间接光解速率在4种CDOM溶液中的变化趋势基本一致, 当pH为7~9时, SMZ的间接光降解速率变化不明显, 当pH=11时, SMZ的光降解能力显著增强, 是因为随着pH值的升高, SMZ的去质子化程度增大, 使SMZ的电子密度升高, 有利于RIs进行亲电攻击.同时, pH值的升高也有利于RIs的生成. Chen等[19]发现pH越高CDOM的降解能力越强, 其产生RIs的能力也随着pH的升高而增强. Garoma等[20]发现水体中·OH稳态浓度水平会随着pH的升高而升高.

|
图 5 pH不同的CDOM存在下磺胺甲 |

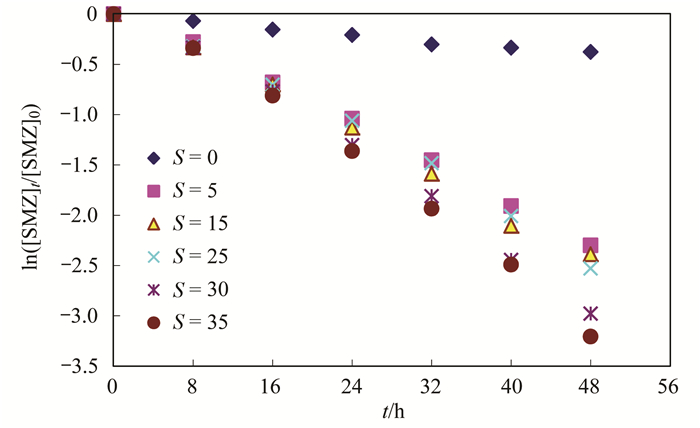
以SMZ母液、JKHA贮备液、Milli-Q水以及IAPSO国际标准海水配制盐度分别为0、5‰、15‰、25‰、30‰和35‰的10 μmol·L-1 SMZ溶液进行光降解实验, 结果如图 6.当盐度从0增大5时, SMZ的光降解速率显著升高, 之后SMZ的光降解速率随着盐度的增大而缓慢增大.海水中有机物的光降解主要由海水的离子强度和卤素离子决定[21]. Parker等[21]发现由于离子强度的作用, 海水中3CDOM*的稳态浓度是淡水条件下的两倍, 有利于有机物污染物的光降解.而卤素离子与HO·反应后生成的卤素活性自由基能加快有机物污染物的降解[22].然而, 卤素离子对于激发态物质具有较强的猝灭能力[23], 当卤素离子浓度较高时, 这种猝灭作用就会显现出来.另外, 盐度的增加有利于CDOM光解产生水合离子[24], 促进H2O2的生成[25], 从而有利于海水中HO·水平的升高[26].
|
图 6 盐度不同的CDOM存在下磺胺甲 |

硝酸根离子也是海水中常见的阴离子之一.有研究发现硝酸根离子在光照的条件下可以生成·OH以促进水体中有机污染物的光降解[27].为研究硝酸根离子对于SMZ光降解的作用, 本文中配制了不同硝酸根浓度(10、20、30以及40μmol·L-1)的盐度为30‰的10μmol·L-1SMZ溶液, 光降解实验结果如图 7所示.硝酸根离子对SMZ光降解的影响不显著.硝酸根离子的光解过程中总是伴随着亚硝酸根离子的产生[28, 29], 而亚硝酸根离子又是·OH的掩蔽剂[30], 即硝酸根离子在光解过程中即是·OH的生产者, 又是·OH的消费者, 当·OH生成量大于亚硝酸根离子生成量时, 硝酸根离子就会对有机污染物光解起促进作用; 而当·OH生成量小于亚硝酸根离子生成量时, 硝酸根离子就会对于有机污染物光解产生抑制作用.

|
图 7 不同硝酸根离子和碳酸根离子浓度梯度下的CDOM存在下磺胺甲 |
碳酸氢根离子是海水中的常见离子, 能与羟基自由基发生反应生成碳酸自由基(·OH+HCO3-→CO3-·+H2O), 由于碳酸自由基与部分有机污染物的反应速率常数大于HO·的反应速率常数, 能够促进这些污染物更快地降解[31].为研究碳酸氢根离子对SMZ光降解的作用, 配制浓度为(1、2、3和4 mmol·L-1)、盐度为30‰的10 μmol·L-1SMZ溶液, 光降解实验结果如图 7.碳酸氢根离子对SMZ的光降解具有轻微促进作用, 随碳酸氢根离子浓度增大, 促进作用减弱.
3 结论(1) 实验所用4种CDOM对SMZ光降解均具有促进作用.当4种CDOM在2mg·L-1的低浓度条件下, JKHA、SRNOM对SMZ间接光降解作用较为显著, 当CDOM浓度达到10mg·L-1时, JKHA、SRNOM对SMZ间接光降解作用远大于SRHA和SRFA.不同来源CDOM对SMZ间接光降解作用的不同主要是由于CDOM组成不同、活性中间体的产生效率不同导致的.
(2) SMZ间接光降解主要由CDOM光降解产生的3CDOM*、·OH、1O2等活性中间体诱发, 不同活性中间体对于SMZ间接光降解的作用不同, 其中, 3CDOM*是SMZ间接光降解的主要贡献者, ·OH亦有贡献, 而1O2在SMZ间接光转化过程中的作用不显著.
(3) 水体pH值影响水体中RIs生成及氧化活性, 当pH为7~9时, SMZ的间接光降解速率变化不明显, 当pH=11时, SMZ的光降解能力显著增强. pH值升高, 有利于RIs的生成和亲电攻击.
(4) 盐度对有机物污染物间接光降解的影响主要来源于离子强度和卤素离子.当盐度从0增大到5‰时, SMZ的光降解速率显著升高, 之后SMZ的光降解速率随着盐度的增大而缓慢增大.硝酸根离子对SMZ光降解的影响不显著.碳酸氢根离子对SMZ的光降解具有轻微促进作用, 随碳酸氢根离子浓度增大, 促进作用减弱.
| [1] | McNeill K, Canonica S. Triplet state dissolved organic matter in aquatic photochemistry:reaction mechanisms, substrate scope, and photophysical properties[J]. Environmental Science:Processes & Impacts, 2016, 18(11): 1381-1399. |
| [2] | Vione D, Minella M, Maurino V, et al. Indirect photochemistry in sunlit surface waters:photoinduced production of reactive transient species[J]. Chemistry:A European Journal, 2014, 20(34): 10590-10606. DOI:10.1002/chem.v20.34 |
| [3] | Remucal C K, Ginder-Vogel M. A critical review of the reactivity of manganese oxides with organic contaminants[J]. Environmental Science:Processes & Impacts, 2014, 16(6): 1247-1266. |
| [4] | Sharpless C M, Blough N V. The importance of charge-transfer interactions in determining chromophoric dissolved organic matter (CDOM) optical and photochemical properties[J]. Environmental Science:Processes & Impacts, 2014, 16(4): 654-671. |
| [5] | Trovó A G, Nogueira R F P, Agüera A, et al. Photodegradation of sulfamethoxazole in various aqueous media:persistence, toxicity and photoproducts assessment[J]. Chemosphere, 2009, 77(10): 1292-1298. DOI:10.1016/j.chemosphere.2009.09.065 |
| [6] | Xu H M, Cooper W J, Jung J, et al. Photosensitized degradation of amoxicillin in natural organic matter isolate solutions[J]. Water Research, 2011, 45(2): 632-638. DOI:10.1016/j.watres.2010.08.024 |
| [7] | Yang W L, Ben Abdelmelek S, Zheng Z, et al. Photochemical transformation of terbutaline (pharmaceutical) in simulated natural waters:degradation kinetics and mechanisms[J]. Water Research, 2013, 47(17): 6558-6565. DOI:10.1016/j.watres.2013.08.029 |
| [8] | Porras J, Bedoya C, Silva-Agredo J, et al. Role of humic substances in the degradation pathways and residual antibacterial activity during the photodecomposition of the antibiotic ciprofloxacin in water[J]. Water Research, 2016, 94: 1-9. DOI:10.1016/j.watres.2016.02.024 |
| [9] | Zhang S Y, Chen J W, Xie Q, et al. Comment on "Effect of dissolved organic matter on the transformation of contaminants induced by excited triplet states and the hydroxyl radical"[J]. Environmental Science & Technology, 2011, 45(18): 7945-7946. |
| [10] | Bahnmüller S, Von Gunten U, Canonica S. Sunlight-induced transformation of sulfadiazine and sulfamethoxazole in surface waters and wastewater effluents[J]. Water Research, 2104, 57: 183-192. |
| [11] | Ryan C C, Tan D T, Arnold W A. Direct and indirect photolysis of sulfamethoxazole and trimethoprim in wastewater treatment plant effluent[J]. Water Research, 2011, 45(3): 1280-1286. DOI:10.1016/j.watres.2010.10.005 |
| [12] | McKay G, Couch K D, Mezyk S P, et al. Investigation of the coupled effects of molecular weight and charge-transfer interactions on the optical and photochemical properties of dissolved organic matter[J]. Environmental Science & Technology, 2016, 50(15): 8093-8102. |
| [13] | Li R, Zhao C, Yao B, et al. Photochemical transformation of aminoglycoside antibiotics in simulated natural waters[J]. Environmental Science & Technology, 2016, 50(6): 2921-2930. |
| [14] | Wenk J, Canonica S. Phenolic antioxidants inhibit the triplet-induced transformation of anilines and sulfonamide antibiotics in aqueous solution[J]. Environmental Science & Technology, 2012, 46(10): 5455-5462. |
| [15] | Kieber R J, Zhou X L, Mopper K. Formation of carbonyl compounds from UV-induced photodegradation of humic substances in natural waters:fate of riverine carbon in the sea[J]. Limnology and Oceanography, 1990, 35(7): 1503-1515. DOI:10.4319/lo.1990.35.7.1503 |
| [16] | Chen Y, Hu C, Hu X X, et al. Indirect photodegradation of amine drugs in aqueous solution under simulated sunlight[J]. Environmental Science & Technology, 2009, 43(8): 2760-2765. |
| [17] | Dubbini A, Censi R, Martena V, et al. Influence of pH and method of crystallization on the solid physical form of indomethacin[J]. International Journal of Pharmaceutics, 2014, 473(1-2): 536-544. DOI:10.1016/j.ijpharm.2014.07.030 |
| [18] | McCabe A J, Arnold W A. Reactivity of triplet excited states of dissolved natural organic matter in stormflow from mixed-use watersheds[J]. Environmental Science & Technology, 2017, 51(17): 9718-9728. |
| [19] | Chen Y, Jiang X, Xiao K K, et al. Enhanced volatile fatty acids (VFAs) production in a thermophilic fermenter with stepwise pH increase-investigation on dissolved organic matter transformation and microbial community shift[J]. Water Research, 2017, 112: 261-268. DOI:10.1016/j.watres.2017.01.067 |
| [20] | Garoma T, Umamaheshwar S K, Mumper A. Removal of sulfadiazine, sulfamethizole, sulfamethoxazole, and sulfathiazole from aqueous solution by ozonation[J]. Chemosphere, 2010, 79(8): 814-820. DOI:10.1016/j.chemosphere.2010.02.060 |
| [21] | Parker K M, Pignatello J J, Mitch W A. Influence of ionic strength on triplet-state natural organic matter loss by energy transfer and electron transfer pathways[J]. Environmental Science & Technology, 2013, 47(19): 10987-10994. |
| [22] | Yang Y, Pignatello J J, Ma J, et al. Comparison of halide impacts on the efficiency of contaminant degradation by sulfate and hydroxyl radical-based advanced oxidation processes (AOPs)[J]. Environmental Science & Technology, 2014, 48(4): 2344-2351. |
| [23] | Formosinho S J, Arnaut L G. Some new perspectives on electron transfer reactions through the intersecting-state model[J]. Journal of Photochemistry and Photobiology A:Chemistry, 1994, 82(1-3): 11-29. DOI:10.1016/1010-6030(93)02000-Y |
| [24] | Assel M, Laenen R, Laubereau A. Ultrafast electron trapping in an aqueous NaCl-solution[J]. Chemical Physics Letters, 1998, 289(3-4): 267-274. DOI:10.1016/S0009-2614(98)00415-1 |
| [25] | Osburn C L, O'Sullivan D W, Boyd T J. Increases in the longwave photobleaching of chromophoric dissolved organic matter in coastal waters[J]. Limnology and Oceanography, 2009, 54(1): 145-159. DOI:10.4319/lo.2009.54.1.0145 |
| [26] | Anastasio C, Newberg J T. Sources and sinks of hydroxyl radical in sea-salt particles[J]. Journal of Geophysical Research, 2007, 112(D10): D10306. |
| [27] | Mack J, Bolton J R. Photochemistry of nitrite and nitrate in aqueous solution:a review[J]. Journal of Photochemistry and Photobiology A:Chemistry, 1999, 128(1-3): 1-13. DOI:10.1016/S1010-6030(99)00155-0 |
| [28] | Wagner I, Strehlow H, Busse G. Flash photolysis of nitrate ions in aqueous solution[J]. Zeitschrift für Physikalische Chemie, 1980, 123(1): 1-33. DOI:10.1524/zpch.1980.123.1.001 |
| [29] | Zafiriou O C, True M B. Nitrite photolysis in seawater by sunlight[J]. Marine Chemistry, 1979, 8(1): 9-32. |
| [30] | Ross F, Ross, A B. Selected specific rates of reactions of transients from water in aqueous solution; Ⅲ Hydroxylradical and perhydroxyl radical ions[M]. NSRDS-NBS 59.National Bureau of Standards, Washington, D.C., US Government Printing Office, 1977. |
| [31] | Lin A Y C, Wang X H, Lee W N. Phototransformation determines the fate of 5-fluorouracil and cyclophosphamide in natural surface waters[J]. Environmental Science & Technology, 2013, 47(9): 4104-4112. |
 2019, Vol. 40
2019, Vol. 40


