2. 中国科学院生态环境研究中心环境水质学国家重点实验室, 北京 100085;
3. 烟台永旭环境保护有限公司, 烟台 265700
2. State Key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China;
3. Yantai Yongxu Environment Protection Co., Ltd., Yantai 265700, China
混凝是水处理过程中常用的工艺, 影响混凝过程的因素包括源水组成[1], 混凝剂的性质[2]等.由于源水受到季节变化等因素的影响而处于不断变化中, 开发经济高效的混凝剂(投加量小, 混凝效果受水质变化影响小)对于提高水处理效果和降低工艺运行的费用具有重要意义[3].
针对某些条件下混凝效果不佳的问题, 主要进行了复合混凝剂的研发[4].混凝的主要作用机制包括电中和, 吸附架桥以及网捕卷扫等[5, 6].常用于开发复合药剂的试剂包括聚丙烯酰胺[7]、聚二甲基二烯丙基氯化铵[8]和聚硅酸[9]等.研究表明阳离子型聚丙烯酰胺助凝剂(CPAM)可吸附水中负电颗粒形成链串进而产生架桥作用, 阴离子型聚丙烯酰胺絮凝剂(APAM)则通过分子链中的极性基团吸附固体悬浮粒子, 使粒子间产生架桥作用或是通过电中和作用使得粒子凝聚而形成大的絮凝物.由于纳米材料具有的特殊性质, 向混凝剂中加入纳米颗粒成为了新的研究方向.聚合氯化铝中加入纳米Fe3O4-SiO2[10]可以增强混凝剂电中和作用从而增强对污染物的去除能力.纳米SiO2-PFS复合絮凝剂对水质pH值适用范围宽, 在处理过程中充分发挥电中和和吸附架桥双重作用, 能够形成更大且易沉降的絮体[11].
综上所述, 目前所用的复合药剂的配制方法中由于用到了有机助凝剂(单体具有毒性[12])或纳米颗粒(水体中有残留带有毒性[13])而面临着一些应用方面的困难, 开发一种环境友好型的复合药剂是研究热点.本文的目的:①研究混凝剂中的阳离子对于不同Al形态的Al系混凝剂混凝过程的影响; ②研究体系中有机物对于含有不同浓度Ca2+混凝剂的混凝过程的影响; ③研究含有Ca2+的混凝剂在不同有机物存在时的混凝过程.
1 材料与方法 1.1 实验仪器六联搅拌仪(梅宇仪器有限公司)用来进行混凝烧杯实验; DOC测定仪(Shimadzu Co., Japan)用来测定混凝后水样的DOC含量; 紫外分光光度计(UV-vis 2910, Hitachi)用来测量混凝剂中铝形态; 电感耦合等离子-原子发射光谱仪(ICP-OES OPTIMA-2000, PerkinElmer, USA)用来测量混凝后水样的余铝含量; 马尔文激光粒度仪(Mastersizer 2000)用来测量混凝过程中的絮体粒径变化; 三维荧光光谱(日立F7000)用来测沉后水有机物组成.
1.2 实验所用的混凝剂及铝型态分布取一定量AlCl3固体于烧杯中, 加入定量蒸馏水, 配制成AlCl3溶液.取一定量的AlCl3溶液在搅拌下缓慢加入碳酸钠粉末至预定碱化度, 静置熟化24 h, 得到实验所需的PACl (聚合氯化铝, 碱化度2.5).混凝剂的Al形态采用Ferron比色法[14]测定, 根据与Ferron反应的动力学分为低聚态Ala、中聚态Alb和高聚态Alc.实验所用混凝剂的Al形态分析结果见表 1.
|
|
表 1 实验所用混凝剂的铝形态分布/% Table 1 Al species distribution for coagulants used in this study/% |
1.3 混凝实验程序
本实验采用500 mL烧杯, 实验程序见表 2.
|
|
表 2 混凝实验程序 Table 2 Parameters for the coagulation experiment |
1.4 储备液的制备
高岭土储备液的制备:称取适量的高岭土颗粒, 用去离子水调和, 并用NaOH溶液调节pH为7.1.在300 r·min-1剪切力下搅拌0.5 h.搅拌过程中适量补加高岭土颗粒和去离子水, 静置24 h, 虹吸法取上半部分, 重量分析法标定高岭土颗粒浓度.
腐殖酸储备液[15](HA)制备:称取1.0 g腐殖酸固体粉末.并加入0.5mol·L-1的NaOH溶液不断搅拌至完全溶解, 制成500 mL储备液调节pH至12, 连续搅拌5 h过0.45 μm膜标定DOC后使用.
蛋白质储备液(BSA)的配制:取一定量的蛋白质固体加入去离子水中, 搅拌24 h过0.45 μm滤膜后标定DOC后使用.
1.5 絮体的强度因子, 恢复因子, 分形维数本实验的混凝过程在500 mL的烧杯中进行.经过10 min慢搅结束后, 提高搅拌速度到200 r·min-1进行5 min的破碎, 破碎后再经过10 min的40 r·min-1的慢搅进行恢复, 利用马尔文激光粒度仪测定混凝过程中的絮体粒径与分形维数.根据先前的研究测定絮体的强度因子(F1)、恢复因子(F2)与分形维数(Df)[16].
1.6 水样的准备本实验水样分为3种, ①纯颗粒物体系:利用高岭土悬浊液母液配制浊度为18.0 NTU的水样; ②纯HA体系:利用HA的母液稀释配制DOC含量为5.0 mg·L-1的HA水样; ③蛋白质与HA混合体系:利用HA与蛋白质的母液配制DOC含量为5.0 mg·L-1的水样, 其中蛋白质与HA的比例为2:3.
2 结果与讨论 2.1 纯颗粒物体系混凝后浊度及余铝变化实验用不同Ca2+浓度改性后混凝剂对纯颗粒物体系进行混凝实验, 混凝后水样剩余浊度以及余铝见图 1.
|
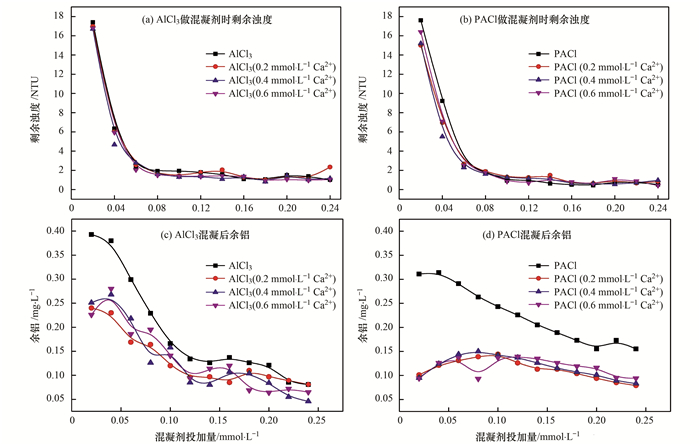
图 1 纯高岭土(浊度18NTU)中不同混凝剂的投加量对混凝过程影响 Fig. 1 Effects of the coagulant dosage on the coagulation performances when the turbidity was adjusted to 18NTU |
图 1(a)和图 1(b)的实验结果表明, 随着混凝剂投加量的增加, 剩余浊度呈现逐渐下降趋势, 混凝剂中的钙离子对于体系剩余浊度无明显影响.有研究表明, 弱碱性条件下钙离子对于高岭土颗粒的团聚无明显作用, 当pH值大于11时可明显增加颗粒的团聚.高岭土表面存在由无机晶体中不平衡取代引起的永久电荷[17]和Al—OH电离形成的负电荷两种电荷.溶液呈碱性时, 电离形成的—AlO—会大量吸附钙离子, 钙离子主要通过与颗粒物或有机物表面的官能团的作用而发挥电中和作用.当pH=8.0时, 少量的Al—OH会发生电离, 其对钙离子的吸附作用下降.通过比较两种混凝剂的混凝过程发现, AlCl3在投加量较低(0.04 mmol·L-1)时浊度去除率较高, 分析原因在于当pH=8.0时, AlCl3中原位形成的Alb含量远高于PACl, 其电中和能力较强[14].混凝剂的作用机制受多种因素的影响, 当投加量较低时, 具有较高Alb含量的AlCl3具有较高的浊度去除率[14, 18].高岭土体系使用不同混凝剂时的余铝实验结果[图 1(c)和图 1(d)]表明, 当投加量较低时, 由于Alc的相对分子质量较Alb的大, 溶解度更低, 因此, 在多数情况下以Alc为优势形态的PACl做混凝剂时的残余铝要低于AlCl3. PACl做混凝剂时, 水中的余铝浓度随着投加量的升高而呈现先上升后下降的过程.分析原因在于投加量较低时, Alc等主要的作用机制是类似静电簇作用[19], 所以其在高岭土颗粒表面的吸附作用会受到表面吸附的Ca2+的影响, 余铝含量升高.
2.2 腐殖酸体系混凝后有机物含量及余铝变化HA作为消毒副产物的重要前驱物, 对于天然水体中的吸附及电子转移过程具有重要的影响, 提高其去除率对于保证混凝效果具有重要的意义.不同混凝剂处理HA体系的DOC含量及余铝变化见图 2.
|
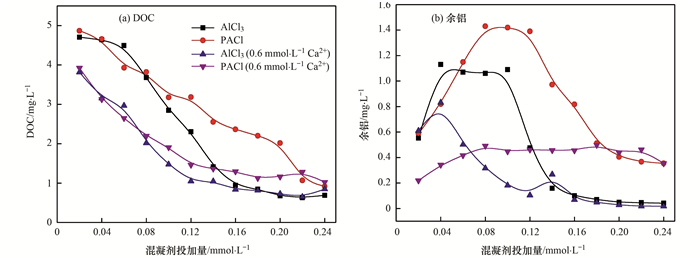
图 2 腐殖酸中不同混凝剂的投加量对有机物含量及余铝的影响 Fig. 2 Effect of different coagulant dosages on the organics content and residual aluminum in the HA system |
由图 2(a)可以发现, 在腐殖酸体系中, 混凝剂中钙离子的存在均有助于腐殖酸絮体的形成, 腐殖酸对水体中的阳离子具有吸附作用, 主要表现为:①钙离子可降低腐殖酸分子的电负性[19]; ②钙离子与腐殖酸中官能团的作用可降低其与Al系混凝剂的作用.以PACl为例, 当混凝剂中无钙离子存在时, 絮体明显形成的投加量为0.22mmol·L-1, 而0.6mmol·L-1钙离子存在时, 絮体明显形成的投加量下降为0.14mmol·L-1.与纯高岭土体系相似, AlCl3形成絮体时的投加量明显低于PACl, 说明AlCl3的电中和能力相比于PACl而言明显增加, 或者是由于腐殖酸体系中的羧基可分解PACl中的Alb, 降低混凝效果[20].通过图 2(b)发现, 低投加量下, 余铝浓度明显增加, 原因是低投加量下铝盐与有机物发生络合反应.此外PACl的余铝含量明显大于AlCl3, 原因在于混凝剂通过两种机制与腐殖酸作用[21], 一是AlCl3带有大量正电荷的Alb与腐殖酸形成Al—HA的共沉物, 此机制在低混凝剂投加量占主要优势, 降低了AlCl3做混凝剂时的余铝浓度, 二是PACl体系中大量的Alc会降低其电中和能力, 有机物的去除率较低.另外, 有钙离子存在时, 余铝浓度明显下降.钙离子的存在降低了腐殖酸分子的负电荷量, 使分子间斥力减小, 从而诱导腐殖酸分子间形成钙离子架桥.对比混凝剂改性前后情况. AlCl3有Ca2+存在时, 余铝含量明显下降, 而PACl有Ca2+时, 余铝含量呈现逐渐上升的趋势(当混凝剂投加量达到0.10 mmol·L-1时, 沉后水余铝浓度超过0.40mg·L-1).分析原因在于, 当使用AlCl3做混凝剂时, 低投加量下, AlCl3的主要作用机制是电中和作用, 故存在的Ca2+可以明显降低余铝浓度, 并可降低—COOH等含氧官能团对于Alb等Al的聚集体的分解作用.而使用PACl做混凝剂时, 低投加量下由于Alc的相对分子质量大于Alb, 故其余铝浓度低于AlCl3做混凝剂[22].
2.3 腐殖酸与蛋白质混合体系有机物含量及余铝变化为进一步研究水体中有机物种类对于DOC去除率的影响, 对BSA与HA混合体系进行实验, 测得剩余DOC含量及余铝浓度见图 3.

|
图 3 腐殖酸与蛋白质混合体系中不同混凝剂的投加量对有机物含量及余铝的影响 Fig. 3 Effect of the coagulant dosage on the organics content and residual aluminum in the HA and BSA systems using different coagulants |
对比图 2(a)与图 3(a)的数据发现, 当体系中有蛋白质存在时, 体系明显形成絮体的投加量(0.12mmol·L-1)低于腐殖酸体系(0.16mmol·L-1).分析原因:在pH=8.0时, 蛋白质分子的电荷量低于腐殖酸, 故混凝剂投加量相比于纯腐殖酸体系下降.官能团的种类与浓度对于混凝效果具有重要的作用, 提高有机物含氧官能团的浓度, 可增强钙离子与含氧官能团络合作用[23].当富氧官能团的浓度水平有显著提高时, 钙离子与水中DOM的络合作用增强.且钙离子可中和有机物颗粒表面负电荷, 通过中和表面电荷降低颗粒稳定性.与腐殖酸相比, 蛋白质分子中含有大量的含氮官能团, 这些官能团的存在会显著降低钙离子的影响, 故钙离子的存在对于混凝后DOC含量无明显影响.由图 3(b)的实验结果可以发现, 随着混凝剂投加量的增加, 余铝浓度呈现逐渐上升的趋势.相比于HA体系而言, 使用PACl+Ca2+做混凝剂, 投加量较低时余铝浓度大于纯HA体系, 进一步证实了Alc在低投加量下的静电簇作用机制[24]会明显受到Ca2+的影响.而当体系中有BSA存在时, 一方面蛋白质会与HA结合降低HA分子的电负性, 降低混凝剂的投加量.另一方面, 含氧官能团的减少进一步影响Alc的静电簇作用, 增大了体系的余铝浓度(当Ca2+存在时更为明显).
2.4 混凝剂中的钙离子对混凝过程絮体粒度的影响为研究钙离子对不同混凝剂混凝过程中絮体粒度变化的影响, 实验在高岭土体系中进行, AlCl3和PACl投加量为0.10mmol·L-1(以Al计), 钙离子浓度为0.6mmol·L-1, 测定絮体的粒径和扫描电镜, 其结果见图 4.
|
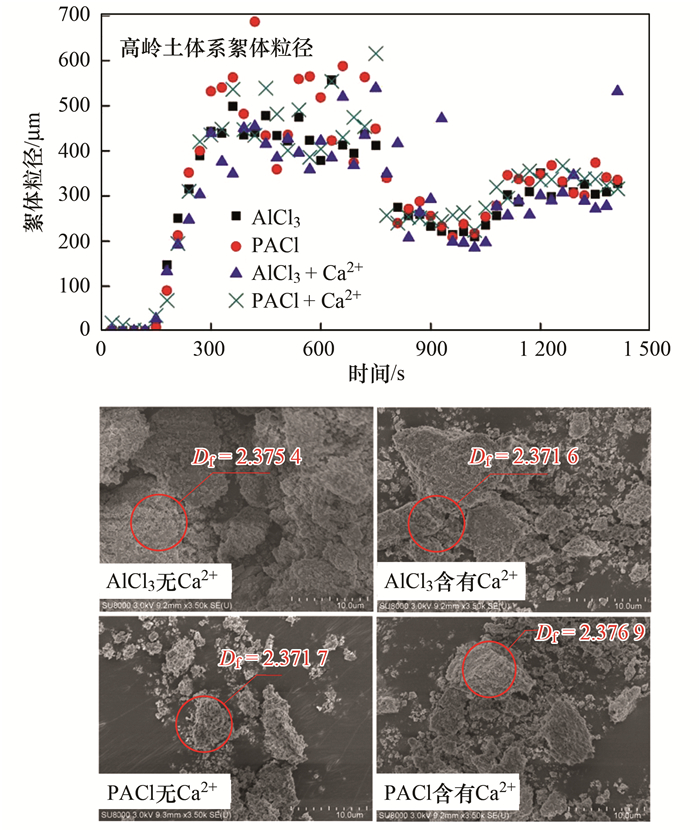
图 4 纯高岭土体系中钙离子对混凝过程絮体粒度的影响 Fig. 4 Effect of the calcium ion on the floc size during the coagulation process in the Kaolin system |
通过图 4可以发现, 不同混凝剂形成的絮体粒径没有明显区别, 且不同混凝剂形成的絮体紧密疏散程度以及分形维数几乎维持不变, 当混凝剂中加入钙离子时絮体紧密程度同样无明显变化, 原因在于在pH=8.0时高岭土表面络合形成的Al—OH几乎很少电离, 钙离子不能与高岭土表面的AlO—进行络合反应[25].
实验在纯腐殖酸体系, AlCl3和PACl投加量为0.16mmol·L-1(为与混合有机物体系对比), 钙离子浓度为0.6mmol·L-1条件下测定絮体的粒径和扫描电镜, 实验结果如图 5.
|
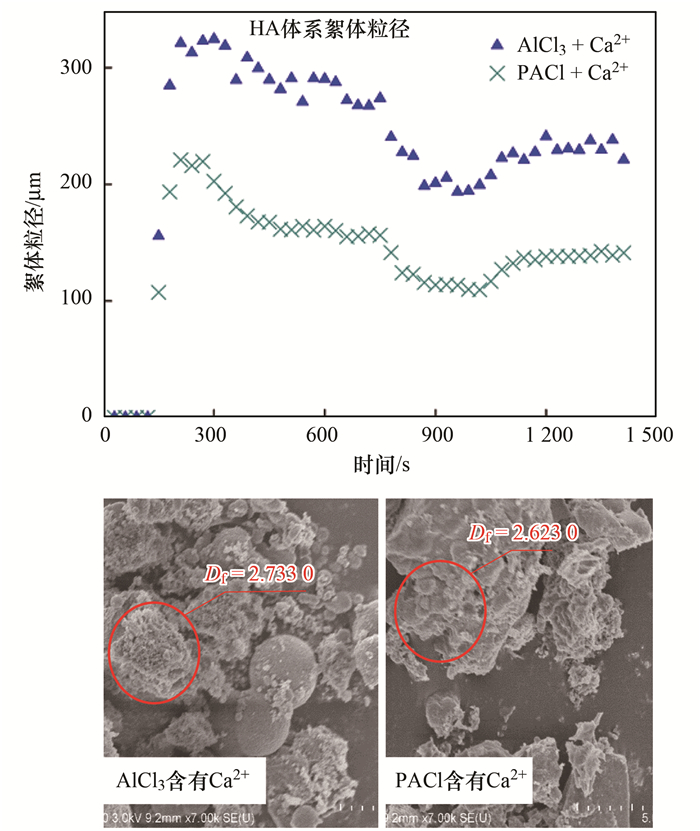
图 5 腐殖酸体系中钙离子对混凝过程絮体粒度的影响 Fig. 5 Effect of the calcium ion on the floc size during the coagulation process in humic acid |
通过图 5可以发现, 两种混凝剂投加量为0.16mmol·L-1, 无钙离子存在的情况下均无絮体生成, 当两种混凝剂投加0.6mmol·L-1的Ca2+时, PACl和AlCl3混凝过后均可形成明显絮体, 这是由于腐殖酸分子自身带有大量负电荷, 引入钙离子一方面可以压缩腐殖酸表面双电层, 减小分子间斥力, 促进分子间凝聚, 同时钙离子能够和腐殖酸表面的羟基发生络合, 形成阳离子桥, 促进絮体生成.此外钙离子存在时AlCl3生成的絮体粒径明显大于PACl(170 μm), 在实验pH值下, AlCl3生成Alb的含量远大于PACl中自身的Alb, 在腐殖酸的混凝过程中电中和作用为主要机制, 故AlCl3形成的絮体粒度较大(280 μm).分形维数的实验结果表明, AlCl3所形成絮体分形维数大于PACl形成絮体分形维数, 形成的絮体更加紧密, 这是由于PACl的主要作用机制是架桥以及网捕卷扫作用, 故形成的絮体分型维数小.实验进一步计算了两种混凝剂的强度因子与恢复因子, 结果见表 3, 通过对比可以发现, PACl的强度因子较高, 这是因为在PACl中有大量稳定存在的Alc, 网捕卷扫作用增加了絮体强度.
|
|
表 3 腐殖酸水样中混凝过程中絮体的强度因子(F1)和恢复因子(F2) Table 3 Strength factor (F1) and recovery factor (F2) of flocs formed during coagulation processes in the HA system |
为了进一步与混合有机物体系对比, 本实验在腐殖酸和蛋白质混合溶液中, AlCl3和PACl投加量为0.16mmol·L-1, 钙离子浓度为0.6mmol·L-1条件下测定絮体的粒径和扫描电镜, 结果见图 6.

|
图 6 腐殖酸与蛋白质混合溶液中钙离子对混凝过程絮体粒度的影响 Fig. 6 Effect of the calcium ion on the floc size in a mixed solution of humic acid and protein |
图 6的实验结果表明, 在混合有机物体系中, AlCl3形成絮体粒度大于PACl, 分析原因在于混凝是多种作用机制同时作用的结果, PACl中电中和能力的缺失使得絮体粒度明显下降. AlCl3加入钙离子后对于絮体粒度无明显影响, 原因在于蛋白质携带负电荷相比纯腐殖酸低(且蛋白质的存在降低了体系中含氧官能团的数量), 大量高正电荷的Alb足以中和有机物表面负电荷形成聚集体. PACl由于主要作用机制是网捕和卷扫作用, 此时存在的钙离可明显增强电中和作用, 有效降低体系的负电荷, 有助于絮体的形成.进一步计算强度因子与恢复因子, 结果见表 4.
|
|
表 4 腐殖酸与蛋白质混合水样中混凝过程中絮体的强度因子(F1)和恢复因子(F2) Table 4 Strength factor (F1) and recovery factor (F2) of flocs formed in the mixed solution of HA and BSA |
分析表 4的数据可以发现, 加入钙离子后AlCl3形成絮体强度因子变小, 恢复因子增大.分析原因在于AlCl3做混凝剂时钙离子主要是增大了电中和能力. PACl的主要作用机制是网捕卷扫作用, 此时存在的钙离子会影响此作用机制(吸附在有机物分子表面的钙离子会影响高聚合态Al聚集体的作用), 故有钙离子存在时恢复因子下降; 而对于强度因子而言, 两种混凝剂有钙离子存在时强度因子明显下降, 说明了钙离子的主要作用机制是增加了电中和作用.
2.5 蛋白质和腐殖酸混合液中有机物三维荧光(3D-EEM)分析为详细了解Ca2+存在下有机物去除情况, 实验在两种混凝剂投加量为0.12 mmol·L-1时加入0.6 mmol·L-1 Ca2+进行EEM图谱扫描, 结果见图 7.
|
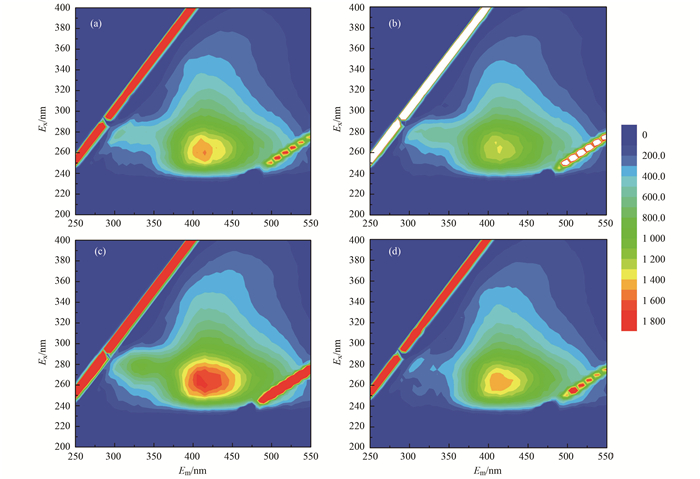
(a)AlCl3无Ca2+; (b)AlCl3含有Ca2+; (c)PACl无Ca2+; (d)PACl含有Ca2+ 图 7 不同混凝剂形成的EEM图谱 Fig. 7 EEM patterns formed by different coagulants |
通过图 7的实验结果可以发现, 同等混凝剂投加量下AlCl3相比于PACl具有较高的有机物去除率.当有钙离子加入时, 两种混凝剂去除有机物的效果均有提高, 荧光图谱在发射波长430 nm, 激发波长265 nm处响应值(此响应值处有机物为腐殖酸, 见表 5)明显降低.为进一步确定混凝剂是否针对体系中有机物进行了针对性去除, 实验进行EEM图谱[26]区域整合(计算各有机物含量的变化), 结果见表 6.
|
|
表 5 腐殖酸与蛋白质混合水样中荧光响应值1) Table 5 Response value of 3DEEM under HA and BSA conditions |
|
|
表 6 腐殖酸与蛋白质混合水样中混凝过程中有机物成分相对占比 Table 6 Relative proportion of organic matter in the coagulation process of an HA and BSA mixed water sample |
通过表 6发现, 与原始水样相比, 混凝后水样中腐殖酸与蛋白质相对含量比值发生明显上升(原始水样比值为1.5), 这说明AlCl3与PACl在混合有机物体系中对蛋白质有针对性去除, 达到去除有机物的目的.另外, 当钙离子存在时水中残余有机物腐殖酸蛋白质比值上升, 有研究表明:腐殖酸和蛋白质的混合液中引入盐溶液, 使腐殖酸与蛋白质的疏水作用相对大于静电斥力[27], 腐殖酸进一步包裹在蛋白质表面, 说明钙离子降低了蛋白质的亲水性, 使得体系中有机物发生团聚.
2.6 pH对不同混凝剂不同水体混凝效果影响由于混凝过程的复杂性, 水体pH值对于改性前后混凝剂混凝过程有重要影响, 实验对纯颗粒物体系在不同pH值条件下采用最优投加量(混凝剂投加量0.10mmol·L-1, Ca2+浓度0.6mmol·L-1)进行烧杯实验, 结果见图 8.

|
图 8 纯高岭土体系中不同pH值对混凝过程浊度和余铝的影响 Fig. 8 Effect of different pH values on the turbidity and residual aluminum in the Kaolin system |
选择的混凝剂投加量在体系pH值为8.0时达到较好的浊度去除率, 故当pH值较低时, Alc的静电簇作用受到抑制, 其混凝作用机制受到影响.当pH值较低时, 体系越易达到网捕卷扫阶段, 故使用AlCl3做混凝剂时仍能保持较高的浊度去除率.此外, 两种混凝剂中投加的钙离子对于浊度的去除及剩余铝浓度没有明显影响, 这与2.1节结论相符.本实验考察了纯腐殖酸体系在最优投加量(混凝剂投加量0.16mmol·L-1, Ca2+浓度0.6mmol·L-1)不同pH条件下剩余DOC浓度以及余铝浓度, 实验结果见图 9.
|
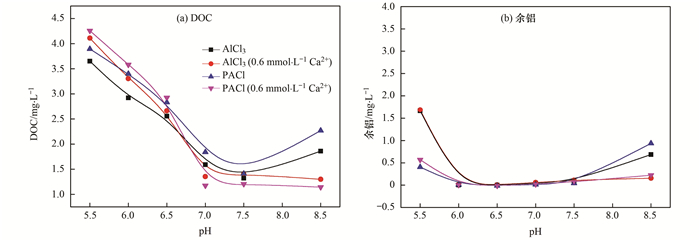
图 9 纯腐殖酸体系中不同pH对混凝过程DOC和余铝的影响 Fig. 9 Effect of different pH values on the DOC and residual aluminum in the HA system |
不同pH值条件下余铝的实验结果表明, 在中性条件下, 沉后水余铝浓度达到最低, 而在酸性或碱性条件下, 余铝浓度均明显上升, 分析原因在于pH值影响混凝剂中的Al形态, 从而造成酸性或碱性条件下余铝浓度升高.在pH=8.5时, Ca2+的存在有助于沉后水中余铝浓度的下降, 在pH=5.5时, 由于PACl的Al形态稳定性, 其余铝浓度低于AlCl3.
图 9(a)实验结果表明:弱碱条件下纯腐殖酸体系中两种改性混凝剂对于DOC的去除率比未改性混凝剂提高10%~20%.余铝降低0.7~1.0mg·L-1.随pH值减小, 钙离子作用减弱, 余铝以及DOC浓度提高.分析原因:一方面在酸性条件下, 大量氢离子抑制—COOH发生水解, 腐殖酸分子无法与Al系混凝剂形成Al—HA共聚体.造成腐殖酸去除率低, 同时DOC以及余铝浓度出现上升趋势; 另一方面酸性条件下, 钙离子无法诱导腐殖酸中官能团形成钙离子架桥, 腐殖酸分子间相互聚集作用减弱.体系中难以形成大聚集体, 水中腐殖酸分子无法沉淀.同时, 当改变体系pH值时, PACl做混凝剂DOC及余铝浓度变化相对较小, 这是由于PACl碱化度高使得PACl中的Al形态相对稳定[14].
由于实际水体中有机物种类复杂, 本研究对混合有机物体系采用最优投加量(混凝剂投加量0.12mmol·L-1, Ca2+浓度0.6mmol·L-1)进行混凝烧杯实验, 考察了有机物以及余铝指标, 结果见图 10.
|
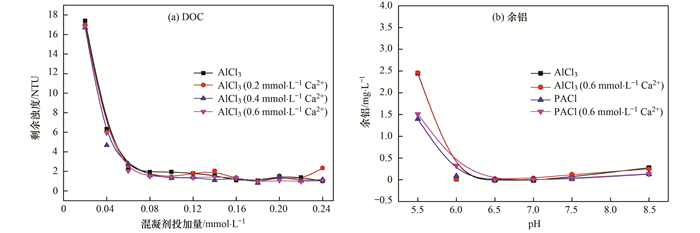
图 10 腐殖酸蛋白质混合体系中不同pH对混凝过程DOC和余铝的影响 Fig. 10 Effect of different pH values on the DOC and residual aluminum in the HA and BSA systems |
对比图 10(a)与图 9(a)实验结果:碱性条件(pH=8.5)下改性后混凝剂混合有机物体系较纯腐殖酸DOC浓度降低0.5~1.0mg·L-1、余铝降低0.2~0.6mg·L-1.分析原因在于蛋白质电负性较低, 混凝剂电中和作用更充分. 图 10(a)中碱性条件下改性后混凝剂DOC降低0.2~0.4mg·L-1, 这是由于Ca2+的存在使得腐殖酸与蛋白质的疏水作用减弱, 进一步发生团聚.随着pH降低DOC去除率降低, 分析原因在于酸性条件(pH=5.5)下腐殖酸的水解作用受到影响, Ca2+与腐殖酸结合受到影响.
3 结论(1) 混凝剂中钙离子在纯高岭土体系中对浊度的去除无明显作用, 但是能够有效控制出水余铝.低投加量下, 对比未改性混凝剂余铝含量可降低0.05mg·L-1.
(2) 在纯HA体系中, pH=8时, 混凝剂中的钙离子可以有效提高有机物的去除效率, 混凝剂投加量为0.08mmol·L-1时出水余铝浓度可降低0.7~0.9mg·L-1, DOC浓度降低1.5~1.8mg·L-1. AlCl3和PACl经过钙离子改性后, 前者DOC浓度较改性后PACl降低0.2mg·L-1.
(3) 在HA和BSA混合有机物体系中, pH=8时, 钙离子能够促进絮体形成, 改性后混凝剂同等投加量(0.12 mm·L-1)下对比纯HA体系, DOC浓度降低0.2~0.5mg·L-1, 絮体粒径明显变大.对比未改性混凝剂, 改性后混凝剂有机物去除量在低投加量(0.02mmol·L-1)可提高0.7~1.0mg·L-1.
(4) 混凝剂在pH为8.5时, Ca2+存在可促进混凝效果, DOC降低0.2~0.6mg·L-1, 余铝降低0.4~0.7mg·L-1.酸性条件下, 钙离子对于混凝过程的影响减弱.
(5) 混凝过程中, 水体中的官能团的种类、数量对于有机物的去除有重要作用.钙离子能够与羧基、羟基等含氧官能团络合提高有机物去除效率.
| [1] |
周玲玲, 张永吉, 叶河秀, 等. 强化混凝对腐殖酸和富里酸去除对比研究[J]. 环境科学, 2012, 33(8): 2680-2684. Zhou L L, Zhang Y J, Ye H X, et al. Comparison study of enhanced coagulation on humic acid and fulvic acid removal[J]. Environmental Science, 2012, 33(8): 2680-2684. |
| [2] |
张大为, 徐慧, 王希, 等. 藻形态及混凝剂组成对混凝-超滤过程的影响[J]. 环境科学, 2017, 38(8): 3281-3289. Zhang D W, Xu H, Wang X, et al. Effects of algal morphology and Al species distribution on the coagulation-ultrafiltration process[J]. Environmental Science, 2017, 38(8): 3281-3289. |
| [3] |
徐磊, 俞文正, 梁亮, 等. 天然有机物对混凝效果影响机制及絮体特性分析[J]. 环境科学, 2013, 34(11): 4290-4294. Xu L, Yu W Z, Liang L, et al. Effect of natural organic matter on coagulation efficiency and characterization of the flocs formed[J]. Environmental Science, 2013, 34(11): 4290-4294. |
| [4] |
贺建栋, 刘鹏宇, 常青, 等. PAC与PDMDAAC复合混凝剂去除高浊度水中有机氯[J]. 中国环境科学, 2016, 36(6): 1738-1745. He J D, Liu P Y, Chang Q, et al. Efficiency of the PAC-PDMDAAC composite coagulant for eliminating the organochlorines in high-turbidity water[J]. China Environmental Science, 2016, 36(6): 1738-1745. DOI:10.3969/j.issn.1000-6923.2016.06.020 |
| [5] | Jiao R Y, Fabris R, Chow C W K, et al. Influence of coagulation mechanisms and floc formation on filterability[J]. Journal of Environmental Sciences, 2017, 57: 338-345. DOI:10.1016/j.jes.2017.01.006 |
| [6] |
骆丽宁, 王丽娟, 杨敏, 等. 胞外物质影响铁盐混凝除铜绿微囊藻的效能与机制[J]. 环境科学学报, 2018, 38(2): 437-442. Luo L N, Wang L J, Yang M, et al. Effect and mechanism of extracellular substances on removal of Microcystis aeruginosa by ferric salt coagulation[J]. Acta Scientiae Circumstantiae, 2018, 38(2): 437-442. |
| [7] |
杨博, 孙宾宾. 聚丙烯酰胺合成研究进展[J]. 当代化工, 2017, 46(2): 286-288. Yang B, Sun B B. Research progress in the synthesis of polyacrylamide[J]. Contemporary Chemical Industry, 2017, 46(2): 286-288. DOI:10.3969/j.issn.1671-0460.2017.02.027 |
| [8] |
李佼佼, 胡琼璨, 张伟锋, 等. 聚二甲基二烯丙基氯化铵的合成及其絮凝性能研究[J]. 精细化工中间体, 2015, 45(3): 70-72. Li J J, Hu Q C, Zhang W F, et al. Synthesis and flocculational performance of polydimethyldiallylammonium chloride[J]. Fine Chemical Intermediates, 2015, 45(3): 70-72. |
| [9] |
赵园园, 张玥, 李素英, 等. 聚硅酸对不同形态铝沉积行为的影响[J]. 环境科学, 2016, 37(10): 3870-3876. Zhao Y Y, Zhang Y, Li S Y, et al. Effect of polysilicic acid on the deposition behavior of different aluminum species[J]. Environmental Science, 2016, 37(10): 3870-3876. |
| [10] | Zhang M, Xiao F, Xu X Z, et al. Novel ferromagnetic nanoparticle composited PACls and their coagulation characteristics[J]. Water Research, 2012, 46(1): 127-135. DOI:10.1016/j.watres.2011.10.025 |
| [11] |
张承飞, 褚玉芬, 李顺武. 纳米复合絮凝剂用于低温低浊水的混凝研究[J]. 水资源与水工程学报, 2010, 21(3): 70-72. Zhang C F, Chu Y F, Li S W. Nano-composite flocculent for the coagulation of low temperature and low turbidity water[J]. Journal of Water Resources & Water Engineering, 2010, 21(3): 70-72. |
| [12] | 王国瑀.聚丙烯酰胺凝胶低毒性替代材料研究[D].北京: 北京化工大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10010-1016323285.htm |
| [13] | Hou J, Wang X X, Hayat T, et al. Ecotoxicological effects and mechanism of CuO nanoparticles to individual organisms[J]. Environmental Pollution, 2017, 221: 209-217. DOI:10.1016/j.envpol.2016.11.066 |
| [14] | Wang D S, Sun W, Xu Y, et al. Speciation stability of inorganic polymer flocculant-PACl[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2004, 243(1-3): 1-10. |
| [15] | Wei J C, Gao B Y, Yue Q Y, et al. Comparison of coagulation behavior and floc structure characteristic of different polyferric-cationic polymer dual-coagulants in humic acid solution[J]. Water Research, 2009, 43(3): 724-732. DOI:10.1016/j.watres.2008.11.004 |
| [16] | Jarvis P, Jefferson B, Parsons S A. Breakage, regrowth, and fractal nature of natural organic matter flocs[J]. Environmental Science & Technology, 2005, 39(7): 2307-2314. |
| [17] | Konan K L, Peyratout C, Bonnet J P, et al. Surface properties of kaolin and illite suspensions in concentrated calcium hydroxide medium[J]. Journal of Colloid and Interface Science, 2007, 307(1): 101-108. DOI:10.1016/j.jcis.2006.10.085 |
| [18] |
曾继军, 齐敦哲, 武仁超, 等. 高效聚合氯化铝应用条件与复合混凝剂的协同优化研究[J]. 供水技术, 2017, 11(6): 5-10. Zeng J J, Qi D Z, Wu R C, et al. Application of purificated Al13 and the investigation of coagulation performances using composite coagulants[J]. Water Technology, 2017, 11(6): 5-10. DOI:10.3969/j.issn.1673-9353.2017.06.002 |
| [19] | Wall N A, Choppin G R. Humic acids coagulation:influence of divalent cations[J]. Applied Geochemistry, 2003, 18(10): 1573-1582. DOI:10.1016/S0883-2927(03)00046-5 |
| [20] |
霍进彦, 赵鹏, 张宏伟, 等. 基于非对称场流分离技术的水环境腐殖酸聚集特性研究[J]. 环境科学学报, 2016, 36(8): 2899-2904. Huo J Y, Zhao P, Zhang H W, et al. The study of aggregation properties of aqueous humic acid based on asymmetric flow field-flow fractionation[J]. Acta Scientiae Circumstantiae, 2016, 36(8): 2899-2904. |
| [21] | Kazpard V, Lartiges B S, Frochot C, et al. Fate of coagulant species and conformational effects during the aggregation of a model of a humic substance with Al13 polycations[J]. Water Research, 2006, 40(10): 1965-1974. DOI:10.1016/j.watres.2006.03.014 |
| [22] |
肖辉煌, 张盼月, 曾光明, 等. 多核聚合形态Al30混凝控制水中腐殖酸与残留铝的研究[J]. 安全与环境学报, 2007, 7(4): 16-19. Xiao H H, Zhang P Y, Zeng G M, et al. Ways to control humic acid and residual aluminum in water by means of coagulation with polynuclear species Al30[J]. Journal of Safety and Environment, 2007, 7(4): 16-19. DOI:10.3969/j.issn.1009-6094.2007.04.005 |
| [23] | Wadhawan T, Simsek H, Kasi M, et al. Dissolved organic nitrogen and its biodegradable portion in a water treatment plant with ozone oxidation[J]. Water Research, 2014, 54: 318-326. DOI:10.1016/j.watres.2014.02.009 |
| [24] | Zhang P Y, Wu Z, Zhang G M, et al. Coagulation characteristics of polyaluminum chlorides PAC-Al30 on humic acid removal from water[J]. Separation & Purification Technology, 2008, 63(3): 642-647. |
| [25] |
闵凡飞, 赵晴, 李宏亮, 等. 煤泥水中高岭土颗粒表面荷电特性研究[J]. 中国矿业大学学报, 2013, 42(2): 284-290. Min F F, Zhao Q, Li H L, et al. Study of electrokinetic properties of kaolinite in coal slime[J]. Journal of China University of Mining & Technology, 2013, 42(2): 284-290. |
| [26] | Baker A. Fluorescence excitation?emission matrix characterization of some sewage-impacted rivers[J]. Environmental Science & Technology, 2001, 35(5): 948-953. |
| [27] | 李艳.土壤腐殖酸与酶蛋白相互作用的机制[D].武汉: 华中农业大学, 2013. |
 2019, Vol. 40
2019, Vol. 40


