2. 浙江工业大学环境学院, 杭州 310032
2. College of Environment, Zhejiang University of Technology, Hangzhou 310032, China
磷作为水生生物生长的一个主要限制性因子, 对地表水体富营养化的进程起到至关重要的作用, 因此降低地表水体上覆水中磷的浓度有助于水体富营养化的防治[1~3].地表水体上覆水中磷既可以是来自外源性磷源, 也可以是来自内源性磷源即底泥磷的释放.当外源性磷源的输入被有效控制之后, 底泥内源磷的释放对上覆水中磷的浓度水平有着不可忽视的影响, 并且仍然可以使地表水体富营养化的状况持续很长一段时间[1, 4].因此, 控制底泥磷的释放, 对于水体富营养化的治理是非常必要的.
当前, 国内外的底泥磷释放控制技术主要包括底泥疏浚[5]、硝酸盐原位处理[6]、曝气供氧[7]、水生植物法[8]、原位覆盖[9~11]以及吸附剂原位钝化[12~14]等.其中, 吸附剂原位钝化技术, 即将吸附剂添加进底泥中作为底泥磷钝化剂, 利用吸附剂的固磷能力增强底泥对磷的吸附能力并降低底泥中磷的释放风险, 近年来得到了研究人员的广泛关注.目前, 已经引起国内外研究人员注意的底泥磷钝化剂有镧改性膨润土[12~14]、给水处理厂废弃铁铝泥[13~15]、热改性富钙凹凸棒土[16]、镧改性沸石[17]、锆改性沸石[18]、锆改性黏土[19]和磁性微粒[20, 21]等.这其中大部分的底泥磷钝化剂为非磁性固体材料, 而对于非磁性的底泥磷钝化剂而言, 它们应用后很难将其从水体中回收回来.这样导致的后果就是, 一方面底泥钝化剂仍然位于底泥中, 当外界环境条件变化时被底泥磷钝化剂所固定的磷可能存在再次释放的风险, 从而降低了吸附剂原位钝化技术的固磷效率, 另一方面底泥磷钝化剂的一次性使用不符合可持续发展的理念[20, 21].而磁性的底泥磷钝化剂有望克服非磁性底泥磷钝化剂的上述缺点, 可能比非磁性底泥磷钝化剂更适合用于底泥磷释放的控制[20, 21].
底泥对水中磷的吸附作用会显著影响底泥与上覆水之间磷的交换, 而底泥特性则会显著影响底泥对磷的吸附作用, 进而影响底泥磷向上覆水的迁移转化过程[2].将磁性的底泥磷钝化剂添加进底泥中后, 底泥的特性预计将会发生改变, 进而底泥对水中磷的吸附作用预计将会随之发生改变, 最终底泥中磷向上覆水体的释放速率预计会极大地降低.因此, 了解磁性吸附剂改良底泥对水中磷的吸附作用, 对于应用磁性吸附剂作为底泥改良剂控制底泥磷释放而言是非常重要的.目前国内外关于底泥对水中磷吸附作用的研究较多[22~25], 但是关于磁性吸附剂改良底泥对水中磷吸附作用的研究却鲜见报道.
有研究表明, 四氧化三铁(Fe3O4)改性沸石不仅具备较强的磁分离能力, 而且对水中磷酸盐具备较强的吸附能力[26].本文的目标就是研究Fe3O4改性沸石改良河道底泥对水中磷酸盐的吸附作用, 以期为应用Fe3O4改性沸石作为底泥磷钝化剂控制河道内源磷释放提供帮助.为此, 本文以重污染河道底泥为研究对象, 通过批量吸附实验首先考察原始和Fe3O4改性沸石改良底泥对水中磷酸盐的吸附动力学和等温线, 然后考察反应温度、离子强度、溶液pH值和溶液共存电解质对原始和Fe3O4改性沸石改良底泥吸附水中磷酸盐的影响, 再通过磷形态连续分级提取法考察被Fe3O4所吸附磷酸盐的磷形态分布特征, 最终阐明Fe3O4改性沸石改良底泥对水中磷酸盐的吸附作用.
1 材料与方法 1.1 实验材料本研究所用到的底泥是从上海市金山工业区红光村一条重污染河道所采集的.河道的底泥被采集上来之后立即运送至实验室平铺使之自然风干, 然后经破碎, 过0.075 mm孔径筛过滤筛分, 所得到的底泥样品装入自封袋进行保存, 以待后续的理化性质分析和模拟实验研究所用.经分析确定该底泥的pH值为7.29, 有机质含量为3.72%, 总磷含量为986 mg ·kg-1, NH4Cl-P(弱吸附态磷)含量为23.0 mg ·kg-1, BD-P(氧化还原敏感态磷)含量为250 mg ·kg-1, NaOH-rP(金属氧化物结合态磷)含量为99.8 mg ·kg-1, NaOH-nrP(有机磷)含量为130 mg ·kg-1, HCl-P(钙结合态磷)含量为426 mg ·kg-1.本研究所用到的化学试剂, 包括FeCl3 ·6H2O、FeSO4 ·7H2O、NaOH、KH2PO4、NaCl、KCl、CaCl2、MgCl2、NaHCO3、Na2SO4和HCl, 均是从中国国药集团化学试剂有限公司所采购的, 均为分析纯试剂.实验所用到的磷储备液采用KH2PO4配制, 浓度以元素磷计, 将磷储备液采用去离子进行稀释制备得到实验所用的磷使用液.本研究所用到的原始沸石源自浙江省缙云县神石矿业有限公司, 它的主要矿物成分为斜发沸石、丝光沸石和石英, 它们的质量分数分别为52%、16%和32%.由此可见, 本研究所用的原始沸石不是纯的斜发沸石或者丝光沸石, 而是它们的复合物. Fe3O4改性沸石(magnetite-modified zeolite, MZ)的详细制备过程采见文献[26].简言之, 将5 g天然沸石与250 mL浓度为0.2 mol ·L-1的Fe3+溶液和250 mL浓度为0.1 mol ·L-1的Fe2+溶液进行混合, 再置于70℃振荡器中进行振荡反应; 反应30 min后, 向上述悬浮物液中加入2 mol ·L-1的NaOH溶液直至溶液的pH值达到10, 并继续反应60 min; 随后通过磁分离的方式获得固体材料, 再对所获得的固体材料进行清洗、烘干和研磨后最终得到MZ[26].
1.2 实验方法 1.2.1 改良底泥制备精确称量30 g所采集底泥加入到锥形瓶中, 再向该锥形瓶中加入3 g制备得到的Fe3O4改性沸石材料, 并与原始底泥进行混合均匀, 然后向该锥形瓶中加入100 mL浓度为0.02 mol ·L-1的KCl溶液; 将放入全部材料后的锥形瓶放到恒温水浴振荡器中, 以25℃的反应温度和150 r ·min-1的振荡频率反应24 h; 反应结束后从锥形瓶中取出湿底泥材料, 经过滤收集、自然风干、研磨后即制备得到Fe3O4改性沸石改良底泥(Fe3O4改性沸石与底泥的质量比为10%, 表示为10% MZ).
1.2.2 吸附实验运用吸附实验的方法, 研究不同初始磷浓度、反应时间、反应温度、溶液pH值、离子强度和共存阴阳离子条件下原始底泥和Fe3O4改性沸石改良底泥对水中磷酸盐的吸附特征.典型的实验步骤为:移取20 mL预先配制的磷溶液放置到锥形瓶中, 并加入质量为0.1 g的原始或改良底泥(低初始磷浓度影响除外), 再将该锥形瓶放到恒温水浴振荡器中振荡一段时间(以一定的反应温度和200 r ·min-1的振荡频率); 振荡反应结束后取出该锥形瓶, 然后对该锥形瓶中的混合液进行离心分离, 并使用钼锑抗分光光度法测定上清液中残留的磷浓度.本研究每组实验设置2个平行.
吸附动力学研究的实验条件设置为:初始磷浓度5 mg ·L-1; pH值7;反应时间0.25、0.5、1、2、4、6、8、14、18、24、36和48 h; 反应温度25℃.低浓度等温吸附研究的实验条件设置:初始磷浓度分别为0、0.1、0.2、0.3、0.4和0.5 mg ·L-1, 底泥投加量为0.2 g, pH值为7, 反应时间为24 h, 反应温度为25℃; 高浓度等温吸附研究的实验条件设置:初始磷浓度分别为2、5、8、10、12和15 mg ·L-1, 底泥投加量为0.1 g, pH值为7, 反应时间为24 h, 反应温度为25℃; 反应温度影响研究的实验条件设置:初始磷浓度为10 mg ·L-1, pH值为7, 反应时间为24 h, 反应温度分别为15、25和35℃. pH值影响研究的实验条件设置:初始磷浓度为5 mg ·L-1, pH值分别为4、5、6、7、8、9、10和11, 反应时间为24 h, 反应温度为25℃.离子强度和共存阴阳离子影响研究的实验条件设置:初始磷浓度为5 mg ·L-1, pH值为7, 反应时间为24 h, 反应温度为25℃, 离子强度影响研究时采用NaCl调节磷溶液的离子强度, NaCl浓度分别0、2、10、20、50和100 mmol ·L-1, 阴阳离子影响研究时磷溶液中NaCl、KCl、CaCl2、MgCl2、Na2SO4或NaHCO3浓度均为2 mmol ·L-1.
未改良和改良底泥对水中磷酸盐的单位吸附量(Q, mg ·kg-1)采用以下公式进行计算:
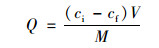
|
(1) |
式中, ci和cf分别为吸附反应前后水中磷酸盐的浓度, mg ·L-1; V为磷酸盐溶液的体积, L; M为底泥投加量, kg.
1.2.3 磷形态分步提取首先通过Fe3O4改性沸石改良底泥与磷溶液之间的反应获得吸附磷酸盐后的Fe3O4改性沸石改良底泥, 即将1.1 g改良底泥与1 L磷酸盐溶液(初始磷浓度为20 mg ·L-1, pH值为7)混合并反应24 h, 改良底泥自然风干后采用磁铁将Fe3O4从改良底泥中回收回来, 随后分别称取2份等质量(10 mg)的Fe3O4置于离心管中, 再分别采用:①NH4Cl溶液(1 mol ·L-1); ②NaHCO3/Na2S2O4(浓度均为0.11 mol ·L-1); ③25℃NaOH(1 mol ·L-1); ④HCl溶液(0.5 mol ·L-1)和⑤85℃NaOH(1 mol ·L-1)进行逐级提取.第①、②、④和⑤步提取所获得的溶液均采用离心分离的方式进一步得到上清液, 然后采用钼酸盐比色法测定上清液中磷浓度, 所得到的磷分别为NH4Cl-P、BD-P、HCl-P和Res-P.第③提取步骤中, 所提取的溶液采用离心分离方式获得上清液, 再将其分为两份, 一份直接采用钼酸盐比色法测定上清液中磷浓度, 所得到的磷为NaOH-rP, 另一份采用过硫酸钾消解, 并采用钼酸盐比色法测定上清液中总磷浓度, 所得到的磷为NaOH提取态总磷(NaOH-TP), 将NaOH-TP减去NaOH-rP, 得到NaOH-nrP. NH4Cl-P、BD-P和NaOH-nrP之和为潜在可移动态磷, 而NaOH-rP、HCl-P和Res-P之和为稳定态磷[27].
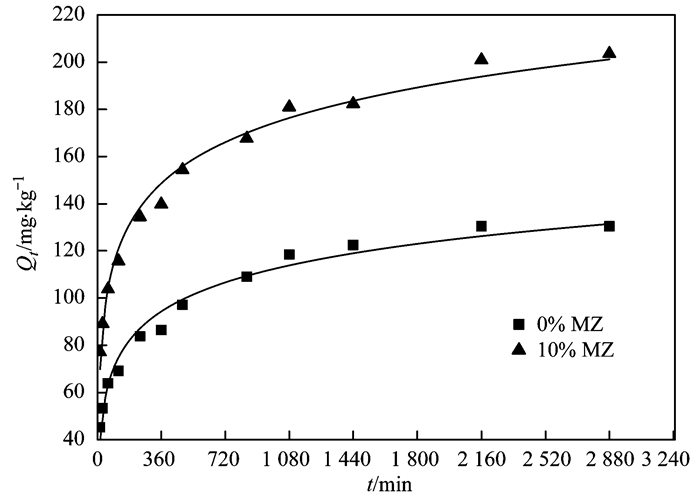
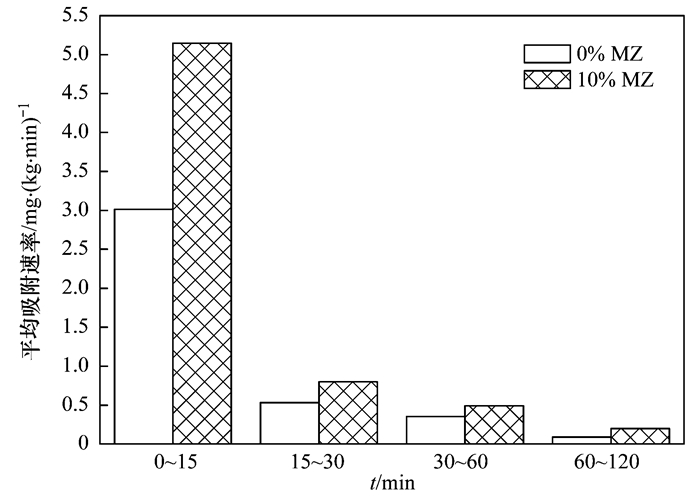
2 结果与讨论 2.1 吸附动力学图 1为未改良底泥和Fe3O4改性沸石改良底泥对水中磷酸盐的吸附动力学曲线. 图 2为改良前后底泥吸附磷酸盐初始阶段的平均吸附速率.从中可见, 未改良和改良底泥对水中磷酸盐的吸附包括一个快速吸附过程和一个慢速吸附过程.也就是, 反应的初期阶段, 磷酸盐吸附速率非常快, 随后吸附速率逐渐下降直至达到吸附平衡.初期快速的吸附主要归功于未改良和改良底泥表面存在大量的空闲的活性吸附位, 随着吸附反应的进行, 底泥表面的活性吸附位逐渐被磷酸盐所占据, 吸附速率随之下降.与未改良底泥相比, 改良底泥的初期吸附速率明显较大, 这意味着添加Fe3O4改性沸石显著增强了底泥对水中磷酸盐的吸附速率, 或者说水中的磷酸盐可以更快地被Fe3O4改性沸石改良底泥所吸附去除.
|
图 1 未改良和改良底泥对水中磷酸盐的吸附动力学曲线 Fig. 1 Adsorption kinetics curves of phosphate on unamended and amended sediments |
|
图 2 初期阶段未改良和改良底泥对水中磷酸盐的平均吸附速率 Fig. 2 Average adsorption rate of phosphate on unamended and amended sediments during the early adsorption stage |
为了识别吸附机制并预测不同反应时间的吸附速率, 采用准一级、准二级、Elovich和颗粒内扩散这4种动力学模型对图 1实验数据进行拟合.这4种动力学模型的数学表达式为[28]:
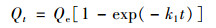
|
(2) |
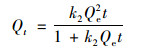
|
(3) |
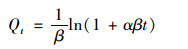
|
(4) |
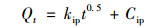
|
(5) |
式中, Qt和Qe分别指任意t时刻和平衡时刻底泥对水中磷酸盐的单位吸附量, mg ·kg-1; k1指准一级动力学模型速率常数, min-1; k2指准二级动力学模型速率常数, kg ·(mg ·min)-1; α[mg ·(kg ·min)-1]和β(kg ·mg-1)分别指Elovich模型的初始吸附速率和解吸常数; kip和Cip分别为颗粒内扩散速率常数(mg ·kg-1 ·min-0.5)和截距(mg ·kg-1).
准一级、准二级和Elovich动力学模型对图 1中实验数据的拟合结果见表 1.从中可见, 拟合相关系数(R2)最大的为Elovich模型(R2为0.978~0.985), 其次为准二级动力学模型(R2为0.798~0.813), 拟合效果最差的是准一级动力学模型(R2为0.589~0.616).这说明Elovich模型可以较好地用于描述未改良和改良底泥对水中磷酸盐的吸附动力学过程, 而准一级和准二级动力学模型则不能用于未改良和改良底泥对水中磷酸盐的吸附动力学过程.通常, 准二级动力学模型可以用于描述吸附剂对水中磷酸盐的化学吸附反应[29].未改良和改良底泥对水中磷酸盐的吸附动力学数据不符合准二级动力学模型, 这说明该吸附不是单纯的化学吸附反应, 而是几种吸附机制共同起作用的吸附反应.原始底泥对水中磷酸盐的吸附能力与底泥中存在的铁/铝氧化物和氢氧化物含量密切相关[30].此外, 天然沸石对水中磷酸盐的吸附能力可以忽略不计, Fe3O4改性沸石对水中磷酸盐的吸附能力主要取决于Fe3O4[26].有研究表明, 铁氧化物的零电荷点(pHPZC)位于5.7~6.2之间[31]; 铝氧化物的pHPZC为大于8.0[32]; Fe3O4的pHPZC约为7.4[33].这意味着, 当溶液pH值为7时, 底泥中铁氧化物表面带负电, 铝氧化物表面带正电, 而Fe3O4表面的净电荷则几乎为零.因此, 未改良和改良底泥可以通过铝氧化物和磷酸盐之间的静电吸引作用吸附水中带负电荷的磷酸盐, 这个结论将会进一步通过离子强度影响实验得到证实.另外, 铁铝氧化物/氢氧化物和Fe3O4也会通过配位体交换并形成内层络合物的机制吸附水中的磷酸盐[26, 32].因此, 未改良和改良底泥吸附水中磷酸盐的另一个机制为配位体交换.由此可见, 静电吸引和配位体交换均是未改良和改良底泥吸附水中磷酸盐的机制, 这与动力学研究的结果是相一致的.计算得到的改良底泥的α值大于未改良底泥.这说明改良底泥的初始吸附速率大于未改良底泥; 与未改良底泥相比, 初始时刻水中的磷酸盐会更快地被改良底泥所吸附去除.
|
|
表 1 未改良和改良底泥对水中磷酸盐的吸附动力学模型拟合参数 Table 1 Adsorption kinetics parameters of phosphate on unamended and amended sediments |
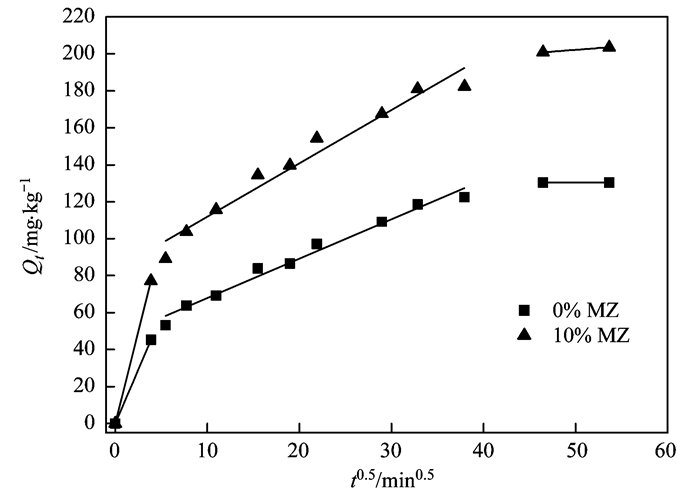
底泥吸附水中磷酸盐的动力学全过程是:①水中的磷酸盐穿过扩散层达到底泥的外表面, 这个过程被称为膜扩散; ②磷酸盐继续向底泥的内部孔道迁移, 这个过程被称为颗粒内扩散; ③磷酸盐被吸附到底泥的表面.采用准一级、准二级和Elovich动力学模型均不能判断膜扩散和颗粒内扩散是否会对吸附速率起到控制作用, 而颗粒内扩散模型[公式(5)]则可以较好地识别膜扩散和颗粒内扩散是否是底泥吸附水中磷酸盐的速率限制步骤.如果Qt对t0.5曲线是一条通过原点的直线, 则颗粒内扩散是控制吸附速率的唯一因素; 否则颗粒内扩散和膜扩散会共同控制吸附速率[34].由图 3可见, 未改良和改良底泥吸附水中磷酸盐的动力学过程可以分为3个阶段:①第一阶段是快速的外表面吸附阶段, 膜扩散是该阶段吸附速率的限制步骤; ②第二阶段为逐渐缓慢吸附阶段, 颗粒内扩散是该阶段吸附速率的限制步骤, 考虑到颗粒内扩散模型的截距不是零, 所以颗粒内扩散不是该阶段唯一的速率限制步骤, 控制该阶段吸附速率的限制步骤为膜扩散和颗粒内扩散; ③第三阶段为最终吸附平衡阶段, 考虑到底泥表面的活性吸附位大部分已经被磷酸盐占据, 因此该阶段的吸附速率非常低, 并且最终会达到吸附平衡, 即吸附速率变为零.
|
图 3 未改良和改良底泥吸附水中磷酸盐的Qt与t0.5曲线 Fig. 3 Fitting curves of Qt versus t0.5 for phosphate adsorption onto unamended and amended sediments |
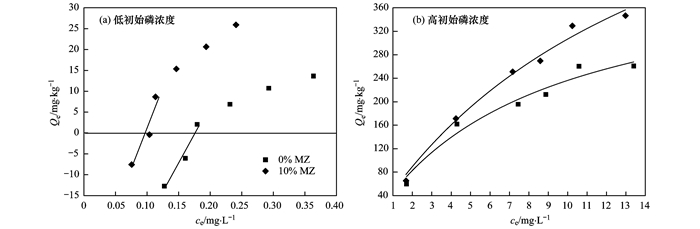
通过改变初始磷浓度获得水中磷酸盐平衡浓度对未改良和Fe3O4改良底泥吸附磷酸盐的影响规律, 即等温吸附线, 实验结果见图 4.从中可以看出, 当水中磷酸盐的平衡浓度较低时, 未改良和改良底泥对水中磷酸盐的单位吸附量均为负值, 这说明此时底泥非但不会吸附水中磷酸盐, 反而会向水中释放磷酸盐, 导致水中磷酸盐浓度的增加; 此外, 当初始磷浓度为0~0.1 mg ·L-1时, 改良底泥向水中释放磷酸盐的量均低于未改良底泥, 这说明添加Fe3O4降低了底泥中磷释放的风险.从图 4还可以看出, 当水中磷酸盐平衡浓度较高时, 未改良和改良底泥对水中磷酸盐的单位吸附量均为正值, 这说明此时底泥会吸附水中的磷酸盐, 导致水中磷酸盐浓度的下降; 此外, 未改良和Fe3O4改良底泥对水中磷酸盐的单位吸附量均随着磷平衡浓度的增加而上升.另外, 从图 4中还可以看出, 当初始磷浓度为0.2~15 mg ·L-1时, 改良底泥的单位吸附量均大于未改良底泥的单位吸附量, 这说明添加Fe3O4改性沸石可以提升底泥的钝磷能力.
|
图 4 未改良和改良底泥对水中磷酸盐的吸附等温线 Fig. 4 Adsorption isotherms of phosphate on unamended and amended sediments |
当水中初始磷浓度较低(0~0.2 mg ·L-1)的时候, 可以采用线性方程[公式(6)]对实验数据进行拟合分析.
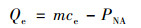
|
(6) |
式中, Qe是底泥对水中磷酸盐的单位吸附量, mg ·kg-1; ce是水中磷酸盐平衡浓度, mg ·L-1; PNA为底泥的本底吸附态磷含量, mg ·kg-1; m为斜率, L ·kg-1.底泥对水中磷酸盐的吸附效率可以采用m值进行评估.进一步采用m和PNA的数值可以计算得到磷吸附-解吸平衡浓度, 即EPC0, 所采用的计算公式为EPC0=PNA/m.
当初始磷浓度较高(2~15 mg ·L-1)的时候, 可以采用Langmuir、Freundlich和D-R(Dubinin-Radushkevic)等温吸附模型对实验数据进行拟合分析. Langmuir[35]和Freundlich[36]吸附方程的表达式为:
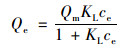
|
(7) |
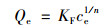
|
(8) |
式中, Qm是底泥对水中磷酸盐的最大单分子层单位吸附量, mg ·kg-1; KL是Langmuir吸附平衡常数, L ·mg-1; KF和1/n均是Freundlich吸附平衡常数.采用分离因数(RL)对Langmuir吸附方程进行进一步分析计算.
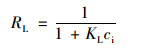
|
(9) |
式中, ci指水中初始磷浓度, mg ·L-1.基于RL值的大小, 等温吸附方程的吸附类型可以分为4类:当RL位于0~1时, 优惠吸附; 当RL>1时, 非优惠吸附; 当RL=1时, 线性吸附; 当RL=0时, 不可逆吸附[34]. D-R吸附方程的表达式为[36]:
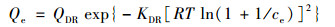
|
(10) |
式中, QDR为根据D-R模型确定的底泥对水中磷酸盐最大单位吸附量, mmol ·kg-1; KDR为D-R常数; R为理想气体常数, 等于8.314×10-3 kJ ·(mol ·K)-1; T为反应温度, K; ce为平衡时刻水中磷酸盐的浓度, mol ·L-1.采用KDR进一步计算得到平均吸附自由能(E, kJ ·mol-1)[36]:
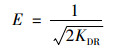
|
(11) |
E的大小可以用来估计吸附反应的类型.当E值位于8 kJ ·mol-1和16 kJ ·mol-1之间时, 吸附反应类型属于离子交换; 当E值小于8 kJ ·mol-1时, 吸附反应类型属于物理吸附, 而E值大于16 kJ ·mol-1则意味着吸附类型为化学吸附[36].
各等温吸附模型对图 4实验数据的拟合结果见表 2.从中可见, 根据线性模型确定的改良底泥的m值大于未改良底泥, 这说明改良底泥对水中低浓度磷酸盐的吸附效率高于未改良底泥.计算确定的改良底泥的EPC0值低于未改良底泥, 这说明改良底泥的磷释放风险低于未改良底泥, 即添加Fe3O4改性沸石降低了底泥中磷的释放风险.
|
|
表 2 未改良和改良底泥对水中磷酸盐的吸附等温模型拟合参数 Table 2 Adsorption isotherm parameters of phosphate on unamended and amended sediments |
Langmuir、Freundlich和D-R吸附方程均可以较好地描述未改良和改良底泥对水中较高浓度磷酸盐的等温吸附行为.根据Langmuir模型计算得到的RL值位于0~1之间, 说明未改良和改良底泥对水体中的磷的吸附属于优惠吸附.改良底泥吸附磷的KF数值大于未改良底泥, 说明Fe3O4改性沸石改良底泥对水中的吸附能力高于未改良的底泥.根据D-R模型计算得到的平均吸附自由能位于8~16 kJ ·mol-1, 这意味着静电吸引作用是未改良和改良底泥吸附水中磷酸盐的一个重要机制.这个结论与动力学研究结果是相一致的.
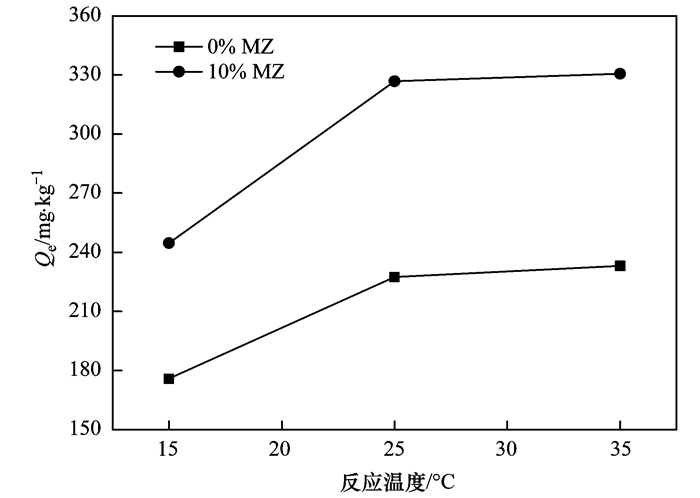
2.3 温度的影响图 5是温度对Fe3O4改性沸石改良底泥和未改良底泥吸附水中磷酸盐的影响.从中可以看出, 随着反应温度的升高, 未改良和改良底泥对水中磷酸盐的单位吸附量均随之增加.这说明增加反应温度有利于未改良和改良底泥对水中磷酸盐的吸附.当反应温度为15~35℃时, 改良底泥对水中磷酸盐的吸附能力均强于未改良底泥, 说明添加Fe3O4改性沸石可以增强底泥对水中磷酸盐的吸附能力.
|
图 5 温度对未改良和改良底泥吸附水中磷酸盐的影响 Fig. 5 Effect of temperature on phosphate adsorption onto unamended and amended sediments |
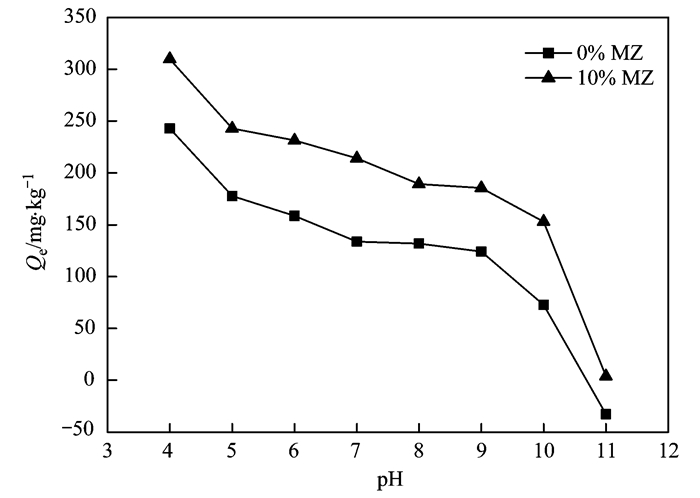
水相(上覆水和孔隙水)的pH值是影响底泥吸附磷酸盐的重要影响因素, 这是因为水相pH值不仅会改变水中磷酸盐的存在形式, 而且也会影响底泥表面官能基团的存在形式和表面的电荷, 进而影响到磷酸盐和底泥之间的作用方式.为此, 本研究考察了溶液pH值对未改良和改良底泥吸附水中磷酸盐的影响, 结果见图 6.从中可见, 随着溶液pH值的增加, 未改良和改良底泥对水中磷酸盐的吸附能力逐渐下降, 特别是当溶液pH值由4增加到5或者由9增加到11时未改良和改良底泥吸磷能力下降特别明显.这说明强碱性条件是不利于未改良和改良底泥对水中磷酸盐的吸附.溶液pH值对原始和改良底泥吸附水中磷酸盐的影响, 这可以从以下几个方面进行解释.首先, 随着溶液pH值的增加, 水中磷酸盐的存在形式会由H2PO4-逐渐转化为HPO42-, 而H2PO4-更有利于通过配位体交换作用被铁铝氧化物和氢氧化物所吸附.其次, 随着溶液pH值的增加, 底泥表面的电荷会逐渐由正电荷转变为负电荷, 正电荷的减少不利于底泥通过静电吸引作用吸附水中带负电荷的磷酸盐, 而负电荷的增加则会导致底泥与水中带负电荷磷酸盐之间静电排斥作用增强, 同样不利于水中磷酸盐的吸附去除.最后, 当溶液pH值较高时, 水中会存在大量的OH-离子, 而OH-会与带负电荷的磷酸盐竞争底泥表面的活性吸附位, 这也是不利于水中磷酸盐被底泥所吸附.此外, 当溶液pH值为4~11时, 改良底泥对水中磷酸盐的吸附能力均明显强于未改良底泥, 这说明向底泥中添加Fe3O4改性沸石可以增强底泥对水中磷酸盐的吸附能力(图 6).
|
图 6 溶液pH值对未改良和改良底泥吸附水中磷酸盐的影响 Fig. 6 Effect of solution pH on phosphate adsorption onto unamended and amended sediments |
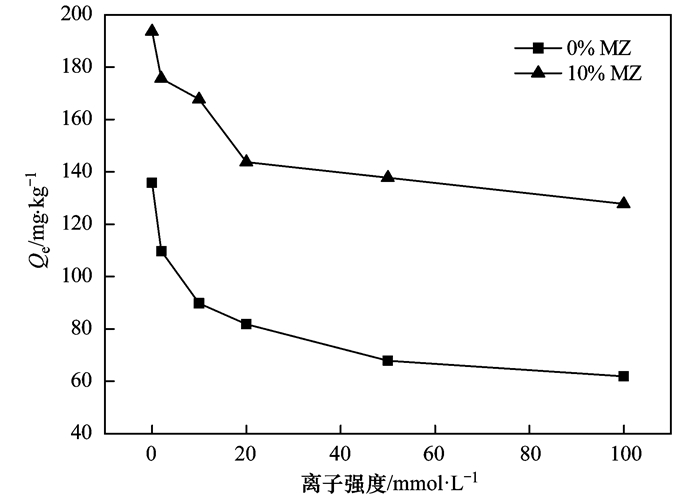
根据离子强度对金属氧化物/氢氧化物吸附水中磷酸盐的影响规律, 可以识别金属氧化物/氢氧化物对水中磷酸盐的吸附作用机制, 也就是静电吸引作用和配位体交换作用[29].如果吸附机制属于静电吸引作用, 则金属氧化物/氢氧化物对水中磷酸盐的吸附能力随着离子强度的增加而降低; 而如果吸附机制属于配位体交换作用, 并且被吸附的磷酸盐形成了内层络合物, 则离子强度对金属氧化物/氢氧化物吸附水中磷酸盐影响忽略不计或者促进吸附[29].为此, 本研究采用NaCl作为溶液离子强度的调节剂, 考察了离子强度对未改良和改良底泥吸附水中磷酸盐的影响, 研究结果见图 7.从中可见, 随着溶液离子强度的增加, 未改良和改良底泥对水中磷酸盐的吸附能力下降.这意味着, 静电吸引是未改良和改良底泥吸附水中磷酸盐的重要作用机制.除此之外, 当溶液的离子强度达到很高(100 mmol ·L-1)时, 未改良和改良底泥对水中磷酸盐的吸附能力仍然很强, 这说明配位体交换是未改良和改良底泥吸附水中磷酸盐另一个重要的作用机制.也就是说, 未改良和改良底泥通过静电吸引和配位体交换的共同作用吸附去除水中的磷酸盐.从图 7还可见, 当离子强度相同时, 改良底泥对水中磷酸盐的吸附能力均明显强于未改良底泥, 这说明添加Fe3O4改性沸石明显增强了底泥对水中磷酸盐的吸附能力.此外, 溶液共存2 mmol ·L-1 NaCl会抑制未改良和改良底泥对水中磷酸盐的吸附.这说明未改良和改良底泥对水中磷酸盐的吸附能力会受到溶液共存Cl-的抑制.究其原因, 这主要是Cl-会与磷酸盐竞争底泥表面带正电荷的活性吸附位, 导致通过静电吸引作用去除的磷酸盐量下降, 从而导致底泥对水中磷酸盐吸附能力的下降.
|
图 7 离子强度对未改良和改良底泥吸附水中磷酸盐的影响 Fig. 7 Effect of ionic strength on phosphate adsorption onto unamended and amended sediments |
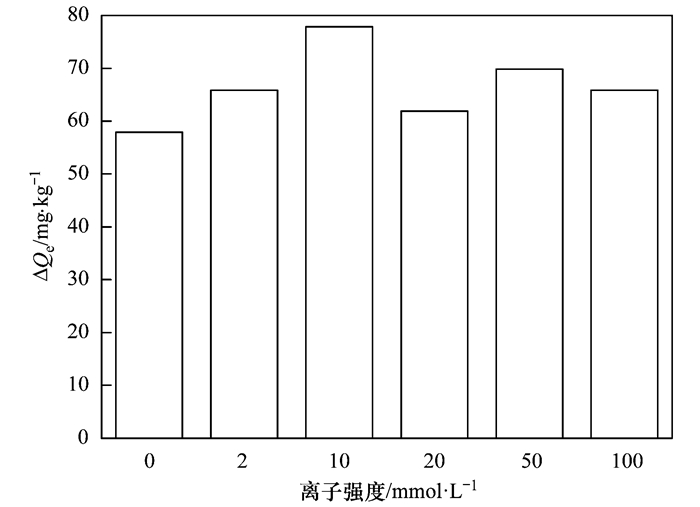
将相同离子强度条件下改良底泥和未改良底泥的磷酸盐单位吸附量相减, 得到离子强度对改良底泥中Fe3O4改性沸石吸附水中磷酸盐的影响, 结果如图 8所示.从中可见, 在离子强度为2~100 mmol ·L-1时改良底泥中Fe3O4改性沸石对水中磷酸盐的单位吸附量高于在离子强度为0 mmol ·L-1时的单位吸附量, 这说明离子强度会促进改良底泥中Fe3O4改性沸石对水中磷酸盐的吸附.这意味着静电吸引作用不是改良底泥中Fe3O4改性沸石吸附磷酸盐的机制, 而水中的磷酸盐主要是通过配位体交换的方式被改良底泥中Fe3O4改性沸石所吸附去除.这也意味着溶液共存的Cl-不会与磷酸盐竞争Fe3O4改性沸石表面上的活性吸附位, 而溶液共存的Na+会促进Fe3O4改性沸石对水中磷酸盐的吸附.
|
ΔQe为改良底泥中Fe3O4改性沸石对水中磷酸盐的单位吸附量 图 8 离子强度对改良底泥中Fe3O4改性沸石吸附水中磷酸盐的影响 Fig. 8 Effect of ionic strength on phosphate adsorption onto Fe3O4-modified zeolite in amended sediment |
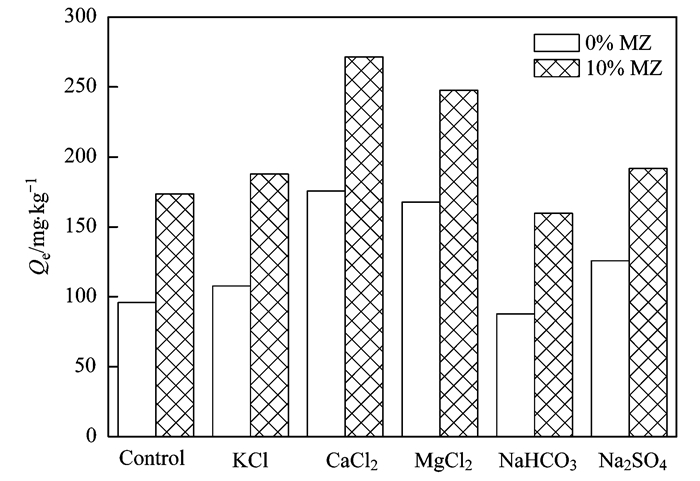
河道上覆水和孔隙水中往往存在Na+、K+、Ca2+、Mg2+、Cl-、HCO3-和SO42-等阴阳离子, 而这些离子可能会对未改良和改良底泥吸附水中磷酸盐产生影响, 从而可能会影响到Fe3O4改性沸石对底泥的修复效果.考虑到2.5节已经考察了溶液共存Na+和Cl-的影响, 为此, 这里重点考察溶液共存的KCl、CaCl2、MgCl2、Na2SO4和NaHCO3等电解质对未改良和改良底泥吸附水中磷酸盐影响, 结果如图 9所示.从中可见, 水中共存的KCl、CaCl2、MgCl2和Na2SO4对未改良和改良底泥吸附水中磷酸盐有促进作用, 且促进效果从大到小的排序为:CaCl2>MgCl2>Na2SO4>KCl.考虑到Cl-会与磷酸盐竞争底泥表面的活性吸附位, 所以溶液共存的Ca2+、Mg2+和K+显然会促进未改良和改良底泥对水中磷酸盐的吸附.考虑到SO42-是阴离子, 其对底泥吸附水中磷酸盐的影响应该是负面的, 所以溶液共存的Na+会促进未改良和改良底泥对水中磷酸盐的吸附.当水中存在NaHCO3时, 未改良和改良底泥对水中磷酸盐的吸附能力下降.考虑到Na+对底泥吸附磷酸盐的影响是正面的, 故水中共存的HCO3-对未改良和改良底泥吸附水中磷酸盐会产生一定的抑制作用.这是因为水中共存的HCO3-会占据原始底泥和改良底泥上的活性吸附位点, 与磷酸根之间形成竞争吸附作用.
|
图 9 共存阴阳离子对未改良和改良底泥吸附水中磷酸盐的影响 Fig. 9 Effect of coexisting anions and cations on phosphate adsorption onto unamended and amended sediments |
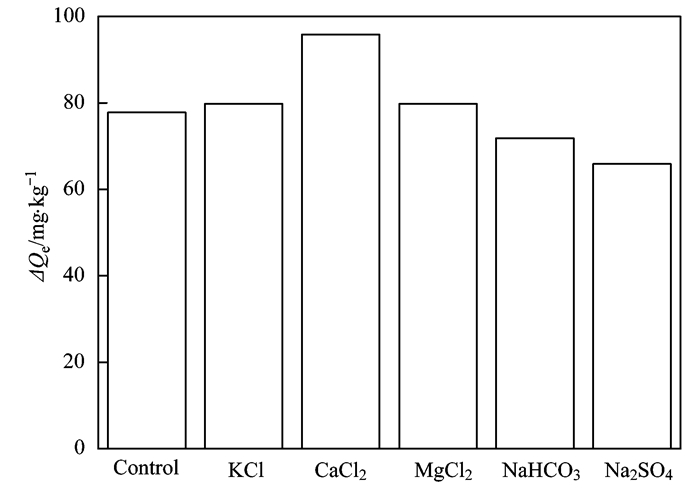
将溶液共存相同电解质条件下改良底泥和未改良底泥的磷酸盐单位吸附量相减, 得到溶液共存电解质对改良底泥中Fe3O4改性沸石吸附水中磷酸盐的影响, 结果如图 10所示.从中可见, 溶液共存的MgCl2和KCl只是略微促进了改良底泥中Fe3O4改性沸石对水中磷酸盐的吸附, 而共存的CaCl2则极大地促进了改良底泥中Fe3O4改性沸石对水中磷酸盐的吸附.考虑到Cl-不会与磷酸盐竞争Fe3O4改性沸石上的吸附位, 故水中共存的Ca2+会显著促进Fe3O4改性沸石对水中磷酸盐的吸附, 而Mg2+和K+的促进作用则明显弱于Ca2+.从图 10还可见, 溶液共存的Na2SO4和NaHCO3抑制了改良底泥中Fe3O4改性沸石对水中磷酸盐的吸附.考虑到Na+的影响是正面的, 故水中共存的SO42-和HCO3-会抑制Fe3O4改性沸石对水中磷酸盐的吸附.
|
ΔQe为改良底泥中Fe3O4改性沸石对水中磷酸盐的单位吸附量 图 10 共存阴阳离子对改良底泥中Fe3O4改性沸石吸附水中磷酸盐的影响 Fig. 10 Effect of coexisting anions and cations on phosphate adsorption onto Fe3O4-modified zeolite in amended sediment |
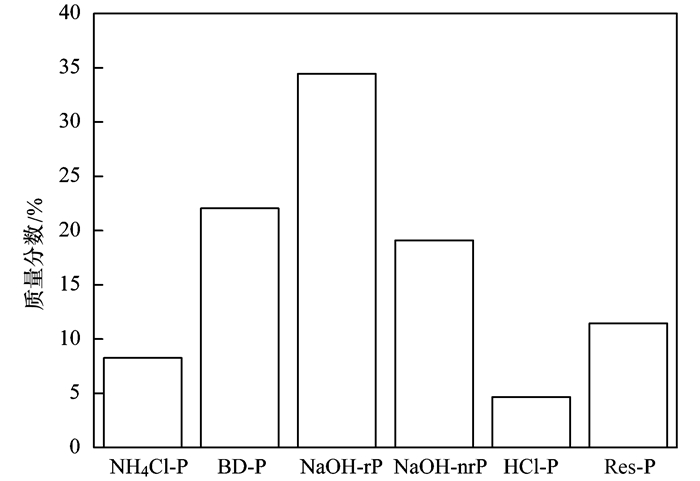
根据以上的研究结果可知, 改良底泥对水中磷酸盐的吸附能力强于未改良底泥.这主要归功于改良底泥中Fe3O4改性沸石对水中磷酸盐较强的吸附能力.确定被改良底泥中Fe3O4改性沸石所吸附磷酸盐的磷赋存形态, 对于应用Fe3O4改性沸石作为改良剂增强底泥吸磷能力而言是非常必要的.为此, 本研究提取分析了吸附磷酸盐后改良底泥中Fe3O4改性沸石的各形态磷含量, 并计算得到各形态磷占总可提取态磷的质量分数, 结果见图 11.从中可见, 被改良底泥中Fe3O4改性沸石所吸附磷酸盐的形态以NaOH-rP所占比例最高, 其次为BD-P, 再次为NaOH-nrP, 剩下的形态从大到小依次为Res-P>NH4Cl-P>HCl-P.磷酸盐属于无机磷, 而吸附磷酸盐后Fe3O4改性沸石中出现了有机磷(NaOH-nrP), 这主要是原始底泥中有机磷被吸附到Fe3O4改性沸石表面上的缘故.
|
图 11 被改良底泥中Fe3O4改性沸石所吸附磷酸盐的磷赋存形态 Fig. 11 Phosphorus fractionation of phosphate-adsorbed Fe3O4-modified zeolite in amended sediment |
NH4Cl-P是指很疏松地被吸附到固体材料表面上的磷; BD-P是指被固定在铁锰氧化物和氢氧化物表面上的磷; NaOH-nrP是指有机磷. NaOH-rP是指能够被NaOH所提取的无机磷, 主要是指被固定在铁氧化物内部和铝氧化物表面的磷; HCl-P是指能够被HCl-P所提取的磷; Res-P是指永久性结合态磷[14, 37, 38]. NH4Cl-P、BD-P和NaOH-nrP属于潜在的可移动态磷, 它们比较容易被重新释放出来.这3种形态磷含量之和占总可提取态磷总量的质量分数达到了49.4%, 这说明将近一半的被改良底泥中Fe3O4改性沸石所固定的磷是容易被重新再次释放出来的.因此, 将Fe3O4改性沸石应用到底泥中一段时间后, 采用措施从底泥中回收回来是非常必要的.
先前的研究已经发现, Fe3O4改性沸石中Fe3O4, 并且通过磁铁检验的方法证实了Fe3O4改性沸石可以很容易地通过外加磁场的作用从水中分离出来[26].因此, 将Fe3O4改性沸石应用到底泥中一段时间后, 可以采用外加磁场的作用[20, 21]将Fe3O4改性沸石从底泥中回收回来.这样做的优势是:不仅可以消除吸附磷后Fe3O4改性沸石对水体的再次污染, 同时由于Fe3O4改性沸石的回收, 可以极大地降低底泥的修复成本.由此可见, 将Fe3O4改性沸石作为改良剂控制底泥中磷的释放, 预计是一种符合可持续发展理念的河道内源磷原位控制方法, 预计应用前景将是非常广阔的.
3 结论(1) 相对于准一级和准二级动力学模型, 未改良和改良底泥对水中磷酸盐的吸附动力学过程更适合采用Elovich模型进行拟合.膜扩散和颗粒内扩散是缓慢吸附阶段的速率限制步骤. Langmuir、Freundlich和Dubinin-Radushkevic模型可以用于描述未改良和改良底泥对水中磷酸盐的等温吸附实验数据.
(2) 随着pH值的增加, 未改良和改良底泥对水中磷酸盐的吸附能力下降.水中共存的阳离子促进了未改良和改良底泥对磷酸盐的吸附, 促进作用从大到小的排序为Ca2+>Mg2+>K+, 而水中共存的HCO3-会抑制未改良和改良底泥对磷酸盐的吸附.
(3) 未改良和改良底泥吸附水中磷酸盐的机制包括静电吸引作用和配位体交换, 而改良底泥中Fe3O4改性沸石则主要依靠配位体交换作用吸附去除水中的磷酸盐.
(4) Fe3O4改性沸石改良底泥对水中磷酸盐的吸附能力强于未改良底泥, 并且前者的磷释放风险低于后者.
(5) 被改良底泥中Fe3O4改性沸石所吸附的磷中, 约49.4%的磷会以潜在可移动磷形式存在, 因此将Fe3O4改性沸石应用到底泥中后需要及时采用外加磁场作用将其从底泥中回收回来, 以消除其潜在的磷再次释放风险.
| [1] | Smith V H, Tilman G D, Nekola J C. Eutrophication:impacts of excess nutrient inputs on freshwater, marine, and terrestrial ecosystems[J]. Environmental Pollution, 1999, 100(1-3): 179-196. DOI:10.1016/S0269-7491(99)00091-3 |
| [2] |
揣小明, 杨柳燕, 程书波, 等. 太湖和呼伦湖沉积物对磷的吸附特征及影响因素[J]. 环境科学, 2014, 35(3): 951-957. Chuai X M, Yang L Y, Cheng S B, et al. Characteristics and influencing factors of phosphorus adsorption on sediment in Lake Taihu and Lake Hulun[J]. Environmental Science, 2014, 35(3): 951-957. |
| [3] |
熊强, 焦立新, 王圣瑞, 等. 滇池沉积物有机磷垂直分布特征及其生物有效性[J]. 环境科学, 2014, 35(11): 4118-4126. Xiong Q, Jiao L X, Wang S R, et al. Characteristics and bioavailability of organic phosphorus from different sources of sediments in Dianchi Lake[J]. Environmental Science, 2014, 35(11): 4118-4126. |
| [4] |
黎睿, 王圣瑞, 肖尚斌, 等. 长江中下游与云南高原湖泊沉积物磷形态及内源磷负荷[J]. 中国环境科学, 2015, 35(6): 1831-1839. Li R, Wang S R, Xiao S B, et al. Sediments phosphorus forms and loading in the lakes of the mid-lower reaches of the Yangtze River and Yunnan Plateau, China[J]. China Environmental Science, 2015, 35(6): 1831-1839. DOI:10.3969/j.issn.1000-6923.2015.06.028 |
| [5] |
陈超, 钟继承, 邵世光, 等. 太湖西北部典型疏浚/对照湖区内源性营养盐释放潜力对比[J]. 湖泊科学, 2014, 26(6): 829-836. Chen C, Zhong J C, Shao S G, et al. On the potential release rates of nutrient from internal sources:a comparative study of typical dredged and un-dredged areas, northwestern Lake Taihu[J]. Journal of Lake Science, 2014, 26(6): 829-836. |
| [6] |
林建伟, 朱志良, 赵建夫, 等. 负载硝酸盐有机改性沸石抑制底泥氮磷释放的效果及机制研究[J]. 环境科学, 2008, 29(2): 356-361. Lin J W, Zhu Z L, Zhao J F, et al. Efficiency and mechanics of surfactant modified zeolite with nitrate adsorbed to control nitrogen and phosphorus release from sediments[J]. Environmental Science, 2008, 29(2): 356-361. |
| [7] |
李勇, 李大鹏, 黄勇, 等. 曝气对重污染河道底泥吸收和持留磷的影响[J]. 黑龙江大学(自然科学学报), 2011, 28(3): 388-392. Li Y, Li D P, Huang Y, et al. Effect of aeration on phosphorus adsorption and immobilization by sediment in heavily polluted canal[J]. Journal of Natural Science of Heilongjiang University, 2011, 28(3): 388-392. |
| [8] |
王永平, 朱广伟, 洪大林, 等. 沉水植物对沉积物-水界面环境特征的影响[J]. 环境科学研究, 2012, 25(10): 1133-1139. Wang Y P, Zhu G W, Hong D L, et al. Effects of macrophytes on the environmental characteristics of sediment-water interface[J]. Research of Environmental Sciences, 2012, 25(10): 1133-1139. |
| [9] |
李静, 朱广伟, 张晓松, 等. 锁磷剂及覆盖技术对长广溪不同污染类型河段底泥磷释放的控制效果[J]. 环境化学, 2015, 34(2): 358-366. Li J, Zhu G W, Zhang X S, et al. Control effect of phoslock and sand-capping on sediment phosphorus release in different polluted sections of Changguangxi River[J]. Environmental Chemistry, 2015, 34(2): 358-366. |
| [10] |
席银, 王圣瑞, 赵海超, 等. 覆盖不同材料对湖泊沉积物磷释放影响机制[J]. 环境化学, 2017, 36(3): 532-541. Xi Y, Wang S R, Zhao H C, et al. Impact of different capping materials on the phosphorus release from lake sediment[J]. Environmental Chemistry, 2017, 36(3): 532-541. |
| [11] | Xu D, Ding S M, Sun Q, et al. Evaluation of in situ capping with clean soils to control phosphate release from sediments[J]. Science of The Total Environment, 2012, 438: 334-341. DOI:10.1016/j.scitotenv.2012.08.053 |
| [12] | Meis S, Spears B M, Maberly S C, et al. Sediment amendment with Phoslock® in Clatto Reservoir (Dundee, UK):investigating changes in sediment elemental composition and phosphorus fractionation[J]. Journal of Environmental Management, 2012, 93(1): 185-193. DOI:10.1016/j.jenvman.2011.09.015 |
| [13] | Wang C H, He R, Wu Y, et al. Bioavailable phosphorus (P) reduction is less than mobile P immobilization in lake sediment for eutrophication control by inactivating agents[J]. Water Research, 2017, 109: 196-206. DOI:10.1016/j.watres.2016.11.045 |
| [14] | Wang C H, Bai L L, Jiang H L, et al. Algal bloom sedimentation induces variable control of lake eutrophication by phosphorus inactivating agents[J]. Science of the Total Environment, 2016, 557-558: 479-488. DOI:10.1016/j.scitotenv.2016.03.082 |
| [15] | Wang C H, Bai L L, Pei Y S. Assessing the stability of phosphorus in lake sediments amended with water treatment residuals[J]. Journal of Environmental Management, 2013, 122: 31-36. DOI:10.1016/j.jenvman.2013.03.007 |
| [16] | Yin H B, Han M X, Tang W Y. Phosphorus sorption and supply from eutrophic lake sediment amended with thermally-treated calcium-rich attapulgite and a safety evaluation[J]. Chemical Engineering Journal, 2016, 285: 671-678. DOI:10.1016/j.cej.2015.10.038 |
| [17] |
李佳, 詹艳慧, 林建伟. 镧改性沸石改良太湖底泥的磷吸附特征[J]. 生态与农村环境学报, 2013, 29(4): 500-506. Li J, Zhan Y H, Lin J W. Effect of la-modified zeolite on phosphate sorption of taihu lake sediments[J]. Journal of Ecology and Rural Environment, 2013, 29(4): 500-506. DOI:10.3969/j.issn.1673-4831.2013.04.017 |
| [18] | Yang M J, Lin J W, Zhan Y H, et al. Immobilization of phosphorus from water and sediment using zirconium-modified zeolites[J]. Environmental Science and Pollution Research, 2015, 22(5): 3606-3619. DOI:10.1007/s11356-014-3604-2 |
| [19] | Lin J W, Wang H, Zhan Y H, et al. Evaluation of sediment amendment with zirconium-reacted bentonite to control phosphorus release[J]. Environmental Earth Sciences, 2016, 75(11): 942. DOI:10.1007/s12665-016-5744-9 |
| [20] | Funes A, Del Arco A, álvarez-Manzaneda I, et al. A microcosm experiment to determine the consequences of magnetic microparticles application on water quality and sediment phosphorus pools[J]. Science of the Total Environment, 2017, 579: 245-253. DOI:10.1016/j.scitotenv.2016.11.120 |
| [21] | Funes A, De Vicente J, Cruz-Pizarro L, et al. Magnetic microparticles as a new tool for lake restoration:A microcosm experiment for evaluating the impact on phosphorus fluxes and sedimentary phosphorus pools[J]. Water Research, 2016, 89: 366-374. DOI:10.1016/j.watres.2015.11.067 |
| [22] | Lin C Y, Wang Z G, He M C, et al. Phosphorus sorption and fraction characteristics in the upper, middle and low reach sediments of the Daliao river systems, China[J]. Journal of Hazardous Materials, 2009, 170(1): 278-285. DOI:10.1016/j.jhazmat.2009.04.102 |
| [23] |
侯诒然, 高勤峰, 董双林, 等. 不同规格刺参的生物扰动作用对沉积物中磷赋存形态及吸附特性的影响[J]. 中国海洋大学学报, 2017, 47(9): 36-45. Hou Y R, Gao Q F, Dong S L, et al. Effect of the bioturbation derived from Sea Cucumber (Apostichopus japonicus) of different size on sediment phosphorus forms and phosphorus adsorption characteristics[J]. Periodical of Ocean University of China, 2017, 47(9): 36-45. |
| [24] |
朱佳美, 曹晓燕, 刘素美, 等. 桑沟湾表层沉积物性质及对磷的吸附特征[J]. 环境科学, 2016, 37(2): 558-564. Zhu J M, Cao X Y, Liu S M, et al. Surface property and sorption characteristics of phosphorus onto surface sediments in Sanggou Bay[J]. Environmental Science, 2016, 37(2): 558-564. |
| [25] | Zhang L, Du Y, Du C, et al. The adsorption/desorption of phosphorus in freshwater sediments from buffer zones:the effects of sediment concentration and pH[J]. Environmental Monitoring and Assessment, 2016, 188: 13. DOI:10.1007/s10661-015-5018-0 |
| [26] |
詹艳慧, 林建伟, 王虹, 等. 四氧化三铁-沸石复合材料去除水中铵和磷酸盐研究[J]. 上海海洋大学学报, 2013, 22(3): 376-383. Zhan Y H, Lin J W, Wang H, et al. Removal of ammonium and phosphate from aqueous solution by magnetite/zeolite composite[J]. Journal of Shanghai University, 2013, 22(3): 376-383. |
| [27] |
张奇, 喻庆国, 王胜龙, 等. 滇西北剑湖沉积物磷形态、空间分布及释放贡献[J]. 环境科学学报, 2017, 37(10): 3792-3803. Zhang Q, Yu Q G, Wang S L, et al. Phosphorus fractions, spatial distribution and release contributions in sediments of Jianhu Lake, Northwestern Yunnan Plateau, China[J]. Acta Scientiae Circumstantiae, 2017, 37(10): 3792-3803. |
| [28] | Tan K L, Hameed B H. Insight into the adsorption kinetics models for the removal of contaminants from aqueous solutions[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 74: 25-48. DOI:10.1016/j.jtice.2017.01.024 |
| [29] | Su Y, Cui H, Li Q, et al. Strong adsorption of phosphate by amorphous zirconium oxide nanoparticles[J]. Water Research, 2013, 47(14): 5018-5026. DOI:10.1016/j.watres.2013.05.044 |
| [30] | Zhou A M, Tang H X, Wang D S. Phosphorus adsorption on natural sediments:modeling and effects of pH and sediment composition[J]. Water Research, 2005, 39(7): 1245-1254. DOI:10.1016/j.watres.2005.01.026 |
| [31] | Mustafa S, Tasleem S, Naeem A. Surface charge properties of Fe2O3 in aqueous and alcoholic mixed solvents[J]. Journal of Colloid and Interface Science, 2004, 275(2): 523-529. DOI:10.1016/j.jcis.2004.02.089 |
| [32] | Lǚ J B, Liu H J, Liu R P, et al. Adsorptive removal of phosphate by a nanostructured Fe-Al-Mn trimetal oxide adsorbent[J]. Powder Technology, 2013, 233: 146-154. DOI:10.1016/j.powtec.2012.08.024 |
| [33] | Rajput S, Pittman Jr C U, Mohan D. Magnetic magnetite (Fe3O4) nanoparticle synthesis and applications for lead (Pb2+) and chromium (Cr6+) removal from water[J]. Journal of Colloid and Interface Science, 2016, 468: 334-346. DOI:10.1016/j.jcis.2015.12.008 |
| [34] | Pathak P D, Mandavgane S A. Preparation and characterization of raw and carbon from banana peel by microwave activation:application in citric acid adsorption[J]. Journal of Environmental Chemical Engineering, 2015, 3(4): 2435-2447. DOI:10.1016/j.jece.2015.08.023 |
| [35] | Langmuir I. The constitution and fundamental properties of solids and liquids. Part Ⅰ. Solids[J]. Journal of the American Chemical Society, 1916, 38(11): 2221-2295. DOI:10.1021/ja02268a002 |
| [36] | De Angelis G, Medeghini L, Conte A M, et al. Recycling of eggshell waste into low-cost adsorbent for Ni removal from wastewater[J]. Journal of Cleaner Production, 2017, 164: 1497-1506. DOI:10.1016/j.jclepro.2017.07.085 |
| [37] | Rydin E. Potentially mobile phosphorus in Lake Erken sediment[J]. Water Research, 2000, 34(7): 2037-2042. DOI:10.1016/S0043-1354(99)00375-9 |
| [38] |
李乐, 王圣瑞, 焦立新, 等. 滇池柱状沉积物磷形态垂向变化及对释放的贡献[J]. 环境科学, 2016, 37(9): 3384-3393. Li L, Wang S R, Jiao L X, et al. Vertical variation of phosphorus forms in Lake Dianchi and contribution to release[J]. Environmental Science, 2016, 37(9): 3384-3393. |
 2018, Vol. 39
2018, Vol. 39


