2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100;
3. 中国海洋大学海洋生命学院, 青岛 266003
2. Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Qingdao 266100, China;
3. College of Marine Life Sciences, Ocean University of China, Qingdao 266003, China
纳米材料是指在三维空间上至少有一维处于纳米级范围或者由纳米级元件构成的材料.由于其具有尺寸小和比表面积大等特点, 使纳米材料表现出尺寸效应、表面效应[1]等特殊性能.纳米银作为一种金属纳米材料, 由于具有非线性光学特性、传热导电性、催化特性以及抗菌性等被广泛应用于传统行业和新兴领域[1~4].随着纳米银的大量使用, 部分纳米银通过不同方式进入河流, 经过河口区最终汇聚到海湾[5].纳米银会释放出银离子, 纳米银颗粒和银离子因静电吸引在细胞膜周围聚集并吸附其上[6, 7], 与细胞膜发生作用, 影响细胞膜的完整性和流动性[8]; 同时纳米银进入细菌体内还会通过阻断菌体内的电子传输系统增强细菌DNA的稳定性, 使DNA失去复制能力[9]; 此外纳米银和银离子会与酶中的硫、氧和氮等电子供体结合、替换酶中金属离子甚至改变酶的三维构象, 致使酶活性钝化甚至失活[9].因此, 纳米银进入河口区后, 会在一定程度上改变河口和海湾区微生物丰度和群落结构, 对生态系统的结构和功能产生影响[9, 10].
反硝化作用是指在厌氧条件下反硝化菌将NO3-还原成N2的过程, 是氮循环过程中不可缺少的关键环节, 其中NO3-还原成NO2-和NO2-还原成气态氮的过程分别由NO3-和NO2-还原酶催化, 功能基因narG和nirS分别编码NO3-和NO2-还原酶的催化中心[11]. VandeVoort等[12]对土壤NO3-还原过程的研究发现, 纳米银颗粒(AgNPs)会显著抑制NO3-还原的速率, 抑制程度与加入的AgNPs浓度有关. Bao等[11]对河流沉积物酶活性的研究发现, 加入AgNPs后, 脲酶活性受到了显著抑制. Xiong等[13]对河口沉积物反硝化作用的研究发现, 纳米氧化铜颗粒(CuONPs)对NO3-还原和NO2-还原都具有明显的抑制效应, CuONPs的加入导致了NO2-的累积, 还会明显抑制NO3-还原酶和NO2-还原酶的活性. Hou等[14]研究了CuONPs对NO3-还原的影响, 发现CuONPs显著降低了nirS的丰度, 表明CuONPs会降低NO3-还原菌的数量.
由于表层沉积物往往同时伴随低氧、高碳氮含量, 并存在明显的有氧-厌氧界面, 所以表层沉积物是反硝化发生的重要源区[15].纳米银会对沉积物反硝化过程产生影响, 进而改变生态系统的生命活动和氮的生物地球化学循环.目前关于纳米银对反硝化作用影响的研究大多局限于单菌株和污水处理系统[16, 17], 而纳米银对实际环境中沉积物反硝化作用影响的相关研究较少.胶州湾是半封闭浅海湾, 沿岸经济发达, 是一个受人类活动影响较大的典型海湾, 因此探讨纳米银对胶州湾河口区和湾内沉积物反硝化作用的影响具有重要意义.本研究通过现场采样带回实验室模拟培养, 分析不同浓度纳米银对胶州湾西北部海区S站和大沽河河口区E站沉积物NO3-和NO2-还原能力、反硝化酶活性及功能基因narG和nirS丰度的影响, 以期为深入探讨纳米银对近海沉积环境的生态影响机制及环境效应提供科学依据.
1 材料与方法 1.1 实验用纳米银及预处理纳米银购自SIGMA-ALDRICH®, 粒径<100 nm, 银纯度>99.5%.纳米银溶液现用现配, 为了防止聚集, 使用前在冰浴条件下, 超声波(230 V, 50 kHz)超声30 min.
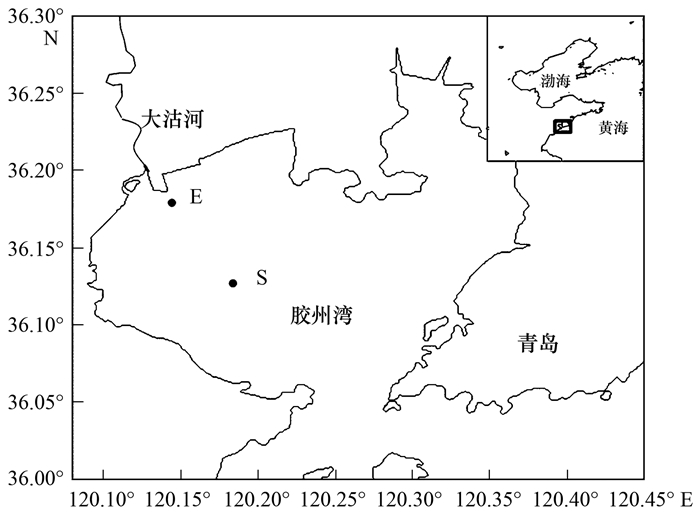
1.2 现场样品采样与预处理本研究所用沉积物样品于2017年7月采自胶州湾西北部海区的E站(36.168 8°N, 120.136 5°E)和大沽河河口区的S站(36.126 9°N, 120.183 8°E), 采样站位见图 1.采用彼得森采泥器采集0~5 cm表层沉积物样品于无菌塑料袋中密封, 用无菌聚乙烯塑料瓶采集底层海水; 采用YSI6600多参数水质仪现场测定pH、盐度等环境参数, 并采集部分沉积物样和水样用于测定其它环境指标.所有样品低温保存立即带回实验室.采集的沉积物样品充分混匀后过1 mm标准筛, 水样用0.22 μm无菌醋酸纤维膜过滤, 用于实验室模拟培养. 2个站位水体和沉积物的主要环境参数见表 1.
|
图 1 采样站位示意 Fig. 1 Sampling stations |
|
|
表 1 各采样点水体和沉积物的主要环境参数 Table 1 Initial environmental factors at the stations |
1.3 实验室模拟培养与样品采集
各站位实验室模拟培养分别设置1个对照组和2个不同浓度的纳米银处理组, C组为对照组(0mg ·L-1)、L组为低纳米银组(135mg ·L-1)、H组为高纳米银组(1 350 mg ·L-1), 各组均设3个重复实验组.
在经0.22 μm滤膜过滤的原位海水中加入C6H12O6和KNO3, 使终质量分数和浓度分别为1%和50 mmol ·L-1; 将纳米银溶解在上述原位海水中, 搅拌均匀并4℃超声30 min, 配制成纳米银质量浓度为0、135、1 350 mg ·L-1的培养液, 各取60 mL分别置于250 mL培养瓶中, 分别取60 g过筛处理后的沉积物于各培养瓶, 混匀.所有培养瓶均通氮气20 min, 使培养环境处于厌氧状态下密封.培养瓶置于80 r ·min-1的恒温振荡器中25℃避光培养6 d, 分别在培养第0、2、4、6 d于各组培养体系取样, 用于测定NO3-、NO2-浓度及酶活性和功能基因丰度.
1.4 样品测定硝酸盐(NO3-)和亚硝酸盐(NO2-):采用QuAAtro营养盐自动分析仪测定; 沉积物类型:采用激光粒度仪[18]测定; 含水率:采用重量法测定.
NO3-和NO2-还原酶活性:于培养瓶中均匀取泥水混合物样品5 mL, 8 000 r ·min-1离心10 min, 弃去上清液, 用100mmol ·L-1的磷酸盐缓冲液(pH=7.4)冲洗, 超声破碎细胞结构, 12 000 r ·min-1离心10 min以去除细胞碎片, 取上清液加入至含有100mmol ·L-1磷酸盐缓冲溶液、1 mmol ·L-1 NaNO2、1mmol ·L-1甲基紫精和5mmol ·L-1 Na2S2O4的厌氧气相瓶中, 在30℃下培养30 min, 根据NO3-和NO2-的减少量计算NO3-和NO2-还原酶的酶活性[11].
1.5 功能基因narG和nirS的测定 1.5.1 DNA的提取所取样品4℃ 8 000 r ·min-1离心15 min, 沉淀样品采用(Sangon Biotech)土壤基因组DNA快速抽提试剂盒提取基因组DNA, 于-80℃保存, 用于后续荧光定量PCR仪测定基因相对丰度.
1.5.2 Real-time PCR将所提取的DNA样品利用荧光定量PCR仪(Roche LightCycler480), 采用SYBR Green Ⅰ法测定narG和nirS相对丰度.实验中采用20 μL反应体系, 由10 μL SYBR Green qPCR Master Mix、0.4 μL正向引物、0.4 μL反向引物、2 μL DNA模板、7.2 μL ddH2O构成. narG和nirS的所用引物(Sangon Biotech)如表 2所示.反应体系在96孔反应板中进行, 每个样品重复3次, 以无菌水作为阴性对照.
|
|
表 2 Real-time PCR实验引物列表 Table 2 Primers used in real-time PCR |
Real-time PCR扩增条件:16S rDNA为95℃预变性3 min, 45个循环(95℃变性7 s, 57℃退火10 s, 72℃延伸15 s). narG: 95℃预变性3 min, 45个循环(95℃变性15 s, 63℃退火30 s, 72℃延伸30 s). nirS: 95℃预变性3 min, 15个循环(95℃变性15 s, 66℃退火20 s, 72℃延伸20 s), 30个循环(95℃变性15 s, 60℃退火20 s, 72℃延伸20 s).各基因最后以0.1℃·s-1速率从60℃升至95℃, 获得扩增DNA片段的熔解曲线.基因的相对丰度采用2-ΔΔCT法[19]计算, 以16S rDNA为管家基因, 各浓度纳米银组与对照组中narG和nirS的相对丰度进行比较.
1.6 数据分析不同处理组间差异的显著性水平采用单因素方差分析法(P<0.05为差异显著, P>0.05为差异不显著), 统计分析采用Spss19完成.
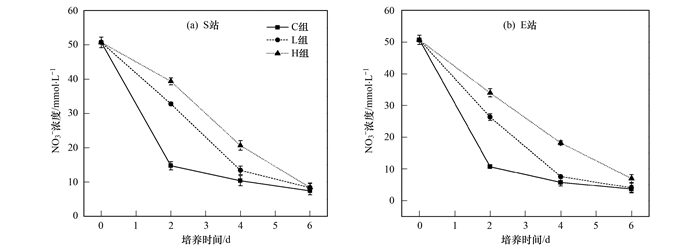
2 结果与分析 2.1 纳米银对不同区域反硝化能力和NO2-累积效应的影响不同浓度纳米银胁迫下胶州湾西北部海区S站和河口区E站沉积物NO3-浓度的变化如图 2所示. S站, L组培养第2 d NO3-还原量为C组的49.8%, 第6 d还原量与C组基本相同; H组在培养第2 d NO3-还原量为C组的31.6%, H组对NO3-还原能力的抑制强度明显高于L组. E站各实验组对NO3-还原能力的抑制情况与S站相似, L、H组在培养第2 d NO3-还原量分别为C组的60.8%和41.7%.两个站位在培养期间H组对NO3-还原能力的抑制强度明显高于L组(P<0.05), L组明显高于C组(P<0.05);纳米银对位于湾内的S站NO3-还原能力的抑制程度明显高于河口区的E站(P<0.05).因此, 纳米银对胶州湾沉积物NO3-还原能力具有明显的抑制作用, 浓度越高、抑制效应越强, 且对胶州湾西北部海区站位的抑制效应大于对河口区的站位.
|
C组为对照组, L组为低浓度组, H组为高浓度组, 下同 图 2 不同浓度纳米银胁迫下胶州湾沉积物NO3-浓度的变化 Fig. 2 Variation of NO3- concentration among different AgNPs concentrations |
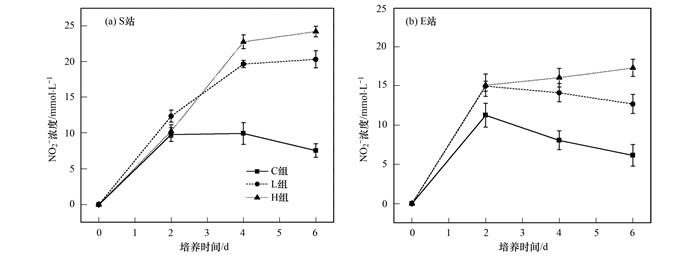
不同浓度纳米银胁迫下S站和E站沉积物NO2-浓度的变化如图 3所示. S站L、H组NO2-浓度从培养第2 d开始即明显高于C组, NO2-的还原能力受到明显抑制, NO2-还原量分别为C组的21.2%和4.2%, 纳米银浓度越高, NO2-的累积效应越强; 到培养第6 d, L、H组NO2-浓度分别为C组的2.69倍和3.20倍, NO2-还原量有所恢复, 分别为C组的61.6%和50.7%, 这可能与亚硝酸盐还原菌对纳米银的影响产生一定的适应机制有关[11]. E站L组NO2-浓度在培养第2 d达峰值, 为C组的1.33倍; H组NO2-浓度表现为持续增长的趋势; L、H组NO2-还原量在培养第2 d分别为C组的32.6%和5.6%, 第6 d有明显恢复, 分别为C组的83.0%和64.6%, 恢复幅度明显高于S站(P < 0.05).
|
图 3 不同浓度纳米银胁迫下胶州湾沉积物NO2-浓度的变化 Fig. 3 Variation of NO2- concentration among different AgNPs concentrations |
由上述结果可见, 纳米银胁迫对两个站位NO2-还原能力均具有明显的抑制效应, 并会造成NO2-积累量的增加, 且纳米银浓度越高, 抑制效应越强(P < 0.05)、积累效应越强(P < 0.05).纳米银对胶州湾西北部海区S站NO2-还原能力的抑制程度明显高于对河口区的E站(P < 0.05), 对S站NO2-累积的增强效应也比E站更显著(P < 0.05), 且E站NO2-还原能力对纳米银胁迫有更强的适应性, 表明纳米银胁迫可能更易造成海湾区NO2-的累积, 其生态影响也大于河口区.
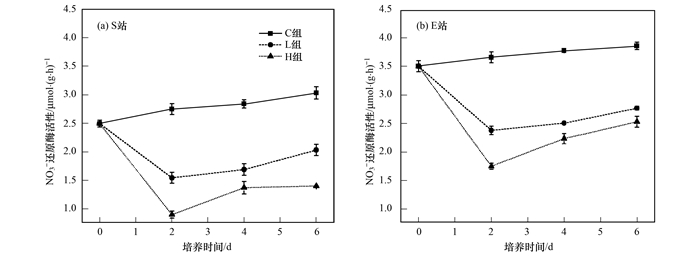
2.2 纳米银对NO3-和NO2-还原酶活性的影响不同浓度纳米银胁迫下S站和E站沉积物NO3-还原酶活性的变化如图 4所示. S站L、H组NO3-还原酶活性表现出先降低后升高的趋势, 最低值出现在培养的第2 d, 分别为C组的56.1%和32.6%; NO3-还原酶活性在培养第6 d有所恢复, 分别为C组的66.9%和46.1%. E站NO3-还原酶活性的变化趋势与S站相同, L、H组在培养第2 d达最低值, 分别为C组的64.9%和47.6%, 第6d恢复至C组的71.7%和65.4%.纳米银对两个站位NO3-还原酶活性均具有明显的抑制作用(P < 0.05), 且浓度越高抑制效应越强(P < 0.05).各组纳米银对胶州湾西北部海区S站NO3-还原酶活性的抑制程度明显大于河口区的E站(P < 0.05), 表明纳米银对海湾区NO3-还原酶活性的影响可能比河口区更大.
|
图 4 不同浓度纳米银胁迫下胶州湾沉积物NO3-还原酶活性的变化 Fig. 4 Variation of NO3- reductase among different AgNPs concentrations |
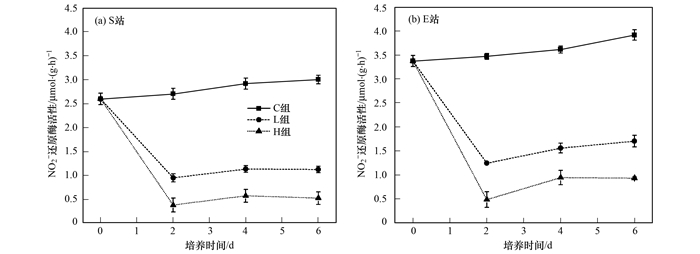
不同浓度纳米银胁迫下位于胶州湾西北部海区的S站和河口区的E站沉积物NO2-还原酶活性的变化如图 5所示. S站L、H组NO2-还原酶活性在培养第2 d即受到明显抑制, 酶活性分别仅为C组的35.1%和14.1%;到培养第6 d, L、H组酶活性均有小幅度恢复, 分别为C组的37.4%和17.5%. E站L、H组NO2-还原酶活性也表现出先降低后升高的趋势, 第2d分别为C组的35.9%和14.2%;第6 d恢复幅度明显, L、H组分别为C组的43.5%和23.8%.纳米银对2个站位NO2-还原酶的影响与对NO3-还原酶的影响类似, 有明显的抑制作用, 且浓度越高抑制效应越强(P < 0.05);纳米银对S站NO2-还原酶活性的抑制作用与E站无显著性差异(P>0.05), 但E站NO2-还原酶活性在培养后期的恢复幅度明显高于S站(P < 0.05), 与纳米银胁迫下NO2-还原能力的恢复情况相一致, 表明河口区反硝化细菌对纳米银胁迫的适应能力可能强于海湾区.
|
图 5 不同浓度纳米银胁迫下胶州湾沉积物NO2-还原酶活性的变化 Fig. 5 Variation of NO2- reductase among different AgNPs concentrations |
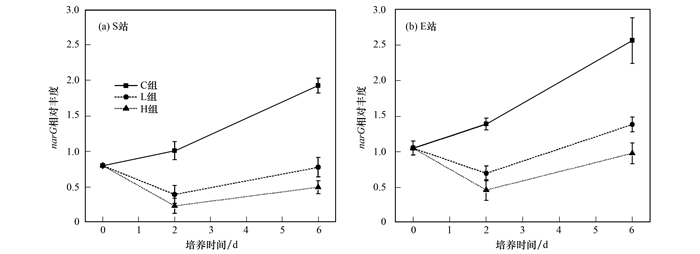
不同浓度纳米银胁迫下S站和E站沉积物narG相对丰度的变化如图 6所示. S站L、H组narG相对丰度表现出先降低后升高的趋势, 培养第2 d分别为C组的38.9%和23.0%;培养第6 d略有恢复, 分别为C组的40.3%和25.7%. E站L、H组narG相对丰度同样表现出先降低后升高的趋势, 培养第2 d分别为C组的49.9%和32.9%;第6 d有所恢复, 分别为C组的53.9%和40.0%.两个站位纳米银对narG相对丰度都表现为抑制作用(P < 0.05), 浓度越高, 抑制作用越大(P < 0.05).纳米银对胶州湾西北部海区S站narG的抑制程度明显大于对河口区的E站(P < 0.05), 表明纳米银对海湾区narG的抑制效应可能大于河口区.
|
图 6 不同浓度纳米银胁迫下胶州湾沉积物narG相对丰度的变化 Fig. 6 Variation of narG relative abundance among different AgNPs concentrations |
不同浓度纳米银胁迫下S站和E站沉积物nirS相对丰度的变化如图 7所示. S站L、H组nirS相对丰度在培养第2 d同样受到明显抑制, 分别为C组的31.2%和21.7%;到培养第6 d有所恢复, 为C组的38.4%和24.2%. E站nirS相对丰度与S站类似, 第2 d分别为C组的46.7%和23.5%;到培养第6 d有所恢复, 为C组的52.1%和30.3%.纳米银对两个站位nirS相对丰度均表现为明显的抑制作用(P < 0.05), 且浓度越高抑制作用越明显(P < 0.05).纳米银对海湾区S站nirS的抑制程度明显大于河口区的E站, 且培养后期H组E站nirS的恢复幅度明显大于S站(P < 0.05), 表明纳米银对海湾区nirS的抑制效应可能大于河口区, 且河口区反硝化细菌对纳米银胁迫的适应性可能更强.

|
图 7 不同浓度纳米银胁迫下胶州湾沉积物nirS相对丰度的变化 Fig. 7 Variation of nirS relative abundance among different AgNPs concentrations |
反硝化作用是将氮素重新以N2释放进入大气的重要途径, 是实现氮循环的关键环节[11]. NO3-还原成NO2-和NO2-还原成NO的过程是反硝化作用的重要步骤, 被认为是水环境中氮的永久去除过程之一, 其中由NO2-转化为NO的过程, 更是反硝化作用有别于其他NO3-代谢的标志性反应, 是反硝化过程中重要的限速步骤[23].本研究中, 纳米银对NO2-还原能力的抑制强度都明显大于对NO3-还原能力的抑制, 表明纳米银对NO2-还原过程的影响大于NO3-还原过程.因此, 纳米银在抑制沉积环境中氮去除能力的同时, 会导致沉积物中NO2-累积量的增加, 并对海洋生物产生毒性效应, 从而进一步影响海洋生态系统的物质循环与能量流动[24, 25].
3.2 纳米银对沉积物反硝化功能影响的关键过程narG和nirS是反硝化作用中两个重要步骤的关键基因, 其转录翻译的产物NO3-还原酶和NO2-还原酶分别在细胞的特定位置发挥催化作用, 保证NO3-还原过程和NO2-还原过程的正常进行[23].本研究NO3-还原过程中, 纳米银对narG的抑制程度明显大于对NO3-还原酶活性的抑制, 而在NO2-还原过程中, 纳米银对NO2-还原酶活性的抑制程度明显大于对nirS的抑制, 表明纳米银对NO3-还原成NO2-过程的影响主要是通过对功能基因丰度的抑制, 而对NO2-还原成NO过程的影响主要是通过对还原酶活性的抑制, 这可能与NO3-还原过程和NO2-还原过程在菌体内的作用部位不同有关. narG编码的NO3-还原酶是一种膜结合酶, 而nirS编码的NO2-还原酶是一种膜外周质酶[23]; 纳米银进入环境中后会部分溶解生成银离子, 在静电吸引作用下, 逐渐与细菌接近并聚集在细菌周围, 纳米银颗粒和银离子会通过引起NO2-还原酶的三维构象改变等方式导致NO2-还原酶失活而无法发挥作用[26], 因此NO2-还原酶作为细胞膜外周质酶对纳米银胁迫更为敏感.
3.3 纳米银对胶州湾不同区域生态影响的比较胶州湾是位于中国黄海中部、山东半岛南部的一个典型半封闭海湾, 受工业废水、生活污水等陆源污染物影响较大.而大沽河是胶州湾最大的入湾河流, 每年向胶州湾输送大量的陆源污染物[24], 作为连接胶州湾和大沽河的纽带, 大沽河河口区和胶州湾西北部海区承载着巨大的营养盐等陆源污染负荷.本研究结果表明, 在纳米银胁迫下, 位于大沽河河口区的E站和胶州湾西北部海区的S站NO3-和NO2-还原能力、NO3-和NO2-还原酶活性、narG和nirS相对丰度均受到明显的抑制. NO3-和NO2-还原能力的抑制将导致沉积物中反硝化作用严重受阻, 阻断N的正常循环途径, 进一步加重水体的富营养化程度.
河口区是纳米银迁移过程中的重要途径, 而海湾区由于盐度更高, 更容易导致纳米颗粒团聚、沉降, 最终聚集在沉积物中, 从而对沉积物环境产生直接和潜在的影响[24].本研究结果表明, 纳米银对S站NO3-和NO2-还原能力、NO3-还原酶活性及narG和nirS相对丰度的抑制效应明显高于E站, 表明胶州湾西北部海区NO3-和NO2-还原菌可能对纳米银的胁迫更加敏感, 因此, 纳米银对胶州湾西北部海湾区沉积环境的生态影响可能也大于河口区.
4 结论(1) 纳米银对胶州湾西北部海区和河口区2个站位沉积物NO3-和NO2-还原能力、NO3-和NO2-还原酶活性及narG和nirS丰度具有抑制效应, 纳米银浓度越高, 抑制效应越明显, 且对nirS的抑制程度大于对narG的抑制程度, 会导致NO2-累积量的增加.
(2) 纳米银对narG相对丰度的抑制程度明显大于对NO3-还原酶的抑制, 对NO2-还原酶的抑制程度明显大于对nirS相对丰度的抑制, 表明纳米银对NO3-还原过程的影响主要是通过对功能基因的抑制, 而对NO2-还原过程的影响主要是通过对还原酶活性的抑制.
(3) 纳米银对胶州湾西北部海区S站反硝化能力和narG、nirS相对丰度的抑制程度明显高于对河口区的E站, 表明湾内的反硝化细菌对纳米银胁迫的敏感性高于河口区, 纳米银对胶州湾西北部海区的生态影响也大于大沽河河口区.
| [1] | Konował E, Sybis M, Modrzejewska-Sikorska A, et al. Synthesis of dextrin-stabilized colloidal silver nanoparticles and their application as modifiers of cement mortar[J]. International Journal of Biological Macromolecules, 2017, 104: 165-172. DOI:10.1016/j.ijbiomac.2017.06.011 |
| [2] | Li M M, Gong Y M, Wang W H, et al. In-situ reduced silver nanoparticles on populus fiber and the catalytic application[J]. Applied Surface Science, 2017, 394: 351-357. DOI:10.1016/j.apsusc.2016.10.094 |
| [3] | McGillicuddy E, Murray I, Kavanagh S, et al. Silver nanoparticles in the environment:sources, detection and ecotoxicology[J]. Science of the Total Environment, 2017, 575: 231-246. DOI:10.1016/j.scitotenv.2016.10.041 |
| [4] | Rasheed T, Bilal M, Iqbal H M N, et al. Green biosynthesis of silver nanoparticles using leaves extract of Artemisia vulgaris and their potential biomedical applications[J]. Colloids and surfaces B:Biointerfaces, 2017, 158: 408-415. DOI:10.1016/j.colsurfb.2017.07.020 |
| [5] | Griffitt R J, Hyndman K, Denslow N D, et al. Comparison of molecular and histological changes in zebrafish gills exposed to metallic nanoparticles[J]. Toxicological Sciences, 2009, 107(2): 404-415. DOI:10.1093/toxsci/kfn256 |
| [6] | Durán N, Marcato P D, de Conti R, et al. Potential use of silver nanoparticles on pathogenic bacteria, their toxicity and possible mechanisms of action[J]. Journal of the Brazilian Chemical Society, 2010, 21(6): 949-959. DOI:10.1590/S0103-50532010000600002 |
| [7] | Venkatesham M, Ayodhya D, Madhusudhan A, et al. A novel green one-step synthesis of silver nanoparticles using chitosan:catalytic activity and antimicrobial studies[J]. Applied Nanoscience, 2014, 4(1): 113-119. DOI:10.1007/s13204-012-0180-y |
| [8] | Barbasz A, Oć wieja M, Roman M. Toxicity of silver nanoparticles towards tumoral human cell lines U-937 and HL-60[J]. Colloids and Surfaces B:Biointerfaces, 2017, 156: 397-404. DOI:10.1016/j.colsurfb.2017.05.027 |
| [9] | Samarajeewa A D, Velicogna J R, Princz J I, et al. Effect of silver nano-particles on soil microbial growth, activity and community diversity in a sandy loam soil[J]. Environmental Pollution, 2017, 220: 504-513. DOI:10.1016/j.envpol.2016.09.094 |
| [10] | Fan W H, Liu T, Li X M, et al. Nano-TiO2 affects Cu speciation, extracellular enzyme activity, and bacterial communities in sediments[J]. Environmental Pollution, 2016, 218: 77-85. |
| [11] | Bao S P, Wang H, Zhang W C, et al. An investigation into the effects of silver nanoparticles on natural microbial communities in two freshwater sediments[J]. Environmental Pollution, 2016, 219: 696-704. DOI:10.1016/j.envpol.2016.06.071 |
| [12] | VandeVoort A R, Skipper H, Arai Y. Macroscopic assessment of nanosilver toxicity to soil denitrification kinetics[J]. Journal of Environmental Quality, 2014, 43(4): 1424-1430. DOI:10.2134/jeq2013.12.0524 |
| [13] | Xiong Z, Su Y, Chen Y, et al. Carbon nanotubes affect the toxicity of CuO nanoparticles to denitrification in marine sediments by altering cellular internalization of nanoparticle[J]. Scientific Reports, 2016, 6: 1-9. DOI:10.1038/s41598-016-0001-8 |
| [14] | Hou J, You G X, Xu Y, et al. Impacts of CuO nanoparticles on nitrogen removal in sequencing batch biofilm reactors after short-term and long-term exposure and the functions of natural organic matter[J]. Environmental Science and Pollution Research, 2016, 23(21): 22116-22125. DOI:10.1007/s11356-016-7281-1 |
| [15] |
杨丽标, 雷坤, 孟伟, 等. 上覆水中碳氮浓度对黄河沉积物反硝化速率的影响[J]. 海洋环境科学, 2016, 35(6): 868-875, 881. Yang L B, Lei K, Meng W, et al. Impact of C and N concentrations on sediments denitrification rate of the Yellow River[J]. Marine Environmental Science, 2016, 35(6): 868-875, 881. |
| [16] | Michels C, Perazzoli S, Soares H M. Inhibition of an enriched culture of ammonia oxidizing bacteria by two different nanoparticles:Silver and magnetite[J]. Science of the Total Environment, 2017, 586: 995-1002. DOI:10.1016/j.scitotenv.2017.02.080 |
| [17] | Zhang Z H, Gao P, Li M Q, et al. Influence of Silver nanoparticles on nutrient removal and microbial communities in SBR process after long-term exposure[J]. Science of the Total Environment, 2016, 569-570: 234-243. DOI:10.1016/j.scitotenv.2016.06.115 |
| [18] | Wang L P, Zheng B H, Nan B X, et al. Diversity of bacterial community and detection of nirS-and nirK-encoding denitrifying bacteria in sandy intertidal sediments along Laizhou Bay of Bohai Sea, China[J]. Marine Pollution Bulletin, 2014, 88(1-2): 215-223. DOI:10.1016/j.marpolbul.2014.09.002 |
| [19] | Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the Method[J]. Methods, 2001, 25(4): 402-408. DOI:10.1006/meth.2001.1262 |
| [20] | Harms G, Layton A C, Dionisi H M, et al. Real-time PCR quantification of nitrifying bacteria in a municipal wastewater treatment plant[J]. Environmental Science and Technology, 2003, 37(2): 343-351. DOI:10.1021/es0257164 |
| [21] | López-Gutiérrez J C, Henry S, Hallet S, et al. Quantification of a novel group of nitrate-reducing bacteria in the environment by real-time PCR[J]. Journal of Microbiological Methods, 2004, 57(3): 399-407. DOI:10.1016/j.mimet.2004.02.009 |
| [22] | Braker G, Fesefeldt A, Witzel K P. Development of PCR primer systems for amplification of nitrite reductase genes (nirK and nirS) to detect denitrifying bacteria in environmental samples[J]. Applied and Environmental Microbiology, 1998, 64(10): 3769-3775. |
| [23] |
郭丽芸, 时飞, 杨柳燕. 反硝化菌功能基因及其分子生态学研究进展[J]. 微生物学通报, 2011, 38(4): 583-590. Guo L Y, Shi F, Yang L Y. Advances in functional genes and molecular ecology in denitrifiers[J]. Microbiology China, 2011, 38(4): 583-590. |
| [24] | Alinsafi A, Adouani N, Béline F, et al. Nitrite effect on nitrous oxide emission from denitrifying activated sludge[J]. Process Biochemistry, 2008, 43(6): 683-689. DOI:10.1016/j.procbio.2008.02.008 |
| [25] |
薛静怡, 宗雅丽, 侯玉, 等. 水产养殖中亚硝酸盐毒性影响及处理的研究进展[J]. 渔业研究, 2017, 39(4): 320-324. Xue J Y, Zong Y L, Hou Y, et al. Research progress on toxicity and treatment of nitrite in aquaculture[J]. Journal of Fisheries Research, 2017, 39(4): 320-324. |
| [26] |
邹秋艳.纳米银与苯酚对反硝化菌活性的复合毒性效应与机制研究[D].哈尔滨: 哈尔滨工业大学, 2015. Zou Q Y. Composite toxic effects and mechanisms of agnps and phenol on pure denitrifying bacteria[D]. Harbin: Harbin Institute of Technology, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10213-1015981506.htm |
 2018, Vol. 39
2018, Vol. 39


