2. 中国科学院地球环境研究所, 黄土与第四纪地质国家重点实验室, 西安 710061
2. State Key Laboratory of Loess and Quaternary Geology, Institute of Earth Environment, Chinese Academy of Sciences, Xi'an 710061, China
在城市大气中, 二次有机气溶胶(secondary organic aerosol, SOA)是PM2.5的重要组分, 占PM2.5质量浓度的20%~75%[1], 其中高达80%的SOA是水溶性的[2, 3].二元羧酸类化合物(二元羧酸、酮羧酸和α-二羰基化合物)是一类重要的水溶性二次有机气溶胶(water-soluble secondary organic aerosol, WSOA)[4], 由于其蒸气压较低(约 < 10-7 Pa)、吸水性较强, 二元羧酸类SOA不仅在大气液相化学中起着重要作用[5, 6], 还可以通过形成云凝结核(cloud condensation nuclei, CCN)影响气溶胶的辐射强迫[7].
二元羧酸的一次源包括生物活动[8]、烹饪活动[9]、煤炭燃烧[10, 11]及机动车尾气[12, 13]等.但是, 有研究表明机动车尾气中排放的二元羧酸微乎其微, 可以忽略不计[14].虽然在受生物质燃烧排放的大气气溶胶中观测到高浓度的二元羧酸及α-二羰基化合物[15, 16], 但对于二元羧酸是由生物质燃烧直接排放的[17]还是由在燃烧过程中排放的有机前体物经二次氧化形成的尚无定论[18].在全球范围内, 相对于一次排放源而言, 二元羧酸主要是由不饱和脂肪酸、多环芳烃与环烷烃等有机前体物经光化学氧化反应产生的[19].其中, 草酸(C2)是分子量最小且含量最高的二元羧酸[4~6].模式研究及云观测结果表明, C2不但能在云滴或含水量较高的气溶胶中由乙二醛、甲基乙二醛和丙酮酸等前体物经液相氧化反应形成, 而且可以由长链的二元羧酸(如丙二酸、丁二酸等)经光化学分解形成[19, 20].
目前, 关于二元羧酸类SOA的研究区域主要包括海洋[21]、森林[22]、高山[3, 6, 23]和城市[24~26]地区, 但主要集中在大城市地区(如北京、南京、西安), 对小城市[27]的研究相对较少.源排放清单显示山东省是我国PM2.5污染最严重、霾天气出现最频繁的省份之一[28].菏泽市位于山东省的西南部, 由于冬季利用煤炭及生物质燃烧取暖, 导致大量碳质气溶胶被释放到大气中造成菏泽市冬季霾天气频发, 致使菏泽市大气质量一直处于山东省末位[29].因为二元羧酸水溶性较高且吸湿性较强, 容易与微小粒子结合形成CCN, 降低大气能见度, 所以在霾天气形成过程中起着重要作用[1, 4].因此对菏泽市冬季PM2.5中二元羧酸类SOA的昼夜变化特征及形成机制的研究具有重要意义, 以期为菏泽市进一步开展PM2.5的化学组成特征及来源解析提供基础数据, 同时为菏泽市乃至整个京津冀地区的PM2.5污染治理提供科学依据.
1 材料与方法 1.1 样品采集采样地点位于菏泽学院教学办公综合楼楼顶(35°16.16 ′N; 115°27.60′E), 距地面约20 m, 周围无高大建筑物及无明显污染源, 能够反映菏泽市市区大气质量状况.为探究菏泽市二元羧酸类极性化合物的昼夜变化特征, 于2017年冬季(12月)利用KC-120H型中流量采样器(青岛崂山电子仪器有限公司)分为昼夜进行PM2.5样品的采集, 昼夜样品各采集12 h(白天07:00~19:00;夜晚19:00~次日07:00), 平均流量为100L ·min-1, 所采用的石英滤膜(Whatman, QM-A)直径为90mm.采样前所有滤膜均在450℃的马弗炉中焙烧6 h, 采样后所有滤膜用铝箔封装并保存在-18℃的冰箱中待分析.另外, 利用紫外吸收分析仪(Thermo Electron Corporation, Model 49C)对O3浓度进行监测.
1.2 二元羧酸类极性化合物分析二元羧酸类极性化合物包括二元羧酸、酮羧酸及α-二羰基化合物, 本研究中采用三氟化硼/正丁醇衍生化的方法[12, 23]进行分析.首先, 取1/4滤膜剪碎置于15 mL样品瓶中, 加入5 mL超纯水(Mili Q, R>18.2 MΩ ·cm), 超声萃取3×15 min, 然后用0.45 μm的水系过滤器过滤以去除杂质, 合并过滤液至15 mL梨形瓶中, 在55℃水温条件下采用旋转蒸发仪蒸发至近干, 加入300 μL的三氟化硼(14%)/正丁醇溶液于100℃反应1 h, 然后依次加入5 mL正己烷、300 μL乙腈和5 mL超纯水, 振荡萃取4次, 合并有机相萃取液采用旋转蒸发仪浓缩至1 mL, 氮吹定容至100 μL待测.衍生化后的样品使用气相色谱-质谱联用仪(Agilent, 7890A-5975C)、气相色谱-氢火焰离子化检测仪(Agilent, 6890-FID)分别进行定性、定量分析.
1.3 水溶性无机离子与左旋葡聚糖的分析取1/8滤膜剪碎并置于15 mL样品瓶中, 加入10 mL去离子水(R>18.2 MΩ ·cm)溶解, 超声萃取4×15 min, 脱色摇床振荡1 h, 然后用0.45 μm的水系过滤器过滤, 过滤后的溶液利用Dionex-500型和Dionex-600型离子色谱仪分别分析阳离子(K+、Na+、NH4+、Ca2+、Mg2+)和阴离子(Cl-、Br-、NO3-、SO42-).对于左旋葡聚糖的分析, 首先将1/8滤膜置于15 mL聚四氟乙烯材质的样品瓶中, 加入10 mL浓度为20 mmol ·L-1的叠氮化钠溶液振荡60 min, 然后用0.22 μm微孔尼龙滤膜过滤, 最后经RP净化小柱(Dionex OnGuard Ⅱ RP)后利用Dionex ICS-5000型离子色谱仪进行监测[30].
1.4 气溶胶酸度和含水量的计算气溶胶的实际酸度(pHIS)、液相水含量(LWC)不能直接通过实验的方式获得, 但可以通过气溶胶模型计算得出, 本研究利用ISORROPIA-Ⅱ模型中的“forward”模式对二者进行计算[24].首先结合实际环境中的温度与相对湿度数据, 计算“Na+-NH4+-K+-Ca2+-Mg2+-Cl--NO3--SO42-”平衡体系的组成与LWC, 然后利用式(1)计算pHIS.

|
(1) |
式中, Hair+(μg ·m-3)是单位体积空气中平衡颗粒水合氢离子的浓度, 其中, Hair+与LWC(μg ·m-3)均利用ISORROPIA-Ⅱ模型计算得出.
2 结果与讨论 2.1 二元羧酸类化合物与左旋葡聚糖的浓度水平与分子组成菏泽市冬季PM2.5中二元羧酸类极性化合物的昼夜变化特征如表 1所示, 其分子组成如图 1所示.菏泽市冬季白天PM2.5的浓度是夜晚的1.3倍, 其平均浓度为(98.2±49.0) μg ·m-3, 高于国家空气质量二级标准(GB 3095-2012, 75 μg ·m-3), 说明菏泽市冬季PM2.5污染较严重.如表 1所示, 白天二元羧酸的总浓度[(1 321±885) ng ·m-3]是夜晚[(641±447) ng ·m-3]的2.1倍, 其平均浓度[(987±778) ng ·m-3]不仅高于高山地区[6, 23]、海洋地区[21]、大陆背景点[31], 还高于中国其他城市(如北京[21]、成都[32]等), 但低于西安[26]和印度的坎普尔[7].与上述地区相同, 白天和夜晚的草酸(C2)均是浓度最高的二元羧酸(表 1).如图 1所示, C2在白天和夜晚分别占二元羧酸总浓度的52%、33%, 其次为邻苯二甲酸(Ph)、丁二酸(C4)、丙二酸(C3)和对苯二甲酸(tPh), 与其他城市地区是相似的, 例如西安(C2>tPh>Ph>C4>C3)[26]、成都(C2>Ph>C4>C3>tPh)[32], 但与受人为污染源较小的偏远地区不同, 例如青海湖[31]、黄山[6]和泰山[23]等, 其分子组成均呈C2>C3>C4>C9>Ph的变化特征.因为在城市地区来自人为污染源的前体物较多(例如多环芳烃和增塑剂等), 导致Ph或tPh的浓度较高, 更甚者远高于C2[10, 25].例如在蒙古的乌兰巴托市, 冬季PM2.5中二元羧酸类SOA的分子组成的顺序为tPh>C2>C4>Ph, 这是因为冬季使用煤炭和木材作为燃料进行取暖和烹饪, 并且一些贫民甚至使用含有聚酯纤维的垃圾、塑料瓶和塑料袋作为生活燃料, 导致该区的tPh急剧上升[10].有研究表明, 煤炭燃烧可排放出大量的芳香族化合物(如萘), 可经二次氧化反应形成Ph等[26].由此可以得出, 菏泽市冬季PM2.5中二元羧酸的污染处于较高水平, 且主要来自煤炭及生活垃圾的燃烧.

|
A:二元羧酸; B:酮羧酸; C:α-二羰基化合物 图 1 菏泽市冬季二元羧酸、酮羧酸及α-二羰基化合物占总二元羧酸类SOA浓度相对含量的昼夜变化特征 Fig. 1 Diurnal variations in relative abundance of dicarboxylic acids, ketocarboxylic acids, and α-dicarbonyls in Heze City in winter |
|
|
表 1 菏泽市2017年冬季二元羧酸、酮羧酸、α-二羰基化合物及其它组分浓度的昼夜变化特征 Table 1 Diurnal variations of dicarboxylic acids, ketocarboxylic acids, α-dicarbonyls and other species from Heze City during daytime and nighttime in winter, 2017 |
菏泽市冬季PM2.5中酮羧酸和α-二羰基化合物的平均浓度分别为(261±158) ng ·m-3和(103±62) ng ·m-3.这两类化合物是由有机前体物经光化学氧化反应形成的或直接由化石燃料和生物质燃烧直接排放, 然后经光化学氧化反应形成二元羧酸, 因此, 这两类化合物是二元羧酸的重要前体物[12, 15].如图 1所示, 浓度最高的酮羧酸为丙酮酸(Pyr)、其次为乙醛酸(ωC2)和4-氧代丁酸(ωC4). α-二羰基化合物包括乙二醛(Gly)和甲基乙二醛(mGly), mGly的平均浓度约是Gly的2倍.因为在大气中mGly与氧化剂(如·OH)发生氧化反应的速度比Gly慢, 且其来源比Gly多, 所以mGly的浓度比Gly高[26, 31].由于左旋葡聚糖(levoglucosan, Levo)的化学性质稳定且不易被氧化, 因此被看作生物质燃烧的指示物[33].由表 1可知, 白天Levo的浓度约是夜晚的1.4倍, 表明白天生物质燃烧活动比夜晚强.
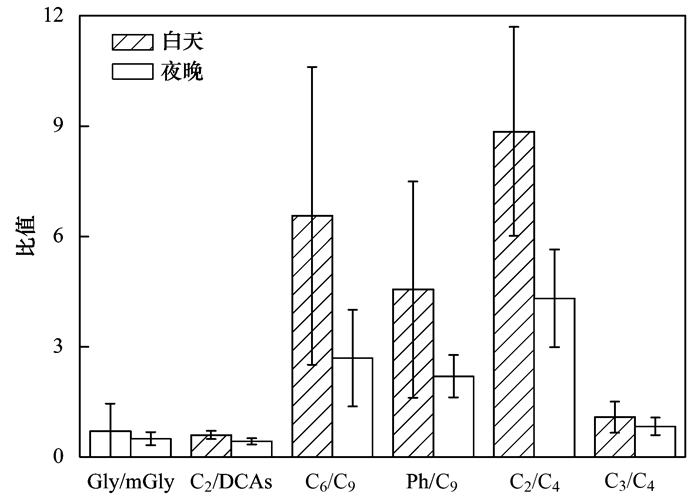
2.2 氧化程度与人为源排放强度的昼夜变化特征有研究表明, 乙二醛与甲基乙二醛的比值(Gly/mGly)可用来表征气溶胶的老化程度, Gly/mGly的比值越小, 气溶胶的老化程度越深, 这是因为气溶胶中mGly与羟基自由基(·OH)的氧化速度比Gly慢[26].由图 2可知, 白天Gly/mGly的比值高于夜晚, 表明白天气溶胶的老化程度比夜晚更深. C2主要是由人为源或生物源排放的气体前体物及长链的二元羧酸经光化学氧化产生的, 因此C2与二元羧酸总浓度的比值(C2/DCAs)可作为气溶胶氧化程度的示踪物, 且C2/DCAs的比值随着气溶胶氧化程度的增强而升高[23, 24]. 白天C2/DCAs的比值约是夜晚的1.4倍, 再次表明白天气溶胶的氧化程度较强, 这是因为与夜晚相比, 白天的太阳辐射较强且温度较高, 有利于前体物经气-固相分配及非均相氧化反应形成C2, 导致白天C2/DCAs的比值比夜晚高. Ph和C6是由来自人为源排放的环己烷类化合物和芳香烃类化合物通过光化学氧化生成的, 被看作人为源的示踪物[12, 15].而C9主要是由来自植物源排放的不饱和脂肪酸经光化学氧化形成的, 被看作自然源的示踪物[4].因此, C6/C9和Ph/C9这两个比值均可用来指示人为源与自然源对气溶胶的相对贡献[15, 16].如图 2所示, 菏泽市冬季C6/C9和Ph/C9的比值均表现出昼高夜低的变化特征, 表明白天人为源的排放对气溶胶的贡献比夜晚大, 与其他城市的研究结果是相同的[32, 34]. C6/C9和Ph/C9的平均比值分别为4.7±3.6、34±24, 不仅高于海洋[21]、高山[4, 6, 23]等偏远地区, 还高于其他城市地区(如北京[34]、西安[26]和印度的坎普尔[7]), 表明菏泽市冬季人为污染所占的比例较高.
|
Ph/C9的数值缩小10倍 图 2 特征性比值的昼夜变化特征 Fig. 2 Diurnal variations of diagnostic ratios |
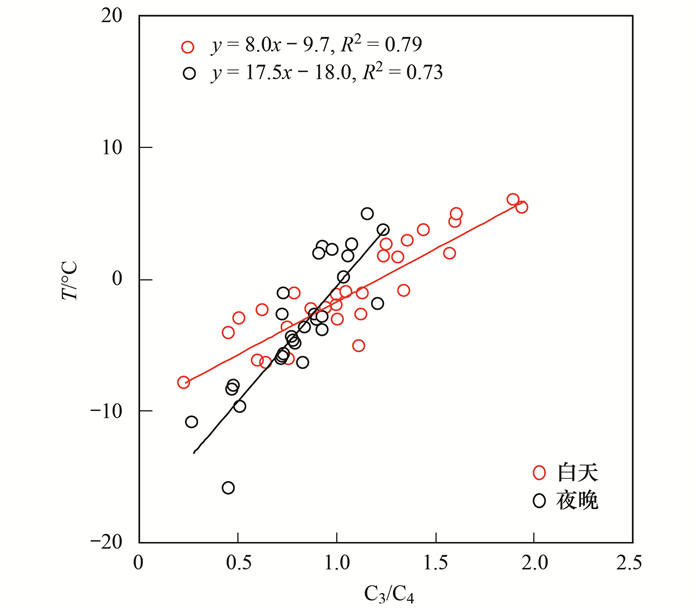
有大量研究已经证实C4可经羟基化反应形成C2和C3, 由于C3的热力学性质极不稳定, C3可进一步形成C2, 因此C2/C4和C3/C4这两个比值常被用来作为有机气溶胶老化的指示物[10, 11].菏泽市C2/C4和C3/C4的平均比值分别为6.6±3.2、1.0±0.4, 不仅低于由汽车尾气(C2/C4:7.1; C3/C4:1.3)[35]排放的气溶胶, 还低于来自长距离传输的老化气溶胶, 如青海湖(C2/C4:11±7.2; C3/C4:2.2±1.3)[31]和太平洋地区(C2/C4:8.7; C3/C4:3.0)[21], 但高于生物质燃烧排放(C2/C4:5.0; C3/C4:0.7)的新鲜气溶胶[36], 表明菏泽市冬季二元羧酸类化合物受汽车尾气及长距离传输的影响较小, 主要来自由生物质燃烧排放的前体物经氧化形成的.另外, C2/C4和C3/C4的比值均呈昼高夜低的变化特征(图 2), 表明白天气溶胶的老化程度比夜晚深. Meng等[4]和Pavuluri等[37]认为当二元羧酸受远源输入的影响较强时, C3/C4的比值与温度间相关性很差, 反之, 受本地源的影响较强.如图 3所示, 菏泽市冬季C3/C4的比值与温度间均呈显著的相关性(R2>0.7), 表明菏泽市二元羧酸主要受本地污染源的影响, 而受长距离传输的影响很小.
|
图 3 C3/C4的比值与温度(T)间的相关性分析 Fig. 3 Linear fit regression of the mass ratios of C3/C4 with temperature (T) during daytime and nighttime |
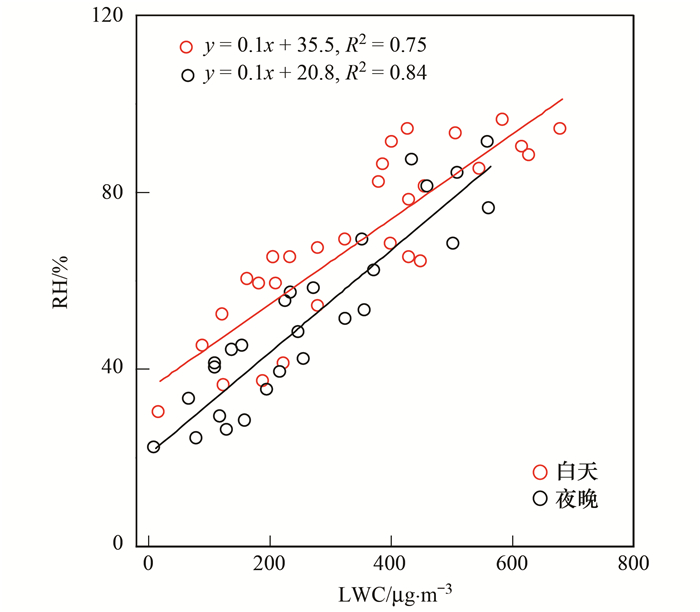
因为C2是分子量最小、浓度最高的二元羧酸, 所以重点讨论C2的形成机制及影响因素.在线数据、外场观测及烟雾箱实验均已证明C2主要是由乙二醛、甲基乙二醛和乙醛酸等前体物在液相中经酸催化氧化反应形成的[4, 11, 20, 38].虽然SO42-与C2在化学组成上没有任何关系, 但由于SO42-是在液相中形成的, 因此SO42-与C2的相关性分析可作为C2液相形成机制的有力证据[10].在本研究中, 无论是白天还是夜晚, C2与SO42-之间均呈显著的相关性[图 4(a)], 说明二者在气溶胶中经历着共同的液相形成过程.基于ISORROPIA-Ⅱ模型的计算, 发现C2与pHIS间具有较强的负相关性[图 4(b)], 表明酸性条件有利于C2的形成. LWC是由相对湿度(RH)与吸湿性组分(例如SO42-、NO3-和NH4+等)共同决定的, 它不仅是气溶胶化学反应的参与者, 也是液相反应的介质, 因此在气溶胶中担任着重要角色[33].如图 5所示, LWC与RH有较强的相关性, 表明RH是影响LWC的一个重要因素.然而, LWC与C2间却未表现出相关性[图 4(c)], 与其他地区的研究结果(华山[4]、黄山[6])是一致的.虽然较高的LWC气溶胶环境有利于更多的气态前体物(如Gly、mGly等)进入液相中形成C2, 但较高的LWC会降低气溶胶的酸度, 使得C2的酸催化氧化反应受到抑制, 所以LWC与C2间的相关性较差.

|
图 4 草酸(C2)的浓度分别与SO42-、实际酸度(pHIS)、液相含水量(LWC)、O3的浓度间的相关性分析 Fig. 4 Linear fit regressions of oxalic acid (C2) with SO42-, in-situ acidity of particles (pHIS), liquid water content (LWC), and O3 during daytime and nighttime |
|
图 5 液相含水量(LWC)与相对湿度(RH)间的相关性分析 Fig. 5 Linear fit regression of liquid water content (LWC) with relative humidity (RH) during daytime and nighttime |
在本研究中, 因为未对羟基自由基(·OH)和硝基自由基(·NO3)等氧化剂进行监测, 而仅监测了O3的浓度, 所以本研究以O3作为氧化剂的示踪物来分析其对C2的形成及气溶胶氧化程度的影响.如图 4(d)与表 2所示, 白天O3的浓度不仅与C2呈显著的相关性, 与气溶胶氧化程度的指示物(C2/DCAs、C2/C4和C3/C4的比值)也呈显著的正相关关系, 但这种显著的相关性在夜晚并未发现. Mochizuki等[22]在日本的富士山的研究结果表明, O3的浓度仅在白天与C2呈显著的相关性.由此可以得出, 白天的O3不仅可以促进C2的生成, 还有利于提高气溶胶的氧化程度, 而夜晚C2的生成可能受到·NO3和H2O2等氧化剂的影响[39].另外, 有研究表明, 温度的升高有利于C2的形成和气溶胶的老化.因此, 无论在白天还是夜晚, 温度与C2的浓度和C2/DCAs的比值均呈显著的正相关关系(表 2).
|
|
表 2 草酸(C2)、特征性比值(C2/DCAs、C2/C4与C3/C4)分别与O3及温度间的相关系数(R2) 1) Table 2 Correlation analysis (R2) of the oxalic acid (C2) and diagnostic rations (C2/DCAs, C2/C4, and C3/C4) with O3 and temperature |
2.4 生物质燃烧对气溶胶的影响
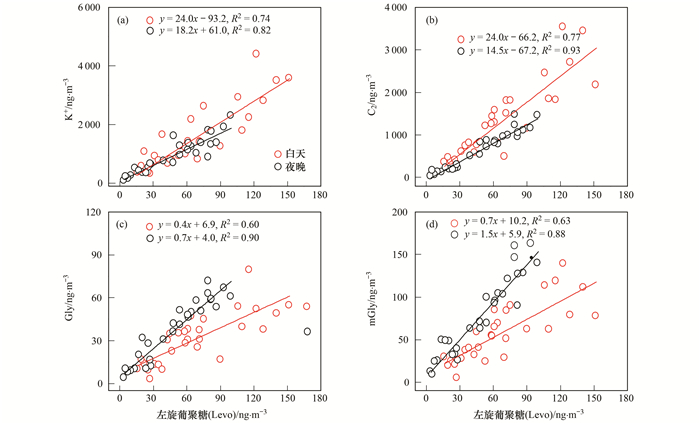
在全球对流层中, 生物质燃烧是痕量气体和大气细颗粒物的第二大来源[40].生物质燃烧不但可以直接排放出糖类、醛类等大量水溶性有机污染物, 而且这些污染物极易发生光化学氧化反应, 进而形成大量水溶性二次有机气溶胶(WSOA), 最终增加了霾天气形成的几率[15, 16]. K+不仅来自矿物粉尘、海洋源, 还来自生物质燃烧[31].因为菏泽属于内陆城市, 离海洋较远, 所以受海洋源的影响可忽略不计[29].如图 6(a)所示, K+虽然与Ca2+的相关性较差(R2 < 0.1), 但是与Levo相关很强(R2>0.7).因为Ca2+是矿物粉尘的示踪物, 所以可以得出菏泽市冬季K+主要来自生物质燃烧源, 而非矿物粉尘源.在由生物质燃烧排放的烟羽中, K+/OC的比值约为0.06(范围为0.03~0.16)[41, 42].如表 1所示, 白天与夜晚K+/OC的比值分别为0.06±0.03、0.06±0.02, 浓度范围分别为0.03~0.13、0.03~0.10, 再次证明生物质燃烧对菏泽市冬季的K+与OC均有重要影响.
|
图 6 左旋葡聚糖(Levo)与K+、草酸(C2)、乙二醛(Gly)、甲基乙二醛(mGly)的相关性分析 Fig. 6 Linear fit regressions of levoglucosan (Levo) with K+, oxalic acid (C2), glyoxal (Gly), and methyglyoxal (mGly) |
有大量研究表明, 生物质燃烧是二元羧酸及α-二羰基化合物的重要来源之一[3, 7, 15, 16, 24].由二元羧酸类化合物的分子组成表明, C2是浓度最高的二元羧酸, 因此本研究利用C2与Levo的相关性来分析生物质燃烧对二元羧酸的影响.由图 6(b)可知, 在白天和夜晚C2与Levo均呈显著的相关性(R2>0.7), 表明生物质燃烧是菏泽市冬季二元羧酸的重要来源之一.白天C2/Levo的比值是夜晚的1.5倍(表 1), 与Sorathia等[7]在印度恒河平原的研究结果一致, 表明白天C2经液相氧化反应的形成过程增强, 这是由于白天LWC的浓度比夜晚高(表 1), 有利于气体前体物转移到液相中继而形成C2. Kawamura等[15, 16]认为生物质燃烧(例如小麦秸秆燃烧)可排放出大量的α-二羰基化合物(Gly和mGly).在菏泽冬季气溶胶中, Gly和mGly与LG间的相关性均很强[图 6(c)、6(d)], 再次证实生物质燃烧是α-二羰基化合物的重要来源之一.
3 结论(1) 菏泽市冬季PM2.5中白天二元羧酸的总浓度是夜晚的2.1倍, 平均浓度为(987±778) ng ·m-3, 其中C2的浓度最高, 其次为Ph、C4、C3和tPh, 与其它城市地区的分子组成是相似的, 但与受人为排放源影响较小的偏远地区不同.
(2) 白天Gly/mGly、C2/DCAs、C2/C4和C3/C4的比值均呈昼高夜低的变化特征, 表明白天气溶胶的老化程度比夜晚更深.另外, C6/C9和Ph/C9的比值也呈昼高夜低的变化特征, 表明白天气溶胶受人为源污染物的影响更大.
(3) 由K+/OC的比值及左旋葡聚糖(Levo)与K+、二元羧酸、α-二羰基化合物的相关性分析可知, 生物质燃烧是菏泽市冬季K+、OC及二元羧酸类化合物的重要来源之一.
| [1] | Huang R J, Zhang Y L, Bozzetti C, et al. High secondary aerosol contribution to particulate pollution during haze events in China[J]. Nature, 2014, 514(7521): 218-222. DOI:10.1038/nature13774 |
| [2] | Hallquist M, Wenger J C, Baltensperger U, et al. The formation, properties and impact of secondary organic aerosol:current and emerging issues[J]. Atmospheric Chemistry and Physics, 2009, 9(14): 5155-5236. |
| [3] | Zhu Y H, Yang L X, Chen J M, et al. Molecular distributions of dicarboxylic acids, oxocarboxylic acids, and α-dicarbonyls in PM2.5 collected at Mt. Tai, in North China in 2014[J]. Atmospheric Chemistry and Physics Discussions, 2018, 1-31. DOI:10.5194/acp-2017-1240 |
| [4] | Meng J J, Wang G H, Li J J, et al. Seasonal characteristics of oxalic acid and related SOA in the free troposphere of Mt. Hua, central China:implications for sources and formation mechanisms[J]. Science of the Total Environment, 2014, 493: 1088-1097. DOI:10.1016/j.scitotenv.2014.04.086 |
| [5] | Bilde M, Barsanti K, Booth M, et al. Saturation vapor pressures and transition enthalpies of low-volatility organic molecules of atmospheric relevance:from dicarboxylic acids to complex mixtures[J]. Chemical Reviews, 2015, 115(10): 4115-4156. DOI:10.1021/cr5005502 |
| [6] |
孟静静, 侯战方, 张二勋, 等. 黄山PM10中二元羧酸类化合物的季节变化特征及其来源[J]. 环境科学, 2017, 38(7): 2688-2697. Meng J J, Hou Z F, Zhang E X, et al. Seasonal variation and sources of dicarboxylic acids and related compounds in PM10 from Mt. Huangshan[J]. Environmental Science, 2017, 38(7): 2688-2697. |
| [7] | Sorathia F, Rajput P, Gupta T. Dicarboxylic acids and levoglucosan in aerosols from Indo-Gangetic Plain:inferences from day night variability during wintertime[J]. Science of the Total Environment, 2018, 624: 451-460. DOI:10.1016/j.scitotenv.2017.12.124 |
| [8] | Dutton M V, Evans C S. Oxalate production by fungi:its role in pathogenicity and ecology in the soil environment[J]. Canadian Journal of Microbiology, 1996, 42(9): 881-895. DOI:10.1139/m96-114 |
| [9] | Rogge W F, Hildemann L M, Mazurek M A, et al. Sources of fine organic aerosol. 1. charbroilers and meat cooking operations[J]. Environmental Science & Technology, 1991, 25(6): 1112-1125. |
| [10] | Jung J, Tsatsral B, Kim Y J, et al. Organic and inorganic aerosol compositions in Ulaanbaatar, Mongolia, during the cold winter of 2007 to 2008:dicarboxylic acids, ketocarboxylic acids, and α-dicarbonyls[J]. Journal of Geophysical Research, 2010, 115(D22): D22203. DOI:10.1029/2010JD014339 |
| [11] | Wang G H, Kawamura K, Cheng C L, et al. Molecular distribution and stable carbon isotopic composition of dicarboxylic acids, ketocarboxylic acids, and α-dicarbonyls in size-resolved atmospheric particles from Xi'an City, China[J]. Environmental Science & Technology, 2012, 46(9): 4783-4791. |
| [12] | Kawamura K, Kaplan I R. Motor exhaust emissions as a primary source for dicarboxylic acids in Los Angeles ambient air[J]. Environmental Science & Technology, 1987, 21(1): 105-110. |
| [13] | Fraser M P, Cass G R, Simoneit B R T. Gas-phase and particle-phase organic compounds emitted from motor vehicle traffic in a Los Angeles roadway tunnel[J]. Environmental Science & Technology, 1998, 32(14): 2051-2060. |
| [14] | Stone E A, Hedman C J, Zhou J B, et al. Insights into the nature of secondary organic aerosol in Mexico City during the MILAGRO experiment 2006[J]. Atmospheric Environment, 2010, 44(3): 312-319. DOI:10.1016/j.atmosenv.2009.10.036 |
| [15] | Kawamura K, Okuzawa K, Aggarwal S G, et al. Determination of gaseous and particulate carbonyls (glycolaldehyde, hydroxyacetone, glyoxal, methylglyoxal, nonanal and decanal) in the atmosphere at Mt. Tai[J]. Atmospheric Chemistry and Physics, 2013, 13(10): 5369-5380. DOI:10.5194/acp-13-5369-2013 |
| [16] | Kawamura K, Tachibana E, Okuzawa K, et al. High abundances of water-soluble dicarboxylic acids, ketocarboxylic acids and α-dicarbonyls in the mountaintop aerosols over the North China Plain during wheat burning season[J]. Atmospheric Chemistry and Physics, 2013, 13(16): 8285-8302. DOI:10.5194/acp-13-8285-2013 |
| [17] | Jaffrezo J L, Davidson C I, Kuhns H D, et al. Biomass burning signatures in the atmosphere of central Greenland[J]. Journal of Geophysical Research, 1998, 103(D23): 31067-31078. |
| [18] | Allen A G, Cardoso A A, da Rocha G O. Influence of sugar cane burning on aerosol soluble ion composition in Southeastern Brazil[J]. Atmospheric Environment, 2004, 38(30): 5025-5038. |
| [19] | Myriokefalitakis S, Tsigaridis K, Mihalopoulos N, et al. In-cloud oxalate formation in the global troposphere:a 3-D modeling study[J]. Atmospheric Chemistry and Physics, 2011, 11(12): 5761-5782. DOI:10.5194/acp-11-5761-2011 |
| [20] | Cheng C L, Li M, Chan C K, et al. Mixing state of oxalic acid containing particles in the rural area of Pearl River Delta, China:implications for the formation mechanism of oxalic acid[J]. Atmospheric Chemistry and Physics, 2017, 17(15): 9519-9533. DOI:10.5194/acp-17-9519-2017 |
| [21] | Hoque M, Kawamura K, Uematsu M. Spatio-temporal distributions of dicarboxylic acids, ω-oxocarboxylic acids, pyruvic acid, α-dicarbonyls and fatty acids in the marine aerosols from the North and South Pacific[J]. Atmospheric Research, 2017, 185: 158-168. DOI:10.1016/j.atmosres.2016.10.022 |
| [22] | Mochizuki T, Kawamura K, Miyazaki Y, et al. Secondary formation of oxalic acid and related organic species from biogenic sources in a larch forest at the northern slope of Mt. Fuji[J]. Atmospheric Environment, 2017, 166: 255-262. DOI:10.1016/j.atmosenv.2017.07.028 |
| [23] |
孟静静, 侯战方, 刘晓迪, 等. 泰山夏季PM2.5中二元羧酸类SOA的分子组成及来源[J]. 环境科学, 2017, 38(2): 445-452. Meng J J, Hou Z F, Liu X D, et al. Compositions and sources of summertime dicarboxylic acids and related SOA in PM2.5 from Mt. Taishan[J]. Environmental Science, 2017, 38(2): 445-452. |
| [24] | Wang J Y, Wang G H, Gao J, et al. Concentrations and stable carbon isotope compositions of oxalic acid and related SOA in Beijing before, during, and after the 2014 APEC[J]. Atmospheric Chemistry and Physics, 2017, 17(2): 981-992. DOI:10.5194/acp-17-981-2017 |
| [25] | Wang G H, Niu S L, Liu C E, et al. Identification of dicarboxylic acids and aldehydes of PM10 and PM2.5 aerosols in Nanjing, China[J]. Atmospheric Environment, 2002, 36(12): 1941-1950. DOI:10.1016/S1352-2310(02)00180-2 |
| [26] | Cheng C L, Wang G H, Zhou B H, et al. Comparison of dicarboxylic acids and related compounds in aerosol samples collected in Xi'an, China during haze and clean periods[J]. Atmospheric Environment, 2013, 81: 443-449. DOI:10.1016/j.atmosenv.2013.09.013 |
| [27] | Liu H X, Kawamura K, Kunwar B, et al. Sources and formation processes of short-chain saturated diacids (C2-C4) in inhalable particles (PM10) from Huangshi City, Central China[J]. Atmosphere, 2017, 8(11): 213. |
| [28] | Cao G L, Zhang X Y, Gong S L, et al. Emission inventories of primary particles and pollutant gases for China[J]. Chinese Science Bulletin, 2011, 56(8): 781-788. DOI:10.1007/s11434-011-4373-7 |
| [29] |
刘泽珺, 吴建会, 张裕芬, 等. 菏泽市PM2.5碳组分季节变化特征[J]. 环境科学, 2017, 38(12): 4943-4950. Liu Z J, Wu J H, Zhang Y F, et al. Seasonal variation of carbon fractions in PM2.5 in Heze[J]. Environmental Science, 2017, 38(12): 4943-4950. |
| [30] |
刘晓迪, 孟静静, 侯战方, 等. 济南市夏、冬季PM2.5中化学组分的季节变化特征及来源解析[J]. 环境科学, 2018, 39(9): 4014-4025. Liu X D, Meng J J, Hou Z F, et al. Seasonal variation and source analysis of chemical characteristic in PM2.5 during the summer and winter in Jinan City[J]. Environmental Science, 2018, 39(9): 4014-4025. |
| [31] | Meng J J, Wang G H, Li J J, et al. Atmospheric oxalic acid and related secondary organic aerosols in Qinghai Lake, a continental background site in Tibet Plateau[J]. Atmospheric Environment, 2013, 79: 582-589. DOI:10.1016/j.atmosenv.2013.07.024 |
| [32] | Cheng C L, Wang G H, Meng J J, et al. Size-resolved airborne particulate oxalic and related secondary organic aerosol species in the urban atmosphere of Chengdu, China[J]. Atmospheric Research, 2015, 161-162: 134-142. |
| [33] | Li J J, Wang G H, Cao J J, et al. Observation of biogenic secondary organic aerosols in the atmosphere of a mountain site in central China:temperature and relative humidity effects[J]. Atmospheric Chemistry and Physics, 2013, 13(22): 11535-11549. DOI:10.5194/acp-13-11535-2013 |
| [34] | He N N, Kawamura K, Okuzawa K, et al. Diurnal and temporal variations of water-soluble dicarboxylic acids and related compounds in aerosols from the northern vicinity of Beijing:implication for photochemical aging during atmospheric transport[J]. Science of the Total Environment, 2014, 499: 154-165. |
| [35] | Ho K F, Lee S C, Cao J J, et al. Dicarboxylic acids, ketocarboxylic acids and dicarbonyls in the urban roadside area of Hong Kong[J]. Atmospheric Environment, 2006, 40(17): 3030-3040. |
| [36] | Kundu S, Kawamura K, Andreae T W, et al. Molecular distributions of dicarboxylic acids, ketocarboxylic acids and α-dicarbonyls in biomass burning aerosols:implications for photochemical production and degradation in smoke layers[J]. Atmospheric Chemistry and Physics, 2010, 10(5): 2209-2225. DOI:10.5194/acp-10-2209-2010 |
| [37] | Pavuluri C M, Kawamura K, Swaminathan T. Water-soluble organic carbon, dicarboxylic acids, ketoacids, and α-dicarbonyls in the tropical Indian aerosols[J]. Journal of Geophysical Research, 2010, 115(D11): D11302. |
| [38] | Gao S, Ng N L, Keywood M, et al. Particle phase acidity and oligomer formation in secondary organic aerosol[J]. Environmental Science & Technology, 2004, 38(24): 6582-6589. |
| [39] | Claeys M, Graham B, Vas G, et al. Formation of secondary organic aerosols through photooxidation of isoprene[J]. Science, 2004, 303(5661): 1173-1176. DOI:10.1126/science.1092805 |
| [40] | Akagi S K, Yokelson R J, Wiedinmyer C, et al. Emission factors for open and domestic biomass burning for use in atmospheric models[J]. Atmospheric Chemistry and Physics, 2011, 11(9): 4039-4072. DOI:10.5194/acp-11-4039-2011 |
| [41] | Andreae M O, Merlet P. Emission of trace gases and aerosols from biomass burning[J]. Global Biogeochemical Cycles, 2001, 15(4): 955-966. |
| [42] | Rajput P, Sarin M, Sharma D, et al. Characteristics and emission budget of carbonaceous species from post-harvest agricultural-waste burning in source region of the Indo-Gangetic Plain[J]. Tellus B:Chemical and Physical Meteorology, 2014, 66(1): 21026. DOI:10.3402/tellusb.v66.21026 |
 2018, Vol. 39
2018, Vol. 39

