2. 江苏华新城市规划市政设计研究院有限公司, 连云港 200000
2. Jiangsu Huaxin Urban Planning & Design Institute Co., Ltd., Lianyungang 200000, China
近年来, 环境中微量有机污染物(OMPs)的赋存[1, 2]及迁移转化[3]引起国内外学者的广泛关注, 这些有机污染物种类复杂, 如抗生素、止痛药、避孕药、镇静药、杀菌剂、除草剂、阻燃剂等[4~6].而城市污水厂是OMPs向环境中迁移的重要途径, 这些物质在污水中的浓度虽低(μg ·L-1或ng ·L-1级浓度水平), 但排放到水体后产生累积效应, 从而对水环境生物及人体健康造成潜在的危害[7~10].现有污水厂多采用活性污泥处理工艺, 大量研究表明活性污泥法处理工艺对大部分OMPs去除效果不佳[11~13], 因此增加污水深度处理是强化削减污水中OMPs的可选方案.
臭氧工艺具有优良的水质净化效果, 从而被广泛应用于污水消毒、氧化分解难降解有机物[14, 15].臭氧和有机分子反应主要基于直接反应和自由基反应[16], 在臭氧分解过程中会诱发产生羟基自由基, 而自由基反应被认为是快速高效的氧化途径[17]. OMPs化学结构复杂, 其在臭氧过程中的氧化规律研究仍不完善.有研究表明, 污水中OMPs在臭氧过程中的去除效果和二级反应速率常数有密切关系[4].由于二级反应速率常数测定过程复杂, 而从分子结构角度解析OMPs在臭氧过程中的去除有助于了解臭氧反应本质.此外, 由于OMPs种类规模巨大, 仅根据选定的污染物评价水质安全具有片面性.臭氧在与出水有机物反应过程中会产生大量未知副产物, 其水质毒性水平未知.而SOS/umu遗传毒性试验是水质遗传毒性分析的ISO标准方法, 其在污水水质安全性评价方面具有重要应用价值[14, 18].因此, 采用生物毒理试验作为化学分析指标的补充, 对于水质风险评价具有重要意义.
本文以厌氧/缺氧/好氧工艺联合臭氧(AAO-O3)作为研究对象, 通过考察14种OMPs在AAO-O3过程中的降解行为, 分析OMPs在活性污泥系统中的去除途径, 并从分子结构角度探究臭氧氧化过程中OMPs的降解机制, 此外通过遗传毒性实验得到更加综合直观的水质安全数据, 对污水深度处理出水的水质安全保障具有重要意义.
1 材料与方法 1.1 仪器与试剂超高效液相色谱串联质谱仪(2777C-ACQYITY UPLC-XevoTM TQ MS, Waters公司, 美国); 臭氧发生器(HY-003-20A, 广州佳环, 中国); 酶标分析仪(RT-6000, 深圳雷杜, 中国); 分光光度计(T6, 北京普析, 中国); Oasis HLB萃取小柱(6 CC 200 mg, Waters公司, 美国); AAO系统及臭氧反应装置由哈尔滨工业大学仪器设备有限公司加工制作. 14种OMPs标准品:诺氟沙星(NOR)、卡马西平(CBZ)、恩诺沙星(ENR)、金霉素(CRT)、磺胺甲嘧啶(SMZ)购自美国药典U. S. pharmacopeial Convention; 磺胺甲恶唑(SMX)、布洛芬(IBP)、阿替洛尔(ATL)、苯扎贝特(BF)、吉非罗齐(GFZ)、萘普生(NPX)、土霉素(OTC)购自美国sigma-aldrich公司; 咖啡因(CFF)购自日本Wako公司; 阿特拉津(ATZ)购自中国Energy Chemical公司.
1.2 实验方案及反应装置AAO反应器进水采用模拟污水(生活污水:人工配水为1:1), 其中生活污水取自哈尔滨工业大学家属区, 人工配水中葡萄糖为0.30 g ·L-1、乙酸钠为0.13g ·L-1、氯化铵为0.20g ·L-1、碳酸氢钠为0.46 g ·L-1、磷酸二氢钠为0.04g ·L-1、硫酸镁为0.05g ·L-1、氯化钙为0.01 g ·L-1.同时在进水水箱中投加14种OMPs母液(200 mg ·L-1), 每种目标物的投加浓度约为20μg ·L-1.
反应器连续运行70 d, 每隔3~5 d取样分析常规指标.为评价AAO-O3对OMPs的降解能力, 在反应器运行稳定后期, 每隔1 d收集二级出水进行臭氧实验, 并对模拟污水、二级出水和臭氧出水进行OMPs及遗传毒性分析.样品分析为一式两份, 通过Microsoft Excel 2010计算每次测试结果的均值及方差.为便于归纳分析, OMPs浓度以3次测试结果的综合均值及方差形式给出, 遗传毒性以每次测试结果均值及方差形式给出.
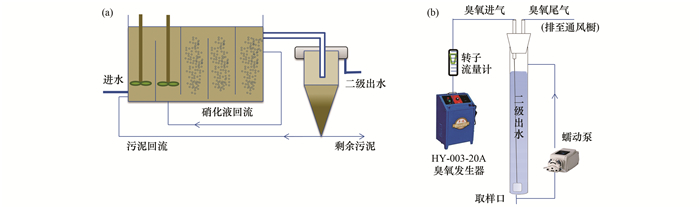
实验装置如图 1, 活性污泥法采用AAO小试装置, 设计流量为2 L ·h-1, 其中厌氧区、缺氧区、好氧区的水力停留时间分别为3、3、9 h.硝化液回流比为200%, 污泥回流比为100%.污泥龄及污泥浓度分别约为18 d和3000 mg ·L-1.
|
(a)AAO系统; (b)批次臭氧装置 图 1 实验装置示意 Fig. 1 Schematic of experimental setups |
臭氧批次实验在玻璃柱中进行, 高度0.8 m, 内径为6 cm, 有效容积2 L.实验前二级出水首先经过0.45 μm玻璃纤维滤膜去除悬浮物以避免干扰[18, 19].臭氧发生器采用空气源, 由玻璃转子流量计控制气体流量为500 mL ·min-1, 通过10 μm孔径钛制曝气头将臭氧分散到水中.控制气态臭氧浓度为5 mg ·L-1, 在20℃室温下反应5 min, 反应结束后关闭臭氧发生器, 继续曝气10 min去除残余臭氧[20], 二级出水中臭氧投加量为6.25 mg ·L-1.实验结束后收集水样并固相萃取进行后续分析.
1.3 OMPs分析 1.3.1 水样预处理本实验选取的14种OMPs是基于环境检出频率和物化性质[4].由于污水中的OMPs浓度很低, 需要固相萃取, 步骤如下:水样收集后, 首先经过0.45 μm玻璃纤维滤膜去除悬浮物, 滤膜不会对OMPs的萃取产生明显影响[5, 20].首先用5 mL甲醇和10 mL超纯水依次活化小柱, 然后水样酸化至pH为2.5过萃取柱.其后萃取柱经过真空干燥2 h后, 用10 mL甲醇洗脱小柱, 收集样品用氮吹仪吹干, 加入1 mL甲醇, 涡旋振荡混匀.取0.5 mL样品过0.22 μm滤膜后进行OMPs分析, 然后将剩余0.5 mL样品用氮气吹干, 然后溶解于0.5 mL二甲基亚砜进行遗传毒性分析.
1.3.2 液质分析采用ACQUITY UPLC BEH C18色谱柱(2.1×50 mm, 1.7 μm)进行OMPs分离, 超高效液相色谱串联质谱仪进行分析.液相方法和质谱条件分别见表 1和表 2.
|
|
表 1 液相梯度洗脱程序1) Table 1 Liquid chromatography with gradient elution program |
|
|
表 2 OMPs分析的质谱条件 Table 2 Mass spectrometer conditions for OMPs analysis |
1.3.3 质量控制与保证
实验用的色谱瓶、瓶盖及玻璃内插管在使用前经过无水乙醇与超纯水分别超声处理30 min, 并冲洗3次, 烘干待用.玻璃内插管一次性使用, 以避免受样品交叉污染.方法的质量控制与保证包括样品空白、样品平行分析、加标回收率.以3倍和10倍信噪比的检测浓度分别定义为方法检出限和定量限[21].采用外标法进行定量分析, 标准曲线浓度范围为0~1 mg ·L-1, 回归方程线性良好, 详见表 2.
1.4 常规指标分析COD、NH4+-N和总氮测试参照文献[22].水中和气态臭氧均采用靛蓝法测定[16, 23].
1.5 遗传毒性实验遗传毒性采用SOS/umu实验方法, 参照《ISO 13829-2000》进行.受试菌种为鼠伤寒沙门菌TA1535/pSK1002, 由清华大学提供.实验样品不经过S9处理, 以4-NQO为阳性对照, 经换算后以4-NQO当量浓度计[18].
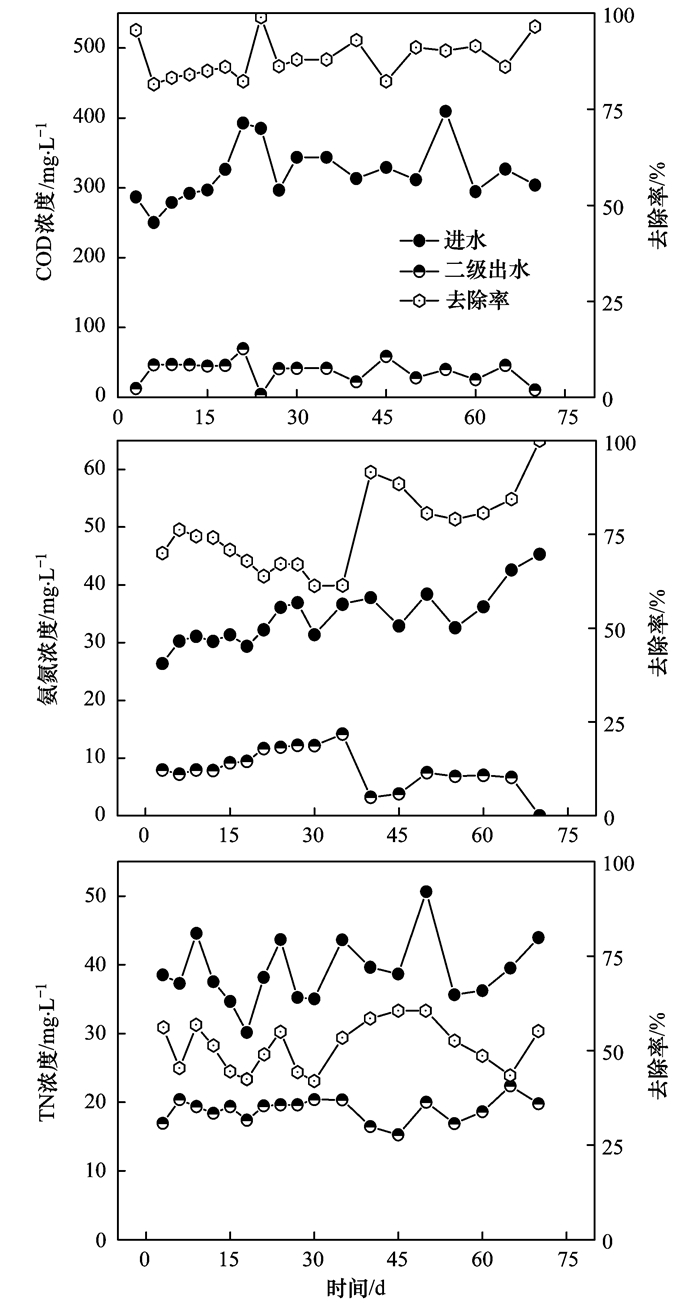
2 结果与讨论 2.1 AAO系统中常规指标的变化AAO反应器连续运行2个月以上, 期间监测进出水的COD、氨氮和总氮来评价AAO反应器的运行状态.由图 2可知, 进水的COD浓度大概在250~400 mg ·L-1之间, 氨氮浓度在25~45 mg ·L-1之间, 总氮浓度在30~50 mg ·L-1之间, 这与实际污水厂进水的各项指标浓度基本一致[24].在反应器运行期间, 二级出水COD浓度在50 mg ·L-1左右, COD去除率约为90%.结果表明AAO反应器运行效果良好, 处理工艺可有效去除污水中大部分有机物.二级出水氨氮浓度在10 mg ·L-1左右, 反应器运行后期氨氮去除率达到75%以上.出水总氮均值为20 mg ·L-1, 去除率在50%左右, 说明反应器的硝化及反硝化作用正常.各项常规指标表明, 反应系统运行正常, 这对于后续的评价OMPs生物降解作用和遗传毒性的削减提供了稳定的条件.
|
图 2 AAO反应器运行期间进出水COD、氨氮和总氮的变化 Fig. 2 Changes of COD, NH4+-N, and TN during operation of the AAO system |
为保证组合工艺对OMPs去除效果的重现性, 实验期间进行了多次取样分析.本文选取的14种OMPs按照药物种类分为:抗生素类药物、抗炎药、降血压血脂药及其他类药物.
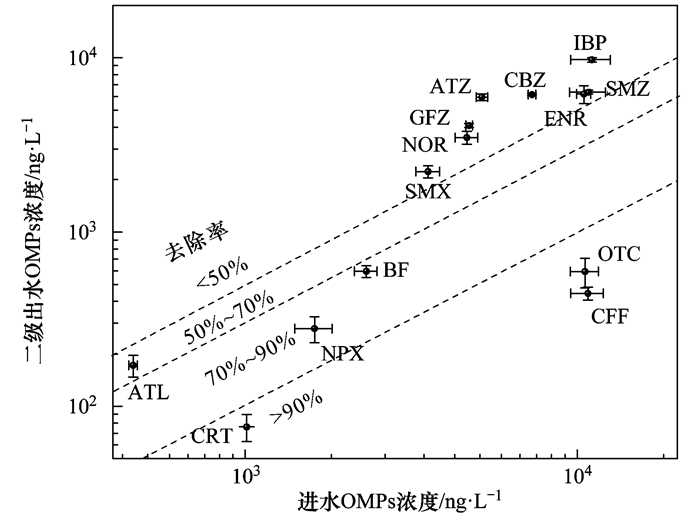
2.2.1 OMPs在AAO工艺中的去除OMPs在AAO系统中的去除效果见图 3.在抗生素类药物中, NOR、ENR、SMX、SMZ在AAO系统中的去除率低于50%, 这类抗生素属于难生物降解有机物.而CRT和OTC去除率大于90%, 传统活性污泥法可有效去除这类抗生素, 这与以AAO工艺为主体的污水厂调研结果相一致[25]; 抗炎药NPX的去除率为83%, 说明NPX较容易通过活性污泥法去除, 而IBP的去除率仅为12%.最近一项研究表明IBP和NPX在污泥系统中均表现出较高的去除率, 这可能与处理系统的运行工况有关[26, 27]; 降血压血脂药中, ATL和BF去除率分别为63%和74%. ATL在不同的报道中去除率有很大波动(介于0%~85%), 主要由于OMPs在生物处理系统中的去除效果受到pH、水温、污泥菌群结构等众多因素的影响[27]. GFZ的去除率为14%, 在二级出水的监控过程中应重点关注; CBZ被广泛认为是一种难生物降解药物[28].在本研究中CBZ在AAO中的去除率约为16%. CFF是一种易生物降解物质[29], 本研究中CFF在AAO中的去除率为96%. ATZ被全球公认为持久性有机污染物的一种[29], 因此近年来被广泛报道. AAO系统中ATZ较低的去除率也验证了其难生物降解特性.
|
图 3 OMPs在AAO中的去除效果 Fig. 3 Removal of OMPs by the AAO system |
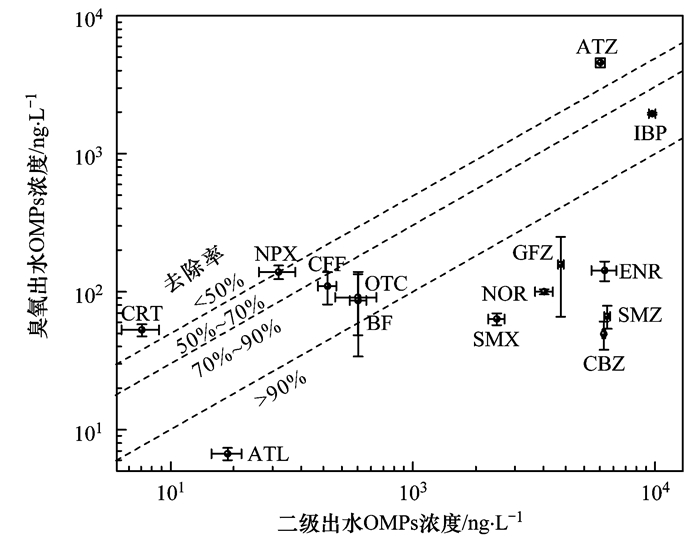
多数OMPs在AAO工艺中不能得到有效去除, 臭氧氧化可有效削减残余药物.由图 4可知, 大部分抗生素在臭氧过程中有效去除, 然而CRT去除率相对较低, 仅为31%;而抗炎类药物NPX和IBP, 去除率分别为50%和80%, 得到部分氧化降解; 降血压血脂类药物ATL和GFZ去除率均为96%, BF去除率为85%, 臭氧氧化作用显著; CBZ在臭氧过程中几乎完全去除(去除率达到99%), 而CFF和ATZ部分去除, 分别为75%和23%.
|
图 4 OMPs在臭氧过程中的去除效果 Fig. 4 Removal of OMPs by ozonation |
二级出水中含有大量出水有机物及还原类物质, 因而影响OMPs的臭氧降解过程.臭氧分子与OMPs分子间的作用主要通过亲电加成作用[16], 有机分子中的不饱和键或芳香性基团存在较大的电子云密度, 易于收到臭氧分子的攻击.由于大部分酚类、苯胺类有机物和臭氧反应速率高于4 L ·(mol ·s)-1(见表 3), 因而反应在很短时间内完成.二者之间的反应属于分子间直接作用, 出水有机物在这个过程中并不会造成明显影响.而出水有机物对于OMPs的臭氧氧化影响主要表现在间接反应过程中[30].臭氧在消耗的过程中会诱发生成HO ·, HO ·与有机分子有非常强的反应活性且无选择性.因此, HO ·的生成量制约着无臭氧反应活性的OMPs的去除效果.据Cai等[30]的研究发现二级出水有机物对于臭氧氧化过程中自由基反应存在3种影响机制:诱发作用、抑制作用、促进作用.在臭氧反应初期会产生大量HO ·(浓度高于10-10mol ·L-1), 但随着反应时间迅速降低. HO ·的“先升后降”现象正是受到出水有机物和还原性物质的作用而导致的[31].本研究中IBP、ATZ、CFF和臭氧反应速率很低, 但在臭氧过程中仍表现出一定程度的去除效果, 这应该归功于臭氧过程中的自由基反应.
2.2.3 组合工艺中OMPs的去除效果由图 5可见, AAO-O3对12种OMPs的去除率达到90%以上, IBP去除率为82%, ATZ去除率仅为11%, 因此在水处理过程中应重点加强ATZ的监测与防控.活性污泥法处理工艺联合臭氧深度处理可有效保证出水中大部分OMPs的去除.然而OMPs的去除率也与其在进水中的浓度有关, 据报道在污水厂进水中OMPs的浓度一般低于1 μg ·L-1[32], 在保证去除率为90%时, 出水中OMPs低于10ng ·L-1, AAO-O3组合工艺可以大大削减污水中OMPs向水环境中的释放.

|
图 5 OMPs在组合工艺中的去除效果 Fig. 5 Removal of OMPs by the hybrid process |
本研究从活性污泥处理法和臭氧氧化两方面, 分别对OMPs在AAO系统中的去除途径及臭氧过程中的氧化机制进行讨论.
2.3.1 OMPs在活性污泥系统中的去除途径分析OMPs在活性污泥法处理工艺中的去除途径主要有污泥吸附和生物降解[10, 33].
OMPs在污泥表面的吸附能力主要和二者的界面特性有关, 如固-水分配系数(Koc)[13]. 表 3中列出了14种OMPs的lgKoc值, lgKoc值越大表明OMPs在固体表面的吸附量越大, 从而更倾向于向污泥表面迁移. CBZ、GFZ、BF、IBP、ATZ的lgKoc值大于2, 说明这几种OMPs通过污泥吸附去除效果较为显著; SMX、SMZ、NPX、ATL、CFF的lgKoc值介于0.5~2之间, 说明其通过污泥吸附去除效果轻微; CRT、OTC、ENR、NOR的lgKoc值小于0.5, 说明其在污泥表面吸附不佳.但是由于大多OMPs在不同pH环境中存在不同的解离状态, 因此仅用lgKoc值来评价OMPs的吸附存在片面性.
|
|
表 3 OMPs的臭氧二级反应速率和固-水分配系数 Table 3 Secondary reaction kinetic constants with ozone and solid-water distribution coefficient for selected OMPs |
OMPs在生物系统中的降解不仅与其物化性质有关, 而且还受到AAO工艺运行条件的影响[27].通过对大量研究总结发现, OMPs在活性污泥系统中的吸附作用和生物降解作用之间没有明确的比例界限[25, 26, 34, 35].此外在实际污水厂的取样过程中, 存在水质波动、悬浮物吸附、分析误差等众多因素影响, 因此评价单独OMPs的生物降解性存在一定难度.
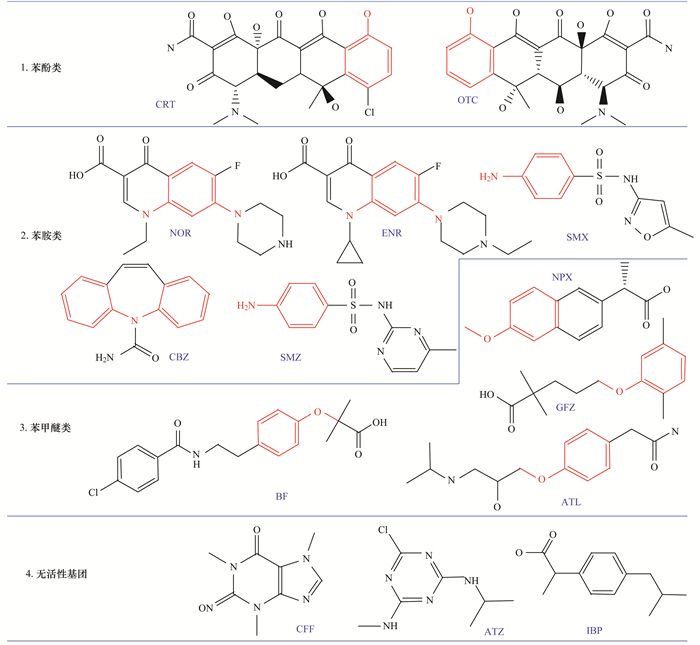
2.3.2 OMPs在臭氧过程中的氧化机制臭氧和芳香族有机物的反应速率很大程度受苯环上取代基的影响[16]. 图 6中展示了本研究中OMPs分子的芳香性基团(红色部分), 根据取代基团的种类将14种OMPs分为:苯酚类、苯胺类、苯甲醚类及无活性基团化合物.
|
图 6 14种OMPs的分子结构及分类 Fig. 6 Molecular structures and classification of 14 selected OMPs |
CRT和OTC含有酚羟基(—OH), —OH是强供电子取代基而增加其反应活性. OTC在臭氧过程中去除率为85%, 很好地解释了分子结构与去除效果之间的联系.然而CRT去除率仅为31%, 应该受苯环上的氯代基团(—Cl)的吸电子作用影响, 降低了CRT与臭氧的反应速率从而导致其去除效果减弱; NOR、ENR、SMX、SMZ、CBZ均含有苯胺基(—NH2).这类有机物和臭氧反应受pH影响很大, 在—NH2处于去质子状态时(中性), 与臭氧反应活性最高.而在—NH2处于质子化状态时(解离), 几乎不与臭氧发生反应[32].由图 4可知, 这5种物质在臭氧过程中去除率均高于90%, 由于二级出水的pH趋于中性, 这主要归功于去质子化—NH2的臭氧氧化作用; 苯甲醚类有机物的活性基团是甲氧取代基(—OCH3), 在苯环伯仲位置的—OCH3会提高与臭氧的反应活性[16].本研究中苯甲醚类有机物的二级反应速率介于2.77~5.69L ·(mol ·s)-1.由于—OCH3不存在解离态, 因此这类有机物与臭氧的反应不会受pH影响; CFF、ATZ、IBP的分子结构中不含有与臭氧反应的活性基团, 因此表现出较低的二级反应速率[0.82~9.6 L ·(mol ·s)-1].这类有机物很难通过单独臭氧氧化进行去除.
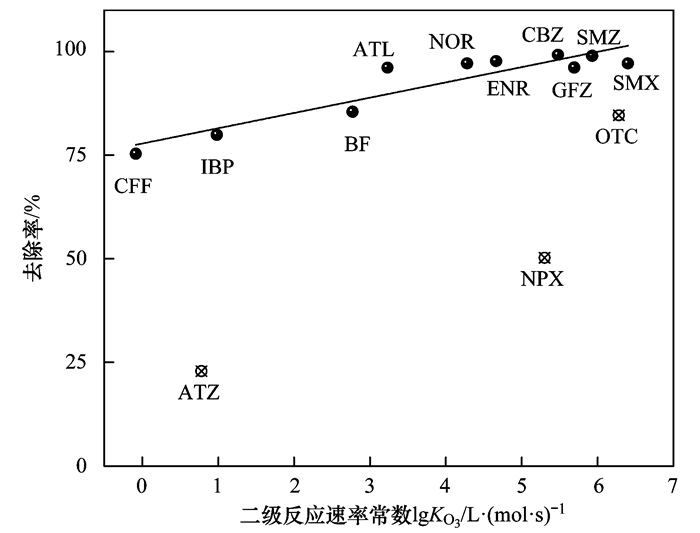
OMPs在臭氧过程中的去除效果与臭氧反应的二级反应速率常数有关[4].由图 7可见, OMPs二级反应速率与其去除率呈正相关, 由于二级反应速率受到反应体系的pH及出水有机物的影响存在离散值(ATZ、NPX、OTC).而对于选定的10种OMPs, 二级反应速率常数与去除率线性良好(R=0.92), 可以有效预测并解释OMPs在臭氧过程中的去除机制.
|
图 7 OMPs的二级反应速率常数和去除率之间的相关性 Fig. 7 Relationship between the secondary reaction rate constant and the removal of OMPs |
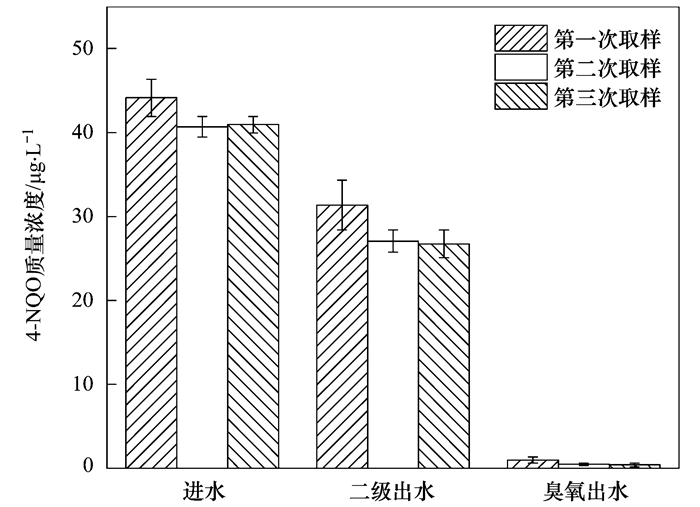
遗传毒性指标可以综合表征污水中有机物的环境风险[36].由图 8可知, 人工模拟污水的遗传毒性(以4-NQO计, 下同)为(41.9±1.6) μg ·L-1, 二级出水的遗传毒性为(28.4±2.1) μg ·L-1, 平均去除率为32%, 低于尹子华等研究的多级AO工艺对遗传毒性的去除率(83%)[36].二级出水对于水环境的遗传毒性风险水平依然较高, 据报道污水厂再生水与地表水的遗传毒性水平一般在10~102 μg ·L-1之间[14], 这对水生生物造成潜在风险.臭氧投加量为6.25 mg ·L-1时, 出水的遗传毒性急剧下降到(0.6±0.3) μg ·L-1(接近于检测限0.1 μg ·L-1), 去除率达到98%, 表明臭氧对于削减污水的遗传毒性效果显著, 该结果与前人的研究结论一致[14].最近一项研究表明污水有机物的光谱学指标可以很好地指示出水有机物遗传毒性的变化[4], 而OMPs造成的遗传毒性风险仍是不可忽视的重要因素, 在今后的研究中也应作为重点研究对象.
|
图 8 组合工艺中遗传毒性的削减 Fig. 8 Reduction of genotoxicity by the hybrid process |
(1) AAO工艺对于部分易生物降解类OMPs去除率大于90%, 如CRT、OTC和CFF, 而对于大部分OMPs去除效果不佳; 臭氧氧化工艺对大部分OMPs去除率可达到90%以上. ATZ、CRT、NPX在臭氧过程中较难氧化去除. AAO-O3组合工艺可以有效控制OMPs的泄漏风险.
(2) 通过对OMPs的分子结构分析, 芳香性结构中含有—OH、—NH2和—OCH3 3种取代基的OMPs臭氧氧化效果显著, 而无芳香性结构的ATZ、CFF、IBP则在臭氧过程中去除效果一般. OMPs与臭氧的二级反应速率常数与其在臭氧过程中的去除率存在较好的正相关性, 从分子结构和反应速率常数角度解析OMPs在臭氧过程中的去除规律具有可行性.
(3) 污水和二级出水遗传毒性水平较高, 活性污泥法对于遗传毒性有一定的削减效果, 但二级出水仍表现出较高的遗传毒性.臭氧氧化可以大大降低二级出水的遗传毒性, 从而减轻污水厂出水的环境风险.
| [1] | Anumol T, Snyder S A. Rapid analysis of trace organic compounds in water by automated online solid-phase extraction coupled to liquid chromatography-tandem mass spectrometry[J]. Talanta, 2015, 132: 77-86. DOI:10.1016/j.talanta.2014.08.011 |
| [2] | Wang Z, Zhang X H, Huang Y, et al. Comprehensive evaluation of pharmaceuticals and personal care products (PPCPs) in typical highly urbanized regions across China[J]. Environmental Pollution, 2015, 204: 223-232. |
| [3] | Altmann J, Ruhl A S, Zietzschmann F, et al. Direct comparison of ozonation and adsorption onto powdered activated carbon for micropollutant removal in advanced wastewater treatment[J]. Water Research, 2014, 55: 185-193. DOI:10.1016/j.watres.2014.02.025 |
| [4] | Chen Z Q, Li M, Wen Q X. Comprehensive evaluation of three sets of advanced wastewater treatment trains for treating secondary effluent:Organic micro-pollutants and bio-toxicity[J]. Chemosphere, 2017, 189: 426-434. |
| [5] |
孙佳薇, 丁炜楠, 张占恩, 等. 污水处理厂中有机磷阻燃剂的污染特征[J]. 环境科学, 2018, 39(5): 2230-2238. Sun J W, Ding W N, Zhang Z E, et al. Pollution characteristics of organophosphorous flame retardants in wastewater treatment plant[J]. Environmental Science, 2018, 39(5): 2230-2238. |
| [6] |
柴玉峰, 张玉秀, 陈梅雪, 等. 冀西北典型北方小城镇污水处理厂中抗生素的分布和去除[J]. 环境科学, 2018, 39(6): 2724-2731. Chai Y F, Zhang Y X, Chen M X, et al. Distribution and treatment effect of antibiotics of typical WWTPs in small town of China[J]. Environmental Science, 2018, 39(6): 2724-2731. |
| [7] | Knopp G, Prasse C, Ternes T A, et al. Elimination of micropollutants and transformation products from a wastewater treatment plant effluent through pilot scale ozonation followed by various activated carbon and biological filters[J]. Water Research, 2016, 100: 580-592. |
| [8] | Michael-Kordatou I, Michael C, Duan X, et al. Dissolved effluent organic matter:Characteristics and potential implications in wastewater treatment and reuse applications[J]. Water Research, 2015, 77: 213-248. DOI:10.1016/j.watres.2015.03.011 |
| [9] | De la Cruz N, Giménez J, Esplugas S, et al. Degradation of 32 emergent contaminants by UV and neutral photo-fenton in domestic wastewater effluent previously treated by activated sludge[J]. Water Research, 2012, 46(6): 1947-1957. |
| [10] | Li B, Zhang T. Biodegradation and adsorption of antibiotics in the activated sludge process[J]. Environmental Science & Technology, 2010, 44(9): 3468-3473. |
| [11] | Cristale J, Ramos D D, Dantas R F, et al. Can activated sludge treatments and advanced oxidation processes remove organophosphorus flame retardants?[J]. Environmental Research, 2016, 144: 11-18. |
| [12] | Ben W W, Zhu B, Yuan X J, et al. Occurrence, removal and risk of organic micropollutants in wastewater treatment plants across China:Comparison of wastewater treatment processes[J]. Water Research, 2018, 130: 38-46. |
| [13] | Alvarino T, Suarez S, Lema J, et al. Understanding the sorption and biotransformation of organic micropollutants in innovative biological wastewater treatment technologies[J]. Science of the Total Environment, 2018, 615: 297-306. |
| [14] | Tang X, Wu Q Y, Yang Y, et al. Genotoxicity removal of reclaimed water during ozonation[J]. Journal of Environmental Sciences, 2014, 26(6): 1243-1248. DOI:10.1016/S1001-0742(13)60595-1 |
| [15] |
侯瑞, 金鑫, 金鹏康, 等. 臭氧-混凝耦合工艺污水深度处理特性及其机制[J]. 环境科学, 2017, 38(2): 640-646. Hou R, Jin X, Jin P K, et al. Characteristics and mechanism of hybrid ozonation-coagulation process in wastewater reclamation[J]. Environmental Science, 2017, 38(2): 640-646. |
| [16] | Jin X H, Peldszus S, Huck P M. Reaction kinetics of selected micropollutants in ozonation and advanced oxidation processes[J]. Water Research, 2012, 46(19): 6519-6530. DOI:10.1016/j.watres.2012.09.026 |
| [17] | Acero J L, Benitez F J, Real F J, et al. Micropollutants removal from retentates generated in ultrafiltration and nanofiltration treatments of municipal secondary effluents by means of coagulation, oxidation, and adsorption processes[J]. Chemical Engineering Journal, 2016, 289: 48-58. DOI:10.1016/j.cej.2015.12.082 |
| [18] | Wang L S, Hu H Y, Wang C. Effect of ammonia nitrogen and dissolved organic matter fractions on the genotoxicity of wastewater effluent during chlorine disinfection[J]. Environmental Science & Technology, 2007, 41(1): 160-165. |
| [19] | Qi W X, Zhang H, Hu C Z, et al. Effect of ozonation on the characteristics of effluent organic matter fractions and subsequent associations with disinfection by-products formation[J]. Science of the Total Environment, 2018, 610-611: 1057-1064. DOI:10.1016/j.scitotenv.2017.08.194 |
| [20] | Tang X, Wu Q Y, Zhao X, et al. Transformation of anti-estrogenic-activity related dissolved organic matter in secondary effluents during ozonation[J]. Water Research, 2014, 48: 605-612. |
| [21] | Tran N H, Hu J Y, Ong S L. Simultaneous determination of PPCPs, EDCs, and artificial sweeteners in environmental water samples using a single-step SPE coupled with HPLC-MS/MS and isotope dilution[J]. Talanta, 2013, 113: 82-92. DOI:10.1016/j.talanta.2013.03.072 |
| [22] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京:中国环境科学出版社, 2002. |
| [23] | Li W T, Cao M J, Young T, et al. Application of UV absorbance and fluorescence indicators to assess the formation of biodegradable dissolved organic carbon and bromate during ozonation[J]. Water Research, 2017, 111: 154-162. |
| [24] | Sun Y, Chen Z, Wu G X, et al. Characteristics of water quality of municipal wastewater treatment plants in China:Implications for resources utilization and management[J]. Journal of Cleaner Production, 2016, 131: 1-9. |
| [25] | Ashfaq M, Li Y, Wang Y W, et al. Occurrence, fate, and mass balance of different classes of pharmaceuticals and personal care products in an anaerobic-anoxic-oxic wastewater treatment plant in Xiamen, China[J]. Water Research, 2017, 123: 655-667. DOI:10.1016/j.watres.2017.07.014 |
| [26] | Ahmed M B, Zhou J L, Ngo H H, et al. Progress in the biological and chemical treatment technologies for emerging contaminant removal from wastewater:A critical review[J]. Journal of Hazardous Materials, 2017, 323: 274-298. DOI:10.1016/j.jhazmat.2016.04.045 |
| [27] | Luo Y L, Guo W S, Ngo H H, et al. A review on the occurrence of micropollutants in the aquatic environment and their fate and removal during wastewater treatment[J]. Science of the Total Environment, 2014, 473-474: 619-641. |
| [28] | Gauthier H, Yargeau V, Cooper D G. Biodegradation of pharmaceuticals by Rhodococcus rhodochrous and Aspergillus niger by co-metabolism[J]. Science of the Total Environment, 2010, 408(7): 1701-1706. DOI:10.1016/j.scitotenv.2009.12.012 |
| [29] |
詹旭, 吕锡武. 持久性有机污染物(POPs)的生物降解研究进展[J]. 中国给水排水, 2006, 22(22): 10-12. Zhan X, Lv X W. Advances of studies on biodegradation of persistent organic pollutants[J]. China Water & Wastewater, 2006, 22(22): 10-12. DOI:10.3321/j.issn:1000-4602.2006.22.003 |
| [30] | Cai M J, Lin Y P. Effects of effluent organic matter (EfOM) on the removal of emerging contaminants by ozonation[J]. Chemosphere, 2016, 151: 332-338. |
| [31] | Buffle M O, Schumacher J, Meylan S, et al. Ozonation and advanced oxidation of wastewater:Effect of o3 dose, pH, DOM and HO--Scavengers on ozone decomposition and HO- generation[J]. Ozone:Science & Engineering, 2006, 28(4): 247-259. |
| [32] | Jin X H, Peldszus S. Selection of representative emerging micropollutants for drinking water treatment studies:A systematic approach[J]. Science of the Total Environment, 2012, 414: 653-663. DOI:10.1016/j.scitotenv.2011.11.035 |
| [33] | Besha A T, Gebreyohannes A Y, Tufa R A, et al. Removal of emerging micropollutants by activated sludge process and membrane bioreactors and the effects of micropollutants on membrane fouling:A review[J]. Journal of Environmental Chemical Engineering, 2017, 5(3): 2395-2414. |
| [34] | Grandclément C, Seyssiecq I, Piram A, et al. From the conventional biological wastewater treatment to hybrid processes, the evaluation of organic micropollutant removal:A review[J]. Water Research, 2017, 111: 297-317. DOI:10.1016/j.watres.2017.01.005 |
| [35] | Barbosa M O, Moreira N F F, Ribeiro A R, et al. Occurrence and removal of organic micropollutants:An overview of the watch list of EU Decision 2015/495[J]. Water Research, 2016, 94: 257-279. DOI:10.1016/j.watres.2016.02.047 |
| [36] |
尹子华, 盛晓琳, 刘锐, 等. 多级A/O工艺强化处理城市污水的效果研究[J]. 环境科学, 2016, 37(9): 3460-3465. Yin Z H, Sheng X L, Liu R, et al. Enhanced pollutants removal in a municipal wastewater treatment plant with multistage A/O process[J]. Environmental Science, 2016, 37(9): 3460-3465. |
 2018, Vol. 39
2018, Vol. 39


