2. 安徽师范大学国土资源与旅游学院, 芜湖 241000;
3. 湖南省土壤肥料研究所, 长沙 410125
2. College of Territorial Resources and Tourism, Anhui Normal University, Wuhu 241000, China;
3. Soil and Fertilizer Institute of Hunan Province, Changsha 410125, China
氧化亚氮(N2O)作为3种最重要的温室气体之一, 增温潜势已为CO2的310倍[1].自20世纪70年代以来N2O排放量增加了43%[2], 当前大气N2O浓度比工业化前增加了20%[3], 不仅影响全球气候, 而且也损害了大气臭氧层[4].湿地作为N2O的重要排放源, 贡献了N2O全球人为源的17%~25%[5].目前, 关于水生生态系统N2O排放的研究已取得较大进展[6].河流系统的氮富集已成为全球各地区面临的重要环境污染问题, 而且其直接贡献于水体N2O排放.大气氮沉降、硝态氮肥、铵态氮肥、土壤流失氮和人类及动物粪便是目前河流氮素富集和N2O排放的潜在主要来源[7].识别水体硝态氮来源是控制水体氮污染, 改善水环境的关键环节.
已知不同硝态氮来源具有其特殊的氮(δ15N)和氧(δ18O)同位素组成[8].由于不同硝态氮来源同位素值的部分重叠、不同来源的混合以及由生物地球化学过程引起的同位素值的改变, 使得利用单一同位素难以准确识别硝态氮来源[9].因此, 硝态氮的氮氧双同位素(δ15N-NO3-、δ18O-NO3-)与其它理化数据的耦合是识别陆地到水体硝态氮来源和探究氮素迁移的强有力工具[10, 11].已有学者利用氮氧双同位素技术开展了水体N2O硝化和反硝化过程的识别[2, 11].同样, 氮氧双同位素技术也已应用于识别水体氮素的无机(如化肥)和有机(人类和畜禽粪便)来源[12], 如大气氮沉降和人畜粪便被普遍认为是城郊溪流表层水体硝态氮主要来源[13, 14].Yang等[11]还发现δ15N变异小且重叠范围过多, 而δ18O变异范围更大, 其在硝态氮来源识别过程中作用更突出.国内对于河流N2O主要产生过程的多同位素研究还较少, 徐文彬[15]进行了对流层大气N2O氮氧稳定同位素负荷平衡的初步探索.而李艳利等[16]和郭庆军等[17]则分别研究了太子河下游河流硝酸盐来源和湖泊沉积物有机质来源及迁移过程.其它研究则针对内陆湖泊悬浮颗粒物有机质、河口及邻近海域表层沉积物有机质和地下河硫酸盐及硝酸盐来源进行了硫氧碳氮的多同位素解析[18~20].综上, 国内对流域水体氮素来源及其迁移转化的研究已取得一定进展, 但多集中于城区河流、内陆湖泊、河口以及地下河等水体, 而农业小流域水系作为陆地生态系统的重要组成部分, 对其氮素来源及其迁移转化过程的研究相对缺失.脱甲河流域为典型亚热带农业小流域, 居民区密集, 农耕活动频繁, 氮素流失及水体面源污染现象明显[21].本研究以脱甲河流域为对象, 通过分析水体NO3--N的δ15N、δ18O以及沉积物有机质δ15N(δ15Norg)、C/N特征, 结合硝化过程中的δ18O-NO3-和水体理化参数, 明确水系N2O关键产生过程, 确定流域氮素来源, 以期为减少流域氮素养分流失、改善流域水环境质量提供理论依据, 并为相似区域氮素流失溯源研究提供参考.
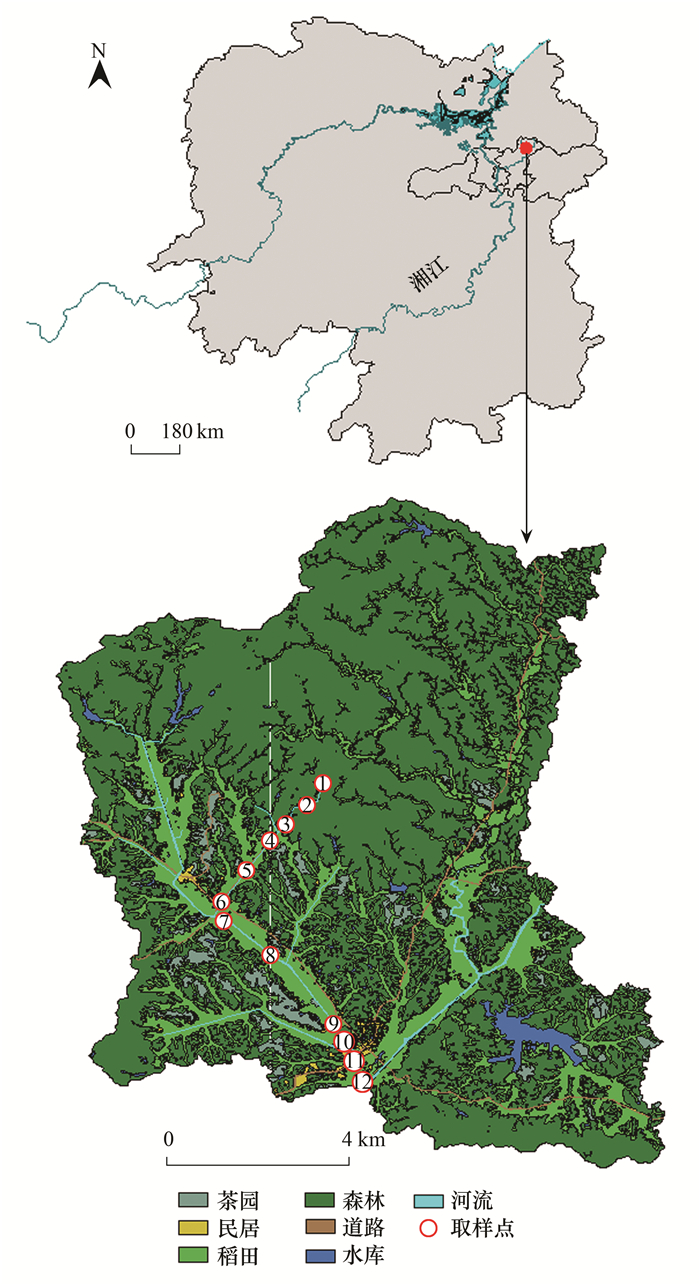
1 材料与方法 1.1 研究区概况脱甲河位于湖南省长沙县金井镇境内(图 1), 属湘江二级支流, 为中亚热带典型农业小流域, 具有独立的汇水系统且水文系统结构完整, 流域面积为52.10 km2, 地理坐标为27°55′~28°40′N, 112°56′~113°30′E.该流域为典型红壤丘陵地貌, 平均海拔98.3 m, 地势呈北高南低趋势.研究区为典型亚热带湿润季风气候, 雨热同期, 年平均气温17.2℃, 年平均降雨量1422 mm[22].流域土地利用类型呈现多样化特征, 有林地、水田、茶园、果园以及菜地等类型, 其中以林地、水田为主, 水稻种植面积占流域面积的32%[22], 土壤类型以红壤为主.除源头区域人类活动较少外, 河流两岸水稻田密布, 农耕活动频繁, 沿岸居民区密集, 农田不合理施肥及氮素污染现象明显[21].
|
图 1 脱甲河流域位置 Fig. 1 Locations of Tuojia River watershed |
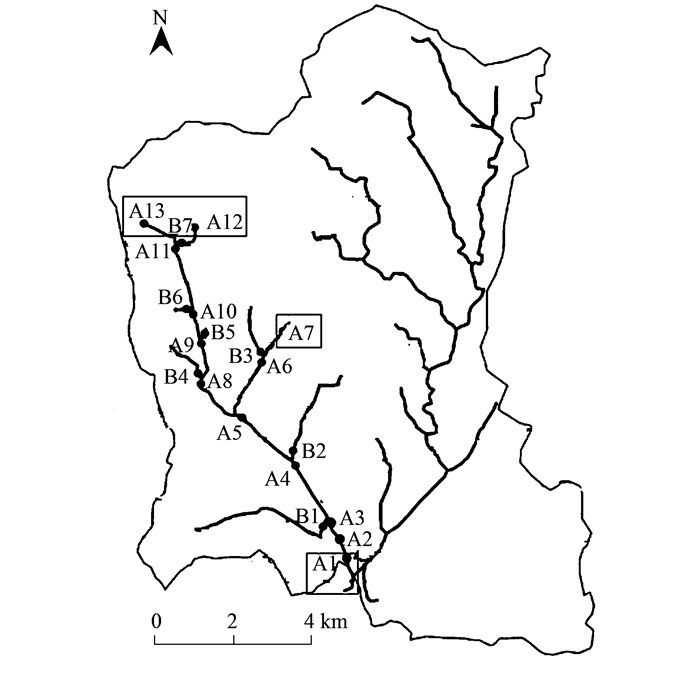
根据流域水系分级特征, 将脱甲河水系由源头至河口分为4级河段(图 2), 分别记为:S1、S2、S3、S4.在河流干支流共设置20个观测点, 其中干流监测点13个(A1~A13), 支流监测点7个(B1~B7), 为探讨流域水系氮素来源, 将氮、氧稳定同位素(δ15N、δ18O)等样品观测点设置在A7、B3、A5、A1, 分别对应S1~S4级河段取样点.
|
图 2 脱甲河采样点分布 Fig. 2 Distributions of sampling points of Tuojia River watershed |
每个采样点取约200 mL表层水体(0~30 cm)水样装入聚乙烯塑料瓶内并贴好标签, 各点3次重复取样, 取样完成后尽快运回实验室.首先用0.45 μm滤膜过滤, 而后移入200 mL玻璃瓶, 再加入10mg·L-1 HgCl2溶液, 放入冰柜于4℃条件下密封保存, 用反硝化细菌法结合痕量气体分析仪(TraceGas)/同位素比质谱仪(Finnigan MAT Delta S)测定硝态氮的氮氧同位素(δ15N-NO3-、δ18O-NO3-)及水体氧同位素(δ18O-H2O)[17].水体硝态氮质量浓度用流动注射仪(FIA-500 star, FOSS)测定.利用顶空-平衡法提取溶存气体, 用质谱仪(IRMS-MAT253)测定气体中溶解氧的δ18O.
1.3.2 沉积物样品采集与δ15N及C/N测定沉积物样品的采集与水样同时进行, 利用分离式土壤原状土取样器获取水下底泥(0~20 cm)土样200 g, 各点设置3个重复.样品运回实验室后, 首先将沉积物样品在60~70℃干燥箱中干燥24~48 h, 烘干的样品用研钵、球磨机粉碎, 后过60目筛.之后称量过筛后的样品, 通过固体自动进样器送入元素分析仪(FLASH EA1112), 样品中含氮物质依次经过元素分析仪的氧化炉和还原炉反应生成N2, 生成的N2通过ConfloⅣ接口进入质谱仪(IRMS-MAT253), 得到沉积物有机氮同位素(δ15Norg)组成[21].采用元素分析仪(FLASH EA2000, Thermo)分析有机碳和总有机氮含量及碳氮比值(C/N).
1.3.3 同位素组成计算及测试精度各稳定同位素的组成(δ)利用公式(1)计算:
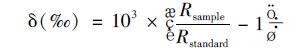
|
(1) |
式中, R表示15N/14N、18O/16O值, 分别对应于标准大气氮气同位素和平均海水标准氧同位素, δ15N和δ18O测试精度分别为±0.2‰和±0.3‰.相关测定在中国科学院亚热带农业生态研究所和中国农业科学院农业环境与可持续发展研究所进行.
1.4 N2O产生过程判据硝化过程中的δ18O-NO3-可用公式(2)计算, 若该过程δ18O-NO3-的组成范围是-10‰~10‰, 即硝化过程可能主导N2O的产生[23].
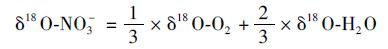
|
(2) |
式中, δ18O-NO3-表示硝化过程中硝酸盐的δ18O, δ18O-O2和δ18O-H2O分别表示大气中O2和水体的δ18O.
而对于反硝化过程的贡献, 可通过δ15N-NO3-和NO3--N浓度及δ15N-NO3-和δ18O-NO3-的关系判断, 若δ15N-NO3-随NO3--N浓度的降低而增加且δ15N-NO3-与δ18O-NO3-的比值(δ15N-NO3-/δ18O-NO3-)为2:1, 则说明反硝化过程主导着N2O的产生[12, 23].
1.5 数据处理与分析利用SPSS 17.0对数据进行统计分析, 利用Excel 2007和R Core Team (2016)对实验数据进行均值和标准误差处理并绘制图表.
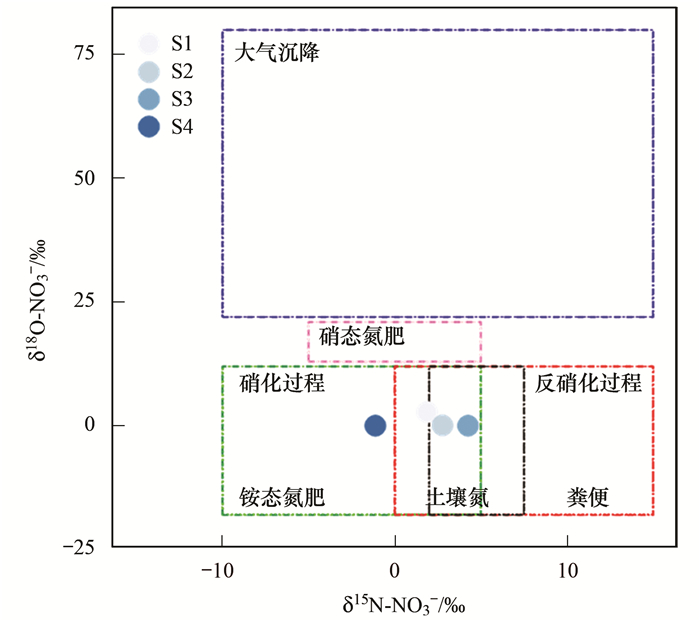
2 结果与分析 2.1 脱甲河水体NO3--N氮氧同位素特征本研究周期内(图 3), 脱甲河水体δ15N-NO3-变化范围是-19.87‰~8.11‰, S1~S4河段δ15N-NO3-均值分别为(1.72±0.92)‰、(2.62±0.72)‰、(4.10±0.46)‰和(-1.28±3.27)‰, S1~S3河段δ15N-NO3-呈现一定的富集趋势; 而δ18O-NO3-在-3.03‰~5.81‰区间内变化, S1~S4河段δ18O-NO3-均值分别为(2.60±0.95)‰、(-0.06±0.77)‰、(0.85±0.52)‰和(-0.62±1.01)‰.河流NO3--N来源呈现多元化特点, 总体为土壤氮、人和动物粪便和铵态氮肥.各级河段水体氮素来源存在显著差异, S1河段主要来源可能是土壤氮和粪便, 而S4河段NO3--N来源于铵态氮肥的硝化反应, S2、S3河段NO3--N可能来源于土壤氮、铵态氮肥和粪肥.
|
图中常见氮素来源的同位素组成参见文献[24~26] 图 3 脱甲河水体硝态氮的氮氧同位素组成 Fig. 3 Composition of nitrogen oxygen isotope of nitrate of Tuojia River waterbody |
脱甲河水体沉积物有机质δ15Norg变化范围是-0.69‰~11.21‰(图 4), S1~S4河段均值分别为(1.91±0.45)‰、(2.96±0.40)‰、(4.72±0.73)‰和(3.23±0.20)‰, 呈现S3河段最高、S1河段最低特点; 沉积物有机质C/N在7.30~12.02范围内变化, S1~S4河段均值分别是10.62±0.35、8.63±0.22、9.05±0.22和9.22±0.28, 最高值位于S1河段, 而最低则在S2河段, S3、S4值较为相近.综合δ15Norg和C/N特征发现, S1河段沉积物有机质氮素来源与其他河段存在不同, 其δ15Norg组成范围及C/N处于土壤有机质组成区间内, 而与污水、C3植物、C4植物及大气沉降氮等的组成差异较大.S2~S4河段沉积物有机质δ15Norg组成范围及C/N则与污水的组成范围相近; 因此, 污水可能为S2~S4河段沉积物有机质氮素的主要来源.

|
图中常见有机质氮素来源的同位素及C/N特征参见文献[27~29] 图 4 脱甲河沉积物有机质的δ15Norg和C/N值分布 Fig. 4 Distributions of δ15Norg and C/N valuesof organic matter in sediment of Tuojia River waterbody |
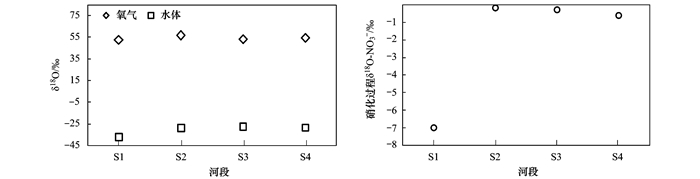
脱甲河流域大气中氧气的δ18O(δ18O-O2)总体变化较平稳(图 5), 各级河段差异不明显, S1~S4河段均值分别为52.71‰、56.66‰、53.54‰和54.73‰.而S1~S4河段δ18O-H2O的均值分别为-36.86‰、-28.59‰、-27.19‰和-28.26‰, S1河段δ18O-H2O最低, 其他3河段之间较为接近, 由S1~S3呈现一定的富集趋势.硝化过程中δ18O-NO3-在S1~S4河段分别是-7.01‰、-0.17‰、-0.28‰和-0.60‰, S1更为偏负且显著低于其他河段, S2~S4河段则较为相近且呈现弱的贫化趋势.S2~S4河段硝化过程中的18O-NO3-相对于S1河段较富集.
|
图 5 大气中氧气、水样及硝化过程中NO3-的δ18O分布 Fig. 5 Distributions of δ18O of oxygen from atmosphere, water samples and nitrate from nitrification |
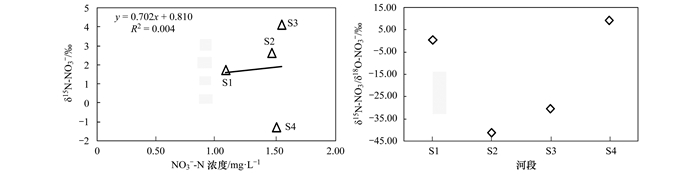
本研究周期内(图 6), 水体硝态氮浓度范围是1.08~1.54 mg·L-1, S1~S4河段分别为1.08、1.46、1.54和1.50 mg·L-1, 靠近源头区域、受人类活动影响小的S1河段最低, 而两岸农田广布且居民点密集的河段较高; 水体硝态氮浓度与其δ15N呈现弱的正相关关系, 即随着水体硝态氮浓度的增加, δ15N-NO3-也呈增加趋势.水体硝态氮的δ15N与其δ18O的比值(δ15N-NO3-/δ18O-NO3-)在S1~S4河段分别为0.66、-41.01、-30.23和9.39, S1、S4河段为正值, 而S2、S3则均为负值, 各河段差异明显.可见硝化过程在脱甲河氮素转化中更占优势, 其对N2O的产生贡献较大.
|
图 6 硝态氮浓度与其δ15N的关系及硝态氮的δ15N与δ18O比值 Fig. 6 Relationship between the nitrate concentration and its δ15N, the ratio of δ15N to δ18O of nitrate |
水体中硝态氮的污染来源具有多元化特点, 包括农业肥料、大气沉降、人和动物粪便、生活污水以及土壤流失氮等[7], 而且不同的硝态氮来源具有其特殊的氮(δ15N)和氧(δ18O)同位素组成范围[8].有研究表明, 大气沉降中δ15N-NO3-的范围是-10‰~10‰[24], 人畜粪便和生活污水中的值在4‰~25‰之间, 复合肥料和土壤有机氮的范围分别是-5‰~5‰和0‰~8‰[25, 26].而大气沉降和硝态氮肥中的δ18O-NO3-范围分别是25‰~75‰和17‰~25‰[24], 人畜粪便和污水中的δ18O-NO3-值为-5‰~10‰[25], 硝化过程中δ18O-NO3-则为-10‰~10‰[23].本研究水体硝态氮δ15N和δ18O组成与土壤流失氮、铵态氮肥和粪肥的范围一致, S3河段出现较高的δ15N值, 可能是靠近城镇区, 有大量未经处理的人和动物排泄物输入.脱甲河与太子河[16]、松花江以及龙泓涧等[30, 31]河流水体硝态氮来源相一致.此外, 与太湖、西湖等[32, 33]湖泊水体硝态氮来源也较为相似, 土壤流失氮和化学肥料均占有重要地位.然而, 梁慧雅等[34]在府河-白洋淀流域的研究发现, 其硝态氮主要来源于生活污水和工业废水, 与本研究结果存在显著差异, 可能是府河为城市河流, 承接了大量生活污水和工业废水输入.另外, Divers等[35]利用混合模型对城市小溪流水体硝态氮来源进行了溯源, 发现基流期主要来源于污水, 而暴雨期则来源于大气沉降和污水, 与脱甲河水体硝态氮来源有较大差异, 可能是城市生态系统和农业生态系统的差异造成的.脱甲河各级河段硝态氮来源也存在差异, 可能与土地利用类型不同相关[36], S1河段靠近河流源头区, 受人类生产生活影响微弱, 可能导致其氮素来源较单一化.而S2、S3河段两岸农田面积广, 农业活动频率高且施氮量大[22], 沿河居民区密布, 农业生产面源排放及生活污水的排入可能促使了其硝态氮来源的多元化且以外源为主.
3.2 沉积物有机质氮素来源碳氮比值是蛋白质含量的重要指示剂, 蛋白质是生物体中最重要的含氮成分, 不同类型的有机质中所含蛋白质不同, 沉积物有机质C/N值可以大体判断沉积有机质的来源是水体自生还是外源输入[29], 而沉积物中有机质的不同来源又有其特定的氮同位素组成, 因此综合利用沉积物有机质的δ15N和C/N能更有效地追溯其氮素来源[17].有研究发现沉积物中有机质的C/N>8, 即可被认为受到2种物源的影响, 而陆源有机质所占的比例越高, C/N值就越大[29].一般认为, 藻类的δ15N范围是4‰~10‰, 其C/N位于3~8之间, 而陆生高等植物的C/N约为20, 甚至更高, 土壤有机质的C/N则在10~13之间变化[27~29].脱甲河S1河段沉积物有机质C/N>10且处于土壤有机质C/N范围内, 而S2~S4河段之间δ15N和C/N组成变化不大, 均与污水的组成范围吻合.本研究与郭庆军等[17]在北京城区公园湖泊的研究结果一致, 土壤有机质与污水对沉积物有机质的贡献突出.而倪兆奎等[29]在太湖的研究发现, 20世纪90年代以来, 太湖沉积物有机质和氮的来源以湖泊自生为主, 因为外源氮输入的有效控制, 使得藻类对沉积物氮的贡献显著增加.另外, 晁海娟等[19]在长江口及邻近海域的研究结果与脱甲河沉积物有机质的来源也存在显著差异, 可能与所处地理位置紧密相关, 长江口受江水和洋流共同影响, 使得其沉积物来源以海陆混合为主, 而本研究区域受农业生产和居民生活影响更为显著.此外, S1河段与赣江南支沉积物有机质来源相似, 均为土壤有机质, 可能主要受水土流失影响; 而与抚河有机质来源则不同, 抚河以自生有机物源为主, 受陆源输入影响较小[37], 脱甲河则受陆源输入影响显著, 内源有机物影响微弱.
3.3 水系N2O关键产生过程已知N2O主要来自硝化过程和反硝化过程, 而反硝化过程又包括普通反硝化、硝化细菌反硝化和好氧反硝化等, 这些复杂生化过程交互反应产生N2O[2, 38, 39].硝化过程中, 羟胺作为氨氧化细菌将氨氧化成亚硝酸盐的中间产物而产生, 而N2O作为羟胺氧化成亚硝酸盐过程的副产品而产生[2].硝化细菌反硝化过程是典型的自养氨氧化细菌将亚硝酸盐还原为N2O的过程, 该过程通常在氧气有限的条件下发生[40].而在异养反硝化过程中, 异养反硝化菌逐步地将硝酸盐或亚硝酸盐还原为N2, N2O作为中间产物而存在[2].然而, 亚硝化氮混合也被认为是N2O产生的重要途径[41, 42], 如Soler-Jofra等[41]发现亚硝化氮混合途径产生的N2O贡献了总的N2O排放的三分之一.有研究表明, 氮氧双同位素不仅有助于追溯流域硝酸盐来源, 也能够有效地识别氮素的迁移转化过程[2, 11].硝态氮的氮氧同位素组成受硝化和反硝化过程共同影响[23], 脱甲河4级河段硝化过程中δ18O-NO3-组成均落在-10‰~10‰范围内[23].自然条件下, 光合作用、微生物活动和蒸发等过程均会影响硝化过程中氧同位素的分馏[43], 脱甲河S1河段硝化过程中的δ18O-NO3-和δ18O-H2O比其他河段明显贫化, 可能受海拔较高、蒸发较弱等因素影响.Soldatova等[43]在鄱阳湖流域的研究也发现淹水稻田的蒸发导致了水体18O的富集, 之后渗入含水层, Yue等[30]在松花江流域也发现蒸发导致水体18O的富集.此外, δ15N-NO3-与NO3--N浓度呈弱的正相关且δ15N-NO3-/δ18O-NO3-均非2:1[23].根据分析结果, 可初步判定脱甲河水体可能以硝化过程脱氮为主, N2O的产生可能由硝化过程所主导.Vavilin等[44]曾指出酸性和中性土壤环境会减缓反硝化过程.Li等[31]在杭州郊区小流域的研究也发现硝化过程和植物吸收是促进该小流域氮素转化的重要生物地球化学过程, 而反硝化过程几乎未发生.另外, Divers等[35]对城市溪流进行研究发现约有19%的污水样品同位素受反硝化过程影响, 硝化过程的影响仍占据优势.然而, Jurado等[45]对地下水N2O动态的研究则发现N2O的累积主要受反硝化过程影响, 较少受硝化过程影响, 与本研究结果差异较明显, 可能与研究对象的地球化学(硝酸盐、铵盐、溶解氧及溶解有机碳等)及水文地质(水位变化、含水层渗透率等)特征有关.目前, 对水体氮素迁移转化过程开展的多为定性化研究, 想要得到量化的更精确的硝化反硝化数据还需进行原位实验或借助其他方法.
4 结论(1) 脱甲河水体δ15N-NO3-和δ18O-NO3-变化范围分别是-19.87‰~8.11‰和-3.03‰~5.81‰, 氮素来源呈现多端元特征, 与流域农业生产及生活排污密切相关; 各河段NO3--N来源存在差异, S1河段来源于土壤流失氮, S2~S4河段来源不仅有土壤流失氮, 而且包括铵态氮肥和粪肥.
(2) 河流沉积物有机质的δ15N和C/N分别在-0.69‰~11.21‰和7.30~12.02之间变化, 有机质氮素来源与S1~S4河段土地利用类型相关, 靠近源头区的S1河段沉积物有机质主要来源是土壤有机质, 而S2~S4河段受农业面源排放及生活排污影响, 污水可能是主要氮素来源.(3)S1~S4河段硝化过程中的δ18O-NO3-分别为-7.01‰、-0.17‰、-0.28‰和-0.60‰, 水体硝态氮浓度与其δ15N呈较弱正相关且δ15N-NO3-/δ18O-NO3-分别为0.66、-41.01、-30.23和9.39.根据硝化反硝化过程判别依据, 各河段氮素转化虽存在差异, 但均以硝化过程占优势, 即硝化过程可能对脱甲河水系N2O的产生贡献较大.
| [1] | Prather M J, Hsu J, Deluca N M, et al. Measuring and modeling the lifetime of nitrous oxide including its variability[J]. Journal of Geophysical Research:Atmospheres, 2015, 120(11): 5693-5705. DOI:10.1002/2015JD023267 |
| [2] | Duan H R, Ye L, Erler D, et al. Quantifying nitrous oxide production pathways in wastewater treatment systems using isotope technology-A critical review[J]. Water Research, 2017, 122: 96-113. DOI:10.1016/j.watres.2017.05.054 |
| [3] | Burgos M, Ortega T, Forja J M. Temporal and spatial variation of N2O production from estuarine and marine shallow systems of Cadiz Bay (SW, Spain)[J]. Science of the Total Environment, 2017, 607-608: 141-151. DOI:10.1016/j.scitotenv.2017.07.021 |
| [4] | Revell L E, Tummon F, Salawitch R J, et al. The changing ozone depletion potential of N2O in a future climate[J]. Geophysical Research Letters, 2015, 42(22): 10047-10055. DOI:10.1002/2015GL065702 |
| [5] | Rosamond M S, Thuss S J, Schiff S L. Dependence of riverine nitrous oxide emissions on dissolved oxygen levels[J]. Nature Geoscience, 2012, 5(10): 715-718. DOI:10.1038/ngeo1556 |
| [6] | Zhang X X, Yin S, Li Y S, et al. Comparison of greenhouse gas emissions from rice paddy fields under different nitrogen fertilization loads in Chongming Island, Eastern China[J]. Science of the Total Environment, 2014, 472: 381-388. DOI:10.1016/j.scitotenv.2013.11.014 |
| [7] | Hinshaw S E, Dahlgren R A. Nitrous oxide fluxes and dissolved N gases (N2 and N2O) within riparian zones along the agriculturally impacted San Joaquin River[J]. Nutrient Cycling in Agroecosystems, 2016, 105(2): 85-102. DOI:10.1007/s10705-016-9777-y |
| [8] | Popescu R, Mimmo T, Dinca O R, et al. Using stable isotopes in tracing contaminant sources in an industrial area:a case study on the hydrological basin of the Olt River, Romania[J]. Science of the Total Environment, 2015, 533: 17-23. DOI:10.1016/j.scitotenv.2015.06.078 |
| [9] | Wang S Q, Zheng W B, Currell M, et al. Relationship between land-use and sources and fate of nitrate in groundwater in a typical recharge area of the North China Plain[J]. Science of the Total Environment, 2017, 609: 607-620. DOI:10.1016/j.scitotenv.2017.07.176 |
| [10] | Wassenaar L I, Hendry M J, Harrington N. Decadal geochemical and isotopic trends for nitrate in a transboundary aquifer and implications for agricultural beneficial management practices[J]. Environmental Science & Technology, 2006, 40(15): 4626-4632. |
| [11] | Yang Y Y, Toor G S. δ15N and δ18O reveal the sources of nitrate-nitrogen in urban residential stormwater runoff[J]. Environmental Science & Technology, 2016, 50(6): 2881-2889. |
| [12] | Kaushal S S, Groffman P M, Band L E, et al. Tracking nonpoint source nitrogen pollution in human-impacted watersheds[J]. Environmental Science & Technology, 2011, 45(19): 8225-8232. |
| [13] | Bettez N D, Groffman P M. Nitrogen deposition in and near an urban ecosystem[J]. Environmental Science & Technology, 2013, 47(11): 6047-6051. |
| [14] | Carey R O, Hochmuth G J, Martinez C J, et al. Evaluating nutrient impacts in urban watersheds:Challenges and research opportunities[J]. Environmental Pollution, 2013, 173: 138-149. DOI:10.1016/j.envpol.2012.10.004 |
| [15] |
徐文彬. 大气N2O的稳定氮同位素质量平衡探讨[J]. 地质地球化学, 1999, 27(2): 22-28. Xu W B. Improved estimates for nitrogen isotope budget balance of tropospheric N2O[J]. Geology-Geochemistry, 1999, 27(2): 22-28. |
| [16] |
李艳利, 杨梓睿, 尹希杰, 等. 太子河下游河流硝酸盐来源及其迁移转化过程[J]. 环境科学, 2018, 39(3): 1076-1084. Li Y L, Yang Z R, Yin X J, et al. Identification of nitrate sources and the fate of nitrate in downstream areas:A case study in the Taizi River basin[J]. Environmental Science, 2018, 39(3): 1076-1084. |
| [17] |
郭庆军, 王春雨, 朱光旭, 等. 氮同位素研究城市湖泊沉积物有机质来源和迁移过程-以北京为例[J]. 矿物岩石地球化学通报, 2015, 34(3): 532-538. Guo Q J, Wang C Y, Zhu G X, et al. Research on the source and migration process of organic matter of lake sediments using nitrogen isotope-A case study in Beijing[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2015, 34(3): 532-538. DOI:10.3969/j.issn.1007-2802.2015.03.009 |
| [18] |
王毛兰, 张丁苓, 赖建平, 等. 鄱阳湖水体悬浮有机质碳氮同位素分布特征及来源探讨[J]. 中国环境科学, 2014, 34(9): 2342-2350. Wang M L, Zhang D L, Lai J P, et al. Distribution and sources of stable organic carbon and nitrogen isotopes in suspended particulate organic matter of Poyang Lake[J]. China Environmental Science, 2014, 34(9): 2342-2350. |
| [19] |
晁海娟, 高建华, 贾建军, 等. 长江口及其邻近海域表层沉积物的有机质物源变化分析[J]. 海洋环境科学, 2017, 36(2): 237-242. Chao H J, Gao J H, Jia J J, et al. Change of organic matter sources in surface sediments over Changjiang estuary and its adjacent waters[J]. Marine Environmental Science, 2017, 36(2): 237-242. |
| [20] |
李瑞, 肖琼, 刘文, 等. 运用硫同位素、氮氧同位素示踪里湖地下河硫酸盐、硝酸盐来源[J]. 环境科学, 2015, 36(8): 2877-2886. Li R, Xiao Q, Liu W, et al. Using δ34S-SO42- and δ15N-NO3-, δ18O-NO3- to trace the sources of sulfur and nitrate in Lihu Lake undergound water, Guangxi, China[J]. Environmental Science, 2015, 36(8): 2877-2886. |
| [21] |
赵强, 秦晓波, 吕成文, 等. 亚热带农业小流域水体氮素及其稳定同位素分布特征[J]. 中国生态农业学报, 2018, 26(1): 136-145. Zhao Q, Qin X B, Lyu C W, et al. Distribution of nitrogen and its stable isotope from a small agricultural catchment in the subtropics[J]. Chinese Journal of Eco-Agriculture, 2018, 26(1): 136-145. |
| [22] |
宋立芳, 王毅, 吴金水, 等. 水稻种植对中亚热带红壤丘陵区小流域氮磷养分输出的影响[J]. 环境科学, 2014, 35(1): 150-156. Song L F, Wang Y, Wu J S, et al. Impact of rice agriculture on nitrogen and phosphorus exports in streams in hilly red soil Earth region of central subtropics[J]. Environmental Science, 2014, 35(1): 150-156. |
| [23] | Kendall C, Elliott E M, Wankel S D.Tracing anthropogenic inputs of nitrogen to ecosystems[M]//Michener R, Lajtha K.Stable Isotopes in Ecology and Environmental Science.2nd ed.Oxford: Blackwell, 2007.375-449. |
| [24] | Kendall C, McDonnell J J. Isotope tracers in catchment hydrology[M]. Amsterdam: Elsevier, 2012. |
| [25] | El Gaouzi F Z J, Sebilo M, Ribstein P, et al. Using δ15N and δ18O values to identify sources of nitrate in karstic springs in the Paris basin (France)[J]. Applied Geochemistry, 2013, 35: 230-243. DOI:10.1016/j.apgeochem.2013.04.015 |
| [26] | Xue D M, De Baets B, van Cleemput O, et al. Use of a Bayesian isotope mixing model to estimate proportional contributions of multiple nitrate sources in surface water[J]. Environmental Pollution, 2012, 161: 43-49. DOI:10.1016/j.envpol.2011.09.033 |
| [27] | Meyers P A. Preservation of elemental and isotopic source identification of sedimentary organic matter[J]. Chemical Geology, 1994, 114(3-4): 289-302. DOI:10.1016/0009-2541(94)90059-0 |
| [28] | Gearing J N.The use of stable isotope ratios for tracing the nearshore-offshore exchange of organic matter[M]//Jansson B O.Coastal-offshore ecosystem interactions.Berlin, Heidelberg: Springer, 1988, 22: 69-101. |
| [29] |
倪兆奎, 李跃进, 王圣瑞, 等. 太湖沉积物有机碳与氮的来源[J]. 生态学报, 2011, 31(16): 4661-4670. Ni Z K, Li Y J, Wang S R, et al. The sources of organic carbon and nitrogen in sediment of Taihu Lake[J]. Acta Ecologica Sinica, 2011, 31(16): 4661-4670. |
| [30] | Yue F J, Liu C Q, Li S L, et al. Analysis of δ15N and δ18O to identify nitrate sources and transformations in Songhua River, Northeast China[J]. Journal of Hydrology, 2014, 519(Pt A): 329-339. |
| [31] | Han L, Huang M S, Ma M H, et al. Evaluating sources and processing of nonpoint source nitrate in a small suburban watershed in China[J]. Journal of Hydrology, 2018, 559: 661-668. DOI:10.1016/j.jhydrol.2017.04.057 |
| [32] | Ding J T, Xi B D, Gao R T, et al. Identifying diffused nitrate sources in a stream in an agricultural field using a dual isotopic approach[J]. Science of the Total Environment, 2014, 484: 10-18. DOI:10.1016/j.scitotenv.2014.03.018 |
| [33] | Jin Z F, Qin X, Chen L X, et al. Using dual isotopes to evaluate sources and transformations of nitrate in the West Lake watershed, eastern China[J]. Journal of Contaminant Hydrology, 2015, 177-178: 64-75. DOI:10.1016/j.jconhyd.2015.02.008 |
| [34] |
梁慧雅, 翟德勤, 孔晓乐, 等. 府河-白洋淀硝酸盐来源判定及迁移转化规律[J]. 中国生态农业学报, 2017, 25(8): 1236-1244. Liang H Y, Zhai D L, Kong X L, et al. Sources, migration and transformation of nitrate in Fuhe River and Baiyangdian Lake, China[J]. Chinese Journal of Eco-Agriculture, 2017, 25(8): 1236-1244. |
| [35] | Divers M T, Elliott E M, Bain D J. Quantification of nitrate sources to an urban stream using dual nitrate isotopes[J]. Environmental Science &Technology, 2014, 48(18): 10580-10587. |
| [36] |
孟志龙, 杨永刚, 秦作栋, 等. 汾河下游流域水体硝酸盐污染过程同位素示踪[J]. 中国环境科学, 2017, 37(3): 1066-1072. Meng Z L, Yang Y G, Qin Z D, et al. Isotopic tracing for nitrate pollution process of water body in the lower reaches of Fenhe River[J]. China Environmental Science, 2017, 37(3): 1066-1072. |
| [37] |
王毛兰, 艾永平, 张丁苓. 鄱阳湖三江口柱状沉积物有机氮同位素特征及其环境指示意义[J]. 中国环境科学, 2015, 35(2): 558-564. Wang M L, Ai Y P, Zhang D L. Stable organic nitrogen isotope in core sediments of the Three Rivers Estuary, Poyang Lake and its environmental implications[J]. China Environmental Science, 2015, 35(2): 558-564. |
| [38] | Devol A H. Denitrification, anammox, and N2 production in marine sediments[J]. Annual Review of Marine Science, 2015, 7: 403-423. DOI:10.1146/annurev-marine-010213-135040 |
| [39] | Sabba F, Picioreanu C, Nerenberg R. Mechanisms of nitrous oxide (N2O) formation and reduction in denitrifying biofilms[J]. Biotechnology and Bioengineering, 2017, 114(12): 2753-2761. DOI:10.1002/bit.26399 |
| [40] | Wrage N, Velthof G L, van Beusichem M L, et al. Role of nitrifier denitrification in the production of nitrous oxide[J]. Soil Biology and Biochemistry, 2001, 33(12-13): 1723-1732. DOI:10.1016/S0038-0717(01)00096-7 |
| [41] | Soler-Jofra A, Stevens B, Hoekstra M, et al. Importance of abiotic hydroxylamine conversion on nitrous oxide emissions during nitritation of reject water[J]. Chemical Engineering Journal, 2016, 287: 720-726. DOI:10.1016/j.cej.2015.11.073 |
| [42] | Terada A, Sugawara S, Hojo K, et al. Hybrid nitrous oxide production from a partial nitrifying bioreactor:hydroxylamine interactions with nitrite[J]. Environmental Science & Technology, 2017, 51(5): 2748-2756. |
| [43] | Soldatova E, Guseva N, Sun Z X, et al. Sources and behaviour of nitrogen compounds in the shallow groundwater of agricultural areas (Poyang Lake basin, China)[J]. Journal of Contaminant Hydrology, 2017, 202: 59-69. DOI:10.1016/j.jconhyd.2017.05.002 |
| [44] | Vavilin V A, Rytov S V. Nonlinear dynamic model describing the fractionation of stable nitrogen isotopes in denitrification process with nitrous oxide formation[J]. Water Resources, 2015, 42(2): 215-219. DOI:10.1134/S0097807815020141 |
| [45] | Jurado A, Borges A V, Brouyère S. Dynamics and emissions of N2O in groundwater:A review[J]. Science of the Total Environment, 2017, 584-585: 207-218. DOI:10.1016/j.scitotenv.2017.01.127 |
 2018, Vol. 39
2018, Vol. 39


