黄河干流宁蒙段自中卫市南昌滩流入宁夏回族自治区, 由石嘴山市麻黄沟流出进入内蒙古自治区, 最后于准格尔旗马乡流出, 全长1227 km, 流域面积20.99万km2, 形成了广阔的宁夏平原和河套平原[1, 2].宁蒙段是沿岸工农业生产以及居民生活用水的重要来源, 也是重要的纳污河道.春季河流解冻, 土壤消融, 工厂废水以及烟气、矿渣等废物的处理会释放重金属物质, 通过土壤下渗、污水排放及大气迁移等方式进入黄河水体; 部分金属甚至吸附到沉积物表面或通过富集作用进入生物体内, 严重危害了动植物生长和人体健康[3~5].
地表水中的腐殖质是土壤腐殖质、水生植物以及浮游生物的分解产物在自然界的长期作用下形成的[6], 主要包括腐殖酸(humic acid, HA)、富里酸(fulvic acid, FA)和胡敏素(humin, HU), 这3种物质占水中溶解性有机物(dissolved organic matter, DOM)的50%~80%[7, 8], 是导致水体色度的主要原因[9].DOM表面含有苯环、羧基、酚羟基等基团[10, 11], 这些基团可与营养元素、痕量金属或疏水性有机物发生相互作用[12, 13], 进而影响其毒性或迁移转化规律.由于不同DOM组分的亲疏水性及官能团结构不同, 其对金属离子的络合能力及毒性影响也不同[14, 15].基于XAD大孔吸附树脂的DOM组分提取是广泛使用的方法.近年来, 不同DOM组分与金属离子相关性的研究已有大量报道.例如, Matar等[16]的研究表明亲水性DOM组分可以通过络合作用降低Cu的生物有效性; 闻怡等[17]发现疏水性组分中包含的FA可以促进Cu与水体悬浮颗粒物之间的吸附作用, 使得Cu最终沉淀进而降低其毒性.
本文以黄河干流宁蒙段(下河沿至头道拐)为研究区域, 采用XAD-4和XAD-8树脂提取法, 将水样中的DOM分为疏水性酸(HOA)、疏水性碱(HOB)、弱疏水性酸(WHOA)和亲水性物质(HYI)这4个组分, 重点分析了DOM及其组分的沿程分布规律, 以及与Cu、Pb、Zn、Cr、As这5种金属离子之间的相互作用关系, 以期为该段水质监测及沿岸饮水工程建设提供参考依据.
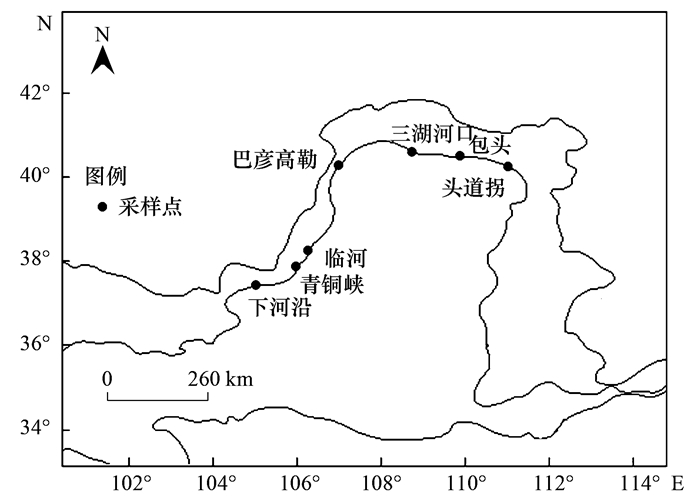
1 材料与方法 1.1 样品采集与分析2015年春季(4月)在黄河干流宁蒙段控制断面7个水文站采集水样(见图 1), 样品采集参考HJ 494-2009水质采样技术指导、HJ/T 91-2002地表水和污水监测技术规范、HJ 493-2009水质样品的保存和管理技术规定、HJ/T 372-2007水质自动采样器技术要求及检测方法, 使用三线九点等体积汇合法.混合水过0.45 μm滤膜后冷冻(-20℃)保存, 测试前置于常温条件下解冻.
|
图 1 黄河宁蒙段采样点位分布示意 Fig. 1 Map of sampling sites along the Ning-Meng section of the Yellow River |
溶解性有机物的极性分离参考文献[18]的方法.利用XAD-8和XAD-4树脂串联, 将水体中的天然有机物分为疏水性酸(HOA)、疏水性碱(HOB)、亲水物质(HYI)和弱疏水酸(WHOA)这4个组分.溶解性有机碳(dissolved organic carbon, DOC)的测定参考国标HJ 501-2009, 使用岛津TOC-VCPN总有机碳分析仪进行测定.紫外可见光谱检测采用岛津UV-1800紫外可见光光度计, 扫描范围200~700 nm, 参比为超纯水.三维荧光光谱采用Cary Eclipse型荧光分光光度计, 激发波长为200~450 nm, 扫描间隔5 nm; 发射波长为270~570 nm, 扫描间隔1 nm; 激发光和发射光的带宽均为10 nm; 扫描速度600 nm ·min-1, 扫描电压800 V, 参比为超纯水.测试结果扣除超纯水空白以消除仪器背景值和拉曼散射, 同时扣除Em < Ex+20 nm以及Em < 2Ex-20 nm区域以零值替换来消除瑞利散射的影响[19].重金属含量参照国标HJ 700-2014, 水样过0.45 μm滤膜后加酸, 采用电感测量耦合等离子体质谱(ICP-MS, Thermo Scientific, X2)进行测定, 测试过程中同时测定质控、空白、加标样品, 确保测试结果的准确性.
1.2 数据处理与分析数据分析与制图采用SPSS 18.0与Origin 9.0软件.对各采样点原水及4种组分的有机碳含量、荧光峰值及重金属含量做Pearson相关性分析, 相关性分析中均以P < 0.05表示显著性差异水平.
2 结果与分析 2.1 DOM沿程变化特征宁蒙段水体DOC含量及组分变化如图 2所示, 7个站点原水DOC含量在2.60~6.39 mg ·L-1范围内.从宁蒙段上游下河沿站至下游头道拐站, DOC值沿程逐渐增加, 其中包头站DOC值最大, 为6.39 mg ·L-1.从DOM组分来看, 除下河沿以外, DOM组分均以亲水性物质HYI为主, 占比58.9%~78.2%;其次是疏水性酸HOA, 占比12.3%~34.2%.下河沿站DOM组分以疏水性有机酸HOA为主(58.9%), 亲水性物质HYI次之(33.4%).Hu等[20]对黄河干流郑州段水体进行组分分析也得到了相似的结果.有研究表明[15, 21], 疏水性组分主要包含富里酸FA和腐殖酸HA, 亲水性组分则为小分子有机物如多糖、蛋白质等, 此外还含有微量的FA.

|
图 2 宁蒙段水体DOC总量及组分沿程变化情况 Fig. 2 Changes in DOC and DOM fractions along the Ning-Meng section of the Yellow River |
通常情况下, 未受污染的天然水体腐殖化程度较高, DOM中疏水性组分比重较大, 尤其是富里酸.而对于作为纳污河流的宁蒙段水体来说, 废水中较多微生物的排入导致河流有机物在分解作用下形成了大量小分子亲水性物质, 因此亲水性组分含量较高, 水体腐殖化程度下降[21].在饮用水工程中, 亲水性组分和疏水性组分分别具有较高的三卤甲烷生成势和含氮消毒副产物生成势, 易产生具有致癌作用的消毒副产物, 因此, 控制DOM组分含量对于饮用水安全有重要作用[20].
2.2 DOM光谱学特征表 1列出了宁蒙段各站点水体比紫外吸收值SUVA254和荧光指数FI值.SUVA254为UV254与DOC的比值, 可以反映水中天然存在的腐殖质类大分子有机物及含有C=C双键、C=O双键的芳香族化合物的多少.宁蒙段水体SUVA254变化范围在1.31~0.63之间, 均小于2, 其中下河沿站最高, 表明该断面水体腐殖化程度最高.Edzwald等[22]的研究结果表明, SUVA254小于2的水体有机质芳香性基团含量较少, 以腐殖化程度较低的亲水性小分子为主, 这与DOM组分表征结果一致.
|
|
表 1 宁蒙段水体水质参数及紫外与荧光特性比较 Table 1 Comparison of water quality parameters, UV, and fluorescence characteristics of DOM along the Ning-Meng section |
荧光指数FI表示激发波长370 nm条件下, 发射波长在450 nm和500 nm处荧光强度的比值.其可以用来判断有机物的来源[23], 当FI在1.7~2.0范围时, 表示水中有机物为生物来源(内源), 如水体中的藻类、细菌及水生植物所产生的有机物和底泥释放的有机物; FI在1.3~1.4范围则表示有机物主要为陆源(外源), 例如地表径流和浅层地下水从土壤中渗沥出的有机物, 这种水体腐殖质含量通常较大且通常含有较高的HOA[24].本研究宁蒙段7个水样FI在1.48~1.71范围内变化, 平均值为1.63, 表明其为陆源和内源的共同作用.其中, 下河沿站FI指数最低, 陆源作用最为明显, 水体腐殖化程度最高; 其他断面FI指数靠近1.7, 内源作用稍占优势, 水中生物分解作用较强, 这与SUVA254所得结果一致.
宁蒙段水体三维荧光光谱(EEM)如图 3所示, 表 2给出了各站点溶解性有机物3种荧光峰激发/发射波长以及峰强IM.对比已有研究结果(表 3)可知, 7个站点水体DOM共出现3个荧光峰, 峰A: Ex/Em=220~260 nm/390~480 nm(紫外区类腐殖质), 主要为类富里酸; 峰C: Ex/Em=300~320 nm/400~430 nm(可见区类腐殖质), 主要为类腐殖酸, 两者产生的荧光峰与羧基、羟基的存在有关[25, 26];峰T1: Ex/Em=230 nm/320~350 nm(色氨酸, 类蛋白质), 该峰的产生与水生生物残体蛋白质降解产物有关, 还可能来自于污水的排入[27, 28].

|
图 3 宁蒙段各站点水体DOM三维荧光光谱图 Fig. 3 EEM contour of DOM along Ning-Meng section of the Yellow River |
|
|
表 2 宁蒙段水体溶解性有机物三维荧光特征 Table 2 EEM characteristics of DOM along the Ning-Meng section |
|
|
表 3 EEM荧光基团及特征吸收峰位置[26, 29, 30] Table 3 Excited and emitted wavelength of fluorescent monomers in EEM plots from the literature |
对比3种荧光峰可以发现, 峰强A>C>T1, 这是由于富里酸含有较多芳香性结构及荧光增强基团, 如羟基、羧基等, 导致A峰荧光强度较高.此外, 水温、离子强度等也会影响荧光峰的强度[21].从沿程变化来看, 下河沿至头道拐站, 水中有机物成分逐渐复杂, 临河站开始出现较明显的C峰和T1峰, 且强度逐渐增大, 结合该段水体氨氮和COD含量升高的特点, 说明水体受污水排放的影响程度逐渐增大, 微生物分解作用逐渐增强, 进而导致水体腐殖化程度逐渐降低.
2.3 重金属含量宁蒙段水体中Cu、Pb、Zn、Cr、As这5种金属离子沿程变化如图 4所示.可以看出, 水中5种金属离子含量均较低(< 6.00 μg ·L-1), 且满足地表水环境质量标准(GB 3838-2002)I类水体标准; 从下河沿至头道拐站, 各站点Pb含量接近于0 μg ·L-1; Zn、As、Cr含量较高且沿程变化较大, Cu含量沿程逐渐上升.临河和包头重金属含量高于其他断面, 这可能与该区域人类活动较强有关.水中重金属含量受到pH值、离子强度及有机物形态等多方面因素的综合影响.黄河水体中较高的悬浮物也会吸附重金属离子并沉积下来, 这可能是导致水中溶解重金属含量较低的原因之一[31~34].

|
图 4 宁蒙段各站点水体重金属含量变化情况 Fig. 4 Distribution of heavy metals in waters of the Ning-Meng section |
采用SPSS考察了下河沿至头道拐各站点DOM 3类荧光峰峰强与4种DOM组分占比的关系, 结果如表 4所示.可知T1峰和C峰与HYI组分占比之间呈显著正相关性.随着HYI组分含量的升高, C峰和T1峰强度有所增大, 说明HYI组分含有的芳香类蛋白质及腐殖酸类物质对这2类荧光峰峰强起主导作用.此外, 组分HOA与T1峰和C峰呈现出显著负相关性, 这是因为HOA中含有更多可产生类腐殖质荧光峰的FA和HA, 负相关性可能与HOA组分有机物浓度较高而产生荧光淬灭效应有关[27]; HOB和WHOA组分含量较低, 对有机物荧光强度的影响较弱, 因此相关性较低.
|
|
表 4 宁蒙段DOM三维荧光峰强度与各组分占比的相关系数1) Table 4 Correlation coefficients of EEM fluorescence maxima and DOM fractions along the Ning-Meng section |
3.2 DOM组分与金属离子的相关性
水中5种金属离子与DOM各组分含量相关性结果如表 5所示.可以看出, DOM与5种重金属之间存在一定程度的相关性, 其中与Cu呈显著正相关性(R=0.921, P < 0.01).对应DOM的4种有机组分发现, Cu与HYI之间呈显著正相关性(R=0.824, P < 0.05), 而与HOA呈负相关(R=-0.785, P < 0.05), 表明宁蒙段水体中HYI组分在DOM与Cu的络合过程中发挥主要作用.
|
|
表 5 宁蒙段DOM组分与重金属之间的相关关系1) Table 5 Correlation matrix of DOM fractions and heavy metals along the Ning-Meng section |
树脂分离富集的HYI组分主要包含多糖、蛋白质等小分子有机物以及微量的腐殖质, 研究表明, 该组分含有的少量亲水性羧基和羟基可以与Cu发生络合反应, 该反应结合程度较低但反应速度较快[15, 35].同时, 对于Cu离子浓度较低的水体, 氨基酸中的含氮基团在与Cu离子的络合过程中也发挥重要的作用[36].
3.3 DOM三维荧光峰与Cu的相关性基于上述研究结果, 进一步分析了宁蒙段DOM 3类荧光峰与Cu离子的相互关系, 考虑到有机物浓度也会对荧光强度产生影响, 以DOM三维荧光峰强度IM和有机碳含量DOC的比值与Cu离子进行相关性分析, 结果见图 5.可以看出, IM/DOC值与Cu离子均呈现出显著的负相关性.由于Cu离子是顺磁性金属离子, 与DOM的络合作用会导致荧光淬灭效应, 因此荧光峰强度降低[37, 38].此外, Cu与T1峰的相关性好于A峰和C峰, 说明水中Cu主要与芳香蛋白质发生络合作用, 而经树脂分级后的芳香类蛋白质主要存在于HYI组分中, 因此HYI与Cu相关性最强.

|
图 5 宁蒙段DOM荧光峰强度和有机碳浓度比值与Cu的相关性 Fig. 5 Relationship between IM/DOC and Cu along the Ning-Meng section |
(1) 黄河宁蒙段水体溶解性有机物(DOM)的产生过程包含陆源和生物来源两种类型.整体上, DOM总量由下河沿至头道拐沿程逐渐增加.XAD树脂分离结果表明, 各断面DOM腐殖化程度较低, 以亲水性的蛋白质类小分子物质(HYI)为主, 疏水性酸(HOA)次之, 这与黄河沿岸排污导致内源作用增强有关.三维荧光光谱图可明显发现类腐殖质和类蛋白质荧光峰, 且从下河沿至头道拐类腐殖质峰逐渐增强, 进一步证实了内源污水输入的影响. T1类蛋白峰和C可见区类腐殖质峰与HYI组分占比呈现出显著正相关性, 说明HYI作为主要组分对有机物荧光的主导作用.
(2) SPSS相关性分析结果表明, DOM与Pb、Zn、Cu、Cr、As这5种金属离子之间呈现不同程度的相互关系, 其中与Cu离子呈显著正相关; 4种组分中HYI与Cu离子相关性最好.这主要因为HYI组分与Cu的络合速度更快而优先发生络合作用, 在金属含量较低的水体中表现更为明显.进一步研究发现, T1类蛋白峰与DOC的比值与Cu离子呈显著负相关, 芳香蛋白类物质荧光峰强度随Cu离子浓度的升高而降低, 这可能是Cu与HYI中的芳香类蛋白质发生络合产生荧光淬灭效应, 从而导致荧光强度降低.
| [1] |
刘晓锋, 李科社, 高宏伟, 等. 黄河干流宁蒙段渔业资源调查及保护对策[J]. 水生态学杂志, 2010, 3(4): 135-141. Liu X F, Li K S, Gao H W, et al. Research and protective strategy of the fishery resource in Ningxia-Neimeng River reach of Yellow River trunk stream[J]. Journal of Hydroecology, 2010, 3(4): 135-141. |
| [2] | 秦毅. 黄河上游河流环境变化与河道响应机理及其调控策略——宁蒙河段为对象[D]. 西安: 西安理工大学, 2009. |
| [3] |
张妍, 李发东, 欧阳竹, 等. 黄河下游引黄灌区地下水重金属分布及健康风险评估[J]. 环境科学, 2013, 34(1): 121-128. Zhang Y, Li F D, Ouyang Z, et al. Distribution and health risk assessment of heavy metals of groundwaters in the irrigation district of the lower reaches of Yellow River[J]. Environment Science, 2013, 34(1): 121-128. |
| [4] | Burton G A Jr. Metal bioavailability and toxicity in sediments[J]. Critical Reviews in Environmental Science & Technology, 2010, 40(9-10): 852-907. |
| [5] | Ahmad J U, Goni M A. Heavy metal contamination in water, soil, and vegetables of the industrial areas in Dhaka, Bangladesh[J]. Environmental Monitoring and Assessment, 2010, 166(1-4): 347-357. DOI:10.1007/s10661-009-1006-6 |
| [6] |
冯华军, 胡立芳, 单丹, 等. 水体腐殖质危害及去除的研究进展[J]. 科技通报, 2008, 24(4): 553-558. Feng H J, Hu L F, Shan D, et al. Assessment on the risk of aquatic humics and prospect on its removal technology[J]. Bulletin of Science and Technology, 2008, 24(4): 553-558. |
| [7] | Klavins M, Eglīte L. Immobilisation of humic substances[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2002, 203(1-3): 47-54. |
| [8] |
田林锋, 胡继伟, 李存雄, 等. 通过DOM的光谱特性对长江源头典型高原深水湖泊进行评价[J]. 中国工程科学, 2010, 12(6): 80-84, 112. Tian L F, Hu J W, Li C X, et al. Evaluation of a typical plateau deep lake by DOM spectral characteristics[J]. Engineering Sciences, 2010, 12(6): 80-84, 112. |
| [9] | Leenheer J A, Croue J P. Peer reviewed:characterizing aquatic dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(1): 18A-26A. |
| [10] | Smith D S, Kramer J R. Multi-site proton interactions with natural organic matter[J]. Environment International, 1999, 25(2-3): 307-314. DOI:10.1016/S0160-4120(98)00108-1 |
| [11] | Al-Rasheed R, Cardin D J. Photocatalytic degradation of humic acid in saline waters:Part 2. Effects of various photocatalytic materials[J]. Applied Catalysis A:General, 2003, 246(1): 39-48. DOI:10.1016/S0926-860X(02)00667-1 |
| [12] | Kang K H, Shin H S, Park H. Characterization of humic substances present in landfill leachates with different landfill ages and its implications[J]. Water Research, 2002, 36(16): 4023-4032. DOI:10.1016/S0043-1354(02)00114-8 |
| [13] | Fooken U, Liebezeit G. Distinction of marine and terrestrial origin of humic acids in North Sea surface sediments by absorption spectroscopy[J]. Marine Geology, 2000, 164(3-4): 173-181. DOI:10.1016/S0025-3227(99)00133-4 |
| [14] | Leenheer J A, Brown G K, MacCarthy P, et al. Models of metal binding structures in fulvic acid from the Suwannee River, Georgia[J]. Environmental Science & Technology, 1998, 32(16): 2410-2416. |
| [15] | Ma H Z, Allen H E, Yin Y J. Characterization of isolated fractions of dissolved organic matter from natural waters and a wastewater effluent[J]. Water Research, 2001, 35(4): 985-996. DOI:10.1016/S0043-1354(00)00350-X |
| [16] | Matar Z, Chebbo G, Troupel M, et al. Influence of organic matter from urban effluents on trace metal speciation and bioavailability in river under strong urban pressure[A]. ln: Xu J M, Wu J J, He Y. Functions of Natural Organic Matter in Changing Environment[C]. Dordrecht: Springer, 2013. 1-4. |
| [17] |
闻怡, 陶澍, 龙爱民, 等. 胡敏酸对铜的鱼鳃生物有效性影响的计算机模拟[J]. 环境科学, 2001, 22(2): 36-40. Wen Y, Tao S, Long A M, et al. Computer simulation of ha influence on copper bioavailability to the fish gills[J]. Environmental Science, 2001, 22(2): 36-40. |
| [18] | Malcolm R L. The uniqueness of humic substances in each of soil, stream and marine environments[J]. Analytica Chimica Acta, 1990, 232: 19-30. DOI:10.1016/S0003-2670(00)81222-2 |
| [19] |
王书航, 王雯雯, 姜霞, 等. 基于三维荧光光谱-平行因子分析技术的蠡湖CDOM分布特征[J]. 中国环境科学, 2016, 36(2): 517-524. Wang S H, Wang W W, Jiang X, et al. Distribution of chromophoric dissolved organic matter in Lihu Lake using excitation-emission matrix fluorescence and parallel factor analysis[J]. China Environmental Science, 2016, 36(2): 517-524. |
| [20] | Hu C Y, Zhu H Z, Lin Y L, et al. Dissolved organic matter fractions and disinfection by-product formation potential from major raw waters in the water-receiving areas of south-to-north water diversion project, China[J]. Desalination and Water Treatment, 2015, 56(6): 1689-1697. DOI:10.1080/19443994.2014.953211 |
| [21] | 吴丰昌. 天然有机质及其与污染物的相互作用[M]. 北京: 科学出版社, 2010: 132-135. |
| [22] | Edzwald J K, Tobiason J E. Enhanced coagulation:US requirements and a broader view[J]. Water Science and Technology, 1999, 40(9): 63-70. DOI:10.2166/wst.1999.0444 |
| [23] | McKnight D M, Boyer E W, Westerhoff P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity[J]. Limnology and Oceanography, 2001, 46(1): 38-48. DOI:10.4319/lo.2001.46.1.0038 |
| [24] |
隋志男, 郅二铨, 姚杰, 等. 三维荧光光谱区域积分法解析辽河七星湿地水体DOM组成及来源[J]. 环境工程技术学报, 2015, 5(2): 114-120. Sui Z N, Zhi E Q, Yao J, et al. Characterization of DOM composition and origin using three-dimensional fluorescence spectroscopy coupled with region integration method in Qixing Wetland[J]. Journal of Environmental Engineering Technology, 2015, 5(2): 114-120. |
| [25] | Senesi N. Molecular and quantitative aspects of the chemistry of fulvic acid and its interactions with metal ions and organic chemicals:Part Ⅱ. The fluorescence spectroscopy approach[J]. Analytica Chimica Acta, 1990, 232: 77-106. |
| [26] | Wu F C, Tanoue E. Isolation and partial characterization of dissolved copper-complexing ligands in streamwaters[J]. Environmental Science & Technology, 2001, 35(18): 3646-3652. |
| [27] |
傅平青, 刘丛强, 吴丰昌. 溶解有机质的三维荧光光谱特征研究[J]. 光谱学与光谱分析, 2005, 25(12): 2024-2028. Fu P Q, Liu C Q, Wu F C. Three-dimensional excitation emission matrix fluorescence spectroscopic characterization of dissolved organic matter[J]. Spectroscopy and Spectral Analysis, 2005, 25(12): 2024-2028. DOI:10.3321/j.issn:1000-0593.2005.12.031 |
| [28] | Yao X, Zhang Y L, Zhu G W, et al. Resolving the variability of CDOM fluorescence to differentiate the sources and fate of DOM in Lake Taihu and its tributaries[J]. Chemosphere, 2011, 82(2): 145-155. DOI:10.1016/j.chemosphere.2010.10.049 |
| [29] | Stedmon C A, Bro R. Characterizing dissolved organic matter fluorescence with parallel factor analysis:a tutorial[J]. Limnology and Oceanography:Methods, 2008, 6(11): 572-579. DOI:10.4319/lom.2008.6.572 |
| [30] | Coble P G, Del Castillo C E, Avril B. Distribution and optical properties of CDOM in the Arabian Sea during the 1995 Southwest Monsoon[J]. Deep Sea Research Part Ⅱ:Topical Studies in Oceanography, 1998, 45(10-11): 2195-2223. DOI:10.1016/S0967-0645(98)00068-X |
| [31] |
徐亚岩, 宋金明, 李学刚, 等. 渤海湾表层沉积物各形态重金属的分布特征与生态风险评价[J]. 环境科学, 2012, 33(3): 732-740. Xu Y Y, Song J M, Li X G, et al. Variation characteristics and potential ecological risk assessment of heavy metals in the surface sediments of Bohai Bay[J]. Environmental Science, 2012, 33(3): 732-740. |
| [32] |
刘志杰, 李培英, 张晓龙, 等. 黄河三角洲滨海湿地表层沉积物重金属区域分布及生态风险评价[J]. 环境科学, 2012, 33(4): 1182-1188. Liu Z J, Li P Y, Zhang X L, et al. Regional distribution and ecological risk evaluation of heavy metals in surface sediments from coastal wetlands of the Yellow River Delta[J]. Environmental Science, 2012, 33(4): 1182-1188. |
| [33] | Bai J H, Huang L B, Yan D H, et al. Contamination characteristics of heavy metals in wetland soils along a tidal ditch of the Yellow River Estuary, China[J]. Stochastic Environmental Research and Risk Assessment, 2011, 25(5): 671-676. DOI:10.1007/s00477-011-0475-7 |
| [34] |
吴斌, 宋金明, 李学刚. 黄河口表层沉积物中重金属的环境地球化学特征[J]. 环境科学, 2013, 34(4): 1324-1332. Wu B, Song J M, Li X G. Environmental characteristics of heavy metals in surface sediments from the Huanghe estuary[J]. Environmental Science, 2013, 34(4): 1324-1332. |
| [35] | Pernet-Coudrier B, Clouzot L, Varrault G, et al. Dissolved organic matter from treated effluent of a major wastewater treatment plant:characterization and influence on copper toxicity[J]. Chemosphere, 2008, 73(4): 593-599. DOI:10.1016/j.chemosphere.2008.05.064 |
| [36] | Croue J P, Benedetti M F, Violleau D, et al. Characterization and copper binding of humic and nonhumic organic matter isolated from the South Platte River:evidence for the presence of nitrogenous binding site[J]. Environmental Science & Technology, 2003, 37(2): 328-336. |
| [37] | 傅平青. 水环境中的溶解有机质及其与金属离子的相互作用——荧光光谱学研究[D]. 贵阳: 中国科学院研究生院(地球化学研究所), 2004. |
| [38] | 施俊. 基于三维荧光光谱的污水处理厂水质快速分析[D]. 扬州: 扬州大学, 2011. |
 2018, Vol. 39
2018, Vol. 39


