对于采用活性污泥法处理工艺的城市污水处理厂, 污泥膨胀和生物泡沫是运行管理过程中普遍存在的主要难题之一, 特别是容易在强化营养物去除的污水处理工艺中发生[1], 而90%以上的活性污泥膨胀都是由丝状菌过度繁殖引起的[2~4].活性污泥法通过特定的功能微生物来完成有机物降解、生物硝化与反硝化、生物除磷等工艺过程, 这意味着微生物的菌群结构和数量分布在很大程度上决定或影响着污水处理厂的污染物去除能力及处理效果[5, 6].以往对引起污泥膨胀的丝状菌类型的鉴定和不同环境条件下活性污泥微生物菌群的解析已有大量的研究[7~10], 但是针对城市污水处理系统中丝状菌污泥膨胀对脱氮除磷功能菌群影响的研究还较少.因此, 研究引起活性污泥膨胀和生物泡沫的丝状菌类型, 从微生物生态学的角度探究脱氮除磷功能菌群分布的变化特征, 对把控城市污水处理厂污泥膨胀时期污水处理效果具有重要的指导意义.
本文基于传统形态学观察和MiSeq高通量测序技术对5座城市污水处理厂引发活性污泥膨胀和生物泡沫的丝状菌类型进行鉴定, 解析非膨胀期污泥、膨胀期污泥和生物泡沫中的脱氮除磷功能微生物群落结构的动态变化规律, 掌握其对污泥膨胀的影响机制, 通过控制污泥膨胀和生物泡沫的发生, 以期为提高城市污水生物除磷脱氮系统的实际效能及运行稳定性提供理论依据.
1 材料与方法 1.1 样品采集调研选取近年来频繁发生污泥膨胀和生物泡沫的5座城市污水处理厂, 污泥膨胀和泡沫的发生期均为冬春低温季节.一般情况下, 将SVI>150 mL·g-1的活性污泥定义为污泥膨胀[11], 因此, SVI均值大于150 mL·g-1时划分为膨胀期, SVI均值小于100 mL·g-1时划分为非膨胀期.本文取非膨胀期和膨胀期污泥进行对比研究, 污泥样品取自各厂生物反应池好氧区末端.膨胀期各厂生物池表面均有不同程度的生物泡沫漂浮, 泡沫样品直接取膨胀期生物池表面漂浮的泡沫进行测试.各厂的污水处理工艺、水质和污泥膨胀参数概况汇总于表 1.
|
|
表 1 5座城市污水处理厂运行概况 Table 1 Performance of and conditions in five municipal wastewater treatment plants |
1.2 实验方法 1.2.1 污泥和泡沫样品染色与镜检方法
将活性污泥或泡沫混合均匀, 取约50 μL样品, 滴放在洁净的载玻片中央并晾干, 经革兰氏染色后, 置于相差显微镜下进行样品观察, 对丝状菌的种类和丰度等进行评价.
1.2.2 DNA提取与高通量测序DNA提取采用土壤DNA提取方法, 高通量测序通过Illumina MiSeq 2000体系完成, 后续通过OTU聚类分析和物种分类学分析, 并进行群落结构和系统发育等深入的统计学数据分析.
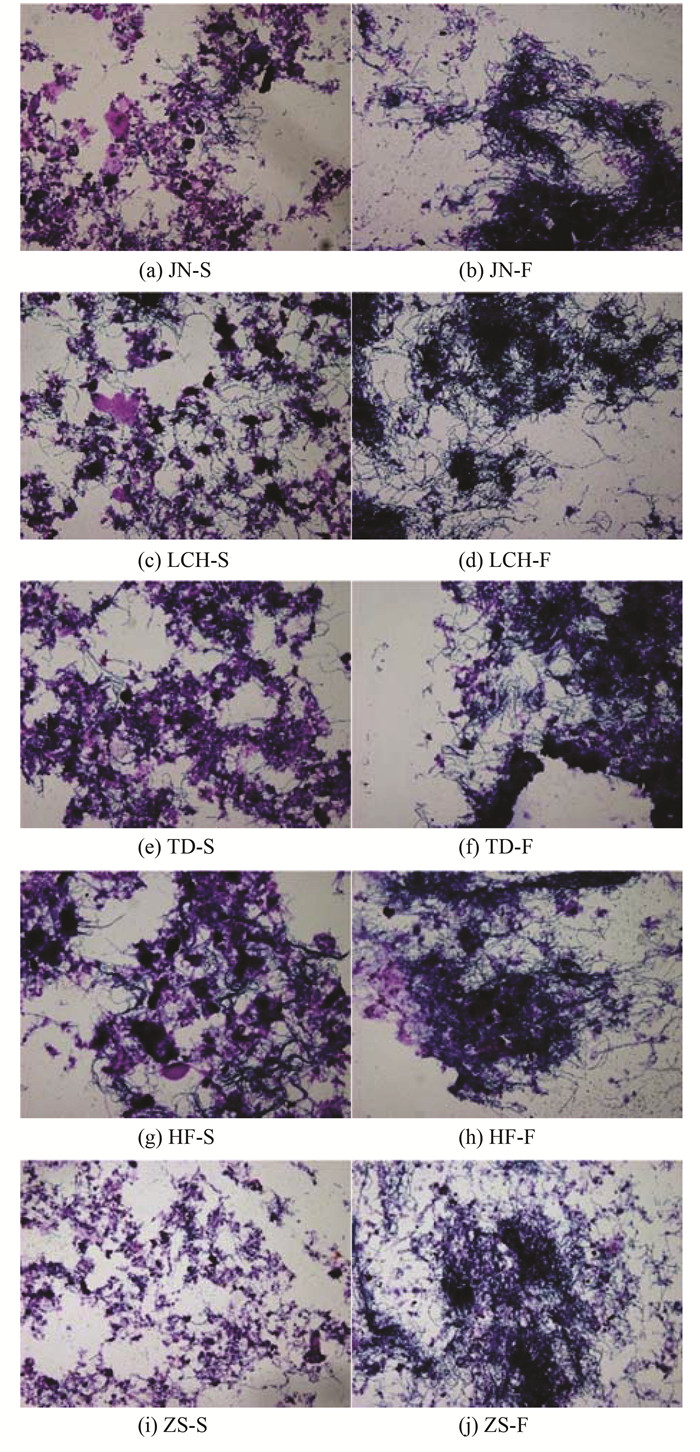
2 结果与讨论 2.1 优势丝状菌的形态学鉴定各厂膨胀期污泥和泡沫中丝状菌类型的形态学鉴定结果如图 1和表 2.膨胀期污泥和泡沫中的丝状菌种类丰富, 共存在不少于8种类型丝状菌; 优势丝状菌主要以微丝菌(M. parvicella)为主, 仅ZS厂的活性污泥中优势丝状菌为Type 0092, 但其与次优丝状菌微丝菌相比数量优势并不明显, 该厂泡沫中仍以微丝菌为主, 由于镜检观察难以对微生物进行严格的量化比较, 因此, 本文2.2节将通过分子生物学手段对各厂优势丝状菌的种类和丰度做进一步验证.除JN厂外, 其他厂均有少量的Type 0092丝状菌, Type 0041在样品中也有一定比例的存在.研究表明, 在许多国家的污水处理厂中微丝菌都是引发污泥膨胀和泡沫的主要菌种之一, 尤其在好氧/厌氧区交替的系统中较活性污泥中其他细菌具有更强的竞争优势[12], 目前大多数污水处理厂为达到脱氮除磷目的, 均采用AAO或厌氧池+氧化沟等厌氧区置于好氧区之前的处理工艺, 这也是导致微丝菌成为优势菌的重要原因, 另外微丝菌受温度和污泥负荷等条件的影响明显, 通常在冬季低温季节和低负荷[ < 0.1 kg·(kg·d)-1, 以BOD5/MLSS计]条件下具有比菌胶团细菌更强的繁殖优势[13, 14].
|
图片字母表示水厂名称-样品类型 样品类型:S代表膨胀期污泥, F代表生物泡沫 图 1 膨胀期污泥和泡沫样品镜检(100×) Fig. 1 Micrographs of activated sludge and foam during bulking period(100×) |
|
|
表 2 丝状菌类型和丰度统计(镜检) Table 2 Types and abundance of filamentous bacteria(microscope) |
借助美国Jenkins等提出的丝状菌丰度表和图判断污泥和泡沫中丝状菌丰度, 结果表明, 各厂泡沫中丝状菌丰度明显高于污泥.其中LCH厂泡沫、TD厂污泥和泡沫、HF厂泡沫中丝状菌均处于过度繁殖状态, 几乎所有的絮体都能观察到丝状菌, 其数量大于菌胶团的数量, 丰度值为最大值6.结合镜检鉴定和各厂SVI值情况, LCH、TD、HF厂污泥膨胀相对严重, JN和ZS厂处于轻微膨胀状态.
2.2 优势丝状菌分子生物学鉴定各厂活性污泥和泡沫中常见丝状菌的MiSeq高通量测序结果如表 3.丝状菌相对丰度均呈现出非膨胀期污泥低于膨胀期污泥、低于泡沫的规律趋势.非膨胀期污泥的优势丝状菌类型多样, 且5座厂之间各不相同, 而膨胀期污泥和泡沫的优势丝状菌均为微丝菌, 说明在非膨胀期丝状菌作为菌胶团细菌的骨架结构, 其在活性污泥总细菌中并不占优势, 各类型丝状菌数量相差不明显; 由于某种环境因素导致丝状菌大量增值时, 其占总细菌的质量分数增加, 破坏了活性污泥菌群结构的平衡, 导致活性污泥沉降性能变差, 引发污泥膨胀和生物泡沫. ZS厂优势丝状菌的MiSeq测序结果与镜检结果有所差异, 由于MiSeq测序可对微生物的丰度进行量化, 且更加客观可靠[15], 因此, 优势丝状菌类型以MiSeq测序结果为准.
|
|
表 3 常见丝状菌相对丰度(MiSeq) Table 3 Relative abundance of common filamentous bacteria (MiSeq) |
从丝状菌的归属来看, M. parvicella、N. limicola Ⅰ、Gordonia、Skermania、Nocardioides均属于放线菌门[16, 17].各厂丝状菌的相对丰度排序为TD、HF、LCH、JN、ZS, 与镜检丰度值和SVI值的排序基本一致.
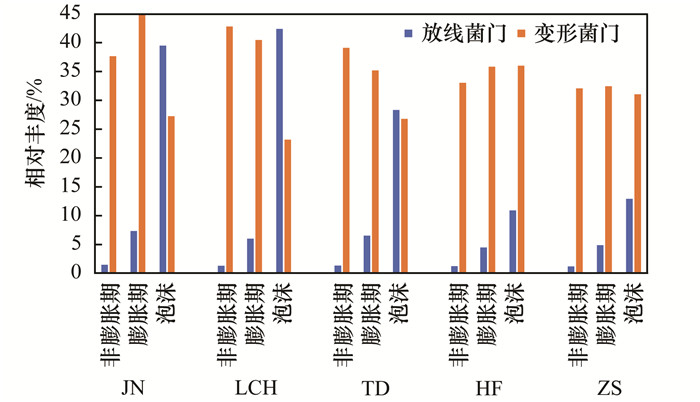
2.3 门、纲水平微生物变化规律考虑到大多数丝状菌属于放线菌门, 而大多数功能菌属于变形菌门[18].各厂不同时期变形菌门和放线菌门的相对丰度对比结果如图 2, 由非膨胀期转变到膨胀期, 活性污泥中放线菌门微生物数量显著增加, 且泡沫中放线菌数量明显高于污泥, 与镜检对丝状菌丰度值的评估结果一致.而变形菌门微生物的数量变化并不明显, 波动幅度低于5%.
|
图 2 不同时期变形菌门和放线菌门的相对丰度 Fig. 2 Relative abundance of Proteobacteria and Actinobacteria during different periods |
各厂不同时期变形菌纲的相对丰度对比结果如图 3, 主要脱氮除磷菌属分布在β-Proteobacter、γ-Proteobacter、α-Proteobacter、δ-Proteobacter.其中β-Proteobacter仍为不同时期的优势变形菌, TD、HF、ZS、JN厂膨胀期β-Proteobacter相对丰度较非膨胀期略微降低, 变化比例低于5%, 泡沫中各厂β-Proteobacter均大幅度低于非膨胀期. β-Proteobacter是活性污泥在脱氮、除磷和其他许多污染物去除中起重要作用的菌群[19], 其相对丰度在一定程度上决定着污水厂污染物的去除效果. γ-Proteobacter在不同时期的变化趋势不明显. α-Proteobacter在各厂膨胀期污泥中含量均最高, 高于泡沫和非膨胀期污泥, 而α-Proteobacter典型的功能菌常被认为是反硝化细菌[20].各厂非膨胀期的δ-Proteobacter相对丰度高于膨胀期, 高于泡沫, 亚硝酸盐氧化菌中的Nitrospina属于δ-Proteobacter.

|
图 3 不同时期变形菌纲相对丰度 Fig. 3 Relative abundance of Proteobacter during different periods |
从主要功能菌所在的门和纲水平的群落结构变化对污染物去除效果的影响来看, 丝状菌污泥膨胀对主要的功能菌变形菌门和变形菌纲微生物的丰度影响不明显, 而各厂膨胀期主要污染物的去除效果较非膨胀期略有降低, 但波动幅度不大, 均在出水达标范围内.
2.4 脱氮功能菌群变化规律对不同时期氨氧化菌(AOB)、亚硝酸盐氧化菌(NOB)、反硝化菌的种属和分布比例变化情况进行对比分析.
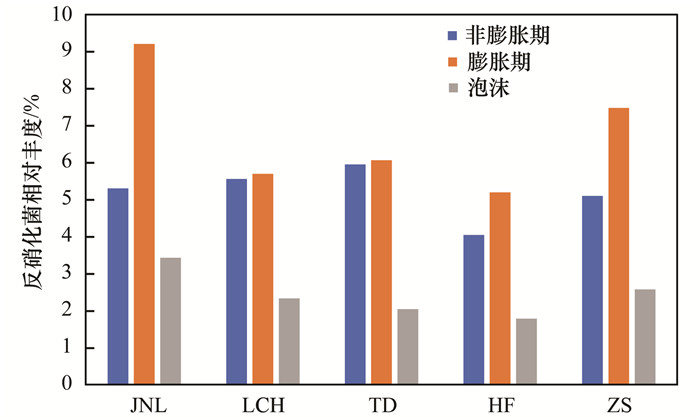
脱氮菌属相对丰度统计结果如表 4, 各厂的AOB包括亚硝化单胞菌属(Nitrosomonas)和亚硝化球菌属(Nitrosococcus), 优势菌属为亚硝化单胞菌.非膨胀期污泥、膨胀期污泥和泡沫中AOB相对丰度范围分别为1.71%~5.21%、0.50%~2.57%、0.34%~1.64%.各厂的NOB包括硝化刺菌属(Nitrospina)和硝化螺菌属(Nitrospira)两种, 优势菌属为硝化螺菌.非膨胀期污泥、膨胀期污泥和泡沫中NOB的相对丰度范围分别为1.60%~2.38%、1.44%~2.77%、0.30%~1.23%.各厂反硝化菌包含陶厄氏菌属(Thauera)、生丝微菌属(Hyphomicrobiμm)等12个种属, 其中陶厄氏菌为各厂的优势反硝化菌, 生丝微菌次之.非膨胀期污泥、膨胀期污泥和泡沫中反硝化菌相对丰度范围分别为4.05%~5.96%、2.20%~9.21%、1.79%~3.40%.
|
|
表 4 脱氮菌属相对丰度/% Table 4 Relative abundance range of denitrification removal bacteria/% |
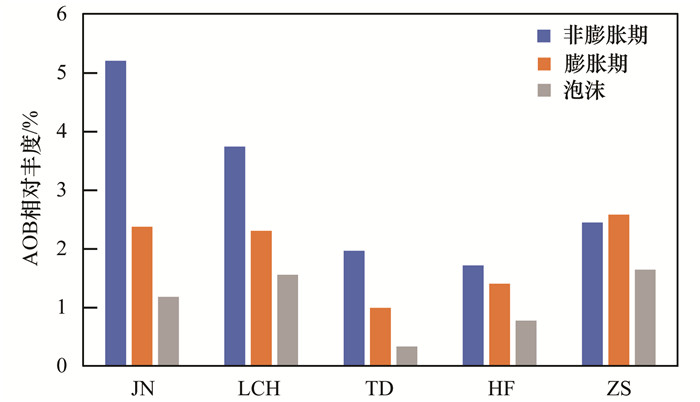
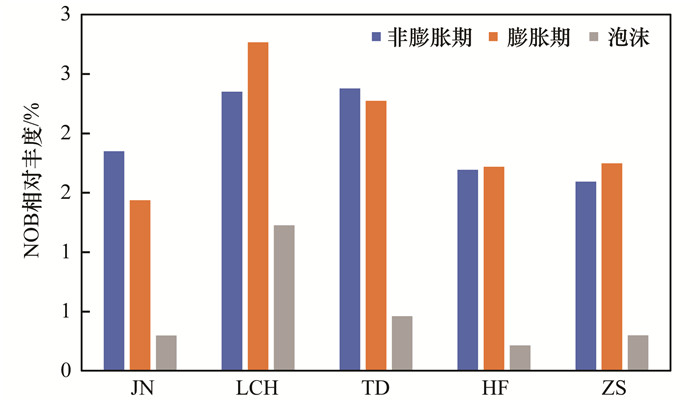
各厂不同时期脱氮菌属的对比情况如图 4~6, AOB相对丰度除ZS厂膨胀期略有升高, 其余各厂均为非膨胀期高于膨胀期, 高于泡沫; 其中JN、TD和LCH厂膨胀期污泥中AOB相对丰度大幅度降低, JN厂降低比例最大, 为54%, 分析JN厂降低幅度较大的原因可能与工艺特征及水温有关.从工艺来看, TD、LCH、ZS厂生物池均有填料, 填料对AOB有较好的固定作用, 降低污泥膨胀对AOB菌群的影响; 从水温来看, 各厂一年中水温最低点均在膨胀期, 但JN厂最低水温为11℃, 其他厂均不低于12℃, 而AOB对水温的耐受力较差[21], 受水温影响而大幅度降低.与AOB相比, NOB受污泥膨胀影响的变化规律并不明显.大体分为两种变化趋势:JN、TD厂NOB的相对丰度膨胀期低于非膨胀期, LCH、HF、ZS厂膨胀期高于非膨胀期.反硝化菌相对丰度在膨胀期普遍高于非膨胀期, 其中JN、ZS厂增加幅度较大, 增加比例分别为73%和47%, 而LCH和TD厂略有增加.各厂泡沫中均有一定比例的脱氮菌属存在.
|
图 4 不同时期AOB相对丰度 Fig. 4 Relative abundance of AOB during different periods |
|
图 5 不同时期NOB相对丰度 Fig. 5 Relative abundance of NOB during different periods |
|
图 6 不同时期反硝化菌相对丰度 Fig. 6 Relative abundance of denitrifying bacterium during different periods |
AOB和NOB都是自养型细菌, 生长缓慢, 对有机负荷、温度、pH、DO等参数的冲击十分敏感, 与异养菌的竞争中处于劣势地位[22].而反硝化菌大多是兼性菌, 其代谢途径丰富多样, 只要环境条件适宜, 反硝化过程就能顺利进行[23].因此, 在底物竞争和不良环境条件下, 微丝菌为主导的丝状菌较菌胶团细菌有绝对优势而大量增殖, AOB和NOB的相对丰度因竞争不利而降低, 反硝化菌因自身的适应能力较强而几乎不受影响.
膨胀期各厂TN和氨氮的去除率较非膨胀期有所降低, 波动幅度在5%左右.城市污水处理厂属于较为复杂的系统, 脱氮菌的功能作用受制于多种环境因素的影响, 膨胀期AOB相对丰度的降低对氨氮的去除率有一定影响, 反硝化菌相对丰度的增加对TN去除效果的影响并不直观, 主要由于反硝化作用还受碳源以及运行管理等因素的影响, 因此, TN在膨胀期的去除率有所降低.
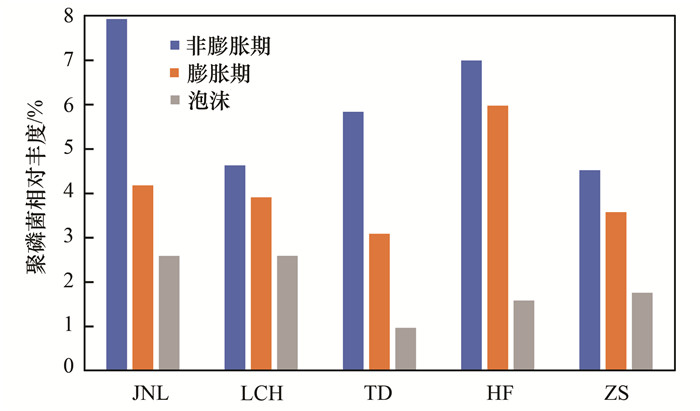
2.5 除磷功能菌群变化规律聚磷菌相对丰度统计结果如表 5和图 7.其中Candidatus Accumulibacter phosphatis相对丰度分布在0.86%~7.71%, 部分厂Dechloromonas菌属的相对丰度超过1%, Tetrasphaera菌属的相对丰度基本都在1%以下, 而Tetrasphaera等菌属在活性污泥中占有较大比例(18%~30%)时, 才被认为是在除磷过程中起主要作用的聚磷菌[24].因此, 各厂优势聚磷菌为Candidatus Accumulibacter phosphatis.非膨胀期污泥、膨胀期污泥和泡沫中PAO相对丰度范围分别为4.63%~7.93%、2.24%~3.91%和0.97%~2.59%.研究表明, 采用定量PCR和FISH等方法检测运行良好的污水处理系统活性污泥中Candidatus Accumulibacter phosphatis时, 其相对丰度一般在4%~24%左右[25, 26], 而本文测试结果中Candidatus Accumulibacter phosphatis在非膨胀期污泥中相对丰度均在该范围内, 而在膨胀期污泥中低于范围最低值.
|
|
表 5 除磷菌属相对丰度范围/% Table 5 Relative abundance range of PAO/% |
|
图 7 不同时期聚磷菌相对丰度对比 Fig. 7 Relative abundance of PAO during different periods |
各厂不同时期聚磷菌的相对丰度变化规律比较明显, 总体呈现出非膨胀期高于膨胀期, 高于泡沫.从非膨胀期到膨胀期, 降低比例范围为15%~47%, 其中JN和TD厂的变化幅度较大, HF厂的变化幅度最小, 推测可能是由于该厂在氧化沟工艺之前设有厌氧池, 对聚磷菌有一定的富集强化作用, 使其在应对污泥膨胀时受到的影响相对较小. Wang等[27]在研究污泥膨胀对城市污水处理系统微生物群落结构影响的研究中也发现Candidatus Accumulibacter phosphatis相对丰度在膨胀期大幅度降低.膨胀期总磷去除率的降低与聚磷菌数量的减少有一定关系, 但影响并不明显, 总磷去除率的波动幅度在3%以内.
3 结论(1) 结合形态学观察和MiSeq高通量测序得知5座城市污水处理厂发生的污泥膨胀均由丝状菌引起, 主要类型为微丝菌(Microthrix parvicella).
(2) 5座城市污水处理厂脱氮除磷优势菌属基本一致, 其中硝化细菌为亚硝化单胞菌(Nitrosomonas)和硝化螺菌(Nitrospira), 反硝化菌为陶厄氏菌(Thauera), 除磷菌为Candidatus Accumulibacter phosphatis.
(3) 不同厂脱氮除磷功能菌受污泥膨胀的影响程度不同, 主要是处理工艺和水温的差异所致.
| [1] | Jenkins D, Richard M G, Daigger G T. Manual on the causes and control of activated sludge bulking, foaming and other solids separation problems[M]. London UK: IWA Publishing, 2004. |
| [2] | Guo F, Zhang T. Profiling bulking and foaming bacteria in activated sludge by high throughput sequencing[J]. Water Research, 2012, 46(8): 2772-2782. DOI:10.1016/j.watres.2012.02.039 |
| [3] | Martins A M P, Pagilla K, Heijnen J J, et al. Filamentous bulking sludge-a critical review[J]. Water Research, 2004, 38(4): 793-817. DOI:10.1016/j.watres.2003.11.005 |
| [4] | 彭永臻, 郭建华. 活性污泥膨胀机理、成因及控制[M]. 北京: 科学出版社, 2012. |
| [5] |
曾薇, 张丽敏, 王安其, 等. 污水处理系统中硝化菌的菌群结构和动态变化[J]. 中国环境科学, 2015, 35(11): 3257-3265. Zeng W, Zhang L M, Wang A Q, et al. Community structures and population dynamics of nitrifying bacteria in activated sludges of wastewater treatment plants[J]. China Environmental Science, 2015, 35(11): 3257-3265. DOI:10.3969/j.issn.1000-6923.2015.11.008 |
| [6] | Gentile M E, Jessup C M, Nyman J L, et al. Correlation of functional instability and community dynamics in denitrifying dispersed-growth reactors[J]. Applied and Environmental Microbiology, 2007, 73(3): 680-690. DOI:10.1128/AEM.01519-06 |
| [7] |
陈燕, 刘国华, 范强, 等. 不同溶解氧条件下A/O系统的除碳脱氮效果和细菌群落结构变化[J]. 环境科学, 2015, 36(7): 2610-2616. Chen Y, Liu G H, Fan Q, et al. Carbon/nitrogen removal and bacterial community structure change in an A/O activated sludge system under different dissolved oxygen conditions[J]. Environmental Science, 2015, 36(7): 2610-2616. |
| [8] |
张著, 高大文, 袁向娟, 等. 营养物质缺乏引起的好氧颗粒污泥膨胀及其恢复[J]. 环境科学, 2012, 33(9): 3197-3201. Zhang Z, Gao D W, Yuan X J, et al. Aerobic granular sludge bulking due to the lack of nutrient and its recovery[J]. Environmental Science, 2012, 33(9): 3197-3201. |
| [9] |
高莎, 金德才, 赵志瑞, 等. A2O工艺活性污泥中可培养丝状细菌的多样性[J]. 环境科学, 2013, 34(7): 2912-2917. Gao S, Jin D C, Zhao Z R, et al. Diversity of culturable filamentous bacteria in the activated sludge from A2O wastewater treatment process[J]. Environmental Science, 2013, 34(7): 2912-2917. |
| [10] |
端正花, 潘留明, 陈晓欧, 等. 低温下活性污泥膨胀的微生物群落结构研究[J]. 环境科学, 2016, 37(3): 1070-1074. Duan Z H, Pan L M, Chen X O, et al. Changes of microbial community structure in activated sludge bulking at low temperature[J]. Environmental Science, 2016, 37(3): 1070-1074. |
| [11] | Palm J C, Jenkins D, Parker D S. Relationship between organic loading, dissolved oxygen concentration and sludge settleability in the completely-mixed activated sludge process[J]. Journal (Water Pollution Control Federation), 1980, 52(10): 2484-2506. |
| [12] | Nielsen P H, Roslev P, Dueholm T E, et al. Microthrix parvicella, a specialized lipid consumer in anaerobic-aerobic activated sludge plants[J]. Water Science and Technology, 2002, 46(1-2): 73-80. DOI:10.2166/wst.2002.0459 |
| [13] | Knoop S, Kunst S. Influence of temperature and sludge loading on activated sludge settling, especially on Microthrix parvicella[J]. Water Science and Technology, 1998, 37(4-5): 27-35. DOI:10.2166/wst.1998.0573 |
| [14] |
陈滢, 彭永臻, 刘敏, 等. 营养物质对污泥沉降性能的影响及污泥膨胀的控制[J]. 环境科学, 2004, 25(6): 54-58. Chen Y, Peng Y Z, Liu M, et al. Effect of nutrient on sludge settling property and bulking controls[J]. Environmental Science, 2004, 25(6): 54-58. |
| [15] | Ye L, Shao M F, Zhang T, et al. Analysis of the bacterial community in a laboratory-scale nitrification reactor and a wastewater treatment plant by 454-pyrosequencing[J]. Water Research, 2011, 45(15): 4390-4398. DOI:10.1016/j.watres.2011.05.028 |
| [16] | Levantesi C, Rossetti S, Thelen K, et al. Phylogeny, physiology and distribution of 'Candidatus Microthrix calida', a new Microthrix species isolated from industrial activated sludge wastewater treatment plants[J]. Environmental Microbiology, 2006, 8(9): 1552-1563. DOI:10.1111/emi.2006.8.issue-9 |
| [17] | Wang P, Yu Z S, Qi R, et al. Detailed comparison of bacterial communities during seasonal sludge bulking in a municipal wastewater treatment plant[J]. Water Research, 2016, 105: 157-166. DOI:10.1016/j.watres.2016.08.050 |
| [18] | Wagner M, Alexander L, Regina N, et al. Bacterial community composition and function in sewage treatment systems[J]. Current Opinion in Biotechnology, 2002, 13(3): 218-227. DOI:10.1016/S0958-1669(02)00315-4 |
| [19] | Oehmen A, Lemos P C, Carvalho G, et al. Advances in enhanced biological phosphorus removal:from micro to macro scale[J]. Water Research, 2007, 41(11): 2271-2300. DOI:10.1016/j.watres.2007.02.030 |
| [20] | Nielsen P H, Mielczarek A T, Kragelund C, et al. A conceptual ecosystem model of microbial communities in enhanced biological phosphorus removal plants[J]. Water Research, 2010, 44(17): 5070-5088. DOI:10.1016/j.watres.2010.07.036 |
| [21] | Hallin S, Lydmark P, Kokalj S, et al. Community survey of ammonia-oxidizing bacteria in full-scale activated sludge processes with different solids retention time[J]. Journal of Applied Microbiology, 2005, 99(3): 629-640. DOI:10.1111/jam.2005.99.issue-3 |
| [22] | Siripong S, Rittmann B E. Diversity study of nitrifying bacteria in full-scale municipal wastewater treatment plants[J]. Water Research, 2007, 41(5): 1110-1120. DOI:10.1016/j.watres.2006.11.050 |
| [23] | Satoh H, Yamakawa T, Kindaichi T, et al. Community structures and activities of nitrifying and denitrifying bacteria in industrial wastewater-treating biofilms[J]. Biotechnology and Bioengineering, 2006, 94(4): 762-772. DOI:10.1002/(ISSN)1097-0290 |
| [24] | Nguyen H T T, Le V Q, Hansen A A, et al. High diversity and abundance of putative polyphosphate-accumulating Tetrasphaera-related bacteria in activated sludge systems[J]. FEMS Microbiology Ecology, 2011, 76(2): 256-267. DOI:10.1111/fem.2011.76.issue-2 |
| [25] | Fukushima T, Uda N, Onuki M, et al. Development of the quantitative PCR method for Candidatus 'Accumulibacter phosphatis' and its application to activated sludge[J]. Journal of Water and Environment Technology, 2007, 5(1): 37-43. DOI:10.2965/jwet.2007.37 |
| [26] | He S M, Gall D L, McMahon K D. "Candidatus Accumulibacter" population structure in enhanced biological phosphorus removal sludges as revealed by polyphosphate kinase genes[J]. Applied and Environmental Microbiology, 2007, 73(18): 5865-5874. DOI:10.1128/AEM.01207-07 |
| [27] | Wang J, Qi R, Liu M M, et al. The potential role of 'Candidatus Microthrix parvicella' in phosphorus removal during sludge bulking in two full-scale enhanced biological phosphorus removal plants[J]. Water Science & Technology, 2014, 70(2): 367-375. |
 2018, Vol. 39
2018, Vol. 39

