2. 流域水资源与生态环境科学湖北省重点实验室, 武汉 430010
2. Key Laboratory of Basin Water Resource and Eco-environmental Science in Hubei Province, Wuhan 430010, China
持久性有机污染物(persistent organic pollutants, POPs)理化性质稳定, 难以降解, 能长期存在于水、沉积物等各种环境介质中, 毒性强且能长距离迁移, 对人类健康会造成严重危害.多环芳烃(PAHs)和邻苯二甲酸酯类(PAEs)是两类典型的POPs. PAHs具有致癌、致畸、致突变的“三致”毒性[1, 2], 美国联邦环保署将16种不带支链的PAHs列入优先控制污染物[3], 其主要来源于含碳物质的不完全燃烧[4]. PAEs作为增塑剂被广泛使用[5], 属于内分泌干扰物[6, 7].
长江武汉段是长江干流上人口最为密集和最重要城市江段之一, 是武汉地区工农业生产和人民生活用水的主要水源地, 其水质直接影响着工业循环水系统的安全运行, 更为重要的是影响着农产品和饮用水安全.长江武汉段PAHs和PAEs污染的相关文献报道主要集中在2011年前. 2005年调查表明长江武汉段干流水相和沉积物中∑PAHs浓度分别为322~6 235 ng·L-1和303~3 995 ng·g-1, PAHs污染主要来源于燃烧源[8, 9]; ∑PAEs浓度分别为34~456 ng·L-1和151 700~450 000 ng·g-1, 长江武汉段PAEs污染处于中等偏上水平[10]. 2011年有研究报道长江武汉段水体DBP和DEHP浓度范围分别为1 308~1 749 ng·L-1(均值1 383 ng·L-1)、1 371~1 536 ng·L-1(均值1 437 ng·L-1), 主要来源于废弃塑料制品等[11].相关研究也表明DBP和DEHP在我国地表水中被普遍检出, 且检出浓度较高[12~13].已有研究仅报道了长江武汉段单独PAHs或PAEs浓度分布、污染水平等, 但缺乏对长江武汉段水体及沉积物两类典型POPs(PAEs和PAHs)污染特征、来源的系统分析研究.
长江两岸密布重化工企业, 各类危、重污染源生产储运集中区与主要饮用水水源交替配置, 生态环境保护形势严峻.国务院印发《关于依托黄金水道推动长江经济带发展的指导意见》, 强调长江经济带生态环境保护工作的重要性. 《长江经济带生态环境保护规划》指出“目前长江经济带污染物排放量大, 风险隐患多, 饮用水安全保障压力大”.但现阶段关于长江经济带核心区域(武汉段)在不同环境介质中POPs研究工作却鲜有报道, 因此无法系统评价长江武汉段POPs污染状况, 不利于长江经济带生态环境评价及保护工作.
相关报道指出PAHs主要是燃烧源及石油源等[14~16], PAEs的主要来源于塑料和重化工工业, 及生活垃圾等[14, 17, 18]; 总体而言, 两类典型POPs主要来源于燃烧过程环境残留、大气的长距离传输及地表径流污染等, 一旦降雨, 有机污染物易随雨水汇入江河, 导致其含量较高.因此, 本文系统分析丰水期两类典型POPs(PAHs和PAEs)在水相、沉积相中的浓度, 揭示现阶段长江武汉段干流丰水期PAHs和PAEs污染特征, 探讨其主要来源, 并开展污染水平分析和污染风险评估, 以期为长江经济带核心区域(武汉段)PAHs和PAEs有效控制提供基础数据和技术支撑.
1 材料与方法 1.1 化学品与试剂16种PAHs混合标准溶液(AccuStandard, 99%), 包括萘(Naphthalene, Nap)、苊(Acenaphthene, Ace)、二氢苊(Acenaphthylene, Acy)、芴(Fluorene, Flu)、菲(Phenanthrene, Phe)、蒽(Anthracene, Ant)、荧蒽(Fluoranthene, Fla)、芘(Pyrene, Pyr)、苯并[a]蒽(Benzo[a]anthracene, BaA)、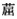
本研究于2016年8月(丰水期)在长江中游典型河段——武汉江段干流布置5个断面, 监测河段总长约57 km, 每个断面左岸、中泓和右岸采集水样和沉积物样品, 共计15个采样点(S1~S15), 如图 1所示.具体采样断面为武汉上游沌口(P1)、汉江汇入口上游(P2)、武汉中游(P3)、倒水河汇入口上游(P4)、武汉下游(P5).
|
图 1 长江武汉段采样点位置示意 Fig. 1 Scheme of sampling sites in the Wuhan section of the Yangtze River(WSYR) |
采用4 L不锈钢小桶采集表层水体(水面下约30 cm), 参考相关研究, 采集后现场过0.22 μm玻璃纤维滤膜, 过滤后水样采用经甲醇活化的固相萃取膜萃取水中的PAHs和PAEs[19, 20], 最后用锡箔纸将固相萃取膜片包裹, 冷藏保存.沉积物样品采用抓斗式采泥器采集, 采集后保存于玻璃培养皿中.
1.3 样品分析 1.3.1 有机前处理过程水样:固相萃取膜带回实验室后, 将10 mL乙酸乙酯加入到萃取膜上, 让洗脱剂与萃取膜接触一段时间(约3 min), 然后短时间开启真空泵, 让洗脱剂缓慢通过固相萃取装置流入接受瓶; 再次加入10 mL乙酸乙酯重复上述步骤; 然后加入10 mL(1+1)二氯甲烷-乙酸乙酯洗脱剂, 重复该步骤2次.将洗脱液用无水硫酸钠除水后浓缩定容, 上机分析.
沉积物:沉积物样品经真空冷冻干燥除水, 过100目筛, 称取约2 g左右(精确到0.000 1 g)加入(1+1)己烷-丙酮混合溶剂, 采用微波萃取(起始温度30℃, 以10℃·min-1速度升温至120℃, 保持20 min), 将萃取液通过硅胶-氧化铝复合柱, 并分别用正己烷、正己烷与二氯甲烷混合溶剂(体积比7:3)洗脱3次.将洗脱液用无水硫酸钠除水后浓缩定容, 上机分析.
1.3.2 气相质谱条件气相色谱条件:HP-5MS色谱柱(30 m×0.25 mm×0.25 μm); 传输线温度280℃; 载气:高纯氦气(≥99.999%), 柱流量:1.2 mL·min-1(恒流模式); 进样模式:不分流进样; 进样体积1 μL; 溶剂延迟4 min.
质谱条件:EI模式, 能量70 eV, 离子源温度230℃; 四级杆温度150℃; 扫描方式:SIM.
PAHs检测升温程序:70℃保持1 min, 以30℃·min-1升至220℃, 保持1min, 再以3℃·min-1升温至280℃, 保持6 min, 分析时间为33 min; 进样口温度:250℃.
PAEs检测升温程序:70℃保持0.5 min, 以25℃·min-1升至190℃, 保持1min, 再以5℃·min-1升温至230℃, 保持0min, 最后以10℃·min-1升温至280℃, 保持8 min, 分析时间为27.3 min; 进样口温度:280℃.
1.3.3 质量控制和质量保证样品分析过程中参考《水环境监测规范》(SL-2013)中QA/QC要求.采用混合标准外标法定量分析样品中PAHs和PAEs, 16种PAHs和6种PAEs标准曲线的相关系数均达到0.99以上.水样16种PAHs的方法检出限范围为0.04~0.39 ng·L-1, 6种PAEs的方法检出限范围为0.12~0.92 ng·L-1; 沉积物中16中PAHs的方法检出限范围为0.08~0.78 ng·g-1, 6种PAEs的方法检出限范围为0.25~1.85 ng·g-1.样品进样后采用Agilent 7890B/5977A气质联用仪的Mass Hunter数据分析软件对16种PAHs和6种PAEs进行定量分析.为避免分析过程中引起的污染, 每分析10个样品时, 做一个样品空白, 分析值为扣减空白后的数值, 小于检出限的数据按未检出计算.
1.3.4 数据分析利用IBM SPSS Statistics 22软件, 采用主成分分析法(PCA)研究长江武汉段水体和沉积物中PAHs和PAEs的来源.
2 结果与讨论 2.1 污染特征 2.1.1 PAHs含量及分布表 1显示了2016年长江武汉段丰水期水体和沉积物中∑PAHs浓度的最小值、最大值、平均值、中位值和标准偏差.水体中16种PAHs, BaA、Chr、BbF、BkF、BaP、InP、DahA、BghiP未检出, 其他全部检出; 沉积物中16种PAHs, BbF、BkF、BaP、InP、DahA、BghiP未检出, 其余全部检出.水体中∑PAHs浓度范围为20.8~90.4 ng·L-1(均值40.7 ng·L-1), 浓度远低于文献报道的2005年长江武汉段干流水体浓度322~6 235 ng·L-1(均值2 095 ng·L-1)[9], 表明长江武汉段水体中∑PAHs浓度比历史监测浓度低.沉积物中∑PAHs含量范围为46.1~424.0 ng·g-1(均值191.8 ng·g-1), 浓度均值远低于2005年长江武汉段沉积物中∑PAHs浓度范围303~3 995 ng·g-1(均值2 032 ng·g-1)[9], 略高于长江口2010~2011年的浓度范围128.5~307.8 ng·g-1[4].可能的原因是本次调查采样断面参考水文断面布设(左右采样点距离岸边约100 m), 与已有报道的2005年采样断面位置不一致, 同时采样点受水文泥沙条件变化等因素的影响, 因此与历史监测浓度差别较大.
|
|
表 1 长江武汉段水体及沉积物中PAHs含量 Table 1 PAHs concentration in water and sediment from WSYR |
图 2显示了水体和沉积物中PAHs单体的浓度情况, 其中Flu为干流水体中均值最高的PAHs单体, Ant为干流沉积物中均值最高的PAHs单体. 16种PAHs可根据含有的苯环数量被划分为2~3环、4环和5~6环, 分别代表低分子、中分子和高分子量的PAHs[21].丰水期长江武汉段干流水体和沉积物主要的PAHs单体是2~3环和4环, 与前期研究结果相似[9], 水体以3环芳烃为主, 其次是4环和2环, 占PAHs总浓度的比例分别为43.03%~92.96%(均值76.98%)、2.97%~55.59%(均值18.42%)、1.38%~8.17%(均值4.60%); 沉积物以3环芳烃为主, 其次是4环和2环, 占PAHs总浓度的比例分别为51.53%~90.08%(均值75.80%)、4.86~45.83%(均值18.46%)、2.51~14.15%(均值5.74%).一般认为由于中、高分子量的PAHs疏水性更强, 更易于赋存于沉积物中, 导致沉积物中PAHs以中、高分子量的PAHs为主, 本研究沉积物中高分子量的PAHs(5~6环)未检出, 相关规律未体现.

|
图 2 长江武汉段8月PAHs单体浓度 Fig. 2 Concentration of PAHs monomers from WSYR in August |
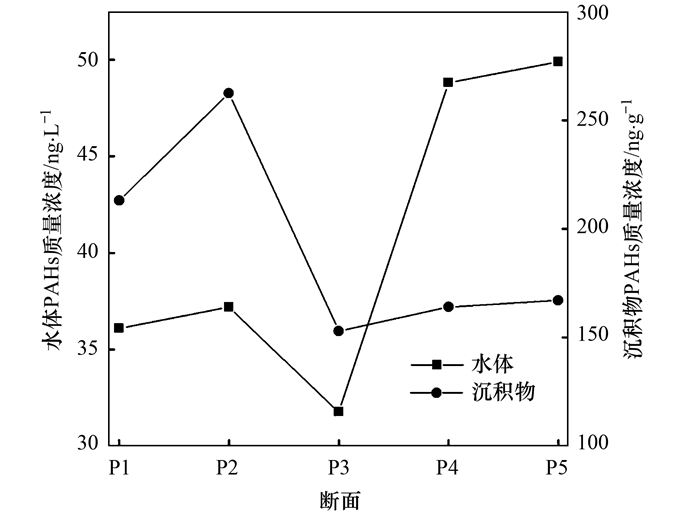
世界卫生组织拟定的饮用水中6种特定PAHs(Fla、BbF、BkF、BaP、BghiP、InP)仅有Fla被检出, 浓度范围是0.3~27.1 ng·L-1(均值4.7 ng·L-1), 远小于地表水6种特定PAHs最高可接受水平200 ng·L-1.长江武汉段干流沉积物中PAHs以2~3环和4环为主, Ant为干流沉积物中含量最高的PAHs单体, 其浓度范围是18.7~160.0 ng·g-1(均值81.2 ng·g-1). 图 3为长江中游武汉段水体和沉积物中∑PAHs的沿程分布特征.总体而言, 长江中游武汉段水体中∑PAHs自上游至下游浓度有上升的趋势, 而沉积物中∑PAHs自上游至下游浓度有降低的趋势.
|
图 3 长江武汉段采样断面8月份水体和沉积物中∑PAHs沿程分布 Fig. 3 Distribution of ∑PAHs in water and sediment from WSYR in August |
由表 2显示了2016年长江武汉段丰水期水体和沉积物中∑PAEs浓度的最小值、最大值、平均值、中位值和标准偏差.水体中6种PAEs, 除BBP未检出, 其他全部检出; 沉积物中6种PAEs, 均被全部检出. 15个采样点中均检测到PAEs, 说明PAEs在环境中广泛存在.长江武汉段干流水体中∑PAEs浓度范围为280.9~779.0 ng·L-1(均值538.6 ng·L-1), 高于2005年水体∑PAEs的浓度34~456 ng·L-1(均值257.8 ng·L-1)[22], 低于2004~2005年长江江苏段的浓度178~1 474 ng·L-1(均值902 ng·L-1)[23].沉积物中∑PAEs含量范围为1 346.2~7 641.1 ng·g-1(均值3 699.5 ng·g-1), 显著低于2005年长江武汉段沉积物中∑PAEs含量(151 700~450 000 ng·g-1)[22].
|
|
表 2 长江武汉段水体及沉积物中PAEs含量 Table 2 PAEs concentration in water and sediment from WSYR |
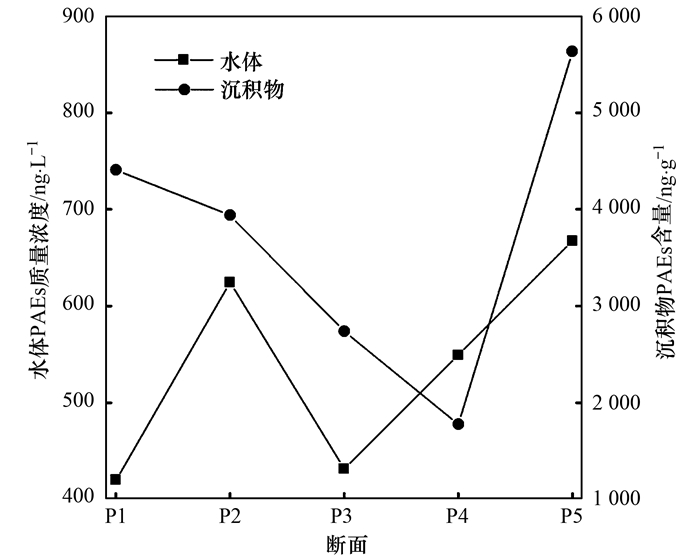
图 4显示了2016年长江武汉段丰水期水体和沉积物中PAEs单体的浓度.水体中DBP和DEHP是主要污染物, 浓度范围分别为143.8~539.5 ng·L-1(均值264.7 ng·L-1)和35.1~347.4 ng·L-1(均值160.7 ng·L-1).沉积物中主要污染物DBP和DEHP的含量范围分别为304.8~4 009.2 ng·g-1(均值1 666.0 ng·g-1)和611.9~3 095.0 ng·g-1(均值1 659.5 ng·g-1).不论是水体还是沉积物, DBP和DEHP均为浓度最高的PAEs类污染物, 与文献报道的2005年长江武汉段研究结果一致[22]. 图 5为长江中游武汉段水体和沉积物中∑PAEs的沿程分布特征.总体而言, 长江中游武汉段水体和沉积物中∑PAEs沿程分布无显著规律, 武汉下游(P5)断面水体和沉积物中∑PAEs较其他监测断面高.

|
图 4 长江武汉段8月份PAEs单体浓度 Fig. 4 Concentration of PAEs monomers from WSYR in August |
|
图 5 长江武汉段采样断面8月水体和沉积物中∑PAEs沿程分布 Fig. 5 Distribution of ∑PAEs in water and sediment from WSYR in August |
PAHs主要通过天然和人为的燃烧过程引入环境, 人为PAHs主要是化石燃料燃烧和石油源[24]. PAEs在许多消费品和建筑材料中被用作增塑剂, 每年生产大量PAEs用于生产软质聚氯乙烯(PVC)和其他塑料产品[25]. PAEs不会与塑料材料化学结合, 并且容易浸入环境中[26].在本研究中, 使用比率和主成分分析来确定PAHs和PAEs的来源.
2.2.1 比率分析水和沉积物中PAHs的来源对水环境保护及水资源管理具有重要意义.不同来源的PAHs有特定的组成特征, 其同分异构体比值常用于指示PAHs在环境介质中的来源[24, 27].由于Ant、Phe、Fla、Pyr等具有相对稳定的特征, Ant/(Phe+Ant)、Fla/(Fla+Pyr)和BaA/(BaA+Chr)的比值被广泛用于PAHs来源分析[28~31].通常认为, Ant/(Phe+Ant)比值小于0.1时, 表示PAHs主要来自石油源, 大于0.1表示主要为燃烧源[28]; 当Fla/(Fla+Pyr)比值小于0.4时, 表示其主要来源为石油源, 介于0.4和0.5之间为液态石油类产品(汽油、煤油、原油等)的燃烧, 大于0.5为煤和草、木柴等生物燃料的燃烧[29]; 当BaA/(BaA+Chr)比值小于0.2时, 其主要来源为石油源, 大于0.35为燃烧源, 介于0.2和0.35之间为混合源[30, 31].如图 6(a)可知, 长江武汉段水体中PAHs主要来自燃烧(包括石油、生物质等); 由图 6(b)得出, 长江武汉段沉积物样品中的PAHs主要来源于石油源和燃烧(包括石油、生物质和煤燃烧)的混合.

|
图 6 长江武汉段8月水体与沉积物中PAHs的比率点 Fig. 6 Ratio plots of PAHs in water and sediment from WSYR in August |
特定PAHs化合物的比例可作为PAHs来源的间接指标, 然而, 这一分析并不能分析各因素与污染源贡献度之间的相互关系, 因此, 采用主成分分析甄别PAHs的来源[32].长江武汉段水体和沉积物中PAHs的主成分分析如图 7所示.主成分的提取以特征根大于1为标准.从水样提取了2个主成分, PC1和PC2分别占总方差的48.45%和29.22%.对于沉积物样品, 提取了3个主成分, PC1和PC2分别占总方差的50.17%和28.39%, 由于PC3相关性较弱(仅占总方差的8.22%), 所以PC3没有出现在图 7(b).

|
图 7 长江武汉段8月水体与沉积物中PAHs的主成分 Fig. 7 Rotated principal components of PAHs in water and sediment from WSYR in August |
如图 7所示, 针对长江武汉段干流水样和沉积物, Fla和Pyr分别是8月样品中PC1的主要贡献者, Acy和Ace均为PC2的主要贡献者. Ace, Acy是具有4个环的中分子量多环芳烃, 其中Ace主要的来源是石油源[33, 34], Acy与化石燃料的不完全燃烧有关[35]. Ant、Ace、Acy是具有3个环的低分子量多环芳烃, 据报道它们与煤和生物质燃烧相关联[36].因此, 长江武汉段水样与沉积物中PAHs主要的来源为煤和生物质等燃烧, 以及石油源, 这一结果与比率分析的结果是一致的.
同时采用主成分分析法来分析长江武汉段干流水体和沉积物中PAEs的来源, 结果如图 8所示.对于8月水体和沉积物样品, 均提取出2个主成分, 每个主成分(PC)的特征根均大于1. 8月水体样品前两个主成分的方差贡献率分别为54.45%和22.46%, 沉积物样品分别为55.72%和18.51%.

|
图 8 长江武汉段8月水体与沉积物中PAEs的主成分 Fig. 8 Rotated principal components of PAEs in water and sediment from WSYR in August |
对于水体样品, PC1中DMP和DEP载荷最高, PC2中DEHP载荷最高.对于沉积物样品, PC1中DBP载荷最高, PC2中DMP载荷最高. DEHP主要来源于塑料和重化工产业[37], 同时也是生活垃圾常见的PAEs类污染物[22]. DEP和DBP被广泛应用于化妆品和个人护理品中[38, 39]. DEP、DBP和DMP也是生活垃圾(例如化妆品、玩具、塑料容器等)中的主要PAEs类污染物[40].可见, 长江武汉段干流水体和沉积物中PAEs的主要来源于塑料和重化工工业, 以及生活垃圾.
2.3 污染水平分析 2.3.1 PAHs分析表 3列举了中国地表水环境质量标准[41]、美国环保署国家水质标准[42]、加拿大环境质量准则[43]中规定的PAHs含量限值.本次调查表明, 长江武汉段水体中∑PAHs浓度范围为20.8~90.4 ng·L-1, 其含量均不超过上述标准规定的限值.
|
|
表 3 不同国家PAHs水质标准1)/ng·L-1 Table 3 Standards for water quality of PAHs by different countries/ng·L-1 |
表 4是长江武汉段与国内外其他河流水体和沉积物中PAHs污染状况比较.从中可以得出, 长江武汉段水体中PAHs污染水平低于黄河、通惠河、太子河, 其中黄河水体中PAHs浓度约为长江武汉段水体PAHs浓度的6倍, 通惠河和太子河水体中PAHs比长江武汉段水体PAHs浓度高1~2个数量级; 与国外河流比较, 长江武汉段水体PAHs污染水平高于法国塞纳河、美国密西西比河.长江武汉段沉积物中PAHs污染水平高于黄河, 低于通惠河及长江口, 其中长江武汉段沉积物中PAHs浓度约为黄河沉积物中PAHs浓度的2.5倍, 通惠河沉积物中PAHs约为长江武汉段沉积物中PAHs浓度的3倍.总体而言, 长江武汉段丰水期水体和沉积物中PAHs污染水平较低.
|
|
表 4 国内外其他河流水体和沉积物中PAHs污染状况1) Table 4 Total PAHs concentration in water and sediment from various sites in the world |
2.3.2 PAEs分析
本次调查得出长江武汉段水体∑PAEs浓度范围为280.9~779.0 ng·L-1.由表 5可知, 长江武汉段水体∑PAEs均低于相关标准(中国地表水环境质量标准[41]、美国环保署国家水质标准[42]及加拿大环境质量准则[43])中规定的限值.
|
|
表 5 不同国家PAEs水质标准1)/ng·L-1 Table 5 Standards for water quality of PAEs by different countries/ng·L-1 |
表 6是长江武汉段与国内外其他河流水体和沉积物中PAEs污染状况比较.可以得出, 长江武汉段水体中PAEs污染水平低于长江江苏段、长江三角洲、黄河中下游, 其中长江三角洲中PAEs浓度约为长江武汉段水体PAEs浓度的8.5倍, 长江江苏段水体中PAEs约为长江武汉段水体PAHs浓度的1.7倍.长江武汉段沉积物中PAEs污染水平显著低于台湾河、英国特伦特河.总体而言, 长江武汉段丰水期水体和沉积物中PAEs污染水平也较低.
|
|
表 6 国内外其他河流水体和沉积物中PAEs污染状况1) Table 6 Total PAEs concentration in water and sediment from various sites in the world |
2.4 污染风险评估 2.4.1 PAHs评估
表 7列出了水生生物暴露于PAHs污染水体的安全标准.安全标准中的数据指示是水生生物, 尤其是牡蛎等滤食软体动物通过食物链进而能够对人类健康构成威胁的PAHs浓度.参考国际不同国家的安全标准, 由表 7可知, 长江武汉段丰水期表层水体中各单体PAHs均未超过各国制定的安全标准, 但∑PAHs均值超过了美国环境质量标准的规定限值.
|
|
表 7 水生生物暴露PAHs水体的安全标准1)/μg·L-1 Table 7 Safety guidelines for aquatic organisms exposed to PAHs in water/μg·L-1 |
沉积物中PAHs的生态毒性, 应用最多的是Long等的研究方法[50].当环境中PAHs的含量低于生物影响范围低值(ERL), 对生物的毒性副作用不明显, 若高于生物影响范围中值(ERM), 对生物会产生毒性副作用.由表 8可知, 长江武汉段丰水期干流沉积物中PAHs单体平均含量均低于ERL, 部分样点PAHs单体(如Ace、Flu、Ant等)的含量超过ERL.总之, 长江武汉段沉积物中PAHs会对周围生物具有潜在的毒性作用, 但毒性副作用不明显.
|
|
表 8 长江武汉段沉积物PAHs的毒性标准1)/ng·g-1 Table 8 Toxicity guidelines of PAHs in sediments from WSYR/ng·g-1 |
2.4.2 PAEs评估
环境水质基准是制定水体环境质量标准限值的基础, 对于预测、评价控制和治理进入水环境中的污染物质, 维护良好生态环境具有重要意义.如表 9所示, 根据毒理学数据和数值计算, 美国环保署制定了PAEs人体健康水质基准.人体健康水质基准代表的是通过饮水和食用水生生物或只通过食用水生生物而对人类不产生有害影响的污染物最大可接受浓度.参考水质基准, 从中可见长江武汉段丰水期表层水体DMP、DEP、DBP、BBP浓度均未超过人体健康水质基准, 但部分样点DEHP质量浓度超过了人体健康水质基准(饮水+食用水生生物). DEHP通过食物链被富集于鱼类、贝类等水生生物体内, 进而通过饮水、皮肤接触、食用鱼类或贝类等途径进入人体内, 对人类健康会产生潜在有害影响.
|
|
表 9 美国环保署PAEs人体健康水质基准1)/μg·L-1 Table 9 Human health water quality criteria for PAEs by EPA/μg·L-1 |
目前有关沉积物中PAEs的环境风险评价研究较少, 尚未建立起统一的评价标准. Van Wezel等[51]通过大量的体内和体外毒理实验, 建议DBP和DEHP的生物影响范围低值(ERL)分别为700 ng·g-1和1 000 ng·g-1, 当相对污染系数(RCF=PAEs/ERL)结果小于1, 不存在PAEs的内分泌干扰和生态毒性风险; 结果大于1, 存在PAEs的内分泌干扰和生态毒性风险.如表 10所示, 除倒水河汇入口上游(P4)断面外, 长江武汉段干流沉积物中DBP和DEHP相对污染系数均大于1.总体而言, 长江武汉段干流沉积物受到DBP和DEHP的污染, 对人类健康会产生潜在有害影响.
|
|
表 10 长江武汉段沉积物中有机污染物均值和相对污染系数 Table 10 Mean and relative pollution coefficient of organic pollutants in sediments from WSYR |
3 结论
(1) 长江武汉段水体和沉积物中∑PAHs浓度分别为20.8~90.4 ng·L-1(均值40.7 ng·L-1)和46.1~424.0 ng·g-1(均值191.8 ng·g-1), ∑PAEs浓度分别为280.9~779.0 ng·L-1 (均值538.6 ng·L-1)和1 346.2~7 641.1 ng·g-1(均值3 699.5 ng·g-1).
(2) 长江武汉段水体中PAHs以2~3环为主, 沉积物中以2~3环和4环为主; 水体和沉积物中浓度较高的PAHs单体分别为Flu和Ant, 水体和沉积物中PAEs均以DEHP和DBP为主.长江武汉段水体两类POPs(PAHs和PAEs)污染水平低.
(3) 长江武汉段水样与沉积物中PAHs主要的来源为煤和生物质燃烧, 以及石油来源; 水体和沉积物中PAEs主要来源于塑料和重化工工业, 以及生活垃圾.
(4) 长江武汉段丰水期水体及沉积物中两类典型POPs(PAHs和PAEs)对人类健康会产生潜在有害影响, 需加强监控.
| [1] | Skarphéeinsdóttir H, Ericson G, Svavarsson J, et al. DNA adducts and polycyclic aromatic hydrocarbon (PAH) tissue levels in blue mussels (Mytilus spp.) from Nordic coastal sites[J]. Marine Environmental Research, 2007, 64(4): 479-491. DOI:10.1016/j.marenvres.2007.03.007 |
| [2] | Engraff M, Solere C, Smith K E C, et al. Aquatic toxicity of PAHs and PAH mixtures at saturation to benthic amphipods:linking toxic effects to chemical activity[J]. Aquatic Toxicology, 2011, 102(3-4): 142-149. DOI:10.1016/j.aquatox.2011.01.009 |
| [3] | Manoli E, Samara C, Konstantinou I, et al. Polycyclic aromatic hydrocarbons in the bulk precipitation and surface waters of Northern Greece[J]. Chemosphere, 2000, 41(12): 1845-1855. DOI:10.1016/S0045-6535(00)00134-X |
| [4] | Wang Y, Shen C C, Shen Z Y, et al. Spatial variation and sources of polycyclic aromatic hydrocarbons (PAHs) in surface sediments from the Yangtze Estuary, China[J]. Environmental Science Processes & Impacts, 2015, 17(7): 1340-1347. |
| [5] | Zhang L L, Liu J L, Liu H Y, et al. The occurrence and ecological risk assessment of phthalate esters (PAEs) in urban aquatic environments of China[J]. Ecotoxicology, 2015, 24(5): 967-984. DOI:10.1007/s10646-015-1446-4 |
| [6] | Xu Z W, Zhang W M, Lv L, et al. A new approach to catalytic degradation of dimethyl phthlate by a macroporous OH-type strongly basic anion exchange resin[J]. Environmental Science & Technology, 2010, 44(8): 3130-3135. |
| [7] | Li B, Liu R X, Gao H J, et al. Spatial distribution and ecological risk assessment of phthalic acid esters and phenols in surface sediment from urban rivers in Northeast China[J]. Environmental Pollution, 2016, 219: 409-415. DOI:10.1016/j.envpol.2016.05.022 |
| [8] |
冯承莲, 夏星辉, 周追, 等. 长江武汉段水体中多环芳烃的分布及来源分析[J]. 环境科学学报, 2007, 27(11): 1900-1908. Feng C L, Xia X H, Zhou Z, et al. Distribution and sources of polycyclic aromatic hydrocarbons in the Wuhan section of the Yangtze River[J]. Acta Scientiae Circumstantiae, 2007, 27(11): 1900-1908. DOI:10.3321/j.issn:0253-2468.2007.11.025 |
| [9] | Feng C L, Xia X H, Shen Z Y, et al. Distribution and sources of polycyclic aromatic hydrocarbons in Wuhan section of the Yangtze River, China[J]. Environmental Monitoring and Assessment, 2007, 133(1-3): 447-458. DOI:10.1007/s10661-006-9599-5 |
| [10] |
王凡, 沙玉娟, 夏星辉, 等. 长江武汉段水体邻苯二甲酸酯分布特征研究[J]. 环境科学, 2008, 29(5): 1163-1169. Wang F, Sha Y J, Xia X H, et al. Distribution characteristics of Phthalic acid esters in the Wuhan section of the Yangtze River[J]. Environmental Science, 2008, 29(5): 1163-1169. |
| [11] |
张彦鹏, 周爱国, 刘存富, 等. 长江流域武汉段水体中邻苯二甲酸酯含量研究[J]. 环境科学与技术, 2011, 34(11): 130-134. Zhang Y P, Zhou A G, Liu C F, et al. Phthalic acid esters in Wuhan section of Yangtze River[J]. Environmental Science & Technology, 2011, 34(11): 130-134. DOI:10.3969/j.issn.1003-6504.2011.11.027 |
| [12] |
唐阵武, 程家丽, 张化永, 等. 长江武汉段水体有机污染的健康风险评价[J]. 水利学报, 2009, 40(9): 1064-1069. Tang Z W, Cheng J L, Zhang H Y, et al. Health risk assessment of organic pollutants in water of Wuhan reach of Yangtze River[J]. Journal of Hydraulic Engineering, 2009, 40(9): 1064-1069. |
| [13] | Wang W L, Wu Q Y, Wang C, et al. Health risk assessment of phthalate esters (PAEs) in drinking water sources of China[J]. Environmental Science and Pollution Research, 2015, 22(5): 3620-3630. DOI:10.1007/s11356-014-3615-z |
| [14] | Wu Y L, Wang H X, Li Y Y, et al. Occurrence of polycyclic aromatic hydrocarbons (PAHs) in seawater from the western Taiwan Strait, China[J]. Marine Pollution Bulletin, 2011, 63(5-12): 459-463. DOI:10.1016/j.marpolbul.2011.03.008 |
| [15] | Floehr T, Scholz-Starke B, Xiao H X, et al. Yangtze three gorges reservoir, China:a holistic assessment of organic pollution, mutagenic effects of sediments and genotoxic impacts on fish[J]. Journal of Environmental Sciences, 2015, 38: 63-82. DOI:10.1016/j.jes.2015.07.013 |
| [16] |
王乙震, 张俊, 周绪申, 等. 白洋淀多环芳烃与有机氯农药季节性污染特征及来源分析[J]. 环境科学, 2017, 38(3): 964-978. Wang Y Z, Zhang J, Zhou X S, et al. Seasonal pollution characteristics and source identification of polycyclic aromatic hydrocarbons and organochlorine pesticides in surface water of Baiyangdian lake[J]. Environmental Science, 2017, 38(3): 964-978. |
| [17] | Zeng F, Cui K, Xie Z, et al. Occurrence of phthalate esters in water and sediment of urban lakes in a subtropical city, Guangzhou, South China[J]. Environment International, 2008, 34(3): 372-380. DOI:10.1016/j.envint.2007.09.002 |
| [18] |
许川, 舒为群, 罗财红, 等. 三峡库区水环境多环芳烃和邻苯二甲酸酯类有机污染物健康风险评价[J]. 环境科学研究, 2007, 20(5): 57-60. Xu C, Shu W Q, Luo C H, et al. Water environmental health risk assessment of PAHs and PAEs in the Three Gorges Reservoir[J]. Research of Environmental Sciences, 2007, 20(5): 57-60. |
| [19] | Limam I, Driss M R. Off-line solid-phase extraction procedure for the determination of polycyclic aromatic hydrocarbons from aqueous matrices[J]. International Journal of Environmental Science and Technology, 2013, 10(5): 973-982. DOI:10.1007/s13762-013-0229-9 |
| [20] | Brown J N, Peake B M. Determination of colloidally-associated polycyclic aromatic hydrocarbons (PAHs) in fresh water using C18 solid phase extraction disks[J]. Analytica Chimica Acta, 2003, 486(2): 159-169. DOI:10.1016/S0003-2670(03)00472-0 |
| [21] | Song X Y, Hu X J, He M M, et al. Distribution and sources of polycyclic aromatic hydrocarbons in the surface water of Taizi River, Northeast of China[J]. Environmental Monitoring & Assessment, 2013, 185(10): 8375-8382. |
| [22] | Wang F, Xia X H, Sha Y J. Distribution of phthalic acid esters in Wuhan section of the Yangtze River, China[J]. Journal of Hazardous Materials, 2008, 154(1-3): 317-324. DOI:10.1016/j.jhazmat.2007.10.028 |
| [23] | He H, Hu G J, Sun C, et al. Trace analysis of persistent toxic substances in the main stream of Jiangsu section of the Yangtze River, China[J]. Environmental Science and Pollution Research, 2011, 18(4): 638-648. DOI:10.1007/s11356-010-0414-z |
| [24] | Zhang Z L, Huang J, Yu G, et al. Occurrence of PAHs, PCBs and organochlorine pesticides in the Tonghui River of Beijing, China[J]. Environmental Pollution, 2004, 130(2): 249-261. DOI:10.1016/j.envpol.2003.12.002 |
| [25] | Guo Y, Kannan K. Comparative assessment of human exposure to phthalate esters from house dust in China and the United States[J]. Environmental Science & Technology, 2011, 45(8): 3788-3794. |
| [26] | Bauer M J, Herrmann R. Estimation of the environmental contamination by phthalic acid esters leaching from household wastes[J]. Science of the Total Environment, 1997, 208(1-2): 49-57. DOI:10.1016/S0048-9697(97)00272-6 |
| [27] | Tuncel S G, Topal T. Polycyclic aromatic hydrocarbons (PAHs) in sea sediments of the Turkish Mediterranean coast, composition and sources[J]. Environmental Science and Pollution Research, 2015, 22(6): 4213-4221. DOI:10.1007/s11356-014-3621-1 |
| [28] | Zhu Y D, Yang Y Y, Liu M X, et al. Concentration, distribution, source, and risk assessment of PAHs and heavy metals in surface water from the Three Gorges Reservoir, China[J]. Human and Ecological Risk Assessment, 2015, 21(6): 1593-1607. DOI:10.1080/10807039.2014.962315 |
| [29] | Li G C, Xia X H, Yang Z F, et al. Distribution and sources of polycyclic aromatic hydrocarbons in the middle and lower reaches of the Yellow River, China[J]. Environmental Pollution, 2006, 144(3): 985-993. DOI:10.1016/j.envpol.2006.01.047 |
| [30] | Baumard P, Budzinski H, Michon Q, et al. Origin and bioavailability of PAHs in the Mediterranean sea from mussel and sediment records[J]. Estuarine, Coastal and Shelf Science, 1998, 47(1): 77-90. DOI:10.1006/ecss.1998.0337 |
| [31] | Yunker M B, Macdonald R W, Vingarzan R, et al. PAHs in the Fraser River basin:a critical appraisal of PAH ratios as indicators of PAH source and composition[J]. Organic Geochemistry, 2002, 33(4): 489-515. DOI:10.1016/S0146-6380(02)00002-5 |
| [32] | Wang Z C, Liu M, Yang Y. Characterization and sources analysis of polycyclic aromatic hydrocarbons in surface sediments in the Yangtze River Estuary[J]. Environmental Earth Sciences, 2015, 73(5): 2453-2462. DOI:10.1007/s12665-014-3594-x |
| [33] | Soclo H H, Garrigues P, Ewald M. Origin of polycyclic aromatic hydrocarbons (PAHs) in coastal marine sediments:case studies in Cotonou (Benin) and Aquitaine (France) areas[J]. Marine Pollution Bulletin, 2000, 40(5): 387-396. DOI:10.1016/S0025-326X(99)00200-3 |
| [34] | Xu J, Yu Y, Wang P, et al. Polycyclic aromatic hydrocarbons in the surface sediments from Yellow River, China[J]. Chemosphere, 2007, 67(7): 1408-1414. DOI:10.1016/j.chemosphere.2006.10.074 |
| [35] | Liu A X, Lang Y H, Xue L D, et al. Probabilistic ecological risk assessment and source apportionment of polycyclic aromatic hydrocarbons in surface sediments from Yellow Sea[J]. Bulletin of Environmental Contamination and Toxicology, 2009, 83(5): 681-687. DOI:10.1007/s00128-009-9870-x |
| [36] | Dong T T T, Lee B K. Characteristics, toxicity, and source apportionment of polycylic aromatic hydrocarbons (PAHs) in road dust of Ulsan, Korea[J]. Chemosphere, 2009, 74(9): 1245-1253. DOI:10.1016/j.chemosphere.2008.11.035 |
| [37] | Simoneit B R T, Medeiros P M, Didyk B M. Combustion products of plastics as indicators for refuse burning in the atmosphere[J]. Environmental Science & Technology, 2005, 39(18): 6961-6970. |
| [38] | Koniecki D, Wang R, Moody R P, et al. Phthalates in cosmetic and personal care products:concentrations and possible dermal exposure[J]. Environmental Research, 2011, 111(3): 329-336. DOI:10.1016/j.envres.2011.01.013 |
| [39] | Romero-Franco M, Hernandez-Ramírez R U, Calafat A M, et al. Personal care product use and urinary levels of phthalate metabolites in Mexican women[J]. Environment International, 2011, 37(5): 867-871. DOI:10.1016/j.envint.2011.02.014 |
| [40] | Zhang L F, Dong L, Ren L J, et al. Concentration and source identification of polycyclic aromatic hydrocarbons and phthalic acid esters in the surface water of the Yangtze River Delta, China[J]. Journal of Environmental Sciences, 2012, 24(2): 335-342. DOI:10.1016/S1001-0742(11)60782-1 |
| [41] |
GB 3838-2002, 地表水环境质量标准[S]. GB 3838-2002, Environmental quality standards for surface water[S]. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zghbcy200206001 |
| [42] | US Environmental Protection Agency. National Recommended Water Quality Criteria[S]. |
| [43] | Canadian Council of Ministers of the Environment (CCME). Canadian Environmental Quality Guidelines[S]. |
| [44] | Fernandes M B, Sicre M A, Boireau A, et al. Polyaromatic hydrocarbon (PAH) distributions in the Seine River and its estuary[J]. Marine Pollution Bulletin, 1997, 34(11): 857-867. DOI:10.1016/S0025-326X(97)00063-5 |
| [45] | Mitra S, Bianchi T S. A preliminary assessment of polycyclic aromatic hydrocarbon distributions in the lower Mississippi River and Gulf of Mexico[J]. Marine Chemistry, 2003, 82(3-4): 273-288. DOI:10.1016/S0304-4203(03)00074-4 |
| [46] | Macías-Zamora J V, Mendoza-Vega E, Villaescusa-Celaya J A. PAHs composition of surface marine sediments:a comparison to potential local sources in Todos Santos Bay, B. C., Mexico[J]. Chemosphere, 2002, 46(3): 459-468. DOI:10.1016/S0045-6535(01)00069-8 |
| [47] | Long J L A, House W A, Parker A, et al. Micro-organic compounds associated with sediments in the Humber rivers[J]. Science of the Total Environment, 1998, 210-211: 229-253. DOI:10.1016/S0048-9697(98)00015-1 |
| [48] |
沙玉娟, 夏星辉, 肖翔群. 黄河中下游水体中邻苯二甲酸酯的分布特征[J]. 中国环境科学, 2006, 26(1): 120-124. Sha Y J, Xia X H, Xiao X Q. Distribution characters of phthalic acid ester in the waters middle and lower reaches of the Yellow River[J]. China Environmental Science, 2006, 26(1): 120-124. |
| [49] | Yuan S Y, Liu C, Liao C S, et al. Occurrence and microbial degradation of phthalate esters in Taiwan river sediments[J]. Chemosphere, 2002, 49(10): 1295-1299. DOI:10.1016/S0045-6535(02)00495-2 |
| [50] | Long E R, Macdonald D D, Smith S L, et al. Incidence of adverse biological effects within ranges of chemical concentrations in marine and estuarine sediments[J]. Environmental Management, 1995, 19(1): 81-97. DOI:10.1007/BF02472006 |
| [51] | Van Wezel A P, Van Vlaardingen P, Posthumus R, et al. Environmental risk limits for two phthalates, with special emphasis on endocrine disruptive properties[J]. Ecotoxicology and Environmental Safety, 2000, 46(3): 305-321. DOI:10.1006/eesa.2000.1930 |
 2018, Vol. 39
2018, Vol. 39


