2. 中国科学院生态环境研究中心城市与区域生态国家重点实验室, 北京 100085;
3. 中国科学院城市环境研究所城市环境与健康重点实验室, 厦门 361021
2. State Key Laboratory of Urban and Regional Ecology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China;
3. Key Laboratory of Urban Environment and Health, Institute of Urban Environment, Chinese Academy of Sciences, Xiamen 361021, China
砷是自然环境中普遍存在的类金属元素, 毒性很大[1].好氧环境中砷以As(Ⅴ)为主, 主要以水合阴离子形式存在.现阶段水体中去除As(Ⅴ)技术主要包括:电絮凝、化学沉淀、过滤、反渗透、离子交换、膜处理、生物法等[2], 而这些技术中吸附去除法因其操作简便、成本低廉等特点, 引起了广泛的关注.
生物炭(biochar, BC)作为一种吸附材料, 被广泛应用于各类吸附研究中[2~5].但生物炭表面带负电荷, 因此阴离子吸附能力较弱[6], 单一生物炭吸附As(Ⅴ)效果不是很理想[7].需要对生物炭进行改性修饰, 从而增加生物炭的吸附As(Ⅴ)能力.提高除As(Ⅴ)能力的方法包括:优化微观结构、表面官能团, 或在生物炭表面负载活性基团[8].然而, 对生物炭进行优化的过程通常是复杂且耗时的, 因此如何能在制作生物炭的过程中既不额外附加繁杂的负载过程, 又能进一步提高生物炭吸附去除As(Ⅴ)能力, 这一问题受到普遍关注.
化学共沉淀法被广泛地用来给生物炭表面负载金属活性基团[4, 9].但通常情况下, 化学共沉淀法负载金属活性基团是在热解生物炭之后, 这样不仅工艺复杂, 而且由于共沉淀还使得生物炭孔隙减小[8].一步热解负载金属盐的生物质生产改性生物炭是非常容易实现的[10, 11].
稀土元素的氧化物因其具有有较高的阴离子吸附能力[1, 2, 6], 已被应用于净化水体的研究.但直接投加稀土元素化合物, 不易回收处理, 并且在增加成本同时还容易造成二次污染问题.因此, 将稀土元素负载于生物炭上既便于回收降低成本, 减轻二次污染的风险, 还可以使稀土元素在生物炭上均匀分布以增加稀土元素对阴离子的吸附能力.但到目前为止, 国内外对负载稀土元素的材料, 大部分集中在使用胶体或直接制备纳米材料上[12~14], 使用生物炭作为载体负载稀土元素的研究较少.并且载稀土材料吸附阴离子的研究多集中于对有机污染物的吸附[5, 6, 15, 16], 吸附As的研究较少, 机制尚不明确.故本研究采用一步热解负载稀土元素镧和铈的稻壳制备生物炭, 拟分析改性后的生物炭对As(Ⅴ)的吸附能力变化, 以及溶液初始pH和溶液初始浓度对生物炭吸附As(Ⅴ)能力的影响, 并分析其吸附机制.
1 材料与方法 1.1 试剂与仪器试剂:硝酸镧[La(NO3)3]、硝酸铈[Ce(NO3)3]、氢氧化钠(NaOH)、硝酸(HNO3)、硝酸钠(NaNO3)、砷酸钠(Na3AsO4)均为分析纯.
实验中所使用的主要仪器有:马弗炉(3-1750A型, 美国Neytech); pH计(FE28-Standard型, 梅特勒); 冷冻干燥机(FD-1-50型, ), 空气恒温振荡器(IS-RDV3型, 美国精骐), 电热恒温干燥箱, 超声混匀仪(KQ-500B型, 昆山舒美).
1.2 生物炭及载镧或铈元素生物炭的制备实验选用水稻稻壳作为烧制生物炭的原料, 取一定量的稻壳加入不锈钢密封罐中, 压实封口后放入马弗炉中, 缺氧条件下40℃·min-1升温至450℃, 停留4 h, 冷却后取出生物炭, 在研钵中磨碎并过80目筛, 收集后标注BC.
载稀土元素生物炭采用一步热解法, 直接热解负载稀土元素的稻壳获得.取140 g稻壳浸泡在1 L 0.1 mol·L-1的La(NO3)3或Ce(NO3)3溶液中, 放置在超声混匀仪上进行超声混匀2 h, 使溶液快速浸入稻壳中.超声后稻壳放入烘箱中(70℃), 直到烘干(24 h).将烘干后的稻壳装入不锈钢密封罐, 放入马弗炉中, 缺氧条件下450℃烧制4 h.冷却后将生物炭取出, 在研钵中磨碎并过80目筛, 分别将载镧和载铈生物炭标注为La-BC、Ce-BC.
1.3 载镧或铈生物炭吸附As(Ⅴ)实验吸附实验中所有As(Ⅴ)溶液均使用去离子水配置, 溶液离子强度均使用NaNO3调节为0.01 mol·L-1, 使用1 mol·L-1NaOH或HNO3调节溶液pH.每组实验均设置3个平行样品. As(Ⅴ)溶液中生物炭的加入量为1 g·L-1.
在考察生物炭吸附As(Ⅴ)能力实验中, 配制As(Ⅴ)溶液浓度为60 mg·L-1, 调节溶液初始pH为7.分别称取1.00 g生物炭于1 L蓝盖瓶中, 并加入1 L As(Ⅴ)溶液, 放在溶液混匀仪中, 25℃恒温混合24 h.实验包括空白(不加生物炭, CK), 普通生物炭(BC), 载镧生物炭(La-BC)和载铈生物炭(Ce-BC).吸附平衡后取约10 mL溶液经0.45 μm水相滤膜过滤, 每个样品分别取3次样, 剩余溶液使用真空抽滤器过滤.收集过滤后生物炭样品, 使用冷冻干燥机干燥, 分别将干燥后的BC、La-BC、Ce-BC标注为BC+As、La-BC+As、Ce-BC+As.
为了考察pH对生物炭吸附As(Ⅴ)的影响, 调节溶液初始pH为5、6、7、8、9. As(Ⅴ)溶液初浓度为60 mg·L-1.分别称取0.04 g生物炭于50 mL离心管中, 并加入40 mL As(Ⅴ)溶液, 放在溶液混匀仪中, 25℃恒温混合24 h.实验包括BC、La-BC、Ce-BC.
考察溶液初始浓度对生物炭吸附As(Ⅴ)的影响实验中, 先配置500 mg·L-1的As(Ⅴ)母液, 再使用0.01 mol·L-1 NaNO3溶液依次稀释至5、10、20、40、60、100 mg·L-1, 并调节溶液初始pH为7.分别称取0.04 g生物炭于50 mL离心管中, 并加入40 mL对应浓度As(Ⅴ)溶液, 放在溶液混匀仪中, 25℃恒温混合24 h.
吸附平衡后的溶液经0.45μm水相滤膜过滤, 使用电感耦合等离子体原子发射光谱仪(ICP-OES)(Optima 700DV型)测定样品中As(Ⅴ)浓度.
1.4 载镧或铈元素生物炭的表征使用扫描电子显微镜(SEM-EDS)(SU-8020, 日立)观察BC、La-BC、Ce-BC、BC+As、La-BC+As、Ce-BC+As.对比吸附As(Ⅴ)前后生物炭外观变化, 使用EDS扫描生物炭表面, 根据元素含量变化, 分析镧或铈元素的负载情况和对As(Ⅴ)的吸附情况.生物炭样品灰分含量测定参照ASTM D1762-84(2013)进行, pH测定参照GB/T 12496.7-1999进行.使用X-射线荧光光谱仪(XRF)(AXIOS-MAX型)分析BC、La-BC、Ce-BC表面元素构成及价态.使用傅氏转换红外光谱分析仪(FTIR)(IS-50型)分析BC、La-BC、Ce-BC、La-BC+As表面有机官能团, 根据谱图出现吸收峰的位置变化分析表面有机官能团变化.使用X-射线光电子能谱分析仪(XPS)(ESCALAB 250Xi型)分析BC、La-BC、Ce-BC、La-BC+As表面元素化学价态、官能团构成, 根据谱图拟合峰相对含量的变化分析生物炭表面官能团构成变化.
1.5 等温吸附曲线模型拟合等温吸附曲线可以用来表征在不同平衡浓度下吸附剂对As(Ⅴ)的吸附量, 并且通过与模型拟合可以得到吸附剂对As(Ⅴ)的理论最大吸附量.本实验中的吸附过程用Langmuir方程[式(1)]、Freundlich方程[式(2)]、Langmuir-Freundlich方程[式(3)]、Temkin方程[式(4)]、Toth方程[式(5)]和Dubinin-Radushkevich方程[式(6)]进行线性拟合[17].

|
(1) |

|
(2) |

|
(3) |

|
(4) |

|
(5) |

|
(6) |
式中, ce(mg·L-1)是吸附达到平衡时溶液中As(Ⅴ)浓度, Qe(mg·g-1)是吸附达到平衡时吸附剂对As(Ⅴ)的平衡吸附量, Qm(mg·g-1)是吸附剂对As(Ⅴ)理论最大吸附量, kL是Langmuir模型常数, kF是Freundlich模型常数, kLF是Langmuir-Freundlich模型常数, n是线性常数, b、A是Temkin模型常数, kT为Toth模型常数, t为Toth模型中不均匀能量参数, kDR为Dubinin-Radushkevich模型常数[5].
2 结果与讨论 2.1 载镧或铈生物炭批量吸附实验 2.1.1 生物炭吸附As(Ⅴ)效果实验在pH=7的条件下, 加入BC后的As(Ⅴ)溶液浓度为66.1 mg·L-1, 与未加入生物炭的As(Ⅴ)溶液浓度(66.7 mg·L-1)的溶液相比, 差别不显著(图 1), 这说明BC对于As(Ⅴ)没有吸附能力.加入La-BC后的As(Ⅴ)溶液浓度(37.7 mg·L-1)明显降低, 去除率达到43.5%, 说明La-BC对As(Ⅴ)有较强的吸附去除能力.加入Ce-BC后的As(Ⅴ)溶液浓度(62.2 mg·L-1), 变化较小, 只去除了6.7%, Ce-BC对As(Ⅴ)吸附能力较弱.

|
BC:生物炭, La-BC:载镧生物炭, Ce-BC:载铈生物炭, 下同 图 1 BC、La-BC、Ce-BC对As(Ⅴ)去除效果 Fig. 1 Effect of BC, La-BC, and Ce-BC on arsenic removal |
在溶液初始浓度相同, 生物炭投加量相同的情况下, pH对BC、La-BC、Ce-BC吸附As(Ⅴ)的影响(图 2)与生物炭吸附效果实验结果相同, 在所研究的pH范围内(pH为5~9), BC对As(Ⅴ)几乎没有吸附能力. La-BC吸附As(Ⅴ)受溶液初始pH影响较大.在酸性条件下(pH为5、6), 表现出较高的吸附能力.这与其他载镧材料吸附水体As(Ⅴ)的实验结果相同[9].随着pH升高, 吸附能力明显降低, pH=5时吸附量最高达到39.1 mg·g-1, pH=9时吸附量最低, 仅为17.6 mg·g-1. Ce-BC对As(Ⅴ)吸附能力同样也受pH的影响, 随pH升高而降低.这一结果与载铈材料吸附溶液中As(Ⅲ)结果相同[12].在pH=5时, 吸附量最大, 为8.1mg·g-1, pH=9时没有吸附能力. pH越高生物炭吸附能力越差这可能是因为载镧或铈吸附剂等电点在6~7附近[1, 9, 16, 18], pH大于7时吸附剂表面带负电, 而As(Ⅴ)在pH为2~7时, 在水中主要以H2AsO4-形式存在[7, 19], 也带负电, 这使得二者之间产生电荷排斥, 使吸附量降低.吸附平衡后溶液pH变化趋势与溶液初始pH相同(图 3), 不再分开讨论.

|
图 2 pH对BC、La-BC、Ce-BC吸附As(Ⅴ)的影响 Fig. 2 Effect of pH on BC, La-BC, and Ce-BC adsorbed As(Ⅴ) |

|
图 3 吸附平衡后溶液pH变化 Fig. 3 The pH of the solution after reaching adsorption equilibrium |
在25℃下, La-BC吸附As(Ⅴ)(图 4), 生物炭加入量相同的情况下, 在溶液初始浓度为5、10、20 mg·L-1时, 吸附量随着溶液浓度的增加, 也随之快速增加; 在溶液初始浓度超过40 mg·L-1后, 吸附量增加得非常缓慢, 稳定在19.5 mg·g-1左右, 这可能是因为La-BC对As(Ⅴ)吸附接近饱和.由此可知, 在一定范围内溶液的初始浓度越高La-BC对As(Ⅴ)的吸附量越大; 超过最大吸附量后溶液初始浓度不再产生影响[12]. Ce-BC吸附As(Ⅴ)时, 在初始浓度为5、10、20 mg·L-1时, 吸附量也随着溶液初始浓度的增加, 随之增加.当溶液初始浓度为40 mg·L-1时达到最大吸附量4.0 mg·g-1, 之后随着溶液初始浓度的增加吸附量趋于稳定.

|
图 4 BC、La-BC、Ce-BC对As(Ⅴ)的等温吸附曲线 Fig. 4 Adsorption isotherms of As(Ⅴ) adsorption by BC, La-BC, and Ce-BC |
根据拟合的数据可以看出(表 1), La-BC与4种模型都有很好的拟合效果.与Langmuir-Freundlich方程拟合的结果最好(R2=0.987), 说明La-BC吸附As(Ⅴ)的吸附过程同时包括单分子层和多分子层吸附. Langmuir方程拟合的相关系数(R2=0.966)高于Freundlich方程拟合的相关系数(R2=0.929), 这说明La-BC对As(Ⅴ)的吸附过程以单分子层吸附为主[5].根据Langmuir方程拟合结果, La-BC对As(Ⅴ)的理论最大吸附量为20.1 mg·g-1. Temkin方程的相关系数(R2=0.952)低于Toth方程(R2=0.967)拟合的相关系数也印证了La-BC吸附As(Ⅴ)的过程是以单分子层吸附为主的这一结论.与Dubinin-Radushkevich拟合相关系数(R2=0.922)低于与Langmuir方程拟合的相关系数(R2=0.966), 说明吸附过程中存在有微孔作用, 但并不是主要吸附过程.
|
|
表 1 吸附等温曲线拟合参数1) Table 1 Isotherm parameters for As(Ⅴ) adsorption |
而Ce-BC吸附As(Ⅴ)的数据与模型拟合相关系数均小于0.9, 结合初始pH对其吸附能力影响的数据, 可以说Ce-BC对As(Ⅴ)吸附能力较差, 不是理想的吸附材料.
2.2 吸附剂的表征实验由扫描电镜图可见3种生物炭表面结构差异明显(图 5).生物炭BC整体呈蜂窝状, 多孔, 大孔壁上有小孔, 这可能与烧制生物炭的稻壳形态有关; 断面整齐, 表面光滑, 附着少量颗粒, 结合EDS能谱图结果, 这些小颗粒的主要元素为C, 可能是被磨碎的小颗粒的生物炭.而负载稀土元素的生物炭La-BC、Ce-BC整体也呈蜂窝状多孔, 大孔壁上有小孔.不同的是后两者表面明显粗糙且附着大量颗粒.与BC相比, 明显后两者的孔壁变薄, 大孔壁上小孔也不明显.负载镧或铈元素后的生物炭表面不光滑、孔壁变薄可能是由负载时使用的La(NO3)3、Ce(NO3)3中NO3-引起的. NO3-具有一定的氧化性, El-Hendawy等[20]通过使用HNO3改变活性炭表面结构, 从而增加活性炭的吸附Pb能力, HNO3对生物炭表面产生腐蚀, 使得生物炭表面不光滑, 孔壁变薄.结合EDS能谱图结果, La-BC和Ce-BC表面颗粒主要构成元素分别为La和Ce, 表面大量的颗粒主要为负载的镧或铈元素化合物颗粒.并且由此可知, 镧和铈元素成功地负载到生物炭表面上.

|
图 5 BC、La-BC、Ce-BC扫描电镜照片和能谱图 Fig. 5 Scanning electron microscope-energy dispersive spectrometer (SEM-EDS) of BC, La-BC, and Ce-BC |
由表 2中可以看到负载镧和铈元素后La-BC、Ce-BC灰分由原来的40.57%(BC)分别增加到50.92%(La-BC)、51.96%(Ce-BC), 这是由于负载了镧或铈元素后, 元素形成结构稳定的金属氧化物, 不易被热解从而使得灰分增加[6, 10].与之前报道[6, 15, 21]不同的是, 本实验中使用稻壳烧制生物炭, 未改性的生物炭本身灰分含量较高(>40%), 而文献中使用木材锯屑烧制的生物炭的低灰分含量很低(BC灰分 < 10%).这可能是由于稻壳本身的硅含量可以达到30%~40%[22], SiO2在高温下不易热解, 导致稻壳炭本身灰分含量较高, 结合EDS(图 5)也可以看到改性生物炭表面有Si元素存在.并且文献[23]报道经H2O2处理后生物炭表面SiO2含量会增加, 本实验中使用的NO3-也可以起到类似H2O2的氧化效果.
|
|
表 2 BC、La-BC、Ce-BC的物理化学性质 Table 2 Physicochemical properties of BC, La-BC, and Ce-BC |
结合XRF的结果(表 2), 在La-BC中La元素是以La2O3存在的, 而在Ce-BC中Ce元素是以CeO4存在的.由此可知, 负载的镧或铈元素在生物炭上的价态分别是La3+和Ce4+. Ce-BC中Ce元素由负载时使用的+3价Ce(NO3)3变为+4价, 可能是因为在Ce(NO3)3溶于水的过程中有一部分Ce3+变成了Ce(OH)3, 据报道[12, 24], Ce(OH)3暴露于空气中后易氧化为Ce(OH)4, 本实验中浸泡过溶液的载铈稻壳又在烘箱中充分烘干, 为Ce3+被氧化提供了良好的条件.这一变价过程, 可能是使Ce-BC对As(Ⅴ)没有吸附能力的原因之一.
负载镧或铈后, 生物炭的pH也发生变化, 由原来的9.33(BC)分别降低为8.74(La-BC)、8.21(Ce-BC), 这可能也是由于负载时使用La(NO3)3、Ce(NO3)3引起的, NO3-可增加生物炭表面的酸性含氧官能团[20, 25, 26], 这使得改性后的生物炭pH变低.
2.3 La-BC吸附As(Ⅴ)吸附机制根据批量吸附实验结果可知, La-BC吸附As(Ⅴ)的吸附机制是以单分子的化学吸附为主.而Ce-BC也在前面的实验中证明了对As(Ⅴ)并没有吸附能力.
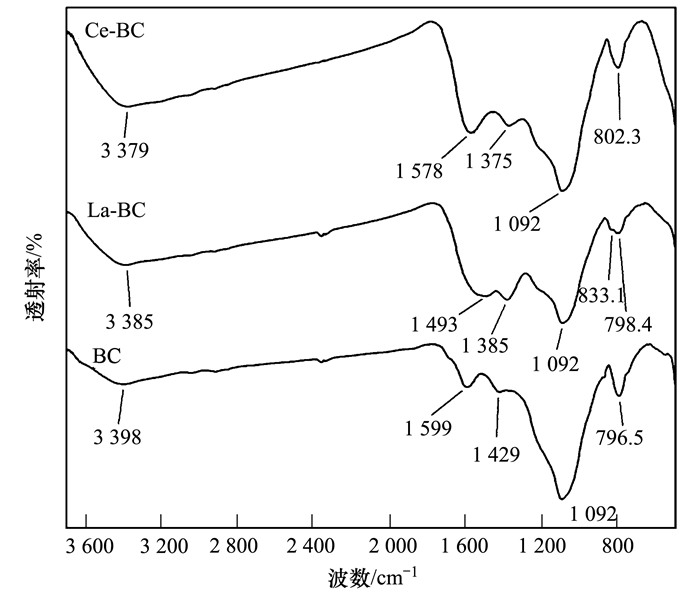
根据红外光谱图(图 6)可以看到, 3种生物炭表面都有分子间氢键[9, 12, 27](3 379、3 385、3 398 cm-1)、芳香烃结构[7, 9, 27](1 578、1 493、1 599、1 429 cm-1)、醇羟基[6, 23](1 092 cm-1).与BC(1 599 cm-1)相比, La-BC(1 493 cm-1)、Ce-BC(1 578 cm-1)芳香烃结构吸收峰位置发生了变化, 这说明生物炭表面产生了不同的芳香烃结构[23].负载镧或铈元素后生物炭表面增加了新的硝基官能团吸收峰[20](1 375 cm-1、1 385 cm-1).根据报道再结合XRF结果样品含有SiO2[23, 28, 29], 在796.5、798.4、802.3 cm-1位置的吸收峰为O—Si结构. La-BC在833.1 cm-1新增一个吸收峰, 这一位置为O—La结构[7, 9].同样负载铈元素的Ce-BC表面没有对应产生与C相连的O—Ce结构, 并且Ce-BC表面芳香烃结构吸收峰位置与La-BC不同, 这说明铈元素在Ce-BC上负载的位置与镧元素在La-BC的位置不同, 这可能是造成Ce-BC对As(Ⅴ)吸附能力不好的另一原因.
|
图 6 BC、La-BC、Ce-BC的傅里叶变换红外光谱图 Fig. 6 Fourier transform infrared spectroscopy (FTIR) spectrum for BC, La-BC, and Ce-BC |
将BC、Ce-BC以及吸附As(Ⅴ)前后的La-BCC1s光电子能谱图[图 7(a)]对比分析可以看到, 负载镧或铈元素后La-BC、Ce-BC表面均产生了C=O(289.3 eV)官能团[8, 11, 12].负载镧或铈元素后O1s光电子能谱图[图 7(b)], La-BC、Ce-BC表面新增加了金属氧化物的特征峰(530.1 eV)[8], 这表明La、Ce是以金属氧化物的形式负载在生物炭上[12], 与XRF的结果相一致.

|
图 7 BC、La-BC、Ce-BC、La-BC+As XPS的C1s和O1s光电子能谱图 Fig. 7 C1s and O1s X-ray photoelectron spectroscopy (XPS) spectrum of BC, La-BC, Ce-BC, and La-BC+As |
La-BC和Ce-BC两种生物炭表面官能团含量(表 3)大致相同, 而两者对As(Ⅴ)吸附能力却有很大差别, 结合前面实验结果, 这可能是由于与La-BC相比, Ce-BC中铈元素为+4价, 在负载的过程中, 表面并没有产生O—Ce结构, 生物炭表面可以参与吸附As(Ⅴ)的官能团没有被激活, 因此不能对As(Ⅴ)进行吸附.对比La-BC吸附前后的含C官能团相对含量变化, 可以看到在C=C含量相对一致的情况下, C=O由吸附前的5.9%减少到吸附后的3.5%, C—O由吸附前的19.3%增加到吸附后的28.1%.由此猜想, C=O官能团参与了La-BC对As(Ⅴ)的吸附过程, 并一部分转化为了C—O[8].同理对比含O官能团相对含量变化, 也可以看到金属氧化物相对含量由10.6%减少到3.1%, 而H—O有49.6%增加至57.8%, 由此金属氧化物即La—O也参与吸附As(Ⅴ), 并转化为La—OH, 与As(Ⅴ)形成络合物[9, 12, 16]吸附As(Ⅴ).
|
|
表 3 BC、La-BC、Ce-BC、La-BC+As各官能团相对含量 Table 3 Relative percentages of O1s and C1s for BC, La-BC, Ce-BC, and La-BC+As |
3 结论
(1) 本研究中制备的La-BC对As(Ⅴ)有较好的吸附能力, 在pH为7时理论最大吸附量为20.1mg·g-1, 吸附过程与Langmuir-Freundlich方程拟合的结果最好, 同时受到单分子层吸附和多分子层吸附的影响, 以单分子层化学吸附为主; BC和Ce-BC对As(Ⅴ)吸附能力较差.
(2) La-BC吸附As(Ⅴ)的化学机制:在负载La元素的过程中由于使用La(NO3)3的氧化作用使生物炭表面产生了C=O官能团, 并使得La3+被成功负载到生物炭上形成La—O官能团.生物炭本身有一部分官能团由于La3+的作用形成新的芳香烃结构, 激活了吸附位点, 使得La-BC上La化合物与As(Ⅴ)形成络合物吸附在生物炭表面.
(3) Ce-BC表面存在C=O官能团和Ce—O官能团, 但对As(Ⅴ)没有吸附能力是由于在负载过程中Ce3+氧化为Ce4+, 在负载的过程中无法激活吸附位点, 进而无法吸附As(Ⅴ).
| [1] |
张伟, 陈静, 张高生. 铁镧复合氧化物纳米吸附剂的制备、表征及As(Ⅲ)吸附性能研究[J]. 环境科学, 2014, 35(11): 4198-4204. Zhang W, Chen J, Zhang G S. Preparation and evaluation of Fe-La composite oxide nanoadsorbent for As(Ⅲ) removal from aqueous solutions[J]. Environmental Science, 2014, 35(11): 4198-4204. |
| [2] |
冯彦房, 薛利红, 杨梖, 等. 载镧生物质炭吸附水体中As(Ⅴ)的过程与机制[J]. 农业环境科学学报, 2015, 34(11): 2190-2197. Feng Y F, Xue L H, Yang B, et al. Adsorption of As(Ⅴ) from aqueous solution by lanthanum oxide-loaded biochar:process and mechanisms[J]. Journal of Agro-Environment Science, 2015, 34(11): 2190-2197. DOI:10.11654/jaes.2015.11.022 |
| [3] |
于志红, 黄一帆, 廉菲, 等. 生物炭-锰氧化物复合材料吸附砷(Ⅲ)的性能研究[J]. 农业环境科学学报, 2015, 34(1): 155-161. Yu Z H, Huang Y F, Lian F, et al. Adsorption of arsenic(Ⅲ) on biochar-manganese oxide composites[J]. Journal of Agro-Environment Science, 2015, 34(1): 155-161. DOI:10.11654/jaes.2015.01.022 |
| [4] |
吕宏虹, 宫艳艳, 唐景春, 等. 生物炭及其复合材料的制备与应用研究进展[J]. 农业环境科学学报, 2015, 34(8): 1429-1440. Lü H H, Gong Y Y, Tang J C, et al. Advances in preparation and applications of biochar and its composites[J]. Journal of Agro-Environment Science, 2015, 34(8): 1429-1440. DOI:10.11654/jaes.2015.08.001 |
| [5] |
李国亭, 冯艳敏, 柴晓琪, 等. 镧改性活性炭纤维高效吸附去除对苯醌[J]. 环境工程学报, 2016, 10(4): 1638-1644. Li G T, Feng Y M, Chai X Q, et al. Efficient adsorptive removal of p-benzoquinone by lanthanum modified activated carbon fibre[J]. Chinese Journal of Environmental Engineering, 2016, 10(4): 1638-1644. DOI:10.12030/j.cjee.20160410 |
| [6] | Wang Z H, Shen D K, Shen F, et al. Phosphate adsorption on lanthanum loaded biochar[J]. Chemosphere, 2016, 150: 1-7. DOI:10.1016/j.chemosphere.2016.02.004 |
| [7] | Jais F M, Ibrahim S, Yoon Y, et al. Enhanced arsenate removal by lanthanum and nano-magnetite composite incorporated palm shell waste-based activated carbon[J]. Separation and Purification Technology, 2016, 169: 93-102. DOI:10.1016/j.seppur.2016.05.034 |
| [8] | Yang J P, Zhao Y C, Ma S M, et al. Mercury removal by magnetic biochar derived from simultaneous activation and magnetization of sawdust[J]. Environmental Science & Technology, 2016, 50(21): 12040-12047. |
| [9] | Zhang W, Fu J, Zhang G S, et al. Enhanced arsenate removal by novel Fe-La composite (hydr)oxides synthesized via coprecipitation[J]. Chemical Engineering Journal, 2014, 251: 69-79. DOI:10.1016/j.cej.2014.04.057 |
| [10] | Wang J, Liao Z W, Ifthikar J, et al. One-step preparation and application of magnetic sludge-derived biochar on acid orange 7 removal via both adsorption and persulfate based oxidation[J]. RSC Advances, 2017, 7(30): 18696-18706. DOI:10.1039/C7RA01425B |
| [11] | Zhang G S, Qu J H, Liu H J, et al. Removal mechanism of As(Ⅲ) by a novel Fe-Mn binary oxide adsorbent:oxidation and sorption[J]. Environmental Science & Technology, 2007, 41(13): 4613-4619. |
| [12] | Zhang L F, Zhu T Y, Liu X, et al. Simultaneous oxidation and adsorption of As(Ⅲ) from water by cerium modified chitosan ultrafine nanobiosorbent[J]. Journal of Hazardous Materials, 2016, 308: 1-10. DOI:10.1016/j.jhazmat.2016.01.015 |
| [13] | Biswas B K, Inoue K, Ghimire K N, et al. Effective removal of arsenic with lanthanum(Ⅲ)-and cerium(Ⅲ)-loaded orange waste gels[J]. Separation Science and Technology, 2008, 43(8): 2144-2165. DOI:10.1080/01496390802064075 |
| [14] | Habuda-Stanić M, Nujić M. Arsenic removal by nanoparticles:a review[J]. Environmental Science and Pollution Research, 2015, 22(11): 8094-8123. DOI:10.1007/s11356-015-4307-z |
| [15] | Wang Z L, Guo H Y, Shen F, et al. Biochar produced from oak sawdust by lanthanum (La)-involved pyrolysis for adsorption of ammonium (NH4+), nitrate (NO3-), and phosphate (PO43-)[J]. Chemosphere, 2015, 119: 646-653. DOI:10.1016/j.chemosphere.2014.07.084 |
| [16] | Yu Y, Wang C H, Guo X, et al. Modification of carbon derived from Sargassum sp. by lanthanum for enhanced adsorption of fluoride[J]. Journal of Colloid and Interface Science, 2015, 441: 113-120. DOI:10.1016/j.jcis.2014.10.039 |
| [17] | Gerente C, Lee V K C, Le Cloirec P, et al. Application of chitosan for the removal of metals from wastewaters by adsorption-mechanisms and models review[J]. Critical Reviews in Environmental Science and Technology, 2007, 37(1): 47-127. |
| [18] | Sharma R, Singh N, Gupta A, et al. Electrospun chitosan-polyvinyl alcohol composite nanofibers loaded with cerium for efficient removal of arsenic from contaminated water[J]. Journal of Materials Chemistry A, 2014, 2(39): 16669-16677. DOI:10.1039/C4TA02363C |
| [19] |
朱义年, 张学洪, 解庆林, 等. 砷酸盐的溶解度及其稳定性随pH值的变化[J]. 环境化学, 2003, 22(5): 478-484. Zhu Y N, Zhang X H, Xie Q L, et al. Dependence of arsenate solubility and stability on pH value[J]. Environmental Chemistry, 2003, 22(5): 478-484. |
| [20] | El-Hendawy A N A. Influence of HNO3 oxidation on the structure and adsorptive properties of corncob-based activated carbon[J]. Carbon, 2003, 41(4): 713-722. DOI:10.1016/S0008-6223(03)00029-0 |
| [21] | Wang S S, Gao B, Zimmerm A R, et al. Removal of arsenic by magnetic biochar prepared from pinewood and natural hematite[J]. Bioresource Technology, 2015, 175: 391-395. DOI:10.1016/j.biortech.2014.10.104 |
| [22] |
方放, 周建斌, 杨继亮. 稻壳炭提取SiO2及制备活性炭联产工艺[J]. 农业工程学报, 2012, 28(23): 184-191. Fang F, Zhou J B, Yang J L. Poly-generation of activated carbon and silica from rice husk charcoal[J]. Transactions of the Chinese Society of Agricultural Engineering, 2012, 28(23): 184-191. |
| [23] | Guo J H, Chen B L. Insights on the molecular mechanism for the recalcitrance of biochars:interactive effects of carbon and silicon Components[J]. Environmental Science & Technology, 2014, 48(16): 9103-9112. |
| [24] | Li R H, Li Q, Gao S A, et al. Exceptional arsenic adsorption performance of hydrous cerium oxide nanoparticles:Part A. Adsorption capacity and mechanism[J]. Chemical Engineering Journal, 2012, 185-186: 127-135. DOI:10.1016/j.cej.2012.01.061 |
| [25] |
孟冠华, 李爱民, 张全兴. 活性炭的表面含氧官能团及其对吸附影响的研究进展[J]. 离子交换与吸附, 2007, 23(1): 88-94. Meng G H, Li A M, Zhang Q X. Studies on the oxygen-containing groups of activated carbon and their effects on the adsorption character[J]. Ion Exchange and Adsorption, 2007, 23(1): 88-94. |
| [26] |
蒋渊, 李坤权, 杨美蓉, 等. 硝酸改性对不同介孔结构生物质炭铅吸附的影响[J]. 环境工程学报, 2016, 10(9): 4887-4894. Jiang Y, Li K Q, Yang M R, et al. Effects of Pb2+ adsorption on biomass-based carbons with different mesoporous structures modified with nitric acid[J]. Chinese Journal of Environmental Engineering, 2016, 10(9): 4887-4894. DOI:10.12030/j.cjee.201503259 |
| [27] | Xu Y L, Chen B L. Organic carbon and inorganic silicon speciation in rice-bran-derived biochars affect its capacity to adsorb cadmium in solution[J]. Journal of Soils and Sediments, 2014, 15(1): 60-70. |
| [28] | Ou E C, Zhou J J, Mao S C, et al. Highly efficient removal of phosphate by lanthanum-doped mesoporous SiO2[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2007, 308(1-3): 47-53. DOI:10.1016/j.colsurfa.2007.05.027 |
| [29] | Liu P, Liu W J, Jiang H, et al. Modification of bio-char derived from fast pyrolysis of biomass and its application in removal of tetracycline from aqueous solution[J]. Bioresource Technology, 2012, 121: 235-240. DOI:10.1016/j.biortech.2012.06.085 |
 2018, Vol. 39
2018, Vol. 39


