2. 中国科学院宁波城市环境观测研究站, 宁波 315830;
3. 安徽师范大学生命科学学院, 芜湖 241000;
4. 宁波市北仑区环境保护局, 宁波 315800
2. Ningbo Urban Environment Observation and Research Station, Chinese Academy of Sciences, Ningbo 315830, China;
3. College of Life Sciences, Anhui Normal University, Wuhu 241000, China;
4. Environmental Protection Agency of Beilun, Ningbo 315800, China
溶解性有机质(dissolved organic matter, DOM)是一类具有复杂组成、结构和环境行为的有机混合物, 普遍存在于湖泊, 河流等自然水体中, 主要是由含氧、氮和硫的氨基酸、脂肪族、芳香族等功能团组成的异质碳氢化合物[1].DOM是连接生命形态碳和无机碳的关键纽带, 参与水生态各种生物地球化学过程, 对水生态系统结构和功能具有重要影响.DOM因水环境不同而产生的形态差异会与污染物发生不同类型的相互作用, 从而影响污染物的溶解、吸附解吸、毒性以及迁移转化特性[2, 3].而且, 在水生态系统中, DOM不仅影响营养物的保持与释放、生物有效性, 还被用来表征水质特征[4].在城镇化程度较高的河流中, 人类活动如污水排放[5], 土地覆盖和景观格局的改变[6]等均会引起河流水体DOM含量和性质的改变.由于DOM对水体的水质和富营养化等有显著影响, 因此一直受到广泛关注, 尤其是对DOM的结构、来源和辨析成为环境科学研究的重点.
荧光溶解性有机物(fluorescent dissolved organic matter, FDOM)是DOM中吸收光能并且发射荧光的物质, 是DOM的重要组成部分.不同类别的类腐殖质和类蛋白物质反映为不同的荧光组分, 对荧光组分进行解析即可实现DOM的辨别与表征.目前对国内外研究FDOM的技术方法较多, 其中三维荧光光谱以其操作简便, 选择性好、所需样品量少且不破坏样品结构等优点, 被广泛应用[7, 8].
三维荧光光谱广泛应用于水体中FDOM的表征, 包括组成、性质、来源和迁移转化, 以解释FDOM在水环境中的动力学特征[9~11].早期研究人员依据荧光特征峰解析FDOM组成结构, 例如类蛋白质峰、类腐殖质峰, 以及峰值的比值来判断水体污染程度[12, 13].但由于环境样品成分复杂, 导致不同物质的荧光响应值叠加, 单凭荧光特征峰也难以解析FDOM的组成和浓度[14].荧光区域积分法(fluorescence regional integration, FRI)是一种利用全区域荧光值对FDOM进行定量研究的方法, 在一定程度上克服了峰值法的不足, 近年来已用于湖泊、河流等水体三维荧光光谱的解析[1, 15].
在过去的30年中, 我国城市化和工业化进程明显加快, 城市化率由1980年的19.4%增加到2012年的52.5%[16].快速的城市化扩张和追求GDP的冲动特别是粗放型的经济发展方式使得我国许多地区面临严重的水质污染[17~19].河流水质的污染直接影响到水体FDOM的含量和性质, 而现有的研究主要集中在河流水质或FDOM性质的表征上, 对城镇河流FDOM荧光特性与水质之间关系还不清楚.因此, 本研究选取长三角快速城镇化典型城市近郊小流域—宁波市北仑区柴桥镇芦江水系为研究区域, 应用三维荧光光谱技术手段, 分析城镇化河流的FDOM组成结构特征, 揭示FDOM的空间分布规律, 阐述FDOM与水质指标的相关性, 以期为城镇化河流水质提升和FDOM的环境行为提供理论支撑.
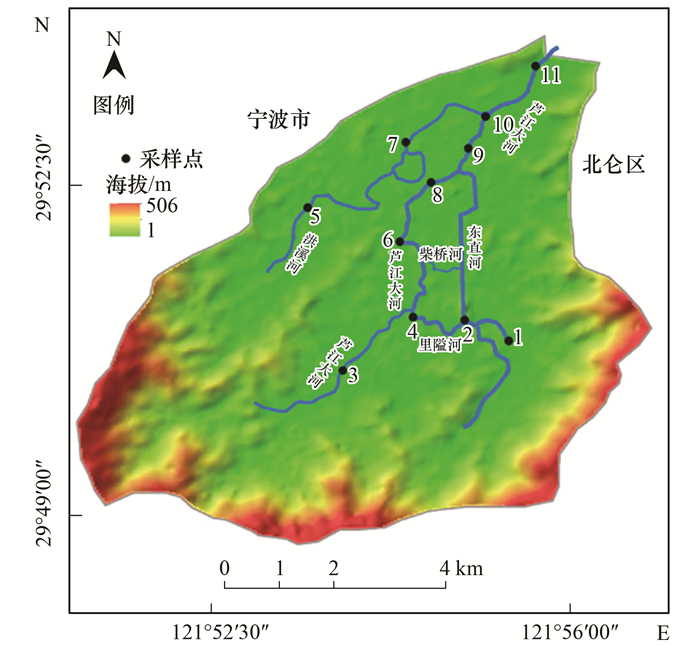
1 材料与方法 1.1 区域概况芦江水系位于浙江省宁波市北仑区柴桥镇, 主河道总长约9 km, 是柴桥镇境内最重要的排水河道.水系内河网密布, 交汇较多, 以南北流向的芦江大河为主河道, 共计4条支流汇入, 由上游至下游分别为里隘河、洪溪河、柴桥河、东直河, 具体分布见图 1.水系污染源分为两类, 上游以面源污染为主, 包括农业化肥施用、畜禽养殖污染等; 中游及下游以点源污染为主, 包括生活污染和工业污染.
|
图 1 采样点分布示意 Fig. 1 Distribution of the sampling sites |
2016年12月布置采样点如图 1所示, 分别在流域不同人类活动区域如农业区、生活区、工业区及无污染区域设置11个样点.其中1、6、7号为受人类活动影响较少的区域; 2、4、5号主要接纳农业污水; 3、8、9号汇入生活污水; 10、11号汇入工业废水.此外, 4号位于芦江大河与里隘河交汇处, 汇集了2、3号两个采样点的来水; 8号位于芦江大河与柴桥河交汇处, 以5、6号的来水及生活污水为主; 10号位于芦江大河与东直河的交汇处, 以上游来水及工业废水为主.
1.3 理化性质检测现场采用多参数数字化分析仪(美国哈希, HQ40D)测定盐度、pH、温度、溶解氧等; 所有水样经0.45 μm滤膜过滤后, 参照《地表水环境质量标准》(GB 3838-2002)进行其他物化指标的测量:采用离子色谱法(赛默飞, ICS-5000)测定Cl-、NO3-、NO2-、PO4-; 采用钼酸铵分光光度法测定TP; 采用TOC仪(德国Elementar, Vario TOC)测定溶解性有机碳(DOC)及TN; 采用流动分析仪(德国Seal, AA3)测定氨氮; 采用ICP-OES(美国PE, Optima 8300)测定Na、Ca; 采用ICP-MS(赛默飞, icap Q)测定Be、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Cd、Ba、Pb等的元素总量, 本文以3种含量较高的重金属Mn、As、Cr作为代表进行讨论.
1.4 荧光光谱检测溶解性有机质的三维荧光光谱采用荧光分光光度计(日立F-4600)测定, 主要程序为:狭缝宽度设置为5 nm, 激发波长(Ex)为220~450 nm, 扫描间隔5 nm; 发射波长(Em)260~600 nm, 扫描间隔1 nm; 扫描速度为2 400 nm·min-1; 以Milli-Q超纯水为实验空白.
1.5 荧光区域积分方法所有水样的三维荧光光谱在解析之前, 减去空白光谱并将发射波长等于激发波长与发射波长等于2倍激发波长包围外的区域光谱值赋值为零, 以修正拉曼散射、瑞利散射对光谱的影响, 再采用荧光区域积分法(FRI)对光谱进行定量分析[1].将光谱划分为5个区域, 其中Ex/Em=220~250/260~320 nm为区域Ⅰ; Ex/Em=220~250/320~380 nm为区域Ⅱ; Ex/Em=220~300/>380 nm为区域Ⅲ; Ex/Em=250~450/280~380 nm为区域Ⅳ; Ex/Em=300~450/>380 nm为区域Ⅴ, 具体分布见文献[1].利用Origin 8.0计算各荧光区域的积分体积Φi, 即为各区域有机物的荧光强度和; 对各区域的积分体积标准化, 即为各区域积分标准体积Φi, n, 代表各区域有机物的相对含量; 各区域积分标准体积占总积分标准体积的比例即为Pi, n.
1.6 数据分析利用SPSS 22.0对数据进行K-S检验、Pearson相关系数计算及层状聚类分析.采用Origin8.0分析处理数据, 采用Matlab进行三维荧光图谱绘制.
2 结果与讨论 2.1 区域水质参数特征芦江水系不同区域采样点各项水质参数见表 1.各采样点温度变化范围在13.0~15.8℃之间; pH平均值为6.63, 水样呈弱酸性.河水已存在轻度污染, 主要污染物为氮、磷、有机物.其中NH4+-N均低于1.5 mg·L-1符合Ⅳ类地表水质标准; TN、TP均值均超过Ⅴ类标准; 而在金属方面, As、Mn、Cr含量均符合Ⅰ类地表水质标准.从变异系数上看, NO2-和TOC变异系数最大, TP、As、TN、NH4+-N次之.
|
|
表 1 水质指标的统计特征 Table 1 Summary statistics of the measured water-quality variables |
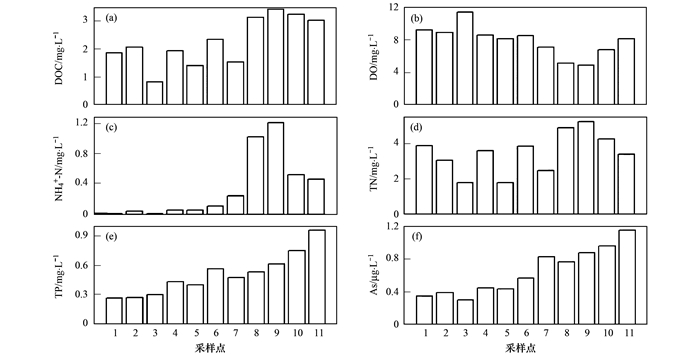
DOC、NH4+-N、TN、TP、As浓度均呈现上游低下游高的趋势(图 2).其中上游1~5号DOC均值为1.63 mg·L-1, 下游8~11号DOC均值为3.22 mg·L-1, 是上游均值的2倍; 8、9号主要排放源为生活污水, 其NH4+-N、TN浓度最高而DO最低, 表明河水因生活污水的排入而引起溶氧水平降低; 10、11号主要排放源为工业废水, TP和As达到峰值分别为0.96 mg·L-1及1.15 μg·L-1, 是上游均值的3.3及3.5倍, 表明工业废水的排入使得河水中磷、金属含量增加.上游1~5号排放源主要为农业污水, 8~11号排放源主要为生活及工业废水.综上所述上游与下游的水质参数差别, 表明农业污水对河水水质无显著影响, 人类活动产生的生活及工业废水引起了河水水质恶化.
|
图 2 各采样点水质参数 Fig. 2 Water quality parameters of the samples |
河水DOC分别与NH4+-N(r=0.81, P < 0.01)、TN(r=0.88, P < 0.01)、TP(r=0.72, P < 0.01)、Mn(r=0.81, P < 0.01)、As(r=0.76, P < 0.01)呈显著正相关, 与DO(r=-0.78, P < 0.01)呈显著负相关.一方面, 由于NH4+-N、TP是生活污水的典型成分, 表明河水中的DOC主要来源于排入河流的生活污水[20]; 另一方面, DOC含量和金属密切相关, 可能是由于FDOM与金属结合而影响了金属的迁移[21].
2.2 不同采样区域点位荧光光谱特征芦江水系各采样点的荧光光谱谱图类似, 主要为5个峰, 如图 3所示.其中Peak B(Ex/Em=220~235/280~320 nm)为类酪氨酸物质; Peak T1(Ex/Em=220~235/320~360 nm)为类色氨酸物质; Peak T2(Ex/Em=250~290/290~330 nm)为微生物代谢产物; Peak A(Ex/Em=220~235/380~440 nm)为紫外光区类富里酸物质; Peak C(Ex/Em=300~400/380~500 nm)为可见光区类富里酸物质[22].

|
图 3 各采样点水样三维荧光光谱 Fig. 3 EEM fluorescence spectra of the samples |
水质污染状况可由类蛋白荧光强度来表征[23, 24].由图 3可见, 芦江水系各样点由上游至下游, Peak B强度呈不断增大的趋势, 由1号的464.8增至11号的1 073.7, 表明河水中污染物浓度不断增加[15]; Peak T1强度增大且呈现出红移, 说明类色氨酸中羟基、羰基、羧基等含量逐步递增; Peak T2在1~6号为尖峰, 在7~11号中尖峰增强且出现了红移的肩峰, 表明下游微生物活性增强[4].
2.3 区域体积积分三维荧光区域的分区见图 3(b), 其中区域Ⅰ为类酪氨酸物质, 区域Ⅱ为类色氨酸物质, 两者均为类芳香蛋白物质; 区域Ⅳ为微生物代谢产物; 区域Ⅲ为紫外光区类富里酸物质, 区域Ⅴ为可见光区类富里酸物质[1].
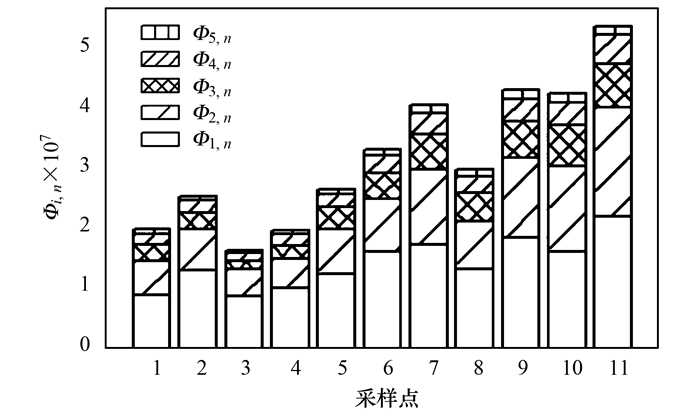
三维荧光区域的积分标准体积(Φi, n, i=1, 2, 3, 4, 5)可间接表征不同荧光组分的相对浓度[25].各区域积分标准体积见图 4, Φi, n均沿河递增, 表明以工业源为主的河水的FDOM中芳香碳含量最大, 生活源其次, 农业源最小[23].图 5为不同点位区域体积积分荧光响应值比例(Pi, n).在所有采样点位, 区域体积积分以类蛋白区域Ⅰ区和Ⅱ区所占比例较大, P1, n、P2, n、P4, n三者总和的变化范围为80.8%~88.9%, 可推出各采样点类蛋白含量较高, 对区域总积分的贡献率较大, 进一步表明生活污水及工业废水是FDOM主要来源之一[5]; P1, n与P2, n变动较大, 其中P1, n范围为38.1%~54.1%, 上游1~5号均值为50.1%, 下游8~9号均值为41.7%, 呈现出上游高下游低的趋势, P2, n则与P1, n相反, 上游低下游高, 这是由于随着污水的排入, 河水中类酪氨酸物质比例减少而类色氨酸物质比例增加, 微生物活跃水平呈现好氧与缺氧差异[23]; P3, n的变化范围为9.1%~15.7%, P5, n的变化范围为2.0%~3.8%, 表明腐殖酸类物质在FDOM中含量较低且相对稳定.
|
图 4 FDOM各组分相对丰度分布 Fig. 4 Distribution of the abundances of the FDOM components |

|
图 5 FDOM各组分百分含量分布 Fig. 5 Distribution of the percentages of the FDOM components |
为进一步研究河流FDOM的来源, 对各采样点的理化性质和荧光强度进行相关性分析.经K-S检验, 所选取的指标均满足正态分布(P>0.05), 采用Pearson相关性分析的结果见表 2.不同区域的积分标准体积(Φi, n, i=1, 2, 3, 4, 5)之间存在显著的相关性, 表明FDOM中的类蛋白物质与类腐殖质物质受到同一因素的影响[26].NH4+-N、亚硝态氮、TP、DOC的质量浓度与Φi, n呈显著正相关关系, 这与文献[27]的报道类似, 可推测FDOM与氮、磷的迁移和转换有关; 而Mn、As、Cr等金属浓度也与Φi, n呈显著正相关, 表明FDOM与金属存有潜在相关性; 已有多项研究中表明金属与FDOM结合而引起荧光猝灭[28, 29], 但也有研究证实Ca2+对荧光具有增强作用[30], 同时淬灭作用也与pH、基团浓度密切相关[28].
|
|
表 2 荧光强度与环境因子之间的相关关系 Table 2 Relationship between the fluorescence intensity and the environmental factors |
为进一步分析不同采样点水体中FDOM的差异性, 以6个光谱和12个水质数据为变量, 对11个采样点进行了聚类分析, 分析结果见图 6.

|
图 6 各采样点聚类分析结果 Fig. 6 Results of cluster analysis of the sampling sites |
在层次聚类分析中, 簇间距离不同会使得样品分类不同[31].如图 6所示, 依据上下游水质差异, 当欧几里得距离小于25时, 11个采样点分为两大类[32], 即上游1~5号采样点及下游6~11号采样点.第一类采样点1~5号均位于芦江大河上游, 该区域来水主要为自然补给水、农业源污水及少量生活污水, FDOM含量较低, 水质较好; 第二类采样点位于中下游, 该区域汇入生活污水及工业废水, 水质变差; 当欧几里得距离小于6时可划分为3个子类.第一个子类采样点位于芦江大河中游, 包括采样点6、7号, 具有水流量大, 汇集其他支流河水的特点, 该区域FDOM的差异来源于水体汇合及FDOM自身地化过程[33]; 第二个子类采样点位于支流柴桥河及东直河, 包括采样点8、9号, 该区域DOC浓度升高DO下降, T1峰出现红移且荧光强度比例上升, 是生活污水汇入的结果; 第三个子类位于芦江大河下游, 包含采样点10、11号, 该区域汇入了工业废水, TP含量持续增加, 金属元素如Mn、As、Cr也有小幅增加, 荧光总值达到了高峰.这一分类结果表明, FDOM的浓度及结构分布存在空间性, EEM结合FRI及聚类分析可进行有效解析.
3 结论(1) 利用三维荧光光谱结合多元统计解析了芦江水系FDOM的组分和结构.FDOM的主成分为类酪氨酸、类色氨酸、类溶解性微生物副产品、类富里酸物质, 其中类蛋白质在FDOM中占据主导地位.各组分呈现显著正相关, 说明各组分具有同源性.
(2) 分析了FDOM组成与水质的相关性.FDOM各组分与氮、磷、金属含量呈正相关, 表明FDOM与氮、磷的迁移转换相关, 而FDOM与金属的相关性涉及机制较复杂, 有待进一步研究.
(3) 芦江水系上游水质受人类活动影响较小, 下游水质则深受人类活动影响.下游FDOM组成与结构呈现城镇河段废水排放分布特征, FDOM随着含氮、磷的陆源排放而进入河流.
致谢: 感谢王瑞杰对文章中图片的润色给予的帮助.| [1] | Chen W, Westerhoff P, Leemheer J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. |
| [2] |
何伟, 白泽琳, 李一龙, 等. 水生生态系统中溶解性有机质表生行为与环境效应研究[J]. 中国科学:地球科学, 2016, 59(3): 341-355. He W, Bai Z L, Li Y L, et al. Advances in environmental behaviors and effects of dissolved organic matter in aquatic ecosystems[J]. Science China Earth Sciences, 2016, 59(4): 746-759. |
| [3] | Shi W, Jin Z F, Hu S Y, et al. Dissolved organic matter affects the bioaccumulation of copper and lead in Chlorella pyrenoidosa:a case of long-term exposure[J]. Chemosphere, 2017, 174: 447-455. DOI:10.1016/j.chemosphere.2017.01.119 |
| [4] |
于会彬, 高红杰, 宋永会, 等. 城镇化河流DOM组成结构及与水质相关性研究[J]. 环境科学学报, 2016, 36(2): 435-441. Yu H B, Gao H J, Song Y H, et al. Study on composition structure of DOM and its correlation with water quality in an urbanized river[J]. Acta Scientiae Circumstantiae, 2016, 36(2): 435-441. |
| [5] | Meng F G, Huang G C, Yang X, et al. Identifying the sources and fate of anthropogenically impacted dissolved organic matter (DOM) in urbanized rivers[J]. Water Research, 2013, 47(14): 5027-5039. DOI:10.1016/j.watres.2013.05.043 |
| [6] | Hosen J D, McDonough O T, Febria C M, et al. Dissolved organic matter quality and bioavailability changes across an urbanization gradient in headwater streams[J]. Environmental Science & Technology, 2014, 48(14): 7817-7824. |
| [7] |
孔赟, 朱亮, 吕梅乐, 等. 三维荧光光谱技术在水环境修复和废水处理中的应用[J]. 生态环境学报, 2012, 21(9): 1647-1654. Kong Y, Zhu L, Lv M L, et al. Research advances in water environment remediation and wastewater treatment based on three dimensional fluorescence spectroscopy technology[J]. Ecology and Environmental Sciences, 2012, 21(9): 1647-1654. |
| [8] |
傅平青, 刘丛强, 吴丰昌. 溶解有机质的三维荧光光谱特征研究[J]. 光谱学与光谱分析, 2005, 25(12): 2024-2028. Fu P Q, Liu C Q, Wu F C. Three-dimensional excitation emission matrix fluorescence spectroscopic characterization of dissolved organic matter[J]. Spectroscopy and Spectral Analysis, 2005, 25(12): 2024-2028. DOI:10.3321/j.issn:1000-0593.2005.12.031 |
| [9] | Yang L Y, Zhuang W E, Chen C T A, et al. Unveiling the transformation and bioavailability of dissolved organic matter in contrasting hydrothermal vents using fluorescence EEM-PARAFAC[J]. Water Research, 2017, 111: 195-203. DOI:10.1016/j.watres.2017.01.001 |
| [10] | Zeng Z, Zheng P, Ding A, et al. Source analysis of organic matter in swine wastewater after anaerobic digestion with EEM-PARAFAC[J]. Environmental Science and Pollution Research, 2017, 24(7): 6770-6778. DOI:10.1007/s11356-016-8324-3 |
| [11] | Hu H D, Ren H Q. Can fluorescence spectrometry be used as a surrogate for predicting the dissolved organic nitrogen and its bioavailable portion in wastewater effluents?[J]. Chemosphere, 2016, 164: 299-303. DOI:10.1016/j.chemosphere.2016.08.080 |
| [12] | Spencer R G M, Bolton L, Baker A. Freeze/thaw and pH effects on freshwater dissolved organic matter fluorescence and absorbance properties from a number of UK locations[J]. Water Research, 2007, 41(13): 2941-2950. DOI:10.1016/j.watres.2007.04.012 |
| [13] |
宋晓娜, 于涛, 张远, 等. 利用三维荧光技术分析太湖水体溶解性有机质的分布特征及来源[J]. 环境科学学报, 2010, 30(11): 2321-2331. Song X N, Yu T, Zhang Y, et al. Distribution characterization and source analysis of dissolved organic matters in Taihu Lake using three dimensional fluorescence excitation-emission matrix[J]. Acta Scientiae Circumstantiae, 2010, 30(11): 2321-2331. |
| [14] | Guo X J, He L S, Li Q, et al. Investigating the spatial variability of dissolved organic matter quantity and composition in Lake Wuliangsuhai[J]. Ecological Engineering, 2014, 62: 93-101. DOI:10.1016/j.ecoleng.2013.10.032 |
| [15] | He X S, Fan Q D. Investigating the effect of landfill leachates on the characteristics of dissolved organic matter in groundwater using excitation-emission matrix fluorescence spectra coupled with fluorescence regional integration and self-organizing map[J]. Environmental Science and Pollution Research, 2016, 23(21): 21229-21237. DOI:10.1007/s11356-016-7308-7 |
| [16] |
王桂新. 城市化基本理论与中国城市化的问题及对策[J]. 人口研究, 2013, 37(6): 43-51. Wang G X. The basic theory of urbanization and problems and countermeasures of China's urbanization[J]. Population Research, 2013, 37(6): 43-51. |
| [17] | Wang X, Li J Q, Li Y X, et al. Is urban development an urban river killer? A case study of Yongding Diversion Channel in Beijing, China[J]. Journal of Environmental Sciences, 2014, 26(6): 1232-1237. DOI:10.1016/S1001-0742(13)60593-8 |
| [18] |
王小娇, 胡国成, 张丽娟, 等. 广西刁江流域主要河流水质评价[J]. 生态科学, 2016, 35(6): 128-135. Wang X J, Hu G C, Zhang L J, et al. Water quality assessment of the Diaojiang River Basin in Guangxi[J]. Ecological Science, 2016, 35(6): 128-135. |
| [19] |
曹霏霏, 杨丽原, 庞绪贵, 等. 山东南四湖沉积物中汞的污染现状及迁移研究[J]. 环境科学, 2015, 36(5): 1615-1621. Cao F F, Yang L J, Pang X G, et al. Pollution status and migration of mercury in the sediments of Nansi Lake in Shandong Province[J]. Environmental Science, 2015, 36(5): 1615-1621. |
| [20] | Spencer R G M, Baker A, Ahad J M E, et al. Discriminatory classification of natural and anthropogenic waters in two U.K. estuaries[J]. Science of the Total Environment, 2007, 373(1): 305-323. DOI:10.1016/j.scitotenv.2006.10.052 |
| [21] | Xu H C, Yan Z S, Cai H Y, et al. Heterogeneity in metal binding by individual fluorescent components in a eutrophic algae-rich lake[J]. Ecotoxicology and Environmental Safety, 2013, 98: 266-272. DOI:10.1016/j.ecoenv.2013.09.008 |
| [22] | Stedmon C A, Markager S, Bro R. Tracing dissolved organic matter in aquatic environments using a new approach to fluorescence spectroscopy[J]. Marine Chemistry, 2003, 82(3-4): 239-254. DOI:10.1016/S0304-4203(03)00072-0 |
| [23] | Wang Z W, Wu Z C, Tang S J. Characterization of dissolved organic matter in a submerged membrane bioreactor by using three-dimensional excitation and emission matrix fluorescence spectroscopy[J]. Water Research, 2009, 43(6): 1533-1540. DOI:10.1016/j.watres.2008.12.033 |
| [24] | Sanchez N P, Skeriotis A T, Miller C M. A PARAFAC-based long-term assessment of DOM in a multi-coagulant drinking water treatment scheme[J]. Environmental Science & Technology, 2014, 48(3): 1582-1591. |
| [25] | Tang Z, Yu G H, Liu D Y, et al. Different analysis techniques for fluorescence excitation-emission matrix spectroscopy to assess compost maturity[J]. Chemosphere, 2011, 82(8): 1202-1208. DOI:10.1016/j.chemosphere.2010.11.032 |
| [26] | Fellman J B, Hood E, Spencer R G M. Fluorescence spectroscopy opens new windows into dissolved organic matter dynamics in freshwater ecosystems:a review[J]. Limnology and Oceanography, 2010, 55(6): 2452-2462. DOI:10.4319/lo.2010.55.6.2452 |
| [27] |
陈永娟, 胡玮璇, 庞树江, 等. 北运河水体中荧光溶解性有机物空间分布特征及来源分析[J]. 环境科学, 2016, 37(8): 3017-3025. Chen Y J, Hu W X, Pang S J, et al. Spatial distribution characteristics and source analysis of dissolved organic matter in Beiyun River[J]. Environmental Science, 2016, 37(8): 3017-3025. |
| [28] | Yamashita Y, Jaffé R. Characterizing the Interactions between trace metals and dissolved organic matter using excitation-emission matrix and parallel factor analysis[J]. Environmental Science & Technology, 2008, 42(19): 7374-7379. |
| [29] | Park J H. Spectroscopic characterization of dissolved organic matter and its interactions with metals in surface waters using size exclusion chromatography[J]. Chemosphere, 2009, 77(4): 485-494. DOI:10.1016/j.chemosphere.2009.07.054 |
| [30] |
傅平青, 刘丛强, 吴丰昌. 三维荧光光谱研究溶解有机质与汞的相互作用[J]. 环境科学, 2004, 25(6): 140-144. Fu P Q, Liu C Q, Wu F C. Three-dimensional excitation emission matrix fluorescence spectroscopic characterization of the complexation between Mercury(Ⅱ) and dissolved organic matter[J]. Environmental Science, 2004, 25(6): 140-144. |
| [31] | Jiang F H, Yang B J, Lee F S C, et al. Multivariate analysis of fluorescence and source identification of dissolved organic matter in Jiaozhou Bay, China[J]. Acta Oceanologica Sinica, 2009, 28(2): 60-72. |
| [32] | Wei Z M, Zhao X Y, Zhu C W, et al. Assessment of humification degree of dissolved organic matter from different composts using fluorescence spectroscopy technology[J]. Chemosphere, 2014, 95: 261-267. DOI:10.1016/j.chemosphere.2013.08.087 |
| [33] | Li P H, Lee S H, Lee S H, et al. Seasonal and storm-driven changes in chemical composition of dissolved organic matter:a case study of a reservoir and its forested tributaries[J]. Environmental Science and Pollution Research, 2016, 23(24): 24834-24845. DOI:10.1007/s11356-016-7720-z |
 2018, Vol. 39
2018, Vol. 39


