2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
低分子量的二元羧酸普遍存在于对流层的大气气溶胶中, 是气溶胶中重要的水溶性有机组分[1, 2].研究报道, 二元羧酸及其相关组分对北太平洋大气气溶胶中水溶性有机碳的贡献为4%~52%[3], 对太平洋中部大气气溶胶中总碳的贡献为16%[4].由于大气气溶胶中的二元羧酸能够改变颗粒物的吸湿性, 从而增强它们作为云凝结核的能力, 影响全球的能量平衡, 进而可能对区域和全球气候变化产生重要影响[5, 6], 因此, 有关大气气溶胶中二元羧酸的研究正在受到广泛关注.
乙二酸是大气气溶胶中二元羧酸的最主要组分[7], 其可以来自一次源和二次源的贡献.一次源包括汽车尾气、化石燃料燃烧、烹饪、生物质燃烧和海洋源等的排放[1], 二次源包括气相有机前体物光化学氧化生成的气态乙二酸在颗粒物上的凝结[8], 以及有机前体物在气溶胶水相中发生的化学氧化生成乙二酸[9, 10].气溶胶中乙二酸的去除主要通过湿沉降过程. Myriokefalitakis等[11]的模式研究显示, 全球尺度上湿沉降可去除大气中约62%的乙二酸, 干沉降去除的仅为4%, 其余34%是通过乙二酸在云中与OH和NO自由基反应去除.
青岛地处山东半岛东南部, 东南濒临黄海, 位于东亚陆源气溶胶向西北太平洋传输的重要通道上, 其大气气溶胶的理化性质同时受到陆源和海源的共同影响.本文利用2012年12月~2013年4月在青岛采集的总悬浮颗粒物样品(TSP), 分析其中乙二酸的浓度, 讨论了冬、春季青岛大气气溶胶中乙二酸的浓度分布特征及影响因素, 以期为认识近海大气中乙二酸对区域气候变化的影响奠定基础.
1 材料与方法 1.1 样品采集于2012年12月1日~2013年1月31日(冬季)及3月1日~4月31日(春季), 在青岛采集TSP样品共计119个, 每个样品的采集时间为12:00至次日的12:00.采集地点设在中国海洋大学鱼山校区达尔文馆楼顶(36°06′N, 120°33′E, 海拔约为65 m), 采样点附近无明显的工业污染源.采样仪器为KC-1000型大流量采样器(青岛崂山电子公司), 采样流量为1.05 m3·min-1.采样膜为预先酸洗过的Whatman41纤维滤膜, 采样结束后将滤膜对折, 放入洁净的聚乙烯封口袋中, 于-20℃冷冻保存直至分析.
采样同期, 记录中国气象局提供的3 h一次的Micaps天气资料, 包括温度、相对湿度、风速、风向、能见度和天气状况等, 太阳辐射数据从http://www.arl.noaa.gov下载.计算每个样品24 h采样周期中气象参数的平均值(风向为矢量平均值), 太阳辐射为每样品采集期间小时辐射数据积分求得的总辐射量.每个样品采集期间的天气状况以>70%的采样时间出现的天气状况计, 即样品采集时若>70%的采样时间内出现雾、霾或烟雾等天气时, 即标记为此样品受到该天气影响; 若采样期间有降雨, 即标记为受降雨影响; 沙尘样品的分类结合天气图资料(出现扬沙和浮尘)和观测数据(样品中代表地壳源的Fe和Al浓度超过10 000 ng·m-3)确定; 若样品采集期间两种或多种天气交替出现则记为混合样品; 未受特殊天气影响的样品标记为晴天(表 1).
|
|
表 1 采样期间受不同天气影响的样品数 Table 1 Number of samples affected by different weathers during sampling |
1.2 样品处理及分析
裁取一定面积的样品膜, 加入一定体积超纯水于冰水浴下超声萃取40 min, 将萃取液通过0.45 μm滤膜过滤后定容至100 mL, 滤液用来分析乙二酸和常量无机离子.同时, 裁取同批次的空白膜, 用相同方法得到空白样品滤液进行对比分析.采用ICS-3000离子色谱仪(美国戴安公司)进行分析, 阳离子(Na+、NH4+、K+、Mg2+、Ca2+)使用CS12A分析柱进行测定, 淋洗液为18 mmol·L-1的甲基磺酸(MSA), 流速为1. 00 mL·min-1.阴离子(F-、Br-、PO43-、Cl-、NO2-、NO3-、SO42-、乙二酸)使用AS11-HC分析柱进行测定, 淋洗液为KOH溶液, 梯度淋洗, 流速为1.20 mL·min-1.样品分析的详细过程和质量控制见文献[12].
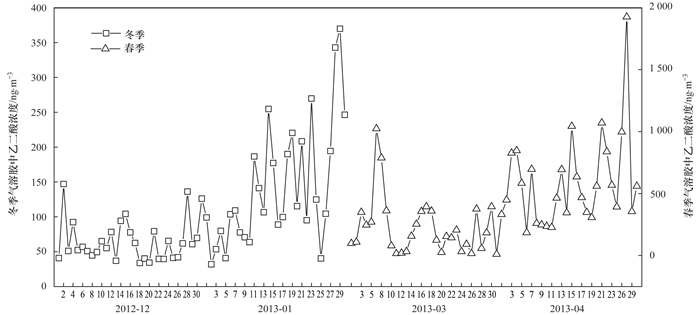
2 结果与讨论 2.1 青岛大气气溶胶中乙二酸的浓度分布特征2012年12月~2013年4月采样期间, 青岛大气气溶胶中乙二酸的浓度为11.1~1 925.9 ng·m-3, 平均浓度为(248.3±291.8)ng·m-3(图 1).冬季, 气溶胶中乙二酸的浓度为31.9~369.9 ng·m-3, 平均为(103.8±75.9)ng·m-3; 春季, 气溶胶中乙二酸的浓度为11.1~1 925.9 ng·m-3, 平均为(400.3±352.7)ng·m-3, 在统计意义上显著高于冬季(P < 0.05). Kundu等[13]在研究韩国济州岛大气气溶胶中乙二酸时也发现其存在春季(537 ng·m-3)高于冬季(349 ng·m-3)的季节变化趋势, 并解释这可能是不同季节乙二酸的来源和光化学过程不同的结果.青岛气溶胶中乙二酸的浓度明显低于印度新德里(1 431±990 ng·m-3)[14]和北京[白天(607±398)ng·m-3; 夜晚(806±604)ng·m-3][15]等污染城市的观测结果, 与韩国济州岛[13]和东海春季(397±374 ng·m-3)[12]的观测结果相近, 但明显高于西北太平洋[30°~45°N, (24.5±14.9) ng·m-3; 10°~30°N, (11.0±5.2) ng·m-3][3]和南大洋(2.4 ng·m-3)[4]等开阔大洋的观测结果.
|
图 1 冬、春季青岛大气气溶胶中乙二酸的浓度 Fig. 1 Concentrations of oxalate in the atmospheric aerosols collected from Qingdao during winter and spring |
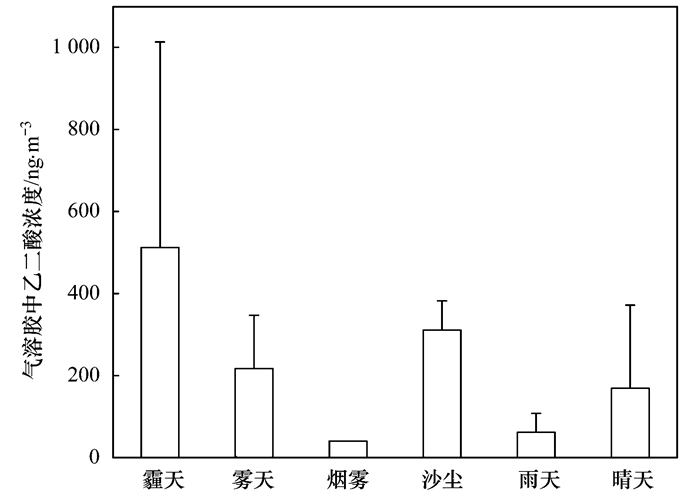
观测期间, 青岛多次出现雾、霾等特殊天气过程(表 1), 所以有机会比较不同天气下大气气溶胶中乙二酸的浓度分布.平均而言, 受霾天影响的样品中乙二酸浓度最高, 为(512.5±500.8)ng·m-3, 受沙尘影响的样品中乙二酸浓度也较高, 为(311.0±71.3)ng·m-3, 雾天和晴天采集的样品中乙二酸浓度相当, 分别为(217.4±129.5)ng·m-3和(169.1±202.5)ng·m-3, 受降雨和烟雾影响的样品中乙二酸的浓度最低, 分别为(62.1±46.0)ng·m-3和40.7 ng·m-3(图 2).统计分析显示, 受霾天影响的样品与晴天时的样品、受沙尘影响的样品与雨天时的样品中乙二酸浓度存在显著性差异(P < 0.05), 但雾天与雨天和晴天样品中的乙二酸浓度均无显著性差异.观测期间, 受烟雾影响的样品只有一个, 可能缺乏代表性, 所以对该样品不做讨论.受霾天影响的样品中乙二酸浓度最高, 这可能是由于霾天大气层结稳定, 风速较低易造成污染物积聚的缘故[16, 17], 尽管雾天时大气层结也稳定, 但雾天存在着一定的湿清除作用, 所以雾天时气溶胶中乙二酸的浓度低于霾天.受沙尘影响的样品中乙二酸浓度较高, 这是由于沙尘天时颗粒物浓度总体水平高, 而乙二酸可随沙尘颗粒一次排放或二次吸附在碱性沙尘颗粒上[18].受降雨影响的样品中乙二酸的浓度明显降低, 这是由于湿沉降的清除作用, 且雨天时太阳辐射低和生物源释放减少的缘故[7].
|
图 2 不同天气条件下青岛大气气溶胶中乙二酸的浓度 Fig. 2 Concentrations of oxalate in Qingdao atmospheric aerosols under different weather conditions |
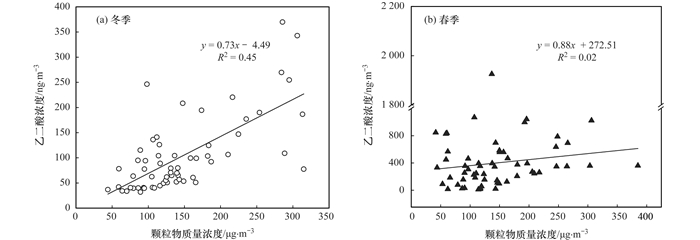
沙尘气溶胶中乙二酸的浓度明显高于雨天和晴天样品中的浓度(图 2), 表明颗粒物效应可能对气溶胶中乙二酸的浓度分布有一定影响.观测期间, 青岛大气气溶胶中乙二酸浓度春季显著高于冬季, 但比较冬、春季气溶胶中颗粒物的质量浓度发现二者基本相当, 平均浓度分别为(147.4±70.4) μg·m-3和(144.4±72.5) μg·m-3, 无显著性差异.比较气溶胶中乙二酸浓度与颗粒物质量浓度的关系(图 3), 发现冬季乙二酸浓度随颗粒物质量浓度增加而增加, 二者存在显著相关关系(P < 0.01), 但春季二者则无相关关系, 表明春季气溶胶中较高的乙二酸浓度不是颗粒物的累积效应造成的.
|
图 3 春季青岛气溶胶中乙二酸与颗粒物质量浓度的关系 Fig. 3 Relationship between oxalate and particle mass concentration in Qingdao aerosols during winter and spring |
进一步比较冬、春季大气乙二酸在单位质量颗粒物上的浓度(气溶胶中乙二酸的浓度与颗粒物质量浓度的比值), 发现春季乙二酸的浓度平均为3 448.6 μg·g-1, 显著高于冬季的709.6 μg·g-1(P < 0.05).与冬季相比, 春季乙二酸在颗粒物上有更大的负载, 这可能是由于春季有更适宜的反应条件促进了有机气态前体物反应生成乙二酸, 或者春季有更强的源强提供较多的反应前体物, 或者春季大气乙二酸有更强的一次源强. Laongsri等[8]的研究曾报道春季较强的光照水平和植物生长释放了更多的挥发性有机前体物, 增强了颗粒态乙二酸的二次生成, 且春季温度相比夏季低减少了乙二酸分配进入气相的比例, 这可能是造成与其他季节相比春季气溶胶中乙二酸浓度最高的原因. Guo等[19]也报道温暖季节气溶胶中乙二酸的浓度高于寒冷季节可能是由于温暖季节大气乙二酸的二次生成过程增强的缘故.
2.2.2 气象因素的影响观测期间, 青岛冬季温度明显低于春季, 平均分别为-0.6℃和7.2℃; 相对湿度冬季高于春季, 平均分别为68.1%和61.2%;风速冬、春季相当, 分别为4.2 m·s-1和4.3 m·s-1, 冬季主导方向为西北风, 春季主导风向为东南风和西北风; 太阳辐射量冬季平均为(10.2±2.2)MJ·m-2, 明显低于春季的(22.1±4.4)MJ·m-2.青岛大气气溶胶中乙二酸与气象因素的相关性分析结果显示(表 2), 冬、春季气溶胶中乙二酸和温度、太阳辐射量呈显著正相关关系, 表明温度和太阳辐射在乙二酸二次生成的光化学氧化过程中起重要作用[1].温度越高、光照水平越强越有利于乙二酸的二次生成[7, 8], 因此, 春季温度和太阳辐射显著高于冬季, 可能是造成春季青岛气溶胶中乙二酸浓度显著高于冬季的主要原因.冬季乙二酸与相对湿度呈显著正相关关系, 但春季二者无显著相关关系, 这表明冬季气溶胶中乙二酸的二次生成过程可能主要来自水相氧化过程, 而春季乙二酸的二次生成则以气相氧化过程为主导[20].冬季气溶胶中乙二酸与SO42-的相关关系(r=0.9)明显强于春季(r=0.5), 也支持了冬季气溶胶中的乙二酸主要来自液相氧化过程[12].冬、春季气溶胶中的乙二酸与能见度均呈显著负相关, 这是由于能见度越低, 表征大气层结越稳定, 易造成污染物的积聚.另外, 春季相比于冬季出现了更多的霾天和沙尘天、更少的雨天和雾天(表 1), 可能也是春季青岛气溶胶中乙二酸浓度显著高于冬季的原因.冬、春季节的主导风向不同, 冬季气溶胶主要受来自西北方向气团的影响, 春季同时受来自东南和西北方向气团的影响, 因此, 冬、春季节气溶胶中乙二酸浓度的差异还可能与其来源有一定关系.
|
|
表 2 青岛大气气溶胶中乙二酸与气象参数的皮尔逊相关系数1) Table 2 Pearson's correlation coefficient of particle oxalate and meteorological conditions in the Qingdao atmosphere |
2.2.3 气溶胶来源的影响
采用正矩阵因子分析法(positive matrix factorization, PMF)对青岛气溶胶的来源进行定量解析. PMF方法是当前一种有效的源解析方法, 已经广泛应用于PM2.5、TSP、干湿沉降以及VOCs等数据的源解析[21, 22].本文采用EPA PMF 3.0模型进行分析, 在分析中除考虑本文所测的乙二酸和Na+、NH4+、K+、Mg2+、Ca2+、Cl-、NO3-、SO42-等8种常量离子外, 还将样品中Fe、Al、V、Mn、Co、Cu、Zn、As、Sr、Cd、Ba、Pb、Ni等13种微量元素的分析结果[22]引入模型, 以便更好地对气溶胶的化学成分谱进行定量的来源解析.经过多次运行分析比较, 最终确定冬季和春季青岛气溶胶的来源均为受到6个因子的影响比较合理, 各组分模型模拟值与实测值基本一致, 除V、Mn、Sr、As的模拟值与实测值的相关系数为0.8~0.9外, 其他组分的相关系数均大于0.9, 模型模拟结果可以反映各组分的真实信息.
PMF解析结果显示, 冬季青岛大气气溶胶主要受到6个因子的影响(图 4).因子1中土壤源的代表性元素Fe和Al的载荷最大, 分别贡献了其总量的48%和68%, 其他主要来自土壤源的元素, 如Ca、Co、Mn、Ba、Sr也有较大载荷, 贡献了其总量的36%~49%, 因此, 判断因子1为土壤源; 因子2中海洋源的代表元素[23] Na+、Cl-和Mg2+的载荷最大, 分别贡献了其总量的52%、42%和32%, 而其他元素的载荷均较低, 因此因子2为海洋源; 因子3中Cu的载荷最大, 为其总量的52%, Cu常被认为是金属冶炼废气排放的标志性元素[24], 因此因子3确定为冶金工业源; 因子4中生物质燃烧的代表性元素[25] K+的载荷最高, 贡献了其总浓度的44%, 而代表土壤源的Al、Fe的载荷均较低, 因此因子4为生物质燃烧源; 因子5中Pb、Cd和Zn有较大载荷, 分别贡献了其总量的61%、55%和41%, Pb和Cd常被认为是机动车燃油排放的产物[24], Zn可来自于机动车润滑油、刹车片和轮胎的磨损[26], 因此确定因子5是机动车一次源; 因子6中NH4+、SO42-和NO3-有较大载荷, 分别贡献了其总量的50%、50%和48%, 这些离子主要来自大气中NH3、SO2、NOx等通过氧化反应、气-粒转化反应及颗粒物表面非均相反应等生成的二次反应产物[27], 因此, 确定因子6代表二次源.春季青岛大气气溶胶主要也受到6个因子的影响(图 5), 同理可以确定这6个因子分别为二次生成源、机动车一次排放源、生物质燃烧源、土壤源、冶金工业源和海洋源.

|
图 4 冬季青岛大气气溶胶PMF解析的源轮廓 Fig. 4 Source profiles of Qingdao aerosols in winter from PMF |

|
图 5 春季青岛大气气溶胶PMF解析的源轮廓 Fig. 5 Source profiles of Qingdao aerosols in spring from PMF |
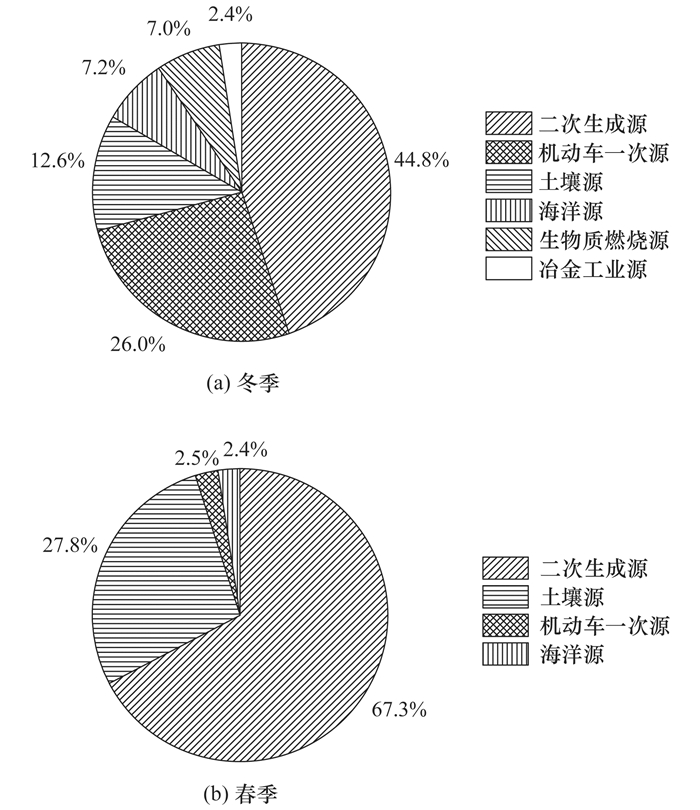
综上分析, 冬季和春季青岛大气气溶胶均受到二次生成源、机动车一次排放源、生物质燃烧源、冶金工业源、土壤源和海洋源等6个因子的影响.它们对冬季气溶胶中乙二酸的贡献以二次生成源的最大, 为44.8%, 其次是机动车一次源和土壤源, 分别贡献了26.0%和12.6%, 海洋源、生物质燃烧源和冶金工业源对青岛气溶胶中乙二酸的贡献较小, 分别为7.2%、7.0%和2.4%(图 6).对春季气溶胶中乙二酸的贡献, 也以二次生成源的贡献最大, 为67.3%, 其次是土壤源, 贡献了27.8%, 机动车一次源和海洋源各贡献了约2.5%, 生物质燃烧源和冶金工业源对春季气溶胶中乙二酸的贡献几乎可以忽略不计.由PMF源解析结果可知, 春季气溶胶中的乙二酸约70%来自二次生成, 冬季的约为45%, 这可能是春季大气中有更多乙二酸生物源前体物的贡献[8, 28], 且春季较高的温度和太阳辐射量为其二次生成过程提供了适宜的反应条件.春季土壤源对乙二酸的贡献较大, 有研究表明, 乙二酸与碱性沙尘气溶胶的中和反应可减少其分配进入气相的比例, 从而造成乙二酸在沙尘气溶胶上的富集[29].另外, Dutton等[30]和Gadd[31]的早期研究指出, 土壤中真菌的代谢作用可将柠檬酸和乙醛酸水解为草酰乙酸, 副产物可产生乙二酸盐, 因此, 土壤扬尘是大气粗颗粒中乙二酸盐的来源.观测期间受沙尘影响的两个样品均采集于春季(表 1), 这可能是春季气溶胶中乙二酸受土壤源贡献比例更大的原因.
|
图 6 不同源对冬、春季青岛大气气溶胶中乙二酸的贡献 Fig. 6 Contributions of different sources to oxalate in Qingdao aerosols during winter and spring |
(1) 青岛大气气溶胶中乙二酸的浓度冬季为(103.8±75.9)ng·m-3, 春季为(400.3±352.7)ng·m-3, 春季显著高于冬季.不同天气状况影响气溶胶中乙二酸的分布, 霾天时乙二酸浓度最高, 其次是沙尘天, 雾天与晴天时的基本相当, 雨天时气溶胶中乙二酸的浓度最低.
(2) 冬季气溶胶中乙二酸浓度与颗粒物浓度呈显著正相关, 表明其与颗粒物累积有一定的关系; 春季二者之间无显著相关关系, 但春季乙二酸在颗粒物上有更大负载.春季温度和太阳辐射显著高于冬季, 可能是造成春季乙二酸浓度显著高于冬季的主要原因.
(3) 冬、春季气溶胶中乙二酸与温度和太阳辐射均有显著正相关关系, 表明光化学氧化的二次生成过程对气溶胶中乙二酸有重要贡献, 其中冬季气溶胶中乙二酸的二次生成可能主要来自水相氧化过程, 春季的则可能主要来自气相氧化过程.
(4) 二次源是青岛大气气溶胶中乙二酸的主要来源, 其贡献冬季约为45%、春季约为70%.冬季气溶胶中乙二酸来自机动车一次源的贡献为26%, 土壤源、海洋源、生物质燃烧源的贡献各约为10%.春季土壤源的贡献约为30%, 其他源的贡献小于3%.
| [1] | Kawamura K, Bikkina S. A review of dicarboxylic acids and related compounds in atmospheric aerosols:Molecular distributions, sources and transformation[J]. Atmospheric Research, 2016, 170: 140-160. DOI:10.1016/j.atmosres.2015.11.018 |
| [2] | Kawamura K, Sakaguchi F. Molecular distributions of water soluble dicarboxylic acids in marine aerosols over the Pacific Ocean including tropics[J]. Journal of Geophysical Research:Atmospheres, 1999, 104(D3): 3501-3509. DOI:10.1029/1998JD100041 |
| [3] | Bikkina S, Kawamura K, Miyazaki Y. Latitudinal distributions of atmospheric dicarboxylic acids, oxocarboxylic acids, and α-dicarbonyls over the western North Pacific:Sources and formation pathways[J]. Journal of Geophysical Research:Atmospheres, 2015, 120(10): 5010-5035. DOI:10.1002/2014JD022235 |
| [4] | Wang H B, Kawamura K, Yamazaki K. Water-Soluble dicarboxylic acids, ketoacids and dicarbonyls in the atmospheric aerosols over the southern ocean and western pacific ocean[J]. Journal of Atmospheric Chemistry, 2006, 53(1): 43-61. DOI:10.1007/s10874-006-1479-4 |
| [5] | Kumar P P, Broekhuizen K, Abbatt J P D. Organic acids as cloud condensation nuclei:Laboratory studies of highly soluble and insoluble species[J]. Atmospheric Chemistry and Physics, 2003, 3(3): 509-520. DOI:10.5194/acp-3-509-2003 |
| [6] | Peng C G, Chan M N, Chan C K. The hygroscopic properties of dicarboxylic and multifunctional acids:Measurements and UNIFAC predictions[J]. Environmental Science & Technology, 2001, 35(22): 4495-4501. |
| [7] | Meng J J, Wang G H, Li J J, et al. Seasonal characteristics of oxalic acid and related SOA in the free troposphere of Mt. Hua, central China:Implications for sources and formation mechanisms[J]. Science of the Total Environment, 2014, 493: 1088-1097. DOI:10.1016/j.scitotenv.2014.04.086 |
| [8] | Laongsri B, Harrison R M. Atmospheric behaviour of particulate oxalate at UK urban background and rural sites[J]. Atmospheric environment, 2013, 71: 319-326. DOI:10.1016/j.atmosenv.2013.02.015 |
| [9] | Carlton A G, Wiedinmyer C, Kroll J H. A review of secondary organic aerosol (SOA) formation from isoprene[J]. Atmospheric Chemistry and Physics, 2009, 9(14): 4987-5005. DOI:10.5194/acp-9-4987-2009 |
| [10] | Ervens B, Turpin B J, Weber R J. Secondary organic aerosol formation in cloud droplets and aqueous particles (aqSOA):a review of laboratory, field and model studies[J]. Atmospheric Chemistry and Physics, 2011, 11(21): 11069-11102. DOI:10.5194/acp-11-11069-2011 |
| [11] | Myriokefalitakis S, Tsigaridis K, Mihalopoulos N, et al. In-cloud oxalate formation in the global troposphere:a 3-D modeling study[J]. Atmospheric Chemistry and Physics, 2011, 11(12): 5761-5782. DOI:10.5194/acp-11-5761-2011 |
| [12] |
陈诚诚, 石金辉, 周冰, 等. 东海大气气溶胶中二元羧酸的分布特征及来源[J]. 环境科学学报, 2013, 33(9): 2378-2387. Chen C C, Shi J H, Zhou B, et al. Distributions and sources of dicarboxylic acids in atmospheric aerosols over the East China Sea[J]. Acta Scientiae Circumstantiae, 2013, 33(9): 2378-2387. |
| [13] | Kundu S, Kawamura K, Lee M. Seasonal variations of diacids, ketoacids, and α-dicarbonyls in aerosols at Gosan, Jeju Island, South Korea:Implications for sources, formation, and degradation during long-range transport[J]. Journal of Geophysical Research:Atmospheres, 2010, 115(D19): D19307. DOI:10.1029/2010JD013973 |
| [14] | Miyazaki Y, Aggarwal S G, Singh K, et al. Dicarboxylic acids and water-soluble organic carbon in aerosols in New Delhi, India, in winter:Characteristics and formation processes[J]. Journal of Geophysical Research:Atmospheres, 2009, 114(D19): D19206. DOI:10.1029/2009JD011790 |
| [15] | He N N, Kawamura K, Okuzawa K, et al. Diurnal and temporal variations of water-soluble dicarboxylic acids and related compounds in aerosols from the northern vicinity of Beijing:Implication for photochemical aging during atmospheric transport[J]. Science of the Total Environment, 2014, 499: 154-165. DOI:10.1016/j.scitotenv.2014.08.050 |
| [16] | Zhao M F, Xiu G X, Qiao T, et al. Characteristics of haze pollution episodes and analysis of a typical winter haze process in Shanghai[J]. Aerosol and Air Quality Research, 2016, 16(7): 1625-1637. DOI:10.4209/aaqr.2016.01.0049 |
| [17] | Yu G H, Zhang Y, Cho S Y, et al. Influence of haze pollution on water-soluble chemical species in PM2.5 and size-resolved particles at an urban site during fall[J]. Journal of Environmental Sciences, 2017, 57: 370-382. DOI:10.1016/j.jes.2016.10.018 |
| [18] | Huang X F, Yu J Z, He L Y, et al. Water-soluble organic carbon and oxalate in aerosols at a coastal urban site in China:Size distribution characteristics, sources, and formation mechanisms[J]. Journal of Geophysical Research:Atmospheres, 2006, 111(D22): D22212. DOI:10.1029/2006JD007408 |
| [19] | Guo T F, Li K, Zhu Y J, et al. Concentration and size distribution of particulate oxalate in marine and coastal atmospheres-Implication for the increased importance of oxalate in nanometer atmospheric particles[J]. Atmospheric Environment, 2016, 142: 19-31. DOI:10.1016/j.atmosenv.2016.07.026 |
| [20] | Zhou Y, Huang X H, Bian Q J, et al. Sources and atmospheric processes impacting oxalate at a suburban coastal site in Hong Kong:Insights inferred from 1 year hourly measurements[J]. Journal of Geophysical Research:Atmospheres, 2015, 120(18): 9772-9788. DOI:10.1002/2015JD023531 |
| [21] | Wang L, Qi J H, Shi J H, et al. Source apportionment of particulate pollutants in the atmosphere over the Northern Yellow Sea[J]. Atmospheric environment, 2013, 70: 425-434. DOI:10.1016/j.atmosenv.2012.12.041 |
| [22] |
仇帅, 张爱滨, 刘明. 青岛大气总悬浮颗粒物中微量元素的含量特征及其来源解析[J]. 环境科学学报, 2015, 35(6): 1667-1675. Qiu S, Zhang A B, Liu M. Concentrations and origins of trace elements in the atmospheric total suspended particulates in Qingdao, China[J]. Acta Scientiae Circumstantiae, 2015, 35(6): 1667-1675. |
| [23] | Koçak M, Kubilay N, Mihalopoulos N. Ionic composition of lower tropospheric aerosols at a Northeastern Mediterranean site:implications regarding sources and long-range transport[J]. Atmospheric Environment, 2004, 38(14): 2067-2077. DOI:10.1016/j.atmosenv.2004.01.030 |
| [24] |
杨卫芬, 银燕, 魏玉香, 等. 霾天气下南京PM2.5中金属元素污染特征及来源分析[J]. 中国环境科学, 2010, 30(1): 12-17. Yang W F, Yin Y, Wei Y X, et al. Characteristics and sources of metal elements in PM2.5 during hazy days in Nanjing[J]. China Environmental Science, 2010, 30(1): 12-17. |
| [25] | Lim J M, Lee J H, Moon J H, et al. Source apportionment of PM10 at a small industrial area using Positive Matrix Factorization[J]. Atmospheric Research, 2010, 95(1): 88-100. DOI:10.1016/j.atmosres.2009.08.009 |
| [26] |
成海容, 王祖武, 冯家良, 等. 武汉市城区大气PM2.5的碳组分与源解析[J]. 生态环境学报, 2012, 21(9): 1574-1579. Cheng H R, Wang Z W, Feng J L, et al. Carbonaceous species composition and source apportionment of PM2.5 in urban atmosphere of Wuhan[J]. Ecology and Environmental Sciences, 2012, 21(9): 1574-1579. |
| [27] | Chan C K, Yao X H. Air pollution in mega cities in China[J]. Atmospheric environment, 2008, 42(1): 1-42. DOI:10.1016/j.atmosenv.2007.09.003 |
| [28] |
郭天锋, 朱玉姣, 于沛然, 等. 青岛城市大气气溶胶中乙二酸的粒径分布及其潜在气候效应[J]. 城市环境与城市生态, 2016, 29(4): 1-6. Guo T F, Zhu Y J, Yu P R, et al. Size distribution and potential climate effect of particulate oxalate in urban atmosphere of Qingdao City[J]. Urban Environment & Urban Ecology, 2016, 29(4): 1-6. |
| [29] | Sullivan R C, Prather K A. Investigations of the diurnal cycle and mixing state of oxalic acid in individual particles in Asian aerosol outflow[J]. Environmental Science & Technology, 2007, 41(23): 8062-8069. |
| [30] | Dutton M V, Evans C S. Oxalate production by fungi:its role in pathogenicity and ecology in the soil environment[J]. Canadian Journal of Microbiology, 1996, 42(9): 881-895. DOI:10.1139/m96-114 |
| [31] | Gadd G M. Fungal production of citric and oxalic acid:importance in metal speciation, physiology and biogeochemical processes[J]. Advances in microbial physiology, 1999, 41: 47-92. DOI:10.1016/S0065-2911(08)60165-4 |
 2018, Vol. 39
2018, Vol. 39


