2. 环境生物与控制教育部重点实验室(湖南大学), 长沙 410082;
3. 湖南省环境保护科学研究院, 长沙 410004
2. Key Laboratory of Environmental Biology and Pollution Control (Hunan University), Ministry of Education, Changsha 410082, China;
3. Hunan Research Academy of Environment Sciences, Changsha 410004, China
作为人类赖以生存的主要资源之一, 土壤是生态环境的重要组成部分, 但是近年来, 由于化工、采矿、冶炼等工业“三废”排放量增加、污水灌溉、肥料施用等原因, 土壤污染问题日益严峻, 严重影响了生态环境质量[1].重金属污染是土壤污染中的重要一类, 重金属不仅能影响植物的生长发育, 而且还能通过食物链的累积进入人体, 最终危害人体健康[2].常见的重金属污染土壤修复技术主要有物理修复、化学修复、生物修复等.其中原位钝化修复技术因其成本低廉、易于实施而受到广泛关注[3~5].目前常用的钝化剂主要有:磷矿粉、羟基磷灰石、过磷酸钙等磷酸盐; 石灰、粉煤灰等碱性材料; 生物污泥、腐殖酸、农家肥等有机材料以及复合类钝化剂[6~9].
磷酸盐是一类广泛应用于土壤重金属污染的钝化剂, 特别是对Pb的钝化效果较显著, 土壤中Pb的形态、磷酸盐的溶解性是制约磷酸盐钝化修复Pb污染土壤的重要因素[10], 易溶性磷酸盐钝化Pb的效果比难溶性磷酸盐好, 但施用易溶性磷酸盐又有造成地表水体富营养化的风险[11].腐殖酸具有丰富的活性功能基团, 能够影响土壤中重金属的活性[12], 还可以活化土壤中难溶性磷, 增加磷的有效性, 作为一种大分子有机聚合物, 它还起到改良土壤结构, 提高土壤肥力的作用[13].粉煤灰表面活性高且含有铁、锰等氧化物, 以其碱性特征和较强的吸附能力被用于钝化土壤中的重金属, 施用粉煤灰可以补偿施加酸性磷酸盐造成的土壤酸化作用, 还可以增加土壤有效磷含量, 并提供多种矿物元素, 进而促进植物的生长[14, 15].在实际环境中, 土壤重金属污染常为多种金属的复合污染, 施用单一的钝化剂难以达到理想的修复效果, 钝化剂配施可以取得较好的修复效果, 还能够克服单一钝化剂存在的问题[16], 而且当今农田土壤的修复, 不仅需要钝化重金属, 还要考虑土壤质量, 因此将腐殖酸、粉煤灰与磷酸盐联合钝化土壤重金属, 既能避免单独施用磷酸盐对土壤环境造成的不利影响, 又能增强对复合重金属污染土壤的修复效果, 还能肥土沃土, 改良土壤, 对农田重金属污染的修复治理具有一定的现实意义.
本研究采用Pb, Cd模拟污染土壤作为实验土壤, 主要进行以下4个方面的研究:①探讨不同钝化处理(腐殖酸、粉煤灰与过磷酸钙单独以及复配施用)对土壤pH值以及速效磷含量的影响; ②利用CaCl2浸取法、三乙三胺五乙酸(DTPA)浸取法和BCR形态分级实验研究不同钝化处理对模拟Pb、Cd污染土壤的钝化修复效果; ③利用Pearson相关矩阵对土壤pH值、土壤速效磷含量与CaCl2、DTPA提取态Pb、Cd含量之间以及土壤中Pb、Cd各形态含量之间进行相关性分析; ④利用X射线衍射仪(XRD)和扫描电子显微镜能谱(SEM-EDS)分析钝化前后土壤表面特征, 探讨钝化修复机制, 以期为腐殖酸、粉煤灰与磷酸盐配施钝化重金属复合污染土壤提供理论依据.
1 材料与方法 1.1 实验材料供试土壤:采自长沙市望城区一实验水稻田土壤, 采样深度为0~20 cm, 自然风干后过20目筛, 参考文献[17]测定其基本理化性质(见表 1).将分析纯试剂Pb(NO3)2、Cd(NO3)2以溶液形式加入到供试土壤中, 使土壤Pb、Cd含量分别达到2 500 mg·kg-1、5 mg·kg-1(国家土壤环境质量三级污染水平的5倍), 利用称重法加入去离子水以保持土壤60%的含水量, 室温条件下老化一个月后风干, 磨细过60目筛制成模拟Pb、Cd污染土壤.
|
|
表 1 供试土壤的基本理化性质 Table 1 Physical and chemical properties of the tested soil |
供试磷酸盐:过磷酸钙[Ca(H2PO4)2·H2O]购自国药集团化学试剂有限公司, 为分析纯化学药品.供试腐殖酸:实验所用腐殖酸为商品腐殖酸, 购自天津光复精细化工研究所, 为化学纯试剂, 主要成分为胡敏酸, 占总碳量的87.54%, pH:4.65, 总碳量:51.97%, 灰份:10%, 水份:< 8%, 含铁量 < 0.3%.供试粉煤灰:取自长沙某电厂, 过200目筛, pH:8.94, 比表面积:218 m2·kg-1, 烧失量:4.63%.
1.2 实验设计本实验共设8个处理组, 分别为:①对照组处理(CK); ②过磷酸钙单一处理(1号); ③腐殖酸单一处理(2号); ④粉煤灰单一处理(3号); ⑤过磷酸钙与腐殖酸复配施用处理(4号); ⑥过磷酸钙与粉煤灰复配施用处理(5号); ⑦过磷酸钙与腐殖酸、粉煤灰复配施用处理:3种钝化剂同时添加(6号); ⑧过磷酸钙与腐殖酸、粉煤灰复配施用处理:先添加过磷酸钙、腐殖酸钝化一周后再添加粉煤灰(7号); 每个处理重复3次.根据前期实验成果以及前人研究[18], 腐殖酸、粉煤灰施用量为土壤质量的3%, 过磷酸钙按照摩尔比P/(Pb+Cd)=4添加.具体实验步骤:称取风干的模拟Pb、Cd污染土壤100 g放入300 mL的塑料烧杯中, 将一定量的钝化剂与土壤充分混匀, 称重法保持土壤60%的含水量, 室温环境下培养1个月后取样, 自然风干磨细后过100目筛备用.
1.3 实验方法与数据分析 1.3.1 土壤pH值、速效磷含量以及CaCl2和DTPA浸取态Pb、Cd含量的测定土壤以及供试材料pH值用去离子水(土水比1:2.5)浸提, SHKF-431型pH计测定; 土壤速效磷含量用pH值为8.50的0.50 mol·L-1 NaHCO3浸提, EvolutionTM 300型分光光度计测定.
CaCl2浸取:取3 g备用土壤于50 mL离心管中, 加入30 mL 0.10 mol·L-1 CaCl2溶液, 振荡2 h, 离心分离, 过滤, 用NexLONTM 300Q型电感耦合等离子体质谱仪(ICP-MS, 美国PerkinElmer公司)测定上清液Pb、Cd浓度, 即为CaCl2浸取态Pb、Cd浓度.
DTPA浸取:取备用土壤10.00 g放入50 mL离心管中, 加入20 mL DTPA提取剂(其成分为:0.005 mol·L-1 DTPA、0.01 mol·L-1 CaCl2和0.10 mol·L-1 TEA-三乙醇胺, pH=7.30), 25℃下(180±20) r·min-1振荡2 h, 离心分离, 过滤, 滤液中的Pb、Cd用ICP-MS测定.
1.3.2 土壤Pb、Cd形态的测定采用改进的BCR三步提取法[19]测定土壤Pb、Cd各个形态的含量, 测定方法如下.
(1) 弱酸提取态 称取过100目筛风干土样0.50 g于50 mL离心管中, 加入25 mL 0.10 mol·L-1醋酸溶液, 25℃下连续振荡16 h, 在3 900 r·min-1下离心15 min, 过滤, 待测.再向残渣中加入20 mL去离子水, 振荡15 min, 在3 900 r·min-1下离心15 min, 倒掉上清液, 留下固体剩余物.
(2) 可还原态 向第一步剩余物中加入25 mL 0.50 mol·L-1盐酸羟胺溶液, 25℃下连续振荡16 h, 在3 900 r·min-1下离心15 min, 过滤后收集待测.同上水洗, 留下固体剩余物.
(3) 可氧化态 向剩余物中缓慢加入5 mL 30%H2O2, 在室温下放置1 h, 继续在(85±2)℃下水浴2 h.取出冷却后, 再加入25 mL 1mol·L-1 NH4OAc(用HNO3调节pH为2), 在25℃下连续振荡16 h, 在3 900 r·min-1下离心15 min, 过滤, 滤液待测.
(4) 残渣态 差减法.
1.3.3 土壤表面微观表征分析称取10.00 g土壤样品, 加入20 mL去离子水在摇床上充分摇动, 然后高速离心10 min, 移去上清液, 风干后过400目筛供X-射线衍射以及扫描电镜分析.采用D8 ADVANCE型X射线衍射仪(XRD, 德国BRUKER AXS公司)扫描土壤样品, 起始角度为10°, 终止角度为45°, 步长为0.02°, 扫描速度为2(°)·min-1.同时用EVO M10型扫描电子显微镜(SEM, 德国CARL ZEISS公司)扫描其表面形状, 并用X-MaxN型X射线能量色散谱(EDS, 英国Oxford公司)确定其表面元素组成.
1.3.4 数据处理与分析数据显著性检验以及Pearson(皮尔森)相关矩阵分析采用SPASS 22.0统计软件完成, XRD图谱物相鉴定和分析结果输出采用分析软件Jade 6.0完成, 所有制图采用Origin 16.0软件完成.
2 结果与讨论 2.1 不同钝化处理对土壤pH、速效磷含量的影响图 1是施加不同钝化剂处理后土壤pH值和速效磷含量.可以看出:与对照组相比, 单独施用腐殖酸和过磷酸钙会显著降低土壤pH值, 这可能是因为通常情况下, 腐殖酸具有弱酸特性, 可与土壤中的碱性物质发生中和反应, 而且能够与土壤中的各种阳离子结合, 对土壤酸碱度有较大的缓冲作用[20], 过磷酸钙作为一种酸性磷肥, 本身酸性较强, 能够酸化土壤; 单独施用粉煤灰处理的土壤pH值显著升高, 这可能是由于碱性材料粉煤灰能与酸性土壤黏粒或有机质中的羧基功能团相互作用, 消耗土壤溶液中的质子, 使土壤pH值提高[21]; 过磷酸钙与腐殖酸配施处理的土壤pH值显著降低, 与对照组相比, 降低了1.02个单位, 而与粉煤灰配施处理的土壤pH值增加了0.266个单位, 但是未达到显著水平; 3种钝化剂配施处理的6号与7号土壤pH值变化有所不同, 6号土壤pH值显著降低了0.53个单位, 而7号土壤pH值升高了0.05个单位, 未达显著水平, 这说明钝化剂的添加顺序不同对土壤pH值的影响也不一样.

|
柱状图上字母不同表示处理间差异显著(P < 0.05),字母相同表示差异不显著,Duncan检验,下同 图 1 不同钝化处理下土壤pH值以及速效磷含量 Fig. 1 The pH values and corresponding contents of available phosphorus under the different passivation processing conditions |
由图 1还可知, 施加不同钝化剂对土壤速效磷含量的影响也不同.与对照组相比, 单独施用过磷酸钙、腐殖酸、粉煤灰处理, 土壤速效磷的含量都显著增加, 含量分别为470.30、172.20、112.32 mg·kg-1, 过磷酸钙可以增加速效磷含量是因为它本身是一种微溶性磷肥, 为纯磷试剂, 腐殖酸、粉煤灰能够增加土壤速效磷含量是因为二者都能活化土壤中原有的固化磷[22, 23]; 过磷酸钙与腐殖酸、粉煤灰配施处理, 速效磷含量分别为716.6 mg·kg-1、504.8 mg·kg-1, 与单独施用过磷酸钙相比显著增加, 这是因为腐殖酸中含有多种官能团, 有较强的离子交换和吸附能力, 可以活化土壤中难溶性磷, 增加磷的有效性[22]; 有研究证明, 粉煤灰可以减少土壤对磷肥的固定, 提高磷肥的有效性[23]; 3种钝化剂配施处理的6号与7号土壤速效磷含量分别为618.4 mg·kg-1、903.16 mg·kg-1, 两者之间差异显著, 这可能是因为是3种钝化剂同时添加的6号土壤中, 酸性的腐殖酸与碱性的粉煤灰发生反应, 互相抑制, 导致对磷的活化作用降低.
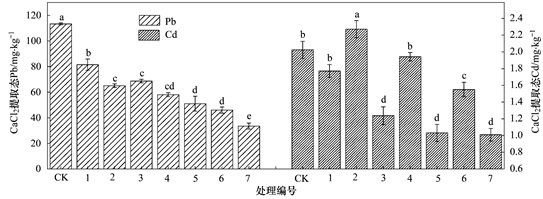
2.2 不同钝化处理对土壤CaCl2和DTPA提取态Pb、Cd含量的影响 2.2.1 CaCl2提取态Pb、CdCaCl2主要提取土壤中水溶态以及部分交换态的重金属, 这部分重金属在土壤中活性最强, 对动植物危害最大[24].从图 2可以看出, 与对照组相比, 单独施用过磷酸钙、腐殖酸、粉煤灰可分别使CaCl2提取态Pb质量分数降低28.09%、42.58%、39.42%, 过磷酸钙分别与腐殖酸、粉煤灰配施处理效果优于过磷酸钙单一处理, 降低率为48.82%、55.01%, 3种钝化剂配施处理的6号、7号土壤降低效果最佳, 分别降低了59.41%、70.44%.由图 2还可知, 与对照相比, 除了腐殖酸单一处理(2号)外, 其它钝化处理都能降低土壤CaCl2提取态Cd质量分数, 其中过磷酸钙与粉煤灰配施处理(5号)以及3种钝化剂配施处理(7号)效果最佳, 分别降低了49.02%、50.11%, 单独施用粉煤灰处理(3号)以及3种钝化剂配施处理(6号)效果次之, 降低率分别为38.90%、23.43%, 单独施用过磷酸钙(1号)以及过磷酸钙与腐殖酸配施处理(4号)分别降低了12.49%、4.07%, 而单独施用腐殖酸处理(2号)增加了12.23%.
|
图 2 不同钝化处理下土壤CaCl2提取态Pb、Cd含量 Fig. 2 Content of extractable Pb and Cd with CaCl2 under the different passivation processing conditions |
对农田土壤来说, 农作物对重金属的吸收情况直接关系到农产品的质量, 评价方法的选择更倾向于评价植物可给性, DTPA通常提取的是重金属水溶态、交换态、有机结合态的总和, 还包括部分氧化物和次生黏土矿物结合的重金属, 由于它们和植物生长最为密切, 最能代表重金属的植物可给性[25].
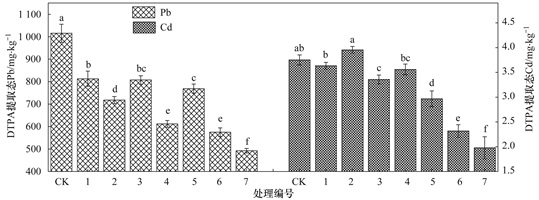
不同钝化剂处理下土壤DTPA提取态Pb、Cd含量见图 3.与对照组相比, 施用不同钝化剂都能显著降低DTPA提取态Pb含量, 其中3种钝化剂配施处理的6号和7号土壤降低效果最佳, 分别降低了43.37%、51.49%, 而且两者之间差异较显著; 过磷酸钙、腐殖酸、粉煤灰单独施用时, DTPA提取态Pb降低率分别为19.97%、29.29%、20.49%;过磷酸钙与腐殖酸、粉煤灰配施处理时, 则分别降低了39.74%、24.30%, 效果优于过磷酸钙单独处理.另外, 不同钝化剂对土壤DTPA提取态Cd含量变化的影响也不同, 与对照相比, 单独施用腐殖酸(2号)处理的DTPA提取态Cd增加了5.42%;而其他处理组DTPA提取态Cd都有所降低, 其中3种钝化剂配施的6号与7号处理效果最显著, 降低率分别为38.21%、47.27%, 单独施用过磷酸钙(1号)以及过磷酸钙与腐殖酸配施(4号)处理分别降低了3.15%、5.11%, 降低效果不显著, 单独施用粉煤灰(3号)以及过磷酸钙与粉煤灰配施(5号)处理则分别降低了10.53%、20.89%, 降低效果较显著.
|
图 3 不同钝化处理下土壤DTPA提取态Pb、Cd含量 Fig. 3 Content of extractable Pb and Cd with DTPA under the different passivation processing conditions |
由上述实验结果可知:施用不同钝化剂对土壤Pb、Cd的钝化效果不同, 总体来说钝化Pb的效果优于Cd, 过磷酸钙与腐殖酸、粉煤灰复配处理的效果优于过磷酸钙单独处理, 单独施用腐殖酸对Pb有钝化作用, 对Cd却有活化作用; 3种钝化剂配施处理对Pb、Cd的钝化效果最佳, 其中先添加过磷酸钙与腐殖酸再添加粉煤灰处理的效果优于同时添加3种钝化剂处理.
有研究表明, 磷酸盐可通过离子交换、表面络合、溶解/沉淀等机制钝化土壤重金属[26], 对于本研究所用的微溶性过磷酸钙, 其钝化重金属的效果主要受控于其溶解速度, 孙桂芳等[22]的研究表明, 腐殖酸可以通过交换吸附、螯合等作用活化土壤难溶性磷, 提高磷的有效性, 而且腐殖酸本身可以通过吸附、络合、氧化还原等作用钝化重金属, 但是由于Cd与腐殖酸形成的是弱配合物, 并且对固体表面亲和力很小, 因此添加腐殖酸会活化重金属Cd[27]; 粉煤灰表面积以及空隙较大, 对重金属有较强的吸附作用, 还含有较多铁、铝氧化物, 可以增加土壤对重金属的吸附点[28], 另外Rautaray等[23]的研究表明, 施用粉煤灰可以提高土壤中磷肥的有效性; 因此, 过磷酸钙与腐殖酸、粉煤灰配施钝化作用效果优于过磷酸钙单独施用的原因是:一方面是因为腐殖酸、粉煤灰本身也能够钝化重金属; 另一方面可能是腐殖酸、粉煤灰通过增强过磷酸钙的溶解来增强其对重金属的钝化作用.
另外, 含磷物质易与重金属特别是Pb形成磷酸盐沉淀, 并且当土壤中存在Cl-、F-等卤素离子时, 可以形成非常稳定的磷铅矿类物质Pb10(PO4)6X2(此处X为F、Cl、Br、OH), 反应式如下:
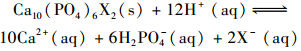
|
(1) |
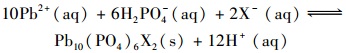
|
(2) |
从反应式(1)能看出, 酸性环境有助于含磷物质的溶解, 从反应式(2)可以看出, 随着反应的进行, 碱性环境将有助于消耗生成的H+, 从而促进生成稳定的磷酸铅盐.因此同样是3种钝化剂配施, 但7号处理效果明显优于6号处理可能是因为7号处理先添加过磷酸钙与腐殖酸, 产生的酸性环境以及腐殖酸本身可以促进过磷酸钙的溶解, 增加速效磷含量, 另外腐殖酸还能增加可溶性Cd离子的含量, 而后添加碱性的粉煤灰可以中和土壤中H+, 促进可溶性金属离子与速效磷反应生成稳定的磷酸盐, 降低重金属的活性.
2.3 土壤pH值和速效磷含量与土壤CaCl2和DTPA浸取态Pb、Cd含量的相关性分析对土壤pH值和速效磷含量与土壤CaCl2和DTPA浸取态Pb、Cd含量做Pearson相关矩阵分析, 结果如表 2所示.从中可以看出, 土壤pH值与CaCl2和DTPA浸取态Pb含量的相关系数仅为0.024和0.239, 而与CaCl2和DTPA浸取态Cd含量的相关系数为-0.786*(P < 0.05)、-0.409;速效磷含量与CaCl2和DTPA浸取态Pb含量的相关系数分别为-0.765*(P < 0.05)、-0.843**(P < 0.01), 与CaCl2和DTPA浸取态Cd含量的相关系数分别为-0.436、-0.716*(P < 0.05);另外土壤pH值与速效磷含量的相关系数为-0.148.分析结果表明, 土壤pH值与CaCl2和DTPA浸取态Pb含量存在正相关关系, 但是相关性不强, 这说明pH值不是控制土壤Pb活性的关键因素或者唯一因素, 这与王碧玲等[29]的研究一致; 土壤pH值与CaCl2和DTPA浸取态Cd含量存在负相关关系, 说明pH值可能是控制Cd活性的关键因素之一.另外, 速效磷含量与CaCl2和DTPA浸取态Pb、Cd含量都存在显著的负相关关系, 这说明土壤速效磷含量越高, 重金属Pb、Cd活性越低, 速效磷含量与土壤Pb、Cd的钝化效果直接相关, 这与王秀丽等[30]的研究结论一致.土壤pH值与速效磷含量呈负相关关系, 这说明土壤pH值可能通过影响磷基材料的溶解, 从而间接影响Pb、Cd的钝化效果.
|
|
表 2 土壤pH值和速效磷含量与土壤CaCl2和DTPA浸取态Pb、Cd含量的皮尔逊相关系数1)(n=8) Table 2 Pearson's correlation coefficient of soil pH values, contents of available phosphorus and contents of extractable Pb, Cd with CaCl2, DTPA(n=8) |
2.4 不同钝化处理对土壤Pb、Cd形态的影响 2.4.1 土壤Pb、Cd各形态
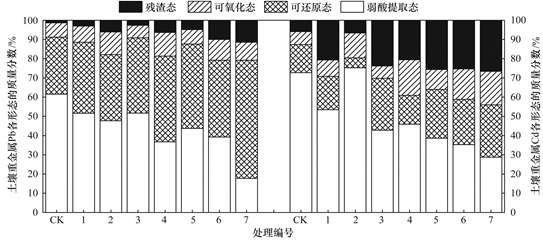
土壤中重金属的形态决定了它对生态环境的危害程度, 非残渣态(弱酸提取态、可还原态和可氧化态总和)比残渣态具有更高的生物有效性, 其中弱酸提取态活性最强, 起危害的主要作用, 残渣态最弱, 施用钝化剂可通过改变重金属的化学形态来减轻其对人体和生态环境造成的危害, 因此可以用形态分级方案来评价重金属污染土壤的钝化效果[31]. 图 4表示施用不同钝化剂对土壤Pb、Cd形态的影响.从中可以看出, 未处理土壤(CK)中Pb、Cd都主要以弱酸提取态存在, 所占质量分数分别为61.56%、72.72%, 弱酸提取态Cd所占质量分数大于Pb, 说明原土壤中Cd的活性大于Pb, 这可能是因为土壤颗粒对Pb的吸附性强于Cd[32]; 添加不同钝化剂之后, 与对照组相比, 土壤中弱酸提取态Pb显著降低, 其中3种钝化剂配施处理的7号处理组土壤降低幅度最大, 降幅达43.85%, 单独施用粉煤灰的3号处理组土壤降幅最小, 降幅仅为9.88%;另外, 除了3号处理组土壤中Pb的可氧化态有所减少, 其他处理组Pb的可还原态、可氧化态以及残渣态质量分数都有所增加, 其中活性最低的残渣态Pb增加1.29%~10.07%, 7号处理土壤增幅最大.与Pb不同, 添加不同钝化剂后, 单独施用腐殖酸(2号)处理的弱酸提取态Cd质量分数有所增加, 增幅为2.5%, 而其他处理组的弱酸提取态Cd质量分数都有所降低, 降幅为19.28%~44.00%, 同时2号处理的可还原态Cd质量分数有所降低, 其他处理组的可还原态Cd都有所增加, 增幅为0.38%~12.62%, 这可能是因为腐殖酸具有较强的络合作用, 将一部分可还原态Cd转化为腐殖酸-Cd弱配合物, 而这种配合物又不稳定, 所以导致活性较高的弱酸提取态Cd含量有所增加[27]; 另外, 所有处理组的残渣态Cd都有所增加, 增加了0.68%~20.70%, 7号实验处理组增幅最大.
|
图 4 不同钝化处理对土壤中重金属Pb、Cd形态的影响 Fig. 4 Effects of different passivation processing conditions on the speciation of Pb and Cd in the heavy metal contaminated soil |
以上结果说明, 钝化剂配施处理的修复效果优于钝化剂单一处理, 钝化剂复配处理能有效减少活性较高的弱酸提取态Pb、Cd含量而增加活性最低的残渣态含量, 其中先添加过磷酸钙和腐殖酸, 然后再添加粉煤灰处理效果最佳.
2.4.2 土壤Pb、Cd各形态含量相关分析对土壤Pb、Cd各形态含量之间做Pearson相关矩阵分析, 结果如表 3所示.结果显示, Pb的4个形态中弱酸提取态与可还原态和残渣态均呈极显著负相关关系, 相关系数分别0.949**和0.904**(P < 0.01);同样, 弱酸提取态Cd与可还原态Cd和残渣态Cd也均呈极显著负相关关系, 相关系数分别0.875**和0.973**(P < 0.01).这表明添加过磷酸钙、腐殖酸以及粉煤灰可以促进污染土壤中的Pb、Cd由活性高的弱酸提取态向活性较低的可还原态以及最稳定的残渣态转化, 从而有效降低Pb、Cd的可迁移性, 以达到钝化的目的.
|
|
表 3 土壤Pb、Cd各形态含量的皮尔逊相关系数(n=8) Table 3 Pearson's correlation coefficient of the contents of Pb and Cd for each speciation in soil (n=8) |
结合图 2~4可知, 3种钝化剂单一处理以及复配处理中, 以先添加过磷酸钙和腐殖酸, 然后再添加粉煤灰处理组效果最好, 其中不同钝化处理对Pb钝化效果排序为:先添加过磷酸钙和腐殖酸, 然后再添加粉煤灰处理>3种钝化剂同时添加处理>过磷酸钙与腐殖酸复配施用处理>腐殖酸单一处理>过磷酸钙与粉煤灰复配施用处理>粉煤灰单一处理>过磷酸钙单一处理, 对Cd钝化效果排序为:先添加过磷酸钙和腐殖酸然后再添加粉煤灰处理>3种钝化剂同时添加处理>过磷酸钙与粉煤灰复配施用处理>粉煤灰单一处理>过磷酸钙单一处理>过磷酸钙与粉煤灰复配施用处理>腐殖酸单一处理.
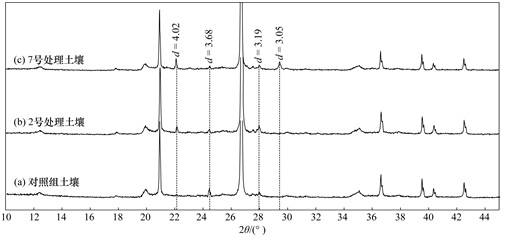
2.5 微观表征与分析X射线衍射仪(XRD)可以确定修复后土壤矿物物相, 从而揭示土壤钝化修复机制, 本研究对未处理对照组土壤(CK)、过磷酸钙单一处理(2号)土壤以及3种钝化剂复配处理(7号)土壤进行物相分析, 结果如图 5所示.结果显示, 原土壤的主要矿物相为SiO2、铁锰氧化物等, 过磷酸钙单一处理的2号土壤的XRD图谱和对照组土壤的十分相似, 但是在d=0.319 nm(2θ=27.89°)的峰明显加强以及在d=0.402 nm(2θ=20.90°)出现较强的额外峰, 通过物相鉴别以及根据Laperche等[33]的研究可以知道这两个峰分别代表Pb-Ca混合的磷酸盐以及Pb3(PO4)2, 这表明微溶性的过磷酸钙钝化Pb的机制可能是离子交换作用以及溶解/沉淀作用, 这与Raicevic等[34]的研究结果一致; 比较3种钝化剂配施的7号土壤与对照组土壤的XRD图谱可以看出7号处理土壤矿物结构与对照组相比没有明显变化, 但在d=0.402 nm(2θ=20.90°)处的峰明显加强, 此峰代表Pb3(PO4)2, 这一点说明过磷酸钙与腐殖酸、粉煤灰配施钝化Pb的主要机制是过磷酸钙的溶解从而形成难溶性的铅磷酸盐矿物; 此外, 在d=0.305 nm(2θ=29.23°)处出现了较强的额外峰, 物相分析表明此峰代表PbFe3(SO4)(PO4)(OH)6, 这可能是因为粉煤灰中的铁锰氧化物通过物理吸附等作用将铅磷酸盐矿物包裹而形成的低溶解性混合金属矿物; 另外7号以及2号处理土壤与对照组处理相比, 在d=0.368 nm(2θ=24.16°)处的峰强度有所减弱, 物相分析表明此峰代表Pb(CO3)2, 根据上节结论可以知道添加3种钝化剂可以将不稳定的铅碳酸盐转化为稳定的铅磷酸盐矿物, 从而降低其活性. Waterlot等[35]的研究说明重金属Cd的修复机制是以同构替换明显优于溶解沉淀, Cd2+通过阳离子交换替换Ca2+, 其主要原因可能是Cd2+的半径(0.097 nm)与Ca2+的半径(0.094 nm)非常接近, 而XRD图谱分析没有发现含Cd的矿物, 这可能是由于Cd本身含量比较少, 而且土壤中含量小于1%~2%的晶体矿物不能被XRD检测到, 或者是形成了新的无定型的非晶体金属矿物[11].
|
图 5 土壤钝化处理前后X射线衍射图谱 Fig. 5 XRD spectra of different soils before and after passivation treatments |
利用扫描电子显微镜能谱(SEM-EDS)对钝化前后的土壤进行扫描拍摄(图 6), 放大倍数均为5 000倍.分析结果显示, 与未钝化的土壤相比, 钝化1个月后的土壤表面更光滑, 其中7号实验处理组土壤表面更明显, 这可能是因为钝化形成的磷酸盐矿物晶体和其他未知晶体矿物在土壤颗粒上形成表面涂层而使表面显得光滑, 它们还可以将重金属离子包缚起来, 阻止重金属离子的浸出.另外EDS图谱(图 7)显示钝化后土壤表面的确出现了重金属Pb、Cd, 而且与对照组相比, 二者含量有所增大, 其中2号实验处理组土壤Pb、Cd含量最高, 7号实验处理组土壤表面P、Fe、Al等元素含量也有所增多, 因此综合本研究的实验结论可以说明单独施用过磷酸钙钝化土壤重金属的机制主要是通过离子交换或表面络合作用形成含有重金属的磷酸盐, 而3种钝化剂复配施用钝化重金属的机制主要是通过溶解/沉淀作用以及粉煤灰中铁锰氧化物表面的物理吸附作用将重金属转化为混合重金属含磷矿物, 这些产物都是具有较低溶解性以及迁移性的物质.

|
(a)对照组土壤;(b)2号处理土壤;(c)7号处理土壤 图 6 土壤钝化前后SEM图(×5 000) Fig. 6 SEM images of the as-prepared soils before and after passivation treatments (×5 000) |

|
图 7 土壤钝化前后EDS能谱图 Fig. 7 EDS energy spectra of the as-prepared soils before and after passivation treatments |
(1) 3种钝化剂单一以及复配处理中, 除了腐殖酸单一处理以外, 其他不同钝化处理都能降低土壤CaCl2和DTPA提取态Pb、Cd含量, 其中先添加过磷酸钙与腐殖酸, 然后再添加碱性粉煤灰的处理组效果最佳, 这是因为先添加过磷酸钙与腐殖酸能够降低土壤pH值, 而酸性环境以及腐殖酸可以促进过磷酸钙的溶解, 增加速效磷含量, 腐殖酸还能提高Cd的活性, 而后添加碱性的粉煤灰可以中和土壤H+, 有利于重金属离子与速效磷反应生成稳定的磷酸盐, 降低重金属的活性.,
(2) 土壤pH值不是控制土壤Pb活性的关键因素或唯一因素, 但是对Cd的活性会产生一定影响, 速效磷含量是控制土壤Pb、Cd活性的主要因素.
(3) 形态分析结果表明, 施用磷酸盐、腐殖酸以及粉煤灰可以促进污染土壤中的Pb、Cd由活性高的弱酸提取态向活性低的残渣态转化, 从而有效降低Pb、Cd的可迁移性和毒性, 以达到修复土壤的目的.
(4) XRD和SEM-EDS分析表明, 单独施用过磷酸钙钝化处理的作用机制主要通过离子交换作用将重金属转化为难溶的Ca-重金属混合磷酸盐, 而3种钝化剂配施的作用机制主要通过溶解/沉淀作用以及物理吸附作用将重金属转化为稳定的磷酸铅矿物沉淀[Pb3(PO4)2]和混合重金属矿物[PbFe3(SO4)(PO4)(OH)6], 降低重金属的溶解性以及迁移性从而有效钝化重金属.
| [1] |
李剑睿, 徐应明, 林大松, 等. 农田重金属污染原位钝化修复研究进展[J]. 生态环境学报, 2014, 23(4): 721-728. Li J R, Xu Y M, Lin D S, et al. In situ immobilization remediation of heavy metals in contaminated soils:a review[J]. Ecology and Environmental Sciences, 2014, 23(4): 721-728. |
| [2] |
陈朗, 宋玉芳, 张薇, 等. 土壤镉污染毒性效应的多指标综合评价[J]. 环境科学, 2008, 29(9): 2606-2612. Chen L, Song Y F, Zhang W, et al. Assessment of toxicity effects for cadmium contamination in soils by means of multi-indexes[J]. Environmental Science, 2008, 29(9): 2606-2612. |
| [3] |
曹心德, 魏晓欣, 代革联, 等. 土壤重金属复合污染及其化学钝化修复技术研究进展[J]. 环境工程学报, 2011, 5(7): 1441-1453. Cao X D, Wei X X, Dai G L, et al. Combined pollution of multiple heavy metals and their chemical immobilization in contaminated soils:a review[J]. Chinese Journal of Environmental Engineering, 2011, 5(7): 1441-1453. |
| [4] | Lee S H, Kim E Y, Park H, et al. In situ stabilization of arsenic and metal-contaminated agricultural soil using industrial by-products[J]. Geoderma, 2011, 161(1-2): 1-7. DOI:10.1016/j.geoderma.2010.11.008 |
| [5] |
龙新宪, 杨肖娥, 倪吾钟. 重金属污染土壤修复技术研究的现状与展望[J]. 应用生态学报, 2002, 13(6): 757-762. Long X X, Yang X E, Ni W Z. Current situation and prospect on the remediation of soils contaminated by heavy metals[J]. Chinese Journal of Applied Ecology, 2002, 13(6): 757-762. |
| [6] |
周航, 周歆, 曾敏, 等. 2种组配改良剂对稻田土壤重金属有效性的效果[J]. 中国环境科学, 2014, 34(2): 437-444. Zhou H, Zhou X, Zeng M, et al. Effects of two combined amendments on heavy metal bioaccumulation in paddy soil[J]. China Environmental Science, 2014, 34(2): 437-444. |
| [7] | Lee S H, Lee J S, Choi Y J, et al. In situ stabilization of cadmium-, lead-, and zinc-contaminated soil using various amendments[J]. Chemosphere, 2009, 77(8): 1069-1075. DOI:10.1016/j.chemosphere.2009.08.056 |
| [8] |
左继超, 高婷婷, 苏小娟, 等. 外源添加磷和有机酸模拟铅污染土壤钝化效果及产物的稳定性研究[J]. 环境科学, 2014, 35(10): 3874-3881. Zuo J C, Gao T T, Su X J, et al. Effect of phosphate and organic acid addition on passivation of simulated Pb contaminated soil and the stability of the product[J]. Environmental Science, 2014, 35(10): 3874-3881. |
| [9] |
何茂. 磷酸盐固定重金属污染土壤中Pb和Cd的研究[D]. 西安: 西安建筑科技大学, 2013. He M. Phosphate fixed heavy metal contaminated soil Pb and Cd[D]. Xi'an:Xi'an University of Architecture and Technology, 2013. http://d.wanfangdata.com.cn/Thesis/D375272 |
| [10] | Miretzky P, Fernandez-Cirelli A. Phosphates for Pb immobilization in soils:a review[J]. Environmental Chemistry Letters, 2008, 6(3): 121-133. DOI:10.1007/s10311-007-0133-y |
| [11] | Hettiarachchi G M, Pierzynski G M, Ransom M D. In situ stabilization of soil Lead using phosphorus and manganese oxide[J]. Environmental Science & Technology, 2000, 34(21): 4614-4619. |
| [12] | 陈慧, 蒋煜峰, 袁建梅, 等. 腐殖酸对污灌土壤中Cu、Cd、Pb、Zn形态影响的研究[M]. . |
| [13] |
王曰鑫, 侯宪文. 腐植酸对土壤中无机磷活化效应的研究[J]. 腐植酸, 2005(2): 7-14. Wang Y X, Hou X W. Study on humic acid activation of inorganic phosphorus in soil[J]. Humic Acid, 2005(2): 7-14. |
| [14] | Gupta A K, Singh R P, Ibrahim M H, et al. Fly ash for agriculture:implications for soil properties, nutrients, heavy metals, plant growth and pest control[A]. In:Lichtfouse E (Ed.). Agroecology and Strategies for Climate Change[M]. Dordrecht:Springer, 2012. 269-286. |
| [15] | Khandakar U R, Ganwar M S, Srivastava P C, et al. Effect of coal:fly ash application on the elemental composition and yield of some crops and on the properties of calcareous soil[J]. Acta Agronomica Hungarica, 1996, 44(2): 141-152. |
| [16] |
吴烈善, 曾东梅, 莫小荣, 等. 不同钝化剂对重金属污染土壤稳定化效应的研究[J]. 环境科学, 2015, 36(1): 309-313. Wu L S, Zeng D M, Mo X R, et al. Immobilization impact of different fixatives on heavy metals contaminated soil[J]. Environmental Science, 2015, 36(1): 309-313. |
| [17] | 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. |
| [18] | Cao R X, Ma L Q, Chen M, et al. Phosphate-induced metal immobilization in a contaminated site[J]. Environmental Pollution, 2003, 122(1): 19-28. DOI:10.1016/S0269-7491(02)00283-X |
| [19] | Nemati K, Abu Bakar N K, Abas M R, et al. Speciation of heavy metals by modified BCR sequential extraction procedure in different depths of sediments from Sungai Buloh, Selangor, Malaysia[J]. Journal of Hazardous Materials, 2011, 192(1): 402-410. |
| [20] |
陈静, 黄占斌. 腐植酸在土壤修复中的作用[J]. 腐植酸, 2014(4): 30-34, 65. Chen J, Huang Z B. Effect of humic acid on soil restoration[J]. Humic Acid, 2014(4): 30-34, 65. |
| [21] | Lombi E, Hamon R E, McGrath S P, et al. Lability of Cd, Cu, and Zn in polluted soils treated with lime, beringite, and red mud and identification of a non-labile colloidal fraction of metals using isotopic techniques[J]. Environmental Science & Technology, 2003, 37(5): 979-984. |
| [22] |
孙桂芳, 金继运, 石元亮. 腐殖酸和改性木质素对土壤磷有效性影响的研究进展[J]. 土壤通报, 2011, 42(4): 1003-1009. Sun G F, Jin J Y, Shi Y L. Advances in the effect of humic acid and modified lignin on availability to crops[J]. Chinese Journal of Soil Science, 2011, 42(4): 1003-1009. |
| [23] | Rautaray S K, Ghosh B C, Mittra B N. Effect of fly ash, organic wastes and chemical fertilizers on yield, nutrient uptake, heavy metal content and residual fertility in a rice-mustard cropping sequence under acid lateritic soils[J]. Bioresource Technology, 2003, 90(3): 275-283. DOI:10.1016/S0960-8524(03)00132-9 |
| [24] |
章明奎, 方利平, 周翠. 污染土壤重金属的生物有效性和移动性评价:四种方法比较[J]. 应用生态学报, 2006, 17(8): 1501-1504. Zhang M K, Fang L P, Zhou C. Evaluation of heavy metals bioavailability and mobility in polluted soils:a comparison of four methods[J]. Chinese Journal of Applied Ecology, 2006, 17(8): 1501-1504. |
| [25] | Lindsay W L, Norvell W A. Development of a DTPA soil test for zinc, iron, manganese, and copper[J]. Soil Science Society of America Journal, 1978, 42(3): 421-428. DOI:10.2136/sssaj1978.03615995004200030009x |
| [26] | Chrysochoou M, Dermatas D, Grubb D G. Phosphate application to firing range soils for Pb immobilization:the unclear role of phosphate[J]. Journal of Hazardous Materials, 2007, 144(1-2): 1-14. DOI:10.1016/j.jhazmat.2007.02.008 |
| [27] | Evangelou M W H, Daghan H, Schaeffer A. The influence of humic acids on the phytoextraction of cadmium from soil[J]. Chemosphere, 2004, 57(3): 207-213. DOI:10.1016/j.chemosphere.2004.06.017 |
| [28] | Ram L C, Masto R E. Fly ash for soil amelioration:A review on the influence of ash blending with inorganic and organic amendments[J]. Earth-Science Reviews, 2014, 128(1): 52-74. |
| [29] |
王碧玲. 含磷物质修复铅锌矿污染土壤的机理和技术[D]. 杭州: 浙江大学, 2008. WANG B L. Mechanism and technology of phosphorus-containing substance for remediation of lead-zinc mine contaminated soil[D].Hangzhou:Zhejiang University, 2008. http://d.wanfangdata.com.cn/Thesis/Y1483003 |
| [30] |
王秀丽, 梁成华, 马子惠, 等. 施用磷酸盐和沸石对土壤镉形态转化的影响[J]. 环境科学, 2015, 36(4): 1437-1444. Wang X L, Liang C H, Ma Z H, et al. Effects of phosphate and zeolite on the transformation of Cd speciation in Soil[J]. Environmental Science, 2015, 36(4): 1437-1444. |
| [31] | Zhu Y G, Chen S B, Yang J C. Effects of soil amendments on lead uptake by two vegetable crops from a lead-contaminated soil from Anhui, China[J]. Environment International, 2004, 30(3): 351-356. DOI:10.1016/j.envint.2003.07.001 |
| [32] | Rinklebe J, Shaheen S M. Assessing the mobilization of Cadmium, Lead, and Nickel using a seven-step sequential extraction technique in contaminated floodplain soil profiles along the central Elbe river, Germany[J]. Water, Air, & Soil Pollution, 2014, 225(8): 2039. |
| [33] | Laperche V, Logan T J, Gaddam P, et al. Effect of apatite amendments on plant uptake of Lead from contaminated soil[J]. Environmental Science & Technology, 1997, 31(10): 2745-2753. |
| [34] | Raicevic S, Perovic V, Zouboulis A I. Theoretical assessment of phosphate amendments for stabilization of (Pb+Zn) in polluted soil[J]. Waste Management, 2009, 29(5): 1779-1784. DOI:10.1016/j.wasman.2008.11.021 |
| [35] | Waterlot C, Pruvot C, Ciesielski H, et al. Effects of a phosphorus amendment and the pH of water used for watering on the mobility and phytoavailability of Cd, Pb and Zn in highly contaminated kitchen garden soils[J]. Ecological Engineering, 2011, 37(7): 1081-1093. DOI:10.1016/j.ecoleng.2010.09.001 |
 2018, Vol. 39
2018, Vol. 39


