2. 西安建筑科技大学陕西省膜分离重点实验室, 西安 710055;
3. 深圳市利赛环保科技有限公司, 深圳 518028
2. Key Laboratory of Membrane Separation of Shaanxi Province, Xi'an University of Architecture and Technology, Xi'an 710055, China;
3. Shenzhen Lisai Environment Protection Science and Technology Co., Ltd., Shenzhen 518028, China
厌氧消化是城市污水处理厂普遍采用的污泥处理技术之一[1, 2], 在实现污泥稳定化的同时, 可将污泥中所含生物质能以甲烷形式回收[3, 4].由于污泥经厌氧消化所产沼气中含有一定量的H2S(>1 000×10-6)[5, 6], 对设备会有一定的腐蚀性[7], 因此沼气在利用前需对其进行脱硫处理.而目前厌氧消化沼气脱硫技术存在成本高、操作复杂等缺点[8].国内、外针对沼气脱硫开展了大量试验研究[9, 10], 认为池内控制技术可有效降低沼气中的H2S含量以减轻后续处理负荷[11, 12], 实现沼气的低成本脱硫.
厌氧消化原位抑硫技术[13, 14]是指通过向消化池中投加氯化铁、磷酸铁或氧化铁等金属离子降低溶解态硫化物浓度, 以抑制沼气中H2S的生成, 常用的抑硫剂多为三氯化铁[15, 16].目前关于厌氧消化原位抑硫的研究多集中在抑硫效率等方面.戴前进等[17]的研究表明, 向中温厌氧消化污泥中投加一定量的FeCl3, 可有效降低H2S的产量. Díaz等[18]的研究发现, 向消化反应器中投加适量FeCl3可以降低沼气中H2S含量.王素春[19]对初沉污泥厌氧消化原位抑硫的技术特性研究表明, 当Fe/S为4.8(摩尔比)时, 沼气中H2S的含量由2 861×10-6降为272.9×10-6, 去除率为90.5%.污泥厌氧消化池采用原位抑硫技术可有效降低H2S浓度[20], 但存在药剂投加量大、仍需后续脱硫处理等缺点.虽然Fe(Ⅲ)的投加可实现原位抑硫, 但消化池的pH也会随之下降, 并促进溶解态硫化物转化为H2S[21, 22], 即Fe(Ⅲ)与pH存在相互影响相互制约的关系.因此, 研究Fe(Ⅲ)对溶解态硫化物的控制及Fe(Ⅲ)与pH交互作用, 对原位抑硫技术的工程应用具有重要意义.
高含固污泥厌氧消化工艺是近年来国内、外研究的热点[23, 24], 该工艺通过提升污泥含固率以实现污泥处理费用的大幅降低[25, 26].针对高含固污泥厌氧消化工艺进行原位抑硫研究发现, 向消化池投加一定量Fe(Ⅲ)后, 沼气H2S含量大幅下降, 说明该工艺具有应用原位抑硫技术的潜力.本研究通过分析不同Fe/S、pH下的高含固污泥厌氧消化原位抑硫效率及硫化物分布, 目的在于:探讨Fe(Ⅲ)原位抑硫技术特性; 分析Fe/S、pH对原位抑硫效率的影响; 描述pH及Fe/S的交互作用并建立Fe-H2S预测方程, 优化运行条件.
1 材料与方法 1.1 试验污泥污泥取自西安市某污水处理厂(采用工艺为A2/O)的剩余污泥, 脱水至含固率10%.其中一部分作为高含固污泥待用, 另一部分经过热水解预处理(165℃、50 min)作为热水解后高含固污泥待用.高含固污泥的主要指标为:SS 101.1 g·L-1、VSS 66.0 g·L-1、pH 6.93, 经过热水解预处理后高含固污泥的主要指标为:SS 65.60 g·L-1、VSS 37.7 g·L-1、pH 5.39.
试验接种污泥分别取自经过稳定运行200 d以上的高含固中温厌氧消化反应器和热水解预处理后高含固中温厌氧消化反应器的消化污泥.
1.2 试验装置本研究所用试验装置包括热水解预处理装置和厌氧消化试验装置.
热水解预处理装置由压力反应容器和加热装置组成.压力反应容器采用KH-200型不锈钢聚四氟乙烯内衬消解罐, 其工作温度<250℃, 工作压力<3 MPa.热水解加热装置为国华HH-S型油浴锅, 导热油为二甲基硅油, 热水解条件为165℃、50 min.
厌氧消化试验装置由恒温振荡器及厌氧消化反应瓶组成.恒温振荡器采用国华SHA-C型恒温振荡器, 水浴温度为35℃±1℃.厌氧消化反应瓶由反应瓶、集气瓶及气体体积测定瓶组成.反应瓶中污泥体积为100 mL, 采用排水集气法记录产气量.
1.3 测试指标及方法试验过程中指标的测定包括常规指标和硫化物指标的测定.
常规指标包括试验污泥的pH及沼气的气体组分. pH采用pH测定仪(上海精科PHS-3C)进行测定.沼气组分采用BEIFEN气相色谱仪(BEIFEN Corp.3420A)进行测定, 色谱柱为TDX-01填充柱, 柱温为80℃, FID检测器温度为100℃.
硫化物测定指标包括总硫化物、溶解态硫化物和H2S.总硫化物采用经酸化-吹脱法预处理的对氨基二甲基苯胺分光光度法进行测定, 溶解态硫化物采用经NaOH-乙酸锌预处理的对氨基二甲基苯胺分光光度法进行测定[27]. H2S采用气相色谱仪(Clarus PE 600)测定[28], 色谱柱为PoraPakQ填充柱, 柱温设为120℃, FPD检测器为350℃.
1.4 连续厌氧消化试验为了探究Fe(Ⅲ)投加对沼气中H2S含量及厌氧消化效率的影响, 本试验向连续运行的高含固污泥厌氧消化反应器进泥中混合FeCl3, 通过测定不同Fe/S下厌氧消化过程所产沼气中H2S的含量, 分析高含固污泥中温厌氧消化原位抑硫技术的抑硫效率以及确定最佳投加比例.各厌氧消化反应瓶(HRT=15 d、35℃±1℃)在接种污泥后, 每日投加含Fe(Ⅲ)高含固污泥, 运行2个周期后(30 d)开始记录产气量并测定沼气组分及H2S含量.
根据铁硫化学反应方程可知, 每生成1摩尔FeS所需的Fe/S为1.75, 所以1.75是理论投加率, 因此自1.75开始投加、步长为1, Fe/S的投加区间为0~7.75.当Fe/S为7.75时, FeCl3的最大投加量为1.48 g·L-1.
1.5 消化污泥Fe(Ⅲ)投加抑硫试验为了进一步分析Fe(Ⅲ)的原位抑硫特性, 选用污泥厌氧消化液作为Fe(Ⅲ)投加沉淀反应的试验环境进行Fe(Ⅲ)投加抑硫试验.通过投加Na2S·9H2O至高含固中温厌氧消化反应器排泥, 将消化液中溶解态硫化物浓度增至100 mg·L-1, 参照1.4节中Fe/S投加Fe(Ⅲ), 搅拌并静置30 min后, 测定溶解态硫化物浓度.
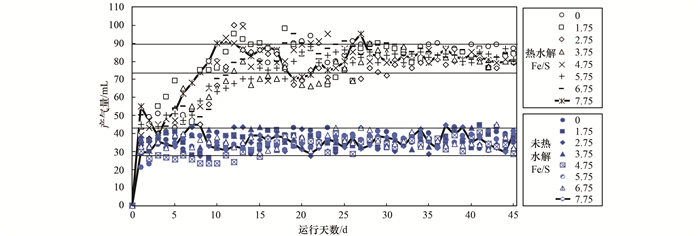
2 结果与分析 2.1 连续厌氧消化试验中Fe/S对产气量的影响通过对连续厌氧消化试验中不同Fe/S反应瓶产气量进行记录及甲烷含量测定, 分析Fe(Ⅲ)对厌氧消化效率的影响, 其日产气量见图 1.从中可知, 在各反应瓶进入稳定运行状态后(>20 d), 各组反应瓶产气量稳定并较为接近.随着Fe/S的变化, 高含固污泥厌氧消化及热水解-高含固污泥厌氧消化的日产气量分别稳定在30~45 mg·L-1和75~90 mg·L-1, 并未出现随着Fe/S的升高产气量急剧下降的现象, 即Fe(Ⅲ)投加对这两种工艺的日产气量影响较小.通过对气体组分的测定发现, 各组沼气中甲烷含量在60%~75%, 处于正常水平[29], 含Fe(Ⅲ)污泥的投加并未导致甲烷浓度大幅下降.
|
图 1 不同Fe/S下高含固污泥厌氧消化的日产气量 Fig. 1 Daily biogas production of high solid anaerobic digestion under different Fe/S ratios |
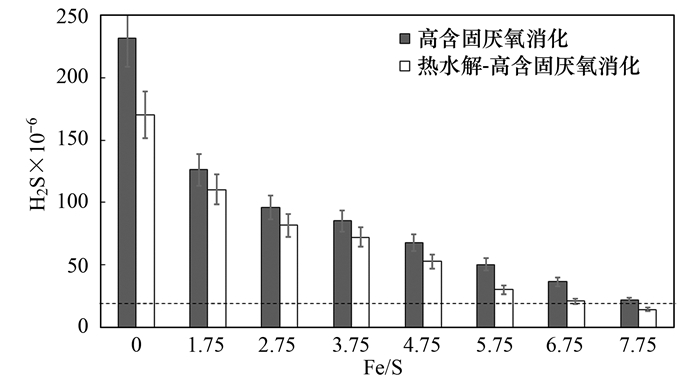
通过对不同Fe/S下热水解前、后含Fe(Ⅲ)高含固污泥厌氧消化抑硫效率进行研究, 分析高含固污泥原位抑硫技术的特性并探讨其应用潜力.含Fe(Ⅲ)高含固污泥和热水解后含Fe(Ⅲ)高含固污泥的中温厌氧消化装置在运行稳定后测定的H2S含量(体积分数)见图 2.
|
图 2 Fe/S对高含固污泥厌氧消化过程中H2S含量的影响 Fig. 2 H2S concentration of biogas during high solid anaerobic digestion under different Fe/S ratios |
由图 2可知, 无论是含Fe(Ⅲ)高含固污泥还是热水解后含Fe(Ⅲ)高含固污泥, 均可发现随着Fe/S的增加, 产气中H2S含量呈现不断降低的趋势.针对含Fe(Ⅲ)高含固污泥, Fe(Ⅲ)的投加导致沼气中H2S含量开始逐渐下降:投加前沼气中H2S含量为231.7×10-6; 在Fe/S为1.75~2.75范围内, Fe(Ⅲ)投加表现出了较高的抑硫效率, H2S抑制率达50%以上; 在Fe/S为2.75~7.75时, Fe(Ⅲ)的抑硫效率增幅开始放缓; 在Fe/S为7.75时, H2S含量为21.37×10-6, 略高于使用标准.
针对热水解后含Fe(Ⅲ)高含固污泥, Fe(Ⅲ)的投加导致沼气中H2S含量开始逐渐下降:投加前H2S含量为170.4×10-6; 当Fe/S由1.75上升至6.75时, 沼气中的H2S含量可降至20.74×10-6; 当进一步增加Fe/S至7.75时, 沼气中H2S浓度可降至14.09×10-6, 满足沼气利用标准.因此, 热水解后高含固污泥抑制H2S的最佳Fe/S为7.75, Fe(Ⅲ)的投加可有效降低沼气中H2S的浓度.
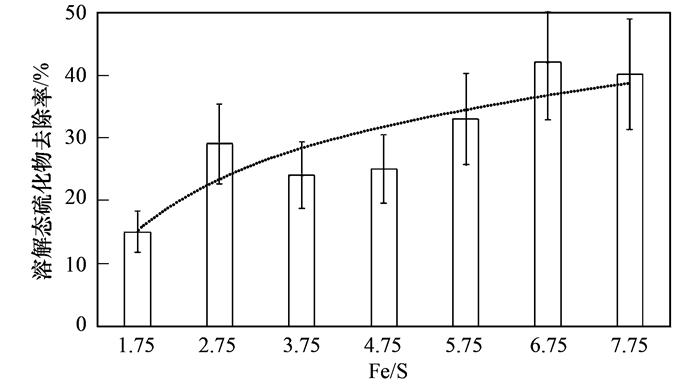
2.3 消化污泥Fe(Ⅲ)投加抑硫试验中Fe/S对溶解态硫化物的影响为了更好地理解Fe(Ⅲ)对溶解态硫化物的去除特性, 对不同Fe(Ⅲ)投加率下溶解态硫化物的去除率进行分析.通过测定平行投加试验中剩余溶解态硫化物的浓度, 并以未投加FeCl3的样品为基准计算溶解态硫化物去除率, 其结果见图 3.
|
图 3 Fe(Ⅲ)的投加对溶解态硫化物的去除 Fig. 3 Removal efficiency of sulfide for different Fe/S ratios |
由图 3可知, FeCl3的投加可有效降低溶解态硫化物浓度.在Fe/S由1.75增至2.75时, 其对应的溶解态硫化物去除率由15%增至29%, 约增加1倍.在Fe/S由2.75增至7.75时, 其对应的溶解态硫化物去除率由29%增至40%, 增加约0.4倍.可以发现随着Fe/S的逐渐增加, 溶解态硫化物去除率增加趋势缓慢, 即所投加的Fe(Ⅲ)并未被高效转化为硫化物沉淀.
3 讨论 3.1 原位抑硫各步转化率的拟合方程在对城市污水处理厂污泥厌氧消化Fe(Ⅲ)原位抑硫特性研究中发现, 不同Fe/S及pH下抑硫效果出现较大差异, 且抑硫效率与Fe/S并未呈现线性关系.为了探究Fe/S对H2S去除效率的影响, 对不同Fe/S、消化pH及碱度下的抑硫效率进行分析.通过对试验结果硫化物平衡核算发现, H2S/(S2-+ H2S)随着Fe/S的增加而增加.当消化池pH降低时, 虽然可转化为H2S的溶解态硫化物总量下降, 但溶解态硫化物会倾向于转化为H2S, 消化池pH的下降会导致抑硫效率下降.因此, 为了降低Fe(Ⅲ)的投加率及其对消化稳定性的影响, 需对Fe(Ⅲ)的投加过程进行进一步解析.
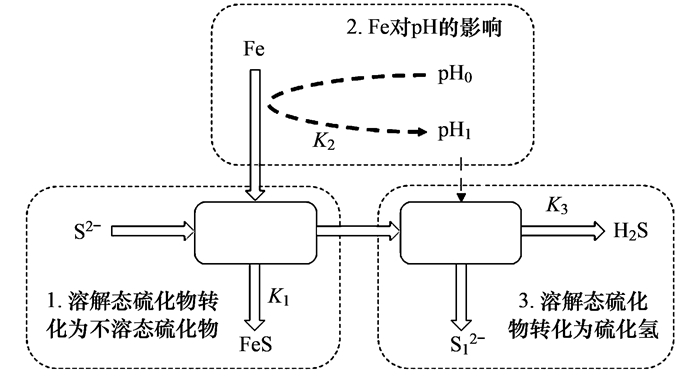
为了分析Fe(Ⅲ)投加对H2S生成规律的影响, 将原位抑硫过程分解为3个步骤(见图 4), 同时依据硫化物的转化过程, 结合图 1及图 2的数据, 拟合各步骤转化率方程, 拟合结果见表 1.
|
图 4 Fe(Ⅲ)原位抑硫中硫化物及Fe(Ⅲ)的转化过程 Fig. 4 Conversion of sulfide and Fe(Ⅲ) during in situ sulfur suppression |
|
|
表 1 原位抑硫各步转化率的拟合结果 Table 1 Fitting results for each step of the in situ sulfur suppression |
3.2 pH及Fe/S对抑硫效率的影响
为了探讨Fe(Ⅲ)投加对H2S生成的影响, 首先假设投加Fe(Ⅲ)对消化池的pH无影响, 即认为pH1与pH0相等.通过对Fe(Ⅲ)投加引起的H2S生成规律进行数学化描述, 建立在不考虑pH变化基础上的Fe-H2S预测方程, 其方程见式(1):
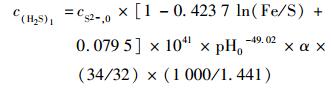
|
(1) |
式中, cS2-, 0为消化池初始硫化物浓度, mg·L-1; α为消化池产气率(以沼气/消化池计, 下同), α取0.5 m3·m-3; c(H2S)1为反应后H2S含量, ×10-6.
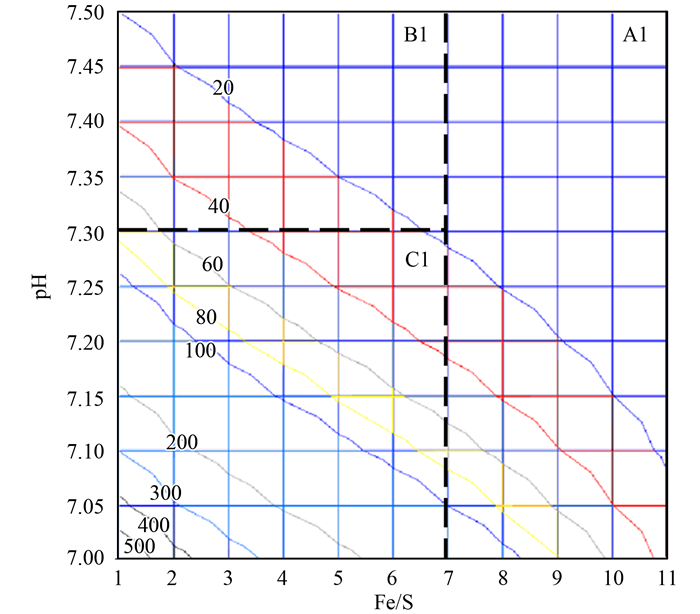
为了便于理解pH及Fe/S对抑硫效率的影响, 以cS2-, 0为1.0 mg·L-1、消化池产气率为0.5 m3·m-3、Fe/S为1~11、pH0为7.00~7.50时为例, 计算沼气中H2S浓度, 计算结果见图 5.
|
图 5 不同pH及Fe/S下沼气中H2S浓度 Fig. 5 Effects of pH and Fe/S on the H2S concentration of biogas |
对所有数据进行无重复双因素方差分析, 结果发现pH和Fe/S的F值均大于对应的Fcrit值, 即Fe/S和pH都对H2S的生成有影响, 且pH(F/Fcrit=17.40)较Fe/S(F/Fcrit=2.85)而言影响更显著.为了更好地模拟出在不同Fe/S变化下对生成H2S含量的影响, 对A1、B1、C1这3个变化区域再进行方差分析.通过对以上A1、B1、C1这3个区域的F和Fcrit值进行比较发现, 3个区域中所有的pH对应的F/Fcrit值均大于Fe/S对应的F/Fcrit值, 说明在这3个区域中pH是主要影响因素, 各分区的分析结果如下.
A1区:随着Fe/S的升高, Fe/S及pH的影响显著性逐渐下降, 出于对厌氧消化池稳定性及效率的考量, 不建议选择该区域进行原位抑硫.
B1区:Fe/S的F/Fcrit值相对最大(F/Fcrit=3.463 2), 由于Fe/S在实际操作中属于可控参数, 因此该范围最适宜于通过调节Fe/S来控制H2S的生成.
C1区:pH的F/Fcrit值最大(F/Fcrit=21.478 2), 即pH在这3个区域中影响最为显著.由于对不同城市污水处理厂污泥进行消化时, 达到稳定状态的pH各不相同, 因此在此区间内原位抑硫效果的稳定性无法保证, 当H2S浓度超标时难以通过技术手段控制.
由方差分析结果可知, 在pH为7.00~7.50、Fe/S为1~11范围内, pH均为主要显著影响因子, 因此提高消化池pH值将有利于大幅降低达到目标H2S含量所需的Fe(Ⅲ)投加量.
3.3 Fe-H2S预测方程对原位抑硫效果的优化试验过程中发现Fe(Ⅲ)的投加会导致消化池pH下降, 因此在实际原位抑硫工程中Fe/S的选定需考虑Fe(Ⅲ)对消化池的影响.为了分析Fe(Ⅲ)投加对H2S生成规律的影响, 建立考虑pH交互作用的Fe-H2S预测方程, 即可在已知溶解态硫化物浓度、消化池pH及单位消化池产气率的前提下预估不同Fe/S的原位抑硫效果.其方程见式(2):
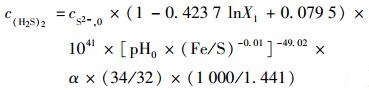
|
(2) |
式中, cS2-, 0为消化池初始硫化物浓度, mg·L-1; α为消化池产气率, α取0.5m3·m-3; c(H2S)2为反应后H2S含量, ×10-6.
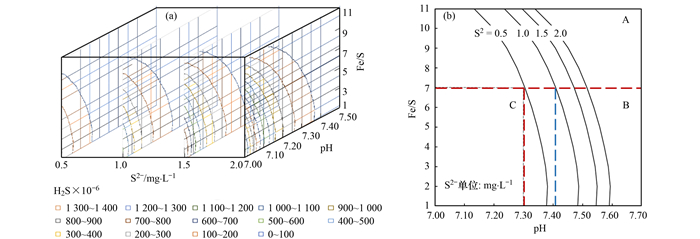
同样为了便于理解上述Fe-H2S方程, 以消化池产气率为0.5m3·m-3、cS2-, 0为0.5~2.0 mg·L-1、pH0为7.00~7.50、Fe/S为1~11时计算反应后H2S含量, 其结果见图 6(a).从中可知, 实现H2S达标排放的Fe/S随着消化池溶解态硫化物浓度以及pH的改变而改变.当溶解态硫化物浓度一定时, 消化池的pH越高, H2S达标排放所需的Fe/S越低.当pH一定的情况下, 溶解态硫化物浓度越低, 使H2S达标排放所需的Fe/S越低.为了探讨不同硫化物浓度下, pH变化对Fe/S的影响, 针对溶解态硫化物在0.5~2.0 mg·L-1时, 绘制H2S含量达标排放曲线(20.00×10-6), 其结果见图 6(b).由图 6(b)可知, 不同硫化物浓度下, 使得H2S达标排放需要的Fe/S不同.通过将投加区域分为A、B、C这3个区域进行分析, 结论可知, 在B区内可以通过调节Fe(Ⅲ)投加量来控制消化池H2S排放含量.各分区的分析结果如下.
|
图 6 Fe/S随pH和溶解态硫化物的变化关系图 Fig. 6 Relationship of Fe/S ratios with pH and dissolved sulfide |
A区:当消化过程中消化池pH低于7.30时, 可通过提高Fe/S使H2S含量达标.对于不同硫化物浓度而言, 随着其浓度的升高, H2S达标排放所需要的最低pH也随之升高.
B区:在消化池pH高于7.30时, 可通过调节Fe/S使H2S达标排放.由于Fe/S在实际操作中属于可控参数, 因此该范围最适宜于通过调节Fe/S来控制H2S生成含量.且在该区域内, 随着硫化物浓度的上升, H2S含量达标排放所需的Fe/S逐渐下降.
C区:该区内难以通过调节Fe/S来控制H2S的生成量, 因为C区中pH为影响H2S含量的显著影响因子.对于高含固污泥厌氧消化而言, 如果消化过程中pH一旦低于7.30, 将难以通过调节Fe/S实现H2S达标排放.
从4条硫化物浓度达标排放曲线的分布来看, 随着硫化物浓度等比例提高, H2S达标排放曲线越来越密, 即所需要投加的Fe(Ⅲ)的量并不与硫化物浓度的提高呈线性关系.高含固污泥厌氧消化的硫化物浓度一般在1.0 mg·L-1左右, 当消化池pH为7.40~7.50之间, 则要使H2S达标排放所需要的最适Fe/S为7.0.污泥厌氧消化过程中, 消化池的消化效果越好, 越适于采用原位抑硫技术.
4 结论(1) 经过热水解处理后的消化污泥, 在增加Fe/S至7.75时, 沼气中H2S含量可降至14.09×10-6, 满足沼气利用标准.
(2) Fe/S及pH对抑硫效率的影响分析结果认为, 在pH为7.00~7.50、Fe/S为1~11范围内pH均为主要显著影响因子, 因此, 提高消化池pH值将有利于大幅降低达到目标H2S含量所需的Fe(Ⅲ)投加量.
(3) Fe与pH的交互作用分析结果认为, 高含固污泥厌氧消化时沼气H2S达标排放所需要的最低Fe/S为7.0.若消化过程中pH一旦低于7.30, 将无法通过调节Fe/S实现沼气中H2S含量达标.
| [1] | Odnell A, Recktenwald M, Stensén K, et al. Activity, life time and effect of hydrolytic enzymes for enhanced biogas production from sludge anaerobic digestion[J]. Water Research, 2016, 103: 462-471. DOI:10.1016/j.watres.2016.07.064 |
| [2] | Yang G, Zhang P Y, Zhang G M, et al. Degradation properties of protein and carbohydrate during sludge anaerobic digestion[J]. Bioresource Technology, 2015, 192: 126-130. DOI:10.1016/j.biortech.2015.05.076 |
| [3] |
卓杨, 韩芸, 程瑶, 等. 高含固污泥水热预处理中碳、氮、磷、硫转化规律[J]. 环境科学, 2015, 36(3): 1006-1012. Zhuo Y, Han Y, Cheng Y, et al. Transformation characteristics of carbon, nitrogen, phosphorus and sulfur during thermal hydrolysis pretreatment of sludge with high solid content[J]. Environmental Science, 2015, 36(3): 1006-1012. |
| [4] | Neumann P, Pesante S, Venegas M, et al. Developments in pre-treatment methods to improve anaerobic digestion of sewage sludge[J]. Reviews in Environmental Science and Bio/Technology, 2016, 15(2): 173-211. DOI:10.1007/s11157-016-9396-8 |
| [5] | Appels L, Baeyens J, Degrève J, et al. Principles and potential of the anaerobic digestion of waste-activated sludge[J]. Progress in Energy and Combustion Science, 2008, 34(6): 755-781. DOI:10.1016/j.pecs.2008.06.002 |
| [6] | Ruan R J, Cao J S, Li C, et al. The influence of micro-oxygen addition on desulfurization performance and microbial communities during waste-activated sludge digestion in a rusty scrap iron-loaded anaerobic digester[J]. Energies, 2017, 10(2): 258. DOI:10.3390/en10020258 |
| [7] |
苏良湖, 张明珠, 张龙江, 等. 水合氧化铁对污泥厌氧消化过程的硫化氢控制[J]. 中国环境科学, 2017, 37(4): 1349-1357. Su L H, Zhang M Z, Zhang L J, et al. The removal of hydrogen sulphide by ferrihydrite during anaerobic digestion of sewage sludge[J]. China Environmental Science, 2017, 37(4): 1349-1357. |
| [8] | Maia D C S, Niklevicz R R, Arioli R, et al. Removal of H2S and CO2 from biogas in bench scale and the pilot scale using a regenerable Fe-EDTA solution[J]. Renewable Energy, 2017, 109: 188-194. DOI:10.1016/j.renene.2017.03.023 |
| [9] | Nägele H J, Steinbrenner J, Hermanns G, et al. Innovative additives for chemical desulphurisation in biogas processes:a comparative study on iron compound products[J]. Biochemical Engineering Journal, 2017, 121: 181-187. DOI:10.1016/j.bej.2017.01.006 |
| [10] | Desloover J, De Vrieze J, Van de Vijver M, et al. Electrochemical nutrient recovery enables ammonia toxicity control and biogas desulfurization in anaerobic digestion[J]. Environmental Science & Technology, 2015, 49(2): 948-955. |
| [11] | Manconi I, Lens P N L. Removal of H2S and volatile organic sulfur compounds by silicone membrane extraction[J]. Journal of Chemical Technology and Biotechnology, 2009, 84(1): 69-77. DOI:10.1002/jctb.v84:1 |
| [12] | Muñoz R, Meier L, Diaz I, et al. A review on the state-of-the-art of physical/chemical and biological technologies for biogas upgrading[J]. Reviews in Environmental Science and Bio/Technology, 2015, 14(4): 727-759. DOI:10.1007/s11157-015-9379-1 |
| [13] | Barelli L, Bidini G, Hernàndez-Balada E, et al. Performance characterization of a novel Fe-based sorbent for anaerobic gas desulfurization finalized to high temperature fuel cell applications[J]. International Journal of Hydrogen Energy, 2017, 42(3): 1859-1874. DOI:10.1016/j.ijhydene.2016.09.070 |
| [14] | McManus D, Martell A E. The evolution, chemistry and applications of chelated iron hydrogen sulfide removal and oxidation processes[J]. Journal of Molecular Catalysis A:Chemical, 1997, 117(1-3): 289-297. DOI:10.1016/S1381-1169(96)00254-3 |
| [15] |
聂玲. 初沉污泥厌氧消化及脱硫的实验研究[D]. 西安: 西安建筑科技大学, 2012. Nie L. Study on anaerobic digestion of primary sludge and desulfuration[D]. Xi'an:Xi'an University of Architecture and Technology, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10703-1012045831.htm |
| [16] | Unseld M, Szepanski C, Lindermeir A, et al. Desulfurization of biogas via dielectric barrier discharges[J]. Chemical Engineering & Technology, 2017, 40(2): 333-339. |
| [17] | 戴前进, 李艺, 方先金. 铁盐调质污泥厌氧消化产气降硫技术试验研究[J]. 给水排水, 2013, 39(5): 129-132. |
| [18] | Díaz I, Ramos I, Fdz-Polanco M. Economic analysis of microaerobic removal of H2S from biogas in full-scale sludge digesters[J]. Bioresource Technology, 2015, 192: 280-286. DOI:10.1016/j.biortech.2015.05.048 |
| [19] |
王素春. 利用Fe(Ⅲ)抑制污泥厌氧消化中硫化氢形成的研究[D]. 西安: 西安建筑科技大学, 2013. Wang S C. Inhibiting the formation of H2S in primary sludge digestion using wastes containing Fe(Ⅲ)[D]. Xi'an:Xi'an University of Architecture and Technology, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10703-1014010738.htm |
| [20] | Jiang H, Li T, Stinner W, et al. Selection of in-situ desulfurizers for chicken manure biogas and prediction of dosage[J]. Polish Journal of Environmental Studies, 2017, 26(1): 155-161. DOI:10.15244/pjoes/64909 |
| [21] | Osorio F, Torres J C. Biogas purification from anaerobic digestion in a wastewater treatment plant for biofuel production[J]. Renewable Energy, 2009, 34(10): 2164-2171. DOI:10.1016/j.renene.2009.02.023 |
| [22] | Dewil R, Baeyens J, Roels J, et al. Distribution of sulphur compounds in sewage sludge treatment[J]. Environmental Engineering Science, 2008, 25(6): 879-886. DOI:10.1089/ees.2007.0143 |
| [23] |
吴静, 王广启, 曹知平, 等. "热水解-高温厌氧消化"工艺处理高含固率剩余污泥的中试研究[J]. 环境科学, 2014, 35(9): 3461-3465. Wu J, Wang G Q, Cao Z P, et al. Pilot study of thermal treatment/thermophilic anaerobic digestion process treating waste activated sludge of high solid content[J]. Environmental Science, 2014, 35(9): 3461-3465. |
| [24] | Duan N N, Dong B, Wu B, et al. High-solid anaerobic digestion of sewage sludge under mesophilic conditions:feasibility study[J]. Bioresource Technology, 2012, 104: 150-156. DOI:10.1016/j.biortech.2011.10.090 |
| [25] |
戴晓虎, 何进, 严寒, 等. 游离氨调控对污泥高含固厌氧消化反应器性能的影响[J]. 环境科学, 2017, 38(2): 679-687. Dai X H, He J, Yan H, et al. Effects of free ammonia regulation on the performance of high solid anaerobic digesters with dewatered sludge[J]. Environmental Science, 2017, 38(2): 679-687. |
| [26] |
韩芸, 代璐, 卓杨, 等. 热水解高含固污泥的有机物分布及厌氧消化特性[J]. 环境化学, 2016, 35(5): 964-971. Han Y, Dai L, Zhuo Y, et al. Organic matter distribution and anaerobic digestion of thermal hydrolysis pretreated high-solid sludge[J]. Environmental Chemistry, 2016, 35(5): 964-971. DOI:10.7524/j.issn.0254-6108.2016.05.2015122202 |
| [27] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002. |
| [28] | Han Y, Zhuo Y, Peng D C, et al. Influence of thermal hydrolysis pretreatment on organic transformation characteristics of high solid anaerobic digestion[J]. Bioresource Technology, 2017, 244: 836-843. DOI:10.1016/j.biortech.2017.07.166 |
| [29] |
王治军, 王伟. 热水解预处理改善污泥的厌氧消化性能[J]. 环境科学, 2005, 26(1): 68-71. Wang Z J, Wang W. Enhancement of sewage sludge anaerobic digestibility by thermal hydrolysis pretreatment[J]. Environmental Science, 2005, 26(1): 68-71. |
 2018, Vol. 39
2018, Vol. 39

