2. 中国科学院生态环境研究中心, 中国科学院饮用水科学与技术重点实验室, 北京 100085
2. Key Laboratory of Drinking Water Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
饮用水源中抗生素的频繁检出使其成为威胁饮用水安全的隐患之一, 从而引起了广泛关注[1~3].其中, 诺氟沙星(NOR)因其具有广谱抗菌、副作用少、价格低廉等特点而被广泛应用于医疗领域, 而用药后的大量残留会随污水进入到周围环境中, 进而通过食物链富集作用危害人体健康.据统计, 我国的多处水源中均检测出NOR且含量相较于其它种类抗生素高很多[4], 因此, 去除水中的环境微量污染物是当前水处理领域一个亟待解决的问题.
相比其它水处理工艺, 吸附法因具有速度快、无二次污染、投资少等优点, 得以广泛应用[5~7].对于吸附技术而言, 吸附剂的开发一直是该方法的核心.在诸多吸附剂中, 树脂吸附因具有机械强度高, 适用范围宽、吸附效率高、化学稳定性高、易再生等优点, 在水处理领域日益受到人们的重视[8~10].然而, 目前大多数吸附树脂(苯乙烯系、丙烯酸系和乙烯吡啶系等)主要以石油资源为原料, 常用交联剂几乎都是二乙烯苯, 均有一定的毒性, 在环境中容易造成二次污染, 实际应用于饮用水处理领域中存在着潜在风险[11, 12].近年来, 对于“绿色”吸附剂的开发已成为水处理领域的研究热点之一.
我国松香资源丰富, 天然无毒, 属于天然可再生资源, 内部含有的三元菲骨架使其具有分子骨架大优点, 因此对其进行化学改性有着重要的应用价值.相比石油基系树脂, 松香基功能高分子聚合树脂因其原料来源丰富、绿色低毒等优点有望成为一类新型的吸附分离材料.目前, 松香基功能高分子聚合材料主要应用于中药成分的提取[13]、染料[14]、金属离子[15]的吸附去除领域, 而对水中抗生素的吸附去除研究尚未见报导.
本文基于前期研究, 以松香为原料进行Diels-Alder双烯加成反应获得交联剂, 并与功能单体聚合得到松香基大孔基体树脂, 在其骨架上修饰极性基团—氨基, 进而得到氨化松香基交联聚合树脂(aminated rosin-based resin, ARBR), 并分析其对水中诺氟沙星的吸附性能, 对其吸附的机制进行了探讨, 以期为拓展松香资源在环境微污染控制中的应用及开发新型水处理材料提供基础依据.
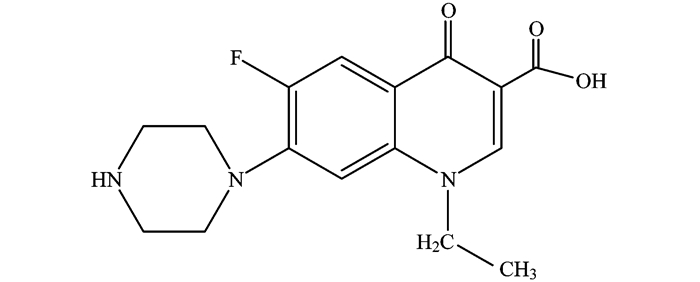
1 材料与方法 1.1 实验材料所有化学试剂均为分析纯试剂, 均购买于上海国药集团. NOR购于梯希爱(上海)化成工业发展有限公司, 分子结构式如图 1所示.实验用水由Millipore纯水器(Millipore公司, 美国)制备的超纯水. D001型大孔吸附树脂购于天津树脂厂. Amberlite XAD-1180、DAX-8、IRA410和IRC748树脂均购于Rohm & Haas公司.
|
图 1 诺氟沙星的分子结构式 Fig. 1 Chemical structure of NOR |
在前期研究的松香基树脂基础上进行氨基化改性得到新型的氨化松香基交联聚合树脂[16].所用ARBR用纯水100℃抽提24 h, 乙醇抽提72 h, 然后水洗至中性, 干燥, 保存备用.采用傅里叶变换红外光谱仪(Nicolet 5700, 美国)对ARBR、吸附NOR后的ARBR进行了化学结构官能团对比分析(用KBr压片, 波数范围是400~4 000 cm-1, 分辨率为4 cm-1); 对吸附剂的表面形貌结构采用扫描电子显微镜(Carl Zeiss SUPRA-55, 德国)进行观察; 使用全自动比表面积测定仪(Micromeritics ASAP2020M, 美国)测定ARBR的比表面积和孔径; 采用电位仪(Malvern Nano-ZS90, 英国)测定树脂的Zeta电位.
1.3 静态吸附-脱附实验分别准确称取一定质量经预处理的ARBR投加至50 mL分别含有不同质量浓度的NOR溶液中, 并用0.1 mol·L-1的NaOH或HCl溶液调节溶液的pH至预定值, 置于振荡器上150 r·min-1振荡24 h, 恒温20℃.对于吸附动力学实验, 在预定的时间内, 取样测定溶液中的NOR随时间的变化规律.吸附等温线实验中, NOR初始浓度范围0.5~200 mg·L-1, 温度分别设定为20、30、40和50℃.收集经吸附饱和的ARBR并置于30℃的烘箱被烘干, 并进行脱附再生实验, 加入50 mL脱附剂在25℃下静态脱附平衡后, 测定脱附溶液中NOR的浓度.为了检验ARBR的实际应用性能, 实际水样样品采自广西南宁的邕江、广西民族大学校内相思湖和实验室内自来水, 过0.45 μm滤膜, 4℃保存备用.
NOR在ARBR上的平衡吸附量qe(mg·g-1)通过式(1)计算:
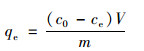
|
(1) |
式中, c0和ce分别为溶液中NOR的初始浓度和平衡浓度(mg·L-1), qe为ARBR的平衡吸附量(mg·g-1), V为溶液的体积(L), m为ARBR的投加量(g).
1.4 分析方法溶液中NOR浓度采用高效液相色谱仪在波长280 nm下测定(Agilent Technologies 1200, 美国)[17].水样的溶解性总有机碳(DOC)采用TOC仪进行测定(TOC-VCPN, 日本岛津公司).每个数据均取自两组平行实验数据的平均值.
2 结果与讨论 2.1 ARBR树脂表征图 2(a)和2(b)为ARBR的扫描电镜图, 从中可看出ARBR外观呈球状, 表面均一, 并拥有丰富的孔结构. ARBR的比表面积为10.65 m2·g-1, 平均孔径58.24 nm, 总孔体积为0.021 cm3·g-1.本研究还将吸附NOR前后的ARBR进行了红外谱图分析, 得到的红外光谱如图 2(c)所示. ARBR图谱中, 2 924 cm-1处是—CH2—拉伸特征峰, 位于1 715 cm-1处的峰是酯基中C=O的伸缩振动特征吸收峰[18].而位于1 174 cm-1和1 257 cm-1处的两个峰是C—O和C—N的伸缩振动的特征吸收.在3 100~3 700 cm-1间出现的宽频吸收峰被认为是N—H伸缩振动吸收峰[19, 20], 并且在1 634 cm-1和1 540 cm-1处的吸收分别为伯胺和仲胺的N—H的特征吸收峰, 这也证明了氨基基团已经成功引入到树脂的骨架上.对比ARBR吸附NOR后的FTIR谱图, 发现C=O特征吸收峰变强并且伯胺N—H的特征峰吸收减弱, 说明NOR在ARBR上的作用位点集中于伯胺基团.

|
(a) ARBR外观SEM图, (b)表面微观形貌SEM图, (c) ARBR红外光谱图 图 2 ARBR的SEM图及吸附前后的红外谱图 Fig. 2 SEM images of ARBR and FTIR spectra of ARBR before and after adsorption |
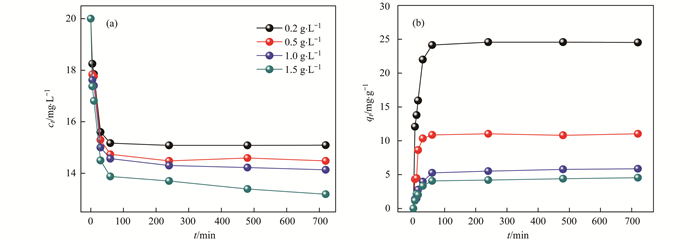
图 3为不同树脂投加量对吸附性能的影响, 及不同投加量对应单位吸附量随时间的变化. 图 3(a)表明, 相同的吸附时间内, 随着ARBR投加量的增加, 对NOR的吸附量逐渐降低.初始阶段, ARBR对NOR的吸附量随着时间的增加而明显增加, 但当60 min后, 吸附达到平衡.当吸附剂投加量由0.2 g·L-1增至0.5 g·L-1, ARBR对NOR的吸附量由24.15 mg·g-1降到了10.86 mg·g-1.当吸附剂投加量由1.0 g·L-1增加到1.5 g·L-1, 吸附量由5.26 mg·g-1减少到4.08 mg·g-1; 对于单位吸附量而言, ARBR对水中NOR的单位吸附量随着吸附剂投加量的增加而降低, 其原因为吸附剂投加量的增加会使吸附剂表面处于不饱和状态的吸附位增多.考虑到经济成本, 因此在后续研究中选取ARBR投加量为1.0 g·L-1.
|
实验条件:c0=20 mg·L-1, pH=6.0, T=20℃±1℃ 图 3 投加量对ARBR去除NOR效果的影响 Fig. 3 Effect of adsorbent dosage on the adsorption capacity on ARBR |
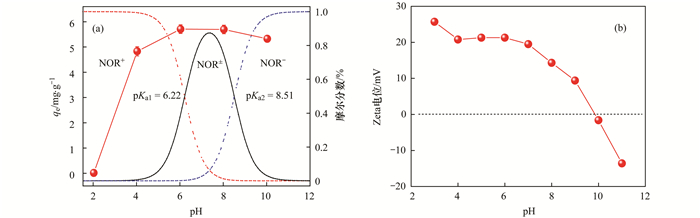
pH通常影响吸附质的存在形式及吸附剂的表面物理化学性质. 图 4分别为pH对NOR在ARBR上吸附量以及其Zeta电位的影响.由图 4(a)可知, 当pH值由2增加到6, 吸附量由0.01 mg·g-1增加至5.71 mg·g-1, 而pH由6增加到10, NOR的吸附量有所下降. NOR的pK值分别为6.22和8.51[21].当pH < 6.22时, NOR以NOR+(阳离子形式)的存在为主; 当溶液pH介于6.22~8.51之间时, NOR主要则以NOR±中性分子形式存在为主; 当pH>8.51时, NOR以NOR-(阴离子形式)存在为主[22]. ARBR的零电荷点(PZC)在9.8附近[图 4(b)].当溶液pH < 2.0时, ARBR表面的氨基会被质子化与带正电荷的NOR之间产生静电斥力, 阻止了它们之间的相互接触, 导致几乎没有NOR分子吸附在树脂上[21].随着pH的升高, 静电斥力逐渐减弱, NOR分子逐步扩散并通过静电吸引、氢键与氨基作用吸附在树脂表面[23].此外, 强酸条件下, 吸附剂和吸附质的氮、氧原子与酸中质子容易形成铵盐和盐, 降低了氮氧的给电子能力, 导致氢键作用力减弱而使吸附能力降低, 进一步说明氢键在吸附过程中起主要作用.
|
实验条件:c0=20 mg·L-1, ARBR投加量=1.0 g·L-1, T=20±1℃ 图 4 溶液pH对ARBR吸附NOR性能的影响和ARBR的Zeta电位 Fig. 4 Effect of solution pH on the adsorption of NOR on ARBR and the Zeta-potential of ARBR |
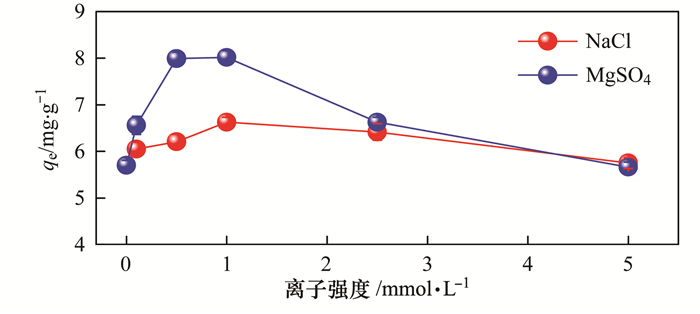
通过向NOR溶液中添加NaCl和MgSO4, 以考察ARBR对NOR吸附性能随离子强度的变化情况, 实验结果如图 5所示.从中可知, 当离子浓度小于1.0 mmol·L-1时, NOR的吸附量随着离子浓度的升高而增加; 当离子溶液浓度大于1.0 mmol·L-1时, 吸附量随着离子浓度增大而有所减少.因此, 共存离子溶液的存在对ARBR去除NOR的行为总体上表现为促进作用.而MgSO4相较于NaCl对NOR的吸附影响表现出更强的促进作用, 其原因可能是前者对NOR与水形成的氢键的破坏作用大于后者[22].
|
实验条件:c0=20 mg·L-1, pH=6.0, ARBR投加量=1.0 g·L-1, T=20±1℃ 图 5 离子强度对ARBR吸附NOR的影响 Fig. 5 Effect of ionic strength on the adsorption of NOR on ARBR |
吸附动力学是重要的吸附速率评价指标之一.由图 3(b)可见, 吸附过程分为两步, 即开始的快速吸附阶段和随后的缓慢吸附阶段.在吸附最初, ARBR对NOR的吸附速率较快, 吸附量迅速增加, 吸附时间在60 min时即可达到平衡.在吸附初期ARBR上的活性位点较多.随着吸附过程的进行, 可用于吸附的活性位点变少并且NOR溶液的浓度降低, 吸附推动力减弱致使吸附逐渐达到平衡.
为进一步理解吸附过程, 采用准一级动力学、准二级动力学模型及粒内扩散模型来拟合实验数据[17], 3种模式表达式如式(2)~(4)所示.
准一级动力学模型:
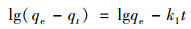
|
(2) |
准二级动力学模型:
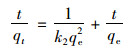
|
(3) |
Weber-Morris颗粒内扩散模型:
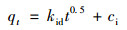
|
(4) |
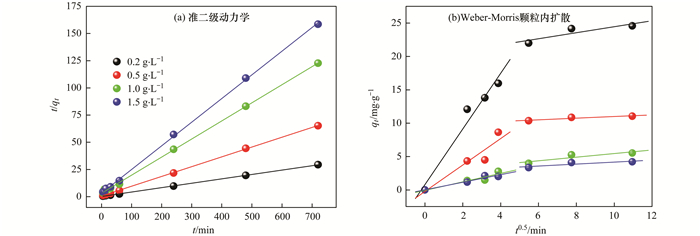
式中, qe和qt(mg·g-1)分别为平衡时和t时刻的吸附量;k1(min-1)为准一级动力学方程的吸附速率常数; k2[g·(mg·min)-1]为准二级动力学的吸附速率常数; kid[mg·(g·min0.5)-1]为内扩散速率常数, 截距ci为与吸附剂表面特性有关的常数.相关模型的拟合参数见表 1, 从中可见, 与准一级动力学模型相比, 准二级动力学模型对实验数据的拟合相关性系数较高(R2﹥0.99), 并且由计算得到的qe, cal值和由实验确定的吸附值比较接近.所以, 准二级动力学模型能更好地描述ARBR对水中NOR的吸附过程, 如图 6(a)所示.由Weber-Morris颗粒内扩散方程的拟合参数可知, 粒内扩散模型不通过原点, 说明吸附过程受其它吸附阶段的共同控制[图 6(b)].
|
|
表 1 吸附动力学模型参数 Table 1 Kinetic parameters for adsorption of NOR onto ARBR |
|
实验条件:c0=20 mg·L-1, T=20℃±1℃ 图 6 ARBR吸附NOR动力学曲线 Fig. 6 Effect of contact time on the adsorption of NOR on ARBR |
吸附等温线是评价吸附剂的吸附能力重要指标.等温实验数据分别采用Langmuir、Freundlich和Temkin等温吸附模型来拟合[24], 模型参数见表 2. ARBR树脂对NOR的单位吸附量随反应温度的增加而增加, 这说明温度越高越利于ARBR对水中NOR的吸附.
|
|
表 2 ARBR吸附水中NOR等温吸附模型参数值 Table 2 Isotherm parameters for adsorption of NOR onto the aminated rosin-based resin at different temperatures |
Langmuir、Freundlich和Temkin吸附等温模型数学表达式分别为式(5)~(7)所示.
Langmuir吸附等温式:
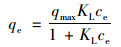
|
(5) |
Freundlich吸附等温式:
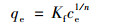
|
(6) |
Temkin吸附等温式:
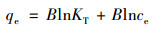
|
(7) |
分离因子:
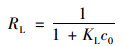
|
(8) |
式中, ce是NOR吸附达到平衡时的浓度(mg·L-1); qe为平衡吸附量(mg·g-1); qmax (mg·g-1)代表最大吸附量; KL (L·mg-1)、Kf (mg·g-1)和KT (mg·g-1)分别为Langmuir、Freumdlich和Temkin吸附速率常数.而分离因子RL如式(8)表示.拟合参数见表 2, 研究发现, 该吸附过程更加符合Langmuir等温吸附模型, R2值均在0.98以上, 说明Langmuir方程常用于描述单分子层吸附为主或稀溶液中的吸附类型. Langmuir等温吸附模型参数分离因子经计算得到的值1>RL>0, 这说明ARBR对NOR的吸附属于物理吸附. Freumdlich等温吸附模型参数值1>n>0, 说明ARBR对NOR的吸附属于优惠吸附.
通过不同温度下的吸附实验可以计算吸附过程的标准吉布斯自由能变(ΔGθ)、焓变(ΔHθ)和熵变(ΔSθ)等吸附的相关热力学参数, 如公式(9)和(10)所列:
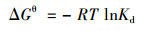
|
(9) |
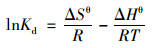
|
(10) |
式中, Kd为平衡吸附常数(L·g-1), 即平衡时刻吸附剂上吸附质数量与溶液中吸附质数量的比值; T为反应温度(K); R为理想气体常数[8.314 J·(mol·K)-1].以lnKd对1/T作图得到直线方程, 由其斜率和截距分别计算相应温度下对应热力学参数, 结果如表 3所示.
|
|
表 3 ARBR吸附水中NOR热力学参数 Table 3 Thermodynamic parameters for the adsorption of NOR on ARBR |
由表 3可知, 不同反应温度条件下计算得到的ΔGθ为负值, 随着温度升高呈减少趋势, 表明吸附过程是自发进行. ΔHθ为48.65 kJ·mol-1进一步表明了该吸附属于吸热过程. ΔSθ值为正, 表明NOR分子吸附到ARBR表面后增加了固液界面上物质的混乱度.通常认为ΔHθ在-40~20 kJ·mol-1范围内属于物理吸附为主, 而ΔGθ在-20~0 kJ·mol-1范围内时也是物理吸附的重要特征之一[25].说明ARBR对NOR的吸附过程是以物理吸附为主.
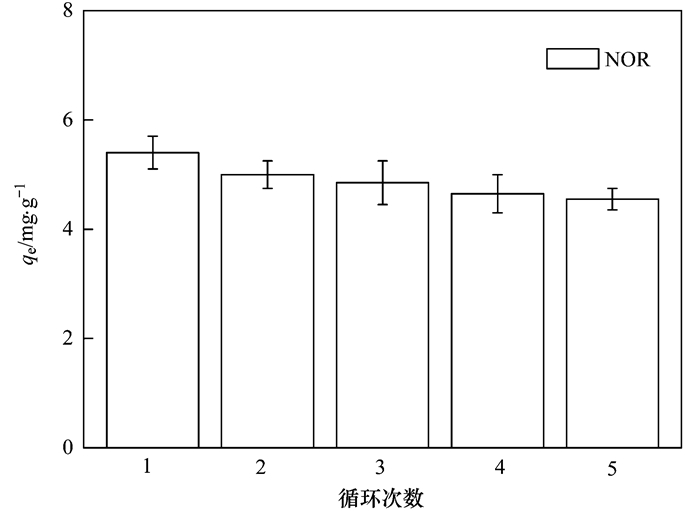
2.7 脱附再生和重复使用研究为了考察ARBR的再生效果, 分别采用0.1 mol·L-1 NaOH、0.1 mol·L-1 HCl、水、乙醇和甲醇对其脱附特性进行评价.相比较其它脱附液而言, 0.1 mol·L-1 HCl洗脱液对ARBR的再生效果最佳.这是因为在酸性条件下吸附剂和吸附质的氮、氧原子与质子形成的铵盐和盐降低了氮氧的给电子能力, 导致形成的氢键作用力减弱而容易被洗脱下来, 进一步证实了氢键在吸附中的主导作用. 图 7表示NOR在ABRB上5次连续循环使用的吸附量, 第一次吸附量为5.3 mg·g-1, 第二次吸附量下降到5.0 mg·g-1, 随后的重复循环中, 对NOR依然保持相对稳定的吸附量.因此, ARBR可再生循环使用, 具备实际应用的潜力.
|
实验条件:c0=20 mg·L-1, pH=6.0, ARBR投加量=1.0 g·L-1, T=20℃±1℃ 图 7 0.1 mol·L-1 HCl脱附液对ARBR的再生效果比较 Fig. 7 Regeneration performance of ARBR by 0.1 mol·L-1 HCl solution |
实验对比了5种商用树脂与ARBR对水中的NOR的吸附性能.由图 8可知, 对NOR的吸附量大小顺序为:D001>ARBR>XAD-1180>DAX-8>IRA410>IRC748.结果表明, 除了D001树脂之外, ARBR对NOR具有较好的吸附去除效果.相比功能单体主要来源于苯乙烯系, ARBR的原料松香绿色环保, 易再生, 在环境微污染水处理领域有潜在的应用前景.

|
实验条件:c0=20 mg·L-1, pH=6.0, ARBR投加量=1.0 g·L-1, T=20℃±1℃ 图 8 ARBR与商业树脂吸附NOR效果对比 Fig. 8 Comparison of NOR adsorption on ARBR with other commercial resins |
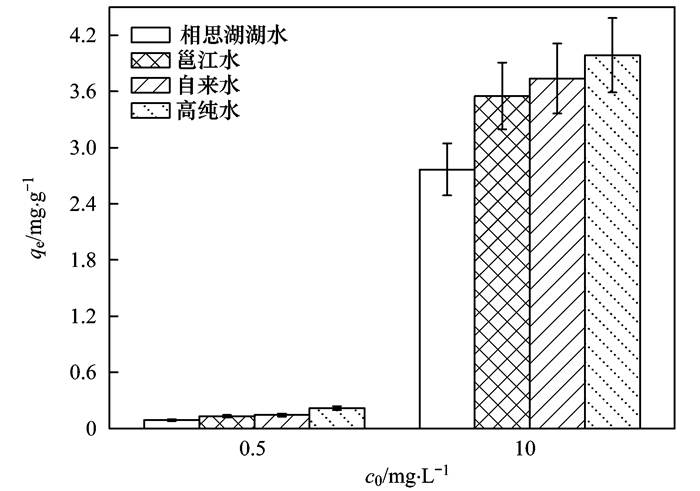
为了进一步检验ARBR的实际应用性能, 实验考察了ARBR在不同原水体系中对NOR的吸附效果(图 9).由图 9可知, 纯水中的吸附量最大, 实际原水对NOR均表现为抑制作用, 其中湖水(DOC=5.2 mg·L-1)对吸附的影响最大.通过比较各水样中的DOC值, 结果表明湖水的DOC=5.2 mg·L-1最高, 其原因可能是实际原水中存在的天然有机物与NOR竞争ARBR上的吸附位点, 进而抑制对NOR的吸附.
|
实验条件:ARBR投加量=1.0 g·L-1, pH=6.0, T=20℃±1℃ 图 9 实际原水对ARBR去除NOR的影响 Fig. 9 Effect of different water matrix samples on NOR adsorption onto ARBR |
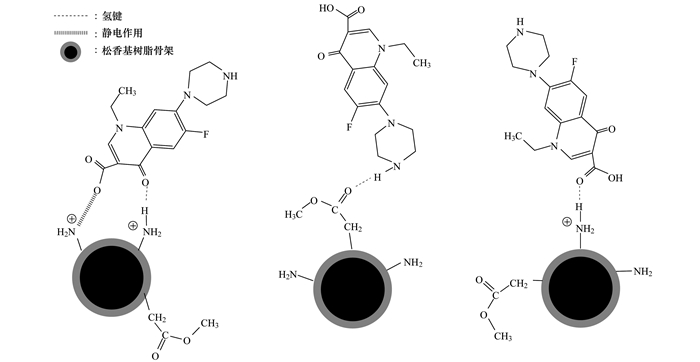
综上所述, ARBR吸附NOR过程中涉及到主要作用力包括氢键和静电作用, 如图 10所示. ①氢键作用:ARBR所带的羰基氧原子、氨基氮原子及氢原子可分别与NOR分子中的氨基的氢原子、羧基氧原子形成氢键作用, 从而增加了ARBR对NOR的吸附亲和力.在酸性条件下, 吸附质与吸附剂所含氨基的氮原子的孤电子对易与质子结合, 使氨基的氮原子失去了氢键受体的作用, 互相间形成的氢键能力减弱, 导致ARBR在酸性条件下对NOR的吸附能力大大下降. ②静电作用:在中性或碱性溶液中, ARBR的正电荷与NOR的负电荷相互吸引形成静电作用力, 促使吸附质分子向树脂表面扩散.
|
图 10 ARBR与NOR分子作用机制 Fig. 10 Proposed interaction mechanisms between NOR molecules and ARBR |
(1) 通过经氨基修饰的松香基吸附树脂ARBR对水中NOR具有较好的吸附能力和亲和能力, 在pH 6~8范围内, 吸附能力较好; 共存离子的存在对ARBR去除NOR的行为总体上表现为促进作用.
(2) ARBR树脂吸附速率较快在60 min内可达到平衡, ARBR吸附NOR吸附动力学符合准二级动力学模型; 由粒子内扩散模型可知, 颗粒内扩散为吸附速率的主要控速步骤.
(3) 等温吸附模型符合Langmuir等温模型, 最大平衡吸附量为30.29 mg·g-1(pH 6.0和20℃), 吸附过程为吸热的物理过程, 在ARBR去除水中的NOR过程中的作用机制主要是氢键和静电作用.
(4) 对NOR的吸附量大小顺序为:D001>ARBR>XAD-1180>DAX-8>IRA410>IRC748. 0.1 mol·L-1的HCl溶液作为脱附剂, 可以有效地脱附树脂吸附的NOR.因此, ARBR树脂作为一种新型的树脂在饮用水微污染控制领域具有潜在的应用价值.
| [1] |
张芹, 张圣虎, 汪贞, 等. 骆马湖表层水体中32种PPCPs类物质的污染水平、分布特征及风险评估[J]. 环境科学, 2017, 38(1): 162-169. Zhang Q, Zhang S H, Wang Z, et al. Pollution level, distribution characteristics and risk assessment of 32 PPCPs in surface water of Luomahu Lake[J]. Environmental Science, 2017, 38(1): 162-169. |
| [2] |
章强, 辛琦, 朱静敏, 等. 中国主要水域抗生素污染现状及其生态环境效应研究进展[J]. 环境化学, 2014, 33(7): 1075-1083. Zhang Q, Zhu Q, Zhu J M, et al. The antibiotic contaminations in the main water bodies in China and the associated environmental and human health impacts[J]. Environmental Chemistry, 2014, 33(7): 1075-1083. DOI:10.7524/j.issn.0254-6108.2014.07.001 |
| [3] | Luo Y L, Guo W S, Ngo H H, et al. A review on the occurrence of micropollutants in the aquatic environment and their fate and removal during wastewater treatment[J]. Science of the Total Environment, 2014, 473-474: 619-641. DOI:10.1016/j.scitotenv.2013.12.065 |
| [4] | Van Doorslaer X, Dewulf J, Van Langenhove H, et al. Fluoroquinolone antibiotics:an emerging class of environmental micropollutants[J]. Science of the Total Environment, 2014, 500-501: 250-269. DOI:10.1016/j.scitotenv.2014.08.075 |
| [5] | Tiwari B, Sellamuthu B, Ouarda Y, et al. Review on fate and mechanism of removal of pharmaceutical pollutants from wastewater using biological approach[J]. Bioresource Technology, 2017, 224: 1-12. DOI:10.1016/j.biortech.2016.11.042 |
| [6] | Peng H B, Pan B, Wu M, et al. Adsorption of ofloxacin and norfloxacin on carbon nanotubes:hydrophobicity-and structure-controlled process[J]. Journal of Hazardous Materials, 2012, 233-234: 89-96. DOI:10.1016/j.jhazmat.2012.06.058 |
| [7] |
王彬斌, 林景东, 万顺利, 等. 氧化镁基生物质炭高效去除水体中磷的特性[J]. 环境科学, 2017, 38(7): 2859-2867. Wang B B, Lin J D, Wan S L, et al. MgO-Biochar for the adsorption of phosphate in water[J]. Environmental Science, 2017, 38(7): 2859-2867. |
| [8] | Wang T Y, Pan X, Ben W W, et al. Adsorptive removal of antibiotics from water using magnetic ion exchange resin[J]. Journal of Environmental Sciences, 2017, 52: 111-117. DOI:10.1016/j.jes.2016.03.017 |
| [9] | Chao Y H, Zhu W S, Yan B, et al. Macroporous polystyrene resins as adsorbents for the removal of tetracycline antibiotics from an aquatic environment[J]. Journal of Applied Polymer Science, 2014, 131(15): 4056. |
| [10] | Zhou Q, Zhang M C, Shuang C D, et al. Preparation of a novel magnetic powder resin for the rapid removal of tetracycline in the aquatic environment[J]. Chinese Chemical Letters, 2012, 23(6): 745-748. DOI:10.1016/j.cclet.2012.01.039 |
| [11] | Zhang M C, Li A M, Zhou Q, et al. Effect of pore size distribution on tetracycline adsorption using magnetic hypercrosslinked resins[J]. Microporous and Mesoporous Materials, 2014, 184: 105-111. DOI:10.1016/j.micromeso.2013.10.010 |
| [12] | Hosseini-Bandegharaei A, Alahabadi A, Rahmani-Sani A, et al. Effect of nitrate and amine functionalization on the adsorption properties of a macroporous resin towards tetracycline antibiotic[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 66: 143-153. DOI:10.1016/j.jtice.2016.06.007 |
| [13] |
左振宇, 郭惠, 曾苑, 等. 松香基吸附树脂对麻黄草提取液中麻黄碱的分离提纯应用研究[J]. 应用化工, 2016, 45(3): 412-416. Zuo Z Y, Guo H, Zeng Y, et al. Separation and purification of ephedrine from ephedra by rosin-based adsorption resin[J]. Applied Chemical Industry, 2016, 45(3): 412-416. |
| [14] | Liu S G, Ding Y Q, Li P F, et al. Adsorption of the anionic dye Congo red from aqueous solution onto natural zeolites modified with N, N-dimethyl dehydroabietylamine oxide[J]. Chemical Engineering Journal, 2014, 248: 135-144. DOI:10.1016/j.cej.2014.03.026 |
| [15] |
李鹏飞, 雷福厚, 严瑞萍, 等. 松香基功能高分子对Cu(Ⅱ)吸附性能的研究[J]. 离子交换与吸附, 2010, 26(6): 533-541. Li P F, Lei F H, Yan R P, et al. Study on the adsorption behavior of the rosin-based functional polymer for Cu(Ⅱ)[J]. Ion Exchange and Adsorption, 2010, 26(6): 533-541. |
| [16] | 广西民族大学. 一种松香基功能高分子及其制备方法[P]. 中国专利, CN 101319036A, 2008-12-10. |
| [17] | Niu H Y, Zhang D, Meng Z F, et al. Fast defluorination and removal of norfloxacin by alginate/Fe@Fe3O4 core/shell structured nanoparticles[J]. Journal of Hazardous Materials, 2012, 227-228: 195-203. DOI:10.1016/j.jhazmat.2012.05.036 |
| [18] | Valle H, Sán chez J, Rivas B L, et al. Poly (N-vinylpyrrolidone-co-2-acrylamido-2-methylpropanesulfonate sodium):synthesis, characterization, and its potential application for the removal of metal ions from aqueous solution[J]. Journal of Applied Polymer Science, 2015, 132(2): 41272. |
| [19] | El-Bahy S M, El-Bah Z M. Synthesis and characterization of a new iminodiacetate chelating resin for removal of toxic heavy metal ions from aqueous solution by batch and fixed bed column methods[J]. Korean Journal of Chemical Engineering, 2016, 33(8): 2492-2501. DOI:10.1007/s11814-016-0070-1 |
| [20] | Pan B J, Zhang W M, Pan B C, et al. Efficient removal of aromatic sulfonates from wastewater by a recyclable polymer:2-naphthalene sulfonate as a representative pollutant[J]. Environmental Science & Technology, 2008, 42(19): 7411-7416. |
| [21] | Pei Z G, Shan X Q, Zhang S Z, et al. Insight to ternary complexes of co-adsorption of norfloxacin and Cu(Ⅱ) onto montmorillonite at different pH using EXAFS[J]. Journal of Hazardous Materials, 2011, 186(1): 842-848. DOI:10.1016/j.jhazmat.2010.11.076 |
| [22] | Yang W B, Lu Y P, Zheng F F, et al. Adsorption behavior and mechanisms of norfloxacin onto porous resins and carbon nanotube[J]. Chemical Engineering Journal, 2012, 179: 112-118. DOI:10.1016/j.cej.2011.10.068 |
| [23] | Jin X S, Liu F Q, Yang X, et al. Adsorption performances and mechanisms of the newly synthesized N, N'-di (carboxymethyl) dithiocarbamate chelating resin toward divalent heavy metal ions from aqueous media[J]. Journal of Hazardous Materials, 2009, 167(1-3): 589-596. DOI:10.1016/j.jhazmat.2009.01.020 |
| [24] | Chen S J, Li Y J, Lü R J, et al. Optimization and modeling of photocatalytic removal of norfloxacin using tungsten bismuth loaded carbon iron complexes based on response surface methodology[J]. Industrial & Engineering Chemistry Research, 2014, 53(26): 10775-10783. |
| [25] | Liu Q S, Zheng T, Wang P, et al. Adsorption isotherm, kinetic and mechanism studies of some substituted phenols on activated carbon fibers[J]. Chemical Engineering Journal, 2010, 157(2-3): 348-356. DOI:10.1016/j.cej.2009.11.013 |
 2018, Vol. 39
2018, Vol. 39


