氨氮是地表水源的主要污染因子之一[1, 2].供水系统中过量的氨氮会使消毒效率降低, 增加氯消毒过程中的需氯量[3], 并产生令人不快的嗅味, 甚至对中枢神经系统易造成伤害[4, 5].饮用水处理中去除氨氮的方法主要有吸附法和生物法.对于吸附法, 国内外研究主要集中在吸附剂改性这方面, 但往往吸附剂的吸附容量有限, 再生困难, 成本较高, 多适用于小型水厂[6~8].对于生物法, 研究成果主要为对普通滤池进行生物强化[9, 10], 目前生物法去除氨氮的技术已比较成熟, 在国内外应用较多, 但其对温度变化幅度大的地表水适应性差, 在自然状态下挂膜较难成功, 且运行管理复杂[11~13].近年来研究发现, 在处理同时含有铁、锰、氨氮复合污染的地下水时, 通过向水中投加高锰酸钾, 可在石英砂滤料表面形成一层能高效去除地下水中氨氮的铁锰复合氧化膜(活性氧化膜)[14~16].该活性氧化膜为非晶态结构, 主要组成元素为铁、锰、钙、氧等[17]. Guo等[18]研究发现该活性氧化膜对地下水中氨氮的去除机制为催化氧化作用.相对传统方法, 此种方法具有可实现铁、锰和氨氮的同步高效去除, 启动成熟时间短(大约26 d), 反应过程几乎没有副产物等优势.
在前期实验工作中发现, 将该活性氧化膜应用于地表水中氨氮的去除时, 其催化氧化活性随着运行时间推移而有所下降.研究发现投加磷酸盐可以促进活性氧化膜的氨氮去除活性, 但对具体的磷酸盐投加量尚未明确, 磷酸盐促进与保持活性氧化膜氨氮去除活性的效果及机制也尚未探讨.因此, 本文基于实验工作中发现的问题, 系统地考察了不同磷酸盐投加量对活性氧化膜去除地表水中氨氮的影响, 研究了冬季低温条件下保持活性氧化膜氨氮去除活性的方法, 并通过灭活滤柱中的微生物, 初步探究了磷酸盐影响活性氧化膜氨氮去除活性的机制, 使活性氧化膜应用于地表水处理成为可能.
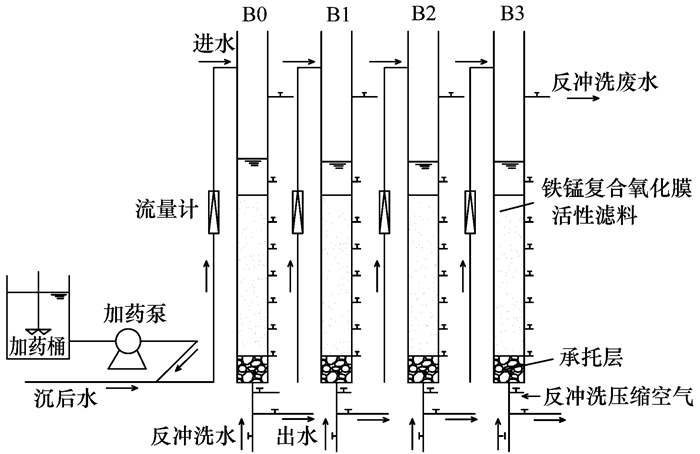
1 材料与方法 1.1 实验装置实验装置主要由4个完全相同的有机玻璃滤柱组成, 分别命名为B0、B1、B2和B3, 如图 1所示.滤料为地下水条件下培养成熟的铁锰复合氧化膜活性滤料, 有效滤层厚度为85 cm, 承托层为20 cm. B0、B1、B2和B3滤柱进行同步实验, 滤速为7 m·h-1.
|
图 1 实验装置示意 Fig. 1 Schematic of the pilot-scale filter |
地表水源水经过混凝沉淀处理后, 通过加药泵向沉后水中投加一定量的氨氮(NH4Cl), 调节进水氨氮浓度, 再由滤柱进行过滤处理.实验期间, 滤柱进水水质参数如表 1所示.
|
|
表 1 滤柱进水水质参数 Table 1 Water quality of the feed water used in the pilot-scale filter system |
1.3 实验方法
夏秋季节水温在17.2~21.9℃范围内, B0滤柱不投加磷酸盐, B1、B2和B3滤柱分别投加5、10和15 μg·L-1磷酸盐(Na2HPO4·12H2O), 研究不同磷酸盐投加量对活性氧化膜氨氮去除效果的影响.通过比较各个滤柱上层65 cm滤层的氨氮体积去除速率(volumetric ammonium removal rate, VARR), 进一步研究活性氧化膜氨氮去除活性的变化, VARR用如下公式计算[11]:
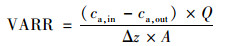
|
(1) |
式中, ca, in和ca, out分别为滤柱进水和取样点出水的氨氮浓度(mg·L-1), Q为进水流量(m3·h-1), A为滤柱的横截面积(m2), Δz为对应取样点的滤层厚度(m).
冬季低温阶段, 水温低于10.5℃时, 活性氧化膜的氨氮去除活性明显下降, 采取增加磷酸盐投加量至30 μg·L-1和将滤层厚度从85 cm增至120 cm两种操作方式以保证系统对氨氮的处理效果, 比较其效果差异, 并考察滤柱的最大氨氮去除能力.
对未投加与投加磷酸盐的两个滤柱中微生物进行灭活.将O3从滤柱底部持续通入150 min, 实验过程中臭氧浓度为1.90~3.92 mg·L-1, 对灭活前后活性氧化膜表面的细菌总数进行测定[19, 20].对比灭活前后滤柱氨氮去除效果的差异, 并对活性氧化膜进行SEM和EDS表征分析, 初步探究磷酸盐影响活性氧化膜氨氮去除活性的机制.
1.4 分析测试方法水样均采用标准方法测定[20].氨氮:纳氏试剂分光光度法; 硝酸盐氮:紫外分光光度法; 亚硝酸盐氮:N-(1-萘基)-乙二胺光度法; TP:钼锑抗分光光度法; 高锰酸盐指数:高锰酸盐指数法; O3:靛蓝二磺酸钠分光光度法[21]; 碱度:酸碱指示剂滴定法; DO浓度:溶氧仪(雷磁JPB-607A); pH:pH计(雷磁PHS-3C); 水温:温度计; 浊度:浊度计(雷磁WGZ-2000); TOC:燃烧氧化-非分散红外吸收法(岛津TOC-ASI); Al:电感耦合等离子体质谱(美国PE 200-ELAN DRC-e); 表面形貌及元素组成:扫描电镜(Quanta 600 FEG); 细菌总数:平板计数法.
2 结果与讨论 2.1 不同磷酸盐投加量对铁锰复合氧化膜活性的影响 2.1.1 不同磷酸盐投加量下的氨氮去除效果不同磷酸盐投加量下滤柱的进出水氨氮浓度变化见图 2.实验期间水温为17.2~21.9℃, 进水氨氮浓度为1.16~1.35 mg·L-1, 未投加磷酸盐、投加5、10和15 μg·L-1磷酸盐4个滤柱的出水氨氮平均浓度分别为0.20、0.05、0.05和0.06 mg·L-1, 氨氮去除率分别为84.4%、96.1%、96.1%和95.3%. 图 3为不同磷酸盐投加量下滤柱的氨氮浓度沿程变化.由图 3(a)可知, 未投加磷酸盐滤柱的氨氮浓度沿程变化曲线随运行时间逐渐上移, 氨氮达标所需滤层从65 cm增至85 cm, 说明未投加磷酸盐条件下活性氧化膜的氨氮去除活性随运行时间逐渐下降.由图 3(b)~3(d)可知, 运行第15 d, 投加磷酸盐滤柱的氨氮去除效果均有明显提升, 氨氮达标所需滤层从65 cm减至45 cm; 运行第29 d, 氨氮去除效果与第15 d相差不大.结合图 2和图 3可知未投加磷酸盐滤柱的氨氮去除活性比投加磷酸盐的低, 且投加5、10和15 μg·L-1磷酸盐滤柱的氨氮去除活性基本一致.说明磷酸盐可以促进活性氧化膜的氨氮去除活性, 且在5~15 μg·L-1磷酸盐投加量条件下其氨氮去除活性基本一致, 此时5 μg·L-1磷酸盐即可保持活性氧化膜的氨氮去除活性.

|
图 2 不同磷酸盐投加量下滤柱进出水氨氮浓度的变化 Fig. 2 Ammonium concentrations in influent and effluent water of the filters at different phosphate dosages |

|
图 3 不同磷酸盐投加量下的氨氮浓度沿程变化 Fig. 3 Ammonium concentrations depth profiles at different phosphate dosages |
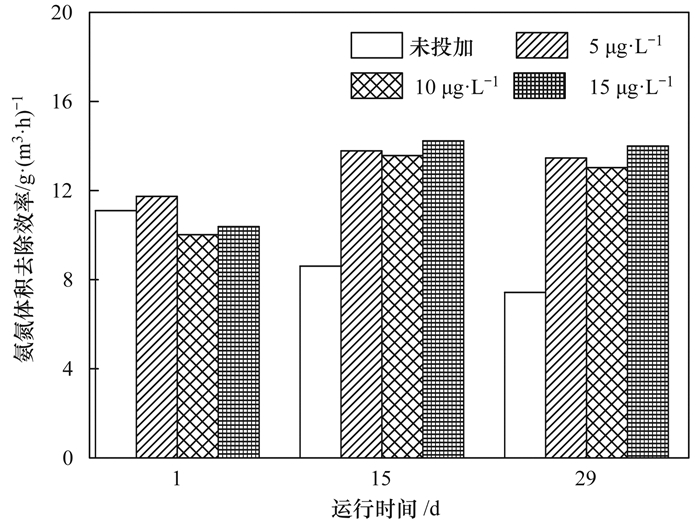
为进一步研究活性氧化膜氨氮去除活性的变化, 对滤柱上层65 cm滤层的氨氮体积去除速率进行了计算, 结果如图 4所示.从中可知随着运行时间的增加, 未投加磷酸盐滤柱的氨氮体积去除效率从最初的11.10 g·(m3·h)-1下降到第29 d的7.43 g·(m3·h)-1, 减少了33.1%, 仅为同期投加5 μg·L-1磷酸盐滤柱的55.2%.随着运行时间的推移, 未投加磷酸盐滤柱的氨氮去除活性逐渐下降, 而投加5~15 μg·L-1磷酸盐滤柱的氨氮去除活性均有所提升且相差不大, 说明此时5 μg·L-1磷酸盐即可保持活性氧化膜的氨氮去除活性, 与图 2和图 3所得结论一致.
|
图 4 不同磷酸盐投加量下的氨氮体积去除效率 Fig. 4 Volumetric ammonium removal rate at different phosphate dosages |
以B2和B3滤柱作为考察对象, 研究冬季低温条件下铁锰复合氧化膜在不同操作方式下活性的保持效果, 如图 5所示.由前面实验结果可知, 投加5、10和15 μg·L-1磷酸盐滤柱的氨氮去除效果基本一致, 故运行初期(1~40 d), B2和B3滤柱均改投5 μg·L-1磷酸盐.运行至第12 d, 水温降低为12.5℃, B2和B3滤柱的出水氨氮均有所升高但仍达标, 说明水温不低于12.5℃时, 5 μg·L-1磷酸盐仍可保持活性氧化膜的氨氮去除活性.运行至第21 d, 因系统故障, 两个滤柱均停止运行35 d(图中折断线), 之后恢复正常运行.运行至第22 d, 水温低于10.5℃, B2和B3滤柱出水氨氮均超标.分析其原因, 可能是因为水温的降低, 导致氨氮去除活性进一步降低, 此时5 μg·L-1磷酸盐已不足以保持活性氧化膜的氨氮去除活性.

|
图 5 不同操作方式下的氨氮去除效果 Fig. 5 Ammonium removal efficiency under different operating conditions |
运行至第41 d, 将B3滤柱磷酸盐投加量增加至30 μg·L-1, B2滤柱滤层厚度增加至120 cm, 并比较其处理效果差异.由图 5(a)可知, B3滤柱投加30 μg·L-1磷酸盐后, 当天出水氨氮浓度达标, 在之后的运行过程中, 其氨氮去除活性持续提升, 运行至第68 d, 氨氮去除率可达95.4%;在水温为6.5℃时, 出水氨氮浓度仍小于0.50 mg·L-1.由图 5(b)可知, B2滤柱滤层厚度从85 cm增加至120 cm后, 出水氨氮浓度降低至0.50 mg·L-1以下, 但运行14 d后(第55 d)出水氨氮浓度再次超标.分析原因可能是冬季低温阶段活性氧化膜本身的活性较低, 增加滤层厚度并不能保持其活性, 仅靠延长水力停留时间(由原先的7.29 min增至10.29 min)虽然短时间内可实现出水氨氮浓度达标, 但随着水温的降低, 活性氧化膜的活性持续降低, 滤柱的出水氨氮浓度会再次超标.运行第65 d, 将B2滤柱的磷酸盐投加量增加至30 μg·L-1, 滤层厚度仍为120 cm, 运行3 d后(第68 d)出水氨氮浓度达标, 且随着运行时间的推移, 其氨氮去除活性迅速提升, 运行7 d后(第72 d), 氨氮去除率可达95.5%.结合图 5可知, 冬季低温条件下仅增加滤层厚度并不能取得稳定的氨氮去除效果, 投加30 μg·L-1磷酸盐可以保证滤柱出水氨氮稳定达标.
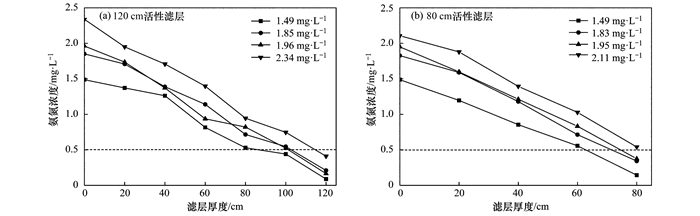
2.2.2 不同滤层厚度的最大安全进水氨氮浓度B2和B3滤柱均投加30 μg·L-1磷酸盐, 氨氮去除效果稳定后, 对其最大氨氮去除能力进行了考察, 结果如图 6所示.从中可知, 水温在6.5~10.5℃之间, 滤速为7 m·h-1时, 120 cm和80 cm活性滤层的最大安全进水氨氮浓度分别为2.34 mg·L-1和1.95 mg·L-1.可以看出在冬季低温条件下, 通过增加磷酸盐投加量, 活性氧化膜仍能高效去除地表水中的氨氮.
|
图 6 不同滤层厚度的最大安全进水氨氮浓度 Fig. 6 Maximum safe concentration of ammonium in the influent for different heights of filter layers |
对比生物法在低温条件下的运行效果, 发现在低温时期普通生物滤池的生物量和生物活性低, 抗冲击负荷能力差, 反冲洗频率高, 难以应对进水氨氮浓度的剧烈波动[22, 23]. Andersson等[24]认为水温是影响生物滤池氨氮处理效果的重要因素, 水温在4~10℃时氨氮去除率仅有10%~40%左右.贺瑞敏[25]认为适当降低水力负荷, 延长水力停留时间, 可以减少低温对去除氨氮的负面影响, 但由于生物滤池中硝化细菌的活性受到严重抑制, 即使在很低的水力负荷条件下, 仍不能达到良好的去除.因而相较于传统的生物法, 活性氧化膜催化氧化去除氨氮的方法在低温时更有优势.
2.3 磷酸盐影响活性氧化膜氨氮去除活性的机制评价饮用水中臭氧消毒效果的指标为CT值(C为臭氧浓度:mg·L-1, T为接触时间:min).美国环保署颁布的地表水处理规程(surface water treatment rule, SWTR)明确臭氧对细菌去除率达99.00%~99.99%的CT值为0.3~1.8 mg·min·L-1[26, 27].水中含有0.30~0.60 mg·L-1的臭氧时, 对细菌、病毒等微生物的内部结构有极强的氧化破坏性, 可达到杀灭细菌的效果, 若臭氧浓度超过1.00 mg·L-1以上便能杀灭芽孢、病毒、真菌等微生物[28].臭氧对硝化细菌也有明显的杀灭效果[29].本实验中臭氧灭活的CT值为285~588 mg·min·L-1, 远大于灭活细菌对CT值的要求, 因而可以有效杀灭滤柱内的微生物.为进一步证明灭活方式有效, 对灭活前后活性氧化膜表面的细菌总数进行测定, 结果见表 2.可以看到, 灭活后活性氧化膜表面的细菌总数为0, 说明臭氧灭活彻底有效.同时Guo等[18]对臭氧灭活前后活性氧化膜的性质变化进行了研究, 结果表明臭氧对活性氧化膜的结构几乎没有影响.因此可以认为, 灭活后活性氧化膜的氨氮去除为催化氧化作用.
|
|
表 2 灭活前后活性氧化膜表面细菌总数的变化 Table 2 Total number of bacteria on the activated oxide film before and after inactivation |
臭氧灭活前和灭活后滤柱的氨氮去除效果变化, 如图 7所示.灭活前, 投加和未投加磷酸盐滤柱的氨氮去除量分别为1.46 mg·L-1和1.07 mg·L-1; 灭活后, 其氨氮去除量分别为1.11 mg·L-1和0.62 mg·L-1.说明活性氧化膜对氨氮的去除同时包括催化氧化作用和生物作用.比较灭活前和灭活后的氨氮去除效果可知, 投加和未投加磷酸盐条件下活性氧化膜的催化氧化活性分别约占总活性的76.0%和57.9%.同时投加磷酸盐条件下, 活性氧化膜的总活性和催化氧化活性分别是未投加磷酸盐条件的1.36倍和1.79倍, 这表明磷酸盐促进了活性氧化膜的催化氧化活性.

|
图 7 活性氧化膜臭氧灭活前后的氨氮浓度沿程变化 Fig. 7 Ammonium concentration depth profiles of the activated oxide film before and after ozone inactivation |
为进一步研究磷酸盐影响活性氧化膜催化氧化活性的机制, 对未投加与投加磷酸盐滤柱的滤料进行SEM和EDS表征分析.由图 8的SEM表征结果可知, 未投加磷酸盐的滤料表面比较粗糙, 而投加磷酸盐的滤料表面较为光滑, 其表面形貌的差异很可能是因为磷酸盐的投加造成的.由图 9的EDS表征结果显示, 未投加与投加磷酸盐的滤料表面元素基本相同, 主要为Mn、O、Al、Ca等.与地下水条件的滤料表面元素[17]对比发现, Al并不是活性氧化膜的原始组成元素, 因此活性氧化膜应用于地表水处理后其催化氧化活性有所下降很有可能是Al在滤料表面积累导致的.未投加与投加磷酸盐条件下的活性氧化膜表面Al原子百分比分别为8.70%和7.18%, 且滤料表面未检测到P元素的存在, 推测可能是磷酸盐与滤料表面的Al结合成其它形态, 使其易于从滤料表面脱落, 从而削弱了Al对活性氧化膜的影响.

|
(a)未投加磷酸盐;(b)投加磷酸盐 图 8 活性氧化膜SEM图 Fig. 8 SEM images of the activated oxide film |

|
图 9 活性氧化膜EDS谱线 Fig. 9 EDS spectra of the activated oxide film |
(1) 磷酸盐可以有效促进与保持铁锰复合氧化膜的氨氮去除活性.水温在12.5℃以上时, 投加5 μg·L-1磷酸盐即可保持活性氧化膜的氨氮去除活性; 冬季低温阶段(水温为6.5~10.5℃时), 仅增加滤层厚度并不能取得稳定的氨氮去除效果, 投加30 μg·L-1磷酸盐可以保持滤柱出水氨氮稳定达标.
(2) 活性氧化膜对氨氮的去除同时包括催化氧化作用和生物作用, 投加和未投加磷酸盐条件下活性氧化膜的催化氧化活性分别约占总活性的76.0%和57.9%.投加磷酸盐条件下, 活性氧化膜的总活性和催化氧化活性分别是未投加磷酸盐条件的1.36倍和1.79倍, 这表明磷酸盐促进了活性氧化膜的催化氧化活性.
(3) 通过SEM和EDS表征可以推测, 活性氧化膜应用于地表水处理后其催化氧化活性有所下降很有可能是Al在滤料表面积累导致的.未投加与投加磷酸盐条件下的活性氧化膜表面Al原子百分比分别为8.70%和7.18%, 且滤料表面未检测到P元素的存在, 磷酸盐影响活性氧化膜催化氧化活性的原因初步推测可能是磷酸盐与滤料表面的Al结合成其它形态, 使其易于从滤料表面脱落, 从而削弱了Al对活性氧化膜的影响.
| [1] | 矫勇, 胡四一. 中国水资源公报2014[M]. 北京: 中国水利水电出版社, 2015. |
| [2] |
周怀东, 彭文启, 杜霞, 等. 中国地表水水质评价[J]. 中国水利水电科学研究院学报, 2004, 2(4): 255-264. Zhou H D, Peng W Q, Du X, et al. Assessment of surface water quality in China[J]. Journal of China Institute of Water Resources and Hydropower Research, 2004, 2(4): 255-264. |
| [3] |
魏彬, 李君, 崔营, 等. 水厂出水加氯消毒的加氯量确定[J]. 中国给水排水, 2010, 26(2): 86-88, 92. Wei B, Li J, Cui Y, et al. Determination of chlorine dosage during chlorination of finished water from waterworks[J]. China Water & Wastewater, 2010, 26(2): 86-88, 92. |
| [4] |
杜志鹏, 刘文君, 张弥, 等. 消毒过程中氨氮对氯耗的影响研究[J]. 中国给水排水, 2006, 22(13): 53-55. Du Z P, Liu W J, Zhang M, et al. Study on impact of ammonia nitrogen on chlorine consumption in disinfection process[J]. China Water & Wastewater, 2006, 22(13): 53-55. DOI:10.3321/j.issn:1000-4602.2006.13.014 |
| [5] | Enns G M. Neurologic damage and neurocognitive dysfunction in urea cycle disorders[J]. Seminars in Pediatric Neurology, 2008, 15(3): 132-139. DOI:10.1016/j.spen.2008.05.007 |
| [6] |
代瑞华, 马捷汀. 改性沸石吸附氨氮及电化学再生研究[J]. 安全与环境学报, 2012, 12(1): 81-85. Dai R H, Ma J T. On ammonia-absorption from sewage by means of modified zeolite and its electrochemical regeneration[J]. Journal of Safety and Environment, 2012, 12(1): 81-85. |
| [7] | Zhang Y J, Mancke R G, Sabelfeld M, et al. Adsorption of trichlorophenol on zeolite and adsorbent regeneration with ozone[J]. Journal of Hazardous Materials, 2014, 271: 178-184. DOI:10.1016/j.jhazmat.2014.02.020 |
| [8] | Wang Y, Kmiya Y, Okuhara T. Removal of low-concentration ammonia in water by ion-exchange using Na-mordenite[J]. Water Research, 2007, 41(2): 269-276. DOI:10.1016/j.watres.2006.10.035 |
| [9] |
夏琼琼, 陈卫, 罗彬. 饮用水生物强化过滤处理效能及其影响因子研究述评[J]. 河海大学学报(自然科学版), 2006, 34(1): 41-45. Xia Q Q, Chen W, Luo B. A review of some advances in research of effect and influencing factors of enhanced biological filtration for drinking water treatment[J]. Journal of Hohai University (Natural Sciences), 2006, 34(1): 41-45. |
| [10] |
杨威, 田家宇, 李圭白. 生物活性滤池饮用水除氨氮的影响因素[J]. 化工学报, 2008, 59(9): 2316-2321. Yang W, Tian J Y, Li G B. Factors influencing ammonia removal of biological activated filter in drinking water treatment[J]. Journal of Chemical Industry and Engineering (China), 2008, 59(9): 2316-2321. |
| [11] | Lee C O, Boe-Hansen R, Musovic S, et al. Effects of dynamic operating conditions on nitrification in biological rapid sand filters for drinking water treatment[J]. Water Research, 2014, 64: 226-236. DOI:10.1016/j.watres.2014.07.001 |
| [12] |
刘冰, 范辉, 余国忠, 等. 氨氮在饮用水生物滤池内的去除机制[J]. 环境科学, 2012, 33(7): 2394-2402. Liu B, Fan H, Yu G Z, et al. Mechanism of NH4+-N removal in drinking water biofilter[J]. Environmental Science, 2012, 33(7): 2394-2402. |
| [13] | Huang X F, Li W G, Zhang D Y, et al. Ammonium removal by a novel oligotrophic Acinetobacter sp. Y16 capable of heterotrophic nitrification-aerobic denitrification at low temperature[J]. Bioresource Technology, 2013, 146: 44-50. DOI:10.1016/j.biortech.2013.07.046 |
| [14] |
布浩, 黄廷林, 郭英明, 等. 石英砂表面活性滤膜去除地下水中氨氮的试验研究[J]. 中国环境科学, 2016, 36(4): 1045-1051. Bu H, Huang T L, Guo Y M, et al. Removal of ammonium from groundwater by a co-oxide filter film coating on quartz sands[J]. China Environmental Science, 2016, 36(4): 1045-1051. |
| [15] |
邵跃宗, 黄廷林, 史昕欣, 等. 地下水中石英砂滤层去除氨氮的动力学方程和基于反应活化能的分析[J]. 环境科学学报, 2016, 36(6): 2067-2071. Shao Y Z, Huang T L, Shi X X, et al. Kinetics of ammonium removal in groundwater by composite oxides film coating on silica sands and the analysis based on activation energy[J]. Acta Scientiae Circumstantiae, 2016, 36(6): 2067-2071. |
| [16] |
汪洋, 黄廷林, 文刚, 等. 地下水中锰对滤料表面氧化膜去除氨氮的影响[J]. 环境工程学报, 2015, 9(12): 5737-5744. Wang Y, Huang T L, Wen G, et al. Effect of manganese on removal of ammonia from groundwater by co-oxides membrane coated sands[J]. Chinese Journal of Environmental Engineering, 2015, 9(12): 5737-5744. DOI:10.12030/j.cjee.20151215 |
| [17] |
曹昕. 铁锰复合氧化物催化氧化去除地下水中氨氮研究[D]. 西安: 西安建筑科技大学, 2015. Cao X. The study on catalytic oxidation of ammonia in groundwater by co-oxides of iron and manganese[D]. Xi'an:Xi'an University of Architecture and Technology, 2015. |
| [18] | Guo Y M, Huang T L, Wen G, et al. The simultaneous removal of ammonium and manganese from groundwater by iron-manganese co-oxide filter film:the role of chemical catalytic oxidation for ammonium removal[J]. Chemical Engineering Journal, 2017, 308: 322-329. DOI:10.1016/j.cej.2016.09.073 |
| [19] | Magic-Knezev A, Van der Kooij D. Optimisation and significance of ATP analysis for measuring active biomass in granular activated carbon filters used in water treatment[J]. Water Research, 2004, 38(18): 3971-3979. DOI:10.1016/j.watres.2004.06.017 |
| [20] | 国家环境保护总局. 水和废水监测分析方法[M]. 北京: 中国环境科学出版社, 2002. |
| [21] | Bader H, Hoigné J. Determination of ozone in water by the indigo method[J]. Water Research, 1981, 15(4): 449-456. DOI:10.1016/0043-1354(81)90054-3 |
| [22] |
杨家轩, 马军, 时玉龙, 等. 气浮/复合滤料生物滤池工艺处理低温、高氨氮原水[J]. 中国给水排水, 2013, 29(21): 5-10. Yang J X, Ma J, Shi Y L, et al. Combined process of sedimentation, dissolved air flotation and biofilter with multi-layer media for treating raw water with heavy pollution and high ammonia nitrogen at low temperature[J]. China Water & Wastewater, 2013, 29(21): 5-10. |
| [23] | Zhang D Y, Li W G, Huang X F, et al. Removal of ammonium in surface water at low temperature by a newly isolated Microbacterium sp. strain SFA13[J]. Bioresource Technology, 2013, 137: 147-152. DOI:10.1016/j.biortech.2013.03.094 |
| [24] | Andersson A, Laurent P, Kihn A, et al. Impact of temperature on nitrification in biological activated carbon (BAC) filters used for drinking water treatment[J]. Water Research, 2001, 35(12): 2923-2934. DOI:10.1016/S0043-1354(00)00579-0 |
| [25] | 贺瑞敏. 曝气生物滤池预处理官厅水库水源水的试验研究[D]. 南京: 河海大学, 2003. |
| [26] | Lev O, Regli S. Evaluation of ozone disinfection systems:characteristic concentration c[J]. Journal of Environmental Engineering, 1992, 118(4): 477-494. DOI:10.1061/(ASCE)0733-9372(1992)118:4(477) |
| [27] | Lev O, Regli S. Evaluation of ozone disinfection systems:characteristic time T[J]. Journal of Environmental Engineering, 1992, 118(2): 268-285. DOI:10.1061/(ASCE)0733-9372(1992)118:2(268) |
| [28] |
齐爱玲. 饮用水臭氧消毒模型的研究[D]. 哈尔滨: 哈尔滨工业大学, 2010. Qi A L. Ozone disinfection model of drinking water[D]. Harbin:Harbin Institute of Technology, 2010. |
| [29] | Zhang G M, Yang J, Liu H Z, et al. Sludge ozonation:disintegration, supernatant changes and mechanisms[J]. Bioresource Technology, 2009, 100(3): 1505-1509. DOI:10.1016/j.biortech.2008.08.041 |
 2018, Vol. 39
2018, Vol. 39


